Стафилококк митис в зеве
Обновлено: 18.04.2024
Прошло много лет после написания первой статьи, посвященной лечению инфекций, вызванных золотистым стафилококком. За это время автор, будем надеяться, немного помудрела и приобрела кое-какой опыт в более детальной диагностике вышеупомянутых состояний, чем и хотела бы поделиться с многоуважаемой аудиторией в надежде, что, возможно, поможет каждому из вас в рутинной ежедневной работе, так как с этой зверюшкой сталкивается буквально каждый, кто надел белый халат и уж тем более хирургический костюм.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Прошло много лет после написания первой статьи, посвященной лечению инфекций, вызванных золотистым стафилококком. За это время автор, будем надеяться, немного помудрела и приобрела кое-какой опыт в более детальной диагностике вышеупомянутых состояний, чем и хотела бы поделиться с многоуважаемой аудиторией в надежде, что, возможно, поможет каждому из вас в рутинной ежедневной работе, так как с этой зверюшкой сталкивается буквально каждый, кто надел белый халат и уж тем более хирургический костюм.
Сначала повторим общеизвестные факты: S.aureus относится к грамположительным коккам и являются чуть ли не основной причиной большого количества инфекций кожи и мягких тканей, а так же ведущей причиной послеоперационных раневых инфекций.
Выделяют следующие разновидности золотистого стафилококка:
- Дикий S.aureus
- MSSA – метициллин-чувствительные стафилококки
- MRSA – метициллин-резистентные, которые обладают устойчивостью ко всему бета-лактамному ряду, сохраняя клинически важную чувствительность к ванкомицину, линезолиду и тигециклину
- VRSA и VISA – ванкомицин-устойчивые штаммы, к счастью, крайне редко встречающиеся и в основном наблюдающиеся в отделениях онкогематологии научно-исследовательских центров у пациентов, проходящих курс полихимиотерапии с последующей трансплантацией костного мозга
И сейчас обсудим первые три более подробно, так как именно они являются той причиной, ради которой повторно поднята данная тема, в том числе и по просьбам читателей (за что выражаем отдельную признательность).
Первое, что необходимо не просто запомнить, а буквально зазубрить наизусть – золотистый стафилококк, он же S.aureus, является нормальным жителем на неповрежденной коже и слизистых оболочках. Еще раз – нормальным, но только на неповрежденной коже и вне зависимости от антибиотикочувствительности пойманных экземпляров. Если кожа по тем или иным причинам поражается (например, сахарным диабетом) или повреждается, стафилококк тут же из милого соседа превращается в злейшего врага. Все как у людей – стоит дать слабину, и ближайшие соседи начнут добивать с ласковой улыбкой.
Таким образом, когда вы получаете результат микробиологического исследования образца, взятого с кожи (или из носоглотки), и видите там золотистого стафа, то должны понимать, кто перед вами, и насколько этот кто-то имеет отношение к текущему процессу.
Второе: если клиника отсутствует, а стафилококк посеялся, надо сделать что? Правильно, повторить посев еще раз. Золотистый стафилококк – это один из немногих микробов, чье наличие в отделяемом материале надо проверять дважды. Единственное исключение – это кровь, взятая непосредственно из сосудистого русла, чаще всего из вены. Наличие стафилококка в крови является поводом к немедленному назначению антибактериальной терапии, так как прямо указывает на наличие инфекции кровотока, а уж какого она генеза, спонтанного или ятрогенного, разбираться будете позже. Во всех остальных ситуациях проводится пересев с тщательным соблюдением техники забора материала (со стенок раны, а не гной, состоящий из дохлых нейтрофилов и нападавших сверху стафилококков) и правил асептики и антисептики, чтобы собственными стафилококками с кожи вновь забранный материал не контаминировать.
Чтобы понять, друг перед нами или враг, познакомимся со стафилококками более подробно.
- Дикий S.aureus, не видавший ни одного антибиотика, выглядит так
.jpg)
.jpg)
И нет, автор не сошла с ума – резистентность к ванкомицину у природных диких золотистых стафилококков – совершенно нормальное явление. Более того, попытка лечить такого возбудителя ванкомицином считается грубейшей ошибкой и закончится полным провалом в силу природной устойчивости к данному препарату. Это третье, о чем помнить необходимо.
Где мы встречаем таких S.aureus чаще всего? В носоглотках грудных младенцев или в их же кале, если придумали посеять. Почему? Потому что это представитель нормальной микрофлоры кожи, и ребенок сглатывает то, что живет в его носоглотке или слизывает с кожи матери. Надо лечить? В данной ситуации – ни в коем случае, иначе побьете нормальную микрофлору кожи и слизистых, и если очень повезет, то для ребенка это пройдет без последствий, но, скорее всего, получим стафилококка, вооруженного пенициллиназами, или MSSA. Повторимся еще раз – только в случае отсутствия клинической картины можно принимать такого рода решения. Во всех иных случаях необходима антибактериальная терапия, причем на длительный (до 28 суток) период времени.
.jpg)
.jpg)
При каких состояниях мы можем увидеть подобных возбудителей?
- Практически при всех инфекциях кожи и мягких тканей
- При внутрибольничных раневых инфекциях
- При диабетической стопе
- У внутривенных наркоманов
Типичным для клинической картины будет довольно агрессивное течение заболевания с яркими клиническими проявлениями ввиду того, что именно такой вид стафилококка обладает определенным набором ферментов, очень быстро расплавляющим окружающие ткани с образованием полостей и большим количеством гнойного отделяемого.
на антибиотикограмме будет выглядеть приблизительно так, оксациллин-резистентный, но ванкомицин-чувствительный (хотя при таком значении МПК уже возможны варианты)
.jpg)
Когда встречается? Все многообразие ятрогенных ВБИ к вашим услугам – почти все раневые инфекции и послеоперационные гнойные осложнения вне зависимости от их локализации. Повторимся в очередной раз – руки надо мыть, и мыть правильно. А еще закрывать маской не только рот, но и нос всем, кто хоть как-то касается открытых ран вне зависимости от причин их образования, так как стоит ране появиться, как стафилококк мгновенно превращается в зверя, осложняющего течение любого послеоперационного периода, особенно после операций, связанных с установками импланта. Более подробно о лечении предлагаем почитать в первой статье.
- В последнем пункте автор, по идее, должна была бы предложить испугаться самыми страшными ванкомицин-резистентными стафилококками и предложить схватиться за голову, но глядя на следующий набор антибиотикограмм, мы предлагаем посмотреть на то, что обычно сваливается с рук медицинского персонала в раны пациентов или контаминирует их биологический материал, который собран или хранится неправильно. Слава микробиологии, что подобные возбудители для пациентов, которые сохранили хоть какие-то остатки неспецифического иммунитета, не опасны, так как проходя эволюционные пути борьбы с ванкомицином, они почти полностью теряют факторы вирулентности. Но так как такие находки – это будни любой микробиологической лаборатории, то и вы о них тоже должны иметь представление. Уточним еще раз – это результаты посевов при полном отсутствии клинической картины бактериальной инфекции.
.jpg)
.jpg)
.jpg)
.jpg)
А теперь, тихо-тихо прошепчем, что иногда так может выглядеть приболевший микробиологический анализатор, который все, что в него не поставят, может определять как подобную страшную зверюгу. Хотя у вашего анализатора может быть какая-то своя болячка, и эти болячки лучше все-таки знать. Именно такого рода антибиотикограммы, как ничто другое наглядно показывают необходимость развития клинического мышления для умения отличать истинного возбудителя от контаминанта или нормального жителя человеческого организма, а также необходимости понимания, как работают методы микробиологической диагностики и варианты их ограничения.
Подведем краткие итоги нынешнего разговора:
- Стафилококк на неповрежденной коже и в носоглотке является нормальным представителем микромира, и лечить его не надо, более того, это может наносить прямой вред (как минимум кошельку)
- Существует целый перечень профессий, где носительство стафилококка строго нежелательно, и именно для этого проводятся контролирующие посевы среди медицинского персонала и работников пищевой отрасли
- Необходимо уверенно различать не только дикие и внутрибольничные штаммы, но и градацию по MRSA и MSSA, так как это прямо влияет на решение о применении конкретных препаратов при проведении эрадикационной терапии
- Антибиотикотерапия стафилококковых инфекций должна быть длительной, а не прерываться через 7-10 дней, даже если пациент демонстрирует положительную динамику. Недобитые золотистые стафилококки умеют метастазировать. Более подробно смотрим предыдущую статью
- Так как S.aureus занимает одно из ведущих мест в структуре внутрибольничных инфекций, особенно связанных с установкой имплантов, правила асептики и антисептики при работе с оными должны соблюдаться максимально жестко, иначе можно повторить дело Хабаровского кардиоцентра
Надеемся, что наш сегодняшний разговор был полезен и прояснил наиболее частые вопросы, связанные с микробиологическими особенностями S.aureus.

Специфика клинических проявлений бактериальной инфекции зависит от места локализации болезнетворных микроорганизмов и их разновидности.
Различают 3 основных типа бактерий, каждая из которых вызывает определенные виды заболеваний.
Чтобы вовремя диагностировать болезни и начать соответствующее лечение, следует рассмотреть характерные симптомы заболеваний горла, которые вызваны размножением анаэробных микробов, т.е. стрептококков.
Стрептококки – что это?
Стрептококки – это анаэробные микробы из семейства лактобацилл, которые имеют шаровидную форму. Они обитают преимущественно в органах дыхания и пищеварительных путях. Чаще всего патогены локализуются в полости носа, горле и толстом кишечнике. Некоторые виды бактерий с легкостью преодолевают межтканевые пространства, поэтому при несвоевременном лечении они могут поражать печень, сердце, мозг и выделительную систему.
Согласно международной классификации, выделяют следующие виды стрептококков:
- альфа-гемолитический (зеленящий);
- бета-гемолитический;
- гамма-стрептококк (негемолитический).
Наибольшую угрозу для здоровья пациента представляет стрептококковая инфекция горла, которая спровоцирована бета-гемолитическим стрептококком. В процессе размножения он выделяет концентрированные токсические вещества, вызывающие тяжелые системные осложнения. Пиогенная бактерия очень часто провоцирует развитие тонзиллита, тонзиллофарингита, скарлатины, трахеобронхита, пневмонии и других заболеваний. Бета-гемолитический стрептококк приводит к развитию ревматизма, воспаления мозга и гломерулонефрита.
Согласно медицинским наблюдениям, дети до 2-3 лет крайне редко болеют стрептококковой инфекцией. Но в период становления иммунной реактивности риск развития бактериального воспаления резко возрастает.
Чтобы вовремя идентифицировать заболевание, стоит рассмотреть типичные проявления самых распространенных инфекционных заболеваний горла.
Стрептококковая ангина
Стрептококковая ангина – бактериальное воспаление зева и компонентов глоточного кольца, а именно – небных миндалин. От момента инфицирования до появления первых признаков болезни проходит не более 4 суток. Как правило, ангина начинается резко, о чем свидетельствует симптомы интоксикации – слабость, мышечная и головная боль, тошнота и т.д.
К типичным проявлениям болезни относят:
- повышение температуры;
- дискомфорт в горле;
- увеличение подчелюстных лимфоузлов;
- ломоту в теле;
- снижение аппетита;
- тошноту;
- лихорадку.
При появлении подобной симптоматики желательно осмотреть ротовую полость больного на предмет воспаления небных миндалин и белого налета на стенках горла. В большинстве случаев бактериальный налет и некоторое увеличение гланд наблюдается на 3 сутки после инфицирования. При обнаружении симптомов нужно обратиться за помощью к ЛОР-врачу.
Болезненность подчелюстных лимфоузлов, отсутствие кашля и белый налет на миндалинах в большинстве случаев свидетельствует о развитии стрептококковой инфекции.
Развитию болезни способствуют дисбактериоз, гиповитаминоз, переохлаждение и нерациональный прием антибактериальных средств. У детей развитие инфекции часто сопровождается образованием гнойных очагов на поверхности гланд. Если не лечить ангину, со временем это приведет к абсцессу паратонзиллярной и заглоточной области.
Скарлатина
Скарлатиной называют детское заболевание, которое вызывается стрептококками типа А (бета-гемолитический). Лихорадка, сыпь на языке и стенках горла – типичные симптомы развития воспаления в горле. Инкубационный период в среднем составляет 3-10 дней. В редких случаях уже через несколько часов после инфицирования пациенты начинают жаловаться на боли в животе, лихорадку, недомогание и ломоту в теле.
Наряду с вышеупомянутыми симптомами, также отмечаются:
- шелушение кожи;
- мелкоточечная сыпь на языке;
- головные боли;
- острый тонзиллит;
- высокая температура;
- отсутствие аппетита;
- тошнота и рвота.
Диффузный гломерулонефрит и некротический лимфаденит – осложнения, которые возникают в случае запоздалого лечения скарлатины.
При осмотре пациента наблюдается покраснение небных дужек, гланд, язычка и задней стенки горла. При несвоевременном обращении к специалисту ангина может перейти в фолликулярную форму. Тогда на небных миндалинах образуются гнойные прожилки с густым слизистым налетом. Одновременно с симптомами интоксикации у больных развивается регионарный лимфаденит, о чем свидетельствует болезненность шейных лимфоузлов при пальпации.
Стрептококковый фарингит

Стрептококковый фарингит – острое воспаление слизистой глотки и лимфоидных тканей на задней стенке горла. Чаще всего заболевание встречается у детей и подростков до 14 лет. Если в воспалительные реакции вовлекаются гланды, у пациентов диагностируют тонзиллофарингит.
Как правило, стрептококки в горле локализуются в лимфаденоидных тканях, вызывая сильный отек и воспаление. В классических случаях типичным считается острое начало болезни, для которого характерны:
- головные боли;
- недомогание;
- высокая температура;
- тахикардия;
- сухой кашель;
- боль при глотании;
- озноб;
- сиплость голоса;
- боли в животе;
- тошнота.
При осмотре больного наблюдается покраснение стенок горла и разрыхление небных миндалин. В местах локализации болезнетворной флоры слизистая покрыта желтоватым налетом. Со временем на мягком небе появляются мелкие красные точки, свидетельствующие о небольших кровоизлияниях.
Для стрептококковых инфекций не типично вовлечение в патологический процесс гортани, которое приводит к частичной или полной потере голоса.
Развернутая симптоматическая картина тонзиллофарингита наблюдается при эпидемиях и крупных вспышках заболевания в больших коллективах. Не так давно инфекционистами было замечено, что в эндемических условиях, т.е. при локальных вспышках инфекций у отдельных лиц, стрептококковая болезнь протекает значительно легче и без осложнений.
В большинстве случае фарингит купируется самопроизвольно даже без применения лекарственных средств. В течение недели температура тела спадает до нормальных отметок, а местные и общие симптомы заболевания сходят на нет. И все-таки, при появлении стрептококкового фарингита у детей стоит обратиться к педиатру, так как при сниженном иммунитете он может дать осложнение на печень и почки.
Течение болезни у детей
Детский организм подвержен аллергизации, поэтому симптомы заболевания проявляются остро. Проникая в кровь, метаболиты бактерий провоцируют аллергические реакции, вследствие чего пораженные воспалением ткани сильно отекают. По этой причине возникает риск критического сужения просвета дыхательных путей, что может привести к удушью.
Если стрептококковая инфекция поражает детей грудничкового возраста, о развитии болезни могут сигнализировать:
- капризность;
- гнойные выделения из носа;
- отказ от пищи;
- плаксивость;
- высокая температура;
- потливость;
- диарея;
- рвота.
Дети постарше могут самостоятельно известить родителей об ухудшении самочувствия. Как правило, они жалуются на недомогание, боли в горле, тошноту, слабость, болезненность в области шеи. При осмотре ротоглотки можно обнаружить белый налет на гландах и корне языка.
При поражении горла стрептококками у детей часто поднимается температура до фебрильных отметок – 38,5-39 градусов.
Гнойные процессы в органах дыхания приводят к ухудшению самочувствия маленького пациента. Из-за нарастания симптомов интоксикации возникает першение в горле, сухой кашель, ломота в теле и т.д. Если в течение 3-4 суток после появления первых признаков болезни на теле возникает мелкая сыпь, скорее всего, ребенок заразился скарлатиной.
Помимо болезней горла, бактериальное воспаление приводит к поражению других жизненно важных органов. Нередко тонзиллиту, скарлатине и фаринготонзиллиту сопутствуют этмоидит, сфеноидит, евстахиит, средний отит и бронхит. В большинстве случаев побочные заболевания возникают при неадекватной терапии или несвоевременно начатом медикаментозном лечении стрептококковой инфекции.
Стрептококк в горле у беременных
Согласно статистическим данным, стрептококк в горле диагностируется примерно у 20-25% женщин именно во время беременности. В первые несколько недель после зачатия в организме происходит гормональная перестройка, которая негативно сказывается на защитных силах организма. Снижение иммунитета является импульсом для стремительного размножения условно-патогенных микробов в органах дыхания.
Чтобы предупредить развитие инфекций в организме женщины, специалисты рекомендуют при планировании и во время беременности употреблять витаминно-минеральные комплексы. Они способствуют активации резервных сил организма, что препятствует снижению его сопротивляемости болезнетворным агентам. О развитии бактериального воспаления в горле могут сигнализировать:
- дискомфорт при глотании;
- недомогание;
- лихорадка;
- покраснение небных дужек;
- точечная сыпь на стенках горла;
- непрекращающийся насморк;
- болезненность лимфоузлов.

Бета-гемолитический стрептококк достаточно легко преодолевает плацентарный барьер, поэтому может вызвать нарушения в развитии плода.
На фоне снижения иммунитета у беременных нередко возникают серьезные осложнения – гнойный отит, заболевания мочевого пузыря, воспаление легких и т.д. Только своевременное реагирование на проблему и грамотное лечение позволяет не только предупредить распространение инфекции, но и снизить вероятность патологического внутриутробного развития ребенка.
Норма стрептококка
Если стрептококк – это условно-патогенный микроорганизм, то какая концентрация бактерий в горле не представляет для человека опасности? Точно сказать о количественной норме патогенов в ЛОР-органах нельзя, так как развитие бактериального воспаления зависит не столько от числа стрептококков в горле, сколько от способности организма противостоять стремительному размножению микробов.
Норма условно-патогенных бактерий в горле – весьма относительный показатель. В зависимости от баланса микрофлоры и индивидуальных особенностей иммунной защиты, показатель нормы у разных людей может существенно отличаться. Согласно микробиологическому анализу, у большинства людей на слизистой горла обитает от 103 до 105 КОЕ/мл бактерий. Однако у некоторых людей даже при концентрации стрептококков 106 КОЕ/мл воспаление не развивается.
Мазок из зева берется только в том случае, если пациент жалуется на симптомы, соответствующие развитию стрептококковой инфекции. В ходе микробиологического исследования удается точно определить возбудителя инфекции и, соответственно, назначить актуальное и эффективное лечение ЛОР-заболевания.
Осложнения
Осложненное течение стрептококковых инфекций чаще всего наблюдается при развитии ангины или фарингита. У людей с пониженной сопротивляемостью организма симптомы развития побочных заболеваний могут проявляться уже через неделю после инфицирования горла. К числу относительно легких осложнений можно отнести:
- гнойный отит;
- лимфаденит;
- воспаление легких;
- гайморит;
- острый бронхит;
- паратонзиллит.
Следует отметить, что осложнения могут возникать даже после выздоровления пациента. Поэтому в течение 2-3 недель после регресса основных проявлений заболевания желательно наблюдаться у специалиста.
К поздним осложнениям, которые проявляются через 14-16 дней после выздоровления, относят:
- менингит;
- миокардит;
- пиелонефрит;
- остеомиелит;
- эндокардит;
- ревматизм.
На фоне стрептококковой бронхопневмонии у больного может возникнуть некротические заболевания легких и плевриты. Появлению осложнений способствует сливание гнойных очагов воспаления между собой. При обнаружении смешанной флоры в горле, т.е. стрептококка и стафилококка, многократно возрастает риск генерализации бактериального воспаления и развития сепсиса.
Принципы лечения
Уничтожить стрептококка, а точнее сократить его численность в органах дыхания, можно только посредством антибиотиков. Правильное и своевременное назначение препаратов – залог успешного лечения и быстрого выздоровления пациента. До точного определения возбудителя инфекции, назначаются противомикробные средства широкого спектра действия. После диагностики схема терапии может корректироваться, что позволяет сократить течение болезни и предупредить осложнения.
Как правило, антибактериальная терапия длится не более 10 дней, после чего больному назначают лекарства общеукрепляющего и иммуностимулирующего действия. При осложненном течении заболевания рекомендуется использовать лекарства в виде инъекционных растворов, которые быстро всасываются в ткани и угнетают размножение микробов. Для уничтожения стрептококковой флоры могут назначаться:
Облегчить течение заболевания можно при приеме лекарств симптоматического действия – жаропонижающие, противоаллергические, сосудосуживающие, противоотечные и т.д.
Рекомендуется дополнять медикаментозное лечение стрептококка в горле средствами народной терапии. Они сглаживают выраженность симптомов заболевания, но при этом не создают нагрузку на почки и печень. В лечении бактериального воспаления горла неплохо зарекомендовали себя отвары из шиповника, чабреца, лекарственной ромашки и шалфея.
Обильное питье ускоряет выведение продуктов жизнедеятельности бактерий из системного кровотока, за счет чего устраняются симптомы интоксикации.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику, как и обзывательство антибактериальной терапии – антибиотикотерапией, а кто мы такие, чтобы отменять традиции.
Рассмотрим основных представителей семейства, на которых больше всего шансов наткнуться в антибиотикограммах.
- Streptococcussanguis – воистину могуч и вездесущ. Обнаруживается в зубных отложениях с самого прорезывания зубов и до конца жизни, где и есть основное место его обитания. Иногда может быть обнаружен на слизистой глотки и в фекалиях, куда попадают транзитом. При этом надо помнить, что этот микроб вносит существенный вклад в процессы, связанные с кариесом, занимая в последующем ведущее место в ассоциациях микроорганизмов, выделяемых из гнойного экссудата при воспалительных процессах в челюстно-лицевой области, включая одонтогенные абсцессы мозга и других органов. Кроме того, они же могут быть выделены их крови и сердечных клапанов больных инфекционным эндокардитом.
- Streptococcussalivarius – также является одним из основных компонентов нормальной микрофлоры полости рта, а также, но в меньшем количестве, может быть выделен со слизистых дыхательного, желудочно-кишечного и урогенитального тракта. Особенно часто выделяются при анализе микрофлоры языка, слюны и фекалий. И крайне редко из крови при менингитах, септицимии и эндокардитах.
- Streptococcusmutans – выделяется с поверхности зубов и фекалий. Этот микроб является кариесогенным, а значит, может в дальнейшем вызывать бактериемию и бактериальный эндокардит у пациентов, не занимающихся регулярной санацией кариозных очагов в полости рта.
- Streptococcusmitis – в норме выделяется из слюны, мокроты фекалий, при этом может выделяться из верхних дыхательных путей и крови при нозокомиальном инфицировании.
- Совсем неверно упоминать в этом блоке стрептококки группы Anginosus -Streptococcusintermedius/S.anginosus/S.constellatus, но так как мы обсуждаем в основном орофарингеальную флору, способную вызвать инфекционные эндокардиты (и чтобы не писать еще один, совсем малюсенький блок), мы упомянем их здесь. В норме они являются представителями пародонтогенной группы. Но стоит представителю группы S.intermedius оттуда выбраться, как он может вызывать абсцессы печени, мозга и эндокардиты, так как проявляет высокую тропность к их тканям.
Диагностические аспекты
Освоив вышеприведенный материал, мы видим, что только обнаружение данных микроорганизмов в стерильных средах может указывать на них как на потенциальных возбудителей. Почему все-таки потенциальных? Да потому, что в 80% случаев это может оказаться банальной контаминацией в связи с несоблюдением техники забора материала (все мы дышим, и если материал забирается с нарушением правил асептики и антисептики и без использования закрытых систем, то налететь в пробирку может много чего и не только из наших рта и носов). Таким образом, посевы нужно повторять.
Обнаружение этого же зоопарка в местах естественного его обитания не говорит нам практически ничего, если только пациент совсем не следит за полостью рта, и тогда ему можно настоятельно рекомендовать посещение стоматолога.
Аспекты антибактериальной терапии
Группа зеленящих стрептококков природно резистентна к тетрациклинам, макролидам и клиндомицину (до 50% штаммов), к биссептолу резистентно более 75%. Таким образом об этих группах мы даже не вспоминаем.
Само лечение должно быть комплексным и часто в сочетании с хирургическим. Выбор конкретных препаратов будет зависеть от локализации процесса, тяжести состояния пациента и выделенного возбудителя
Например, чувствительность Streptococcus mitis будет выглядеть так (нажмите на картинку для увеличения):
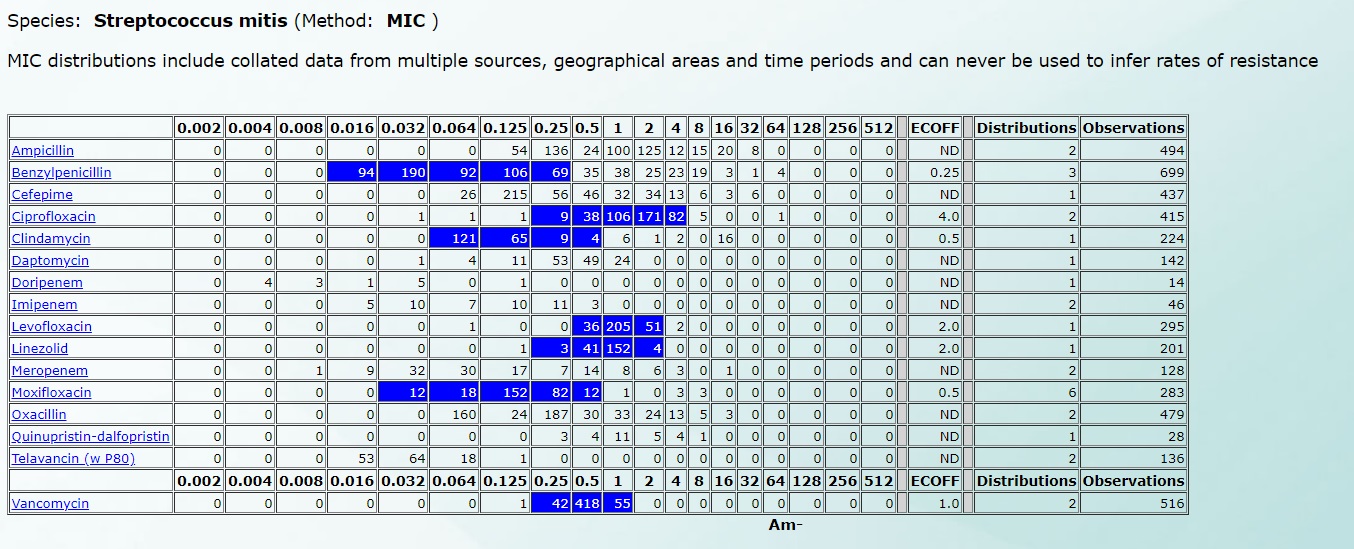
А чувствительность к Streptococcus mutans – вот так (нажмите на картинку для увеличения):
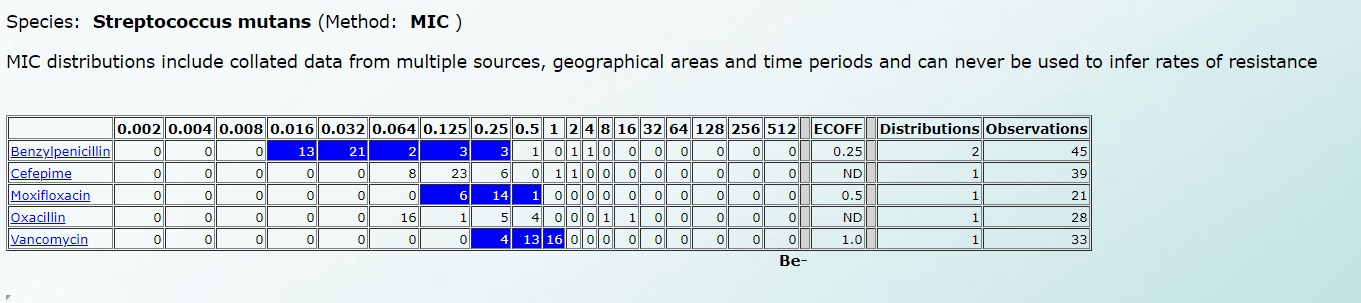
Подробнее все рассмотреть можно по этой ссылке, ведь именно на этой базе данных работают автоматические и полуавтоматические анализаторы в микробиологических лабораториях.
Препаратами выбора будут являться:
- Пенициллин в высоких дозировках (до 24 млн ЕД в сутки), возможно, в сочетании с аминогликозидами
- Цефтриаксон
- Ванкомицин
Как и в случае с любым стрептококком, крайне важно соблюдать длительность лечения, и она должна быть не менее 10-14 дней. Исключение составляет бактериальный эндокардит, там сроки лечения как минимум удваиваются.
В заключение хотелось бы сказать, что как ни прискорбно это сознавать, но недоступность, в первую очередь финансовая, адекватной стоматологической помощи вновь привела к всплеску заболеваний связанных с неблагополучием в полости рта, таким образом, мы вновь вынуждены вспоминать, что инфекционный эндокардит – это не только болезнь наркоманов и лиц со сниженным иммунным статусом, но и тех, у кого недостаточно средств на хорошего стоматолога, а потому и нам не лишне иногда осматривать полость рта у пациентов с инфекциями кровотока или абсцессами в головном мозге или печени.
История применения антибактериальных препаратов переживает определенную цикличность. В доантибиотиковую эру среди возбудителей тяжелых инфекций преобладали Гр(+) возбудители, потом пришли антибиотики, и во время второй мировой основными возбудителями стали Гр(-) возбудители (по принципу «свято место пусто не бывает), но тут Гр(+) опять подняли голову, т.к. выяснилось, что свыше 80% штаммов стафилококков продуцируют пенициллиназу и разрушают бензилпенициллин и аминопенициллины.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: врач – клинический фармаколог Трубачева Е.С.
Staphylococcus aureus делится на две группы – мецитиллинчувствительные (MSSA) и мецитиллинрезистентные (MRSA):
1. MSSA вырабатывают беталактамазы – пенициллиназы, которые разрушают незащищенные пенициллины, но сохраняют высокую чувствительность к оксациллину и цефазолину. Кроме того они обладают лейкоцидином Пантона-Валентайна, который вызывает распад тканей практически в любом очаге, что служит косвенным подтверждением стафилококковой инфекции еще до получения микробиологического анализа.
2. MRSA в свою очередь подразделяются на госпитальные, которые характеризуются тем, что:
- являются полирезистентными, т.е. нечувствительные ко всему классу бета-лактамов, включая карбапенемы;
- у них отсутствует лейкоцидин Пантона-Валентайна, поэтому реже возникают деструктивные процессы (пациенты просто тихо и долго гниют, в отличие от инфекций, вызванных дикими штаммами)
- вызывают нозокомиальные пневмонии, инфекции кожи, ран, сепсис, бак эндокардит протезированных клапанов, инфекции имплантов.
и внебольничные MRSA, характеризующиеся:
- полирезистентностью;
- наличием лейкоцидина Пантона-Валентайна, благодаря которому они более агрессивны и вызывают некротизирующие заболевания кожи, сосудов и легких (особенно четко роль лейкоцидина Пантона-Валентайна видна в развитии некротизирующей пневмонии);
- в основном характерны для наркоманов и лиц без определенного места жительства.
Факторами риска MRSA инфекций являются
- назофарингеальная колонизация MRSA;
- лечение бета-лактамами (выбивается чувствительная флора и ее место занимает MRSA;
- нахождение в ОРИТ;
- повреждение кожи при длительной госпитализации более 2-х недель (п/о раны, ожоги, язвы);
- внутрисосудистые катетеры и импланты;
- мед. работники и члены их семей (соседи – реаниматологи или хирурги, если семьи между собой общаются)
Для чего мы все это вспоминаем? Дело в том, что основные проблемы, связанные со стафилококковой инфекцией, это:
- Широкое распространение в медицине и как следствие недооценка проблемы.
- Назначение эмпирической терапии без учета риска MRSA, и как следствие – отсрочка адекватной терапии, что в случае золотистого стафилококка в прямом смысле смерти подобно.
- Клиническая эффективность антибиотика in vitro не всегда тоже самое что in vivo (мы все таки отличаемся от чашки Петри).
- Неадекватное дозирование и длительность терапии (недостаточные дозы и короткие курсы) – отсюда осложнения и рецидивы.
- Высокая летальность при неадекватной терапии
Проводить антистафилококковую терапию меньше 3-х, а то и 4-х недель нельзя, так как для этого возбудителя характерно развитие метастатических очагов и весь процесс пойдет по новому, только с учетом еще и того, что возбудитель окажется резистентным к ранее проводимой терапии.
Когда можно лечить 2 недели стафилококковую инфекцию?
- В/в катетер или другой источник инфекции удален (хорошо если катетер, а если речь об импланте – его же не удалишь).
- Инфекционный эндокардит исключен по данным чрезпищеводной ЭХО-КГ.
- Отсутствуют импланты (протезированный клапан, кардиостимулятор, А-В фистула).
- Нормализация температуры и отрицательная гемокультура в течение 72 ч после удаления источника инфекции.
- Нет признаков метастатических очагов на других органах и тканях.
Во всех остальных случаях лечим 21-28 дней. А что происходит у нас? Максимум 10-14 дней пролечили и отпустили.
Антистафилококковые препараты мы обязаны назначить сразу как только получили положительную гемокультуру на стафилококк однократно! И только потом проводим повторную проверку, так как максимально раннее начало антибактериальной терапии в 2-3 раза снижает летальность.
Итак, как уже стало понятно, основную проблему представляют устойчивые формы S.aureus. Для их эрадикации были синтезированы и предлагаются к использованию следующие препараты
- Гликопептиды – Ванкомицин (1958 год) – категория доказательств IА
- Стрептогранины – Синерцид (в РФ отсут)
- Оксазолиндиноны – Линезолид – категория доказательств IА
- Липопептиды – Даптомицин – категория доказательств IА – Тигециклин – категория доказательств IIВ
1. Ванкомицин
Внедрен в практику в 1958 году, а первый устойчивый штамм стафилококка поймали только в 1996 году. Проблема с ванкомицинустойчивыми штамма стафилококка в том, что до сих пор нет отработанных схем преодоления этой самой устойчивости. Помимо прочего у возбудителей непрерывно нарастает МПК (минимальная подавляющая концентрация) к ванкомицину и сейчас при МПК 2 мы говорим о резистентном штамме.
Еще одна проблема – это плохо очищенные формы препарата. Если ванкомицин плохо очищен, то риск токсических нефропатий достигает 20%. К сожалению надо констатировать тот факт, что Ванкомицин отечественного разлива относится к плохо очищенным формам.
Основным и самым грозным осложнением является развитие острой почечной недостаточности, а она развивается у 40% пациентов, если дозировка препарата составляет более 4 гр/сут. А потому вводить данный препарат можно только под контролем клиренса креатинина (КК). То есть первый анализ мы проводим до введения препарата, второй через 2-3 дня и смотрим, если имеет место падение КК: если он падает на 25% – это говорит о нефротоксичном действии препарата, если на 50%, то препарат следует немедленно отменить.
Ванкомицин является бактериостатическим антибиотиком, эффективность действия мы оцениваем не ранее чем через 72 часа, а то и на 5-е сутки от начала терапии. Доза должна подбираться в соответствии с МПК возбудителя и под постоянным контролем клиренса креатинина. То есть для использования этого препарата нам необходимы хорошая клиническая и микробиологическая лаборатории.
Современные рекомендации по дозированию препарата выглядят следующим образом:
У Вас есть возможность это делать? У меня такой возможности не было и нет до сих пор, а потому мы до сих пор используем этот препарат как саперы на минном поле, где ошибиться можно только один раз.
Активность против MSSA у Ванкомицина сопоставима с плацебо, а значит применять его можно только при верифицированной MRSA, либо комбинировать с препаратами, активными против MSSA (цефазолином, например)
Следует так же помнить о том, что Ванкомицин, в виду строения его молекулы, а особенно ее размера, плохо проникает в ткани и проблемными его локализациями будут дыхательные пути, ЦНС, клапаны сердца и кости. А потому быстрого действия там не дождешься и терапия требуется очень и очень длительная.
В заключении хотелось бы сказать, что препарат хорош, но будет лучше, если вы его не будете назначать в самостоятельном режиме, а вызовете врача – клинического фармаколога, ибо назначение и дозировка таких вот препаратов входит в его непосредственные обязанности.
Что делать если клин. фарма нет, а пациент есть. И что надо соблюсти, чтобы безопасно применять ванкомицин?
- Использовать хроматографически очищенные препараты – Ванкоцин, Эдицин (в настоящих условиях это практически невозможно, торги они не выигрывают)
- Требуется коррекция гиповолемии, сердечной недостаточности (перфузия почек должна быть нормальное, иначе усугубим нефротоксический эффект)
- Избегать комбинаций с нефро- или ототоксичными препаратами (аминогликозидами, НПВС и т.д.)
- Коррекция режима дозирования по клиренсу креатинина. Если в течение 2-3-х дней он снизился вдвое от изначального, а данных за то, что он мог рухнуть не только от Ванко нет – это проявление нефротоксичности препарата.
2. Линезолид
Является чистым бактериостатиком. Производителем неоднократно заявлялось, что препарат эффективнее Ванкомицина, однако проведенные независимые метаанализы клинических исследований хорошего качества рандомизированных и с двойным слепым контролем показали, что единственное, где Линезолид имеет преимущество – это вентилятор-ассоциированный пневмонии, вызванные MRSA. В других случаях, в т.ч. и стафилококковой пневмонии, преимуществ нет никаких. Зато стоимость лечения повышается в разы.
Еще один момент, о котором умалчивается – это безопасность применения Линезолида. Да, нефротоксичности нет, но по данным того же метаанализа частота возникновения тромбоцитопений при его использовании в 11,72 раза выше чем в группе плацебо.
Таким образом, Линезолид является препаратом выбора при нозокомиальной вентилятор-ассоциированной MRSA пневмонии, где при его использовании летальность ощутимо ниже, чем при использовании ванкомицина.
3. Тигециклин (или тайгециклин)
Давайте разберемся и с ним, тем более к вам будут часто приходить и рассказывать про него как про самый препаратистый антибиотик в мире.
- Препарат позиционируется как новый класс антибиотиков, на деле это производный тетерациклина со всеми исходящими отсюда последствиями.
- Он является бактериостатиком, как все тетрациклины
- Имеет хорошую тканевую фармакокинетику, но при этом крайне низкие концентрации в плазме крови (ангиогенные инфекции из его показаний выпадают сразу)
А теперь о том, куда его следует применять:
- В качестве средства целенаправленной этиотропной терапии НИ, вызванных полирезистентными бактериями:
- БРЛС: альтернатива карбопенемам
- Ацинетобактер – альтернатива сульбактаму
- Клебсиела и E.coli – устойчивые к карбопенемам
- Stenotrophomonas maltophilia
Повторюсь еще раз, место его применения это ЦЕЛЕНАПРАВЛЕННАЯ ЭТИОТРОПНАЯ ТЕРАПИЯ, т.е. когда микроб четко установлен в результате бактериологического исследования вместе с чувствительностью к антибиотикам.
Повторюсь еще раз – место этого препарата в лечении грам-отрицательной инфекции, но никак не стафилококков. Да и вообще это препарат крайне глубокого резерва, как по характеристикам, так и по цене, т.к. в ближайшие 10 лет не будет ни одного нового препарата с Гр(-) активностью, так как их просто нет даже в проекте (медицина традиционно не успевает за возбудителями, а только пытается их догонять, о чем мы в самом начале и говорили, прослеживая эволюцию возбудителей)
4. Даптомицин.
Препарат появился у нас недавно, хотя во всем мире применяется уже очень давно (в Штатах с 2003 года)
Препарат относится к классу липопептидов и от всех имеющихся на данный момент антиMRSA препаратов отличается тем, что является бактерицидным. И этот самый эффект развивается у него очень быстро и нам не надо ждать нескольких дней. То есть антибактериальный эффект мы можем оценивать как и у всех бактерицидных препаратов через 48 часов от начала применения, а это очень важно у больных в тяжелом состоянии. Еще одним несомненным плюсом является то, что не происходит лизиса клеток и не увеличивается интоксикация.
Основными показаниями к применению являются:
- Эндокардит,
- Менингит,
- Остеомиелит,
- Инфекции у больных с нейтропенией,
- Сепсис стафилококковой этиологии
Также препарат может использоваться в эмпирической терапии (кстати, единственный из всех имеющихся на данный момент) Гр(+)инфекций, так как активность против MSSA и MRSA одинаковая.
Кроме того, препарат проявляет активность против MRSA в биопленках, а значит нет необходимости в удалении протезов и имплантов. А значит Даптомицин показан при ангиогенных инфекциях (бактериемиях), остеомиелите, бактериальном эндокардите.
- Препарат откровенно дорог
- В связи с крупным размером молекулы имеются проблемы с тканевой кинетикой, а потому пневмонии и инфекции ЦНС на данный момент мы им не лечим.
- Побочные эффекты – миалгии, производитель говорит о необходимости следить за КФК и обращать пристальное внимание на пациентов уже имеющих подобные проблемы.
- Описано несколько случаев эозинофильных пневмоний, а потому и на это следует обращать внимание, так как при своевременной диагностике и вовремя назначенной терапии, данный вид пневмонии проходит без следа.
Итак, сводя все к общему знаменателю:
Ванкомицин мы используем тогда, когда у нас верифицирован MRSA стафилококк, имеется хорошая микробиологическая лаборатория, которая нам даст его МПК и это МПК не будет больше 2 (иначе он уже резистентен), в наличие есть клинический фармаколог, который посчитает дозу, будет ее контролировать и корригировать согласно изменениям клиренса креатинина. Но при этом мы помним о том, что препарат не работает на MSSA. И конечно же мы продолжаем помнить о его высокой нефротоксичности, если не имеем возможности пользоваться высокоочищенными формами.
Тигециклину нечего делать антистафилококковой терапии, этот препарат предназначен только для этиотропной терапии Гр(-)инфекции.
В связи с высокой активностью против MRSA и MSSA, быстрым бактерицидным эффектом является препаратом выбора при ангиогенных инфекциях, сепсисе и инфекционном эндокардите, а также препаратом выбора при эмпирической терапии MRSA+MSSA. Не использовать при лечении нозокомиальных пневмоний и инфекций ЦНС.
Читайте также:

