Стафилококковый менингит у новорожденного
Обновлено: 18.04.2024
Осложнения острого бактериального менингита у новорожденного и детей
а) Васкулит представляет собой компонент патологического комплекса гнойного менингита. Он может привести к тромбозу вен или мелких и изредка крупных артерий с вторичными некрозами (Taft et al., 1986). Локализация ишемических очагов непостоянная, от четко отграниченных участков до диффузных некротических поражений, способных вызывать мультикистозную энцефаломаляцию. Ишемические повреждения встречаются и без тромбозов сосудов. Воспаление сосудистых стенок капилляров ЦНС может позволить микроорганизмам проникнуть в паренхиму мозга с появлением небольших очагов септических некрозов. Вероятно, такие некрозы дают начало абсцессам мозга, которые в редких случаях осложняют бактериальный менингит.
Васкулит шунтирующих вен также играет важную роль в генезе субдуральных кровоизлияний. Очаговая мозговая симптоматика, такая как гемиплегия или моноплегия, также являются следствием васкулита. Инфаркт в спинном мозге является необычным осложнением, связанным с вовлечением сосудов. Это было отмечено только в одном случае (Boothman et al., 1988). В случае появления двустороннего сенсорного или моторного дефицита в ходе течения бактериального менингита следует предположить инфаркт спинного мозга (Glista et al., 1980). Другие необычные неврологические симптомы включают в себя двигательные расстройства (Burstein и Breningstall, 1986), дисфункцию гипоталамуса и центральный несахарный диабет (Greger et al., 1986). Нейровизуализация позволяет тонкую оценку типа и локализации соответствующих поражений. Они обычно представлены участками пониженной плотности с периартериальной или более широкой локализацией. Некоторые поражения могут содержать геморрагический компонент.
Очаговая мозговая симптоматика, такая как паралич III, VI или реже VII черепных нервов, встречается при пересечении воспаленных лептоменингеальных пространств. Такие параличи обычно возникают как следствие перенесенного менингита. Ранее сообщалось об опсоклонусе (Rivner et al., 1982).
Припадки, которые встречаются у 30-40% детей, страдающих острым бактериальным менингитом, могут быть вторичными в связи с лихорадкой или возбуждением мозга при их генерализации и развитии на ранних стадиях заболевания. Парциальные припадки из-за локализованного поражения полушарий, как правило, развиваются в результате васкулита. В некоторых случаях развивается эпилептический статус, требующий незамедлительного лечения для предотвращения стойких повреждений.
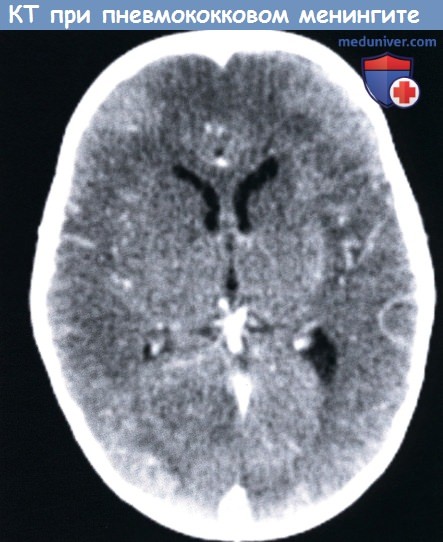
КТ с контрастным усилением у десятимесячного мальчика с пневмококковым менингитом: мозговой инфаркт вызванный васкулопатией,
небольшая левосторонняя субдуральная эмпиема и тромбоз заднего саггитального синуса.
б) Субдуральные кровоизлияния все больше признаются в качестве осложнений острого бактериального менингита и встречаются у 20-50% больных детей, но обычно в виде ограниченного слоя и объема клинически они малозначимы (Syrogiannopoulos et al., 1986, Cabral et al., 1987). Большинство кровоизлияний локализуются с обеих сторон над лобно-теменными областями. Субдуральная жидкость редко содержит кровь, но имеет непропорционально высокое соотношение альбумина с глобулином (Rabe et al., 1968). Постоянная или рецидивирующая лихорадка, очаговая неврологическая симптоматика и устойчиво положительные культуры СМЖ, вероятно, более тесно связаны с повреждениями коры, чем с наличием кровоизлияний (Syrogiannopoulos et al., 1986; Snedeker et al., 1990). Массивные кровоизлияния, сопровождающиеся увеличением окружности головы или повышением ВЧД, встречаются редко, но требуют выполнения дренирования.
Большинство субдуральных скоплений разрешается самостоятельно. Snedeker et al. (1990) обнаружили, что пациенты с кровоизлияниями более склонны к неврологическим расстройствам и судорогам на протяжении острого периода заболевания, но потеря слуха, приступы и задержка развития не встречались с большей частотой при последующем наблюдении. Субдуральная эмпиема является редкой (Jacobson и Farmer, 1981). Эмпиема часто характеризуется сохранением лихорадки и симптомов инфекции и признаков, связанных с очаговой симптоматикой, такой как судороги и гемиплегии. Диагноз устанавливается на основании методов нейровизуализации, которые показывают скопления вне ткани мозга с периферическим усилением сигнала. Диффузионно-взвешенные изображения (ДВИ) оказались эффективными для дифференциальной диагностики кровоизлияний и эмпиемы (Hunter и Morriss, 2003).
в) Повышенное внутричерепное давление (ВЧД) тяжелой степени является серьезным осложнением бактериального менингита и может возникнуть в результате разных механизмов: гидроцефалия из-за измененной абсорбции СМЖ или нарушенного тока, или в связи с отеком ткани мозга. Острая гидроцефалия вызвана повышенной резистентностью к циркуляции и резорбции ликвора из-за наличия тонкого лептоменингеального экссудата в базальных цистернах или по конвекситальной поверхности мозга вблизи пахионовых грануляций, или вследствие вентрикулита с обструкцией водопровода. Это обычно преходящее явление, но может привести к возникновению поздней гидроцефалии, если разовьется обширный менингеальный фиброз. Отек мозга., очевидно, происходит в результате нескольких механизмов. Они включают в себя цитотоксический отек, ускоренный гибелью клеток из-за инфекции, вазогенный отек из-за увеличенной капиллярной проницаемости, связанной с воспалительным ответом на инфекционный процесс, и интерстициальный отек при нарушении обычной резорбции СМЖ. SIADH может встречаться с острым бактериальным менингитом (Kaplan и Feigin, 1978) и приводить к гипонатриемии и гипотонии внеклеточной жидкости, усугубляя отек мозга.
Клинические проявления высокого ВЧД не всегда могут быть очевидны. Они включают снижение уровня сознания, головную боль и рвоту, напряжение родничка и расхождение швов, патологический зрачковый ответ и гипертензию с брадикардией (рефлекс Кушинга). Отек сосочка зрительного нерва встречается редко, особенно на ранних стадиях. Компьютерная томография может выявить исчезновение дифференцировки на серое и белое вещество, сдавление желудочков и борозд и уменьшенные базальные цистерны. МРТ может показать набухание извилин, а ДВИ поможет при различении цитотоксического отека (ограниченное распространение) от вазогенного отека. Мониторинг ВЧД может быть неотъемлемой частью лечения в случаях выраженной или устойчивой внутричерепной гипертензии (Goitein et al., 1983; Minns et al., 1989). Лечение заключается в фиксации головного конца кровати с подъемом, примерно на 30° и назначении маннитола или других гиперосмолярных веществ (для уменьшения цитотоксического отека). Более активные меры описаны в отдельной статье на сайте. Внутричерепная гипертензия связана с уменьшением мозговой перфузии и сниженной скоростью кровотока в мозге (McMenamin и Volpe, 1984), так что необходимо избегать даже незначительных эпизодов системной гипотонии, способных приводить к серьезным последствиям (Kaplan и Fishman, 1988).
в) Вентрикулиты почти постоянно встречаются у новорожденных детей с менингитом, но сравнительно редки у детей старшего возраста. Когда вентрикулит сопровождается стенозом сильвиева водопровода, инфекция становится ограниченной (пиоцефалия) и может проявляться как абсцесс мозга. В большинстве случаев диагноз вентрикулита ставится по устойчиво положительным культурам ликвора с наличием или без клинических проявлений. Сканирование мозга может позволить определить вентрикулит с аномальным расширением желудочков мозга и отеком прилежащих перивентрикулярных областей белого вещества. В полостях желудочков может появляться взвесь (Fukui et al., 2001). Вентрикулит может отреагировать на высокие дозы парентеральных антибиотиков, но может потребоваться местное лечение и дренирование. При отсроченном лечении у выживших развивается склонность к гидроцефалии.
Устойчивая лихорадка и другие септические осложнения являются результатом одновременной бактериемии. Они включают септический артрит, перикардит, пневмонию, эндофтальмит и гипопион (Kaplan и Fishman, 1988). Артрит, появляющийся через 5-7 дней антибиотикотерапии, вероятно, опосредован иммунными механизмами и часто реагирует на противовоспалительные средства (Rush et al., 1986). В тяжелых случаях могут наблюдаться гастроинтестинальное кровотечение, анемия и диссеминированное внутрисосудистое свертывание, особенно, но не исключительно при менингококковом менингите. В 13% случаев лихорадка продолжается 10 дней и более, особенно при пневмококковом менингите, и вторично рецидивирует у 16% пациентов (Lin et ah, 1984). Лихорадка может быть связана с сохранением очагов воспаления, поверхностным тромбофлебитом из-за внутривенных инфузий, нозокомиальных инфекций или септических или асептических абсцессов. Чаще всего причина не выявляется. В таких случаях показана люмбальная пункция. Если ребенок на вид здоров и показатели СМЖ приближаются к нормальным, антимикробная терапия может быть прекращена в обычные сроки.
МРТ в Т1 -режиме: билатеральные значительные экстрааксиальные скопления,
преимущественно в субдуральном пространстве, у ребенка с пневмококковым менингитом. MPT до контрастирования (слева) и после контрастирования (справа):
вентрикулит и вторичная гидроцефалия как осложнение двустороннего менингоэнцефалита.
г) Неврологические осложнения. Неврологические осложнения затрагивают почти половину пациентов, перенесших менингит, и даже у лиц с нормальными познавательными способностями в сравнении с бывшим ранее качество жизни значительно снижается. Наиболее распространенными проблемами, наблюдающимися после менингита, являются трудности с обучением и нейромоторные расстройства, потеря слуха, эпилепсия, речевые и языковые проблемы, рубцы (особенно после менингококковой инфекции), нарушения зрения и заболевания глаз, и нарушения поведения. Результаты исследований сильно варьируют, также зависящие от этиологии микроорганизмов.
Тяжелый дефицит обучения и нейромоторный дефицит обнаружены у 5-10% детей (Grimwood et ah, 1995, 2000; Bedford et ah, 2001), перенесших бактериальный менингит, немного хуже последствия среди новорожденных (11%) (Stevens et ah, 2003) и в развивающихся странах. Подавляющее большинство этих детей обучаются по специальным программам или посещают специальные школы. Эти дети с более высокой частотой осложнений имеют худший исход. Существуют некоторые расхождения между результатами различных исследований.
Feldman и Michaels (1988) сообщили, что успехи в школьном обучении 10-12-летних детей после гемофильного менингита (Н. influenzae) не имели значимых отличий от их сибсов, не отмечено неспособности к обучению, дефицита внимания или поведенческих отклонений. Pomeroy et ah (1990) и Taylor et ah (1990) также обнаружили более низкий уровень стойких осложнений (всего примерно 14%) и лишь 1% и 4% пациентов соответственно стали тяжелыми инвалидами. Baraffet ah, (1993) проанализировали исходы у 4920 детей, перенесших менингит, в 45 опубликованных работах после 1955 г. Из этих детей 1602 ребенка были включены в 19 проспективных исследований, проведенных в развитых странах, у 4,2% были выявлены расстройства обучения или умственная отсталость; у 3,5% наблюдались мышечные спазмы или парезы; у 4,2% судороги; у 16,4% отмечался минимум один основной неблагоприятный исход, включая интеллектуальные осложнения, неврологический дефицит, судороги или глухоту. Различные возбудители были связаны с разными исходами; худшие исходы наблюдались у перенесших пневмококковый менингит, 15,3% развившихся осложнений по сравнению с 7,5% у детей с менингитами, вызванными N. meningitidis и 3,8% с H. influenzae. Grimwood et ah (1995) исследовали 158 детей, выживших после менингита в период между 1983 и 1986 годами (74% с H. influenzae тип В): в 8,5% случаев дефицит был значительным (IQ
Нейросенсорная тугоухость среднетяжелой и тяжелой степени встречается у 10% детей с менингитом (Pomeroy et ah, 1990; Taylor et ah, 1990; BarafF et ah, 1993) и является двусторонней в 4-5% случаев. Потеря слуха, как полагают, развивается в результате лабиринтита, предположительно, в связи с распространением воспаления из субарахноидального пространства через водопровод улитки (Kaplan et ah, 1981;Eaveyetah, 1985).Риск развития глухоты повышается, если концентрация глюкозы в ликворе при госпитализации менее 1,1 ммоль/л (Dodge et ah, 1984), при судорогах наблюдавшихся до поступления и если стерилизация СМЖ запаздывает. Лечение цефуроксимом связано с задержкой стерилизации ликвора по сравнению с цефтриаксоном, и это могло повлиять на ранние испытания дексаметазона (Schaad et ah, 1990; van de Beek et ah, 2007). Глухота, видимо, появляется рано при менингите. Это трудно обнаружить клинически, поэтому систематическая оценка слуха должна проводиться до выписки из стационара по вызванной при аудиометрии реакции (Vienny et ah, 1984; Cohen et ah, 1988).
Повторное обследование рекомендовано после выписки, если отклонения выявлялись при первоначальной оценке. Ранние вызванные реакции могут быть с временными изменениями примерно в 20% случаев, с восстановлением за 1-2 месяца (Vienny et al., 1984). Тугоухость не связана с возрастом пациентов и продолжительностью заболевания до госпитализации, таким образом, маловероятно ее предотвращение при постановке раннего диагноза. Использование дексаметазона в лечении уменьшает частоту нарушения слуха. Глухота чаще отмечается у детей с атаксией, но встречается и при ее отсутствии у большинства пациентов. Атаксия, по всей вероятности, имеет вестибулярное происхождение, хотя в некоторых случаях возможны дисфункции мозжечка (Kaplan et al., 1981). Практически все пациенты в состоянии компенсировать дефицит баланса за несколько недель и месяцев.
Стойкая эпилепсия встречается у 2-5% пациентов (Pomeroy et al., 1990; Taylor et al., 1990; Baraff et al., 1993). Она может быть изолированной, но часто связана с трудностями в обучении и другими неврологическими осложнениями разной степени тяжести. Такие осложнения являются следствием паренхиматозных изменений в результате прямого или токсического воздействия патогенных микроорганизмов, васкулитов, и возможно, гипоксии и повышенного ВЧД.
Хроническая гидроцефалия — нетипичное последствие острого детского бактериального менингита. Она вызывается менингеальным фиброзом базальных цистерн или конвекситальной поверхности мозга, или стенозом сильвиева водопровода в результате гранулематозного эпендиматита. Хроническая гидроцефалия может быть следствием ранней обструктивной гидроцефалии. Чаще всего она развивается незаметно, оставаясь нераспознанной в течение недель и месяцев. Поэтому после перенесенного менингита у новорожденных показано систематическое ультразвуковое обследование ЦНС, так как расширение желудочков может развиться задолго до увеличения окружности головы. Ведение на ранних стадиях осуществляется путем внешнего дренажа с последующим шунтированием.
Другие неврологические осложнения включают гемиплегию, тетраплегию и слабость в конечностях, которые встречаются у 1 -4% пациентов. Слепота вследствие гнойного менингита развивается редко. Это может быть связано с внутриглазной патологией, с невритом глазного нерва или иметь кортикальное происхождение.
Стрептококковый менингит - (m. streptococcica) гнойный менингит, возникающий при генерализации стрептококковой инфекции или при проникновении возбудителей в мозговые оболочки из близлежащих органов (среднего уха, околоносовых пазух и др.). Характеризуется бурным началом с развитием отека-набухания головного мозга, энцефалической очаговой симптоматики, поражением других органов и систем.
Что провоцирует / Причины Стрептококкового менингита:
Возбудителем менингита являются стрептококки, которые представляют собой сферические или овоидные клетки размером 0,5–2,0 мкм, в мазках располагающиеся парами или короткими цепочками, при неблагоприятных условиях могут приобретать вытянутую или ланцетовидную форму, напоминая коккобациллы. Неподвижны, спор и капсул не образуют, анаэробы или факультативные анаэробы, температурный оптимум - 37 °С. По наличию спе¬цифических углеводов в клеточной стенке выделяют 17 серогрупп, обозначаемых заглавными буквами латинского алфавита.
Гемолитические стрептококки группы А являются основными возбудителями болезней у человека. Они ответственны за фарингиты, скарлатину, целлюлиты, рожистые воспаления, пиодермии, импетиго, стрептококковый синдром токсического шока, септический эндокардит, острый гломерулонефрит и другие заболевания.
Стрептококки группы В заселяют носоглотку, ЖКТ и влагалище. Серовары 1а и 111 тропны к тканям ЦНС и дыхательных путей и наиболее часто вызывают менингиты и пневмонии у новорожденных, а также поражения кожных покровов, мягких тканей, пневмонии, эндокардиты, менингиты и эндометриты, поражения мочевых путей и осложнения хирургических ран при кесаревом сечении.
Возбудителем менингита является гемолитический или зеленящий стрептококк, обладающий выраженными токсическими свойствами, которые обусловливают вирулентность микроба и его агрессивность. Основными из них являются: фимбриальный белок, капсула и С5а-пептидаза.
Фимбриальный белок - основной фактор вирулентности, являющийся типоспецифическим антигеном. Он препятствует фагоцитозу, связывает фибриноген, фибрин и продукты их деградации, адсорбирует их на своей поверхности, маскируя рецепторы для компонентов комплемента и опсонинов, вызывает активацию лимфоцитов и образование антител с низким аффинитетом.
Капсула является вторым по значимости фактором вирулентности. Она защищает стрептококи от антимикробного потенциала фагоцитов и способствует адгезии к эпителию.
Третьим фактором вирулентности является С5а-пептидаза, которая подавляет активность фагоцитов. Важную роль в патогенезе играют также стрептокиназа, гиалуронидаза, эритрогенные (пирогенные) токсины, кардиогепатический токсин, стрептолизин О и S.
Несмотря на широкое распространение стрептококковой инфекции с обширной и разнообразной патологией, гнойные менингиты стрептококковой природы встречаются редко. Возбудителями являются гемолитический и зеленящий стрептококки (И. Г. Вайнштейн, Н. И. Гращенков, 1962). Подчеркивая редкость заболевания, Ноуnе и Herzen (1950) указывают, что в мировой литературе до 1948 г. они нашли только 63 случая стрептококкового менингита. По статистическим данным, стрептококковый менингит наблюдается преимущественно у грудных и маленьких детей, чаще возникая в период стрептококковой септицемии при гнойном отите, роже лица, воспалении придаточных полостей носа, эндокардите, тромбофлебите мозговых синусов и других гнойных очагах (Biedel, 1950; Baccheta, Digilio, 1960; Mannik, Baringer, Stokes, 1962). В значительном проценте случаев источник гнойного менингита остается невыясненным (Hoyne, Herzen, 1950).
Эпидемиология
Резервуаром является больной человек или бактерионоситель. Основные пути передачи: контактный, воздушно-капельный и алиментарный (через инфицированные пищевые продукты, например молоко). Болеют дети любого возраста, но чаще новорожденные, у которых менингит развивается как проявление сепсиса. У 50 % новорожденных наиболее часто заражение происходит вертикальным путем - при прохождении плода по родовым путям, инфицированным стрептококками.
Значительная колонизация родовых путей матери стрептококками приводит к раннему развитию менингита (в течение первых 5 суток), а у детей, инфицированных небольшой дозой, менингит развивается значительно позднее (от 6 суток до 3 мес.). У 50 % больных новорожденных, не имеющих конкретного очага инфицирования, менингит развивается в течение 24 часов, при этом смертность достигает 37 %. Из общего числа детей с поздними проявлениями инфицирования, развития менингита и бактериемии погибают 10–20 %, а у 50 % выживших детей наблюдаются грубые остаточные явления. У больных септическим эндокардитом менингит может возникнуть как результат эмболии сосудов мозговых оболочек.
Патогенез (что происходит?) во время Стрептококкового менингита:
Чаще всего входными воротами инфекции являются поврежденные кожные покровы (опрелости, участки мацерации, ожоги, раны), а также слизистые оболочки носоглотки, верхних дыхательных путей (стрептодермия, флегмона, абсцесс, гнойно-некротический ринит, назофарингит, отит, трахеобронхит и др.). Однако в большинстве случаев источник развития гнойного менингита выявить не удается. Исход инфицирования стрептококком новорожденного ребенка в прямой степени зависит от состояния его клеточных и гуморальных факторов защиты и величины инфицирующей дозы.
В месте внедрения стрептококк вызывает не только катаральное, но и гнойно-некротическое воспаления, откуда быстро разносится по всему организму лимфогенно или гематогенно. Находящийся в крови стрептококк, его токсины, ферменты, приводят к активации и повышению уровня биологически активных веществ, нарушению гемостаза, обменных процессов с развитием ацидоза, повышением проницаемости клеточных и сосудистых мембран, а также ГЭБ. Это способствует проникновению стрептококка в ЦНС, поражению мозговых оболочек и вещества мозга.
Симптомы Стрептококкового менингита:
Клинические проявления стрептококкового менингита не имеют специфических черт, отличающих его от других вторичных гнойных менингитов.
Заболевание начинается остро, с повышения температуры тела, анорексии, озноба, головной боли, рвоты, иногда повторной, выраженных менингеальных симптомов. Возможно развитие энцефалических проявлений в виде нарушения сознания, клонико-тонических судорог, тремора конечностей. Характерными для стрептококкового менингита являются признаки тяжелой септицемии: высокая с большими размахами температура тела, геморрагическая сыпь, увеличение размеров сердца, глухость сердечных тонов. Закономерно страдают функции паренхиматозных органов, возникает гепатолиенальный синдром, почечная недостаточность, поражение надпочечников. При остром течении болезни признаки тяжелой септицемии и энцефалические проявления могут преобладать над менингеальными симптомами. Стрептококковый менингит при эндокардите часто сопровождается поражением сосудов мозга с кровоизлияниями в подпаутинное пространство, ранним возникновением очаговой симптоматики. Характерно развитие отека-набухания головного мозга, но абсцессы мозга развиваются редко.
Стафилококковый и стрептококковый менингиты, как правило, бывают вторичными. Выделяют контактные и гематогенные формы. Контактные гнойные мненигиты развиваются при остеомиелите костей черепа и позвоночника, эпидурите, абсцессе мозга, хроническом гнойном среднем отите, синусите. Гематогенные менингиты возникают при сепсисе, остром стафилококковом и стрептококковом эндокардите. Воспалительный процесс в оболочках мозга характеризуется склонностью к абсцедированию.
Начало болезни острое. Основной жалобой являются сильные головные боли разлитого или локального характера. Со 2-3-го дня болезни выявляется менингеальная симптоматика, общая гиперестезия кожи, иногда судорожный синдром. Часто поражаются черепные нервы, возможно появление патологических рефлексов, в тяжелых случаях наблюдаются расстройства сознания и нарушение стволовых функций. Цереброспинальная жидкость опалесцирующая или мутная, ее давление резко повышено; плеоцитоз преимущественно нейтрофильный или смешанный в пределах от нескольких сотен до 3-3 тыс. клеток в 1 мкл; содержание сахара и хлоридов снижено, белка повышено. При исследовании крови обнаруживают нейтрофильный лейкоцитоз, увеличение СОЭ. Диагноз основывается на данных анамнеза, клинических проявлениях и результатах исследования крови и цереброспинальной жидкости (обнаружение в них возбудителя).
Необходимо раннее активное лечение первичного гнойного очага на фоне антибактериальной терапии оксациллином, аминогликозидами, цефалоспоринами, бисептолом и др. (в зависимости от чувствительности выделенного штамма возбудителя). Антибактериальную терапию сочетают с применением антистафилококкового гамма-глобулина, антистафилококковой плазмы, бактериофага, иммуномодуляторов. Прогноз тяжелый, определяется как непосредственным поражением ЦНС, так и течением общего септического процесса.
Диагностика Стрептококкового менингита:
Основные диагностические критерии стрептококкового менингита:
1. Эпиданамнез: заболевание развивается на фоне стрептококкового сепсиса, реже - другого стрептококкового заболевания, возбудитель распространяется гематогенно или лимфогенно, болеют дети любого возраста, но чаще новорожденные.
2. Начало менингита острое, с развитием признаков тяжелой септицемии: значительных размахов температурной реакции, наличия геморрагической сыпи, гепатолиенального синдрома и выраженных менингеальных симптомов.
3. Нередко быстро развивается отек-набухание головного мозга, энцефалическая очаговая симптоматика.
4. Часто протекает с вовлечением в инфекционный процесс других жизненно важных органов и систем (печени, сердца, легких, надпочечников).
5. Выделение гемолитического стрептококка из ЦСЖ, крови подтверждает этиологический диагноз.
Лабораторная диагностика
Общий анализ крови. В периферической крови обнаруживается лейкоцитоз, нейтрофилез, сдвиг формулы крови влево, повышенная СОЭ.
Исследование ликвора. В цереброспинальной жидкости выявляется высокий нейтрофильный плеоцитоз (тысячи клеток в 1 мкл), повышение содержания белка (1–10 г/л) и снижение уровня глюкозы. При бактериоскопии обнаруживают грамотрицательные кокки.
Бактериологическое исследование. Выделение возбудителя является наиболее достоверным методом. Производят его путем посева крови, слизи из носа и зева, мокроты, ликвора на кровяной агар. На жидких средах стрептококки дают придонный, поднимающийся вверх рост. Для дифференцирования выявленные микроорганизмы засевают на тиогликолевую среду, полужидкий агар.
Бактериоскопическое исследование. При бактериоскопии в мазках выявляют типичные грамположительные кокки, образующие короткие цепочки, но могут быть обнаружены и полиморфные формы.
Серологическое исследование. Серотипирование проводят в реакции латекс-агглютинации или коагглютинации с помощью моноклональных антител, меченных флюоресцинами.
Лечение Стрептококкового менингита:
Вторичный гнойный менингит протекает не менее тяжело, чем менингококковый менингит. Лечение надо начинать уже на догоспитальном этапе с введения пенициллина. Его назначают по 200 000 - 300 000 ЕД/кг массы тела в сутки внутримышечно.
При пневмококковом менингите доза пенициллина составляет 300 000-500 000 ЕД/кг в сутки, при тяжелом состоянии - 1 000 000 ЕД/кг в сутки. При стрептококковом менингите пенициллин назначают по 200 000 ЕД/кг в сутки.
При стафилококковом и стрептококковом менингите внутримышечно применяют также полусинтетические пенициллины (метициллин, оксациллин, ампициллин) в дозе 200-300 мг/кг в сутки. Можно назначить левомицетина сукцинат натрия в дозе 60-80 мг/кг в сутки, клафоран - по 50-80 мг/кг в сутки.
При менингите, вызванном палочкой Пфейффера-Афанасьева, кишечной палочкой, бациллой Фридлендера или сальмонеллами, максимальный эффект дает левомицетина сукцинат натрия, который назначают в дозе 60-80 мг/кг в сутки внутримышечно с интервалом в 6 - 8 ч. Эффективен также неомицина сульфат - по 50 000 ЕД/кг 2 раза в сутки.
Рекомендуют также морфоциклин - по 150 мг 2 раза в сутки внутривенно капельно.
При стафилококковом менингите вводят стафилококковый анатоксин в дозе 0,1-0,3-0,5-0,7-1 мл внутримышечно, антистафилокковый гамма-глобулин - по 1 - 2 дозы внутримышечно в течение 6 - 10 дней, иммунизированную антистафилококковую плазму - по 250 мл 1 раз в 3 дня.
Профилактика Стрептококкового менингита:
В профилактике стрептококковых менингитов важную роль играет популяризация сведений о путях распространения инфекции, Так как заболевание чаще передается воздушно-капельным путем, больной и окружающие должны знать, что инфицирование возможно при разговоре, кашле, чихании. Важную роль в профилактике менингита играют гигиенические навыки, бытовые условия.
К каким докторам следует обращаться если у Вас Стрептококковый менингит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Стрептококкового менингита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Острый бактериальный менингит у новорожденного и детей: причины, клиника, диагностика
Каждый год более 1,2 миллиона людей заболевают острым бактериальным менингитом, причем более чем 170 тысяч случаев имеют летальный исход, большинство из которых приходится на детский возраст (ВОЗ, 1998,2008). Несмотря на новые антибиотики и лечение, смертность за последние 20 лет по существу осталась неизменной. Среди выживших, примерно у половины имеются неврологические или другие осложнения после заболевания. Несколько факторов способствует этой неутешительной ситуации: отсроченная постановка диагноза из-за неспецифического характера симптомов, появление устойчивых штаммов болезнетворных микроорганизмов, слабость иммунологической защиты новорожденных детей, и отсутствие возможности предотвратить ущерб от воспалительного ответа хозяина посредством добавочных нейропротекторных или противовоспалительных механизмов.
а) Эпидемиология. Относительная заболеваемость острым бактериальным менингитом изменяется соответственно возрасту, социальным условиям жизни, географическому местоположению и политике иммунизации. В развитых странах за прошлое десятилетие эпидемиология острого бактериального менингита претерпела разительную перемену, и уровень заболеваемости снизился приблизительно до 4-5 случаев на 100000 населения, тогда как во многих развивающихся странах он остается высоким в пределах 40-50 случаев на 100000.
Вакцинация вызвала радикальное изменение в относительной частоте трех основных патогенных микроорганизмов — Haemophilus influenzae, Neisseria meningitidis и Streptococcus pneumoniae. H. influenzae тип В (HiB) был наиболее распространенным возбудителем детского бактериального менингита в Великобритании, с показателями заболеваемости в пределах 21-44 на 100000 среди детей до пяти лет, с пиковым возрастом 6-7 месяцев и коэффициентами смертности 2,4-4,3% (Вооу и Мохon, 1993; Вооу et al., 1993; Anderson et al., 1995; Heath и Me Vernon, 2002). После введения в начале 1990-х во многих странах комбинированной белково-полисахаридной вакцины против HiB, число случаев гемофильного менингита снизилось более чем на 90% (Schuchat et al., 1997), и S. pneumoniae и N. meningitides стали самыми обычными болезнетворными микроорганизмами.
В настоящее время в Европе уровень распространенности пневмококкового менингита составляет примерно 0,5 на 100000 населения; связанная с ним смертность 25%, но может достигать 45% среди очень молодых. Более чем у 30% выживших остаются постоянные неврологические осложнения (Lexau et al., 2005). Эта картина существенно хуже в развивающихся странах. Существует сезонное изменение с пиком в зимние месяцы. Дети младшего возраста наиболее подвержены риску, и 60% случаев приходится на возраст до двух лет. Комбинированная семивалентная белково-полисахаридная пневмококковая вакцина стала доступной в 2000 г. и была включена в британский национальный календарь прививок с 2006 г.
В тех странах, где эта вакцина включена в программу иммунизации, наблюдалось разительное снижение уровня инвазивной пневмококковой болезни, с сохранением N. meningitidis в качестве основного патогенного микроорганизма. Уровень заболеваемости N. meningitidis составляет около 1-3 на 100000 населения в Европе с самими обычными серотипами группы В и С. Вакцинация доступна, но пока еще только для групп А, С, Y и W135. C комбинированной полисахаридно-белковой вакциной против группы С. Она была включена в протокол иммунизации во многих развитых странах после введения в Великобритании в 1999 г. В Северной Америке недавно запущена 4-валентная вакцина для других групп (А, С, Y и W135) (Расе и Pollard, 2007).
Еще одной проблемой эпидемиологии стало появление резистентных к лекарственным средствам штаммов патогенных микроорганизмов, среди которых серьезную опасность представляет резистентный к пенициллину пневмококк (ПРП), встречающийся благодаря мутациям в одном или нескольких пенициллин-связывающих белках. Появление ПРП непосредственно связано распространением антибактериальных средств, и в определенных странах проблема больше, чем в других. В настоящее время в Великобритании менее 3% пневмококков являются ПРП, а в Испании, США и Южной Африке показатели выше. Резистентность пневмококков проверяется лабораторным анализом минимальной концентрации ингибитора (Minimum Inhibitory Concentration, MIC), и может быстро определяться с помощью специальных тестов с ПЦР для определения гена связывающего белка пенициллина 2b (ПРП2b). Устойчивость к пенициллину и хлорамфениколу при менингококковой инфекции также увеличивается, но к счастью, остается редкой.
б) Патофизиология и иммунология. Эффективная инвазия инфекции в ЦНС включает 4 стадии: в первой происходит, адгезия и колонизация патогенных микроорганизмов, часто из комменсалов носоглотки; вторая представляет собой инвазию в слизистую оболочку с последующим размножением и бактериемией; третья состоит в проникновении в подпаутинное пространство с преодолением ГЭБ, с пока еще не установленным механизмом; и наконец, размножение патогенов в подпаутинном пространстве, вызывающее воспалительный ответ хозяина.
• Адгезия и колонизация. Точные механизмы, посредством которых бактерии прикрепляются и проникают в слизистую оболочку, все еще неясны. Вовлекаются многочисленные поверхностные белки микроорганизмов (например, холиновые связывающие белки, сиаловая кислота и нейраминидаза на S. pneumoniae и К1-полисахарид на Е. coli) (Koedel et al„ 2002) и специфические рецепторы хозяина (например, pIgR). В случае менингококка пили прикрепляется к рецепторам CD46 и 66 клеток слизистой оболочки.
• Инвазия и размножение. Поверхностные белки (например, Psp А и С) и капсула пневмококков помогают сопротивляться фагоцитозу и разрушению комплиментом, для того, чтобы преодолеть защиту хозяина и выжить в пределах кровотока.
• Внедрение в ЦНС. Для проникновения патогенов в ЦНС должны быть нарушены ГЭБ и барьер между кровью и спинномозговой жидкостью (СМЖ). В этот процесс вовлечены различные гликоконъюгаты и рецепторы (например, фактор активации тромбоцитов). Было продемонстрировано, что количество бактерий в заражающем материале крови важно для возникновения менингита у экспериментальных животных, и это может также иметь место у людей (Moxon et al., 1974).
• Размножение. В СМЖ, в области ослабленной защиты хозяина, выживание и размножение патогенов наиболее вероятны. Тем не менее, их присутствие стимулирует перемещение лейкоцитов в СМЖ посредством многошагового процесса, включающего в себя различные адгезивные молекулы и лиганды (например, селектины и интегрины) с миграцией по градиенту хемотаксиса. При разрушении болезнетворных микроорганизмов запускается воспалительный каскад, который приводит к вторичному повреждению ткани. Стимуляция происходит через клеточую стенку (например, LPS у грамотрицательных микроорганизмов, таких как N. meningitidis и Н. influenzae и пептидогликаны у грамположительных микроорганизмов, таких как S. pneumoniae) (Tuomanen et al., 1985), прямо от пневмолизина (Friedland et al., 1995), и непосредственно через бактериальную ДНК (Deng et al., 2001). Через несколько часов запускаются провоспалительные цитокины, включая ФНО-α (TNFα) (Bazzoni и Beutler, 1996) и интерлейкины 1β, 6 и 8.
Они ускоряют каскад других цитокинов, хемокинов, протеолитических ферментов и реактивных кислородных радикалов и промежуточных форм азота из макрофагов, нейтрофилов и тромбоцитов. В экспериментах на крысах назначение дексаметазона и антиоксидантов показало частичное уменьшение эффекта (Auer et al, 2000). Гиперемия сосудов и повышение проницаемости кровеносных сосудов приводит к цитотоксическому и вазогенному отеку ткани мозга и увеличенному внутричерепному давлению (ВЧД), что в дальнейшем снижает церебральное перфузионное давление (ЦПД), увеличивая риск вклинения и необратимого повреждения головного мозга. Объем СМЖ увеличивается в течение первых двух или трех дней болезни (Ashwal et al., 1992), и уровни эндотоксинов (Mertsola, 1991) и других цитокинов (Arditi et al., 1989) коррелируют с тяжестью расстройств (Dulkerian et al., 1995). Частым осложнением является васкулит, приводящий к инфаркту в 2-19% случаев. Уровень мозгового кровообращения снижен на 30-70% у 30% пациентов (Ashwal et al., 1992), но авторегуляция кровообращения в основном сохранена (Ashwal et al., 1990).
Отек (цитотоксический, вазогенный и межуточный) встречается часто, как изолированно, так и с острой обструктивной гидроцефалией, обусловленной гнойным экссудатом в полостях, и может вызывать внутричерепную гипертензию и вторичное выбухание мозговой ткани. Это в свою очередь может еще больше препятствовать мозговому кровообращению (Minns et al., 1989), запуская порочный круг. Также происходит повреждение нейронов путем апоптоза, особенно в зубчатой извилине гиппокампа. Это имеет особое значение, поскольку есть доказательства, что это повреждение — причина связанных с менингитом трудностей в обучении (Loeffler et al., 2001). В экспериментах на животных гиппокампальное повреждение существенно уменьшалось в результате блокады активации каспазы-3 или управления специфическими каспаза-3-ингибиторами (Braun et al., 1999). Появление менингеального выпота может привести к хронической гидроцефалии, особенно у детей младшего возраста.
Гидроцефалия также может быть результатом стеноза сильвиева водопровода, который может возникнуть вследствие вентрикулита. Последний чрезвычайно распространен среди новорожденных и был выявлен в 92% патологоанатомических исследований (Berman и Banker, 1966), но также присутствует и у детей старшего возраста в более низкой пропорции (приблизительно 10%).

г) Клинические проявления и диагностика. Важность ранней постановки диагноза очевидна. Тем не менее, поздняя диагностика остается частой, потому что менингит относительно редко распознается в общей практике в сравнении с частыми, главным образом, вирусными, заболеваниями, сопровождающимися лихорадкой. Часто менингиту в течение нескольких дней предшествует лихорадка, поэтому невозможно определить его фактическое начало; в результате 33-40% пациентов до постановки диагноза получали антибиотики (Kaplan et al., 1986). Характер начала заболевания имеет важное прогностическое значение: прогрессирующее начало, сливающееся с предыдущими проявлениями болезни, часто прогнозирует благоприятный исход, в то время как молниеносное начало неблагоприятно (Radetsky, 1992, Kilpi et al., 1993). Лихорадка, тошнота, головная боль, сопровождающаяся рвотой, вялость и некоторое расстройство сознания (чаще умеренное оцепенение, чем кома) указывают на диагноз (Gururaj et al., 1973). Ригидность мышц шеи, а иногда также мышц спины, и симптом Кернига требуют выполнения люмбальной пункции.
На очень ранних стадиях единственными симптомами могут быть раздражительность и перемены настроения в сочетании с лихорадкой. Генерализованные припадки встречаются у 30-40% детей с острым бактериальным менингитом, особенно среди детей младше четырех лет. В одном исследовании 328 детей с первичными припадками на фоне лихорадки и без менингеальных знаков, менингит был диагностирован только у четырех детей по данным люмбальной пункции (1,2%), все они были в возрасте до 18 месяцев (Rutter и Smales, 1977). И хотя люмбальная пункция не должна быть рутинным методом исследования среди детей в возрасте до 18 месяцев, у которых могут отсутствовать менингеальные симптомы при лихорадочных припадках, она обязательна в случаях, когда ребенок не возвращается в абсолютно нормальное состояние вскоре после эпизодов припадков. Аналогично, люмбальная пункция проводится и детям до одного года при наличии малейших сомнений. Менингит у новорожденных может сопровождаться фебрилитетом или гипотермией и проявляться в виде затруднений при кормлении и дыхании. Ригидность мышц шеи и изменения родничка нетипичны. Люмбальная пункция обычно выполняется при любых септических проявлениях у нездоровых новорожденных.
Наличие пятнисто-папуллезной сыпи может служить ранним симптомом менингококкового сепсиса или проявлением вирусного заболевания. Петехии и пурпура говорят в пользу менингококковой инфекции, хотя также периодически встречаются при наличии вторичного сепсиса при гемофильной (тип В), пневмококковой инфекции или при некоторых вирусных заболеваниях (например, ECHO 9). Очаговая неврологическая симптоматика, такая как паралич черепных нервов или гемипарез обычно развивается поздно в ходе течения бактериального менингита, или раньше в качестве осложнения повышенного ВЧД (особенно параличи VI пары черепных нервов). Отек сосочка зрительного нерва редко заметен на ранних этапах; в сущности, наличие отека сосочка зрительного нерва должно вызывать подозрение о наличии очагового внутричерепного процесса, такого как абсцесс мозга или массивное повреждение, и является показанием к нейровизуализации до проведения люмбальной пункции.
При всех возможных рисках люмбальной пункции при менингитах на фоне повышенного ВЧД (Klein et al., 1986), отказ от выполнения пункции на раннем этапе заболевания значительно осложнит уход за больным ребенком. Диагноз на основе СМЖ, как было показано, изменил тактику ведения в 72% случаев с отсрочкой люмбальной пункции до тех пор, пока назначение антибиотиков повышало уровень стерильной СМЖ с 3% до 44%. Вероятность отека мозговой ткани, с предполагаемым риском смерти оценивается на уровне 4,3% (Rennick et al., 1993) и 6% (Wright et al., 1993; Lambert,1994). Люмбальная пункция, как предполагается, вызывает опущение мозгового конуса спинного мозга, хотя данных для определения явления как причины или следствия нет, а отеки мозговой ткани могут возникать и спонтанно.
Применение КТ для обнаружения отека или повышенного ВЧД чрезвычайно ограничено (Pike et al., 1990, Heyderman et al., 1992), и не способно предсказать риск опущения конуса. Данные полученные при компьютерной томографии заставили изменить тактику ведения пациентов в 5% случаев, при этом спинальная пункция откладывалась в среднем на 2,5 часа (Gopal et al., 1999). Кроме того, нормальные данные КТ не означают безопасное выполнение пункции, и в 36% случаев опущения, КТ было в пределах нормального. Используя строгий отбор пациентов, количество проведенных КТ можно значительно уменьшить (Hasbun et al., 2001). Mellor (1992) советовал откладывать спинномозговую пункцию по крайней мере на 30 минут после припадков, так как известно, что они вызывают транзиторное повышение ВЧД, и назначение маннитола перед проведением люмбальной пункции показано в сомнительных случаях, что обеспечивало эффективное снижение уровня ВЧД и повышение ЦПД и скорости кровотока (Goh и Minns, 1993). Другим противопоказанием к проведению спинальной пункции является необходимость срочного лечения шока (Lambert, 1994).
Это касаетс, прежде всего, менингококковой инфекции, диагностируемой по культуре крови. Таким образом, целесообразно отложить спинномозговую пункцию в случаях тяжелого угнетения сознания, когда ребенок находится в состоянии шока и когда имеется расширение зрачков, офтальмопарез или отек диска зрительного нерва.

е) Лабораторная диагностика:
Количество клеток в СМЖ при бактериальном менингите обычно колеблется между 1000 и 10000/мм 3 , и первоначально преобладают полиморфноядерные лейкоциты, но уровень более пяти одноядерных клеток считается ненормальным, а в 10% случаев отмечается преобладание лимфоцитов на ранних этапах. В норме нейтрофилы отсутствуют, но в цитоцентрифугированных образцах может быть обнаружен случайный единичный нейтрофил. После пункции возможно соотношение нейтрофилов и эритроцитов равное 1:700, если в периферической крови количество клеток красной крови и белых кровяных телец в пределах нормы.
Микроорганизмы можно обнаружить в мазках как внутриклеточно, так и внеклеточно. Окраска по Граму положительная в 25% случаев, в зависимости от концентрации патогенов в СМЖ (Onorato et al., 1980). Использование акридинового оранжевого, флюорохрома, окрашивающего нуклеиновые кислоты некоторых является исключение других возможно поддающихся лечению причин. Тщательные клинические, неврологические и лабораторные методы обследования определяются для каждого конкретного случая.

2. Другие лабораторные процедуры. Культура крови положительна в 80-90% случаев нелеченного менингита. Иногда культура крови может быть положительна, в то время как культура СМЖ отрицательная и, таким образом, информативна для терапии. Посевы из носа и зева не являются специфичными и чувствительными. Культура мочи и мазки из поражений кожи, окрашенные по Граму, дают возможность непосредственной идентификации патогенов.
Бактериологическое исследование жидкости из среднего уха, полученной при аспирации, в случаях сопутствующего среднего отита может выявить тот же микроорганизм, что и в ликворе, но это явление непостоянно, и даже при выявлении бактерии в обеих жидкостях нередко возможны разные штаммы.
Проводится подсчет форменных элементов крови с анализом воспалительного ответа. Обычно имеет место подъем лейкоцитов и повышенный уровень С-реактивного белка (Hansson et al., 1993).
3. Нейровизуализация. Визуализация на ранних этапах может быть нормальной, или показывать менингеальное повышение с контрастом, но его главным образом применяют для исключения другой патологии ЦНС и для диагностики осложнений (Klein et al., 1986) (см. ниже). Riordan et al., (1993) перечисляют следующие показания к КТ: длительное угнетение сознания, длительные частичные или поздние припадки, очаговые неврологические отклонения, увеличение окружности головы, подтверждение продолжающейся инфекции, и рецидивирующие симптомы и признаки. МРТ имеет дополнительные преимущества повышенной чувствительности, но не всегда доступно.

Стафилококк чаще всего поражает маленьких детей с ослабленным иммунитетом или другими сопутствующими инфекциями. Часто стафилококк, сальмонеллы и кишечную палочку находят у малышей с дисбактериозом. Таким образом, именно нарушения местного иммунитета оказываются основной причиной возникновения стафилококковой инфекции.
Примечательно, что стафилококки являются чрезвычайно устойчивыми к действию многих антибиотиков, поэтому всегда есть риск того, что ребенок заболеет гнойно-септической болезнью.
Как же ребенок может заразиться стафилококком? Носителями этой опасной бактерии являются как больные, так и здоровые люди, ведь существуют разные формы носительства инфекции (временная и постоянная). Течение заболевания также может происходить в легких и тяжелых формах. Стафилококк вызывает сепсис, менингит, пневмонию, абсцессы и гнойные воспаления кожи и других тканей. При генерализации воспалительного процесса у новорожденных детей часто развивается сепсис.
Представление о том, что микроорганизм поражает только кишечник ошибочно. Объекты поражения стафилококковой инфекцией крайне вариативны: верхние и нижние дыхательные пути, слизистые оболочки рта, носа, кишечника, кожные покровы, костная и хрящевая ткани и т.д.
Детский организм поражают стафилококки трех групп:
Эпидермальный стафилококк. Среди разновидностей стафилококков, эпидермальный обладает средним инфекционным потенциалом. Встречается на кожных покровах и слизистых, но при нормальной работе иммунитета носителя никак себя не проявляет. Признаки бактериального поражения проявляются только в том случае, если иммунитет носителя ослаблен: после перенесенного оперативного вмешательства, вирусного заболевания и т.д. Новорожденные, особенно недоношенные дети подвержены инфицированию в особенности.
Золотистый стафилококк. Наиболее опасный и крайне вирулентный микроорганизм. У нормальных здоровых детей золотистый стафилококк пребывает в латентном состоянии. Из всех разновидностей данных микроорганизмов наиболее агрессивен.
Признаки и симптомы стафилококка у детей
В большинстве случаев (от 48% до 78%) именно бактерии стафилококка становятся причиной воспалительных заболеваний дыхательных путей, часто встречающихся у детей.
Стафилококковая пневмония может возникать после инфицирования ребенка в стационаре или родильном отделении. Болезнь нередко развивается молниеносно, с деструкцией легочной ткани и другими осложнениями. Токсины, вырабатываемые стафилококком, вызывают тяжелую интоксикацию организма, что в сочетании с пневмонией вызывает нарушение дыхательной системы и кровообращения. Больной ребенок беспокоен, мечется в постели, может стонать и кричать. Характерными симптомами также являются озноб, потливость, сухой кашель и одутловатость лица.
Стафилококковый энтероколит является чрезвычайно тяжелым кишечным заболеванием. В 13% случаев оно заканчивается летальным исходом. Заболеванию подвержены недоношенные и слабые дети. Провоцируют его также перенесенные ранее острые респираторные заболевания, приём антибиотиков, искусственное вскармливание и нарушения биоценоза кишечника.
Характер проявлений зависит, в первую очередьтипа микроорганизма:
Сапрофитный стафилококк. Для сапрофитного стафилококка характерно поражение мочеполовой системы.
Симптоматика включает в себя:
Боли внизу живота (у женщин);
Возможное развитие кольпита (у женщин);
Жжение и рези при мочеиспускании;
Боли в области почек.
Общие признаки интоксикации (редко).
Эпидермальный стафилококк даёт о себе знать одной главной особенностью: боли в области органов, а на поздних стадиях — функциональные нарушения их работы.
Золотистый стафилококк характерен развитием гнойно-некротических очагов в месте поражения. Нередко именно он становится причиной формирования фурункулов, катаральной ангины и др.
Общие и местные симптомы стафилококка у детей
Систематизируя симптоматику, можно обобщить все проявления в две большие группы: общие и местные.
Гнойное отделяемое в биологических жидкостях. Слизь из носа, мокрота с примесями гноя говорят о поражении слизистых оболочек верхних или нижних дыхательных путей.
Симптомы интоксикации. Головная боль, повышение температуры до 37.6-38.1 градуса Цельсия, гиперемия или, наоборот, бледность кожных покровов, тошнота и рвота (у детей явление особенно частое).
Нарушения со стороны желудочно-кишечного тракта. Диарея, вздутие живота, излишняя продукция кишечных газов и т.д.
У аллергически-настроенных детей возможны и иммунные реакции на токсины и ферменты, которые стафилококк выделяет в процессе своей жизнедеятельности.
Факторы риска
Интенсивность и характер проявлений зависят от множества факторов:
Возраст. Симптоматика зависит от возраста ребенка. Грудные дети страдают от стафилококковой инфекции чаще, и симптомы проявляются куда тяжелее.
Среда обитания и среда проникновения микроорганизма. Способ попадания в организм обуславливает объект поражения. Если стафилококк проник в организм с частицами пыли — проявятся поражения верхних или нижних дыхательных путей. Если с пищей — пострадает горло или кишечник.
Состояние здоровья ребенка-носителя. Между тяжестью заболевания, яркостью проявлений и ослаблением иммунной системы существует прямая зависимость. Она обозначается вполне очевидным образом: чем более ослаблен иммунитет, тем ярче проявления и тем тяжелее течение стафилококковой инфекции.
Разновидность микроорганизма. Тяжелее всего протекают поражения золотистым стафилококком.
Разновидность микроорганизма (наиболее агрессивен и опасен золотистый стафилококк, именно он в 90% случаев становится причиной инфекционных заболеваний у детей).
Причины стафилококка у детей
Существует несколько причин развития стафилококковой инфекции у детей:
Преждевременное рождение ребенка. Особенно часто страдают недоношенные дети. Причина кроется в недостаточном развитии иммунитета ребенка в утробе матери. Не меньше подвержены стафилококковому заражению дети, рожденные с помощью кесарева сечения. Иммунные проблемы и инфицирование могут дать знать о себе и в более позднее от рождения время;
Нарушения правил ухода за новорожденными детьми;
Несоблюдение правил гигиены. Стафилококковое заражение, своего рода, болезнь грязных рук. Поскольку микроорганизм крайне устойчив ко всем неблагоприятным воздействиям, он широко распространен и встретить его можно не выходя из дома. Несоблюдение элементарных правил гигиены (в том числе употребление грязных фруктов и овощей и др.) приводит к быстрому инфицированию. Проблема касается детей старшего возраста (1 год и старше), а также родителей новорожденных.
Патологические процессы в период вынашивания плода и лактации. Мать может быть инфицирована стафилококком, и при этом не подозревать. Патогенный микроорганизм может проникнуть с молоком и по ряду других причин. Так, инфицирование может случиться ещё в период вынашивания плода.
Недостаток веса. Недостаток массы тела приводит к ослаблению иммунитета.
Стафилококк у ребенка в горле, в кишечнике, в носу

Данные формы поражения имеют свои специфические проявления, по-разному диагностируются и лечатся:
Стафилококк на слизистой горла проявляет себя острой катаральной ангиной, тонзиллитом и стоматитом.
Для формы характерны специфические симптомы:
Отечность и покраснение миндалин;
Гнойные высыпания на поверхности слизистой, а также слизистых полости рта (стоматит);
Общие проявления интоксикации.
Стафилококк на слизистой кишечника провоцирует типичные признаки развития острого колита (причем поражен может быть как толстый, так и тонкий кишечник, то есть заболевание примет форму энтероколита).
Симптоматика включает в себя:
Боли в животе (блуждающие, распирающие);
Дискомфортные ощущения в эпигастральной области (тяжесть, вздутие, ощущение распирания);
Примеси гноя, крови, зеленой слизи в кале;
Поносы или запоры, тенезмы (ложные болезненные позывы опорожнить кишечник).
Трудность носового дыхания (по причине отечности);
Симптомы интоксикации организма.
Диагностика стафилококка у детей
Диагностика стафилококкового поражения достаточно сложна и требует большого уровня профессионализма от врача-специалиста. Диагностические мероприятия различаются, в зависимости от пораженного органа.
В целом, обследования включают в себя:
Сбор анамнеза включает в себя устный опрос родителей ребенка на очном приеме. Если ребенок находится в достаточном возрасте и говорит самостоятельно — дополнительно опрашивают его самого. Учитывают жалобы, предшествующие обстоятельства и т.д.
Мазки из горла и носа берутся для определения конкретного штамма бактерии, точно с теми же целями проводятся посевы микрофлоры на питательные среды. С помощью двух данных диагностических методов выводится культура инфекционного агента и определяется чувствительность бактерии к антибиотикам.
Общий анализ крови почти всегда даёт картину воспалительного процесса разной интенсивности: лейкоцитоз, высокая СОЭ, повышенное количество эритроцитов, чрезмерно повышенный гемоглобин и т.д.
В моче или кале могут быть обнаружены специфические возбудители заболевания.
Если патологический процесс заходит слишком далеко, колит, вызванный стафилококком может перейти в язвенный тип, тогда для оценки состояния толстой кишки проводят эндоскопическое исследование.
Лечение стафилококка у детей
Лечение стафилококковой инфекции — задача непростая. Когда речь идёт о лечении инфекционной патологии у детей — задача по понятным причинам усложняется ещё больше. Успех лечения стафилококковой инфекции у детей во многом зависит от своевременно обнаруженной болезни и качественной комплексной терапии, предусматривающей применение специальных препаратов антистафилококкового действия.
Очень важно как можно быстрее обратиться к педиатру, сдать анализы и получить лечение.
Терапия комплексная и включает в себя ряд терапевтических мероприятий:
Местная терапия. Заключается в нанесении лекарственных препаратов на кожные покровы и слизистые оболочки, пораженные стафилококком (гнойничковые высыпания, фурункулы и т.д.). Применяются: зеленка, пероксид водорода, мазь Вишневского.
Прием антибиотиков. Лечение антибиотиками при инфекционных патологиях (а стафилококковых особенно) должно быть осторожным. Стафилококк обладает поразительной приспособляемостью. Неграмотное антибактериальное лечение приведет к формированию бактерии, обладающей огромной сопротивляемостью и вирулентностью. Целесообразно принимать только те средства, к которым стафилококк чувствителен (для этого следует исходить из результатов бактериологических исследований, врач назначит нужный антибиотик).
Смазывания, полоскания. Для борьбы с бактерией на слизистых носа и горла применяют смазывания и полоскания антисептиками.
Для лечения стафилококка у детей всегда используют витамин С, стимулирующий иммунитет и поддерживающий ослабленный организм малыша. При наружных гнойных поражениях рекомендуется делать ванночки и частые припарки. Кожа ребенка должна быть максимально чистой и сухой. Контролировать нужно также чистоту ногтей и белья больного ребенка. Следует постоянно обрабатывать язвочки, удалять струпья и гной. Обработке и дезинфекции подлежат также бытовые предметы, посуда и одежда, которой пользовался больной ребенок.
Профилактика
Для профилактики стафилококковой инфекции необходимо соблюдать санитарные нормы и осуществлять эпидемический контроль. Беременные женщины, роженицы и новорожденные должны обязательно проходить обследование. При обнаружении гнойных воспалительных заболеваний они подлежат госпитализации и лечению в отделениях с инфекционным режимом.
Таким образом, стафилококковая инфекция представляет большую опасность для детей (как новорожденных, так и для детей старшего возраста). Особенно опасен и коварен золотистый стафилококк, обладающий высокой вирулентностью и токсической способностью. Симптоматика — крайне специфична и проявляется у каждого ребенка индивидуально. В целом — налицо картина воспаления и гнойного поражения кожи и слизистых оболочек организма (нос, горло, кишечник).

Читайте также:

