Стрептококк группы в идентификация
Обновлено: 18.04.2024
НИИ акушерства и гинекологии им. Д.О. Отта РАМН, Санкт-Петербург
НИИ акушерства и гинекологии им. Д.О. Отта РАМН, Санкт-Петербург
Журнал: Российский вестник акушера-гинеколога. 2017;17(6): 96‑100
НИИ акушерства и гинекологии им. Д.О. Отта РАМН, Санкт-Петербург
НИИ акушерства и гинекологии им. Д.О. Отта РАМН, Санкт-Петербург
НИИ акушерства и гинекологии им. Д.О. Отта РАМН, Санкт-Петербург
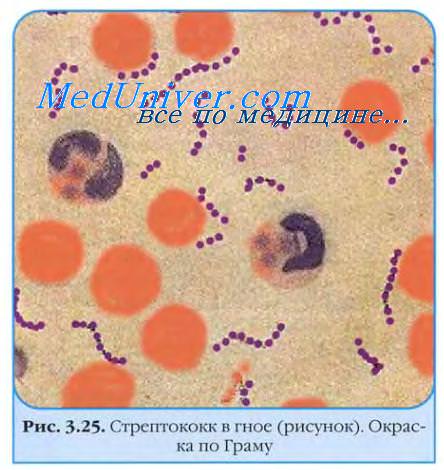
Streptococcus agalactiae (Streptococcus group B по R. Lancefield) — грамположительные кокки, образующие короткие цепочки, факультативные анаэробы, способные проявлять гемолитическую активность. Стрептококк группы В (СГВ), являющийся обитателем прямой кишки, периодически распространяется на другие локусы (влагалище, урогенитальный тракт, кожу и пр.). У большинства взрослых людей колонизация протекает бессимптомно, однако СГВ может быть причиной воспалительных заболеваний урогенитальной области, таких как вульвовагинит, уретрит, цистит и др. Наиболее высокий уровень колонизации отмечен у сексуально активных женщин репродуктивного возраста и беременных [1—3]. Известно, что S. agalactiae выделяется из влагалища у 20—40% женщин. У беременных СГВ выделяют в 7—30% наблюдений [4]. Из них 60—75% остаются СГВ-носителями до конца беременности, что достоверно связано с самопроизвольными выкидышами, преждевременными родами, преждевременным излитием околоплодных вод, ранними септицемиями новорожденных. Кроме того, у колонизированных стрептококком группы В беременных чаще развиваются инфекции мочевыводящих путей, возможен хориоамнионит в родах, а также послеродовой эндометрит [5—7]. Контаминация плода в родах стрептококком группы В происходит у каждой второй роженицы, но только у 2—5% инфицированных новорожденных развиваются тяжелые формы СГВ-инфекций с летальностью 20—70%, особенно при преждевременных родах [8]. Тяжелые инфекции ассоциированы с длительными родами и ранним разрывом плодных оболочек. Чаще всего стрептококковый сепсис регистрируют у новорожденных, родившихся у матерей с высокой степенью колонизации влагалища, тем не менее около 30% неонатального сепсиса регистрируют при небольшом количестве S. agalactiae в родовых путях [9]. Заражение плода происходит при заглатывании и аспирации инфицированных околоплодных вод или интраканаликулярно [10—12].
Согласно клиническим рекомендациям, показаниями для обследования женщин на наличие стрептококка группы В являются воспалительные заболевания урогенитального тракта, бессимптомная бактериурия беременной, преждевременные роды, СГВ-инфекция новорожденного в анамнезе, повышение температуры тела в родах, длительный безводный промежуток [13].
Выделение S. agalactiae из мочи и/или вагинально-ректального содержимого считается основанием для назначения этиотропной терапии при наличии клинических проявлений. Показаниями для антибиотикопрофилактики в родах являются положительный скрининг на СГВ в поздние сроки беременности (35—37 нед) и наличие акушерских факторов риска [14].
Поиск новых лекарственных препаратов, действующих на СГВ, является весьма актуальным. Кроме того, крайне важна возможность использования этих препаратов в ранние сроки беременности.
Материал и методы
Депантол — это вагинальные суппозитории, содержащие 100 мг декспантенола и 16 мг хлоргексидина биглюконата в виде 20% раствора. В качестве вспомогательных веществ используется смесь макроголов (макрогол 400, макрогол 1500).
В исследовании использовали основы препаратов (декспантенол, хлоргексидин и макрогол), входящих в состав депантола.
Декспантенол (ДП-гель, ДП 1:10) — прозрачная вязкая гелевая субстанция, хорошо растворимая в дистиллированной воде. Чувствительность микроорганизмов определяли как к цельному препарату, так и в разведении 1:10. Декспантенол относится к фармакологическим группам витаминов и витаминоподобных веществ, регенерантов и репарантов, а также к дерматотропным средствам. Он восполняет дефицит пантотеновой кислоты, обладает противовоспалительным действием, стимулирует процессы регенерации.
Хлоргексидин (ХГ) — прозрачная жидкость. Чувствительность микроорганизмов определяли к 20% раствору вещества, входящему в состав препарата Депантол. Хлоргексидин является антисептическим препаратом, активным в отношении широкого спектра микроорганизмов, включая грамположительные и грамотрицательные бактерии, простейшие и вирусы.
Макрогол 400 (М) — прозрачная жидкость.
Готовили микробную взвесь чистой культуры S. agalactiae, доводили до 0,5 по МакФарланду, наносили на Blood Muller-Hinton Agar и равномерно с помощью шпателя распределяли по поверхности среды. После этого 50 мкл тестируемого раствора вносили в пробитые в агаре отверстия диаметром 5 мм. Гель наносили стерильной калиброванной петлей непосредственно на поверхность агара. Инкубировали 24 ч при 37 °C в атмосфере 5% CO2.
Учет результатов чувствительности микроорганизмов к препарату проводили визуально, замеряя диаметр зоны задержки роста в миллиметрах.
Результаты
Все 25 штаммов S. agalactiae (100%) оказались чувствительными к хлоргексидину (ХГ). Зоны задержки роста вокруг отверстий с внесенным препаратом составили от 16 до 26 мм (рис. 1, 2, Рис. 1. Доля штаммов S. agalactiae, чувствительных к действующим веществам, входящим в состав депантола. Рис. 2. Рост S. agalactiae (штамм № 2) на чашке Петри с BloodMuller-HintonAgar. Зона задержки роста вокруг ДП 1:10 составляет 23 мм, вокруг ХГ — 26 мм. Рост крупных колоний стрептококка на поверхности агара в месте нанесения ДП-геля. Отсутствие зоны задержки роста вокруг М. Примечание. МК — молочная кислота, К — клотримазол. 3). Данные результаты подтверждают, что в настоящее время хлоргексидин остается одним из наиболее активных катионных антисептиков, принцип бактерицидного действия которого, как известно, заключается в последовательно протекающих процессах диссоциации солей хлоргексидина, связывании катионов с отрицательно заряженной мембраной и нарушении осмотического равновесия бактериальной клетки (потеря калия, фосфора) [15].
Интересные результаты получены и при определении чувствительности клинических изолятов S. agalactiae к декспантенолу. Чувствительными к декспантенолу в разведении 1:10 (ДП 1:10) оказались 17 (68%) штаммов стрептококков. Зоны задержки роста составили от 18 до 28 мм (см. рис. 1). Резистентными были квалифицированы штаммы, не имеющие зоны задержки роста вокруг отверстия с внесенным препаратом.

На поверхности агара, обработанной неразведенным декспантенолом (ДП-гель), в 80% случаев наблюдался следующий эффект: имело место видимое увеличение размеров колоний S. agalactiae при одновременном снижении их количества. Наблюдался рост не в форме газона, а в виде отдельных, более крупных колоний (см. рис. 2). Один штамм (4%) имел зону задержки роста вокруг нанесенного неразведенного геля (см. рис. 3). Рис. 3. Рост S. agalactiae (штамм № 15) на чашке Петри с BloodMuller-HintonAgar. Зона задержки вокруг ДП 1:10 составляет 22 мм, вокруг ХГ — 23 мм. Рост крупных колоний стрептококка на поверхности агара в месте нанесения ДП-геля и небольшая зона задержки роста (3 мм). Отсутствие зоны задержки роста вокруг М. Примечание. МК — молочная кислота, К — клотримазол.
Все штаммы стрептококков оказались резистентны к макроголу 400, используемому в качестве вспомогательного вещества суппозитория.
СГВ проявляет стабильную чувствительность к пенициллину и другим β-лактамным антибиотикам. В последние годы значительно возросла резистентность S. agalactiae к линкозамидам, макролидам, тетрациклинам, хлорамфениколу. В некоторых странах частота выделения устойчивых к клиндамицину штаммов достигла 13—20%, а к эритромицину — 25—32%. В ряде случаев встречается сочетание устойчивости к нескольким группам антибиотиков одновременно. В последнее время в Японии и США выделили штаммы S. agalactiae с высоким уровнем устойчивости к широкому спектру фторхинолонов [16, 17]. Проблема селекции микроорганизмов, устойчивых к антимикробным препаратам, в том числе стрептококков группы В, является поводом к поиску новых средств для этиотропной терапии и профилактики передачи СГВ от матери плоду.
F. Facchinetti и соавт. [18] в рандомизированном контролируемом исследовании показали высокую эффективность интравагинального применения 140 мл 0,2% раствора хлоргексидина каждые 6 ч в сравнении с внутривенным введением ампициллина в дозе 2 г каждые 6 ч для предупреждения вертикальной передачи стрептококка группы В. Полученные результаты свидетельствуют о том, что в группе хлоргексидина (109 беременных) число колонизации новорожденных стрептококком группы В составило 15,6%, что было сопоставимо с показателями группы ампициллина (108 беременных) — 12%, причем в группе хлоргексидина показатели колонизации новорожденных E. coli были статистически достоверно лучшими (лишь 1,8%; p<0,05) по сравнению с группой ампициллина (7,4%).
В 2006—2008 гг. нами была проведена оценка эффективности суппозиториев и вагинальных таблеток Гексикон, содержащих в своем составе хлоргексидина биглюконат, в лечении бактериального вагиноза. Была установлена клиническая и микробиологическая эффективность применения разных схем терапии препаратом Гексикон по окончании лечения, которая составила 66,7% для схемы в 1 суппозиторий в течение 7 дней и 96,7% для схемы в 2 суппозитория в течение 7 дней. Что касается вагинальных таблеток Гексикон, нами проведена III фаза сравнительного открытого рандомизированного исследования эффективности и безопасности препарата Гексикон (таблетки вагинальные) в сравнении с препаратом Трихопол (таблетки вагинальные) у пациенток с бактериальным вагинозом. Было показано, что вагинальные таблетки Гексикон, применяемые по 1 и 2 таблетки в течение 7 дней, сопоставимы по эффективности с вагинальными таблетками Трихопол, используемыми для лечения бактериального вагиноза. Эффективность терапии бактериального вагиноза препаратом Гексикон составила 93,3 и 100% соответственно при использовании их 1 и 2 раза в сутки.
Настоящее исследование подтвердило высокую эффективность ХГ и в отношении S. agalactiae.
Декспантенол входит в состав широкой линейки коммерческих препаратов и известен как стимулятор регенерации тканей с противовоспалительным и дерматопротективным действием. Прямой антимикробный эффект декспантенола мало изучен. В нашем опыте более 2/3 штаммов стрептококков группы В оказались чувствительными к декспантенолу в разведении 1:10, что доказывает перспективность применения декспантенола, особенно в сочетании с антисептическим средством, для комплексной терапии и химиопрофилактики инфекций, вызываемых стрептококками группы В.
Выводы
Клинические проявления стрептококковой инфекции группы B. Клиника стрептококковых поражений группы Б. Микробиологическая диагностика стрептококков группы B. Лечение инфекций вызванных стрептококками группы В.
Принципы микробиологической диагностики стрептококковой инфекции группы B аналогичны таковым при выделении стрептококков группы А. Колонии, выросшие на КА, через 24 ч после посева прозрачные или мутноватые, выпуклые, диаметром 0,5-1,0 мм, окружены зоной гемолиза (5-15% изолятов может не проявлять гемолитических свойств). S. agalactiae обычно не чувствителен к бацитрацину и триметоприм сульфаметоксазолу, что определяют в тесте с соответствующими дисками.
Весьма специфичен тест гидролиза гиппурата. Обычно его используют для дифференцировки со S. pyogenes (даёт отрицательную реакцию). Другая дифференцирующая реакция — САМР-тест, основанный на феномене усиления гемолитического действия золотистого стафилококка в присутствии гемолизинов других бактерий (рис. 12-9).

Дальнейшую идентификацию стрептококковой инфекции группы B проводят путём серотипирования в реакции латекс-агглютинации или коаглютинации с коммерческими реагентами либо при помощи инкубации мазков с моноклональными AT, меченными флюоресцеинами. Микроорганизмы можно быстро идентифицировать в мазках отделяемого влагалища, используя коммерческие наборы, аналогичные применяемым для выявления стрептококков группы А.
Лечение стрептококковой инфекции группы B
Подходы и методы терапии инфекций, вызванных стрептококками группы В, аналогичны таковым, применяемым для лечения поражений, обусловленных стрептококками группы А.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Микробиологическая диагностика стрептококка. Диагностика стрептококковой инфекции. Выявление стрептококка. Выделение стрептококка.
Основу микробиологической диагностики стрептококковой инфекции составляют выделение и идентификация возбудителя. При этом обычно биохимические характеристики изолятов не изучают. Прочие методы диагностики стрептококковой инфекции имеют различные ограничения.
Через 24 ч на КА стрептококки группы А образуют блестящие вязкие колонии (рис. 2, см. цветную вклейку). В жидких средах бактерии дают придонный, иногда поднимающийся вверх рост. Весьма информативные методы раннего выявления стрептококков — определение чувствительности к антимикробным агентам методом дисков.
Наиболее часто их используют для идентификации стрептококков в мазках из зева. Для дифференцировки стрептококков группы А от прочих b-гемолитических стрептококков применяют тест чувствительности к бацитрацину. Более чем в 99% случаев изоляты стрептококков группы А чувствительны к бацитрацину, тогда как представители других серогрупп обычно устойчивы (рис. 12-8). Также можно применить тест чувствительности к триметоприм-сульфаметоксазолу.

Стрептококки групп А и В обычно чувствительны к действию антимикробного агента.
По сравнению с чувствительностью к бацитрацину более специфичен тест гидролиза пиррол идонил-b-нафтиламида (ПИР-тест). S. pyogenes — единственный стрептококк, дающий положительную реакцию. Для этого в пробирки вносят полоски фильтровальной бумаги, пропитанные ПИР. Под действием бактериальных пептидаз ПИР расщепляется до b-нафтиламида, и после внесения 0,01% раствора p-диметиламиноциннамальальдегида полоски окрашиваются в вишнёво-красный цвет.
Стрептококки группы А легко можно выявить в мазках из зева, используя коммерческие наборы; групповой А-Аг экстрагируют химическими реагентами или ферментами и идентифицируют в реакциях латекс-агглютинации, коагглютинации или ИФА. Для экспресс-диагностики ревматического процесса и гломерулонефрита можно определять AT к стрептолизину О или стрептодорназе; серологические исследования также позволяют выявить носителей. Следует помнить, что AT к стрептолизину О не образуются при кожных инфекциях, вызываемых стрептококками группы А.
Лечение стрептококковой инфекции
Основу лечения стрептококковой инфекции составляет адекватная антибактериальная химиотерапия. Лечение ревматизма проводят пенициллинами короткого действия, профилактику — пенициллинами длительного действия (бициллин-5), причём антибиотикопрофилактику предпочтительно проводить круглогодично.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Стрептококки группы В. Streptococcus agalactiae. Эпидемиология стрептококков группы Б. Патогенез поражений стрептококками группы В.
Стрептококки группы Б обычно колонизируют носоглотку, ЖКТ и влагалище; подавляющую часть изолятов составляет S. agalactiae. Серологически стрептококки группы В разделяют на серовары la, lb, Ic, II и III. Бактерии сероваров 1а и III тропны к тканям ЦНС и дыхательных путей, они часто вызывают менингиты у новорожденных. Наиболее типичен вертикальный путь заражения — при прохождении плода по родовым путям, инфицированным стрептококками. Подобным образом происходит заражение не менее 50% детей, составляющих группу риска. У детей, родившихся у женщин со значительной колонизацией родовых путей, чаще регистрируют раннее развитие менингита (в течение первых 5 сут), а у детей, инфицированных большим количеством возбудителей, подобные поражения наблюдают позднее (от 6 сут до 3 мес).
Патогенез поражений стрептококков группы В
Гематогенное диссеминирование стрептококков группы В во многом обусловлено дефицитом специфических AT, Clq и С4 компонентов комплемента (небольшое содержание последних коррелирует с низкой бактерицидной активностью в целом). Определенную роль играет полисахаридная капсула, снижающая эффективность фагоцитарных реакций. В отличие от бактерий группы А, капсула стрептококков группы В проявляет иммуногенпые свойства, и AT к её Аг (в достаточном количестве) способны оказывать протективное действие. Как патогенетический фактор следует рассматривать и нейраминидазу, модифицирующую мембрану клеток хозяина, что облегчает адгезию микроорганизмов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Стрептококки – это факультативно-аэробные бактерии, паразитирующие в организме человека и животных. Основные места их локации – дыхательная и пищеварительная системы (особенно полость носа, рта, толстый кишечник).
Классификация бактерий данной группы проводится по типу гемолиза (разрушения красных кровяных клеток с выделением в окружающую среду гемоглобина):
- неполный гемолиз с приданием его зоне зеленоватого оттенка – альфа-гемолитические стрептококки;
- полный гемолиз – бета-гемолитические стрептококки;
- негемолитические стрептококки.
Существует также деление бета-гемолитических стрептококков на подгруппы: А, В и т.д. до U.
Наиболее клинически значимыми являются несколько видов:
1. Бета-гемолитический (пиогенный) стрептококк группы А (S.pyogenes) является широко распространенным неподвижным, не образующим споры, грамположительным микроорганизмом.
Наиболее часто он образует колонии на коже и слизистых оболочках. В отдельные периоды после наступления холодов носителем S.pyogenes является почти каждый 4-й ребенок школьного возраста. Источником заражения может быть как больной человек, так и носитель инфекции. Передача возбудителя может происходить воздушно-капельным путем, при контакте с больным и с пищей. Зарождение и развитие болезни может происходить под действием токсинов, которые вырабатывает бактерия. К ним, в частности, относятся дезоксирибонуклеаза, стрептолизин, гиалуронидаза, гемолизин, стрептокеназы (А и В).
Болезни, причиной которых является инфицирование пиогенным стафилококком, можно разделить на три группы: поверхностные заболевания, внутренние инфекции; токсинопосредствованные (причиной развития которых стали вырабатываемые микроорганизмом токсины).
К поверхностным инфекциям относятся:
- ангина;
- фарингит;
- импетиго (кожная инфекция);
- рожа (покраснение участков кожи, сопровождаемое повышением температуры тела и общим отравление организма).
Внутренние инфекции, вызываемые стрептококком группы А:
- некротический фасциит (поражение поверхностной и глубокой соединительной оболочки, покрывающей нервы, сосуды, органы и мышцы (фасции), а также подкожной клетчатки);
- миозит (воспаление скелетных мышц);
- менингит (воспаление оболочек головного и спинного мозга);
- эндокардит (воспаление внутренней оболочки сердца);
- пневмония (воспаление легких);
- послеродовой сепсис (общее воспаление, вызванное попаданием микробов в кровь и распространением их по органам).
Инфекция, вызванная токсинами, продуцируемыми бактериями:
- скарлатина;
- синдром токсического шока.
Для детей заражение S.pyogenes чревато психическими расстройствами или появлением нервного тика.
Лицам с аллергией к пенициллину и другим бета-лактамным противобактериальным средствам рекомендуется при проведении анализа исследовать чувствительность к антибиотикам.
2. Streptococcus pneumoniae. Пневмококк Streptococcus pneumoniae является представителем рода стрептококков S. pneumoniae. Бактерия вызывает инфекционные заболевания разной локации и степени тяжести. Так, в результате присутствия бактерии может развиться пневмония, бронхит, тонзиллит (ангина), фарингит (воспаление слизистой и лимфоидной тканей глотки), риносинусит (воспаление слизистой носа и околоносовых пазух). Также пневмококк является причиной обострения хронических болезней (бронхит, обструктивная болезнь легких). Способность проникать в кровь вызывает развитие:
- сепсиса (общего поражения организма);
- менингита (воспаления оболочек мозга);
- артрита (воспаления суставов);
- молниеносной пурпуры (опасного для жизни заболевания, проявляемого пятнами крови, синяками, изменением цвета кожи);
- аортита (воспаления стенки аорты);
- эндокардита (воспаления внутренней оболочки сердца);
- фасциита (поражения фасции – соединительной ткани, покрывающей сосуды, нервы, органы и мышцы организма);
- миозита (воспаления скелетных мышц) и пр.
Наибольшую опасность Streptococcus pneumoniae представляет для детей, пожилых людей и пациентов с иммунодефицитом. Заражение женщин происходит в 2 раза реже, чем мужчин. Заболевание менингитом, вызванным пневмококком, наблюдается среди пациентов самого разного возраста. Симптомы инфекции чаще всего проявляются при снижении сопротивляемости организма (переохлаждение – как частный случай).
Инфекция передается воздушно-капельным путем. Не исключено заражение ребенка в утробе от инфицированной матери. Вспышки инфекции не имеют какой-либо системы, появляются от случая к случаю, но наиболее часто – в холодное время года.
3. Бета-гемолитический стрептококк группы В (Streptococcus group В) является неподвижной, не образующей спор, грамположительной бактерией, чаще всего создающей колонии в желудочно-кишечном тракте, носоглотке, влагалище. В подавляющем количестве случаев в роли изолятора выступает S. agalactiae. Все стрептококки, входящие в группу В, разделены на несколько серотипов, в частности на la, lb, Ic, II и III.
Представители серотипов la и III привязаны к тканям дыхательного тракта и центральной нервной системы. Они являются возбудителями менингита (воспаления оболочек мозга) и пневмонии (воспаления легких) у новорожденных детей. В то же время присутствие стрептококков группы В во влагалище является нормальным – они выявляются у 5-35% обследованных беременных. Колонизация влагалища, не сопровождаемая симптомами, наблюдается в 20 случаев из 100. Особенно характерно присутствие бактерии у женщин, моложе 20 лет, которые ведут интенсивную половую жизнь с предохранением внутриматочными средствами.
Чаще всего заражение инфекцией происходит от матери к ребенку при прохождении его через родовые пути, в которых присутствуют стрептококки. Из всех детей, входящих в группу риска, половина заражена именно таким образом. Если колонизация родовых путей значительна, то в течение пяти суток велика опасность развития менингита. При большом количестве возбудителя, попавшего в детский организм, не исключено развитие болезни в период от 6 до 90 суток.
Хотя опасность заражения высока, фактическая частота развития стрептококковой инфекции с явными симптомами составляет в возрасте до недели 1,3-3:1000, после недели – 1-1,7:1000. По данным наблюдений в среднем из 100 зараженных детей только у одного обнаруживаются явные признаки инфекции.
Кроме матери, которая представляет для ребенка потенциальную опасность, заражение стрептококком может произойти от медперсонала роддома – 16-47% сотрудников родильного отделения являются носителями инфекции. Также не исключено заражение одним младенцем другого. Если даже мать ребенка здорова, то риск заразиться стрептококковой инфекцией в больнице достаточно велик – от 13 до 43%.
Во избежание послеродовых осложнений беременным женщинам рекомендуется на 33-37 неделе пройти профилактическое обследование. Это позволит своевременно выявить стрептококковую инфекцию для последующего лечения антибиотиками при родах.
Streptococcus viridans состоит в основном из непатогенных бактерий, некоторые из которых при гемолизе окрашивают среду в зеленый тон.
При выявлении агента (агентов) инфекции определяется его (их) чувствительность к следующим антибиотикам:
- Ампициллин (AM)/Клоксациллин;
- Ципрофлоксацин (CIP);
- Рифампин (RA)/Рифампицин;
- Тетрациклин (TE);
- Хлорамфеникол (C);
- Цефаклор (CEC);
- Оксациллин (OX1);
- Гентамицин (GM);
- Эритромицин (E);
- Левофлоксацин (LVX);
- Амоксициллин (AMC)/Клавуланат;
- Нитрофурантоин (FT).
Соскоб берется только в ротовой полости. Оптимальным является отбор материала утром натощак, после сна.
Перед взятием соскоба запрещается:
- проводить гигиену ротовой полости;
- принимать пищу и питье;
- жевать жвачку;
- курить.
Допускается отбор материала также через 2-3 часа после еды.
Целью посева на стрептококк является:
- подтверждение бактериальной природы острого фарингита и тонзиллита (ангины);
- диагностика скарлатины при подозрении на нее;
- подтверждение уничтожения бактерии после применения противобактериальных средств.
Поскольку бактерии S.pyogenes и S. agalactiae на 100% чувствительны к бета-лактамным антибиотикам, возможно проведение обследования без определения чувствительности к противобактериальным препаратам.
Если у пациента наблюдается непереносимость бета-лактамы или аллергическая реакция на нее, то возможен индивидуальный подбор препарата. В таком случае определение чувствительности к противомикробным средствам проводить необходимо.
Ф.И.О.: Иванов Сидор Петрович Пол: м Дата рождения: хх.хх.хххх
Дата исследования: хх.хх.хххх
Исследование
Результат
Нормы интерпретации
Примечание
[405] Посев на Стрептококк (дых. пути) (идентификация агента и чувствительность к а/б)
Дата выдачи (дата исследования): хх.хх.хххх
Соскоб с миндалин
Streptococcus Viridans 10*4 –
0 - 10x3 КОЕ/ТАМП
0 - 10x3 КОЕ/ТАМП
Ф.И.О.: Петрова Инна Ивановна Пол: ж Дата рождения: хх.хх.хххх
Дата исследования: хх.хх.хххх
[405] Посев на Стрептококк (дых. пути) (идентификация агента и чувствительность к а/б)
Читайте также:

