Стрептококк и стафилококк вызывают мононуклеоз
Обновлено: 24.04.2024
Инфекционный мононуклеоз (mononucleosis infectiosa, болезнь Филатова, ангина моноцитарная, лимфобластоз доброкачественный) - острое антропонозное вирусное инфекционное заболевание с лихорадкой, поражением ротоглотки, лимфатических узлов, печени и селезёнки и специфическими изменениями гемограммы.
Что провоцирует / Причины Инфекционного мононуклеоза:
Возбудитель инфекционного мононуклеоза- ДНК-геномный вирус рода Lymphocryptovirus подсемейства Gammaherpesvirinae семейства Herpesviridae. Вирус способен реплицироваться, в том числе в В-лимфоцитах; в отличие от других вирусов герпеса он не вызывает гибели клеток, а напротив, активирует их пролиферацию. Вирионы включают специфические антигены: капсидный (VCA), ядерный (EBNA), ранний (ЕА) и мембранный (МА) антигены. Каждый из них образуется в определённой последовательности и индуцирует синтез соответствующих антител. В крови больных инфекционным мононуклеозом сначала появляются антитела к капсидному антигену, позднее вырабатываются антитела к ЕА и МА. Возбудитель малоустойчив во внешней среде и быстро гибнет при высыхании, под действием высокой температуры и дезинфектантов.
Инфекционный мононуклеоз - только одна из форм инфекции вирусом Эпстайна-Барр, который также вызывает лимфому Бёркитта и носоглоточную карциному. Его роль в патогенезе ряда других патологических состояний недостаточно изучена.
Резервуар и источник инфекции - человек с манифестной или стёртой формой болезни, а также носитель возбудителя. Инфицированные лица выделяют вирус с последних дней инкубации и на протяжении 6-18 мес после первичной инфекции. В смывах из ротоглотки у 15-25% серопозитивных здоровых людей также обнаруживают вирус. Эпидемический процесс поддерживают лица, ранее перенёсшие инфекцию и на протяжении долгого времени выделяющие возбудитель со слюной.
Механизм передачи - аэрозольный, путь передачи - воздушно-капельный. Очень часто вирус выделяется со слюной, поэтому возможно заражение контактным путём (при поцелуях, половым путём, через руки, игрушки и предметы обихода). Возможна передача инфекции при переливаниях крови, а также во время родов.
Естественная восприимчивость людей высокая, однако, преобладают лёгкие и стёртые формы болезни. О наличии врождённого пассивного иммунитета может свидетельствовать крайне низкая заболеваемость детей первого года жизни. Иммунодефицитные состояния способствуют генерализации инфекции.
Патогенез (что происходит?) во время Инфекционного мононуклеоза:
Проникновение вируса в верхние отделы дыхательных путей приводит к поражению эпителия и лимфоидной ткани рото- и носоглотки. Отмечают отёк слизистой оболочки, увеличение миндалин и регионарных лимфатических узлов. При последующей вирусемии возбудитель внедряется в В-лимфоциты; находясь в их цитоплазме, он диссеминирует по всему организму. Распространение вируса приводит к системной гиперплазии лимфоидной и ретикулярной тканей, в связи с чем в периферической крови появляются атипичные мононуклеары. Развиваются лимфаденопатия, отёк слизистой оболочки носовых раковин и ротоглотки, увеличиваются печень и селезёнка. Гистологически выявляют гиперплазию лимфоретикулярной ткани во всех органах, лимфоцитарную перипортальную инфильтрацию печени с незначительными дистрофическими изменениями гепатоцитов.
Репликация вируса в В-лимфоцитах стимулирует их активную пролиферацию и дифференцировку в плазмоциты. Последние секретируют иммуноглобулины низкой специфичности. Одновременно в острый период заболевания нарастают количество и активность Т-лимфоцитов. Т-супрессоры сдерживают пролиферацию и дифференцировку В-лимфоцитов. Цитотоксические Т-лимфоциты уничтожают инфицированные вирусом клетки, распознавая мембранные вирус-индуцированные антигены. Однако вирус остаётся в организме и персистирует в нём в течение всей последующей жизни, обусловливая хроническое течение заболевания с реактивацией инфекции при снижении иммунитета.
Выраженность иммунологических реакций при инфекционном мононуклеозе позволяет считать его болезнью иммунной системы, поэтому его относят к группе заболеваний СПИД-ассоциированного комплекса.
Симптомы Инфекционного мононуклеоза:
Инкубационный период варьирует от 5 дней до 1,5 мес. Возможен продромальный период, не имеющий специфической симптоматики. В этих случаях заболевание развивается постепенно: в течение нескольких дней наблюдают субфебрильную температуру тела, недомогание, слабость, повышенную утомляемость, катаральные явления в верхних дыхательных путях - заложенность носа, гиперемию слизистой оболочки ротоглотки, увеличение и гиперемию миндалин.
При остром начале заболевания температура тела быстро поднимается до высоких цифр. Больные жалуются на головную боль, боли в горле при глотании, озноб, усиленное потоотделение, ломоту в теле. В дальнейшем температурная кривая может быть различной; длительность лихорадки варьирует от нескольких дней до 1 мес и более.
К концу первой недели заболевания развивается период разгара болезни. Характерно появление всех основных клинических синдромов: общетоксических явлений, ангины, лимфаденопатии, гепатолиенального синдрома. Самочувствие больного ухудшается, отмечают высокую температуру тела, озноб, головную боль и ломоту в теле. Могут появиться заложенность носа с затруднением носового дыхания, гнусавость голоса. Поражения зева проявляются нарастанием боли в горле, развитием ангины в катаральной, язвенно-некротической, фолликулярной или плёнчатой форме. Гиперемия слизистой оболочки выражена нерезко, на миндалинах появляются рыхлые желтоватые легко снимающиеся налёты. В некоторых случаях налёты могут напоминать дифтерийные. На слизистой оболочке мягкого нёба возможно появление геморрагических элементов, задняя стенка глотки резко гиперемированная, разрыхлённая, зернистая, с гиперплазированными фолликулами.
С первых же дней развивается лимфаденопатия. Увеличенные лимфатические узлы можно обнаружить во всех доступных пальпации областях; характерна симметричность их поражения. Наиболее часто при мононуклеозе увеличиваются затылочные, подчелюстные и особенно заднешейные лимфатические узлы с обеих сторон по ходу грудино-ключично-сосцевидных мышц. Лимфатические узлы уплотнены, подвижны, при пальпации безболезненны или болезненны незначительно. Их размеры варьируют от горошины до грецкого ореха. Подкожная клетчатка вокруг лимфатических узлов в некоторых случаях может быть отёчной.
У большинства больных в период разгара заболевания отмечают увеличение печени и селезёнки. В некоторых случаях развивается желтушный синдром: усиливаются диспептические явления (снижение аппетита, тошнота), темнеет моча, появляется иктеричность склер и кожи, в сыворотке крови нарастает содержание билирубина и повышается активность аминотрансфераз.
Иногда появляется экзантема пятнисто-папулёзного характера. Она не имеет определённой локализации, не сопровождается зудом и быстро исчезает без лечения, не оставляя изменений на коже.
Вслед за периодом разгара заболевания, продолжающимся в среднем 2-3 нед, наступает период реконвалесценции. Самочувствие больного улучшается, нормализуется температура тела, постепенно исчезают ангина и гепатолиенальный синдром. В дальнейшем нормализуются размеры лимфатических узлов. Длительность периода реконвалесценции индивидуальна, иногда субфебрильная температура тела и лимфаденопатия сохраняются в течение нескольких недель.
Заболевание может протекать длительно, со сменой периодов обострений и ремиссий, из-за чего его общая продолжительность может затягиваться до 1,5 лет.
Клинические проявления инфекционного мононуклеоза у взрослых больных отличаются рядом особенностей. Заболевание часто начинается с постепенного развития продромальных явлений, лихорадка часто сохранятся более 2 нед, выраженность лимфаденопатии и гиперплазии миндалин меньше, чем у детей. Вместе с тем у взрослых чаще наблюдают проявления заболевания, связанные с вовлечением в процесс печени и развитием желтушного синдрома.
Осложнения инфекционного мононуклеоза
Наиболее частое осложнение - присоединение бактериальных инфекций, вызванных золотистым стафилококком, стрептококками и др. Также возможны менингоэнцефалит, обструкция верхних отделов респираторного тракта увеличенными миндалинами. В редких случаях отмечают двустороннюю интерстициальную инфильтрацию лёгких с тяжёлой гипоксией, тяжёлый гепатит (у детей), тромбоцитопению, разрывы селезёнки. В большинстве случаев прогноз заболевания благоприятный.
Диагностика Инфекционного мононуклеоза:
Инфекционный мононуклеоз следует отличать от лимфогранулематоза и лимфолейкоза, ангин кокковой и иной этиологии, дифтерии ротоглотки, а также вирусных гепатитов, псевдотуберкулёза, краснухи, токсоплазмоза, хламидийных пневмоний и орни-тоза, некоторых форм аденовирусной инфекции, ЦМВ-инфекции, первичных проявлений ВИЧ-инфекции. Инфекционный мононуклеоз отличает сочетание основных пяти клинических синдромов: общетоксических явлений, двусторонней ангины, полиаденопатии (особенно с поражением лимфатических узлов по ходу грудино-ключично-сосцевидных мышц с обеих сторон), гепатолиенального синдрома, специфических изменений гемограммы. В некоторых случаях возможны желтуха и (или) экзантема пятнисто-папулёзного характера.
Лабораторная диагностика инфекционного мононуклеоза
Наиболее характерный признак - изменения клеточного состава крови. В гемограмме выявляют умеренный лейкоцитоз, относительную нейтропению со сдвигом лейкоцитарной формулы влево, значительное увеличение количества лимфоцитов и моноцитов (суммарно более 60%). В крови присутствуют атипичные мононуклеары - клетки с широкой базофильной цитоплазмой, имеющие различную форму. Их наличие в крови определило современное название болезни. Диагностическое значение имеет увеличение количества атипичных мононуклеаров с широкой цитоплазмой не менее чем до 10-12%, хотя число этих клеток может достигать 80-90%. Следует заметить, что отсутствие атипичных мононуклеаров при характерных клинических проявлениях заболевания не противоречит предполагаемому диагнозу, поскольку их появление в периферической крови может задерживаться до конца 2-3-й недели болезни.
В период реконвалесценции количество нейтрофилов, лимфоцитов и моноцитов постепенно нормализуется, однако довольно часто длительно сохраняются атипичные мононуклеары.
Вирусологические методы диагностики (выделение вируса из ротоглотки) на практике не применяют. Методом ПЦР можно выявлять вирусную ДНК в цельной крови и сыворотке.
Разработаны серологические методы определения антител различных классов к капсидным (VCA) антигенам. Сывороточные IgM к VCA-антигенам можно обнаружить уже в инкубационный период; в дальнейшем их выявляют у всех больных (это служит достоверным подтверждением диагноза). Исчезают IgM к VCA-антигенам лишь через 2-3 мес после выздоровления. После перенесённого заболевания пожизненно сохраняются IgG к VCA-антигенам.
При отсутствии возможности определения анти-VCA-IgM до сих пор применяют серологические методы обнаружения гетерофильных антител. Они образуются в результате поликлональной активации В-лимфоцитов. Наиболее популярны реакция Пауля-Буннеля с эритроцитами барана (диагностический титр 1:32) и более чувствительная реакция Гоффа-Бауэра с эритроцитами лошади. Недостаточная специфичность реакций снижает их диагностическую ценность.
Всем больным с инфекционным мононуклеозом или при подозрении на него нужно проводить 3-кратное (в острый период, затем через 3 и 6 мес) лабораторное обследование на антител к антигенам ВИЧ, поскольку в стадию первичных проявлений ВИЧ-инфекции также возможен мононуклеозоподобный синдром.
Лечение Инфекционного мононуклеоза:
Больных лёгкими и среднетяжёлыми формами инфекционного мононуклеоза можно лечить на дому. Необходимость постельного режима определяется выраженностью интоксикации. В случаях заболевания с проявлениями гепатита рекомендуют диету (стол №5).
Специфическая терапия не разработана. Проводят дезинтоксикационную терапию, десенсибилизирующее, симптоматическое и общеукрепляющее лечение, полоскания ротоглотки растворами антисептиков. Антибиотики при отсутствии бактериальных осложнений не назначают. При гипертоксическом течении заболевания, а также при угрозе асфиксии, обусловленной отёком глотки и выраженным увеличением миндалин, назначают короткий курс лечения глюкокортикоидами (преднизолон внутрь в суточной дозе 1-1,5 мг/кг в течение 3-4 дней).
Профилактика Инфекционного мононуклеоза:
Общие меры профилактики аналогичны таковым при ОРВИ. Меры специфической профилактики не разработаны. Неспецифическую профилактику осуществляют повышением общей и иммунологической резистентности организма.
К каким докторам следует обращаться если у Вас Инфекционный мононуклеоз:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Инфекционного мононуклеоза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Замучил хронический гайморит? Страдаете от постоянного насморка? Уже потеряли всякую надежду вздохнуть свободно? Воспалительные процессы в окол.
Для жителей районов Савеловский, Беговой, Аэропорт, Хорошевский
Скидки для друзей из социальных сетей!
Эта акция - для наших друзей в "Одноклассниках", "ВКонтакте", "Яндекс.Дзене", YouTube и Telegram! Если вы являетесь другом или подписчиком стр.
Второе мнение
Балашова Юлия Вячеславовна
Варнель Ольга Леонидовна
Высшая квалификационная категория, заведующая отделением оториноларингологии
Капустина Анна Александровна
Пономарева Лариса Викторовна
Высшая квалификационная категория
Пышный Дмитрий Владимирович
Высшая квалификационная категория, кандидат медицинских наук
Рамазанова Гюнай Альнияз-кызы
Кандидат медицинских наук
Мы в Telegram и "Одноклассниках"
Мононуклеоз – острое инфекционное заболевание, при котором поражается лимфатическая система. При моноуклеозе болит и воспаляется горло, больной постоянно утомлен, беспокоен, у него увеличена печень и лимфатические узлы. Мононуклеоз характеризуется увеличением моноцитов в циркулирующей крови.
Источник инфекции – инфицированный человек. Инфекция передается воздушно-капельно, чаще со слюной человека (при поцелуях), через переливание крови.
50% населения заболевают этой инфекцией в подростковом возрасте: девочки в 14-16 лет, мальчики в 16-18 лет. Люди старше 40 лет этой болезнью заражаются реже. Но у ВИЧ-инфицированных болезнь может наступить в любом возрасте.
Инфекционный мононуклеоз (еще эту болезнь называют железистой лихорадкой, моноцитарной ангиной) характеризуется лихорадкой, лимфаденопатией, тонзиллитом, увеличением размера печени и селезенки, может приобрести хронический характер. Возбудитель болезни – вирус Эпштейна-Барра, ВЭБ (группа вирусов герпеса).
Кроме увеличения размеров печени и селезенки, болезнь проявляется болями в животе, диспепсией, небольшими нарушениями функциональных способностей печени. В первые дни болезни происходят изменения в крови, лейкоцитоз, увеличение одноядерных клеток: лимфоцитов и моноцитов. Повышается СОЭ. Появляются атипичные клетки с одним ядром среднего и крупного размера – атипичные мононуклеары.
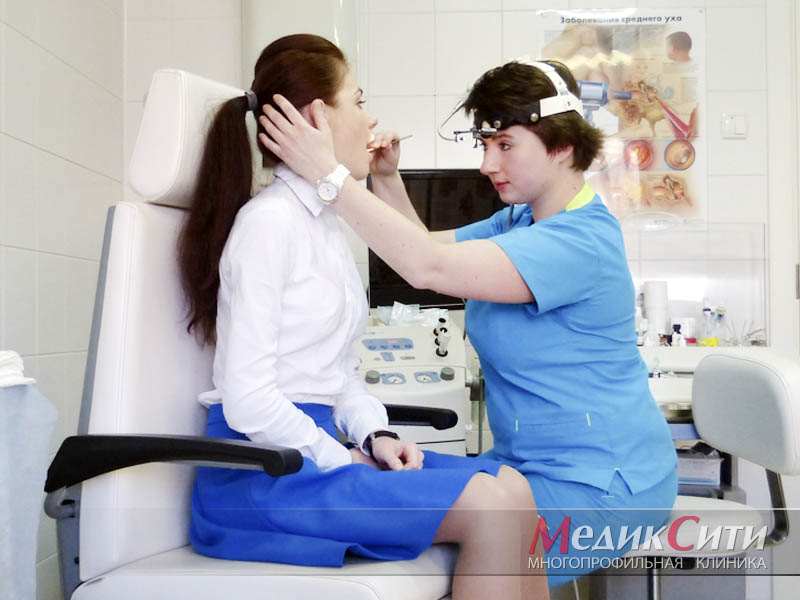
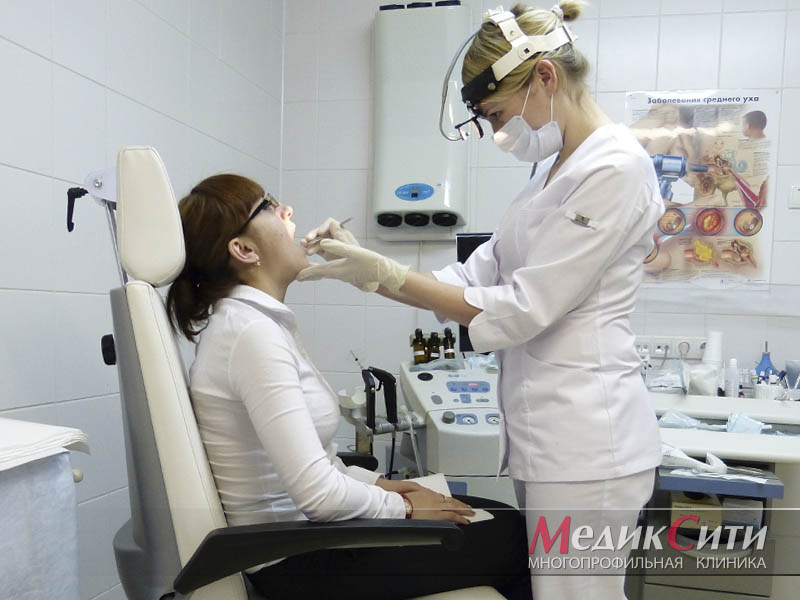
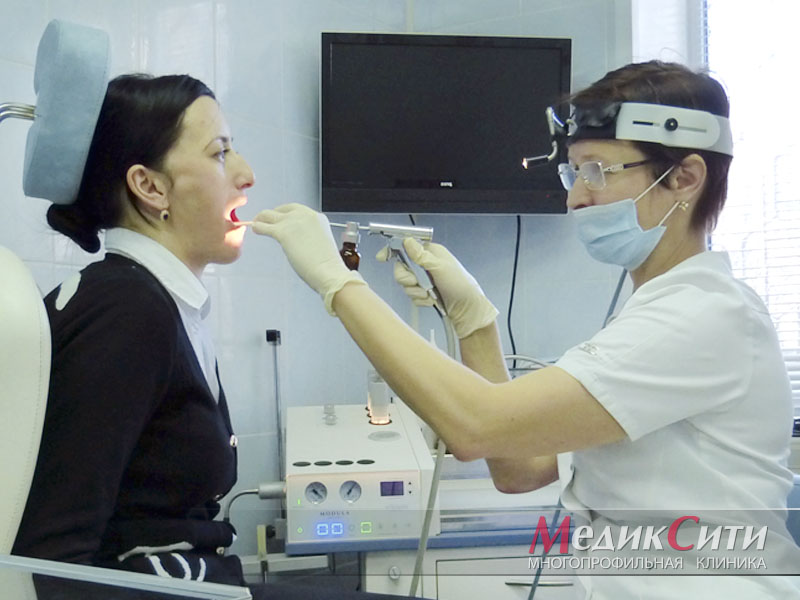
Симптомы мононуклеоза
Инфекционный мононуклеоз характеризуется поражением лимфоидной ткани носа, глотки, миндалин.
Другие симптомы болезни:
- увеличение подчелюстных, подмышечных, локтевых, паховых, заднешейных, трахеобронхиальных лимфоузлов;
- большое количество широкоплазменных моноуклеаров;
- лихорадка, увеличение лимфатических узлов, тонзиллит;
- боль в горле;
- затрудненное носовое дыхание;
- голос с носовым оттенком и др.
Болезнь сопровождается фолликулярной, лакунарной или катаральной ангиной, неприятным сладковато-приторным запахом изо рта.
Патогенез мононуклеоза
Вирус Эпштейна-Барра появляется в организме человека через слизистые носоглотки, затем распространяется по организму и накапливается в лимфоузлах. Вирус поддерживают В-лимфоциты, имеющие поверхностные рецепторы для вируса.
На самом пике болезни специфические вирусные антигены можно обнаружить у более чем 20% ядер В-лимфоцитов.
Когда инфекционный процесс пошел на убыль, вирусы мононуклеоза наблюдаются только в единичных В-лимфоцитах и эпителиальных тканях носоглотки. Когда часть пораженных клеток погибает, и освободившийся вирус поражает новые клетки, начинает неправильно работать клеточный и гуморальный иммунитет. Поэтому может образоваться супер-инфекция и наслоиться вторичная инфекция (чаще всего вызванная стафилококками или стрептококками).
При мононуклеозе вирус поражает лимфоидную и ретикулярную ткань, это приводит к увеличению лимфоузлов, также увеличиваются печень и селезенка.
Иммунитет при мононуклеозе стойкий. Инфекция может распространяться в виде бессимптомных и стертых форм, у 50-80% населения обнаружены антитела к этому вирусу.
Как протекает болезнь
Инкубационный период мононуклеоза - около недели. Заболевание начинается остро. 2-4 день характеризуются ярко выраженной лихорадкой и общей интоксикацией организма.
С первых дней человек чувствует слабость, головную боль, немного позже появляются боли при глотании. Температура поднимается до 38 - 40 градусов. На 5 день у больного может начаться тонзиллит. Он может быть катаральным, лакунарным или язвенно-некротическим. Поражаются лимфатические узлы. На теле может появиться сыпь, которая через 1-3 дня бесследно пропадает. Наблюдаются изменения в печени.
В периферической крови можно наблюдать лейкоцитоз. Число лимфоцитов, моноцитов и атипичных мононуклеаров достигает в первую неделю 80 -90%. После мононуклеоза мононуклеарная реакция может держаться от полугода до нескольких лет.
Возможны несколько вариантов исхода острого инфекционного процесса ВЭБ (мононуклеоза):
- выздоровление;
- бессимптомное вирусоносительство;
- хроническая рецидивирующая инфекция (хронический инфекционный мононуклеоз);
- развитие онкологического процесса (лимфомы, назофарингеальная карцинома, лейкоплакия языка и ротовой полости, рак желудка и кишечника);
- развитие аутоиммунного заболевания (ревматоидный артрит, системная красная волчанка).
Осложнения после болезни
Осложнения после инфекционного мононуклеоза бывают не очень часто, но довольно серьезные:
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ).
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ). Практикующие врачи в своей повседневной практике чаще сталкиваются с клинически манифестными формами первичной Эпштейна–Барр-вирусной инфекции (ЭБВИ) в виде острой, как правило, не верифицированной респираторной инфекцией (более 40% случаев) или инфекционным мононуклеозом (около 18% всех заболеваний) [1, 2]. В большинстве случаев эти заболевания протекают доброкачественно и заканчиваются выздоровлением, но с пожизненной персистенцией ВЭБ в организме переболевшего [1, 3–5].
Однако в 10–25% случаев первичное инфицирование ВЭБ, протекающее бессимптомно, и острая ЭБВИ могут иметь неблагоприятные последствия [6–9] с формированием лимфопролиферативных и онкологических заболеваний, синдрома хронической усталости, ВЭБ-ассоциированного гемофагоцитарного синдрома и др. [7, 9, 11–14].
До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ВЭБ. Перед врачом, к которому обращается пациент с острой ЭБВИ, всегда встает вопрос: что предпринять в каждом конкретном случае, чтобы максимально снизить риск развития хронической ЭБВИ и ВЭБ-ассоциированных патологических состояний Этот вопрос не праздный, и ответить на него действительно очень трудно, т. к. до сих пор нет четкой патогенетически обоснованной схемы лечения больных, а имеющиеся рекомендации часто противоречат друг другу.
По мнению многих исследователей, лечение ЭБВИ-мононуклеоза (ЭБВИМ) не требует назначения специфической терапии [15–17]. Лечение больных, как правило, проводится в амбулаторных условиях, изоляция пациента не требуется. Показаниями к госпитализации следует считать длительную лихорадку, выраженный синдром тонзиллита и/или синдром ангины, полилимфаденопатию, желтуху, анемию, обструкцию дыхательных путей, боли в животе и развитие осложнений (хирургических, неврологических, гематологических, со стороны сердечно-сосудистой и дыхательной системы, синдром Рейе).
При легком и среднетяжелом течении ЭБВ ИМ больным целесообразно рекомендовать палатный или общий режим с возвращением к обычной деятельности на адекватном для каждого конкретного больного физическом и энергетическом уровне. Проведенное многоцентровое исследование показало, что необоснованно рекомендуемый строгий постельный режим удлиняет период выздоровления и сопровождается длительным астеническим синдромом, требующим нередко медикаментозного лечения [18].
При легком течении ЭБВ ИМ лечение больных ограничивается поддерживающей терапией, включающей адекватную гидратацию, полоскание ротоглотки раствором антисептиков (с добавлением 2% раствора лидокаина (ксилокаина) при выраженном дискомфорте в глотке), нестероидные противовоспалительные препараты, такие как парацетамол (Ацетаминофен, Тайленол). По мнению ряда авторов назначение блокаторов Н2 рецепторов, витаминов, гепатопротекторов и местная обработка миндалин различными антисептиками являются малоэффективными и необоснованными способами лечения [19, 20]. Из экзотических методов лечения следует упомянуть рекомендуемое Ф. Г. Боковым и соавт. (2006) применение мегадоз бифидобактерий при лечении больных острым мононуклеозом [21].
Мнения о целесообразности назначения антибактериальных препаратов при лечении ЭБВИМ весьма противоречивы. По мнению Gershburg E. (2005) тонзиллит при ИМ часто асептический и назначение антибактериальной терапии не оправдано. Также нет смысла в применении антибактериальных средств при катаральной ангине [4]. Показанием для назначения антибактериальных препаратов является присоединение вторичной бактериальной инфекции (развитие у больного лакунарной или некротической ангины, таких осложнений, как пневмония, плеврит и др.), о чем свидетельствуют сохраняющиеся более трех суток выраженные воспалительные изменения показателей крови и фебрильная лихорадка. Выбор препарата зависит от чувствительности микрофлоры на миндалинах больного к антибиотикам и возможных побочных реакций со стороны органов и систем.
По данным H. Fota-Markowcka et al. (2002) у больных чаще выделяют гемофильную палочку, стафилококк и пиогенный стрептококк, реже — грибы рода Candida [22], поэтому следует признать обоснованным назначение этим больным препаратов из группы цефалоспоринов 2–3 поколения, линкосамидов, макролидов и противогрибковых средств (флуконазол) в терапевтических дозах на 5–7 дней (реже — 10 дней) [4]. Некоторые авторы при наличии некротической ангины и гнилостном запахе изо рта, вызванных, вероятно, ассоциированной анаэробной флорой, рекомендуют использовать метронидазол по 0,75 г/сут, разделенных на 3 приема, в течение 7–10 дней.
Противопоказаны препараты из группы аминопенициллинов (ампициллин, амоксициллин (Флемоксин Солютаб, Хиконцил), амоксициллин с клавуланатом (Амоксиклав, Моксиклав, Аугментин)) из-за возможности развития аллергической реакции в виде экзантемы. Появление сыпи на аминопенициллины не является IgE-зависимой реакцией, поэтому применение блокаторов Н1 гистаминовых рецепторов не имеет ни профилактического, ни лечебного эффекта [19].
По мнению ряда авторов до настоящего времени сохраняется эмпирический подход к назначению глюкокортикостероидов больным с ЭБВИ [23]. Глюкокортикостероиды (преднизолон, преднизон (Делтазон, Метикортен, Оразон, Ликвид Пред), Солу Кортеф (гидрокортизон), дексаметазон) рекомендуются больным с тяжелым течением ЭБВИМ, с обструкцией дыхательных путей, неврологическими и гематологическими осложнениями (тяжелая тромбоцитопения, гемолитическая анемия) [4, 24]. Суточная доза преднизолона составляет 60–80 мг в течение 3–5 дней (реже 7 дней) с последующей быстрой отменой препарата. Одинаковой точки зрения на назначение этим больным глюкокортикостероидов при развитии миокардита, перикардита и поражениях ЦНС нет.
При тяжелом течении ЭБВИМ показана внутривенная дезинтоксикационная терапия, при разрыве селезенки — хирургическое лечение.
Наиболее дискуссионным остается вопрос о назначении противовирусной терапии больным с ЭБВИ. В настоящее время известен большой перечень препаратов, являющихся ингибиторами ВЭБ репликации в культуре клеток [4, 25–27].
I. Подавляющие активность ДНК-полимеразы ВЭБ:
- ациклические аналоги нуклеозидов (ацикловир, ганцикловир, пенцикловир, валацикловир, валганцикловир, фамцикловир);
- ациклические аналоги нуклеотидов (цидофовир, адефовир);
- аналоги пирофосфатов (Фоскарнет (фоскавир), фосфоноацетиловая кислота);
- 4 оксо-дигидрохинолины (возможно).
II. Различные соединения, не ингибирующие вирусной ДНК-полимеразы (механизм изучается): марибавир, бета-L-5 урацил йододиоксолан, индолокарбазол.
Однако проведенный метаанализ пяти рандомизированных контролируемых испытаний с участием 339 больных ЭБВИМ, принимавших ацикловир (Зовиракс), показал неэффективность препарата [28, 29].
Одна из возможных причин кроется в цикле развития ВЭБ, в котором ДНК вируса имеет линейную либо циркулярную (эписома) структуру и размножается в ядре клетки хозяина. Активная репликация вируса происходит при продуктивной (литической) стадии инфекционного процесса (ДНК ВЭБ линейной формы). При острой ЭБВИ и активации хронической ЭБВИ происходит цитолитический цикл развития вируса, при котором он запускает экспрессию собственных ранних антигенов и активирует некоторые гены клеток макроорганизма, продукты которых участвуют в репликации ВЭБ. При латентной ЭБВИ ДНК вируса имеет вид эписомы (круговой суперспиральный геном), находящейся в ядре. Циркулярный геном ДНК ВЭБ характерен для CD21+ лимфоцитов, в которых даже при первичном инфицировании вирусом практически не наблюдается литической стадии инфекционного процесса, а ДНК воспроизводится в виде эписомы синхронно с клеточным делением инфицированных клеток. Гибель пораженных ВЭБ В лимфоцитов связана не с опосредованным вирусом цитолизом, а с действием цитотоксических лимфоцитов [4].
При назначении противовирусных препаратов при ЭБВИ врач должен помнить, что их клиническая эффективность зависит от правильной трактовки клинических проявлений болезни, стадии инфекционного процесса и цикла развития вируса на этой стадии. Однако не менее важным является и тот факт, что большинство симптомов ЭБВИ связаны не с прямым цитопатическим действием вируса в инфицированных тканях, а с опосредованным иммунопатологическим ответом ВЭБ-инфицированных В лимфоцитов, циркулирующих в крови и находящихся в клетках пораженных органов. Именно поэтому аналоги нуклеозидов (ацикловир, ганцикловир и др.) и ингибиторы полимеразы (Фоскарнет), подавляющие репликацию ВЭБ и уменьшающие содержание вируса в слюне (но не санирующие ее полностью [4], не оказывают клинического эффекта на тяжесть и продолжительность симптомов ЭБВИМ.
Показаниями для лечения ЭБВИМ противовирусными препаратами являются: тяжелое, осложненное течение болезни, необходимость профилактики ВЭБ-ассоциированной В-клеточной лимфопролиферации у иммунокомпрометированных пациентов, ВЭБ-ассоциированная лейкоплакия. Bannett N. J., Domachowske J. (2010) рекомендуют применять ацикловир (Зовиракс) внутрь в дозе 800 мг внутрь 5 раз в сутки в течение 10 дней (или 10 мг/кг каждые 8 часов в течение 7–10 дней). При поражениях нервной системы предпочтителен внутривенный способ введения препарата в дозе 30 мг/кг/сут 3 раза в сутки в течение 7–10 дней.
По мнению E. Gershburg, J. S. Pagano (2005), если под действием каких-либо факторов (например, иммуномодуляторов, при ВЭБ-ассоциированных злокачественных опухолях — применение лучевой терапии, гемцитабина, доксорубицина, аргинина бутирата и др.) удается перевести ДНК ВЭБ из эписомы в активную репликативную форму, т. е. активировать литический цикл вируса, то в этом случае можно ожидать клинический эффект от противовирусной терапии.
В комплексной терапии рекомендуется внутривенное введение иммуноглобулинов (Гаммар-П, Полигам, Сандоглобулин, Альфаглобин и др.) 400 мг/кг/сут, № 4–5.
В последние годы все чаще для лечения ЭБВИ стали применять рекомбинантные альфа-интерфероны (Интрон А, Роферон-А, Реаферон-ЕС) по 1 млн ME в/м в течение 5–7 дней или через день; при хронической активной ЭБВИ — 3 млн ME в/м 3 раза в неделю, курс 12–36 недель.
Медикаментозная коррекция астенического синдрома при хронической ЭБВИ включает назначение адаптогенов, высоких доз витаминов группы В, ноотропных препаратов, антидепрессантов, психостимуляторов, препаратов с прохолинергическим механизмом действия и корректоров клеточного метаболизма [30–32].
Залогом успешного лечения больного с ЭБВИ являются комплексная терапия и строго индивидуальная тактика ведения как в стационаре, так и во время диспансерного наблюдения.
Литература
И. В. Шестакова, доктор медицинских наук, доцент
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
МГМСУ, Москва
Коварный инфекционный мононуклеоз: разберемся, чем он опасен и как его обнаружить
Сейчас все чаще можно услышать сложное и несколько пугающее название болезни — инфекционный мононуклеоз (ИМ). Но даже если это название для вас ново, вероятность, что вы или ваш ребенок уже столкнулись с его возбудителем, достаточно велика. При том, что распространенность этой болезни весьма широка, она не всегда диагностируется правильно. Это связано с тем, что проявляться мононуклеоз может по-разному — как у детей, так и у взрослых. Он способен умело маскироваться и имеет тенденцию к хронитизации. Неудивительно, что мононуклеоз считается крайне коварным явлением.
Давайте разберемся с его причинами, симптомами и, что особенно важно, с его диагностикой!

Что вызывает мононуклеоз?
Мононуклеоз у детей: симптомы и течение
Чаще всего первые проявления инфекционного мононуклеоза возникают у детей раннего возраста и впоследствии у подростков в пубертатном периоде. В любом случае для детского возраста характерно острое начало инфекции.
Какие симптомы в этом случае можно заметить?
В целом острая фаза инфекционного мононуклеоза длится около двух-трех недель. Как и другие разновидности герпес-вирусов, вирус Эпштейна — Барр склонен к сохранению в организме в латентном состоянии на всю жизнь.

Проявления инфекционного мононуклеоза у взрослых
Каковы проявления инфекционного мононуклеоза у взрослых?
Чем хуже обстоят дела с иммунитетом, тем чаще и мощнее будут рецидивы инфекции.
Скрытые опасности вируса Эпштейна — Барр
Ученые выявили тесную связь вируса Эпштейна — Барр с развитием некоторых видов новообразований (назофарингеальной карциономы) и болезней крови (лимфомы Бёркитта). Своевременное лечение обострений инфекционного мононуклеоза может снизить риск подобных осложнений.
Зачем нужна проверка на вирус Эпштейна — Барр?
Частые ангины, признаки ухудшения работы печени и другие перечисленные выше проявления встречаются при многих заболеваниях, что вызывает трудности в постановке диагноза на основе клинических проявлений. Возможности современных лабораторных исследований позволяют быстро прояснить ситуацию и сделать дифференциальную диагностику намного проще и точней.
Заболевания, под которые может маскироваться инфекция, вызванная вирусом Эпштейна — Барр:
Лабораторные тесты — это единственный и надежный способ обеспечить такую реализацию диагностики инфекционного мононуклеоза, результат который будет точным и информативным.

Лабораторная диагностика инфекционного мононуклеоза
Существует три главных критерия для лабораторного подтверждения диагноза:
Первые два пункта оцениваются с помощью развернутого общего анализа крови с лейкоцитарной формулой. Такой анализ позволяет установить процентное соотношение разных видов белых кровяных телец, выявить мононуклеары — измененные на фоне активности вируса Эпштейна — Барр белые кровяные клетки.
Серологический тест включает определение иммуноглобулинов класса М и G к нескольким видам вирусных антигенов (в том числе к капсидному, раннему и ядерному антигену) и позволяет сделать вывод о давности заражения, переходе инфекции в хроническую форму и ее реактивации (новом обострении).
Существует еще один метод диагностики инфекционного мононуклеоза, вызванного вирусом Эпштейна — Барр, — метод полимеразной циклической реакции (ПЦР). Данный метод молекулярной биологии, основанный на выявлении ДНК возбудителей инфекции, является сегодня одним из самых точных и чувствительных методов диагностики инфекционных заболеваний. ПЦР позволяет определять не только наличие инфекции, признаки ее реактивации, но вирусную нагрузку, то есть количественное присутствие вирусной ДНК в крови. Применение метода ПЦР в настоящее время можно считать лучшим вариантом для выявления первичной инфекции ВЭБ у детей раннего возраста, а также у лиц с иммунодефицитными состояниями, когда серодиагностика малоэффективна.
Диагностика инфекционного мононуклеоза в LAB4U

В сухом остатке:
Для первичной диагностики вируса Эпштейна — Барр у детей раннего возраста (до 3-х лет) применяется метод ПЦР-диагностики. Это исследование и ряд других, которые могут потребоваться при комплексном обследовании при наличии инфекционного мононуклеоза, можно всегда найти в каталоге онлайн-лаборатории LAB4U.
Причины и возбудитель
Возбудитель ИМ — вирус Эпштейн-Барра — ВЭБ (Epstein-Barr virus — EBV) — крупный оболочечный ДНК-содержащий вирус 4-типа из семейства Herpesviridae, подсемейства у Herpesviridae, рода Lymphocryptovirus.
На основании различий в строении генома и способности вызывать реакцию бласттрансформации В-лимфоцитов выделяют 2 штамма ВЭБ: наиболее активный в реакции тип 1(A) и менее активный — тип 2(B). Тип 1(A) имеет повсеместное распространение, тип 2(B) встречается преимущественно на Африканском континенте и ряде стран Северной Америки.
ВЭБ имеет овальную форму с диаметром 150-200 нм. Геном вируса представлен двумя молекулами ДНК, заключенными в икосаэдрический капсид, состоящий из 162 капсомеров. Комплекс капсидных белков вируса (р150, р18, р23) представляют его капсидный антиген — VCA (Viral capsid anti- gen). Иммунодоминантными белками в этом комплексе являются р 18 и р23.
На самых ранних этапах репликации EBV в организме инфицированного человека появляется высокоиммуногенный комплекс вирусных белков (р54 и р138), названный ранним антигеном ЕА (early antigen).
Мишенями для ВЭБ являются клетки, имеющие на своей поверхности рецептор CD21. Это эпителиоциты слизистых оболочек носо- и ротоглотки, выводных протоков слюнных желез; В-лимфоциты (прежде всего, находящиеся в фолликуллярных структурах лимфоидного кольца Пирогова- Ланганса и периферической лимфоидной ткани); дендритные клетки; эпителий шейки матки.
Узнать больше
Иммуносупрессивное действие ВЭБ с одной стороны обуславливает длительную (пожизненную) персистенцию вируса в организме с возможностью периодических обострений заболевания, с другой — объясняет возможную роль вируса в развитии иммуно- и онкопатологии. Вирус неустойчив к факторам внешней среды, быстро погибает под действием дезинфектантов, при высыхании в режиме комнатной температуры.
Эпидемиология
Источник инфекции — человек с острой и хронической манифестной или латентной формой ЭБВИ. Инфицированные лица активно выделяют вирус с последних дней инкубации и на протяжении 6-18 месяцев после первичной инфекции. Более чем у 90% бессимптомных серопозитивных индивидуумов вирус содержится в орофарингеальном секрете.
Основной механизм передачи — воздушно-капельный, путь передачи — аэрозольный. В основном ВЭБ передается при прямом близком контакте через слюну (при поцелуях, через игрушки, на которых есть зараженная слюна), содержащую клетки орофарингеального эпителия. Заражение возможно при несоблюдении санитарно-гигиенических правил обработки посуды в системе общественного питания, а также при использовании "общих” стаканов, бутылок и т.п. Также возможен парентеральный (при трансплантации органов и гемотрансфузиях) и половой пути передачи. Установлена возможность вертикальной передачи возбудителя с развитием врожденной ЭБВИ. ВЭБ передается при переливании препаратов крови, а также при трансплантации. Восприимчивым к заражению является все неиммунное население независимо от возраста.
Патогенез
Поступление ВЭБ в фолликулярные лимфатические структуры слизистой ротоглотки, в регионарные лимфоузлы, внедрение его в В-лимфоциты, их трансформация в лимфобластоидные клетки. Презентация антигенов вируса макрофагами и ДК иммунокомпетентным клеткам - начало формирования гуморального и клеточного иммунитета. Лимфогенная и гематогенная диссеминация ВЭБ.
Начальный период (от нескольких часов до 1 недели). Основные проявления: боли в горле, тонзиллит, фарингит, аденоидит, увеличение регионарных лимфоузлов. Интоксикационный синдром проявляется лихорадкой, ознобами, потливостью, слабостью в теле.
Период разгара (от 1 до 3-х и более недель). Происходит нарастание специфического иммунитета, некротические изменения на слизистых в месте входных ворот. Может присоединиться или активизироваться бактериальная флора (фолликулярная, лакунарная, некротическая ангины). Происходит продолжение выделения вируса со слюной и отделяемым носо- и ротоглотки.
Период реконвалесценции (от 1 до 3-4 месяцев). Пик формирования специфического иммунитета. Пораженные органы и ткани восстанавливаются. В большинстве случаев наступает клиническое выздоровление. В организме большинства переболевших вирус будет пребывать всю их жизнь.
Патоморфология
В связи с низкой летальностью патоморфология ИМ представлена в основном по результатам исследований биопсийного материала.
При патологоанатомическом исследовании макроскопически констатируется увеличение всех групп лимфатических узлов, миндалин и других лимфоидных образований глотки, селезенки, печени. При гистологическом исследовании выявляют пролиферацию лимфоидных и ретикулярных клеток, в печени перипортальную инфильтрацию лимфоидными элементами. В тяжелых случаях возможны очаговые некрозы в лимфоидных органах, появление лимфоидных инфильтратов в легких, почках, ЦНС и других органах. Редкие смертельные исходы чаще всего обусловлены разрывом селезенки, гематологическими осложнениями (гемолиз, тромбоцитопеническая пурпура) или поражением ЦНС.
Симптомы и классификация
По типу инфекционный мононуклеоз бывает таких форм:
- типичная,
- атипичные (стертая, бессимптомная)
По тяжести выделяют такие формы болезни:
- легкая,
- среднетяжелая,
- тяжелая.
По течению ИМ бывает не осложненным или осложненным.
В МКБ-10 (1995) обозначается так: В27.0 "Мононуклеоз, вызванный гамма-герпетическим вирусом".
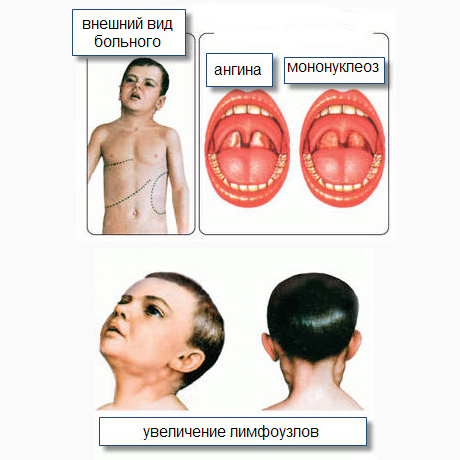
Ниже представлена наиболее типичная клиническая картина ИМ, наблюдаемая при среднетяжелом течении заболевания.
Инкубационный период — от 8 до 21 дней (максимально до 6-8 недель).
Начальный период (до 4-5 дней). Начало болезни может быть как острым, так и постепенным. Фебрильная лихорадка сопровождается прогрессирующей слабостью, головной болью, снижением аппетита и другими симптомами интоксикации. Гиперплазия третьей глоточной миндалины, расположенной на своде носоглотки, нарушение лимфооттока клинически реализуется появлением признаков аденоидита: заложенности носа, "гнусавости” голоса, ночного храпа (даже у маленьких детей), отека век, пастозности верхней половины лица.
Пациенты жалуются на умеренные боли в горле. Объективно — катаральные явления на миндалинах и слизистой ротоглотке. Обращает на себя внимание несоответствие умеренных катаральных явлений в ротоглотке с выраженностью интоксикационного синдрома. Уже сейчас могут изменяться контуры шеи за счет значительного увеличения шейных, затылочных, подчелюстных лимфоузлов. Лимфоузлы умеренно болезненны при пальпации, не спаяны между собой и с окружающими тканями, отчетливо контурированы, окружающая их подкожная клетчатка не отечна.
Период разгара (от 1 до 3-х и более недель) самочувствие больного ухудшается: лихорадка может достигать 40"С, сопровождается ознобом, усилением головной боли. Боли в горле при глотании усиливаются. Объективно выявляется симптоматика острого тонзиллофарингита, который может протекать в катаральной, фолликулярной, пленчатой или язвенно-некротической формах. Чаще всего наблюдается картина лакунарной ангины: гипертрофия миндалин до 2-3 степени, наличие на них рыхлых белесоватых налетов в виде островков, "столбов”. В некоторых случаях налеты могут напоминать дифтерийные - трудно снимаемые пленки, плотно связанные с подлежащей тканью.
На слизистой оболочке мягкого и твердого неба возможно появление множественных петехий, задняя стенка глотки резко гиперемированная, разрыхленная, зернистая, с множественными мелкими гиперплазированными фолликулами. Длительность ангины достигает 2-3 недель. Явления тонзиллита не имеют строгой корреляции с выраженностью интоксикационого синдрома.
Лимфоаденопатия приобретает генерализованный характер. Размеры лимфатических узлов варьируют от горошины до грецкого ореха (0,5-Зсм), пальпируются в виде единичных лимфоузлов или цепочки. Уже с 6-го дня болезни у большинства больных отмечается увеличение печени и селезенки. Стоит отметить, что селезенка увеличивается больше, чем печень.
Период реконвалесценции (от 1 до 3-4 месяцев).
Самочувствие больного постепенно улучшается, нормализуется температура тела, исчезают клинические симптомы острого тонзиллофарингита. Лимфоаденопатия регрессирует медленно — на протяжении 1,5 и более месяцев. Гепатолиенальный синдром может определяться в течение 3-6 месяцев. Длительность периода реконвалесценции индивидуальна, иногда субфебрильная температура тела сохраняются в течение нескольких недель. В периоде реконвалесценции выражен астенический синдром — слабость и недомогание могут сохраняться несколько месяцев. Если у больного нормальный иммунитет (защитные силы организма), он выздоравливает за 3-4 месяца.
Критериями тяжести течения ИМ служат:
- выраженность интоксикационного синдрома,
- выраженность изменений со стороны лимфоидной ткани,
- изменения гемограммы,
- наличие осложнений.
При легкой форме общее состояние пациента изменено незначительно, температура повышается до уровня 37-37,5˚ С, наблюдаются катаральные изменения носо- и ротоглотки воспалительного характера. Лимфатические узлы увеличены незначительно. Гепатоспленомегалия слабо выраженна. Обратное развитие симптомов происходит быстро (к концу 2-й нед).
При тяжелой форме фиксируется высокая лихорадка (температура тела свыше 39,5°С), выраженная интоксикация (вялость, адинамия, рвота, головная боль, анорексия) сохраняються свыше 3 недель. Гиперплазия лимфоидной ткани, расположенной на своде носоглотки проявляется в нарушении носового дыхания вплоть до его отсутствия, характерном внешнем виде больного (одутловатое "аденоидное лицо”). Поражение небных миндалин характеризуется тяжелым гнойно-некротическим, иногда фибринозным воспалением. Наблюдаются генерализованная лимфаденопатия, выраженная гепатоспленомегалия. Высокая вероятность осложнений. Обратное развитие симптомов происходит медленно, в течение 4-5 недель.
У больных инфекционным мононукпеозом отмечается параллелизм между тяжестью заболевания и количеством атипичных мононуклеаров в периферической крови.
Атипичные формы
Стертая — с неполным, со слабо выраженным, быстро проходящим симптомокомплексом.
Бессимптомная — клинические признаки болезни отсутствуют. Диагноз в этом случае возможен по лабораторным данным с учетом эпидемической ситуации.
Осложнения. Специфические:
-
(вследствие надгортанного стеноза, связанного со значительным увеличением лимфоидных образований глоточного кольца Пирогова-Вальдейера); , который может произойти спонтанно или от физических воздействий (например, при пальпации);
- поражения нервной системы (энцефалит, менингит, парезы черепных нервов, синдром Гийена-Барре); , тромбоцитопения, нейтропения.
- В редких случаях отмечают двустороннюю интерстициальную пневмонию с выраженной гипоксией.
Наиболее частое неспецифическое осложнение — присоединение бактериальных инфекций (отиты, синуситы, пневмонии и др.), вызванных золотистым стафилококком, стрептококками и др. Осложнения заболевания могут возникать в разные периоды, в том числе в периоде отдаленной реконвалесценции.
Исходы инфекционного мононуклеоза
1. Выздоровление. У большинства переболевших ИМ формируется стойкий противовирусный иммунитет, обеспечивающие полное клиническое выздоровление. Тем не менее, у них небольшое количество В-лимфоцитов (примерно от 1 до 50 на 1 млн. В-лимфоцитов), либо эпителиальных клеток содержат в ядре ДНК ЕВУ в виде циркулярной структуры (эписомы). При этом в непермиссивных (неразрешаюших) условиях репликация вируса столь низка, что не выявляется в ПЦР.
2. Переход в латентную инфекцию или бессимптомное вирусоносительство. При отсутствии у переболевшего клинических проявлений заболевания в 15-20% случаев методом ПЦР (при чувствительности метода 10 копий в пробе) в их эпителиоцитах (в слюне) или В-лимфоцитах выявляется репликация вируса. У таких пациентов спустя годы и даже десятилетия могут развиться ВЭБ-ассоциированные пролиферативные заболевания: развитие онкологического (лимфопролиферативного) процесса (множественные поликлональные лимфомы (лимфома Беркитта), назофарингеальная карцинома, лейкоплакии языка и слизистых ротовой полости, рак желудка и кишечника и др.).
3. Формирование хронической активной формы инфекции. У отдельных индивидуумов продолжающаяся активная репликация вируса сопровождается развитием клинической картины хронической формы ЭБВИ. У таких пациентов на протяжении от одного года до нескольких лет постоянно сохраняется или периодически возобновляется выраженная в различной степени мононуклеозоподобная симптоматика, нередко в сочетании с различными органными поражениями.
Поражение ЦНС, миокарда, почек, гемофагоцитрный синдром, длительный субфебрилитет неясного генеза, клинические признаки вторичного иммунодефицита (рецидивирующие бактериальные, грибковые и микст-инфекции респираторного, ЖКТ, кожи и слизистых) могут быть и единственными проявлениями хронической ЭБВИ. Критериями диагноза хронической EBV-инфекции у пациента являются: факт перенесения им не далее, чем за 6 месяцев до обращения ИМ и иммуно- гистологического подтверждения роли EBV в поражении органов по выявлению ядерного антигена вируса методом антикомплементарной иммунофлюоресценции.
4. Развитие аутоиммунных заболеваний — системной красной волчанки, ревматоидного артрита, синдрома Шегрена и др. Следует отметить, что две последние группы заболеваний могут развиваться через большой промежуток времени после инфицирования).
5. Развитие лимфопролиферативных процессов (лимфома, назофарингеальная карцинома, лейкоплакия языка и слизистых ротовой полости, рак желудка и кишечника и др.).
6. Обсуждается возможное участие ВЭБ в возникновении синдрома хронической усталости.
Читайте также:

