Стрептококк пиогенес лечение антибиотиками
Обновлено: 18.04.2024
Тонзиллофарингит является частым заболеванием в детском возрасте. Среди бактериальных возбудителей основную роль играет beta-гемолитический стрептококк группы А (БГСА). Установлено, что эффективность коротких курсов ряда антибиотиков сопоставима с 10-днев
Жалоба на боль в горле является одним из наиболее частых поводов для обращения за медицинской помощью к педиатру. Основной причиной боли в горле является воспаление небных миндалин и слизистой оболочки глотки — тонзиллофарингит. Данный термин широко используется в научной литературе, несмотря на то, что согласно Международной классификации болезней тонзиллит и фарингит являются отдельными нозологиями.
Ключевой проблемой антибактериальной терапии при тонзиллофарингитах у детей является определение показаний к ее назначению. Установлено, что чаще всего острый тонзиллофарингит является проявлением острой вирусной инфекции (ОРВИ) и, соответственно, не требует назначения антибактериальной терапии. Среди бактериальных возбудителей тонзиллофарингита у детей безусловным лидером является β-гемолитический стрептококк группы А (БГСА, Streptococcus pyogenes), на долю которого приходится 15–36% случаев острого тонзиллофарингита [1–3]. В 2012–2013 гг. мы обследовали 119 детей с острым тонзиллофарингитом с помощью экспресс-теста на БГСА с высокой диагностической точностью (Стрептатест), положительный результат получен у 19% больных.
Необходимость обязательного назначения антибактериальной терапии при стрептококковом тонзиллофарингите не вызывает сомнений. В систематическом обзоре Кокрановского сотрудничества (2013 г.), в который вошли десятки исследований (начиная с 1951 г.), было показано, что назначение антибиотиков при боли в горле существенно снижает вероятность осложнений — как поздних негнойных (острая ревматическая лихорадка), так и ранних гнойных (средний отит, синусит, паратонзиллярный абсцесс) [4].
Решение обозначенной проблемы кроется в своевременной верификации стрептококкового тонзиллофарингита. В многочисленных исследованиях показано, что внедрение методов экпресс-диагностики, обладающих высокой чувствительностью и специфичностью, позволяет непосредственно при осмотре всего за несколько минут пациента выявить заболевание, вызванное БГСА, дает возможность, с одной стороны, своевременно назначить антибактериальную терапию при стрептококковом тонзиллофарингите, а с другой стороны — значительно снизить частоту необоснованного назначения антибиотиков [5–6].
В то же время существует еще целый ряд актуальных проблем антибактериальной терапии при тонзиллофарингитах у детей, которые требуют обсуждения. Это проблемы, связанные с выбором антибактериального препарата, и режима его применения.
Бактерии рода Streptococcus, в том числе БГСА, не способны продуцировать β-лактамазы. Кроме того, данный возбудитель не обладает и другими механизмами резистентности к β-лактамным антибиотикам. До настоящего времени в мире не выделено ни одно штамма БГСА, резистентного к пенициллинам, цефалоспоринам и карбапенемам. Также возбудитель в 100% случаев сохраняет чувствительность к гликопептидам и оксазолидинонам. В то же время наблюдается резистентность БГСА к макролидам, линкозамидам, фениколам, тетрациклинам, фторхинолонам, сульфаниламидам [7].
В ходе многоцентровых российских исследований, проводившихся в 2001–2005 гг., была оценена резистентность более 1000 штаммов БГСА (табл. 1): выявлен очень высокий уровень резистентности БГСА к тетрациклинам, высокий к хлорамфениколу, небольшой уровень резистентности к 14- и 15-членным макролидам (менее 10%), минимальная резистентность к 16-членным макролидам и линкозамидам (менее 2%) и отсутствие резистентности к фторхинолонам [8].
Учитывая высокую стабильную активность пенициллина в отношении БГСА, этот антибиотик (феноксиметилпенициллин перорально, а также бензатинпенициллин внутримышечно) в течение многих лет рассматривается как препарат выбора для лечения стрептококкового тонзиллофарингита и в отечественных, и в зарубежных руководствах [9–12]. В ряде руководств в качестве препарата выбора также рассматривается амоксициллин [10–11].
Однако в 80-х годах XX века была выявлена серьезная проблема — нарастающая частота клинической и микробиологической неэффективности пенициллина при стрептококковом тонзиллофарингите, по данным отдельных исследований эрадикации БГСА не удавалось достичь у каждого четвертого пациента [13]. Вместе с тем было установлено, что другие антибиотики превосходят пенициллин по эффективности, в частности, если частота формирования носительства БГСА у детей после стрептококкового тонзиллофарингита при лечении пенициллином составила 11,3%, то при использовании макролидов и цефалоспоринов она была существенно меньше — 7,1% и 4,3% соответственно [14].
Изучение несоответствия эффективности пенициллина in vitro и in vivo при стрептококковом тонзиллофарингите позволило определить ключевую причину данного феномена — наличие в миндалинах у пациентов ко-патогенных бактерий (Bacteroides spp., Staphylococcus aureus и др.), которые продуцируют β-лактамазы и, соответственно, разрушают природные пенициллины и аминопенициллины [15–16]. Поэтому у пациентов, недавно получавших β-лактамные антибиотики, а также в случае рецидивирования тонзиллофарингита, в современных руководствах рекомендуется назначение препаратов, которые устойчивы к действию β-лактамаз, — ингибиторозащищенных аминопенициллинов и цефалоспоринов, а в отдельных случаях — линкозамидов [9–12].
Дополнительным фактором, ограничивающим применение пенициллина при тонзиллофарингите, является возможная аллергическая реакция на данный препарат, которая по данным различных исследований составляет от 1% до 20% случаев [17]. В случае аллергии на пенициллин рекомендуется применение макролидов или линкозамидов [9–11].
Суммированные рекомендации по антибактериальной терапии при стрептококковом тонзиллофарингите в современных руководствах можно представить в виде алгоритма (табл. 2).
Данный алгоритм основывается на двух основных факторах, определяющих выбор антибиотика. Однако в научной литературе представлены данные еще о ряде факторов, влияющих на эффективность антибактериальной терапии стрептококкового тонзиллофарингита. В частности, показано, что эффективность антибактериальной терапии зависит от частоты носительства штаммов бактерий, продуцирующих β-лактамазы, в целом в популяции, а не только у больных тонзиллофарингитом. В исследовании, проводившемся в течение года, была проанализирована по месяцам эффективность амоксициллина при стрептококковом тонзиллофарингите у детей и частота выявления в ротоглотке у здоровых детей штаммов бактерий, продуцирующих β-лактамазы. Частота неудач при использовании амоксициллина в течение года колебалась от 8% до 32%, и при этом прослеживалась очевидная корреляция с частотой носительства штаммов бактерий, продуцирующих β-лактамазы (рис. 1) [18].
В качестве одной из возможных причин неэффективности пенициллина при стрептококковом тонзиллофарингите рассматривается подавление пенициллинами α-гемолитических стрептококков, которые являются представителями нормальной микрофлоры ротоглотки и препятствуют колонизации БГСА [19].
Учитывая названные дополнительные факторы, влияющие на выбор антибактериального препарата, большой интерес представляет применение цефалоспоринов в лечении стрептококкового тонзиллофарингита у детей. Препараты данной группы устойчивы к действию многих β-лактамаз [20], они оказывают меньшее по сравнению с пенициллинами влияние на α-гемолитические стрептококки, что способствует более эффективной эрадикации БГСА [22, 23].
Данные 35 доказательных клинических исследований (более 7000 пациентов), оценивавших эффективности различных цефалоспоринов при стрептококковом тонзиллофарингите у детей, были обобщены в метаанализе. В анализировавшихся исследованиях сравнивался 10-дневный курс перорального цефалоспорина 1–3 поколения и перорального пенициллина. Данные метаанализа показали, что цефалоспорины значительно превосходят пенициллин по клинической и микробиологической эффективности (p < 0,00001) (рис. 2) [24].
Одним из препаратов, показавших существенно большую эффективность, чем пенициллин, является пероральный цефалоспорин III поколения цефиксим. В многоцентровом рандомизированном контролируемом исследовании было проведено сравнение эффективности и безопасности 10-дневных курсов цефиксима и пенициллина у 154 детей от 2 до 12 лет со стрептококковым тонзиллофарингитом. Клинический эффект был достигнут у всех пациентов. Микробиологическая эффективность составила 83% для группы детей, получавших цефиксим, и 77% — для группы детей, получавших пенициллин. Нежелательные явления в обеих группах были единичными [25]. В аналогичном рандомизированном исследовании, включавшем 110 детей со стрептококковым тонзиллофарингитом, микробиологическая эффективность цефиксима была существенно выше, чем у пенициллина, — 94% против 77% (p < 0,05) [26].
При стрептококковом тонзиллофарингите важно не только обеспечить выздоровление пациента от инфекционного заболевания, но и предотвратить развитие поздних осложнений и распространение инфекции. Поэтому целью антибактериальной терапии является эрадикация возбудителя. Проведенные исследования показали, что высокий уровень эрадикации достигается при использовании 10-дневного курса лечения пенициллином. Такая же длительность курса лечения рекомендуется и при использовании большинства других антибиотиков [10, 27]. Установлено, что в случае нарушения назначенной врачом длительности курса лечения пенициллином эффективность терапии при стрептококковом тонзиллофарингите снижается в среднем на 20% [28]. Еще более 50 лет назад были проведены исследования, которые показали, что назначенный 10-дневный курс лечения не выполняют подавляющее большинство больных. В одном исследовании было показано, что только 46% детей с тонзиллофарингитом продолжают получать пенициллиин на 3-й день терапии, 31% — на 6-й день и 8% — на 9-й день [29]. В аналогичном исследовании показатели были лучше: 81% пациентов принимали пенициллин на 5-й день лечения и 56% — на 9-й день. Авторы изучили факторы, которые влияют на выполнение рекомендаций врача. Было показано, что длительность курса терапии не зависела от возраста и пола ребенка, оцененной врачом тяжести заболевания и длительности сохранения симптомов. Одновременно было установлено, что на длительность лечения влияли оценка матерью тяжести состояния ребенка, назначение терапии врачом, длительно наблюдающим ребенка, или другим врачом, а также отношение матери к врачу [30].
Учитывая низкую комплаентность при 10-дневном курсе антибактериальной терапии тонзиллофарингита, а также неодинаковую эффективность различных антибиотиков, большой интерес представляют клинические исследования эффективности сокращенных курсов лечения стрептококкового тонзиллофарингита. В ряде исследований было показано, что 6-дневный курс амоксициллина, 4–5-дневный курс цефалоспоринов и 5-дневный курс азитромицина сопоставимы по эффективности с 10-дневным курсом пенициллина. При этом отмечен ряд преимуществ коротких курсов: более высокая комплаентность, меньшая частота нежелательных эффектов, лучшее отношение родителей пациента к лечению, снижение стоимости лечения [31]. В 2009 г. был опубликован систематический обзор Кокрановского сотрудничества, в котором проведено сравнение эффективности при остром стрептококковом тонзиллофарингите у детей коротких курсов антибактериальной терапии по сравнению с 10-дневным курсом пенициллина. В обзоре проанализированы 20 исследований, включавших более 13 000 пациентов. Короткие курсы более эффективных антибиотиков характеризовались более быстрым прекращением лихорадки и боли в горле. По частоте рецидивов тонзиллофарингита 10-дневный курс пенициллина и короткий курс других исследованных антибактериальных препаратов не имели достоверных отличий [32].
Одним из препаратов, эффективность короткого курса которого доказана при стрептококковом фарингите, также является цефиксим. В рандомизированном исследовании, включавшем 160 детей со стрептококковой ангиной, сравнивалась эффективность 5-дневного курса цефиксима и 10-дневного курса пенициллина. Клиническая эффективность была достигнута у 96% пациентов, которые лечились цефиксимом, и у 97,4% пациентов, получавших пенициллин, эрадикация БГСА достигнута соответственно у 82,8% и 88,2% детей. В течение 4 недель после окончания лечения рецидивы заболевания отмечены у 6 пациентов, получавших цефиксим, и у 8 пациентов, получавших пенициллин. В целом достоверных отличий результатов лечения в исследуемых группах не выявлено, что позволило авторам сделать вывод о сопоставимой эффективности короткого курса цефиксима и стандартного курса пенициллина [33]. Важной фармакокинетической особенностью цефиксима является относительно длительный период полувыведения, который позволяет принимать препарат 1 раз в сутки [34], что способствует повышению приверженности к лечению.
В нашей клинике был обобщен опыт применения цефиксима (Супракс®) с оценкой клинической эффективности и безопасности в качестве препарата эмпирической терапии при инфекции дыхательных путей у детей в возрасте от 1 до 12 лет, в том числе у пациентов с острым тонзиллитом и обострением хронического тонзиллита. У всех детей с тонзиллитом была отмечена быстрая положительная динамика. В целом в исследовании была отмечена хорошая переносимость цефиксима — у 8,3% больных отмечены нежелательные явления в виде легкой диареи, которая не требовала отмены препарата [34].
Цефалоспорин III поколения для перорального применения цефиксим обладает высокой активностью в отношении многих клинически значимых грамположительных и грамотрицательных бактерий. Хорошая биодоступность препарата после приема внутрь (около 50%) позволяет создать высокую сывороточную концентрацию и эффективные концентрации в тканях. Проведенные исследования свидетельствуют о высокой эффективности цефиксима при тонзиллофарингите, препарат входит в Стандарт Министерства здравоохранения Российской Федерации по оказанию первичной медико-санитарной помощи при остром тонзиллите у детей и взрослых в амбулаторных условиях [35]. На российском фармацевтическом рынке представлен оригинальный препарат цефиксима — Супракс®, который выпускается в виде гранул для приготовления суспензии, диспергируемых таблеток и капсул, что дает возможность использовать его у детей начиная с раннего возраста.
Литература
И. А. Дронов 1 , кандидат медицинских наук
Н. А. Геппе, доктор медицинских наук, профессор
У. С. Малявина, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова, Москва
Abstract. Tonsillitis-pharyngitis is frequent childish disease. Among pathogenic bacteria the main role plays A group β-hemolytic streptococcus (GAS). Effectiveness of short courses of treatment with antibiotics may be compared with 10-days course of treatment with penicillin. Clinical trial showed that oral intake of III generation cephalosporin — cefixime is highly efficient with children with streptococcus tonsillitis-pharyngitis including treatment by short courses.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор раздела: Трубачева Елена Сергеевна, врач – клинический фармаколог, более 15 лет занимающаяся практическими вопросами лечения и профилактики внутрибольничных инфекций и эпидемиологического надзора. Автор множества печатных работ на указанную тематику.
"Идея "Азбуки антибиотиков" вынашивалась в течение трех лет как способ донести сложные вещи максимально понятным языком для тех, кто только начинает постигать этот действительно сложный раздел практической медицины, и дать импульс к дальнейшему изучению, не продираясь через дебри терминологии и смежных дисциплин, теряя интерес по дороге."
Тема эта очень узконаправленная, и вопрос в том, насколько она может быть интересна широкому кругу читателей. Однако ради одних только отдаленных последствий заболеваний, вызванных S. agalactiae, ее стоит рассмотреть.
Стрептококки – это большая разнородная группа микроорганизмов, включающая следующие группы.
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста.
Пневмококк, он же Streptococcus pneumoniae, является одним из основных возбудителей заболеваний верхних и нижних дыхательных путей. Однако проблема в том, что те же заболевания точно так же и с той же симптоматикой вызывает и множество вирусов, а потому микробиологическая диагностика буквально жизненно необходима, причем не когда-то там, а прямо здесь и сейчас.
В этой статье мы поговорим о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Информация о препаратах, отпускаемых по рецепту, размещенная на сайте, предназначена только для специалистов. Информация, содержащаяся на сайте, не должна использоваться пациентами для принятия самостоятельного решения о применении представленных лекарственных препаратов и не может служить заменой очной консультации врача.
Свидетельство о регистрации средства массовой информации Эл № ФС77-79153 выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) 15 сентября 2020 года.

Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику, как и обзывательство антибактериальной терапии – антибиотикотерапией, а кто мы такие, чтобы отменять традиции.
Рассмотрим основных представителей семейства, на которых больше всего шансов наткнуться в антибиотикограммах.
- Streptococcussanguis – воистину могуч и вездесущ. Обнаруживается в зубных отложениях с самого прорезывания зубов и до конца жизни, где и есть основное место его обитания. Иногда может быть обнаружен на слизистой глотки и в фекалиях, куда попадают транзитом. При этом надо помнить, что этот микроб вносит существенный вклад в процессы, связанные с кариесом, занимая в последующем ведущее место в ассоциациях микроорганизмов, выделяемых из гнойного экссудата при воспалительных процессах в челюстно-лицевой области, включая одонтогенные абсцессы мозга и других органов. Кроме того, они же могут быть выделены их крови и сердечных клапанов больных инфекционным эндокардитом.
- Streptococcussalivarius – также является одним из основных компонентов нормальной микрофлоры полости рта, а также, но в меньшем количестве, может быть выделен со слизистых дыхательного, желудочно-кишечного и урогенитального тракта. Особенно часто выделяются при анализе микрофлоры языка, слюны и фекалий. И крайне редко из крови при менингитах, септицимии и эндокардитах.
- Streptococcusmutans – выделяется с поверхности зубов и фекалий. Этот микроб является кариесогенным, а значит, может в дальнейшем вызывать бактериемию и бактериальный эндокардит у пациентов, не занимающихся регулярной санацией кариозных очагов в полости рта.
- Streptococcusmitis – в норме выделяется из слюны, мокроты фекалий, при этом может выделяться из верхних дыхательных путей и крови при нозокомиальном инфицировании.
- Совсем неверно упоминать в этом блоке стрептококки группы Anginosus -Streptococcusintermedius/S.anginosus/S.constellatus, но так как мы обсуждаем в основном орофарингеальную флору, способную вызвать инфекционные эндокардиты (и чтобы не писать еще один, совсем малюсенький блок), мы упомянем их здесь. В норме они являются представителями пародонтогенной группы. Но стоит представителю группы S.intermedius оттуда выбраться, как он может вызывать абсцессы печени, мозга и эндокардиты, так как проявляет высокую тропность к их тканям.
Диагностические аспекты
Освоив вышеприведенный материал, мы видим, что только обнаружение данных микроорганизмов в стерильных средах может указывать на них как на потенциальных возбудителей. Почему все-таки потенциальных? Да потому, что в 80% случаев это может оказаться банальной контаминацией в связи с несоблюдением техники забора материала (все мы дышим, и если материал забирается с нарушением правил асептики и антисептики и без использования закрытых систем, то налететь в пробирку может много чего и не только из наших рта и носов). Таким образом, посевы нужно повторять.
Обнаружение этого же зоопарка в местах естественного его обитания не говорит нам практически ничего, если только пациент совсем не следит за полостью рта, и тогда ему можно настоятельно рекомендовать посещение стоматолога.
Аспекты антибактериальной терапии
Группа зеленящих стрептококков природно резистентна к тетрациклинам, макролидам и клиндомицину (до 50% штаммов), к биссептолу резистентно более 75%. Таким образом об этих группах мы даже не вспоминаем.
Само лечение должно быть комплексным и часто в сочетании с хирургическим. Выбор конкретных препаратов будет зависеть от локализации процесса, тяжести состояния пациента и выделенного возбудителя
Например, чувствительность Streptococcus mitis будет выглядеть так (нажмите на картинку для увеличения):
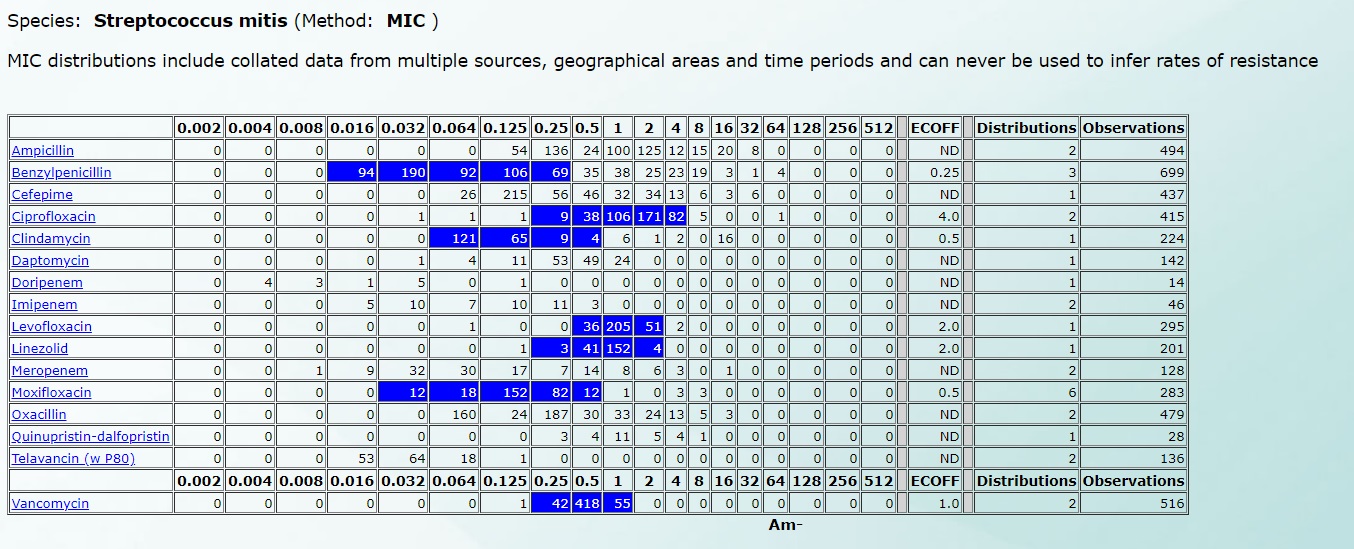
А чувствительность к Streptococcus mutans – вот так (нажмите на картинку для увеличения):
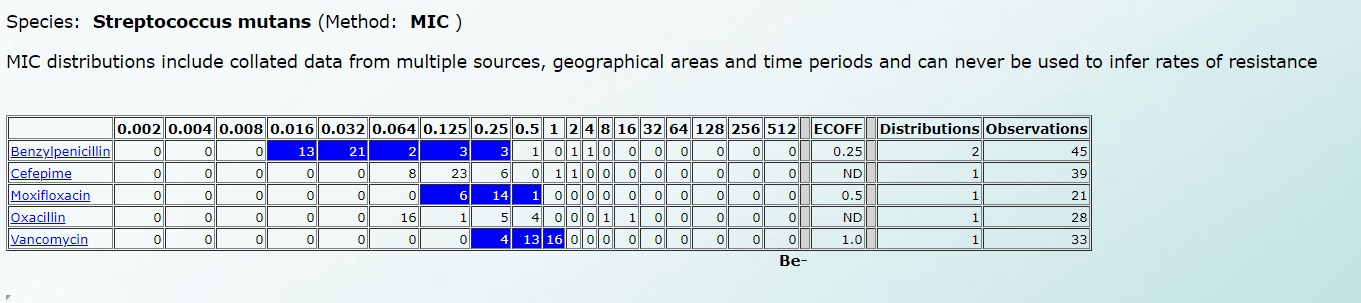
Подробнее все рассмотреть можно по этой ссылке, ведь именно на этой базе данных работают автоматические и полуавтоматические анализаторы в микробиологических лабораториях.
Препаратами выбора будут являться:
- Пенициллин в высоких дозировках (до 24 млн ЕД в сутки), возможно, в сочетании с аминогликозидами
- Цефтриаксон
- Ванкомицин
Как и в случае с любым стрептококком, крайне важно соблюдать длительность лечения, и она должна быть не менее 10-14 дней. Исключение составляет бактериальный эндокардит, там сроки лечения как минимум удваиваются.
В заключение хотелось бы сказать, что как ни прискорбно это сознавать, но недоступность, в первую очередь финансовая, адекватной стоматологической помощи вновь привела к всплеску заболеваний связанных с неблагополучием в полости рта, таким образом, мы вновь вынуждены вспоминать, что инфекционный эндокардит – это не только болезнь наркоманов и лиц со сниженным иммунным статусом, но и тех, у кого недостаточно средств на хорошего стоматолога, а потому и нам не лишне иногда осматривать полость рта у пациентов с инфекциями кровотока или абсцессами в головном мозге или печени.
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Микробиологические аспекты
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста. Так что без клинической картины острого фарингита не надо хвататься за антибиотики, как собственно и что-то сеять вне обострений.
100% штаммов чувствительны к пенициллинам, при этом Резистентность к макролидам в Европе – от 2 до 32%, в США – 7%. У нас в связи с великой любовью к этой группе, особенно среди педиатров, скорее всего, как в Европе. То есть о макролидах в этой ситуации надо забыть, к тому же тем же азитромицином не получится создать необходимую экспозицию в связи с ограничениями по срокам применения.
Клинические аспекты
При всем вышеперечисленном БГСА – зверь страшный, и основная проблема в том, что страх к нему мы почти потеряли. Лирическое отступление on. Именно этот зверь был постоянной причиной хирургических инфекций и родильной горячки (послеродового сепсиса) в доантибиотиковую эру. А женщины, как вы помните, умирали от нее, как мухи, пока Земмельвейс не заставил врачей мыть руки (за что закончил в психушке), но они их хотя бы на руках таскать перестали. Но даже сейчас, не дай бог, хирургу со стрептококковой ангиной подойти к операционному столу, и к концу первых суток стрептококк организует очень больную и страшно воняющую проблему в конкретной послеоперационной ране. Лирическое отступление off.
Потому напомним, что S.pyogenes может вызывать следующие заболевания:
- Фарингиты
- Поражения кожи и мягких тканей – целлюлиты, эризипелоид, лимфангит, рожа
- Некротические миозиты и фасцииты
- Послеродовый сепсис
- Пневмонии
- Сепсис
- Бактериальные эндокардиты (раньше редко, все же ангины и скарлатины старая школа требовала лечить строго 14 дней и ампициллином в задницу: сейчас стали встречаться почаще – привет коротким курсам антибиотиков при лечении ангин)
- Действие токсинов запускают синдром токсического шока и скарлатину
- Аутоиммунное воздействие приводит к ревматическим лихорадкам, с последующими возможным формированием пороков сердца и острому гломерулонефриту
- Послеоперационные раневые инфекции первых суток
Практические вопросы диагностики:
Микробиологическая диагностика S.pyogenes не представляет никакого труда, здесь в прямом смысле достаточно покрасить мазок по Граму. Все упирается в организационные аспекты – пока мазок доберется до лаборатории, пока покрасят. Пока ответят, пациент успеет много раз осложнится, если это стрептококк, или выздороветь, если это был фарингит и вызвавший его вирус (все-таки до 60% фарингитов вызваны вирусами, а не бактериальной флорой). Не хотелось бы останавливаться подробно на каждом перечисленном заболевании, но не упомянуть о диагностике острого фарингита, которая чаще всего и запускает множество вторичных осложнений, мы не можем. Для облегчения диагностики острого существуют несколько диагностических шкал. Автору более всего симпатична шкала Мак-Айзека в виду максимальной простоты ее использования.
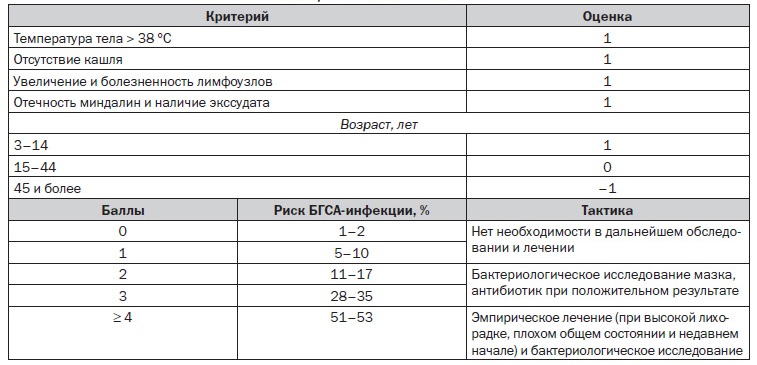
Но самым быстрым тестом для точной диагностики на месте является стрептатест, который в течение пяти минут дает ответ о вероятности наличия БГСА у больного с острым фарингитом.
Аспекты медикаментозного лечения
- Итак, мы определили, что имеем дело с БГСА, и тогда препаратами выбора в амбулаторной практике будут являться аминопенициллины, так как их много, они доступны, и главное, к ним 100% чувствительность у возбудителя.
Если ангина произошла впервые в жизни – лечим 10 дней. Если имеем дело с постоянными рецидивами – 14 дней, так как зверь может уйти во внутриклеточное состояние, оттуда руля процессом, и, чтобы до него добраться, доза должна быть выше средней, а курс лечения соответствующим.
Когда БГСА может уйти внутрь клетки? На тех самых пресловутых 5-7 днях, когда налеты с миндалин только сошли, температура только-только нормализовалась, а антибиотик взяли и отменили. И хорошо, если после подобного произойдет только рецидивирование фарингита, а не начнутся такие осложнения, как ревматизм, гломерулонефриты и далее по списку.
- Если пациент оказался в стационаре и ему обеспечен венозный доступ, то могут использоваться и пенициллины, и ампициллин в разных его вариациях. Главное – правильная доза, правильная кратность и ПРАВИЛЬНАЯ ДЛИТЕЛЬНОСТЬ КУРСА. Идеальный вариант из серии "дешево и сердито". Но обязательно должна быть доказанная микробиология.
При непереносимости пенициллинов помним о клиндамицине как об их адекватной замене.
- Пиогенный стрептококк, как мы выше упомянули, является причиной ранней послеоперационной раневой инфекции. Напомним, что стандартная послеоперационная раневая инфекция развивается к седьмым суткам. А если это произошло в первые сутки, да к тому же страшно завоняло (пиогенный стрептококк недаром называют мясоедным), немедленно делаем мазок, бежим с ним в лабораторию (можно даже своими ногами – это же ваш пациент осложнился, там так же бегом делают мазок по Граму, обнаруживают цепочки, и после этого начинаем лить аминопенициллин в вену, если не использовали его для периоперационной антибиотикопрофилактики (если использовали, то просто продолжаете дальше). Если совсем все бедно, можно пенициллин – 12 млн в сутки. Но если вы провели правильную периоперационную антибиотикопрофилактику, учли все риски и не забыли про свой личный стрептококк в горле, то риск ранней раневой минимален, а если профилактика продленная на 72 часа, то она и раскрутиться не успеет.
- При инфекциях кожи и мягких тканей, а также стрептококковом сепсисе препаратами выбора будут клиндамицин (который блокирует выработку токсических продуктов) в сочетании с пенициллином (24 млн ЕД в сутки) – это наиболее предпочтительная и малозатратная комбинация
Альтернативой в режиме монотерапии могут служить:
-
600 мг в/в каждые 6 часов 2,0 каждые шесть часов 2-3 г в/в каждые 6 часов или цефтриаксон по 2 г в сутки внутривенно в расчете 15 мг/кг в/в каждые 12 часов
Почему максимально важно соблюдать как дозировку, так и кратность введения читаем тут – /vracham/antibiotikoterapiya/polozheniya (часть 1 и часть 2).
В заключение хочется снова воскликнуть – пожалуйста, помните о пиогенном стрептококке и о правильной длительности его лечения.
Что подразумевают под острым тонзиллитом? Почему при БГСА-тонзиллите необходима антибактериальная терапия? Какие антибактериальные средства выбрать? Острый тонзиллит (ангина) 1 — заболевание, которое характеризуется острым воспалением одного ил
Что подразумевают под острым тонзиллитом?
Почему при БГСА-тонзиллите необходима антибактериальная терапия?
Какие антибактериальные средства выбрать?

Острый тонзиллит (ангина) 1 — заболевание, которое характеризуется острым воспалением одного или нескольких лимфоидных образований глоточного кольца (чаще небных миндалин) и принадлежит к числу широко распространенных инфекций верхних дыхательных путей.
Наиболее значимым бактериальным возбудителем острого тонзиллита является β-гемолитический стрептококк группы А (Streptococcus pyogenes, БГСА). Реже острый тонзиллит вызывают вирусы, стрептококки групп C и G, Arcanobacterium haemolyticum, Neisseria gonorrhoeae, Corynebacterium diphtheria (дифтерия), анаэробы и спирохеты (ангина Симановского — Плаута — Венсана), крайне редко — микоплазмы и хламидии.
БГСА передается воздушно-капельным путем. Источниками инфекции являются больные и реже бессимптомные носители. Вероятность заражения увеличивается при высокой степени обсемененности и тесном контакте с больным. Вспышки острого БГСА-тонзиллита чаще всего встречаются в организованных коллективах (в детских дошкольных учреждениях, школах, воинских частях и т. д.). Поражаются преимущественно дети в возрасте 5-15 лет, а также лица молодого трудоспособного возраста. Наибольшая заболеваемость отмечается в зимне-весенний период.
Высокая частота заболевания, контагиозность инфекции, большие трудопотери, влекущие за собой экономический ущерб, возможность развития серьезных осложнений — все это свидетельствует о том, что проблема БГСА-тонзиллита по-прежнему стоит достаточно остро как в научном, так и в практическом аспекте.
Клиническая картина. Инкубационный период при остром БГСА- тонзиллите составляет от нескольких часов до 2-4 дней. Для этого заболевания характерны острое начало с повышением температуры до 37,5–39°С, познабливание или озноб, головная боль, общее недомогание, боль в горле, усиливающаяся при глотании; нередки артралгии и миалгии. У детей могут быть тошнота, рвота, боли в животе. Развернутая клиническая картина наблюдается, как правило, на вторые сутки с момента начала заболевания, когда общие симптомы достигают максимальной выраженности. При осмотре выявляется покраснение небных дужек, язычка, задней стенки глотки. Миндалины гиперемированы, отечны, часто с гнойным налетом желтовато-белого цвета. Налет рыхлый, пористый, легко удаляется шпателем с поверхности миндалин без кровоточащего дефекта. У всех больных отмечаются уплотнение, увеличение и болезненность при пальпации шейных лимфатических узлов на уровне угла нижней челюсти (регионарный лимфаденит). В анализах крови — повышенный лейкоцитоз (9-12 10 9 /л), сдвиг лейкоцитарной формулы влево, ускорение СОЭ (иногда до 40-50 мм/ч), появление С-реактивного белка. Длительность периода разгара (без лечения) составляет примерно 5-7 дней. В дальнейшем при отсутствии осложнений основные клинические проявления болезни (лихорадка, симптомы интоксикации, воспалительные изменения в миндалинах) быстро исчезают, нормализуется картина периферической крови. Симптомы регионарного лимфаденита могут сохраняться до 10-12 дней.
Диагноз БГСА-тонзиллита подтверждается микробиологическим исследованием мазка с поверхности миндалин и/или задней стенки глотки. При соблюдении правил техники забора образца чувствительность метода достигает 90 %, а специфичность — 95-99 %. Популярные за рубежом методы экспресс-диагностики А-стрептококкового антигена в мазках из зева дают возможность получить ответ через 15-20 мин. В то же время следует подчеркнуть, что культуральный метод не позволяет дифференцировать активную инфекцию от БГСА-носительства, а современные экспресс-тесты, несмотря на их высокую специфичность (95-100%), характеризуются сравнительно низкой чувствительностью (60-80%), то есть отрицательный результат быстрой диагностики не исключает стрептококковой этиологии заболевания.
Дифференциальная диагностика острого БГСА-тонзиллита, основанная только на клинических признаках, нередко представляет собой достаточно трудную задачу даже для опытных врачей. Однако необходимо отметить, что наличие респираторных симптомов (кашля, ринита, охриплости голоса и др.), а также сопутствующие конъюнктивит, стоматит или диарея указывают на вирусную этиологию острого тонзиллита. В отличие от скарлатины для острого БГСА-тонзиллита не характерны какие-либо виды высыпаний на коже и слизистых. При локализованной дифтерии ротоглотки налет с миндалин снимается с трудом, не растирается на предметном стекле, не растворяется в воде, а медленно оседает на дно сосуда; после удаления налета отмечается кровоточивость подлежащих тканей. Ангинозная форма инфекционного мононуклеоза, как правило, начинается с распространенного поражения лимфатических узлов (шейных, затылочных, подмышечных, абдоминальных, паховых), симптоматика тонзиллита развивается на 3-5-й день болезни, при исследовании периферической крови выявляется лейкоцитоз с преобладанием мононуклеаров (до 60-80%). Ангина Симановского — Плаута — Венсана характеризуется слабо выраженными признаками общей интоксикации и явлениями одностороннего язвенно-некротического тонзиллита, при этом возможно распространение некротического процесса на мягкое и твердое небо, десны, заднюю стенку глотки и гортань.
Поскольку БГСА-тонзиллит по своей сути — самокупирующееся заболевание и может заканчиваться полным выздоровлением (даже при отсутствии лечения) без каких-либо осложнений, у некоторых врачей по-прежнему существуют сомнения в отношении тщательности курации таких больных. Совершенно необоснованно отдается предпочтение местному лечению (полосканиям, ингаляциям и др.) в ущерб системной антибиотикотерапии. Подобный подход ни в коей мере не оправдывает себя и может привести к весьма печальным для больного последствиям.
Лечение. Несмотря на то что БГСА по-прежнему сохраняет практически полную чувствительность к β-лактамным антибиотикам, в последние годы отмечаются определенные проблемы в терапии тонзиллитов, вызванных этим микроорганизмом. По данным разных авторов, частота неудач пенициллинотерапии БГСА-тонзиллитов составляет 25-30%, а в некоторых случаях — даже 38%. Одной из возможных причин этого может быть гидролиз пенициллина специфическими ферментами — β-лактамазами, которые продуцируются микроорганизмами — копатогенами (золотистым стафилококком, гемофильной палочкой и др.), присутствующими в глубоких тканях миндалин, особенно при наличии хронических воспалительных процессов в последних.
Как видно из табл. 1, препараты пенициллинового ряда остаются средствами выбора только при лечении острого БГСА-тонзиллита. На сегодняшний день оптимальным препаратом из группы оральных пенициллинов представляется амоксициллин, который по противострептококковой активности аналогичен ампициллину и феноксиметилпенициллину, но существенно превосходит их по своим фармакокинетическим характеристикам, отличаясь большей биодоступностью (95, 40 и 50 % соответственно) и меньшей степенью связывания с сывороточными белками (17, 22 и 80 %). При сомнительной комплаентности (исполнительности) больного, а также в определенных клинико-эпидемиологических ситуациях показано назначение однократной инъекции бензатин-пенициллина.
Феноксиметилпенициллин целесообразно назначать только детям младшего возраста, учитывая наличие лекарственной формы в виде суспензии, а также несколько большую комплаентность, обеспечиваемую благодаря контролю со стороны родителей, чего нельзя сказать о подростках.
Наряду с пенициллинами несомненного внимания заслуживает представитель оральных цефалоспоринов I поколения цефадроксил, высокая эффективность которого в терапии БГСА-тонзиллитов, а также хорошая переносимость подтверждены в ходе многочисленных клинических исследований.
При непереносимости β-лактамных антибиотиков целесообразно назначать макролиды (спирамицин, азитромицин, рокситромицин, кларитромицин, мидекамицин). Наряду с высокой противострептококковой активностью преимуществами этих препаратов являются способность создавать высокую тканевую концентрацию в очаге инфекции, более короткий (в частности, для азитромицина) курс лечения, хорошая переносимость. Применение эритромицина — первого представителя антибиотиков данного класса — в настоящее время существенно сократилось, особенно в терапевтической практике, поскольку он чаще других макролидов вызывает нежелательные эффекты со стороны желудочно-кишечного тракта, обусловленные стимулирующим действием эритромицина на моторику желудка и кишечника.
Антибиотики-линкозамины (линкомицин, клиндамицин) назначают при БГСА-тонзиллите только при непереносимости как b-лактамов, так и макролидов. Широко применять эти препараты при данной нозологической форме не рекомендуется. Известно, что при частом применении оральных пенициллинов чувствительность к ним со стороны зеленящих стрептококков, локализующихся в ротовой полости, существенно снижается. Поэтому у данной категории пациентов, среди которых немало больных с ревматическими пороками сердца, линкозамины рассматриваются как препараты первого ряда для профилактики инфекционного эндокардита при выполнении различных стоматологических манипуляций.
При наличии хронического рецидивирующего БГСА-тонзиллита вероятность колонизации очага инфекции микроорганизмами, продуцирующими b-лактамазы, достаточно высока. В этом случае целесообразно проведение курса лечения ингибитор-защищенными пенициллинами (амоксициллин/клавуланат) или оральными цефалоспоринами II поколения (цефуроксим — аксетил), а при непереносимости b-лактамных антибиотиков — линкозаминами (табл. 2). Указанные антибиотики рассматриваются также как препараты второго ряда для случаев, когда пенициллинотерапия острого БГСА-тонзиллита оказывается безуспешной (что чаще встречается при использовании феноксиметилпенициллина). Универсальной же схемы, обеспечивающей 100%-ную элиминацию БГСА из носоглотки, в мировой клинической практике не сууществует.
Необходимо отметить, что применение тетрациклинов, сульфаниламидов, ко-тримоксазола и хлорамфеникола при БГСА-инфекции глотки в настоящее время не оправдано по причине высокой частоты резистентности и, следовательно, низких показателей эффективности терапии.
Таким образом, в современных условиях вопросы своевременной и качественной диагностики и рациональной антибиотикотерапии БГСА-тонзиллита сохраняют свою актуальность. Появившиеся в последние годы новые антибактериальные средства существенно расширили возможности антимикробной терапии БГСА-тонзиллита, но полностью данную проблему не решили. В связи с этим многие исследователи возлагают большие надежды на создание вакцины, содержащей эпитопы М-протеинов ревматогенных БГСА- штаммов, не вступающих в перекрестную реакцию с тканевыми антигенами человеческого организма. Такая вакцина, в частности в рамках первичной профилактики ОРЛ, очень необходима в первую очередь лицам с генетическими маркерами, указывающими на предрасположенность к заболеванию.
Назначение антибиотиков при катаральной ангине и неосложненных формах хронического тонзиллита не всегда оправданно, тем более без четкого представления о возбудителе.
На этих стадиях заболевания, еще не отягощенных суперинфекцией, альтернативным лечением может стать гомеопатия. Это регулирующая терапия, воздействующая на процессы саморегуляции с помощью лекарств, подобранных индивидуально с учетом реакции больного. С позиций классической гомеопатии ангина и хронический тонзиллит являются не локальными заболеваниями, а частным проявлениями конституционной слабости и наследственной предрасположенности.
1 В зарубежной литературе широко используются взаимозаменяемые термины "тонзиллофарингит" и "фарингит".
Читайте также:

