Стрептококки группы а пожирающие плоть
Обновлено: 24.04.2024
В этой статье мы поговорим о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Почему за исключением S. pyogenes? Да потому что данного возбудителя мы рассмотрели в отдельной статье. Кроме того, мы уже говорим практически на одном языке, а потому можем себе позволить поговорить о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Микробиологические аспекты
Для начала разберемся с классификациями, чтобы понимать принципы разнесения стрептококков по группам. Так сложилось, что для классификации стрептококков используются их фенотипические характеристики, а именно характеристики по гемолитическим свойствам:
- β-гемолитические стрептококки вызывают полный гемолиз эритроцитов питательной среды с формированием прозрачной зоны вокруг колоний на кровяном агаре
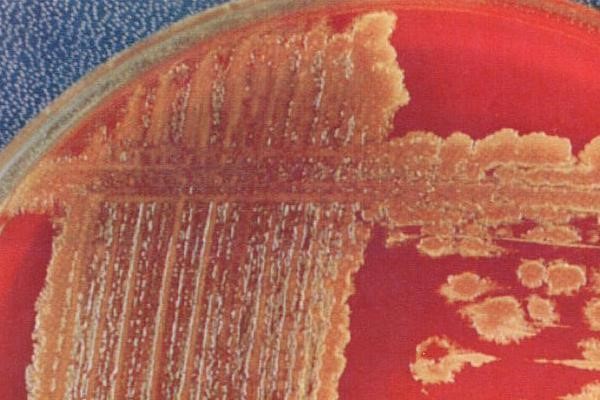
- α-гемолитические (зеленящие) образуют зеленоватый ореол вокруг колоний в результате неполного разложения гемоглобина
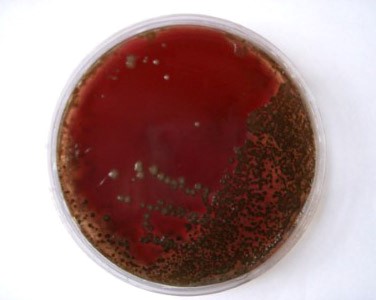
- γ-гемолитические по-другому именуются негемолитическими, то есть ничего никуда из крови не разлагают.
Собственно, почему кровь? Дело в том, что стрептококки крайне требовательны к питательным средам и к условиям, в которых их растят. И чтобы они выросли, в питательные среды (в основном, жидкие) необходимо или добавлять мясной экстракт, или использовать коммерческие питательные среды с добавлением крови барана, или 5%-й кровяной агар – и все это с большим количеством дополнительных компонентов. Для определения характера гемолиза традиционно используется среда с 5%-й дефибринированной кровью барана.
Подобное разделение по группам и типам гемолиза является решающим для деления стрептококков, имеющих медицинское значение, позволяя разделить патогенные и условно-патогенные микроорганизмы. Про патогенные мы уже поговорили ранее, теперь будем вести разговор о более обширной группе условно-патогенных представителей и начнем со стрептококков групп A, C, D и F, оставив для отдельного разговора группу В и единственного ее представителя – S. agalactiae.
Основными характеристиками представителей этих групп является то, что все они:
- Обладают β-гемолитической активностью
- Относятся к нормальной микрофлоре человека и животных
- Могут вызывать оппортунистические инфекции в различных локализациях
- Fc-антиген, способный взаимодействовать с Fc-фрагментом IgG, тем самым угнетая систему комплемента и подавляя активность фагоцитов. Кроме того, он же активирует выработку аутоиммунных антител, которые в дальнейшем участвуют в развитии иммунного воспаления;
- Р-антиген, обладающий иммуносупрессивной активностью и являющийся общим для всех стрептококков. Он подавляет выработку антител и усиливает реакции гиперчувствительности замедленного типа.
Кроме того, стрептококки имеют такой фактор патогенности, как М-протеин, который нарушает фагоцитарную активность путем маскировки рецепторов для комплемента, что очень затрудняет борьбу с этими возбудителями.
Клинические аспекты
1. Streptococcus dysgalactiae – объединяет двух представителей Streptococcus dysgalactiae subsp. dysgalactiae и Streptococcus dysgalactiae subsp. equisimilis. Первый живет на животных (и вызывает маститы у коров, на человеке в качестве возбудителя пока не ловили), второй на человеке – в верхних дыхательных путях и влагалище – и может быть причиной менингита, септических артритов и инфекций кожи (при условии наличия соответствующей симптоматики и в отсутствии других вероятных возбудителей).
2. Стрептококки группы Anginosus (S. anginosus, S. constellatus, S. intermedius) относятся к представителям нормальной флоры человека. Обрести зубы и стать возбудителями инфекции их могут заставить травмы, оперативные вмешательства, сахарный диабет, онкологические заболевания и иммунодефициты различной этиологии. Сами по себе на человека не бросаются и обнаружение оных вне клинической картины истребления не требует.
- S.anginosus – в норме обитает в полости рта, верхних дыхательных путях и влагалище. При патологии может быть высеян из урогенитальной и желудочно-кишечной локализаций.
- S. constellatus – в норме живет в верхних дыхательных путях и ЖКТ. При патологических процессах могут быть обнаружены где угодно.
- S. intermedius – в норме обитает в полости рта и верхних дыхательных путях. При патологических процессах в основном высевается из мозга, из крови при эндокардитах и из печеночных абсцессов (проще говоря оттуда, где в норме все должно быть стерильно).
3. S. equi клинического значения не имеет, так как является зоонозом и вызывает ветеринарные проблемы у коров, лошадей, морских свинок, овец и коз. Иногда – при употреблении зараженных молочных продуктов – может быть обнаружен у людей, больных нефритом.
4. S. canis, как понятно из названия, выделяют от собак. У людей могут вызывать инфекции мягких тканей, пневмонии, сепсис, остеомиелит.
5. S. iniae – обнаруживается у дельфинов и рыб. А также у людей, занятых на обработке замороженной рыбы. Крайне редко вызывает заболевание (описаны всего несколько случаев), хорошо лечится бета-лактамами и макролидами.
6. И несколько чисто зоонозных представителей, не имеющих медицинского значения, но иногда сеющихся с людей, которые за этими животными ухаживают или лечат:
- S. porcinus – вызывает абсцессы глотки свиней, пневмонию и аборты;
- S. didelphis – вызывает инфекции кожи, печени, легких и селезенки у опоссумов;
- S. phocae – выделяется у морских котиков при пневмонии у оных.
Как мы увидели, в большинстве своем перечисленные возбудители относятся к нормальной микрофлоре верхних дыхательных путей, кожи, ЖКТ и урогенитального тракта, а чтобы они вызвали заболевание, во внутреннюю среду организма должно проникнуть очень большое количество оных, при этом иммунная система должна быть подавлена тем или иным образом. Чаще всего такую роль играют медицинские вмешательства (инъекции, операции, катетеризация сосудов, гемодиализ и т. п.) на фоне тяжелых основных или сопутствующих заболеваний. Тогда стрептококки способны вызвать инфекции кожи и мягких тканей, верхних дыхательных путей, эндокардиты и сепсис, инфекции урогенитального тракта, при этом строгой локализации процесса соответствующим возбудителем уже не будет, а будет инфекция, связанная с медицинским вмешательством.
Что делать?
Как можно раньше провести бактериологическую диагностику и главным в ней будет правильная техника взятия биологического материала, чтобы точно исключить его контаминацию ни в чем не повинными мирными соседями, просмотрев истинного возбудителя. Техника взятия материала и правила транспортировки в лабораторию подробно расписаны здесь.
Чем лечить?
Этот вопрос мы можем задать только тогда, когда точно понимаем, что именно вышеуказанные зверушки являются возбудителями и никто за ними не прячется. Хорошая новость в том, что стрептококки до сих пор сохранили высокую чувствительность к бета-лактамам вообще и к пенициллинам в частности, то есть лечить их дешево. Плохая новость в том, что фактически утеряна чувствительность к макролидам, и поэтому они не могут быть препаратами выбора – это обязательно надо учитывать при назначении стартовой терапии.
Кроме того, стрептококки продолжают демонстрировать высокую чувствительность к ванкомицину, но в виду неоднозначности самого препарата в плане безопасности его применения, им тоже не следует злоупотреблять и включать его в схему лечения только в случае наличия аллергии к пенициллиновому ряду.
Итак, мы закончили краткое рассмотрение представителей стрептококков групп A, C, D, F и G, и нам осталось рассмотреть только одного представителя из группы В, а именно S.agalactiae, чем мы и займемся в следующей статье.
Стрептококковые инфекции вызванные Streptococcus pyogenes: диагностика, лечение, профилактика
Стрептококки — грамположительные кокки, располагающиеся в микропрепарате в виде цепочки или парами. Факультативные анаэробы требовательны к питательным средам. Хорошо растут на средах с большим содержанием крови. Колонии бета-гемолитического стрептококка на кровяном агаре окружены зоной полного гемолиза, а-гемолитического стрептококка — зоной частичного гемолиза.
Дальнейшая идентификация основана на изучении биохимических и серологических (классификация Лэнсфилд) свойств возбудителя. Исследуемый материал — мазок из зева, раневое отделяемое, кровь и др.
Стрептококковые инфекции вызванные Streptococcus pyogenes
Носительство в глотке S. pyogenes протекает бессимптомно примерно у 5—30% населения. Передача инфекции осуществляется посредством аэрозольного и контактного механизмов. Заражение может произойти в любом возрасте, но чаще всего инфекция возникает у детей.
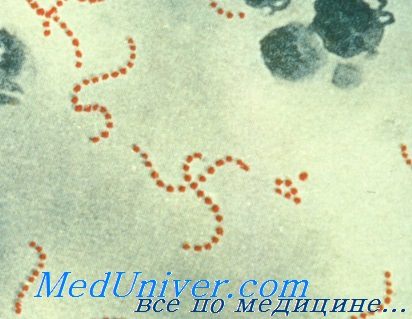
Патогенез стрептококковых инфекций вызванных Streptococcus pyogenes
S. pyogenes имеет углеводный (полисахаридный) группоспецифический антиген А (антиген Лэнсфилд) и группоспецифический белковый М-антиген, и располагающиеся на поверхности микроорганизма М-протеином (антиген), препятствующий лейкоцитарному фагоцитозу.
Антитела к М-протеину и располагающимся на поверхности микроорганизма М-протеину (антиген) формируют устойчивый иммунитет к последующей инфекции, вызванной микроорганизмами с такими же типами М-протеина. Кроме того, S. pyogenes продуцируют несколько токсинов: эритрогенный токсин (вызывает сыпь при скарлатине) и пирогенные экзотоксины А, В и С. Адгезию обеспечивают рецепторы к фибронектину.
Возбудители способны долгое время персистировать внутри клеток эпителия зева, а потому некоторые антибиотики (не проникающие внутриклеточно) не избавляют пациента от носительства.
Клинические признаки стрептококковых инфекций вызванных Streptococcus pyogenes
S. pyogenes входит в число десяти самых смертоносных возбудителей в мире. Он вызывает три вида патологических состояний:
• Инфекционное заболевание. S. pyogenes — самая частая причина развития бактериального фарингита. Кроме того, он вызывает рожу, импетиго, целлюлит, раневые инфекции и реже некротизирующий фасцит и пневмонию. Иногда развивается септицемия, приводящая к метастазирующим инфекциям (остеомиелит). Инфекционный процесс, обусловленный S. pyogenes, характеризуется острым началом с деструкцией поражённых тканей и быстро прогрессирующим течением.
Неотъемлемой частью патогенеза, развивающегося выраженного интоксикационного синдрома, является способность S. pyogenes продуцировать токсины.
• Токсин — индуцированные синдромы, протекающие на фоне инфекционного заболевания. Инфекционное заболевание, связанное с S. pyogenes, может протекать в виде генерализованного процесса или, оставаясь локализованным, сопровождаться системными проявлениями, связанными с действием экзотоксинов.
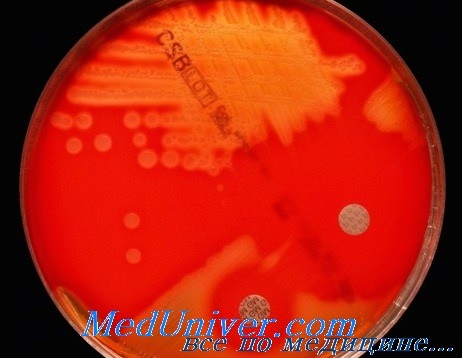
Например, действие эритрогенного токсина обусловливает возникновение сыпи при скарлатине, а пирогенные токсины становятся причиной стрептококкового шока, часто приводящего к смерти пациента вследствие полиорганной патологии. • Постинфекционные аутоиммунные заболевания. Перекрёстное взаимодействие антител к антигенам бактерии и структурным компонентам собственных тканей организма иногда приводит к развитию аутоиммунных заболеваний: ревматической лихорадке, гломерулонефриту или узловатой эритеме.
Достаточно редкая в странах с развитой рыночной экономикой ревматическая лихорадка — частая причина смерти и инвалидизации населения в регионах с низким уровнем жизни и нищетой.
Профилактика стрептококковых инфекций вызванных Streptococcus pyogenes
Распространение S. pyogenes в хирургических отделениях и родильных домах происходит достаточно быстро. Именно поэтому больных и носителей стрептококковой инфекции нужно немедленно изолировать в отдельные боксы на срок не менее 48 ч от начала проведения эффективной антибиотикотерапии. Своевременное полноценное лечение позволяет избежать развития вторичных аутоиммунных заболеваний (ревматическая лихорадка).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Негемолитические стрептококки. Зеленящие стрептококки. Патогенез и клиника поражений зеленящими стрептококками. Микробиологическая диагностика негемолитических стрептококков. Выделение зеленящих стрептококков.
Негемолитические стрептококки представлены гетерогенной группой бактерий, дающих а-гемолиз (неполный). Они также лишены групповых Аг, но значительно отличаются от пневмококков. Поскольку большая их часть вызывает позеленение кровяных сред, они также известны как зеленящие стрептококки. Бактерии входят в состав микробных ценозов полости рта (составляют 30—60% всей микрофлоры) и кишечника человека.
Патогенез и клиника поражений зеленящими стрептококками
Негемолитические стрептококки отличает низкая вирулентность; вызываемые ими системные поражения можно в определённой степени рассматривать как оппортунистические .
Основную их часть составляют бактериальные эндокардиты, развивающиеся после проникновения негемолитических стрептококков в кровоток при травмировании слизистых оболочек (например, после чистки зубов, пережёвывании грубой пищи). Эндокардиты носят злокачественный характер и сопровождаются поражением сердечных клапанов. Способность вызывать эндокардиты обусловлена особенностями структуры гликанов (декстранов) клеточной стенки бактерий, облегчающих адгезию стрептококков к агрегатам тромбоцитов и фибрина на поврежденных клапанах. Для поражений характерны эмболии периферических сосудов: в ЦНС их отмечают в 30% случаев, в селезёнке — в 40% (данные аутопсий), в кожных покровах и глазах — в 20-40%.
Вторая по значимости, но несравненно более частая, патология — кариозное поражение зубов, вызываемое зеленящими стрептококками биогруппы mutans. Микроорганизмы содержат поверхностный белок, связывающий гликопротеины слюны, и (совместно с другими бактериями) образуют бактериальные бляшки на поверхности зубов. Бактерии разлагают сахарозу, поступающую с пищей, до молочной кислоты, вызывающей деминерализацию зубной эмали.
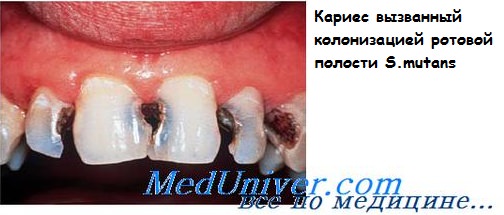
Микробиологическая диагностика зеленящих стрептококков
Микробиологическая диагностика негемолитических стрептококков аналогична мероприятиям, провидимым для выделения и идентификации прочих стрептококков. На наличие возбудителей указывает появление мелких (диаметром около 0,5 мм) колоний, окружённых зоной а-гемолиза. Дальнейшую дифферешш-ровку обычно проводят по отсутствию способности расти в жидких средах, содержащих 6,5% NaCl, и гидролизовать эскулин в присутствии солей жёлчных кислот (могут быть положительны у 10% изолятов); также дифференцирующим признаком считают отсутствие чувствительности к оптохину (последний не ингибирует рост бактерий). Дополнительным признаком служит высокая чувствительность большинства изолятов к пенициллину.
Лечение инфекций вызванных негемолитическими стрептококками
Лечение инфекций вызванных зеленящими стрептококками принципиально не отличается от проводимого при других стрептококковых инфекциях.
- Вернуться в оглавление раздела "Микробиология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Микробиологические аспекты
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста. Так что без клинической картины острого фарингита не надо хвататься за антибиотики, как собственно и что-то сеять вне обострений.
100% штаммов чувствительны к пенициллинам, при этом Резистентность к макролидам в Европе – от 2 до 32%, в США – 7%. У нас в связи с великой любовью к этой группе, особенно среди педиатров, скорее всего, как в Европе. То есть о макролидах в этой ситуации надо забыть, к тому же тем же азитромицином не получится создать необходимую экспозицию в связи с ограничениями по срокам применения.
Клинические аспекты
При всем вышеперечисленном БГСА – зверь страшный, и основная проблема в том, что страх к нему мы почти потеряли. Лирическое отступление on. Именно этот зверь был постоянной причиной хирургических инфекций и родильной горячки (послеродового сепсиса) в доантибиотиковую эру. А женщины, как вы помните, умирали от нее, как мухи, пока Земмельвейс не заставил врачей мыть руки (за что закончил в психушке), но они их хотя бы на руках таскать перестали. Но даже сейчас, не дай бог, хирургу со стрептококковой ангиной подойти к операционному столу, и к концу первых суток стрептококк организует очень больную и страшно воняющую проблему в конкретной послеоперационной ране. Лирическое отступление off.
Потому напомним, что S.pyogenes может вызывать следующие заболевания:
- Фарингиты
- Поражения кожи и мягких тканей – целлюлиты, эризипелоид, лимфангит, рожа
- Некротические миозиты и фасцииты
- Послеродовый сепсис
- Пневмонии
- Сепсис
- Бактериальные эндокардиты (раньше редко, все же ангины и скарлатины старая школа требовала лечить строго 14 дней и ампициллином в задницу: сейчас стали встречаться почаще – привет коротким курсам антибиотиков при лечении ангин)
- Действие токсинов запускают синдром токсического шока и скарлатину
- Аутоиммунное воздействие приводит к ревматическим лихорадкам, с последующими возможным формированием пороков сердца и острому гломерулонефриту
- Послеоперационные раневые инфекции первых суток
Практические вопросы диагностики:
Микробиологическая диагностика S.pyogenes не представляет никакого труда, здесь в прямом смысле достаточно покрасить мазок по Граму. Все упирается в организационные аспекты – пока мазок доберется до лаборатории, пока покрасят. Пока ответят, пациент успеет много раз осложнится, если это стрептококк, или выздороветь, если это был фарингит и вызвавший его вирус (все-таки до 60% фарингитов вызваны вирусами, а не бактериальной флорой). Не хотелось бы останавливаться подробно на каждом перечисленном заболевании, но не упомянуть о диагностике острого фарингита, которая чаще всего и запускает множество вторичных осложнений, мы не можем. Для облегчения диагностики острого существуют несколько диагностических шкал. Автору более всего симпатична шкала Мак-Айзека в виду максимальной простоты ее использования.
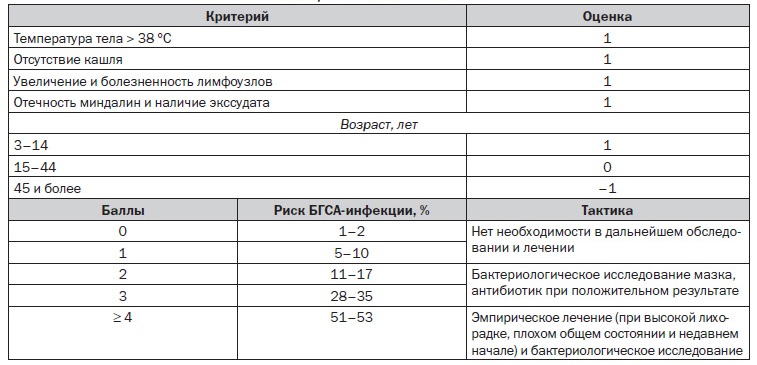
Но самым быстрым тестом для точной диагностики на месте является стрептатест, который в течение пяти минут дает ответ о вероятности наличия БГСА у больного с острым фарингитом.
Аспекты медикаментозного лечения
- Итак, мы определили, что имеем дело с БГСА, и тогда препаратами выбора в амбулаторной практике будут являться аминопенициллины, так как их много, они доступны, и главное, к ним 100% чувствительность у возбудителя.
Если ангина произошла впервые в жизни – лечим 10 дней. Если имеем дело с постоянными рецидивами – 14 дней, так как зверь может уйти во внутриклеточное состояние, оттуда руля процессом, и, чтобы до него добраться, доза должна быть выше средней, а курс лечения соответствующим.
Когда БГСА может уйти внутрь клетки? На тех самых пресловутых 5-7 днях, когда налеты с миндалин только сошли, температура только-только нормализовалась, а антибиотик взяли и отменили. И хорошо, если после подобного произойдет только рецидивирование фарингита, а не начнутся такие осложнения, как ревматизм, гломерулонефриты и далее по списку.
- Если пациент оказался в стационаре и ему обеспечен венозный доступ, то могут использоваться и пенициллины, и ампициллин в разных его вариациях. Главное – правильная доза, правильная кратность и ПРАВИЛЬНАЯ ДЛИТЕЛЬНОСТЬ КУРСА. Идеальный вариант из серии "дешево и сердито". Но обязательно должна быть доказанная микробиология.
При непереносимости пенициллинов помним о клиндамицине как об их адекватной замене.
- Пиогенный стрептококк, как мы выше упомянули, является причиной ранней послеоперационной раневой инфекции. Напомним, что стандартная послеоперационная раневая инфекция развивается к седьмым суткам. А если это произошло в первые сутки, да к тому же страшно завоняло (пиогенный стрептококк недаром называют мясоедным), немедленно делаем мазок, бежим с ним в лабораторию (можно даже своими ногами – это же ваш пациент осложнился, там так же бегом делают мазок по Граму, обнаруживают цепочки, и после этого начинаем лить аминопенициллин в вену, если не использовали его для периоперационной антибиотикопрофилактики (если использовали, то просто продолжаете дальше). Если совсем все бедно, можно пенициллин – 12 млн в сутки. Но если вы провели правильную периоперационную антибиотикопрофилактику, учли все риски и не забыли про свой личный стрептококк в горле, то риск ранней раневой минимален, а если профилактика продленная на 72 часа, то она и раскрутиться не успеет.
- При инфекциях кожи и мягких тканей, а также стрептококковом сепсисе препаратами выбора будут клиндамицин (который блокирует выработку токсических продуктов) в сочетании с пенициллином (24 млн ЕД в сутки) – это наиболее предпочтительная и малозатратная комбинация
Альтернативой в режиме монотерапии могут служить:
-
600 мг в/в каждые 6 часов 2,0 каждые шесть часов 2-3 г в/в каждые 6 часов или цефтриаксон по 2 г в сутки внутривенно в расчете 15 мг/кг в/в каждые 12 часов
Почему максимально важно соблюдать как дозировку, так и кратность введения читаем тут – /vracham/antibiotikoterapiya/polozheniya (часть 1 и часть 2).
В заключение хочется снова воскликнуть – пожалуйста, помните о пиогенном стрептококке и о правильной длительности его лечения.
Читайте также:

