Стрептококки из за анального секса
Обновлено: 25.04.2024
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику, как и обзывательство антибактериальной терапии – антибиотикотерапией, а кто мы такие, чтобы отменять традиции.
Рассмотрим основных представителей семейства, на которых больше всего шансов наткнуться в антибиотикограммах.
- Streptococcussanguis – воистину могуч и вездесущ. Обнаруживается в зубных отложениях с самого прорезывания зубов и до конца жизни, где и есть основное место его обитания. Иногда может быть обнаружен на слизистой глотки и в фекалиях, куда попадают транзитом. При этом надо помнить, что этот микроб вносит существенный вклад в процессы, связанные с кариесом, занимая в последующем ведущее место в ассоциациях микроорганизмов, выделяемых из гнойного экссудата при воспалительных процессах в челюстно-лицевой области, включая одонтогенные абсцессы мозга и других органов. Кроме того, они же могут быть выделены их крови и сердечных клапанов больных инфекционным эндокардитом.
- Streptococcussalivarius – также является одним из основных компонентов нормальной микрофлоры полости рта, а также, но в меньшем количестве, может быть выделен со слизистых дыхательного, желудочно-кишечного и урогенитального тракта. Особенно часто выделяются при анализе микрофлоры языка, слюны и фекалий. И крайне редко из крови при менингитах, септицимии и эндокардитах.
- Streptococcusmutans – выделяется с поверхности зубов и фекалий. Этот микроб является кариесогенным, а значит, может в дальнейшем вызывать бактериемию и бактериальный эндокардит у пациентов, не занимающихся регулярной санацией кариозных очагов в полости рта.
- Streptococcusmitis – в норме выделяется из слюны, мокроты фекалий, при этом может выделяться из верхних дыхательных путей и крови при нозокомиальном инфицировании.
- Совсем неверно упоминать в этом блоке стрептококки группы Anginosus -Streptococcusintermedius/S.anginosus/S.constellatus, но так как мы обсуждаем в основном орофарингеальную флору, способную вызвать инфекционные эндокардиты (и чтобы не писать еще один, совсем малюсенький блок), мы упомянем их здесь. В норме они являются представителями пародонтогенной группы. Но стоит представителю группы S.intermedius оттуда выбраться, как он может вызывать абсцессы печени, мозга и эндокардиты, так как проявляет высокую тропность к их тканям.
Диагностические аспекты
Освоив вышеприведенный материал, мы видим, что только обнаружение данных микроорганизмов в стерильных средах может указывать на них как на потенциальных возбудителей. Почему все-таки потенциальных? Да потому, что в 80% случаев это может оказаться банальной контаминацией в связи с несоблюдением техники забора материала (все мы дышим, и если материал забирается с нарушением правил асептики и антисептики и без использования закрытых систем, то налететь в пробирку может много чего и не только из наших рта и носов). Таким образом, посевы нужно повторять.
Обнаружение этого же зоопарка в местах естественного его обитания не говорит нам практически ничего, если только пациент совсем не следит за полостью рта, и тогда ему можно настоятельно рекомендовать посещение стоматолога.
Аспекты антибактериальной терапии
Группа зеленящих стрептококков природно резистентна к тетрациклинам, макролидам и клиндомицину (до 50% штаммов), к биссептолу резистентно более 75%. Таким образом об этих группах мы даже не вспоминаем.
Само лечение должно быть комплексным и часто в сочетании с хирургическим. Выбор конкретных препаратов будет зависеть от локализации процесса, тяжести состояния пациента и выделенного возбудителя
Например, чувствительность Streptococcus mitis будет выглядеть так (нажмите на картинку для увеличения):
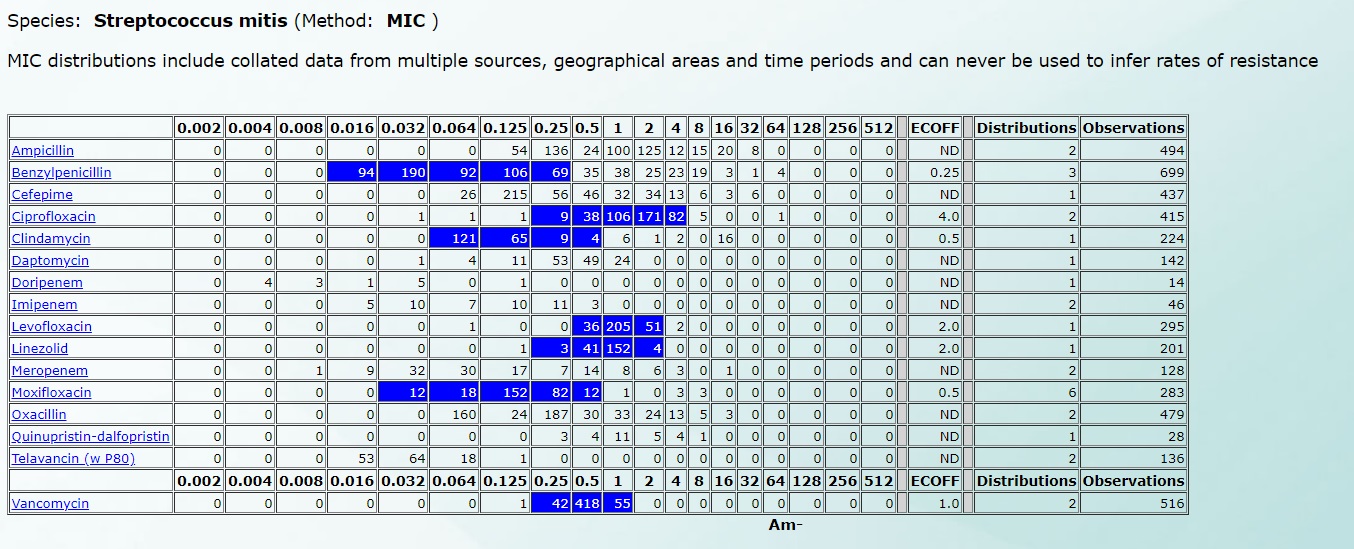
А чувствительность к Streptococcus mutans – вот так (нажмите на картинку для увеличения):
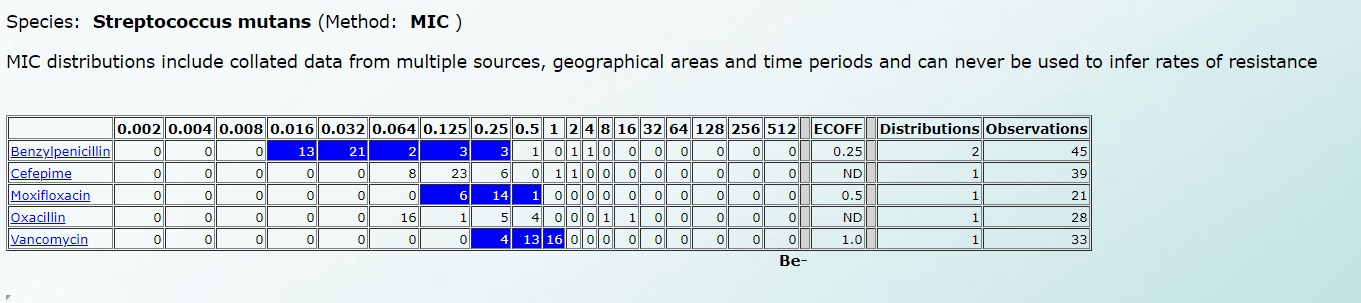
Подробнее все рассмотреть можно по этой ссылке, ведь именно на этой базе данных работают автоматические и полуавтоматические анализаторы в микробиологических лабораториях.
Препаратами выбора будут являться:
- Пенициллин в высоких дозировках (до 24 млн ЕД в сутки), возможно, в сочетании с аминогликозидами
- Цефтриаксон
- Ванкомицин
Как и в случае с любым стрептококком, крайне важно соблюдать длительность лечения, и она должна быть не менее 10-14 дней. Исключение составляет бактериальный эндокардит, там сроки лечения как минимум удваиваются.
В заключение хотелось бы сказать, что как ни прискорбно это сознавать, но недоступность, в первую очередь финансовая, адекватной стоматологической помощи вновь привела к всплеску заболеваний связанных с неблагополучием в полости рта, таким образом, мы вновь вынуждены вспоминать, что инфекционный эндокардит – это не только болезнь наркоманов и лиц со сниженным иммунным статусом, но и тех, у кого недостаточно средств на хорошего стоматолога, а потому и нам не лишне иногда осматривать полость рта у пациентов с инфекциями кровотока или абсцессами в головном мозге или печени.
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Микробиологические аспекты
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста. Так что без клинической картины острого фарингита не надо хвататься за антибиотики, как собственно и что-то сеять вне обострений.
100% штаммов чувствительны к пенициллинам, при этом Резистентность к макролидам в Европе – от 2 до 32%, в США – 7%. У нас в связи с великой любовью к этой группе, особенно среди педиатров, скорее всего, как в Европе. То есть о макролидах в этой ситуации надо забыть, к тому же тем же азитромицином не получится создать необходимую экспозицию в связи с ограничениями по срокам применения.
Клинические аспекты
При всем вышеперечисленном БГСА – зверь страшный, и основная проблема в том, что страх к нему мы почти потеряли. Лирическое отступление on. Именно этот зверь был постоянной причиной хирургических инфекций и родильной горячки (послеродового сепсиса) в доантибиотиковую эру. А женщины, как вы помните, умирали от нее, как мухи, пока Земмельвейс не заставил врачей мыть руки (за что закончил в психушке), но они их хотя бы на руках таскать перестали. Но даже сейчас, не дай бог, хирургу со стрептококковой ангиной подойти к операционному столу, и к концу первых суток стрептококк организует очень больную и страшно воняющую проблему в конкретной послеоперационной ране. Лирическое отступление off.
Потому напомним, что S.pyogenes может вызывать следующие заболевания:
- Фарингиты
- Поражения кожи и мягких тканей – целлюлиты, эризипелоид, лимфангит, рожа
- Некротические миозиты и фасцииты
- Послеродовый сепсис
- Пневмонии
- Сепсис
- Бактериальные эндокардиты (раньше редко, все же ангины и скарлатины старая школа требовала лечить строго 14 дней и ампициллином в задницу: сейчас стали встречаться почаще – привет коротким курсам антибиотиков при лечении ангин)
- Действие токсинов запускают синдром токсического шока и скарлатину
- Аутоиммунное воздействие приводит к ревматическим лихорадкам, с последующими возможным формированием пороков сердца и острому гломерулонефриту
- Послеоперационные раневые инфекции первых суток
Практические вопросы диагностики:
Микробиологическая диагностика S.pyogenes не представляет никакого труда, здесь в прямом смысле достаточно покрасить мазок по Граму. Все упирается в организационные аспекты – пока мазок доберется до лаборатории, пока покрасят. Пока ответят, пациент успеет много раз осложнится, если это стрептококк, или выздороветь, если это был фарингит и вызвавший его вирус (все-таки до 60% фарингитов вызваны вирусами, а не бактериальной флорой). Не хотелось бы останавливаться подробно на каждом перечисленном заболевании, но не упомянуть о диагностике острого фарингита, которая чаще всего и запускает множество вторичных осложнений, мы не можем. Для облегчения диагностики острого существуют несколько диагностических шкал. Автору более всего симпатична шкала Мак-Айзека в виду максимальной простоты ее использования.
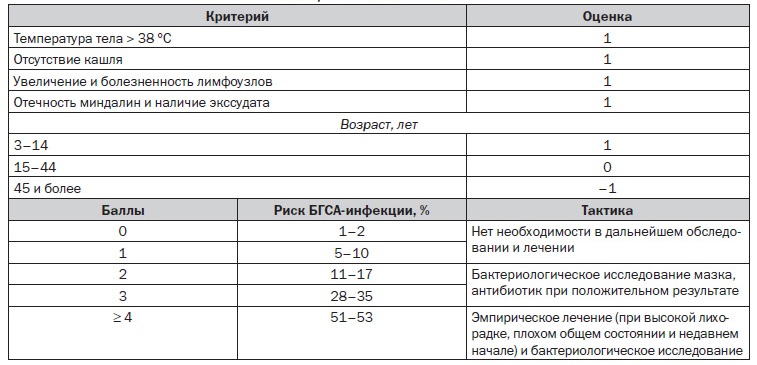
Но самым быстрым тестом для точной диагностики на месте является стрептатест, который в течение пяти минут дает ответ о вероятности наличия БГСА у больного с острым фарингитом.
Аспекты медикаментозного лечения
- Итак, мы определили, что имеем дело с БГСА, и тогда препаратами выбора в амбулаторной практике будут являться аминопенициллины, так как их много, они доступны, и главное, к ним 100% чувствительность у возбудителя.
Если ангина произошла впервые в жизни – лечим 10 дней. Если имеем дело с постоянными рецидивами – 14 дней, так как зверь может уйти во внутриклеточное состояние, оттуда руля процессом, и, чтобы до него добраться, доза должна быть выше средней, а курс лечения соответствующим.
Когда БГСА может уйти внутрь клетки? На тех самых пресловутых 5-7 днях, когда налеты с миндалин только сошли, температура только-только нормализовалась, а антибиотик взяли и отменили. И хорошо, если после подобного произойдет только рецидивирование фарингита, а не начнутся такие осложнения, как ревматизм, гломерулонефриты и далее по списку.
- Если пациент оказался в стационаре и ему обеспечен венозный доступ, то могут использоваться и пенициллины, и ампициллин в разных его вариациях. Главное – правильная доза, правильная кратность и ПРАВИЛЬНАЯ ДЛИТЕЛЬНОСТЬ КУРСА. Идеальный вариант из серии "дешево и сердито". Но обязательно должна быть доказанная микробиология.
При непереносимости пенициллинов помним о клиндамицине как об их адекватной замене.
- Пиогенный стрептококк, как мы выше упомянули, является причиной ранней послеоперационной раневой инфекции. Напомним, что стандартная послеоперационная раневая инфекция развивается к седьмым суткам. А если это произошло в первые сутки, да к тому же страшно завоняло (пиогенный стрептококк недаром называют мясоедным), немедленно делаем мазок, бежим с ним в лабораторию (можно даже своими ногами – это же ваш пациент осложнился, там так же бегом делают мазок по Граму, обнаруживают цепочки, и после этого начинаем лить аминопенициллин в вену, если не использовали его для периоперационной антибиотикопрофилактики (если использовали, то просто продолжаете дальше). Если совсем все бедно, можно пенициллин – 12 млн в сутки. Но если вы провели правильную периоперационную антибиотикопрофилактику, учли все риски и не забыли про свой личный стрептококк в горле, то риск ранней раневой минимален, а если профилактика продленная на 72 часа, то она и раскрутиться не успеет.
- При инфекциях кожи и мягких тканей, а также стрептококковом сепсисе препаратами выбора будут клиндамицин (который блокирует выработку токсических продуктов) в сочетании с пенициллином (24 млн ЕД в сутки) – это наиболее предпочтительная и малозатратная комбинация
Альтернативой в режиме монотерапии могут служить:
-
600 мг в/в каждые 6 часов 2,0 каждые шесть часов 2-3 г в/в каждые 6 часов или цефтриаксон по 2 г в сутки внутривенно в расчете 15 мг/кг в/в каждые 12 часов
Почему максимально важно соблюдать как дозировку, так и кратность введения читаем тут – /vracham/antibiotikoterapiya/polozheniya (часть 1 и часть 2).
В заключение хочется снова воскликнуть – пожалуйста, помните о пиогенном стрептококке и о правильной длительности его лечения.
Основным источником развития болезни служат патогенные микроорганизмы.

Причины заболевания
Причина бактериального простатита – поражение предстательной железы грамотрицательными микроорганизмами:
- chlamydia trachomatis – хламидии;
- streptococcus – стрептококки;
- staphylococcus aureus – стафилококк золотистый;
- klebsiella – клебсиеллы;
- pseudomonas aeruginosa – палочка синегнойная;
- enterobacter – энтеробактеры;
- trichomonas vaginalis – трихомонады;
- escherichia coli – кишечная палочка;
- neisseria gonorrhoeae – гонококки;
- proteus – протеи;
- enterococcus – энтерококки.
Такие микроорганизмы вызывают бактериальный простатит при наличии других предрасполагающих факторов. Хроническая форма заболевания обусловливается, как правило, полимикробностью.

Факторы, способствующие развитию простатита
Среди предрасполагающих обстоятельств отмечают следующие:
- регулярное переохлаждение организма;
- нерегулярность половой активности;
- заболевания, связанные с нарушениями иммунной системы;
- хронические патологии мочеполовой системы;
- малоподвижный образ жизни – отсутствие физических нагрузок, сидячая работа;
- травмы органов малого таза;
- другие хронические патологии ЖКТ, ЛОР органов и так далее.
Существует мнение специалистов, что риск развития симптомов бактериального простатита у мужчин повышается при факторах интоксикации. К ним относятся злоупотребление алкоголем, никотином, наркотическими веществами.
Разновидности болезни
Существует несколько типов классификации заболевания, в зависимости от симптомов, этиологии, характеру и длительности течения, рецидивов, других сопутствующих факторов.
При определении типа простатита бактериального у мужчин учитываются следующие параметры:
- причина – инфекция, бактерии;
- тип патогенного агента, вызвавшего воспаление;
- наличие застоя секрета и эякулята;
- фиброзные проявления;
- путь инфицирования;
- специфика течения – острая, хроническая, атипичная форма;
- фаза активности воспалительного процесса;
- стадия развития.
Чаще всего за основу классификации принимается алгоритм, предложенный американскими учеными из National Institutes of Health.
Наличие острого воспалительного процесса
Рецидивирующее течение заболевания
Синдром хронической тазовой боли
Наличие болевого синдрома на протяжении не менее 3 месяцев
Диагностика
Заболевание имеет характерную клиническую картину, поэтому постановка диагноза не представляет трудностей. Но уролог должен дифференцировать именно этот тип патологии от других, согласно классификации. Перед тем как лечить бактериальный простатит, проводится полное обследование, которое включает:
- опрос пациента;
- ректальное исследование простаты методом пальпации;
- общий клинический и бактериальный анализ мочи и крови;
- тест на ПЦР (полимеразную цепную реакцию) для выявления ДНК возбудителя и определения стадии заболевания;
- забор и посев секрета уретры для выявления тяжести воспаления и изучения внутренней флоры.
Могут потребоваться и дополнительные методики обследования:
- ПСА – тест на простат-специфический антиген с целью выявления онкологических процессов в предстательной железе;
- ТРУЗИ – трансабдоминальное УЗИ;
- спермограмма – при подозрении развития бесплодия;
- уродинамика – для определения источника нарушения процесса мочеиспускания.
Важную роль играют признаки бактериального простатита. Именно клиническая картина является для уролога основным фактором постановки диагноза и определения лечения.

Симптомы
Проявления острой и хронической формы заболевания могут отличаться. Во втором случае признаки выражены менее ярко или отсутствуют. При остром течении симптомы бактериального простатита:
- болевой синдром в области крестца и промежности;
- боль при мочеиспускании и опорожнении кишечника;
- учащенное мочеиспускание (особенно по ночам);
- выделения из уретры;
- жжение в области уретры.
В тканях простаты отсутствуют болевые рецепторы. Причиной развития дискомфорта становится вовлечение органов малого таза и нервных путей в воспалительный процесс. Боль может быть разной интенсивности – от ноющей до острой. Могут иррадиировать в мошонку, поясничную область.
Частые позывы к мочеиспусканию связаны с появлением отечности и увеличением объема простаты. Поскольку сужается просвет мочеточника, возникает чувство неполного опорожнения мочевого пузыря. Постепенно признаки дизурии могут ослабевать, но при декомпенсации возвращаются вновь.
На начальной стадии патологии наблюдается проблема с потенцией различного характера:
- ослабевание эрекции или учащение во время сна;
- стертый оргазм;
- болезненность при семяизвержении.
Незамедлительное лечение бактериального простатита требуется еще и по причине нарушений психического состояния пациента. Мужчины страдают от бессонницы, депрессий, раздражительности. Угроза импотенции, которая является осложнением заболевания, становится поводом для проблем с эмоционально-психическим фоном.

Антибиотики
Лечение бактериального простатита у мужчин основывается на комплексных схемах. Антибиотики – основная группа препаратов, входящая в программу терапии. Антибактериальные лекарственные средства подбираются с учетом чувствительности инфекционного агента. Препараты широкого спектра действия хорошо проникают в ткани простаты. К ним относятся:
- Фторхинолоновая группа – обладают выраженной противомикробной активностью, нарушают синтез ДНК бактерий, что приводит к их гибели. Существует 4 поколения препаратов. Чаще всего назначают Офлоксацин, Ципрофлоксацин и другие.
- Тетрациклины – активны в отношении грамположительных патогенов. Тетрациклин, Доксициклин.
- Группа макролидов – считаются наименее токсичными антибиотиками. Оказывают бактериостатическое действие, сохраняют высокую концентрацию в тканях. К ним относятся: Лейкомицин, Азитромицин и другие.
Кроме антибиотиков пациентам, страдающим от хронической формы патологии, назначают препараты:
- альфа-адреноблокаторы – нормализуют кровоток и лимфоток, снимают тонус сосудов;
- противоотечные – Омник и другие;
- обезболивающие;
- нестероидные противовоспалительные средства;
- для поддержания иммунитета – комплекс витаминов и иммуномодуляторы.
В комплекс лечения входит физиотерапия, часто используется массаж простаты для улучшения дренажа предстательной железы. Хороший результат показывает лазерная терапия.
Сколько лечить бактериальный простатит? Заболевание довольно сложное, требует длительного курса терапии – приема антибиотиков на протяжении 4 – 8 недель. После этого понадобится восстанавливающий период.
Питание
Этот фактор также играет большую роль, правильный рацион поможет быстрее восстановиться после болезни и снизить риск рецидивов. Питание рекомендуется подбирать, согласно следующим принципам:
- продукты с содержанием всех необходимых организму микроэлементов;
- пища должна хорошо усваиваться, не быть тяжелой;
- продукты с высоким содержанием клетчатки стимулируют процесс пищеварения и не допускают дисфункций кишечника;
- контроль питьевого режима поможет предотвратить обезвоживание.
Основная задача при составлении рациона – нормализовать работу кишечника, так как запоры являются одной из причин обострений простатита.

Диета
Существует перечень разрешенных и запрещенных продуктов. Строгую диету необходимо соблюдать при острой форме заболевания, но и впоследствии стоит придерживаться правильного рациона. В пищу можно употреблять:
- каши;
- отварное нежирное мясо, рыбу;
- морепродукты;
- овощи и фрукты;
- зелень;
- кисломолочные продукты.
Острые, копченые, жирные блюда – под запретом. Также важно отказаться от употребления алкоголя и ограничить курение.
Лишний вес – фактор, провоцирующий рецидивы бактериального простатита. Не обязательно постоянно держать строгую диету. Просто нужно выбрать для себя вариант питания с оптимальным балансом углеводов, белков и жиров.

Возможные осложнения
Один из главных вопросов урологу – можно ли вылечить бактериальный простатит? Если начать терапию своевременно и строго выполнять все рекомендации врача, добиться длительной ремиссии и даже полного излечения вполне возможно.
Но далеко не всегда пациенты обращаются к специалисту вовремя. Причиной может быть банальный стыд или отсутствие симптомов. При длительном развитии заболевания возникают осложнения:
- увеличение отека;
- абсцесс простаты;
- патологии яичек и придатков – везикулит, орхит;
- заболевания почек и мочевыводящих путей;
- гиперплазия простаты;
- онкология;
- бесплодие.
Распространение инфекции приводит к более серьезным проблемам и усугублению патологии.
Профилактика
При наличии симптомов бактериального простатита у мужчин лечение будет тем эффективнее, чем раньше пациент обратится к врачу. Но можно предпринять меры, чтобы не допустить патологии:
- не переохлаждаться;
- соблюдать правила личной гигиены;
- помнить о безопасном сексе;
- избегать сомнительных и беспорядочных интимных связей;
- полноценно питаться;
- не забывать о физической нагрузке;
- не допускать длительного сексуального воздержания;
- контролировать работу кишечника.
Другие статьи:

Удаление излишней растительности на лице может проводиться разными способами. Но наиболее высокий и пролонгированный результат дает лазерная эпиляция верхней губы. Такой метод избавления от усиков безопасный и практически безболезненный. Кроме того, лазер оказывает благоприятное воздействие на кожу в целом. Методика способствует оздоровлению, омоложению кожного покрова и моментальной регенерации тканей.

Существуют разные косметологические методики, позволяющие улучшить состояние кожи, избавиться от дефектов, восстановить здоровый цвет и сияние. Одна из техник – кислотный пилинг, помогает перезапустить метаболические процессы дермы на клеточном уровне. Методика дает пролонгированный эффект, способствует ускоренной регенерации тканей.

Один из альтернативных медицинских методов лечения – гирудотерапия или дозированное кровопускание с помощью пиявок. Для этого используется специально выведенный вид кольчатых червей из класса поясковых (Clitellata). Методика имеет свои плюсы и минусы, перечень противопоказаний, показывает высокую эффективность при терапии различных заболеваний.
Что такое анальная трещина? Причины возникновения, диагностику и методы лечения разберем в статье доктора Богданова Дениса Валерьевича, проктолога со стажем в 21 год.
Над статьей доктора Богданова Дениса Валерьевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Анальная трещина — рана, дефект слизистой, возникающий на стыке анодермы (эпителия анального канала) и слизистой оболочки прямой кишки. Форма дефекта чаще линейная, встречаются эллиптические раны и раны треугольной формы. Возникшая впервые острая трещина приносит весьма болезненные ощущения больному, в основном во время дефекации. [1] [2] Заболевание носит социальную значимость, занимая 3-е место среди проктологических нозологий и возникая чаще у лиц молодого, трудоспособного возраста.
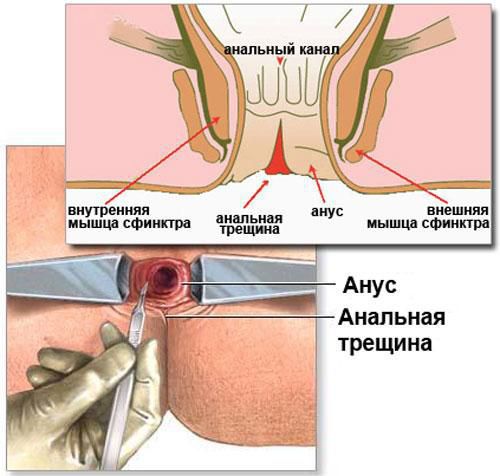
Причины образования раневого дефекта, фиссуры — травмы слизистой прямой кишки или анодермы (от твердого кала, как следствие запоров; при повышении внутрибрюшного давления, беременности, родах, поднятии тяжестей; после анального секса, применения секс-пособий; после медицинских процедур — например, клизм; в результате хронических воспалительных заболеваний ЖКТ, дисбиоза толстого кишечника; при злоупотреблении алкоголем, длительной диарее и пр.)
Дефект может заживать спонтанно или под воздействием фармакологических препаратов — так и случается в 90% случаев острых трещин. Оставшаяся часть рискует попасть в число пациентов с хронической анальной трещиной (ХАТ).
Переход острой формы заболевания в хроническую происходит под действием ряда факторов:
- стойкий спазм внутреннего сфинктера анального канала (ВнАС). Сфинктерометрия в ряде исследований показала наличие спазма всех волокон внутреннего сфинктера у 87% испытуемых и дистальной порции у оставшихся 13% — то есть все обследуемые имели спазм ВнАС; [3]
- регулярное нарушение консистенции каловых масс (плотный стул приводит к дополнительному травмированию стенок кишки, мешающему процессам регенерации);
- отсутствие своевременного и адекватного лечения.
Период, определяющий хронизацию трещины, — обычно 1,5-2 месяца. Существующий в анодерме более 8 недель дефект диагностируется как хроническая анальная трещина. Длительность патологического процесса определяет последующий выбор терапии.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы анальной трещины
При острых трещинах:
Общие кровопотери при острой патологии незначительны и не приводят к анемизации больного. Самые значимые для пациентов проявления — это резкая болезненность во время стула. Если отмечаются обильные кровотечения, это может свидетельствовать о сопутствующем геморрое.
При хронических трещинах:
- Болевые ощущения несколько отличаются от таковых при острой патологии. Длительность болей может быть до нескольких часов. Интенсивность их, как правило, сильнее. Боли описываются пациентами, как жгуче-режущие. Боли могут отсутствовать при дефекации и начинаться спустя 20-40 минут после нее.
- Выделения крови незначительные. В большинстве случаев могут вовсе отсутствовать.
- Сфинктероспазм. Проявляется затруднением при отхождении кала.
Триада перечисленных симптомов, особенно боли и сфинктероспазм, может послужить причиной появления боязни дефекации, усугубляя нарушения стула и препятствуя тем самым адекватному заживлению хронических анальных трещин. Хроническое воспаление в зоне дефекта анодермы приводит к деструкции эластических волокон в анодерме, отчего последняя теряет свою пластичность, в ней изменяется течение процессов регенерации.
- Еще один симптом, встречающийся в небольшом проценте случаев — зуд в области раны.
Многие исследования [4] [5] указывают на наличие сопутствующего хронического воспалительного процесса в аноректальной области при трещинах. Криптиты, проктиты, папиллиты осложняют течение заболевания. Последовательность появления болезней — образовалась ли сначала трещина, или первичными были хронические воспалительные процессы в кишечнике — при сочетании данных нозологий ответ на вопрос бывает строго индивидуальным, терапия же подобных сочетанных патологий практически не различается.
Патогенез анальной трещины
В большинстве случаев образование острой трещины является следствием травмы анодермы или слизистой прямой кишки. Травмирующим агентом чаще всего бывают плотные каловые массы. Запоры, будь то алиментарные, атонические, рефлекторные или неврогенные, приводят к поверхностному повреждению целостности анального канала.
Второй ключевой момент в формировании трещины, особенно хронической анальной трещины — стойкий спазм внутреннего анального сфинктера (ВнАС). Если наружный сфинктер, который состоит из волокон поперечно-полосатой мускулатуры, является произвольно регулируемым, то внутренний сфинктер, в составе которого присутствуют гладкомышечные клетки, регулируется непроизвольно. Базальный тонус ВнАС большую часть времени контролируется симпатической частью нервной системы, и поэтому сфинктер практически все время находится в состоянии максимального сокращения (это обеспечивает до 85% базального тонуса, остальную часть запирательной функции ВнАС дополняют геморроидальные узлы). При измерении величина назального тонуса АС составляет 90-100 мм.рт.ст, что практически равняется значениям давления в ветвях нижней прямокишечной артерии.
Механизмы, регулирующие тонус ВнАС:
- Автономные постганглионарные нервные парасимпатичекие и симпатические волокна;
- Нервные сплетения (Ауэрбаховский и Мейснеровский) в стенке толстой кишки. Эти образования контролируют и перистальтику, и локальные рефлексы, в том числе ингибиторный рефлекс, расслабляющий ВнАС. Сплетения относятся к норадренергическим, и оксид азота, являясь медиатором в синапсах данных волокон, приводит к релаксации ВнАС;
- Уровень внеклеточного Ca, транспортирующегося через каналы L-типа.
Считается, что возникновение первичного дефекта слизистой не приводит к физиологически быстрому заживлению у ряда больных из-за особенностей строения ЖКТ — малой величины аноректального угла, снижения перфузии крови в области передней и особенно задней комиссуры и недостаточности ректального ингибиторного рефлекса (РАИР). В инструментальных исследованиях выявлены частые случаи (до 85%) недоразвития конечных ветвей внутренней срамной и нижней прямокишечной артерий, питающих эндотелий и подлежащие ткани в области ишиоректальной ямки. Исследования, позволившие установить данный факт: постмортальная ангиография и допплеровская флоуметрия у здоровых лиц. [6]
Подробные исследования микробной флоры лиц, страдающих анальными трещинами, подтвердили факты нарушения симбионтного равновесия в микрофлоре дистальных отделов толстого кишечника (в т.ч. резкое снижение или исчезновение в ее составе лакто и бифидобактерий), увеличение персистентного потенциала патогенных микроорганизмов (увеличение их антилизоцимной активности). [7]
Дополнительное патологическое влияние имеет повышенный уровень провоспалительных цитокинов, антител к эндотелию, и снижение выработки оксида азота.
Все перечисленные факторы в различной степени выраженности способствуют нарушениям процессов регенерации и хронизации анальных трещин.
Классификация и стадии развития анальной трещины
Классифицируют трещины заднего прохода по длительности патологического процесса [1]:
Острыми трещинами считаются дефекты слизистой, анодермы, возникшие 4-8 недель назад, без наличия рубцовых, соединительнотканных разрастаний в области дна и краев раны.
По расположению раневого дефекта чаще встречаются задние трещины, реже передние или множественные трещины. Характерно их расположение вдоль срединной линии.
Передние трещины обычно диагностируются у женщин, ввиду особенностей анатомического строения (ригидность, малоподвижность передней стенки обусловлена прикреплением к ней ректовагинальной перегородки).
Расположение фиссур по боковым стенкам анального канала встречается не часто.
Осложнения анальной трещины
Осложнения — прямое следствие хронических воспалительных процессов в перианальной области.
Пектеноз. Пектеноз — рубцовое изменения стенок анального канала, приводящее к стойкому его сужению. Хронические воспалительные процессы при трещинах заднего прохода неизменно приводят к развитию фиброзных изменений в тканях, когда нормальные мышечные и эластические волокна в области поверхностного эпителиального дефекта замещаются соединительными тканями. Иногда такие процессы носят достаточно обширную локализацию и фиброзное замещение происходит на протяжении всей окружности сфинктера (особенно при множественных трещинах). Развивающиеся рубцовые изменения приводят к необратимому стенозированию (сужению) анального канала. Подобное состояние требует сложной восстановительной операции с радикальным иссечением фиброзной ткани.
Диагностика анальной трещины
При проведении диагностического обследования простую трещину заднего канала дифференцируют с полипом анального канала, раком слизистой дистального отдела прямой кишки и анодермы, туберкулезной и сифилитической язвами (твердый шанкр при первичном сифилитическом комплексе). Кроме того, следует провести тщательное исследование слизистой прямой кишки для исключения трещины, сопутствующей неспецифическому язвенному колиту или болезни Крона. Последние нозологии особенно вероятны при множественных трещинах, при отсутствии спазма сфинктера.
После опроса больного проводится осмотр аноректальной области, пальцевое исследование и аноскопия. Ректороманоскопия необходима для изучения состояния слизистой прямой кишки, с целью исключения патологических процессов в толстом кишечнике (болезни Крона, неспецифического язвенного колита, злокачественных новообразований и пр.).
При выраженном спазме сфинктера, сильном болевом синдроме зачастую полноценно провести визуализацию, диагностику хронической трещины не представляется возможным. Также трудности возникают при наличии лишнего веса у пациента, когда анальная воронка относительно глубокая и осмотреть анальный канал полностью не представляется возможным. В подобных случаях можно применить блокаду с анестетиками.
Лечение анальной трещины
Острые фиссуры заднего прохода показаны к консервативной терапии.
1. Патогенетически обоснованным и обязательным компонентом в комплексном лечении является нормализация стула, профилактика запоров. Мягкий стул исключит дополнительную травматизацию раневой поверхности.
2.Нормальное течение репаративного процесса обеспечат меры по снижению сфинктероспазма: применение 0,4% нитроглицериновой мази [3] 2 р/д или другого донатора оксида азота — 1% мази изосорбита динитрата 3 р/д с длительностью лечения в 8 недель. Побочные эффекты препаратов нитроглицеринового ряда (головные боли, тахикардия, ортостатическая гипотензия, тахикардия) побуждают досрочно прекратить лечение в 20% случаев.
Адекватную замену выбирают среди нифедипиновой мази (2% гель-дилтиазем) или инъекций ботулотоксинами (БТ). Последние переносятся больными сравнительно хорошо, имеют стойкий эффект даже после 1 инъекции — до 2-3 месяцев. Дозировку подбирают индивидуально, исходя из массы пациента и способа введения. Из немногих отрицательных эффектов можно назвать временное развитие несостоятельности анального сфинктера, инконтиненции.
Если отсутствует эффект от консервативного лечения, есть признаки хронизации трещины, возникают осложнения (пектеноз, свищ) — это показания к хирургическому лечению.
Хронические трещины
В отдельных случаях лечение начинают с медикаментозных средств, описанных в вышеизложенном разделе. Основным методом лечения все же является хирургическое лечение. При показаниях к оперативному лечению операцией выбора становится иссечение трещины с дозированной боковой сфинктеротомией ВнАС [10]. Обоснованным объемом рассечения называют длину разреза, соответствующую протяженности самой трещины, и избежание рассечения мышечных волокон выше зубчатой линии (для профилактики инконтиненции). В послеоперационном периоде для дополнительного сфинктеродилатирующего эффекта применяют нитроглицериновые мази. Имеются достоверные данные о положительном эффекте применения топического метронидазола после фиссуротомии. [9]
Топическая антибактериальная терапия в большинстве случаев значительно сокращает длительность болевого синдрома (до 5 дней вместо стандартных 28) [7] и снижает клинические и объективные проявления неспецифического проктита значительно раньше, чем у пациентов без применения антибиотикотерапии.
Прогноз. Профилактика
Логичными мерами в отношении предупреждения появления фиссур заднего прохода является устранение причин, способствующих их появлению:
- Коррекция питания, лечение запоров и нормализация стула. Употребление достаточного количества балластных веществ: пищевых волокон, клетчатки. Максимальное исключение из рациона рафинированных продуктов, высокоуглеводистой пищи (изделий из сдобного теста, хлеба высшего сорта, кондитерских изделий и т. п.). Включение в меню большого количества овощей, кисломолочных продуктов.
- Если алиментарная коррекция не приводит к нормализации стула, применяют фармпрепараты (осмотические и контактные слабительные).
- Исключение прочих факторов, приводящих к травматизации слизистой прямой кишки.
- Лечение хронических заболеваний ЖКТ.
- Устранение дисбиоза кишечника. [11]
При своевременном лечении и полноценной профилактике прогноз заболевания благоприятный, в большинстве случаев отмечается полное излечение.
Читайте также:

