Стрептококки в кишечнике лечение дисбактериоза
Обновлено: 17.04.2024
Изучение микрофлоры кишечника началось в 1886 г., когда F. Escherich описал кишечную палочку (Bacterium coli communae). В 1908 году Нобелевский лауреат русский ученый Илья Ильич Мечников доказал необходимость кишечных бактерий для здоровья и долголетия. К
Изучение микрофлоры кишечника началось в 1886 г., когда F. Escherich описал кишечную палочку (Bacterium coli communae). В 1908 году Нобелевский лауреат русский ученый Илья Ильич Мечников доказал необходимость кишечных бактерий для здоровья и долголетия. К настоящему времени в кишечнике здорового человека установлено наличие 500 видов микробов. Нормальная микробная флора является одним из барьеров на пути бактерий, попадающих в кишечник. Она стимулирует иммунную защиту, увеличивает секрецию IgA в просвет кишки. Кишечные палочки, энтерококки, бифидобактерии, ацидофильные палочки обладают антагонистическими свойствами и способны подавлять рост патогенных микроорганизмов. Нарушение состава микрофлоры приводит к снижению сопротивляемости организма кишечным инфекциям.
Различают мукоидную микрофлору (М-микрофлора) — микроорганизмы, ассоциированные со слизистой оболочкой кишечника, и полостную микрофлору (П-микрофлору) — микроорганизмы, локализующиеся в просвете кишечника.
По отношению к макроорганизму представителей кишечного биоценоза делят на 4 группы:
облигатная микрофлора (основная микрофлора кишечника — бифидобактерии, лактобациллы, нормальные кишечные палочки, пропионобактерии, пептострептококки, энтерококки);
факультативная (условно-патогенные и сапрофитные микроорганизмы — бактероиды, стафилококки, стрептококки, пептококки, дрожжеподобные грибы, вейонеллы, фузобактерии, бациллы);
транзиторная (случайные микроорганизмы, не способные к длительному пребыванию в организме, — флавобактерии, псевдомонады);
При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями, улучшая трофику слизистой оболочки. Недостаточное количество клетчатки в диете ведет к снижению синтеза короткоцепочечных жирных кислот. В результате возникают дистрофические изменения эпителия и повышается проницаемость кишечного барьера для антигенов пищевого и микробного происхождения.
Под влиянием микробных ферментов в подвздошной кишке происходит деконъюгация желчных кислот (ЖК) и преобразование первичных ЖК во вторичные ЖК. В физиологических условиях 80–95% ЖК реабсорбируется, остальные выделяются с калом в виде метаболитов. Последние способствуют формированию каловых масс, тормозят всасывание воды, препятствуя излишней дегидратации кала. Избыточное бактериальное обсеменение тонкой кишки ведет к преждевременной деконъюгации ЖК и секреторной диарее.
Таким образом, морфологическое и функциональное состояние кишечника зависит от состава его микрофлоры.
В тощей кишке здоровых людей находится до 100 000 бактерий в 1 мл содержимого. Основную часть их составляют стрептококки, стафилококки, молочнокислые палочки. В дистальном отделе подвздошной кишки количество микробов увеличивается за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий.
Микробный состав кала не отражает полную картину кишечного биоценоза, не дает оперативной информации о составе микроорганизмов в кишечнике. На практике учитываются данные лишь о 15–20 видах микробов, содержащихся в кале. Обычно исследуют количество бифидобактерий, лактобацилл, энтеробактерий, кишечных палочек, протея, энтерококка, золотистого стафилококка, синегнойной палочки и кандид.
Степень тяжести дисбиоза определяется степенью снижения бифидобактерий и других облигатных микроорганизмов и повышения числа условно-патогенных и патогенных видов.
I степень — снижение количества облигатных представителей (бифидобактерий и/или лактобацилл) на 1–2 порядка, без увеличения условно-патогенной микрофлоры (УПМ), нарастание количества УПМ при нормальном числе бифидобактерий. II степень — умеренное или значительное снижение числа бифидобактерий, сочетающееся с выраженными изменениями аэробной микрофлоры (редукция лактобацилл, появление измененных форм кишечной палочки, УПМ в высоких количествах). III степень — большое количество УПМ как одного вида, так и в ассоциациях, выделение патогенных микроорганизмов (Мехтиев С. Н., Гриневич В. Б., Захаренко С. М.).
В клинике дисбиоза выделяют следующие ключевые синдромы:
интестинальный синдром (вздутие живота, урчание кишечника, склонность к запорам или жидкий стул с непереваренными остатками пищи);
вторичный синдром мальабсорбции (упорная диарея с нарушением всасывания моносахаридов, электролитов),
Новые подходы в диагностике дисбиоза
Альтернативу рутинным бактериологическим исследованиям составляют химические методы дифференциации микроорганизмов и, в частности, газовая хроматография (ГХ) в сочетании с масс-спектрометрией (ГХ-МС). Метод основан на определении компонентов бактериальных клеток, появляющихся в результате их естественного отмирания или атаки иммунной системы. В качестве маркеров используют минорные липидные компоненты мембран микробов. По их содержанию можно в течение нескольких часов определить до 170 видов бактерий и грибов в различных биосредах.
Почти 50% биомассы пристеночной микрофлоры составляют актиномицеты, занимающие промежуточное положение между бактериями и грибами. Около 25% микробной флоры представлено аэробными кокками (стафилококки, стрептококки, энтерококки и коринеформные бактерии). Число бифидо- и лактобацилл колеблется от 20 до 30%. Другие анаэробы (пептострептококки, бактероиды, клостридии, пропионобактерии) составляют около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной численности микрофлоры слизистой оболочки.
До 90–95% микробов толстой кишки составляют анаэробы (бифидобактерии и бактероиды) и только 5–10% всех бактерий — строгая аэробная и факультативная флора (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Свойства микробов, населяющих кишечник, не всегда учитываются при назначении антибиотиков. Антибактериальные препараты подавляют рост не только патогенных микроорганизмов, но и нормальную микрофлору. В результате размножаются сапрофитные микробы с высокой устойчивостью к лекарственным препаратам, приобретающие патогенные свойства.
Диарея, ассоциированная с применением антибиотиков
У больных, получающих антибактериальную терапию, может развиваться диарея, вызванная дисбиозом кишечника (ААД — антибиотик-ассоциированная диарея). Частота такой диареи колеблется в пределах 5–25%. Причиной ее является снижение количества микробов, чувствительных к антибиотику, и появление резистентных штаммов, отсутствующих в норме. Наиболее известным представителем таких микроорганизмов является патогенный штамм Clostridium difficile (Cl. difficile), но причиной диареи, ассоциированной с антибиотиками, могут быть и другие микробы, способные усиливать секрецию ионов и воды, повреждать стенку кишки. Это стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка, клебсиелла. По типу диареи ААД обычно относят к секреторному и воспалительному типам.
Антибиотик-ассоциированную диарею наиболее часто вызывают линкомицин, ампициллин, клиндамицин, бензилпенициллин, цефалоспорины, тетрациклины, эритромицин. Способ введения антибиотика не имеет большого значения. При приеме внутрь помимо эрадикации микроорганизмов происходит воздействие антибиотика на слизистую оболочку тонкой кишки. При парентеральном введении антибиотики воздействуют на биоценоз кишечника, выделяясь со слюной, желчью, секретами тонкой и толстой кишок.
Симптомы ААД у большинства больных обычно появляются во время лечения, а у 30% — в пределах 7–10 дней после его прекращения.
Этиологическим фактором ААД большинство исследователей считают клостридии, в частности Cl. difficile. Среди взрослого населения уровень ее носительства низкий и равен 2–3%. Условиями размножения Cl. difficile являются анаэробная среда и угнетение нормальной микрофлоры кишечника.
Клинические проявления ААД варьируют от легкой диареи до тяжелого псевдомембранозного колита (ПМК). ПМК — острое заболевание кишечника, являющееся осложнением антибактериальной терапии. Установлено, что его вызывает Cl. difficile.
Симптоматика
Основным симптомом ААД является обильная водянистая диарея, началу которой предшествует назначение антибиотиков в течение нескольких дней и более. Затем появляются схваткообразные боли в животе, стихающие после стула. В случаях, когда возникает лихорадка, в крови нарастает лейкоцитоз, а в кале появляются лейкоциты, нужно заподозрить ПМК.
После отмены антибиотика у ряда больных симптомы быстро исчезают. При ПМК, несмотря на прекращение антибиотикотерапии, в большинстве случаев частота стула растет, появляются дегидратация и гипопротеинемия. В тяжелых случаях быстро наступает обезвоживание, развиваются токсическое расширение и перфорация толстой кишки, возможен летальный исход.
Диагноз
Диагноз ААД устанавливают на основании связи диареи с применением антибиотиков. Диагноз ПМК подтверждается бактериологическим исследованием кала и определением в нем токсина Cl. difficile. Частота обнаружения токсина в кале больных с ААД не превышает 15%.
У больных диареей, ассоциированной с Cl. difficile, наблюдается значительный лейкоцитоз. Имеются данные, что у больных с лейкоцитозом 15800 и выше высока вероятность развития ПМК, вызванного Cl. difficile. Это объясняется тем, что токсин А, выделяемый Cl. difficile, вызывает воспаление, секрецию жидкости, лихорадку и судороги. Поэтому у всех больных с ААД, протекающей с интоксикацией и лейкоцитозом 15800 и выше, следует считать причиной диареи Cl. difficile.
Парфенов А. И., Осипов Г. А., Богомолов П. О применили метод ГХ-МС для оценки состава микробной флоры тонкой кишки у 30 больных ААД и установили, что диарея может быть связана не только с инфекционным агентом (Cl. difficile), но с существенным изменением нормальной микрофлоры в сторону увеличения численности от 7 до 30 из 50 контролируемых микроорганизмов. При этом общая колонизация тонкой кишки увеличивается в 2–5 раз по сравнению с нормой.
У больных ААД чаще всего морфологические изменения толстой кишки отсутствуют. В тяжелых случаях при эндоскопии выявляют 3 типа изменений: 1) катаральное воспаление (отек и гиперемия) слизистой оболочки; 2) эрозивно-геморрагическое поражение; 3) псевдомембранозное поражение.
Дифференциальный диагноз
Связь диареи с антибиотикотерапией обычно не создает трудностей в диагностике ААД. В тяжелых случаях картина ПМК может напоминать холеру или фульминантную форму язвенного колита, болезнь Крона. Однако для последних характерна более или менее выраженная кровавая диарея, нехарактерная для ПМК. Тем не менее возможность развития эрозивно-геморрагических изменений слизистой оболочки при ААД не исключает появления кровянистых выделений из прямой кишки у некоторых больных.
Лечение ААД
Этиотропной терапией ААД и ПМК, вызванных Cl. difficile, большинство авторов считает назначение ванкомицина и метронидазола (трихопола, метрогила).
Немедленно отменяют антибиотик, вызвавший диарею. Назначают ванкомицин в начальной дозе 125 мг внутрь 4 раза в сутки, при необходимости дозу увеличивают до 500 мг 4 раза в сутки. Лечение продолжают в течение 7–10 сут. Метронидазол дают по 0,5 г внутрь 2 раза в сутки (или по 0,25 г 4 раза в сутки).
Применяют также бацитрацин по 25 тыс. ME внутрь 4 раза в сутки. Лечение проводят в течение 7–10 сут. Бацитрацин почти не всасывается, в связи с чем в толстой кишке создается высокая концентрация препарата. При обезвоживании применяют инфузионную терапию и оральную регидратацию (Регидрон, Цитроглюкосолан). Для связывания токсина А назначают Холестирамин.
Поскольку количество микробов, обеспечивающих лечебный эффект, на несколько порядков превышает дозы обычных бакпрепаратов, обсуждается вопрос о локальной доставке пробиотиков в кишечник. Это можно делать с помощью клизм на основе солевых растворов, через назодуоденальный зонд или колоноскоп. Привлекает внимание последний способ, т. к. как при этом пробиотики вводятся непосредственно в проксимальный отдел ободочной кишки.
Линекс содержит молочнокислые бактерии, резистентные к действию антибиотиков. Взрослым и детям старше 12 лет назначают по 2 капсулы 3 раза/сут после еды, запивая небольшим количеством жидкости. Длительность лечения составляет в среднем 1–2 мес. При применении препарата в рекомендуемых дозах побочное действие не отмечено. Противопоказания — повышенная чувствительность к компонентам препарата или молочным продуктам. Проведенные исследования не выявили наличия у Линекса тератогенного действия, не сообщалось об отрицательном влиянии препарата при беременности и в период лактации. Для сохранения жизнеспособности компонентов препарата не рекомендуется запивать Линекс горячими напитками, следует воздерживаться от употребления алкоголя.
Клинические проявления аллергии на молочнокислые бактерии сходны с проявлениями аллергии на молочные продукты, поэтому при появлении симптомов аллергии прием препарата следует прекратить для выяснения ее причин. О случаях передозировки Линекса не сообщалось. Не отмечено его нежелательного взаимодействия с другими препаратами. Состав препарата Линекс позволяет принимать его одновременно с антибактериальными средствами.
Для симптоматического лечения диареи применяются также: адсорбент аттапульгит, по 1,2–1,5 г после каждого жидкого стула; лоперамид, 2–4 мг внутрь после каждой дефекации (не более 8 мг/сут); дифеноксилат/атропин (Ломотил), 5 мг внутрь 4 раза в сутки до прекращения поноса; настойка белладонны, 5–10 капель внутрь 3 раза в сутки перед едой; гиосциамин (Левсин) 0,125 мг под язык по мере необходимости или по 0,375 мг внутрь 2 раза в сутки; спазмолитик дицикловерин, 20 мг внутрь 4 раза в сутки; кодеин, 30 мг внутрь 2–4 раза в сутки; октреотид (100–600 мг/сут п/к в 2–4 приема) — синтетический аналог соматостатина; энтеросорбенты (Смекта, Эспумизан).
Лечение собственно дисбиоза
Стандартная терапия дисбиоза нацелена на устранение избыточного бактериального обсеменения тонкой кишки, восстановление нормальной микрофлоры, улучшение кишечного пищеварения и всасывания, восстановление моторики кишечника и повышение иммунореактивности организма.
Антибактериальные препараты применяют по показаниям для подавления роста патогенной микрофлоры в тонкой кишке. Обычно назначают антибиотики из группы фторхинолонов, пенициллинов, цефалоспорины, тетрациклины или метронидазол. Препараты принимают внутрь в обычных дозах в течение 7–10 дней.
Оптимальным является использование средств, оказывающих минимальное влияние на симбионтную микрофлору и подавляющих рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов. К ним относятся антисептики: Интетрикс, Энтерол, Бактисубтил, Нифуроксазид и др. При тяжелых формах стафилококкового дисбиоза применяют антибиотики: офлоксацин, оксациллин, амоксициллин. Их назначают на срок 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение натамицина, флуконазола и иных микостатиков.
Бактериальные препараты (пробиотики) можно назначать без предварительной антибактериальной терапии или после нее. Применяют Бифидумбактерин, Пробифор, Бификол, Лактобактерин, Линекс, Бифиформ, Нормофлорины Л, Д, Б, Полибактерин, Наринэ, Аципол, Нутролин В, Тревис.
Еще один способ лечения дисбиоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов (пребиотиками). Один из таких препаратов — Хилак-форте, стерильный концентрат продуктов обмена веществ нормальной микрофлоры: молочная кислота, лактоза, аминокислоты и жирные кислоты. Эти вещества способствуют восстановлению биологической среды в кишечнике, необходимой для существования нормальной микрофлоры, подавляют рост патогенных бактерий, улучшают трофику и функцию эпителиоцитов и колоноцитов. Один миллилитр препарата содержит биологически активные вещества 100 миллиардов нормальных микроорганизмов. Хилак-форте назначают по 60 капель 3 раза в день на срок 4 нед в сочетании с антибактериальными препаратами или после их применения.
Кроме того, применяется сироп лактулозы (Дюфалак, Порталак), подкисляющий кишечный сок и угнетающий рост патогенной микрофлоры. Активное вещество — синтетический дисахарид, который не гидролизуется в тонкой кишке и поступает в ободочную кишку в неизмененном виде, где расщепляется под действием флоры толстой кишки с образованием низкомолекулярных органических кислот, что приводит к снижению рН содержимого кишечника.
Под действием препарата увеличивается поглощение аммиака толстой кишкой и выведение его из организма, стимулируется рост ацидофильных бактерий (в т. ч. лактобактерий), подавляется размножение протеолитических бактерий и уменьшается образование азотсодержащих токсических веществ. Клинический эффект наступает через 2 дня лечения. Препарат в форме сиропа для приема внутрь назначают взрослым в дозе 15–45 мл/сут, поддерживающая доза равна 10–25 мл/сут. Препарат следует принимать 1 раз/сут утром во время еды, с водой, любой другой жидкостью или пищей.
Побочное действие со стороны пищеварительной системы: в первые дни — метеоризм (проходящий самостоятельно через 2 дня); при длительном применении в высоких дозах возможны боли в области живота, диарея. Противопоказания: галактоземия; непроходимость кишечника; повышенная чувствительность к компонентам препарата. Лактулозу можно применять при беременности и в период лактации по показаниям. Препарат следует с осторожностью назначать больным сахарным диабетом.
Из других пребиотиков нужно отметить кальция пантотенат (участвует в процессах ацетилирования и окисления в клетках, углеводном и жировом обмене, синтезе ацетилхолина, утилизируется бифидобактериями и способствует увеличению их массы), аминометилбензойную кислоту (Памба, Амбен) — ингибитор фибринолиза, подавляет протеолитические ферменты условно-патогенных бактерий, стимулируя рост нормальной микрофлоры, лизоцим (обладает бифидогенным, иммуномодулирующим, противовоспалительным действием, улучшает пищеварение, подавляет патогенную флору).
В лечении дисбиоза рекомендуется использовать фитопрепараты. Они являются кишечными антисептиками, подавляют патогенную и сохраняют сапрофитную микрофлору. Фитосборы нормализуют аппетит, улучшают пищеварение, моторику кишечника, оказывают противомикробное и иммуномодулирующее действие, способствуют регенерации слизистой оболочки. Выраженный бактерицидный эффект дают зверобой, календула, эвкалипт, тысячелистник, лапчатка, шалфей, душица, брусника, подорожник. Иммунокорригирующее действие оказывают крапива, мелисса, мать-и-мачеха, подорожник, фиалка трехцветная, череда. Богаты витаминами брусника, крапива, малина, смородина, рябина, шиповник.
Больным с нарушенным полостным пищеварением назначают панкреатические ферменты (Креон, Панцитрат). С целью улучшения функции всасывания используют Эссенциале форте Н, лоперамид (Имодиум) и тримебутин.
Для повышения реактивности организма ослабленным больным при тяжелом дисбиозе целесообразно назначать Анаферон, Иммунал, Ликопид и другие иммуномодуляторы. Курс лечения должен продолжаться в среднем 4 нед. Одновременно назначают витаминно-минеральные комплексы (Витаминерал, Алфавит и др.).
По вопросам литературы обращайтесь в редакцию.
В. В. Скворцов, доктор медицинских наук
ВолГМУ, Волгоград

Стрептококковые инфекции и роль здоровой микрофлоры в их профилактике
С этими паразитирующими в человеке бактериями впервые столкнулись выдающийся австрийский хирург Теодор Бильрот и не менее знаменитый французский химик и микробиолог Луи Пастер. Первый обнаружил их в 1874 году, когда лечил рожистое воспаление, второй – спустя несколько лет при обследовании пациентов с гнойными заболеваниями и сепсисом. Со временем выяснилось, что данные микроорганизмы обитают также в организмах животных и представляют собой целое семейство, которое объединяет одно: они провоцируют различные заболевания.
Знакомьтесь: стрептококк!
Стрептококк или, по-латыни, Streptococcus, представляет собой, говоря научным языком, род шаровидных либо овоидных грамположительных факультативно-анаэробных бактерий. Располагаются попарно или в виде различной длины цепочек. Относятся к семейству Streptococcaceae. Оно включает в себя многочисленные виды, имеющие определенные различия. Как по физиологическим, так и биохимическим признакам, в том числе и по степени патогенного воздействия на человека.
Способны образовывать мелкие колонии (это на поверхностях твердых сред). Придонный же рост дают в жидких средах. Подразделяются на три экологические группы. К первой относится S. Pyogenes, ее представители патогенны только для человека, ко второй – патогенные и для людей, и для животных S. Faccalis, S. agalactia и др. Третья группа представлена условно-патогенными оральными стрептококками S. Mitis, S. mutans и другими.
Болезни, вызываемые стрептококком
Стрептококковые инфекции чаще всего поражают дыхательную систему и кожу. Для этой группы заболеваний характерно возникновение осложнений самого разного характера со стороны внутренних органов. Расскажем о некоторых недугах, вызываемых этими микроорганизмами.

Рожа, рожистое воспаление
Скарлатина. Классическое течение характеризуется повышением температуры до 38 градусов и выше, головной болью и так называемым малиновым, обложенным налетом с выступающими яркими сосочками, языком. Также характерны: боли в горле в момент глотания, покраснение заднего нёба и миндалин, возможно возникновение гнойных пробок. Данное заболевание чревато осложнениями: миокардитом, гломерулонефритом и другими.

Язык ребенка со скарлатиной
Ангина стрептококковая. Ее симптомы схожи на проявления других ангин. Чаще всего появляется боль в горле, повышается температура, возникают озноб и общая слабость, а миндалины, задняя стенка глотки и мягкое нёбо – краснеют. Впоследствии возможно появление гнойного налета, увеличиваются шейные лимфоузлы. Вызываемая стрептококком ангина чревата серьезнейшим осложнением – острой ревматической лихорадкой (ревматизмом), поражающей в свою очередь клапаны сердца и формирующей приобретенные пороки.
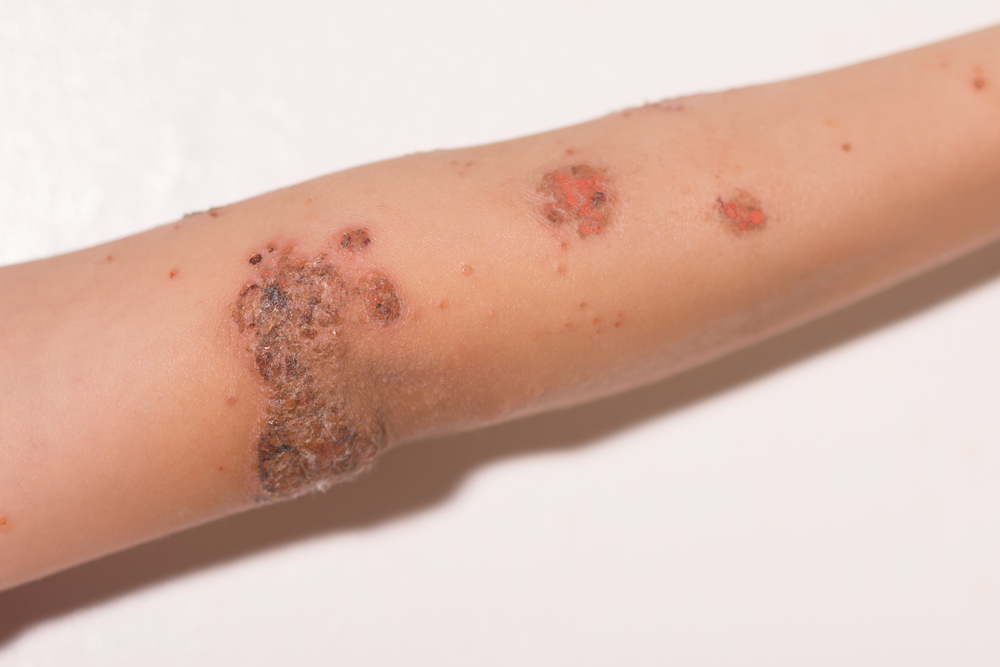
Импетиго на руке ребенка
Некротический фасциит. Заболевание характеризуется острым началом. В области поражения наблюдается легкое покраснение кожи, пальпация пораженного участка вызывает резкую и сильную боль. Мышцы в патологический процесс не вовлекаются, больной чувствует слабость и повышенную утомляемость, его лихорадит. За несколько часов покрасневший участок увеличивается в размерах, кожа на нем отекает, обретает темно-красный или даже бордовый цвет. Из-за гибели нервов может наступить полная потеря чувствительности.
Здоровая флора против стрептококка
Возникновение любой стрептококковой инфекции сигнализирует о неблагополучии в организме. Например, о снижении общего иммунитета. Или нарушении нормальной микрофлоры кишечника (дисбактериозе), когда полезные для человека лактобактерии и бифидобактерии сдают свои позиции, уступая жизненное пространство условно-патогенной микрофлоре. К ней, собственно, относятся и бактерии-стрептококки. Поэтому наряду с другими способами профилактики (прежде всего, соблюдением личной гигиены, избеганием прямых контактов с больными людьми, а также выявлением скрытых носителей) не следует пренебрегать здоровьем кишечника.
Подспорьем становятся пробиотики
Однако зачастую только правильным питанием проблему дисбактериоза как одного из возможных факторов, благоприятствующих возникновению и развитию стрептококковых инфекций, не решить. Особенно, если человек ранее перенес ту или иную из них, его организм дополнительно ослаблен антибиотической терапией и есть риск рецидива заболевания. В таких случаях настоящим подспорьем становятся пробиотики – живые молочнокислые микроорганизмы (лакто- и бифидобактерии, в том числе дрожжи). Помимо улучшения пищеварения, общего состояния желудочно-кишечного тракта и укрепления иммунитета, они вырабатывают биотин, фолиевую кислоту, витамин К и другие необходимые нутриенты.

Дисбактериоз — нарушение микробного равновесия в кишечнике.
Дисбактериоз не местное, а общее нарушение, лежащее в основе многих болезней. Например, длительно не проходящая простуда у ребенка или взрослого свидетельствует о дефекте иммунного статуса, причиной которого может быть дисбактериоз. Женщина, страдающая в период беременности дисбактериозом, родит ребенка, который с рождения будет страдать этим тяжелым недугом. У ребенка развиваются длительные кишечные расстройства, экссудативный диатез, снижается иммунный статус, что приводит к частым и длительным простудам.
Дисбактериоз порождает хронические запоры и диарею, метеоризм и всевозможные гастриты, язвы двенадцатиперстной кишки и другие неприятные болезни. Медикаментозное лечение этих болезней зачастую неэффективно из-за того, что не устранена причина их появления — дисбактериоз.
Как быстро и эффективно вылечить дисбактериоз
Причины, вызывающие дисбактериоз.
- Прежде всего, дисбактериоз вызывают: анацидный гастрит, панкреатит, холециститы и заболевания желчевыводящих путей.
- Дисбактериозом заканчиваются нелеченные паразитарные инфекции — лямблиоз, трихомоноз; присутствие гельминтов: остриц, аскарид и других.
- Аллергии, иммунодефицит, гиповитаминоз, гипоксии, также могут провоцировать развитие болезни.
- Пренебрежение режимом и правилами рационального питания – другая причина нарушения микрофлоры.
- Развитию лекарственного дисбактериоза способствует длительный приём антибиотиков,
сульфаниламидов, иммунодепрессантов, гистаминоблокаторов, туберкулостатиков. - Изменение микрофлоры может быть вызвано длительным воздействием стресса.
Симптомы дисбактериоза.
Лечение дисбактериоза.
Прежде всего, следует избавиться от болезней, способствующих его развитию. Конечно, надо понимать, что излечение – это процесс длительный, когда ряд последовательных действий должны следовать строго друг за другом.

Лечение начинается с уничтожения патогенной микрофлоры, в изобилии присутствующей на всём протяжении желудочно-кишечного тракта. Неоценимую помощь в этом окажет фитотерапия. Травы помогут уничтожению патогенных микроорганизмов, обитающих в кишечнике, очистят от токсинов, наладив его нормальную работу. Для этого применяют: анис обыкновенный, листья ежевики, кровохлебку, мать–и–мачеху, аир, веронику лекарственную, — растения с выраженными антибактериальными свойствами.
Несомненным плюсом представителей семейства лишайников: цетрарии исландской, пармелии, кладонии альпийской, является их антибактериальная активность, при сохранении состава нормальной флоры. В основе их действия – усниновая кислота – мощный растительный антибиотик.
Сбор, эффективно излечивающий дисбактериоз, содержит наряду с лишайниками, растения, обладающие выраженным антибактериальным эффектом: слоевище цетрарии исландской — 3 ч., побеги багульника — 1 ч., анисовые семена – 1 ч., трава чабреца — 1 ч., эвкалипт — 1 ч. Применяемый не менее 20 дней, сбор губителен для гнилостной флоры. При грибковом поражении кишечника, дополните сбор листьями грецкого ореха, дымянкой. Однако, не стоит забывать и про хорошо всем известные чеснок и лук репчатый.
Помимо адсорбции патогенных макромолекул и аллергенов и их выведением, характерной особенностью этой группы препаратов являются их специфические иммуномодулирующие свойства.
Очевидно, что недостаток пищеварительных соков приводит к плохому расщеплению пищи, и, как следствие, развитию гнилостных и бродильных процессов.
Растительные горечи, в изобилии присутствующие в составе лишайников, помимо замечательного антибактериального эффекта, отлично стимулируют желудочно-кишечную секрецию, приводя к улучшению обменных процессов. Это свойство горечей поможет наладить работу кишечника и состояние слизистых оболочек. Подойдут: тысячелистник, вахта трёхлистная, аир болотный. А плоды шиповника, рябины, чёрной смородины, череда трехраздельная — помогут насытить организм витаминами. Дополнить фитотерапию желательно приёмом пищеварительных ферментов: фестала, панзинорма форте, мезима.
Восстановление микрофлоры
И, наконец, бактерийные препараты (пробиотики). Их задача – колонизация в кишечник нормальной флоры.
Другая важная задача бифидобактерий и лактобактерий – участие в синтезе витаминов, расщеплении белков,
жиров, углеводов. Отлично восстанавливает микрофлору напиток, приготовленный на основе молочной сыворотки (Бионапиток «Гармония жизни).
Вывод

Род Streptococcus включает в себя почти 40 видов. Стрептококки получили свое название от греческих слов streptos — цепочка и kokkos — зернышко, поскольку под микроскопом эти бактерии располагаются в виде бусинок, как бы нанизанных на нитку. Хотя встречаются и исключения, например пневмококки образуют только пары. Ученые разделили стрептококки на группы по наличию определенных полисахаридов, и обозначили эти группы латинскими буквами от А до V. Самые опасные для человека те стрептококки, которые входят в группу А.
По способности разрушать эритроциты крови в специальных бактериологических агаровых средах, принято делить стрептококки на ? (альфа-зеленящие), ? (бета-гемолитические) и ? (гамма). В результатах бактериологических исследований вы можете встретить и одно, и другое обозначение, в зависимости от того, какими методами пользуется лаборатория.
Стрептококки относятся к условно патогенным микроорганизмам. То есть в норме бактерии рода Streptococcus могут присутствовать в организме (пневмококки в ротоглотке, энтерококки в кишечнике), и он неплохо справляется с пагубным влиянием бактерий. Но стоит ослабнуть иммунитету и стрептококки тут как тут. А состояние иммунной системы зависит не только (и не столько) от врожденных и приобретенных свойств, но и от состояния микрофлоры. Список же болезней, которые могут вызывать стрептококки, весьма велик:
- Пародонтит;
- Фарингит;
- Ангина;
- Бронхит;
- Пневмония;
- Скарлатина;
- Абсцесс;
- Гломерулонефрит;
- Ревматизм;
- Стрептодермия;
- Эндокардит;
- Лимфаденит
- Рожистое воспаление;
- Воспаления мочеполовой системы;
- Флегмона;
- Сепсис.
Как стрептококк вызывает болезни и какие существуют методы профилактики стрептококковых инфекций?

Способность стрептококков вызывать болезни базируется на токсинах (ядовитых веществах), которые в процессе жизнедеятельности вырабатывают бактерии. К стрептококковым токсинам относятся:
- стрептолизин, который разрушает клеточные стенки человеческого организма;
- эритрогенин, приводящий к повышению температуры, возникновению аллергической реакции (сыпь при скарлатине) и способствующий развитию септического шока;
- лейкоцидин, повреждающий лейкоциты – клетки иммунной системы;
- кардиогепатический токсин, который вызывает поражение диафрагмы (мышцы, служащей для расширения легких при дыхании).
Кардиогепатический токсин также вызывает образование гранулем, то есть узелков в печени и способствует разрушению миокарда сердца.
Поскольку стрептококки являются, как уже было сказано, условно патогенными бактериями, то человек может быть их носителем и даже не подозревать об этом. Главным путем передачи инфекции является воздушно-капельный. Нередко также встречаются больные, заразившиеся контактно-бытовым путем. Проникновение внутрь тканей и в кровь происходит через слизистую оболочку дыхательных путей и через раны (царапины).
Состояние иммунной системы играет огромную роль в вопросе борьбы с заболеванием, поэтому очень важно укреплять иммунитет всеми доступными способами: закаливанием, умеренными физическими нагрузками, сбалансированным питанием (особенно у детей). Необходимо контролировать состояние микрофлоры кишечника, ведь в нем сосредоточено 70% иммунных клеток. Если иммунитет напряжен борьбой с дисбактериозами, то таким оппортунистам, как стрептококк, путь открыт.
Нельзя забывать и о профилактических мероприятиях, в частности, о личной гигиене, элементарные правила которой (мытье рук, чистка зубов, индивидуальная посуда и т.д.) помогут уничтожить миллиарды микроорганизмов. Даже простое мыло и стиральный порошок зачастую оказываются весьма эффективными в борьбе со стрептококками, находящимися во внешней среде.
Какие процессы происходят в местах, где внедрился стрептококк?
В первую очередь развивается воспалительный очаг, который может быть серозным, гнойным или некротическим (с омертвением тканей). Затем бактерии с помощью специальных ферментов преодолевают барьеры и внедряются в кровь, а оттуда попадают в ткани органов, находящихся на удалении от места первичного проникновения. Токсины, которые выделяют бактерии, вызывают подъем температуры, головную боль, рвоту, галлюцинации. К тому же эти токсины способны вызывать аллергические реакции, которые приводят к нарушениям работы сердца, почек, суставов (ревматизм).
Лечение стрептококковых инфекций всегда сопровождается назначением антибиотиков. Как правило, используются антибиотики пенициллового ряда, поскольку к остальным группам антибиотиков у стрептококков за долгие годы выработалась устойчивость. Если инфекция была не распознана и антибиотические препараты применялись неправильно, это приводит к бессимптомному носительству и человек становится опасен для окружающих. Более того, при малейшем напряжении иммунной системы стрептококки дают о себе знать. Хронические фарингиты, тонзиллиты, приводят к тому, что в итоге приходится удалять пораженные стрептококками лимфоузлы – миндалины (гланды). Это – крайняя мера.
Кроме того, лечение антибиотиками у детей может привести к ряду хронических заболеваний, в частности – дисбактериозам. Поэтому после лечения (а иногда и в процессе) назначают прием препаратов, нормализующих микрофлору и содержащих лакто-и бифидобактерии. Кстати, эти же биопрепараты способствуют уменьшению аллергических проявлений. А кислая среда, создаваемая препаратами на основе бифидобактерий, во-первых, нейтрализует токсины, во-вторых, препятствует размножению патогенных бактерий, ну и в-третьих, укрепляет иммунитет.
Читайте также:

