Суперинфекция это тяжелая генерализованная форма инфекционного процесса
Обновлено: 15.04.2024
Экзогенная инфекция возникает в результате заражения человека патогенными микроорганизмами. Поступающими из окружающей среды с пищей. Водой. Воздухом. Почвой, выделениями больного человека, реконвалесцента и микробоносителя.
Эндогенная инфекция вызывается представителями нормальной микрофлоры – условно – патогенными м/о самого индивидуума. Она часто возникает при иммунодефицитных состояниях организма.
Очаговая инфекция, – при которой м/о локализуются в местном очаге и не распространяются по организму. Например, при фурункулезе стафилококки находятся в волосяных фолликулах. При ангине стрептококки обнаруживаются в миндалинах, при конъюнктивитах возбудитель локализуется на конъюнктиве глаза.
Генерализованная инфекция, – при которой возбудитель распространяется по организму лимфогенным или гематогенным путями.
Моноинфекция вызывается одним видом м/о.
Смешанная инфекция – вызывается двумя и более видами м/о.
Вторичная инфекция, - при которой к первоначальной . основной. Уже развившейся болезни присоединяется другая. Вызываемая новым возбудителем. Например, при заболевании брюшным тифом может возникнуть пневмония, вызванная другими бактериями или вирусами.
Реинфекция – заболевание, возникающее после перенесенной инфекции в случае повторного заражения тем же возбудителем, например реинфекции при дизентерии, гонорее. При других болезнях, перенесение которых не завершается образованием напряженного иммунитета.
Суперинфекция – в тех случаях когда инфицирование м/о тем же возбудителем происходит до выздоровления.
Рецидивом называют возврат клинических проявлений болезни без повторного заражения за сет оставшихся в организме возбудителей, например рецидивы при рожистом воспалении, остеомиелите, возвратном тифе.
Каждая манифестная инфекция характеризуется определенным симптомокомплексом и циклическим течением болезни, т.е последовательной сменой отдельных ее периодов, отличающихся продолжительностью, клиническими симптомами, микробиологическими, иммунологическими и эпидемиологическими особенностями. Инкубационный период начинается от момента проникновения инфекционного агента в организм человека до появления первых предвестников заболевания. Продолжительность инкубационного периода при большинстве бактериальных инфекций колеблется от нескольких часов до нескольких недель, в зависимости от нозологической формы.
Микробиологическая и иммунологическая характеристика периодов инфекционных болезней.
Период инфекционного заболевания
Поведение возбудителя
Выделение возбудителя в окружающую среду
Иммунный ответ
Адгезия на чувствительных клетках миндалин, дыхательных путей, желудочно-кишечного, мочеполового трактов
Как правило, не выделяется
Антитела не обнаруживаются
Колонизация чувствительных клеток. Проявление первых неспецифических симптомов заболевания
Интенсивное размножение. Проявление специфических симптомов заболевания
Появление антител класса IgМ, IgА в конце периода происходит замена антител класса IgМ антителами классов IgG и IgА
Прекращение размножения и гибель возбудителя. Нормализация функций больного
Выделение возбудителя, прекращающееся после выздоровления больного или переходящее в микробоносительство
Нарастание титра антител классов IgG, IgА. При ряде заболеваний формируется реакция гиперчувствительности замедленного типа.
Больной в этот период не представляет опасности для окружающих, поскольку возбудитель обычно не выделяется из организма человека в окружающую среду.
Инкубационный период сменяется продромальным периодом (продрома), который продолжается от нескольких часов до нескольких дней. В данный период возбудитель интенсивно размножается и колонизирует ткань в месте его локализации, а также начинает продуцировать соответствующие ферменты и токсины. При многих инфекционных заболеваниях возбудители в период продромы не выделяются во внешнюю среду. Исключения составляет корь, коклюш и некоторые другие.
Разгар болезни характеризуется появлением специфических симптомов. В начале данного периода обнаруживаются специфические антитела в сыворотке крови больного, титр которых в дальнейшем увеличивается. Возбудитель продолжает интенсивно размножаться в организме, накапливаются значительные количества токсинов и ферментов, поступающих в кровь. Вместе с тем происходит выделение возбудителя из организма больного, вследствие чего он представляет опасность для окружающих.
Разгар заболевания переходит в период реконвалесценции (выздоровления), во время которого постепенно восстанавливаются физиологические функции пораженных клеток, тканей, органов и всего организма в целом. Продолжительность данного периода зависит от состояния организма хозяина, реабилитационных мероприятий и т.д. Титр антител достигает максимума.
При многих заболеваниях в период реконвалесценции возбудитель выделяется из организма человека в большом количестве. Пути выделения зависят от локализации инфекционного процесса. Например, при респираторной инфекции – из носоглотки и полости рта с капельками слюны и слизи; при кишечной инфекции – и испражнениями и мочой; при гнойно-воспалительных заболеваниях – с гноем и отделяемым пораженных участков тканей и т.д. В определенных условиях реконвалесценция переходит в микробоносительство, продолжительность которого может измеряться многими месяцами. При локализации возбудителя в крови. Например при возвратном в крови, например при возвратном тифе, риккетсиозах , арбовирусных и других инфекциях, он не выделяется из организма.
В ряде случаев инфекционная болезнь заканчивается летально. Трупы инфекционных больных подлежат дезинфекции, поскольку содержат инфекционные агенты, которые представляют опасность при попадании во внешнюю среду.
Феномен адгезии состоит из нескольких этапов, в результате которых микробные клетки прикрепляются или прилипают к поверхности эпителия. С одной стороны, в этом задействованы неспецифические физико-химические механизма, обеспечивающие контакт между клетками возбудителя и организма хозяина и связанные с гидрофобностью микробных клеток, суммой энергий отталкивания и притяжения. С другой стороны, способность к адгезии определяется специфическими химическими группировками определенного строения – лигандами, находящимися на поверхности микроорганизмов, и рецепторами клеток, которые должны соответствовать друг другу. В противном случае адгезия не происходит.
Адгезины, отвечающие за прилипание возбудителя к клеткам микроорганизма, очень разнообразны. Их уникальное строение, свойственное определенным видам и даже штаммам, обуславливает определенную специфичность данного процесса. Этим объясняется способность одних микроорганизмов прикрепляться и колонизировать преимущественно эпителий дыхательных путей. Других – кишечного тракта, третьих – мочевыделительной системы и т.д.
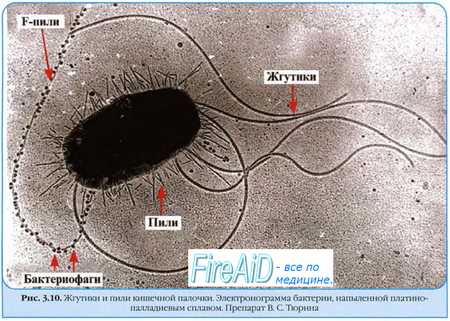
Адгезины многих грамотрицательных бактерий связаны с пилями разных видов. Их обозначают номерами, символами пилей или колонизирующих факторов. Которые они содержат.
У грамположительных бактерий эта функция связана с тейхоевыми и липотейхоевыми кислотами клеточной стенки, капсулой и капсулоподобной оболочкой.
Рецепторы клеток тканей человека также неоднородны по своему составу. Их подразделяют на нативные, индуцированные и приобретенные. Нативные рецепторы располагаются на эпителиальных клетках, участвуя в адгезии соответствующих бактерий.
Индуцированные рецепторы образуются только после адсорбции вирусов (например, вируса гриппа) на чувствительных клетках, после чего на них могут адгезироваться стафилококки и другие бактерии. Это объясняется тем, что рецептором для этих бактерий служит вирусный гемагглютинин, который встраивается в ЦМ эпителиальных клеток. Данное положение приобретает важное значение для понимания механизмов возникновения вторичных бактериальных инфекций при первичных вирусных заболеваниях, например при гриппе.
Колонизация
Представляет собой процесс размножения микробов в месте адгезии. Эта стадия обеспечивает накопление микроорганизмов до такой критической концентрации, которая способна вызвать патологическое действие.
Вирулентность патогенных микроорганизмов может проявиться в инвазии, т.е. проникновении через слизистые и соединительнотканные барьеры в подлежащие ткани. Эту способность связывают с продукцией таких ферментов, как гиалуронидаза и нейраминидаза. Гиалуронидазу образуют Clostridium perfringens, некоторые бактерии родов Streptococcus,Staphylococcus и др. Данный фермент специфически расщепляет гиалуроновую кислоту, входящую в состав межклеточного вещества, тем самым повышая проницаемость слизистых оболочек и соединительной ткани.
Инфекционные болезни характеризуются специфичностью, контагиозностью и цикличностью.
Специфичность инфекции
Каждую инфекционную болезнь вызывает конкретный возбудитель. Однако известны инфекции (например, гнойно-воспалительные процессы), вызываемые различными микробами. С другой стороны, один возбудитель (например, стрептококк) способен вызывать различные поражения.
Контагиозность инфекционного заболевания. Индекс контагиозности инфекции.
Контагиозность (заразительность) определяет способность возбудителя передаваться от одного лица к другому и скорость его распространения в восприимчивой популяции. Для количественной оценки контагиозности предложен индекс контагиозности — процент переболевших лиц в популяции за определённый период (например, заболеваемость гриппом в определённом городе за 1 год).
Цикличность инфекционного заболевания
Развитие конкретного инфекционного заболевания ограничено во времени, сопровождается цикличностью процесса и сменой клинических периодов.
Стадии инфекционной болезни. Периоды инфекционной болезни.
Инкубационный период [от лат. incubatio, лежать, спать где-либо]. Обычно между проникновением инфекционного агента в организм и проявлением клинических признаков существует определённый для каждой болезни промежуток времени — инкубационный период, характерный только для экзогенных инфекций. В этот период возбудитель размножается, происходит накопление как возбудителя, так и выделяемых им токсинов до определённой пороговой величины, за которой организм начинает отвечать клинически выраженными реакциями. Продолжительность инкубационного периода может варьировать от часов и суток до нескольких лет.
Период развития болезни. На этой фазе и проявляются черты индивидуальности болезни либо общие для многих инфекционных процессов признаки — лихорадка, воспалительные изменения и др. Б клинически выраженной фазе можно выделить стадии нарастания симптомов (stadium wcrementum), расцвета болезни (stadium acme) и угасания проявлений (stadium decrementum).
Реконвалесценция [от лат. re-, повторность действия, + convalescentia, выздоровление]. Период выздоровления, или реконвалесценции как конечный период инфекционной болезни может быть быстрым (кризис) или медленным (лизис), а также характеризоваться переходом в хроническое состояние. Б благоприятных случаях клинические проявления обычно исчезают быстрее, чем наступает нормализация морфологических нарушений органов и тканей и полное удаление возбудителя из организма. Выздоровление может быть полным либо сопровождаться развитием осложнений (например, со стороны ЦНС, костно-мышечного аппарата или сердечно-сосудистой системы). Период окончательного удаления инфекционного агента может затягиваться и для некоторых инфекций (например, брюшного тифа) может исчисляться неделями.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
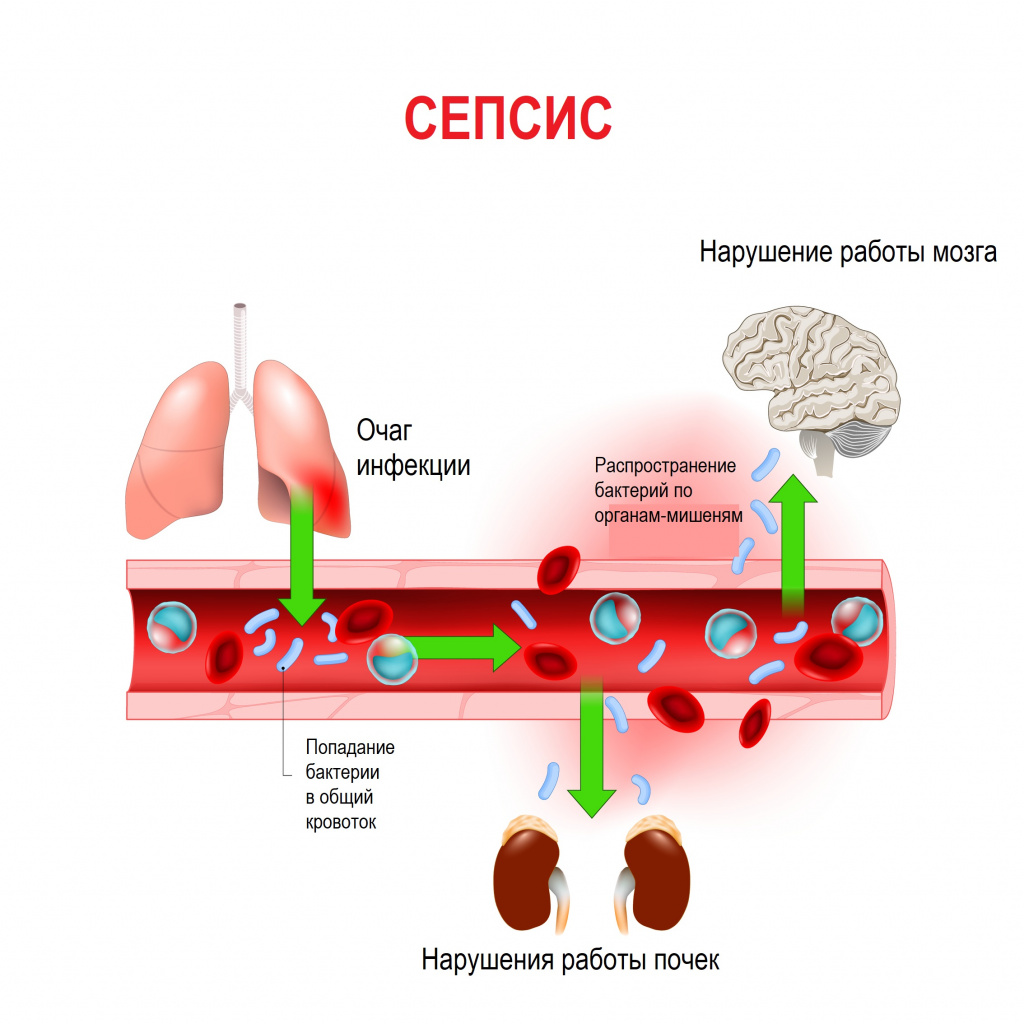
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
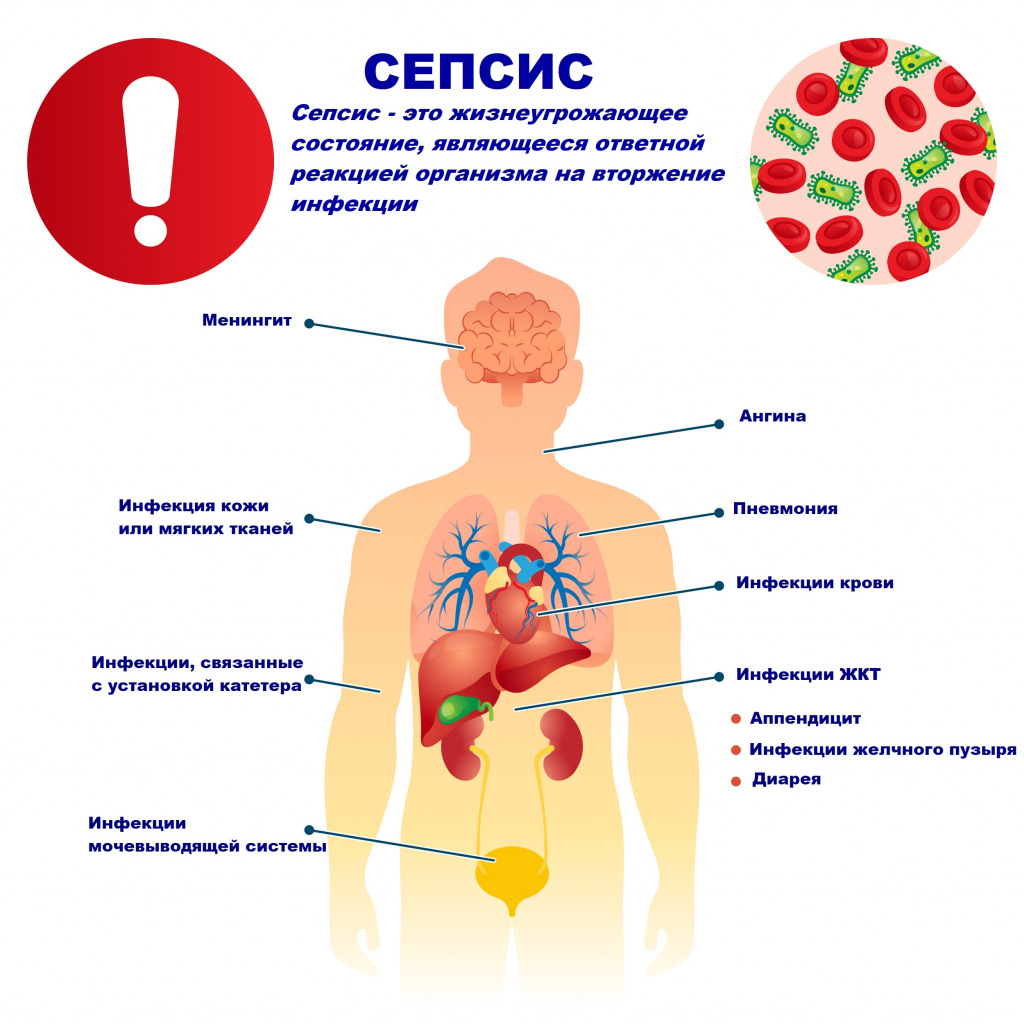
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус Эпштейна–Барр: причины появления, симптомы, диагностика и способы лечения.
Вирус Эпштейна–Барр может инфицировать различные типы клеток, включая B-клетки иммунной системы (разновидность лейкоцитов – белых кровяных телец) и эпителиальные клетки слизистых оболочек.
ВЭБ является представителем ДНК-содержащих вирусов из семейства Herpesviridae (герпесвирусы), подсемейства гамма-герпесвирусов и рода лимфокриптовирусов. В процессе репликации (самокопирования) вируса экспрессируется свыше 70 различных вирусспецифических белков. В настоящее время выделены группы иммуногенных белков, определение антител к которым дает возможность дифференцировать стадию инфекции (ЕА – ранний антиген, ЕВNА-1 — ядерный антиген, VCA — капсидный антиген, LMP — латентный мембранный белок).
Другой способ заражения – контактно-бытовой (вирус передается через зубные щетки, столовые приборы, полотенца и т.д.). ВЭБ также может распространяться через кровь и сперму.
ВЭБ размножается в В-лимфоцитах и эпителиальных клетках, в связи с чем характерно многообразие клинических проявлений данной патологии. Важной отличительной чертой вируса является то, что он не тормозит и не нарушает размножение В-лимфоцитов, а, наоборот, стимулирует его. В этом заключается особенность возбудителя - он размножается в клетках иммунной системы, заставляя их клонировать свою, вирусную, ДНК.
Хронический воспалительный процесс, вызванный ВЭБ, приводит к структурным и метаболическим нарушениям пораженных тканей, что является причиной возникновения разнообразной соматической патологии.
Классификация вируса Эпштейна-Барр
Единой классификации вирусной инфекции Эпштейна-Барр (ВИЭБ) не существует, к использованию в практической медицине предлагается следующая:
- по времени инфицирования – врожденная и приобретенная;
- по форме заболевания – типичная (инфекционный мононуклеоз) и атипичная: стертая, асимптомная, с поражением внутренних органов;
- по тяжести течения – легкая, средней степени и тяжелая;
- по продолжительности течения – острая, затяжная, хроническая;
- по фазе активности – активная и неактивная;
- смешанная инфекция – чаще всего наблюдается в сочетании с цитомегаловирусом.
- Инфекционный мононуклеоз (железистая лихорадка, болезнь Филатова) – распространенное инфекционное заболевание, основными проявлениями которого является подъем температуры до высоких значений, увеличение лимфатических узлов, воспаление слизистой оболочки глотки, увеличение печени и селезенки. ВЭБ в данном случае проникает через эпителий слизистых оболочек верхних дыхательных путей.
- Лимфогранулематоз (болезнь Ходжкина) и некоторые виды неходжкинских лимфом – группа заболеваний, объединенных злокачественной моноклональной пролиферацией лимфоидных клеток в лимфоузлах, костном мозге, селезенке, печени и желудочно-кишечном тракте.
- Синдром хронической усталости – состояние, характеризующееся длительным чувством усталости, которое не проходит после продолжительного отдыха.
- Синдром Алисы в стране чудес – состояние, клиническим проявлением которого является нарушение ощущения своего тела и отдельных его частей. Человек ощущает себя или части своего тела очень большими или очень маленькими по сравнению с действительностью.
- Гепатит, спровоцированный ВЭБ, часто является осложнением инфекционного мононуклеоза. Появляется слабость, тошнота, желтушность кожи и слизистых, увеличивается печень.
- Герпетическая инфекция в виде генитального или лабиального (на губах) поражения. Также возможен стоматит, вызванный ВЭБ. При активации инфекции появляется чувство жжения и боль, а затем множество маленьких пузырьков.
- Посттрансплантационная лимфопролиферативная болезнь – вторичное злокачественное заболевание, развивающееся после трансплантации гемопоэтических стволовых клеток (метод лечения, применяемый при онкологии, заболеваниях крови и др.), ассоциированное с ВЭБ-инфекцией.
- Рассеянный склероз – хроническое аутоиммунное заболевание, при котором поражается миелиновая оболочка нервных волокон головного и спинного мозга. Характеризуется большим количеством симптомов и зависит от уровня поражения: часто снижается мышечная сила, угасают рефлексы, появляются параличи (обездвиженность) различных локализаций.
- Волосатая лейкоплакия – на слизистой оболочке языка по бокам, на спинке либо на его нижней части появляются белые участки с шероховатой поверхностью. Они безболезненны и не причиняют существенного дискомфорта. Основная опасность заключается в возможности озлокачествления измененных клеток слизистой.
- Назофарингеальная карцинома – злокачественное образование глотки. Среди его симптомов часто встречаются заложенность носа, потеря слуха, частые отиты, появление крови в слюне, кровянистые выделения из носа, увеличение лимфоузлов, головные боли.
- Аутоиммунный тиреоидит – хроническое заболевание щитовидной железы, при котором в организме образуются антитела к тканям щитовидной железы. При данном заболевании возможно появление зоба (увеличение щитовидной железы), развитие симптомов гипотиреоза: отеки, повышенная утомляемость, сонливость, запоры, сухость кожи, выпадение волос.
Лабораторное обследование включает:
-
вирус Эпштейна–Барр, определение ДНК в крови (Epstein Barr virus, DNA);
Читайте также:

