Таблетки 225 для вич
Обновлено: 19.04.2024
С самого зарождения эпидемии ВИЧ медицинское научное сообщество было занято поиском эффективного способа предотвращения передачи ВИЧ-инфекции.
Кроме использования средств барьерной контрацепции (презервативов) существуют и иные способы обезопасить себя от ВИЧ-инфекции. Самый главный из них — PrEP, или так называемая доконтактная профилактика (ДКП).
Препараты PrEP — это те же вещества, которыми лечат ВИЧ, но принимаются они по усеченной, неполной схеме. Механизм действия ДКП прост: если лекарство успело попасть в организм заранее, то при попадании в него вируса оно способно убить ВИЧ еще до того, как тот успеет закрепиться в нем.
Защита, которую предлагает PrEP, достаточно надежна и приближается к 100 %, если принимать таблетки правильно.
Что это за таблетки?
Сразу стоит дать названия, существуют две схемы ДКП, которые рекомендованы для использования:
(в одной таблетке — тогда они называются Трувада, либо по отдельности);
Почему именно эти препараты? Для того чтобы ответить на вопрос, можно или нет использовать конкретное лекарство для ДКП, надо провести клиническое исследование. Без клинических исследований подтвердить такой тезис невозможно. Поэтому придерживаться стоит тех схем, которые уже были испытаны и утверждены в качестве PrEP.
Именно поэтому, когда мы говорим о доконтактной профилактике, как правило, речь идет о двух препаратах, как это уже было сказано: тенофовире и эмтрицитабине. Если вы обратитесь в аптеку, то их комбинация в одной таблетке будет стоить порядка 14 000 рублей. Однако допустимо применение и других апробированных для ДКП лекарств. Например, тенофовира и ламивудина. Эта схема также одобрена Всемирной организацией здравоохранения (ВОЗ), они, купленные по отдельности, будут стоить не 14 000, а порядка 1000 рублей.
Какой схемой воспользоваться — решать вам. В целом ДКП сейчас доступна в разных формах для пациентов с разным достатком, и самые дешевые ее схемы могут стоить не более двух тысяч рублей в месяц.
А можно подробнее про механизм действия?
Можно. Итак, доконтактная профилактика заключается в приеме двух препаратов, относящихся к классу ингибиторов обратной транскриптазы, ВИЧ-отрицательными людьми. То есть людьми, в чьем организме вируса пока еще нет.
Что делают эти препараты? На картинке ниже вы можете увидеть жизненный цикл вируса иммунодефицита, как он прикрепляется к клетке и вбрасывает внутрь нее свой генетический материал.
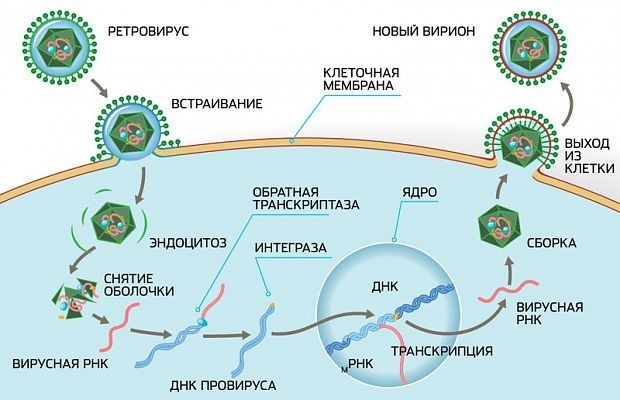
Этот генетический материал под воздействием особого фермента — обратной транскриптазы — запускает процесс репликации новых вирусов.
Два исследования — iPrEx и Partners (оба они проводились в США и Западной Европе) — продемонстрировали крайне высокую эффективность защиты PrEP, в отдельных случаях приближающуюся к 99 %.
В обоих лекарство тенофовир + эмтрицитабин, известное как Трувада, тестировалось на людях, относящихся к ключевым, то есть наиболее уязвимым для эпидемии, группам, — на мужчинах, практикующих секс с мужчинами, и трансгендерных женщинах (mtf). И именно у них этот метод профилактики показал свою наибольшую эффективность.
(Противо)показания к началу ДКП
В настоящее время в России ДКП одобрена Министерством здравоохранения в качестве дополнительного метода профилактики ВИЧ-инфекции и даже попала в клинические рекомендации, так что врач, пусть пока и не имеет возможности выдавать ее бесплатно, как выдаются препараты АРВТ, все же может легально рассказать своим пациентам, где можно приобрести необходимые таблетки, что для этого нужно сделать и как их принимать.
Главным противопоказанием к началу ДКП, конечно, является наличие у пациента ВИЧ-инфекции или симптомов, указывающих на так называемую острую фазу ВИЧ, которая имеет место примерно через две недели после проникновения вируса в организм.
Побочные эффекты
Безопасна ли ДКП? Да. Она безопасна. Оба режима одинаково эффективны. Всего в настоящий момент мы знаем лишь о семи случаях получения вируса на PrEP. А учитывая, что во всем мире примерно полмиллиона человек принимают доконтактную профилактику, семь случаев — это весьма немного.
Два из них были связаны с низкой приверженностью (пропуском приема профилактического препарата), два — с наличием резистентного к эмтрицитабину штамма ВИЧ. Два человека были инфицированы еще до начала доконтактной профилактики. Буквально недавно мировые СМИ сообщили о еще одном случае инфицирования ВИЧ на доконтактной профилактике. На этот раз вирус получил активист в Австралии, который более пяти лет принимал PrEP именно в разовом режиме.
Сейчас идет расследование этого инцидента, и мы пока не знаем точно, в чем была его причина. Что же касается побочных эффектов, они встречаются крайне редко и при должном внимании врача легко контролируются.
Долгосрочные эффекты, например деминерализация костной ткани, появляются не сразу, и, по большому счету, слишком бояться их не стоит. Деминерализация костной ткани, связанная с тенофовиром, проходит в течение, как правило, месяца после остановки приема и не является необратимой. То же самое касается снижения функции почек.
Когда он появится на наших прилавках — сказать сложно. Но в любом случае стоит помнить: даже если это лекарство и появится в России, ДКП — это не витамины, которые можно принимать самостоятельно. Любые побочные эффекты должен отслеживать врач, равно как и назначать сам препарат. Кому стоит обратиться к ДКП, а кому повременить? В идеале такое решение должен принимать не сам пациент в режиме самолечения, а специалист, обладающий достаточной квалификацией.
Как правильно приостановить прием ДКП?
Если вы мужчина или трансгендерная женщина и хотите безопасно прекратить прием доконтактной профилактики, вам необходимо принимать ДКП как минимум еще два дня после последнего рискованного полового контакта. И только через два дня в случае отсутствия в течение этого времени опасных контактов перестать пить таблетки.
Для женщин на ДКП необходимо как минимум семь дней приема ДКП после последнего рискованного контакта. Это связано с особенностями женского организма и того, как ведут себя препараты PrEP в нем.
Чтобы возобновить прием доконтактной профилактики, вы должны быть уверены в отсутствии рисков в период без ДКП. Если риски все же были, то необходимо сделать тест на ВИЧ. Но помните про период серонегативного окна — 4-6 недель с момента последнего риска.
Чтобы начать пить доконтактную профилактику на постоянной основе, необходимо непрерывно принимать ДКП на протяжении семи дней до первого рискованного контакта. Либо (только для мужчин) можно принять двойную дозировку, а затем каждые 24 часа принимать по одной дозе ДКП.
Постконтактная профилактика ВИЧ (ПКП)
Если опасный контакт все-таки случился, а вы не успели обезопасить себя ни с помощью презерватива, ни с помощью препаратов ДКП, и со времени контакта прошло не более 72 часов, избежать инфицирования вам может помочь так называемая постконтактная профилактика.
Заключается она в том, что в указанный срок вам необходимо начать прием препаратов, которыми обычно лечат ВИЧ-инфекцию, но, в отличие от PrEP, тут принимать лекарства придется в полной дозировке, такой, какую принимают люди, у которых уже диагностирована инфекция.
Многочисленными исследованиями доказано: если начать такой прием вовремя, есть большой шанс, что вирус не успеет закрепиться в организме и заболевания удастся избежать. Идеально начать прием лекарств в первые два часа или хотя бы в первые сутки после контакта. Чем позже будет начат такой прием, тем меньше вероятность, что терапия сработает.
Курс профилактики длится 28 дней, и по завершении его необходимо сделать тест, чтобы удостовериться в его эффективности.
Важно! Лекарства, которые вам придется принимать, по факту продаются БЕЗ РЕЦЕПТА, но найти их можно не в каждой аптеке. Поэтому времени на раздумья у вас немного. Возможно, на то, чтобы собрать необходимую комбинацию таблеток, у вас может уйти более суток, так что поиск стоит начать прямо сейчас.
Всего вам придется купить три препарата и принимать нужно будет все три. По отдельности они не работают.
Общая информация
Более 20 лет прошло с тех пор, как на фармацевтическом рынке появился новый класс антиретровирусных препаратов — ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ). В 1996 году американское Управление по санитарному надзору по качеству пищевых продуктов и медикаментов FDA одобрило невирапин, в 1997 году — делавирдин, а годом позже — эфавиренц. Однако, у значительной части пациентов с помощью ННИОТ не удалось добиться оптимального терапевтического ответа вследствие накопленной устойчивости вируса к монотерапии и/или неоптимальных режимов комбинированной терапии, поэтому усилия учёных всего мира были направлены на разработку новых молекул, с улучшенным профилем устойчивости. И они увенчались успехом.
Сегодня FDA одобрено применение пяти ННИОТ [1]:
-
;
- делавирдина;
- эфавиренца;
- этравирина;
- рилпивирина.
Представители ННИОТ принадлежат к разным классам ЛС по химической структуре, но имеют общий уникальный механизм действия: их взаимодействие с обратной транскриптазой ВИЧ-1 запускает цепь изменений, подавляющих активность этого фермента. Для ННИОТ характерна специфичность к ВИЧ-1, что делает их селективными ингибиторами вируса [1, 2].
Сегодня разрабатываются ННИОТ следующего, третьего поколения. Для улучшения приверженности лечению и снижения риска ошибок в дозировках при приёме препаратов была создана комбинация эфавиренц + два НИОТ (эмтрицабин и тенофовир) в одной таблетке, которую принимают один раз в день.
Фармакологическое действие
По всей видимости, ННИОТ вмешиваются в различные этапы реакций обратной транскриптазы ВИЧ-1. За счёт этого препараты блокируют активность РНК- и ДНК-зависимой ДНК-полимеразы, вызывая разрушение активного центра фермента [1, 2].
ННИОТ не оказывают значимого ингибирующего эффекта на ДНК-полимеразу клеток эукариот, таких как ДНК-полимеразы человека.
Следует отметить, что большинство ННИОТ не активны в отношении ВИЧ-2 — второго серотипа вируса иммунодефицита, который встречается гораздо реже ВИЧ-1 (преимущественно в Африке), является менее вирулентным и агрессивным по сравнению с первым серотипом [2]. При этом, исследования in vitro демонстрируют активность этравирина в отношении ВИЧ-2 [3].
Устойчивость к ННИОТ
ВИЧ-инфекция характеризуется очень высокой скоростью репликации: вирус производит от 1 до 10 миллиардов новых вирусных частиц в день у нелеченного инфицированного. Наряду со специфическими свойствами обратной транкриптазы ВИЧ, а также большой длиной вирусного генома (около 10 000 нуклеотидов) это создаёт предпосылки к высокой частоте развития мутаций: мутантный ген в каждом положении нуклеотида в вирусном геноме вырабатывается каждый день.
Как правило, развитие мутаций тесно связано с неоптимальной схемой лечения, например, монотерапией. Оно также ставит под угрозу эффективность последующих схем антиретровирусной терапии, поскольку в каждом классе препаратов наблюдается перекрёстная резистентность [4].
Мутации в домене гена обратной транскриптазы изменяют способность ННИОТ связывать фермент. Устойчивость препаратов первого поколения была связана с мутациями в нескольких кодонах. Однако, чтобы вызвать клиническую неэффективность делавирдина, эфавиренца или невирапина, достаточно наличия мутации К103N или Y181C [4].
Препараты второго поколения более устойчивы, для развития резистентности к ним необходимо более одной мутации. Клинические исследования выявили 17 мутаций устойчивости, связанных со снижением ответа на терапию этравирином [5]. Различные мутации в разной степени влияют на восприимчивость вирусов к этравирину. Рилпивирин, будучи препаратом с более высоким генетическим барьером, чем ННИОТ первого поколения, всё же связан с более частыми случаями развития устойчивости по сравнению с этравирином [6].
Фармакокинетика ННИОТ
ННИОТ демонстрируют значительную индивидуальную фармакокинетическую вариабельность. Все одобренные в настоящее время препараты этой группы используют систему цитохрома Р450 для метаболизма и оказывают или индукционное, или ингибирующее действие на определённые изоферменты (например, CYP3A4, CYP2C9). Это приводит к значительному потенциалу лекарственного взаимодействия [7].
За исключением невирапина, ННИОТ в существенной степени связываются с белками (98–99 %), в первую очередь с альбумином и альфа-кислотным гликопротеином. Периоды полураспада ННИОТ в сыворотке крови довольно продолжительны и составляют от 25 до 55 часов, за исключением делавирдина, имеющего более короткий период полувыведения (2–11 часов) [7].
Побочные эффекты
Самым частым побочным эффектом ННИОТ считается сыпь: она развивается в течение первых нескольких недель терапии и проходит при продолжении лечения. Все препараты этого класса, за исключением этравирина, обладают определённой гепатотоксичностью. Так, делавирдин и эфавиренц могут повышать уровень трансаминаз, в то время как невирапин способен вызывать тяжёлое поражение печени, включая некроз [8].
Эфавиренц способен вызывать неблагоприятные реакции со стороны центральной нервной системы — бессонницу, яркие сновидения, головокружение, спутанность создания и галлюцинации. Рилпивирин также связан с неврологическими побочными эффектами, но реже, чем эфавиренц [6].
Устойчивость к побочным эффектам со стороны ЦНС на фоне приёма эфавиренца обычно возникает после нескольких недель терапии. Их можно корректировать за счёт приёма препарата перед сном и отказа от применения во время еды. Лишь у небольшого числа пациентов воздействие на ЦНС может сохраняться и даже потребовать отмены препарата [9].
Использование эфавиренца также связано с повышением риска суицидов примерно в два раза по сравнению с плацебо. Они присутствуют как в начале лечения, так и при длительном применении. К группам риска по развитию суицидальной наклонности на фоне лечения эфавиренцом относятся пациенты, принимающие психоактивные препараты, имеющие психиатрический анамнез, с массой тела менее 60 кг, а также употребляющие инъекционные наркотические средства [10].
Особенности отдельных ННИОТ
Невирапин
Используется, как минимум, в сочетании с двумя другими антиретровирусными препаратами. Относительно безопасен при беременности. Хорошо проникает через гематоэнцефалический барьер, подвергается печёночному метаболизму (период полувыведения — 28 часов). Препарат индуцирует и собственный метаболизм, поэтому дозу увеличивают постепенно. В начале терапии его назначают один раз в день, а спустя две недели увеличивают кратность приёма до двух раз в день (при хорошей переносимости) [1, 4, 10].
Как правило, невирапин применяется в странах третьего мира, в том числе и для антиретровирусной терапии во время беременности. Результаты исследований показали, что он превосходит зидовудин по эффективности при однократном введении во время родов, однако приводит к развитию резистентности у леченных матерей, что может отрицательно повлиять на терапевтический ответ антиретровирусной терапии в дальнейшем [1, 8].
Делавирдин
Принадлежит к семейству бис (гетеро-арил) пиперазинов, открытых учёными компании Upjohn Laboratories. Имеет более объёмную кристаллическую структуру по сравнению с другими ННИОТ, благодаря чему выступает за пределы гидрофобного кармана, с которым связывается. Это объясняет его особый профиль устойчивости. Мутация, связанная с развитием резистентности к делавирдину, расположена на участке места связывания ННИОТ с карманом. Она вызывает гиперчувствительность ко всем другим препаратам этой подгруппы [1, 4].
Как и невирапин, делавирдин применяют в схемах лечения, когда возникает резистентность, которую невозможно предотвратить. Сегодня этот препарат назначают крайне редко.
Эфавиренц
Представитель подкласса бензоксазинов, открытый исследователями Merck в 1995 году. В отличие от невирапина и делавирдина, был изучен в исследованиях III фазы в качестве компонента лечения ННИОТ и продемонстрировал высокую эффективность.
Этравирин
Принадлежит к семейству диарилпиримидиновых соединений, стал результатом многолетних исследовательских усилий учёных из компаний Janssen Research Foundation и Tibotec, направленных на открытие новых ННИОТ с оптимальным профилем устойчивости и повышенным генетическим барьером для развития резистентности. In vitro демонстрирует более высокий генетический барьер устойчивости по сравнению с невирапином и эфавиренцем [4].
Период полувыведения этравирина составляет 41 час. Препарат назначают два раза в день после еды. Самый распространённый побочный эффект — сыпь, которая, как правило, появляется в течение первых 6 недель терапии. Также на фоне применения нередко развивается периферическая нейропатия [1, 10].
Обладает активностью против штаммов ВИЧ, резистентных к ННИОТ. Из-за потенциально значительных побочных эффектов не применяют в комбинации с другими ННИОТ. Обладает аддитивной противовирусной активностью в комбинации с ингибиторами протеазы ВИЧ, нуколеозидными ингибиторами обратной транскриптазы, а также с ингибитором слияния энвуфиртидом [4].
Рилпивирин
Ещё одно соединение, ставшее результатом дальнейшей оптимизации в рамках ННИОТ, направленной на создание препарата с лучшим профилем устойчивости. In vitro демонстрирует профиль резистентности и генетический барьер, сопоставимый с таковым у этравирина. Отличается высокой биодоступностью, в том числе по сравнению с этравирином. Фармакокинетические свойства позволяют применять один раз в день. Переносится лучше, чем эфавиренц, с более низкой частотой невропсихиатрических нежелательных явлений, сыпью, меньшим количеством липидных нарушений [4, 10].
История антиретровирусной (АРВ) терапии едва разменяла третий десяток, но это был колоссальный путь. Если в 1996 году пациентам были доступны только токсичные и малоэффективные лекарства, которые нужно было пить каждый день и горстями, то уже сейчас вовсю испытывают инъекции, способные подавлять размножение вируса на несколько месяцев. Но это на западе.
Если вы живете в России, то таблетки все еще нужно пить каждый день и (часто) горстями. Тем временем, весь мир стремительно переходит на комбинированные препараты. Сейчас их нельзя назвать революцией в терапии ВИЧ-инфекции, но комбинированные формы - их еще называют таблетками “все в одном” – определенно гораздо лучше обычной АРВ-терапиии.
Во-первых, они берут количеством: для подавления вирусной нагрузки человек принимает всего одну таблетку в день вместо четырех – восьми. Благодаря этому людям, живущим с ВИЧ, не приходится подчинять свое расписание приёму лекарств, не приходится таскать с собой мешок таблеток на случай, если ночуешь не дома, не приходится испытывать столько дискомфорта при проглатывании таблеток (да, для некоторых людей это стресс), не приходится ловить на себе косые взгляды и объяснять случайным людям особенности своего диагноза.
Приверженность к лечению – аккуратный и ежедневный прием лекарств –главное условие успешной терапии ВИЧ-инфекции. Чтобы ее достичь, таблеток в схеме должно быть меньше.
Плохая новость: в России пока недоступны все комбинированные формы, которые есть в мире. Но нужно подготовиться к тому, что когда-то они будут и у нас. Поэтому мы решили вспомнить историю таблеток “все в одном” с момента их появления.
Все больше исследований доказывают, что терапия ВИЧ-инфекции таблетками “все в одном” показывает лучшие результаты, чем схемы с несколькими таблетками, прежде всего, благодаря большей приверженности: у таких пациентов меньше случаев прерываний терапии и достоверно чаще отмечается неопределяемая вирусная нагрузка. Широкое внедрение “монорежимов” – это не прихоть, а необходимость.
Атрипла
Препарат одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США 12 июля 2006 года.
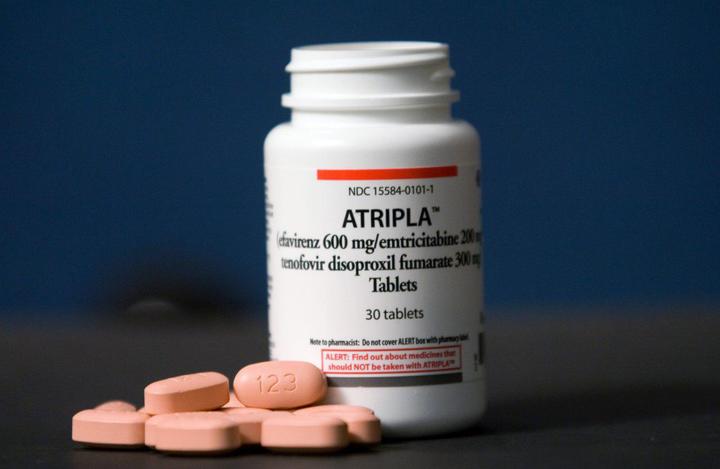
Ветеран монорежима представляет собой комбинацию из 200 мг эмтрицитабина, 300 мг тенофовира дизопроксила фумарата (TDF) и 600 мг эфавиренза. Препарат имеет ряд побочных эффектов. Среди них головокружение, головная боль, боли в животе. Длительный прием TDF может негативно влиять на состояние костей и почек. Препарат рекомендуют принимать на пустой желудок или с пищей (нежирной) – в зависимости от реакции организма. Лекарство также может взаимодействовать с другими препаратами.
Несмотря на все недостатки, Атрипла остается одним из двух препаратов “все в одном”, которые доступны в России.
Эвиплера/ Комплера
Препарат одобрен FDA в августе 2011 года.
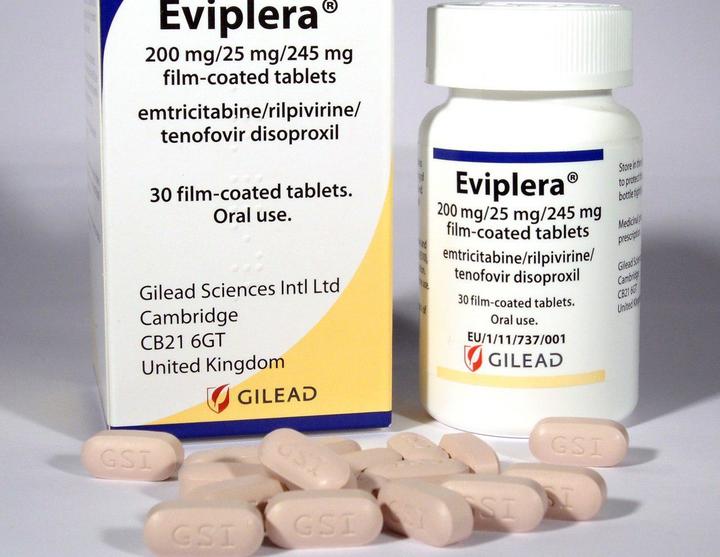
Содержит 200 мг эмтрицитабина, 300 мг TDF и 25 мг рилпивирина. Принимают с едой. Препарат подходит как для новичков, которые раньше не принимали терапию, так и для тех, кто хочет перейти на него с другой схемы лекарств.
Побочные эффекты (повышенный уровень холестерина, потеря аппетита, депрессия, слишком яркие сны, тошнота, рвота, головные боли) выражены меньше, чем у Атриплы, за счет содержания рилпивирина вместо эфавиренза.
Эвиплеру стоит с осторожностью принимать с препаратами против эпилепсии (карбамазепин, окскарбазепин, фенобарбитал), антибиотиками для лечения туберкулеза (рифампицин, рифабутин) и со зверобоем. Действие препарата также могут блокировать лекарства от изжоги (Гевискон, Ренни), препараты из группы омепразола. Поэтому пациентов настоятельно просят сообщать врачу, принимают ли они лекарства для желудка, даже если это происходит не ежедневно.
Второй и пока последний в списке препарат, доступный в России.
Стрибилд (Стрибильд)
Препарат одобрен FDA в августе 2012 года.
Комбинация 200 мг эмтрицитабина, 300 мг TDF, 150 мг элвитегравира и 150 мг кобицистата (препарат-бустер). Принимают один раз в день с едой.
Побочные эффекты схожи с Эвиплерой. Противопоказано пить препарат одновременно с добавками, содержащими кальций, железо, магний, алюминий или цинк. Промежуток между приемом должен составлять не менее 4 часов. Совместный прием гормональных препаратов требует консультации специалиста.
Триумек (Трайомек)
Препарат одобрен FDA в августе 2014 года.
Объединяет 50 мг долутегравира, 600 мг абакавира и 300 мг ламивудина. Лекарство нужно принимать с едой или без еды, но лучше утром, поскольку вечерний прием долутегравира может вызвать бессонницу.
Помимо стандартных побочных эффектов (сонливость, депрессия, головная боль) выделяют боли в суставах, ринит, кашель, желудочный рефлюкс и потерю аппетита. Как и Стрибилд, Триумек плохо сочетается с препаратами кальция и железа. Кроме того, абакавир и долутегравир могу вызывать аллергическую реакцию.
Генвойя
Препарат одобрен FDA в ноябре 2015 года.
Генвойя – это 200 мг эмтрицитабина, 10 мг тенофовира алафенамида (TAF), 150 мг эльвитрагравира и 150 мг кобицистата. Принимается с едой.
Побочные эффекты фактически аналогичны тем, что наблюдаются у Стрибилда, но с небольшой разницей. В составе Генвойи содержится так называемый “новый” тенофовир. При равном противовирусном эффекте и практически одинаковой цене, схема с TAF имеет значительно меньше побочных эффектов. Благодаря этому FDA исключило из аннотации к препарату предупреждение о негативном воздействии на костную ткань. Стоит отметить, что в США уже обновляют рекомендации по лечению ВИЧ-инфекции, где Стрибилд отходит на второй план как устаревший, а предпочтение отдают Генвойе.
Одефси
Препарат одобрен в марте 2016 года.
Состоит из 25 мг рилпивирина, 200 мг эмтрицитабина и 25 мг TAF. Аналог Эвиплеры/Комплеры, но с “новым” тенофовиром вместо “старого”.
Принимают один раз в день с пищей. Побочные эффекты и рекомендации по лекарственной сочетаемости аналогичны Эвиплере. Одефси, как и Генвойя, гораздо меньше влияет на состояние почек и костей за счет содержания TAF.
Не рекомендуется применять совместно с омепразолом (препарат для лечения гастрита и язвы). Кроме того, некоторые антибиотики для лечения туберкулеза могут снижать уровень TAF.
Юлука (Джулука)
Препарат одобрен FDA в ноябре 2017 года.

Первый полный безнуклеозидный режим терапии, в котором содержится только два препарата вместо трёх и более, как в стандартных схемах лечения ВИЧ-инфекции. Содержит 50 мг долутегравира и 25 мг рилпивирина. Подходит для продолжения терапии пациентов, чья вирусная нагрузка стабильно подавлена последние полгода или дольше.
Побочные эффекты те же, что и у долутегравира и рилпивирина. Но уже сейчас специалисты FDA отмечают, что токсичность препарата ниже, чем у классических схем из трех-четырех препаратов. Это связано с меньших количеством действующих веществ и отсутствием в схеме нуклеозидных (нуклеотидных) аналогов.
Перед началом приёма стоит исключить мутации вируса, которые ведут к резистентности к рилпивирину.
Биктарви
Препарат одобрен FDA в феврале 2018 года.
Содержит 200 мг эмтрицитабина и 25 мг TAF и 50 мг нового препарата под названием биктегравир. Известно, что производитель биктегравира пока не собирается выпускать его в форме отдельной таблетки – только в составе комбинированной формы.
Новый препарат считается одним из самых минимальных по количеству действующего вещества. При приеме "Биктарви" рекомендуют контролировать функцию почек.
Symfi и Symfi Lo
Препарат одобрен FDA в марте 2018 года.

Symfi включает 600 мг эфавиренза, 300 мг ламивудина и (внезапно) 300 мг TDF. Symfi Lo содержит 400 (а не 600) мг эфавиренца, 300 мг ламивудина и 300 мг TDF. Принимать рекомендуют натощак.
За счёт содержания TDF препарат может вызывать проблемы с почками и костями. У некоторые пациентов на фоне приёма препарата развивается депрессия.
У Symfi Lo лучше переносимость, благодаря меньшей дозе эфавиренза.
Symtuza
Препарат одобрен FDA в июле 2018 года.
Новейший препарат включает 800 мг дарунавира, 150 мг кобицистата, 200 мг эмтрицитабина и 10 мг TAF.
Противопоказания и побочные эффекты аналогичны препаратам с теми же действующими веществами. Однако токсичное влияние на почки и скелет ниже, благодаря малому содержанию тенофовира.
При этом, кобицистат может усиливать действие других препаратов, потенциально увеличивая риск серьезных побочных эффектов.
Первые антиретровирусные препараты — нуклеозидные ингибиторы обратной транскриптазы — были лишь частично эффективны в отношении вируса иммунодефицита человека. Только с появлением следующего класса, ингибиторов протеазы, удалось достичь контроля над заболеванием и резко снизить смертность. Им, а также ингибиторам ещё одного жизненно важного для лечения ВИЧ фермента — интегразы, и посвящена наша следующая статья из цикла об антиретровирусных препаратах.
Ингибиторы протеазы: механизм действия
Внедрение в клиническую практику ингибиторов протеазы стало краеугольным камнем лечения ВИЧ. Их добавление в схему терапии к двум нуклеозидным ингибиторам обратной транскриптазы (НИОТ) позволило уменьшить количество пациентов с прогрессирующим течением заболевания (до развития СПИДа или смерти) в два раза. У 90 % пациентов, получавших комбинацию из трёх препаратов, число частиц РНК ВИЧ в крови снизилось с более чем 20 000 на миллилитр до менее чем 500 на миллилитр за 24 недели терапии [1].
Механизм действия ингибиторов протеазы основан на их способности блокировать один из ферментов, служащих важным элементом созревания вируса в жизненном цикле ВИЧ. Геном ВИЧ кодирует длинный полипептид. После удаления оболочки вируса и обратной транскрипции генома РНК образуется полипептид, содержащий все продукты вирусных генов, включая структурные белки и ферменты. Затем протеаза ВИЧ расщепляет его на составляющие вирусные белки. При подавлении активности протеазы этот процесс блокируется, что приводит к нарушению созревания вирусной мРНК, в результате чего образуются вирусные частицы, не способные заражать новые клетки [1].
Первыми ингибиторами протеазы стали пептидомиметические молекулы, схожие с пептидом-предшественником и конкурирующие с ним. Однако, как и большинство пептидомиметических белков, ранние ингибиторы протеазы имели существенный фармакокинетический недостаток: они плохо всасывались и быстро выводились при пероральном приёме. Проблема была решена заменой участка пиридина в структуре ингибиторов протеазы на тиазол, менее богатый электронами. Благодаря этому удалось повысить метаболическую стабильность молекулы и улучшить растворимость вещества в воде, а также увеличить его эффективность в отношении вируса [1, 2].
Общие свойства ингибиторов протеазы
Препараты этой группы снижают концентрацию вирусной РНК, увеличивают количество белых кровяных клеток, отвечающих за реакцию иммунной системы на инфекцию (CD-4 клеток) и, в итоге, улучшают выживаемость при включении в терапию наряду с антиретровирусными препаратами других классов.
В целом ингибиторы протеазы имеют сходные терапевтические эффекты. Их активность в отношении ВИЧ-1 и ВИЧ-2 расценивается как высокая, а устойчивость к ним развивается медленно.
Фармакокинетика
Ингибиторы протеазы интенсивно метаболизируются изоферментами системы цитохрома Р450, в частности, CYP3A4, что открывает возможности для целого ряда межлекарственных взаимодействий. Средства, индуцирующие активность ферментов Р450, например, рифампицин или экстракт зверобоя, ускоряют метаболизм ингибиторов протеазы, уменьшая их концентрацию в плазме и терапевтическую эффективность. И наоборот: препараты-ингибиторы ферментов Р450, такие как кетоконазол или циметидин, повышают уровень ингибиторов протеазы в плазме, что связано с увеличением токсичности последних [2].
На сегодня наиболее мощным ингибитором CYP3A4 является ритонавир. Он специально комбинируется с другими ингибиторами протеазы, являющимися субстратами CYP3A4 для продления их периода полувыведения [4].
Ингибиторы протеазы лучше всасываются при приёме во время или после еды [2, 3].
Показания
Препараты этого класса применяются для лечения ВИЧ-инфекции, профилактики передачи инфекции от матери к ребёнку и постконтактной профилактики заболевания.
Противопоказания
Противопоказано одновременное применение ритонавира с препаратами, выведение которых зависит от активности CYP3A4, во избежание токсичности антиретровирусной терапии.
Побочные эффекты
Неблагоприятные реакции при применении ингибиторов протеазы включают [2, 3, 4]:
- желудочно-кишечные расстройства, в частности, диарею с неустановленным механизмом, которая осложняется тем, что она нередко становится одним из осложнений ВИЧ;
- гиперлипидемию — общий побочный эффект для всех ингибиторов протеазы, реже возникает при приёме атазанавира; по всей видимости, нарушение липидного обмена связано с перераспределением жировой ткани, характерным для ВИЧ, которое обостряется при приёме ингибиторов протеазы;
- гипергликемию, инсулинорезистентность, которые развиваются, вероятно, в результате подавления ингибиторами протеаз переносчика глюкозы, что приводит к подавлению активности поглощения глюкозы клетками; с меньшей вероятностью этот побочный эффект проявляет атазанавир по сравнению с другими ингибиторами протеазы;
- сыпь, чаще всего возникает при приёме ампренавира.
Известен и ряд уникальных побочных эффектов: так, при приёме атазанавира может фиксироваться гипербилирубинемия, которая не считается признаком гепатотоксичности препарата, а на фоне применения индинавира возникает кристаллурия и нефролитиаз, что связано с плохой растворимостью препарата в воде. Поэтому пациентам, получающим индинавир, рекомендуют увеличить потребление жидкости во время лечения.
Особые указания
Использование ритонавира в качестве единственного ингибитора протеазы ограничено из‑за его выраженных пищеварительных побочных эффектов в терапевтических дозировках. Сегодня препарат применяют в низких дозах для повышения активности других ингибиторов протеаз. Одним из самых частых комбинированных препаратов, используемых для лечения ВИЧ, сегодня является лопинавир + ритонавир. Следует обратить внимание на то, что капсулы и растворы ритонавира содержат этиловый спирт, поэтому пациентам, получающим препарат, необходимо избегать приёма препаратов, вызывающих дисульфирамовую реакцию, в частности, дисульфирама и метронидазола [4].
Ингибиторы интегразы: механизм действия
Интеграза наряду с обратной транскриптазой и протеазой — один из ключевых участников репликации ВИЧ-1. Она катализирует процессы, приводящие к перемещению ДНК или её фрагментов внутри генома или между геномами. Будучи частью прединтеграционного комплекса, интеграза распознаёт длинные терминальные повторы на концах двойной цепи вновь синтезированной вирусной ДНК, отщепляет по два или по три основания с каждого конца, а также участвует в транспортировке вирусной ДНК в ядро клетки-мишени, где определяет предпочтительный сайт внедрения вирусной ДНК в хромосому и осуществляет её интеграцию в клеточный геном [5].
Ингибиторы интегразы, связываясь с её активным участком и блокируя этап переноса цепей во время интеграции ретровирусной ДНК, предотвращают образование ковалентных связей с ДНК хозяина и включение ВИЧ в геном хозяина [4].
В отличие от обратной транскриптазы и протеазы, интеграза не имеет близких аналогов в эукариотической клетке, поэтому у препаратов, избирательно действующих на неё, побочные эффекты должны быть минимальны [5].
Первым ингибитором протеазы стал ралтегравир, одобренный Администрацией по продуктам питания и лекарственным препаратам США в 2007 году [6]. Сегодня наряду с ралтегравиром используются ещё 4 препарата этого класса: элвитегравир, долутегравир, биктегравир и каботегравир. В разработке находится ещё две молекулы, одна из которых, по всей вероятности, имеет длительность действия до 4 раз больше по сравнению с ралтегравиром и, возможно, будет отнесена к ингибиторам интегразы второго поколения.
Общие свойства ингибиторов протеаз
Механизмы устойчивости к ингибиторам интегразы отличаются от таковых к другим классам антиретровирусных препаратов. Если в основе резистентности большинства ненуклеозидных ингибиторов обратной транскриптазы и ингибиторов протеазы лежит изменение конфигурации активного центра фермента и следующее за ним блокирование присоединения молекулы лекарства, то в случае с ингибиторами интегразы, по всей вероятности, имеют место другие феномены, причём для разных мутаций они могут отличаться [7]. Считается, что ралтегравир имеет низкий генетический барьер для развития устойчивости, поскольку единичная точечная мутация ВИЧ может приводить к изменению способности интегразы к ингибированию. Возможно, имеет место перекрёстная резистентность между ингибиторами интегразы [4].
Фармакокинетика
Основной путь выведения ралтегравира — через печень, тем не менее коррекция дозы препарата у пациентов с печёночной недостаточностью лёгкой и средней степени тяжести не требуется. Почечное выведение играет незначительную роль в метаболизме ингибиторов протеазы, поэтому при почечной недостаточности дозу не пересматривают.
Ралтегравир не является субстратом для ферментов цитохрома CYP450, не ингибирует и не индуцирует их, с чем связана низкая частота лекарственных взаимодействий.
Показания
Ингибиторы протеазы показаны при ВИЧ-1 инфекции у пациентов, у которых выработалась устойчивость к другим классам антиретровирусных препаратов.
Противопоказания
Не имеют терапевтического значения ввиду высокого профиля безопасности препаратов.
Побочные эффекты
Поскольку антиретровирусные препараты обычно назначаются в комбинированных схемах, возникают сложности с определением неблагоприятных реакций, связанных с конкретным классом или лекарственным средством. В целом ингибиторы протеазы хорошо переносятся. В контролируемых исследованиях побочные эффекты при приёме ралтегравира были сопоставимы с таковыми при приёме плацебо. Ралтегравир считается одним из самых безопасных препаратов для лечения ВИЧ-инфекции благодаря минимальному риску развития нежелательных явлений, причём как у пациентов, ранее не получавших антиретровирусную терапию, так и уже имевших опыт лечения препаратами других классов [4, 8].
Особые указания
В настоящее время существуют ограниченные данные об активности ингибиторов протеазы в отношении ВИЧ-2.
Во время клинических исследований наблюдалось небольшое, статистически незначимое увеличение заболеваемости раком у пациентов, получавших ралтегравир, по сравнению с пациентами, получавшими плацебо.
Как и в случае с большинством других антиретровирусных препаратов, безопасность ингибиторов интегразы при применении во время беременности не установлена.
Читайте также:

