Тканевый белок при дисбактериозе
Обновлено: 19.04.2024
Дисбактериоз – качественное и количественное изменение микрофлоры в организме на любом его участке, включая кожные покровы, кишечник, полость рта, влагалище и другие области, населяемые микроорганизмами. Патология встречается при многих заболеваниях, длительном или неконтролируемом употреблении антибиотиков и иммунодепрессантов, развивается под влиянием вредных факторов окружающей среды.
Состояние опасно сопутствующим снижением иммунитета, нарушением барьерной функции кожи и слизистых оболочек, через которые патогенная флора проникает во внутренние органы.
Роль микробиоты в организме
Микробиота – это экосистема, внутри которой уживаются более семи тысяч видов микроорганизмов, включая бактерии, вирусы, бактериофаги, простейшие, археи и грибы. Они живут на кожных покровах, слизистых оболочках, в пищеварительном тракте и играют важную роль в поддержании иммунитета.
- участвует в пищеварении, способствуя переработке пищи и лучшему усвоению питательных веществ;
- стимулирует рост клеток кишечной стенки – энтероцитов;
- поддерживает иммунитет в активном состоянии;
- не допускает роста опасных микроорганизмов, способных вызвать воспаление и инфекционный процесс;
- контролирует метаболические процессы, энергетический и жировой обмены;
- синтезирует биологически активные вещества, участвующие в гормональной и нейрорегуляции.
При снижении количества полезных микроорганизмов, таких как бифидо- и лактобактерии, кишечная палочка и других, занимаемые ими ранее участки активно заселяют патогенные бактерии – преимущественно пептококки, грибы рода Кандида, стафилококки и клостридии.
Причины дисбиоза
Дисбактериоз никогда не возникает первично, он развивается вследствие дисфункции органов и систем либо под действием медикаментов и химических веществ, отрицательно влияющих на микроорганизмы.
- острый и хронический стресс;
- чрезмерная физическая нагрузка;
- неблагоприятные экологические условия, вредные производственные факторы;
- генетическая предрасположенность;
- иммунодефицитные состояния;
- беременность и гормональный дисбаланс, например, гиперандрогения у женщин;
- нарушение биоритмов, акклиматизация;
- активный прием антибиотиков, цитостатиков, сульфаниламидов, заместительная гормональная терапия;
- травмы и воспалительные заболевания, сопровождающиеся активацией иммунитета.
Одна из причин кожного дисбактериоза – чрезмерная гигиена, применение агрессивных уходовых средств, смывающих защитный водно-жировой слой с эпителия.
- присутствие в пище разного рода химических добавок – солей натрия и сернистой кислоты, наночастиц металлов и антибиотиков;
- голодание либо резкое изменение рациона, обилие в нем животных жиров и белков, сахара, крахмала, недостаток клетчатки, витаминов и минеральных веществ;
- инфекционные процессы, глистная инвазия в кишечнике;
- снижение пищеварительной функции внутренних органов при панкреатите, гепатите, гастрите и других заболеваниях;
- нарушение моторики кишечника;
- хирургические вмешательства на органах ЖКТ.
Классификация дисбактериоза
- кожи;
- половых органов;
- мочевыделительных путей;
- ротовой полости;
- органов дыхания.
Также, в зависимости от длительности процесса и выраженности симптомов, выделяют острый и хронический дисбактериоз.
- I степень — недостаток представителей нормальной микрофлоры;
- II степень — преобладание условно-патогенных микроорганизмов;
- III степень — присоединение патогенной флоры.
Кишечный дисбактериоз протекает в три стадии:
- Латентный дисбиоз. Клинические проявления патологии отсутствуют. Нарушение микрофлоры выявляется только по результатам анализов.
- Локальная или местная форма дисбиоза. Сопровождается симптоматикой колита или энтероколита.
- Стадия развития осложнений. Появляются признаки инсулинорезистентности, нейровегетативных нарушений, хронического колита, дерматита и вагинита.
Симптомы нарушенной микрофлоры
- Диспепсический синдром – расстройство стула, иногда с чередованием запора и диареи, метеоризм, вздутие живота, отрыжка и неприятный привкус во рту, урчание в кишечнике.
- Повышенная чувствительность к определенной пище, в особенности к злакам и молочным продуктам, а также аллергическая реакция на переносимые ранее продукты. Наиболее часто встречается при дисбактериозе у детей. Проявления могут быть различными: крапивница, кожный зуд, приступы удушья, ангионевротический отек, жидкий пенящийся стул, резкая боль в животе, тошнота вплоть до рвоты, понижение артериального давления.
- Синдром мальабсорбции – нарушение всасывания питательных веществ проявляется их недостаточностью в организме. Развивается симптоматика белково-энергетической недостаточности, гиповитаминозов, преимущественно витаминов группы В, анемии, нарушения ионного баланса, дефицита кальция.
- Интоксикационный синдром. Характерны слабость, снижение аппетита, повышение температуры тела, головная боль.
- Частые ОРЗ, ОРВИ, обострения герпетической инфекции, грибковые заболевания вследствие снижения иммунитета.
Проявления дисбактериоза кишечника у взрослых зависят от пола пациента. У женщин болезненные ощущения в животе усиливаются перед менструацией. Наблюдается повышенная активность сальных желез, на лице и на теле появляются высыпания. Слизистая оболочка влагалища раздражается, больную беспокоит зуд и жжение вульвы. Кожа становится сухой, дряблой и шелушится. Дисбактериоз кишечника у мужчин сопровождается ухудшением потенции, проблемами с мочеиспусканием.
По мере прогрессирования дисбактериоза присоединяются и симптомы осложнений.
При нейропсихическом расстройстве появляются слабость, апатия, тревожность, пониженное настроение, снижение концентрации внимания и стрессоустойчивости, навязчивые мысли, судороги.
Для инсулинорезистентности характерны прибавка в весе, высокая концентрация глюкозы и липидов крови, ощущение тяжести в правом подреберье. При генерализованной воспалительной или аутоиммунной реакции возможно появление боли в суставах, сыпи на коже, примеси слизи либо крови в испражнениях, повышения температуры тела, озноба, быстрой утомляемости.
Для кожного дисбиоза характерны сыпь на теле, дряблость, краснота, зуд, сухость либо избыточная жирность кожных покровов. При дисбактериозе влагалища проявляются молочница – творожистые выделения белого цвета, жжение и зуд в области наружных половых органов. При дисбалансе флоры ротовой полости прогрессируют стоматит, пародонтоз и кариес, ощущаются неприятный привкус и запах изо рта, появляется белый налет на языке.
Осложнения дисбиоза
- нейропсихические расстройства: депрессия, болезнь Альцгеймера, рассеянный склероз, шизофрения, аутизм, болезнь Паркинсона;
- инсулинорезистентность, дислипидемия, ожирение, сахарный диабет 2 типа, артериальная гипертензия, жировой гепатоз печени;
- аутоиммунные патологии: сахарный диабет I типа, ревматоидный артрит, системная красная волчанка, первичный склерозирующий холангит;
- аллергические заболевания: бронхиальная астма, атопический дерматит, аллергия на пищевые продукты;
- системные воспаления: болезнь Крона, неспецифический язвенный колит, синдром раздраженного кишечника, целиакия и колоректальный рак;
- заражение венерическими заболеваниями, в том числе ВИЧ-инфекцией;
- при генитальном дисбактериозе во время беременности – преждевременные роды;
- сердечно-сосудистые заболевания вследствие активации патогенных бактерий пародонта, способствующих атеросклеротическим процессам и развитию ИБС;
- аденокарцинома и плоскоклеточный рак пищевода при дисбактериозе полости рта.
Диагностика дисбактериоза
-
. Обращают внимание на признаки анемии, уровень лейкоцитов в крови и их распределение по видам. . Выполняется для определения степени выраженности интоксикации и нарушения обмена веществ вследствие их неправильного всасывания в кишечнике. . Оценка физических и химических свойств кала, а также разнообразных компонентов и включений различного происхождения – копрограмма. . Бактериологический посев – это биологическое исследование испражнений с целью определения состава и количества микроорганизмов, обитающих в пищеварительном тракте человека. Также проводится биохимический анализ кала на предмет маркеров дисбиоза, таких как метаболиты летучих жирных кислот, производимых микроорганизмами. . Визуальная оценка состояния органов пищеварения. . Проводится преимущественно детям перед назначением соответствующего лечения.
Лечение дисбактериоза
- острой и жареной пищи, копченых деликатесов;
- продуктов, насыщенных сахарами;
- быстроусвояемых углеводов;
- яблок, бананов, винограда;
- а также ограничение молочных продуктов.
Полезными для микрофлоры считаются продукты, обогащенные клетчаткой – цельнозерновая выпечка, крупы, за исключением белого риса, овощи, листовая зелень и сушеные фрукты. Рекомендована также кисломолочная продукция, содержащая пребиотики и стимулирующая рост полезной микрофлоры.
- Противомикробных средств синтетического происхождения – кишечных антисептиков.
- Пробиотиков. Это готовые лакто-бифидопробиотики в дозах свыше 10 9 в одной капсуле.
- Пребиотиков. Представляют собой вещества, способствующие росту и размножению полезной флоры.
- Синбиотиков. Комплексные препараты, содержащие как сами микроорганизмы, так и необходимые для их развития компоненты.
- Бактериофагов. Эффективны для борьбы с инфекцией при второй степени дисбаланса микрофлоры. Метод лечения чаще используют при дисбактериозе у грудничка, когда противопоказано применение антибиотиков.
- Иммуномодуляторов. Применяются для восстановления иммунитета.
- Антибиотиков. Назначаются при распространенной форме дисбактериоза – в случае выраженных симптомов интоксикации, продолжительной диареи, тяжелого иммунодефицита и лабораторно-подтвержденного дисбиоза третьей степени.
Также применяются средства патогенетической терапии для восстановления моторики кишечника, уменьшения воспаления и восстановления ферментной активности органов пищеварения. Для облегчения проявлений диареи, боли в животе, метеоризма назначаются препараты симптоматической терапии.
Профилактика
Профилактика дисбактериоза включает сбалансированное питание, активный образ жизни, минимизацию стрессов и факторов, способных спровоцировать кишечное расстройство и дисбаланс микрофлоры.
Для предотвращения нарушения микрофлоры у новорожденных рекомендуется отдавать предпочтение естественному родоразрешению и грудному вскармливанию.
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых достигает 10 14 , что на порядок выше общей численности клеточного состава человеческого организма. Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 10 11 бактерий, что составляет 30% сухого остатка кишечного содержимого.
Нормальная микробная флора кишечника
В тощей кишке здоровых людей находится до 10 5 бактерий в 1 мл кишечного содержимого. Основную массу этих бактерий составляют стрептококки, стафилококки, молочнокислые палочки, другие грамположительные аэробные бактерии и грибы. В дистальном отделе подвздошной кишки количество микробов увеличивается до 10 7 –10 8 , в первую очередь за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий. Недавно нами было установлено, что концентрация пристеночной микрофлоры тощей кишки на 6 порядков выше, чем в ее полости, и составляет 10 11 кл/мл. Около 50% биомассы пристеночной микрофлоры составляют актиномицеты, примерно 25% — аэробные кокки (стафилококки, стрептококки, энтерококки и коринеформные бактерии), от 20 до 30% приходится на бифидобактерии и лактобациллы.
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
До 90-95% микробов в толстой кишке составляют анаэробы (бифидобактерии и бактероиды), и только 5-10% всех бактерий приходится на строгую аэробную и факультативную флору (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Площадь внутренней поверхности кишечника составляет около 200 м 2 . Она надежно защищена от проникновения пищевых антигенов, микробов и вирусов. Важную роль в организации этой защиты играет иммунная система организма. Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
В развитии дисбактериоза толстой кишки большую роль играют ятрогенные факторы: применение антибиотиков и сульфаниламидов, иммунодепрессантов, стероидных гормонов, рентгенотерапия, хирургические вмешательства. Антибактериальные препараты значительно подавляют не только патогенную микробную флору, но и рост нормальной микрофлоры в толстой кишке. В результате размножаются микробы, попавшие извне, или эндогенные виды, устойчивые к лекарственным препаратам (стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка).
Клинические особенности дисбактериоза
Клинические проявления чрезмерного роста микроорганизмов в тонкой кишке могут полностью отсутствовать, выступать в качестве одного из патогенетических факторов хронической рецидивирующей диареи, а при некоторых болезнях, например, дивертикулезе тонкой кишки, частичной кишечной непроходимости или после хирургических операций на желудке и кишечнике, приводить к тяжелой диарее, стеаторее и В 12 -дефицитной анемии.
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
Лечение
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нарушенной моторики кишечника;
- стимулирование реактивности организма.
Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Желудочно-кишечный тракт (ЖКТ) выполняет не только пищеварительную, но и иммунную функцию, в частности, участвует в реализации защитных реакций организма против патогенных, условно-патогенных микроорганизмов и многих неорганически
Желудочно-кишечный тракт (ЖКТ) выполняет не только пищеварительную, но и иммунную функцию, в частности, участвует в реализации защитных реакций организма против патогенных, условно-патогенных микроорганизмов и многих неорганических веществ.
Местный иммунитет кишечника
Около 80% всех иммунокомпетентных клеток организма локализовано именно в слизистой оболочке кишечника; около 25% слизистой оболочки кишечника состоит из иммунологически активной ткани и клеток; каждый метр кишечника содержит около 1010 лимфоцитов [1].
Иммунокомпетентная (лимфоидная) ткань ЖКТ представлена организованными структурами (пейеровы бляшки, аппендикс, миндалины, лимфатические узлы) и отдельными клеточными элементами (интраэпителиальные лимфоциты, плазматические клетки, макрофаги, тучные клетки, гранулоциты). Популяция клеток лимфоидной ткани разнородна и состоит из множества групп, подгрупп и клонов клеток с различными функциональными свойствами и специфичностью рецепторов к антигенам [2, 3].
В слизистой оболочке кишечника есть также клетки, вырабатывающие иммуноглобулины других классов, но их значительно меньше. Так, соотношение плазматических клеток, продуцирующих IgA, IgM, IgG, равно соответственно 20:3:1 [2].
Важнейшее свойство системы местного иммунитета кишечника — феномен рециркуляции лимфоцитов. Сенсибилизированные антигенами (как пищевыми, так и инфекционными) лимфоциты пейеровых бляшек мигрируют в брыжеечные лимфатические узлы, а оттуда по лимфатическим сосудам через грудной проток и систему кровообращения направляются к собственному слою слизистой оболочки кишечника, главным образом в качестве клеток, секретирующих IgA. Этот механизм обеспечивает формирование клонов лимфоцитов и образование специфических антител в участках слизистой оболочки, отдаленных от очага первичной сенсибилизации. В процессе сенсибилизации плазматических клеток с последующим клонированием лимфоцитов, вырабатывающих антитела с определенными свойствами (аналогичными тем, которые выступили матрицей), участвуют не только нативные молекулы иммуноглобулинов, но и активные Fc- и F(ab’)2-фрагменты.
Клеточный иммунитет кишечника в отличие от системы секретируемых им антител изучен недостаточно. Известно, что после перорального воздействия антигенов системные клеточные иммунные реакции выявляются редко. Очевидно, когда здоровые люди получают безвредные антигены (например, антигены нормофлоры), в слизистой оболочке кишечника не развиваются реакции клеточного иммунитета [2].
Регуляция иммунных реакций слизистой оболочки кишечника представляет собой сложный процесс, который может изменяться в различных ситуациях, таких как: наличие или отсутствие повреждения слизистой оболочки, сохранение целостности и функциональности биопленки, наличие острых или хронических инфекций, зрелость иммунной системы, состояние питания и генетический потенциал индивидуума. В результате повреждения слизистой оболочки могут возникнуть изменения иммунологической реактивности, хотя в этой ситуации трудно различить первичные и вторичные эффекты.
Роль кишечной микрофлоры в иммунных реакциях
Микрофлора кишечника защищает человека от колонизации экзогенными патогенными микроорганизмами и подавляет рост уже имеющихся в кишечнике патогенных микроорганизмов за счет конкуренции за питательные вещества и участки связывания, а также выработки определенных ингибирующих рост патогенов субстанций. Кроме того, бактерии участвуют в реализации иммунологических защитных механизмов [5].
Известно, что одна из функций нормофлоры — иммунотропная, заключающаяся в стимуляции синтеза иммуноглобулинов, потенцировании механизмов неспецифической резистентности, системного и местного иммунитета, пропердина, комплемента, лизоцима, а также в стимуляции созревания системы фагоцитирующих мононуклеаров и лимфоидного аппарата кишечника [6, 7]. Нормофлора активирует не только местный иммунитет кишечника, но и иммунную систему всего организма, что подтверждается в опытах на безмикробных животных [8]. Основные направления деятельности индигенной (нормальной) микрофлоры в обеспечении нормального иммунного ответа: изменение иммуногенности чужеродных белков путем протеолиза; снижение секреции медиаторов воспаления в кишечнике; снижение интестинальной проницаемости; направление антигена к пейеровым бляшкам. Эти же эффекты реализуются в пробиотических препаратах [5].
В кишечнике бактерии являются важнейшей составной частью биопленки: гликокаликс — слизь — IgA — нормофлора. Биопленка покрывает слизистую кишечника изнутри, занимает все выпуклости, образуемые энтероцитами, и защищает слизистую оболочку от дегидратации, физической и химической агрессии, а также от атак микроорганизмов, бактериальных токсинов, паразитов [9].
На фоне снижения бифидо- и лактобактерий повышается проницаемость эпителиального барьера кишечника для макромолекул пищи и дефицит секреторного IgA [10]. В свою очередь, дефицит секреторного IgA может приводить к развитию заболеваний кишечника и к частым синубронхиальным инфекциям, а в конечном итоге — к предрасположенности к атопии и аутоиммунным заболеваниям [11].
Проведенные на животных исследования показали, что при нарушениях биоценоза в ЖКТ развивается аутоиммунизация к комплексному антигену кишечной стенки, а применение иммунобиологических препаратов предотвращает этот процесс [12].
Дисбактериоз как иммунная дисфункция
Иммунная система регулирует баланс биоценоза кишечника, т. е. механизмы саморегуляции нормофлоры контролируются местным иммунитетом кишечника. Поскольку любой микроорганизм является антигеном, должны существовать механизмы отторжения чужеродных микроорганизмов, а также толерантности и создания благоприятных условий для нормофлоры.
Известно, что через плаценту от матери плоду передаются IgG, то есть иммуноглобулины, обеспечивающие иммунологическую память. Антитела классов М и А через плаценту не проходят, что объясняет недостаточную защищенность новорожденного против грамотрицательных микроорганизмов (энтеробактерии, сальмонеллы) [13]. Кроме того, доказано, что первые микроорганизмы, попадающие в кишечник, появляются там в процессе и после рождения ребенка и прикрепляются к определенным рецепторам [14]. Процесс специфической адгезии условно-патогенных и болезнетворных микроорганизмов к слизистой оболочке ЖКТ может блокироваться среди прочих факторов присутствием IgA и лизоцимом, которые, в свою очередь, способствуют адгезии к рецепторам представителей бифидо- и лактофлоры [15].
Подтверждением роли IgA в предотвращении колонизации слизистых оболочек посторонними микроорганизмами является тот факт, что 99% бактерий представителей нормофлоры не покрыты секреторными иммуноглобулинами. Напротив, энтеробактерии, стафилококки, другие условно-патогенные и сапрофитные микроорганизмы полностью покрыты IgA [8]. В основе этого явления лежит феномен иммунологической толерантности к нормофлоре.
У новорожденных и детей раннего возраста транзиторная иммунная недостаточность — биологическая закономерность, в основном относящаяся к гуморальному иммунитету [13]. У детей этой возрастной группы значительно чаще, чем у детей старше года, возникают стойкие нарушения биоценоза кишечника, что отчасти связано с недостаточностью иммунной системы.
Физиологическая недостаточность системы местного иммунитета кишечника в первые три мес жизни ребенка компенсируется поступлением IgA и других защитных факторов с женским молоком. При грудном вскармливании ежесуточно ребенок получает до 1,5 г IgА. У детей, находящихся на искусственном или раннем смешанном вскармливании, т. е. лишенных защитных факторов женского молока, значительно чаще наблюдаются пищевые аллергии и дисбактериозы кишечника, что отмечается большинством исследователей в этой области.
Проникновение инфекционных агентов на слизистые оболочки ЖКТ и других органов вызывает ответную реакцию системы местного иммунитета в виде нарастания концентрации IgA, который вырабатывается при участии нормофлоры. Соответственно, может возникнуть ситуация, когда микробиологический дисбаланс одного типа будет способствовать усугублению микроэкологических нарушений. Так, снижение количества нормофлоры влечет за собой дефицит IgA, в результате чего повышается колонизация слизистых оболочек условно-патогенной флорой (УПФ).
Врожденные и транзиторные аномалии системы местного иммунитета кишечника снижают резистентность организма не столько к агрессивным вирулентным микроорганизмам, сколько к УПФ. С ними связана устойчивость кишечного дисбактериоза [16].
Практически у 100% людей с приобретенными иммунодефицитами (в результате радиационного воздействия и других иммуносупрессорных факторах) имеются нарушения состава кишечной микрофлоры, при этом у них отмечается не только повышенный рост УПФ, но и резкое снижение нормофлоры [8], то есть нарушаются и защитная функция местного иммунитета, и иммунологическая толерантность, что может косвенно свидетельствовать о том, что система местного иммунитета способствует не только элиминации чужеродных микроорганизмов, но и создает оптимальные условия (а не только иммунологическую толерантность) для нормофлоры.
Учитывая значительное взаимодействие между биоценозом кишечника и системой местного иммунитета кишечника, целесообразно считать дисбактериоз не только микробиологической, но и иммунологической проблемой, что должно отражаться в лечебной тактике.
Иммунокоррекция при дисбактериозе кишечника
Развитие дисбактериоза свидетельствует о недостаточности работы системы местного иммунитета кишечника. Полностью поддерживая тезис о вторичности нарушений биоценоза (дисбактериоз всегда вторичен и причинно обусловлен), можно считать, что одной из причин развития любого дисбактериоза является иммунологическая дисфункция и, прежде всего, недостаточность гуморального иммунитета.
У детей первых месяцев жизни транзиторная иммунная недостаточность — это биологическая закономерность, в основном относящаяся к гуморальному иммунитету. Именно поэтому у детей этой возрастной группы значительно чаще, чем у детей старше года, возникают стойкие и транзиторные нарушения биоценоза кишечника без каких-либо других видимых причин. Затем причинами иммунной дисфункции могут быть хронические вялотекущие паразитарные или микробные инфекции, острые кишечные инфекции, острые респираторные заболевания, детские инфекции, вакцинации; неблагоприятные экологические факторы; стрессы; применение антибиотиков и др. Очень часто проявления дисбактериоза отмечаются через некоторое время после перечисленных воздействий.
Основное средство для иммунокоррекции дисбактериоза — комплексный иммуноглобулиновый препарат (КИП), разработанный сотрудниками МНИИЭМ им. Г. Н. Габричевского [17]. Материалом для получения КИП служит донорская плазма от нескольких тысяч доноров, поэтому можно говорить о коллективном иммунитете. КИП, в отличие от нормального иммуноглобулина человека, содержит иммуноглобулины трех классов: 50% IgG, 25% IgM, 25% IgA. КИП характеризуется повышенным содержанием антител к энтеробактериям (шигеллы, сальмонеллы, эшерихии, протей, клебсиелла и др.), Pseudomonas aeruginosa, стафилококкам, а также к ротавирусам. Таким образом, в состав КИП входят иммуноглобулины 3 классов к основным видам патогенной и условно-патогенной флоры. Специфические антитела, содержащиеся в КИП, нейтрализуют действие энтеропатогенных микроорганизмов, что достигается наличием в препарате антител одинаковой специфичности, но разных классов, способствующих агглютинации, нейтрализации и преципитации инфекционных агентов.
Препарат представляет собой лиофилизированную смесь во флаконах. 1 стандартная доза содержит 300 мг белка и следовые количества консервантов. Введенный через рот, КИП частично расщепляется в желудке и двенадцатиперстной кишке на активные составляющие: Fc- и F(ab’)2-фрагменты, которые сохраняют серологическую и антигенсвязывающую активность иммуноглобулинов [18]. Эти фрагменты имеют слишком большую молекулярную массу, чтобы проникнуть в системный кровоток через слизистую оболочку кишечника, поэтому КИП оказывает в основном местное действие в просвете, на слизистых оболочках и в собственном слое слизистой оболочки, проникая в кровоток в микроколичествах путем пиноцитоза и т. п. Действие КИП происходит на протяжении всего ЖКТ, но особенно в толстом кишечнике, где сосредоточено большое количество лимфоидной ткани (пейеровы бляшки).
Кроме действия на иммунитет кишечника, КИП обладает прямым антимикробным действием за счет содержания в нем антител классов М и А. Эти иммуноглобулины, связываясь с комплементом, вызывают лизис бактерий. Поэтому КИП может использоваться без добавления других антибактериальных препаратов [19].
Для коррекции микробиологических нарушений КИП назначают курсом 5–10 дней по 1 дозе 1 раз в сутки (утром за 30 мин до еды). Пятидневный курс рекомендован при следующих типах дисбактериоза:
Пролонгированные курсы КИП (десятидневный или два пятидневных курса с интервалом между ними 5 дней — схема 5+5) показаны:
Пролонгированные курсы при описанных ситуациях оказались эффективнее традиционного пятидневного курса, что подтвердило специальное исследование [20].
Кроме КИП во флаконах существуют свечные формы, а также комбинации КИП с интерфероном (Кипферон). Кипферон в свечах обладает местным действием в дистальных отделах прямой кишки и общим иммуностимулирующим действием за счет всасывания в геморроидальном сплетении прямой кишки (система нижней полой вены).
КИП в свечах используется у детей со следующими показаниями: запоры, сопровождающиеся развитием трещин прямой кишки; симптомы колита; профилактика и лечение респираторных инфекций у детей старше 1 года; а также совместно с КИП во флаконах, применяемым per os, для усиления иммуностимулирующего действия у детей с выраженным ослаблением иммунитета.
Курс лечения КИП в свечах составляет 5–10 дней, по 1/2–1 свече однократно на ночь, после опорожнения кишечника. Улучшение самочувствия ребенка наступает в процессе лечения или по окончании курса. Эффект применения КИП в свечах подтверждается лабораторными исследованиями.
Кроме коррекции дисбактериоза КИП используют в сочетании с традиционной этиотропной и патогенетической терапией для лечения острых кишечных инфекций установленной или неясной этиологии, особенно у детей раннего возраста [21, 22]. У больных на 2–3 день уменьшается интоксикация, снижается кратность стула, улучшается его консистенция, исчезают патологические примеси, а на 5–6 день наступает нормализация стула. Исследование микрофлоры кишечника показывает санацию организма от возбудителя, при этом, в отличие от использования антибиотиков, уменьшения количества нормофлоры не наблюдается. Свечи с КИП показаны для лечения острых кишечных инфекций у выборочного контингента детей (при рвоте, непереносимости орального введения и т. д.).
Безопасность использования КИП
КИП с осторожностью следует применять у детей с аллергией на белок, реакцией на введение иммуноглобулинов в анамнезе, а также при других ситуациях, чреватых развитием побочных реакций при использовании, и противопоказаниях к применению иммуноглобулинов.
Технология получения КИП, включающая спиртовое фракционирование сыворотки с последующим осаждением фракции иммуноглобулинов полиэтиленгликолем, исключает возможность передачи с препаратом вирусов гепатита В, ВИЧ и других патогенных микроорганизмов. Кроме того, донорская или плацентарная кровь, из которых получают плазму для приготовления КИП, а также серии готового препарата тщательно проверяют. Поэтому опасения инфицирования посредством приема КИП не обоснованы [23].
Клинически выраженные аллергические реакции при приеме КИП наблюдались крайне редко. В некоторых случаях (особенно при совместном использовании с бактериофагами) отмечалось кратковременное ухудшение самочувствия, усиление имевшихся до начала лечения симптомов, что, по-видимому, связано с лизисом УПФ. У некоторых детей на фоне приема КИП снижался аппетит, но восстанавливался всегда быстро и самостоятельно.
Использование КИП пролонгированными курсами не увеличило частоту побочных эффектов по сравнению с традиционными схемами. Для подстраховки в отдельных случаях одновременно с приемом КИП можно назначать антигистаминные препараты.
По вопросам литературы обращайтесь в редакцию.
Ю. А. Копанев, кандидат медицинских наук НИИ эпидемиологии и микробиологии им. Г. Н. Габричевского, Москва
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Диcбактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Дисбактериоз, или дисбиоз – это качественное и количественное изменение микрофлоры в организме. Для него характерно увеличение или резкое уменьшение бактерий, снижение их разнообразия. Дисбактериоз может возникнуть на любом участке, где присутствуют бактерии, включая кожу, влагалище, ротовую полость и т.д.
Микрофлора играет важную роль в поддержании работы иммунной системы, но существует и обратная связь – при серьезном снижении иммунитета возникает дисбактериоз.
Причины появления дисбактериоза
В кишечнике человека присутствует от 70 до 80% клеток иммунной системы. Поэтому любая нестабильность кишечной микрофлоры может нарушить естественные защитные механизмы организма, настроенные против болезней и недомоганий.
Дисбактериоз кишечника связан не только с кишечными расстройствами, но и с множеством других состояний, на первый взгляд не относящихся к пищеварению, – кожными проблемами (акне, экзема), неврологическими расстройствами и т.д.
Среди причин развития дисбактериоза отмечают:
- Увеличение числа болезнетворных бактерий и дрожжевых грибов (например, кандида) и недостаток полезных микроорганизмов.
- Проникновение микроорганизмов, в норме находящихся в толстом отделе кишечника, в тонкий кишечник. Это происходит при хронических заболеваниях, характеризующихся поражением слизистой оболочки желудочно-кишечного тракта (болезнь Крона или неспецифический язвенный колит).
- К другим факторам врачи относят генетическую предрасположенность, несбалансированное питание с низким содержанием клетчатки, но с высоким содержанием сахара и обработанных продуктов, физический и психологический стресс, чрезмерное потребление алкоголя, частое применение антибактериальных препаратов и средств от изжоги, плохую гигиену полости рта.
- Дисбактериоз у практически здоровых лиц:
- возрастной дисбактериоз – изменения микрофлоры у людей пожилого возраста;
- сезонный дисбактериоз – изменения микрофлоры в холодное время года;
- нутритивный дисбактериоз – связанный с несбалансированным питанием;
- профессиональный дисбактериоз – при различных профессиональных вредностях.
- Дисбактериоз, сопровождающий различные заболевания органов пищеварения (желудка, поджелудочной железы, печени и желчевыводящих путей, кишечника, при синдроме мальабсорбции (нарушенном всасывании питательных веществ)).
- Дисбактериоз при других заболеваниях:
- инфекционных,
- иммунодефицитных,
- при гипо- и авитаминозах (уменьшенном поступлении в организм или плохой усвояемости необходимых витаминов),
- при интоксикациях и воздействии на организм человека радионуклидов (радиоактивных изотопов, которые можно встретить в местах с повышенным радиационным фоном, в ограниченном количестве и под строгим контролем они используются для диагностики и лечения некоторых заболеваний).
- Лекарственный дисбактериоз. Возникает вследствие приема антибиотиков, иммунодепрессантов, антацидов, антисекреторных, слабительных средств, химиотерапии и других лекарственных препаратов.
- Стрессорный дисбактериоз. Возникает как результат длительного эмоционального или физического стресса.
- Бессимптомная форма дисбактериоза.
- Локальная, или местная форма дисбактериоза. Наблюдается при развитии локального воспалительного процесса в кишечнике (у больного появляются симптомы колита или энтерита – воспалительных заболеваний толстого или тонкого кишечника).
- Распространенная форма дисбактериоза. Проявляется выраженными нарушениями пищеварения.
- 1-я степень тяжести;
- 2-я степень тяжести;
- 3-я степень тяжести;
- 4-я степень тяжести.
- Исключить прием слабительных, ферментативных препаратов, сорбентов, введение ректальных свечей, масел.
- По возможности сдавать общий анализ кала не ранее, чем через семь дней после окончания приема антибиотиков.
- Ограничить прием лекарственных препаратов и продуктов, способных изменить цвет кала за трое суток до сдачи анализа.
- Несоблюдение рекомендаций по питанию, применение клизмы, выполнение незадолго до сдачи анализа рентгеноскопического или эндоскопического исследования.
- Нарушение правил сбора кала, включающее использование нестерильного контейнера для сбора биоматериала или сбор непосредственно из унитаза, в результате чего в него попали чужеродные микроорганизмы из мочи, выделений половых органов, воды из унитаза и т. д.
- Несоблюдение условий хранения и транспортировки кала (биоматериал доставлен в лабораторию позже максимально установленного времени с момента сбора).
Симптомы дисбактериоза зависят от формы и степени тяжести течения заболевания. Пациенты могут предъявлять жалобы на расстройство желудка, тошноту, диарею или запор, повышенное газообразование и вздутие живота, снижение аппетита, необъяснимую усталость и проблемы с концентрацией внимания, неприятный запах изо рта, высыпания на коже.
Диагностика заболевания
При постановке диагноза врач обращает внимание на жалобы, симптомы заболевания и результаты осмотра. Но для оценки степени тяжести дисбактериоза обычно требуются лабораторные и инструментальные обследования.
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
Копрограмма, общий анализ кала: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показания к назначению исследования
Копрограмма – это лабораторное исследование кала, с помощью которого оцениваются его различные характеристики и выявляются некоторые заболевания желудочно-кишечного тракта (ЖКТ), включая воспалительные процессы и дисбактериоз микрофлоры кишечника.
При отсутствии патологий ЖКТ вся пища, которую употребляет человек, проходя через желудочно-кишечный тракт, подвергается интенсивному воздействию желудочного сока, желчи, пищеварительных ферментов и т.д. В результате пищевые продукты расщепляются на простейшие вещества, которые всасываются через слизистую оболочку кишечника в кровь и лимфу. В толстый кишечник попадают непереваренные пищевые остатки, где из них частично всасывается вода. В норме в прямую кишку попадают каловые массы, примерно на 70% состоящие из воды и на 30% из сухих пищевых остатков.
Если нарушается какая-либо функция органов желудочно-кишечного тракта, начинаются сбои в процессе всасывания пищевых продуктов, что отражается на характеристиках кала.
Таким образом, общий анализ кала назначают для диагностики заболеваний органов желудочно-кишечного тракта (патологии печени, желудка, поджелудочной железы, двенадцатиперстной, тонкой и толстой кишки, желчного пузыря и желчевыводящих путей), при подозрении на кишечные инфекции, для оценки результатов терапии заболеваний ЖКТ, в ходе диагностики злокачественных новообразований и генетических патологий, а также для установления непереносимости различных продуктов.
Подготовка к процедуре
Подготовка к копрограмме требует соблюдения некоторых рекомендаций, которые позволяют получить корректный результат исследования.
Накануне исследования не проводить диагностические процедуры, оказывающие раздражающее действие на анальное отверстие и прямую кишку (клизмы, ректороманоскопию, колоноскопию).
Забор кала можно выполнить самостоятельно в домашних условиях после самостоятельного акта дефекации (а не после клизмы). Для этого лучше использовать медицинское судно или горшок, предварительно тщательно вымытые, или одноразовую пеленку.
Непосредственно после акта дефекации следует набрать шпателем каловые массы в контейнер, заполнив его примерно на 30%. Важно, чтобы в собираемый биоматериал не попали следы мочи, менструальных выделений или воды из унитаза.
Полученный биоматериал нужно доставить в лабораторию в день сбора, хранить контейнер можно в холодильнике при температуре от +4 до +8°С не более 6-8 часов.
Контейнер для сбора биоматериала
Срок исполнения
До 4 рабочих дней (не включая день взятия биоматериала).
Что может повлиять на результаты
Если результат копрограммы кажется вам некорректным, анализ лучше сдать еще раз, придерживаясь всех рекомендаций по подготовке и правилам сбора.
Копрограмма, общий анализ кала
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т. д.
Нормальные значения
| Показатель | Значение |
| Макроскопическое исследование | |
| Консистенция | Плотная |
| Форма | Оформленный |
| Цвет | Коричневый |
| Запах | каловый, нерезкий |
| pH | 6 – 8 |
| Слизь | Отсутствует |
| Кровь | Отсутствует |
| Остатки непереваренной пищи | Отсутствуют |
| Химическое исследование | |
| Реакция на скрытую кровь | Отрицательная |
| Реакция на белок | Отрицательная |
| Реакция на стеркобилин | Положительная |
| Реакция на билирубин | Отрицательная |
| Микроскопическое исследование | |
| Мышечные волокна с исчерченностью | Отсутствуют |
| Мышечные волокна без исчерченности | ед. в препарате |
| Соединительная ткань | Отсутствует |
| Жир нейтральный | Отсутствует |
| Жирные кислоты | Отсутствует |
| Соли жирных кислот | незначительное количество |
| Растительная клетчатка переваренная | ед. в препарате |
| Растительная клетчатка непереваренная | ед. в препарате |
| Крахмал внутриклеточный | Отсутствует |
| Крахмал внеклеточный | Отсутствует |
| Йодофильная флора нормальная | ед. в препарате |
| Йодофильная флора патологическая | Отсутствует |
| Кристаллы | Отсутствуют |
| Слизь | Отсутствует |
| Эпителий цилиндрический | Отсутствует |
| Эпителий плоский | Отсутствует |
| Лейкоциты | Отсутствуют |
| Эритроциты | Отсутствуют |
| Простейшие | Отсутствуют |
| Яйца глистов | Отсутствуют |
| Дрожжевые грибы | Отсутствуют |
Расшифровка показателей
Консистенция
Жидкие каловые массы могут говорить об излишне активной перистальтике кишечника, колите, наличии протозойной инвазии.
Слишком тугие каловые массы свидетельствует об избыточном всасывании жидкости в кишечнике, запорах, обезвоживании организма.
Пенистый кал возникает при недостаточности функции поджелудочной железы или нарушении секреторной функции желудка.
Кашицеобразный кал может говорить о диспепсии, колите или ускоренной эвакуации каловых масс из толстого отдела кишечника.
Горохообразный кал бывает при геморрое, трещинах ануса, язвах, голоданиях, микседеме (слизистом отеке).
Кал в виде тонкой ленты отмечается при стенозе тонкого отдела кишечника, а также при наличии в нем новообразований.
Черный цвет (цвет дегтя) каловым массам может придавать употребление в пищу некоторых продуктов (смородины, аронии, вишни), прием препаратов с висмутом или железом, а также кровотечение в желудке или двенадцатиперстной кишке, цирроз печени.
Красный оттенок появляется при кровотечении в толстом отделе кишечника.
Светло-коричневый цвет кала возникает при печеночной недостаточности или закупорке желчных протоков.
Светло-желтый цвет кала бывает при патологиях поджелудочной железы и вследствие чрезмерного употребления молочных продуктов.
Темно-коричневый цвет говорит об избытке мяса в рационе питания, а также о повышении секреторной функции в толстом отделе кишечника.
Зеленый кал – признак брюшного тифа.
Запах
Гнилостный запах возникает из-за образования в кишечнике сероводорода и говорит о наличии язвенного колита или о распаде тканей, туберкулезе, гнилостной диспепсии.
Кислый запах говорит об усилении процессов брожения.
Зловонный запах свидетельствует о нарушении в работе поджелудочной железы, недостатке желчи, поступающей в кишечник.
Кислотность
Повышение pH наблюдается у грудных детей на искусственном вскармливании, у взрослых - при гнилостной диспепсии, а также при высокой активности кишечной микрофлоры.
Снижение pH происходит в случае нарушения процесса всасывания в тонком отделе кишечника, при чрезмерном употреблении в пищу углеводов, при усилении процессов брожения.
Слизь может находиться как на поверхности кала, так и внутри него, обнаруживается при язвенном колите и запорах.
Кровь
Кровь в кале определяется при кровотечениях в ЖКТ, вызванных новообразованиями, полипами, язвами, геморроем, воспалительными процессами.
Избыточное количество бактерий и грибов может стать причиной ложноположительного ответа.
Остатки непереваренной пищи
Непереваренная пища в кале (лиенторея) свидетельствует о нарушении функции поджелудочной железы, хроническом гастрите, ускоренной перистальтике.
Непереваренные пищевые волокна в анализе кала
Белок
Наличие в кале белка говорит о патологиях двенадцатиперстной кишки или желудка, колите, энтерите, геморрое и некоторых других заболеваниях ЖКТ.
Отсутствие или значительное уменьшение стеркобилина в кале (реакция на стеркобилин отрицательная) указывает на закупорку желчного протока или резкое снижение функциональной активности печени. Увеличение количества стеркобилина в каловых массах наблюдается при усиленном желчеотделении, гемолитической желтухе.
Билирубин
Обнаружение в кале взрослого человека билирубина указывает на нарушение процесса его восстановления в кишечнике под действием микрофлоры. Это говорит о дисбактериозе кишечника, об усилении перистальтики или о приеме антибактериальных препаратов во время подготовки к сдаче анализа или незадолго до этого.
Соединительная ткань и мышечные волокна
Являются недопереваренными остатками мяса и встречаются при недостатке ферментов поджелудочной железы.
Жир
Жир в кале – один из признаков недостаточной функции поджелудочной железы или нарушения отделения желчи.
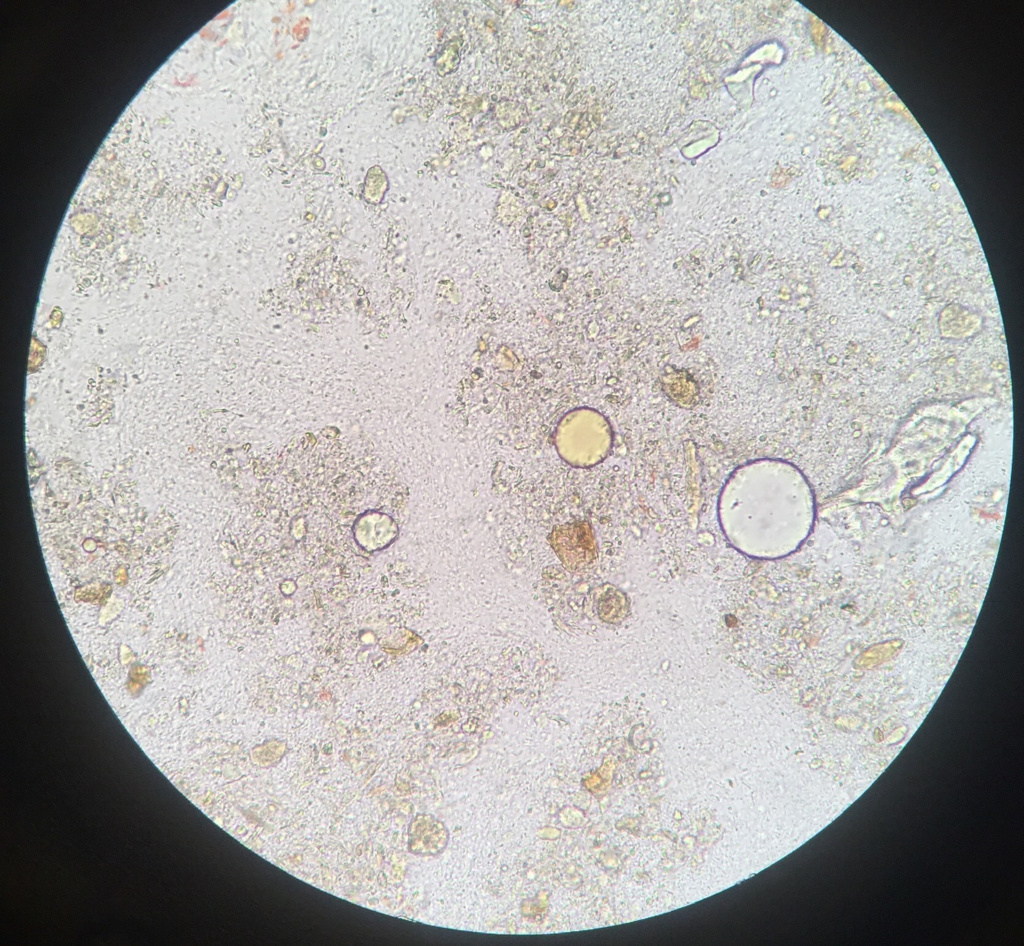
Избыточное количество жира в кале (стеаторея)
Растительная клетчатка
Большое количество переваренной растительной клетчатки в кале свидетельствует о быстром прохождении пищи через желудок из-за снижения его секреторной функции, отсутствия в нем соляной кислоты, а также об избыточном количестве бактерий в толстом кишечнике и их проникновении в отделы тонкого кишечника. Непереваренная клетчатка диагностического значения не имеет, так как в ЖКТ нет ферментов для ее расщепления.
Крахмал
Повышенное содержание крахмала в кале, появляющееся при недостатке процессов переваривания в желудке, тонкой кишке и нарушении функции поджелудочной железы, называется амилореей. Кроме того, много крахмала может обнаруживаться во время диареи.
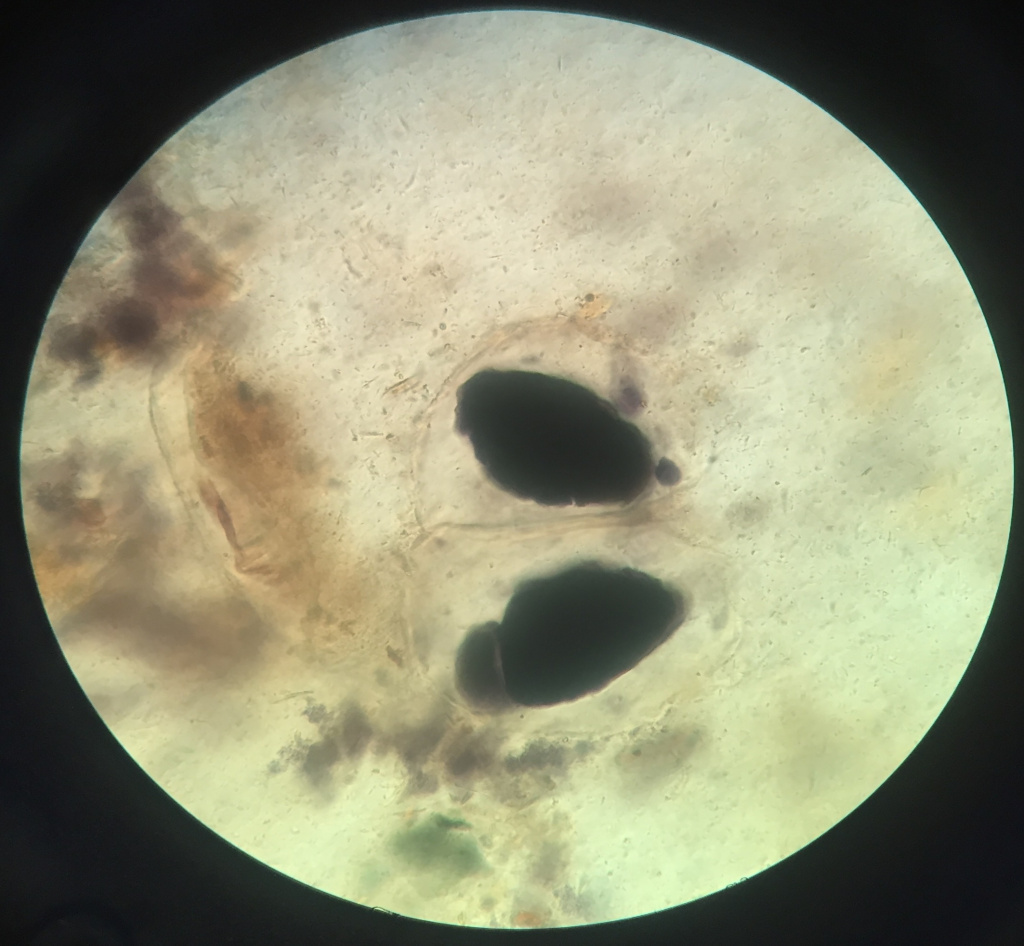
Внутриклеточные гранулы крахмала в анализе кала
Йодофильная флора (патологическая)
Присутствие патологической микрофлоры (стафилококков, энтерококков, кишечной палочки и пр.) свидетельствует об уменьшении количества полезных бактерий в кишечнике и, соответственно, о дисбактериозе. При потреблении большого количества углеводов начинают усиленно размножаться клостридии, вызывая бродильный дисбиоз.
Кристаллы оксалата кальция в кале говорят о недостаточности функции желудка, глистных инвазиях, аллергии.
Кристаллы триппельфосфатов свидетельствуют об усиленном гниении белков в толстой кишке.
Значительное количество цилиндрического эпителия в кале обнаруживается при острых и хронических колитах. Наличие клеток плоского эпителия диагностического значения не имеет.
Лейкоциты в каловых массах появляются при колитах и энтеритах кишечника, дизентерии, туберкулезе кишечника.
Эритроциты появляются в каловых массах при геморрое, трещинах прямой кишки, язвенных процессах в толстом отделе кишечника, при распаде опухолей.
Непатогенные простейшие присутствуют у здоровых людей. Патогенных можно обнаружить в каловых массах, доставленных в лабораторию не позднее двух часов после сбора биоматериала. Их наличие говорит об инвазии.
Яйца гельминтов в кале указывают на глистную инвазию.
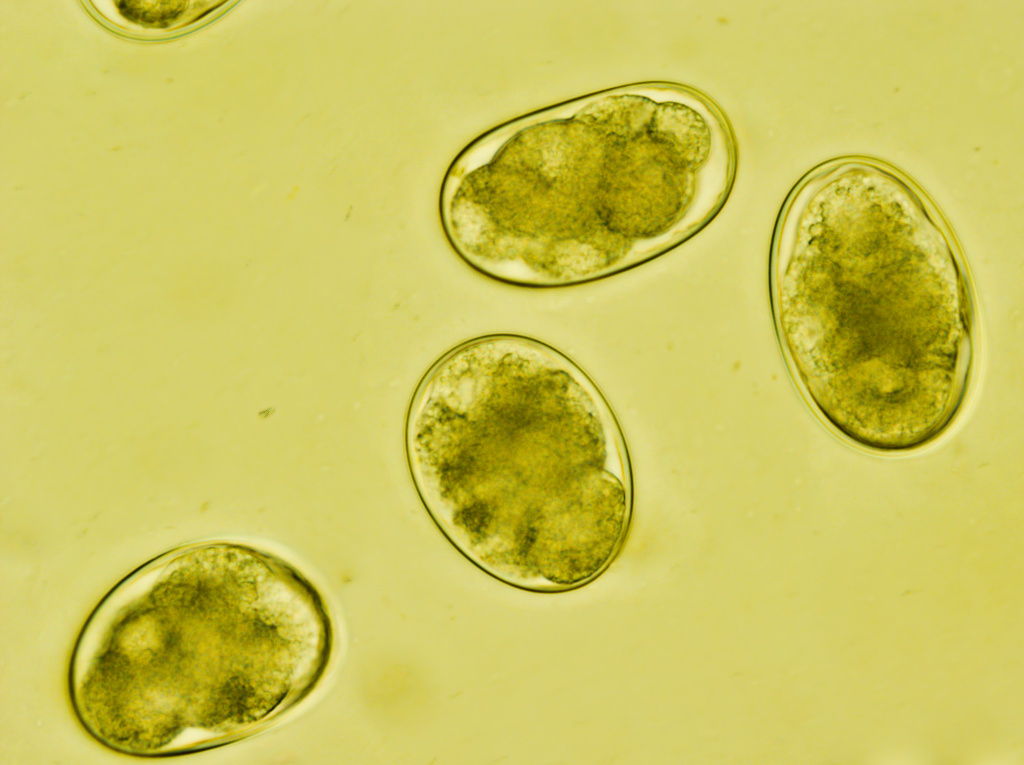
Личинки круглых червей рода Strongyloides в кале
Дрожжевые грибы
Могут присутствовать в кале при проведении терапии кортикостероидами или антибактериальными препаратами. Наличие грибка Candida albicans говорит о поражении кишечника.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Читайте также:

