Токсоплазмоз могут ли от этого быть выкидыши
Обновлено: 23.04.2024
Токсоплазмоз - это паразитарное заболевание, характеризующееся поражением нервной системы, глаз, скелетной мускулатуры и мышцы сердца, а также увеличением лимфоузлов, печени и селезенки. Склонно к хроническому течению.
Распространенность токсоплазмоза в мире невероятно высока, в основном за счет стран Африки, а также Латинской и Южной Америки, в которых инфицированность населения доходит до 90%. Показатели в Европе и Северной Америке ниже – 25-50% населения.
Что провоцирует / Причины Токсоплазмоза:
Возбудитель токсоплазмоза Toxoplasma gondii относится к типу простейших (Protozoa), классу споровиков (Sporozoa), отряду кокцидий (Coccidia). Токсоплазмы подвижны и имеют форму дуги, арки или напоминают дольку апельсина. Встречаются также овальные и округлые формы. Тип движения у токсоплазмы скользящий.
Патогенез (что происходит?) во время Токсоплазмоза:
Жизненный цикл токсоплазмы включает стадии полового и бесполого размножения. Токсоплазмоз распространен во многих странах. Человек заражается от домашних животных, чаще всего от кошек, которые являются окончательным хозяином паразита. В их организме происходит половое размножение возбудителя. Больные токсоплазмозом животные выделяют паразитов с мочой, слюной, молоком. Человек является промежуточным хозяином. Заражение происходит алиментарным (наиболее часто), капельным, через поврежденные кожу и слизистые оболочки, трансмиссивным (при укусе членистоногих) путем. Возможно, внутриутробное заражение при проникновении паразита от матери к плоду через плаценту. Токсоплазмой инфицированы от 50 до 80% взрослого населения.
Пути заражения токсоплазмозом
Заражение человека происходит при употреблении мясных продуктов и яиц, не прошедших достаточную термическую обработку. Не исключена возможность заражения при попадании возбудителя на слизистые оболочки и поврежденные кожные покровы, трансмиссивным и др. путём. Наблюдается и внутриутробное заражение.
Факторы, которые могут способствовать появлению в организме паразита и повышают риск возникновения токсоплазмоза:
• Дотрагиваться грязными руками до рта после контакта с землей, после уборки кошачьего туалета, или любого другого контакта с кошачьими экскрементами.
• Принимать в пищу сырое или не до конца приготовленное мясо, особенно свинину, мясо ягненка или оленину.
• Прикасаться ко рту после контакта с сырым или непрожаренным/непроваренным мясом.
• Пересадка органов или переливание крови (очень редко).
• Если женщина беременна, и она заразилась токсоплазмозом, инфекция может от нее передаться ребенку, что может привести к серьезным последствиям.
В организме человека токсоплазмы размножаются в кишечнике, распространяются лимфогенным и гематогенным путем. Фаза лимфогенного заноса (увеличиваются и воспаляются лимфатические узлы) сменяется гематогенной диссиминацией. Стадия нахождения паразита в крови короткая (несколько дней). Попадая во внутренние органы, токсоплазмы вызывают в них воспалительные явления. Особенно часто поражаются нервная система, сетчатка, печень, миокард. В этих органах токсоплазмы находятся внутриклеточно и экстрацеллюлярно. Скопления паразитов называются псевдоцистами. Токсоплазмы способны образовывать цисты в тканях, вызывая состояние латентной инфекции. Активизация паразита происходит при неблагоприятных для макроорганизма условиях и снижении его иммунологической реактивности. В патогенезе токсоплазмозного поражения нервной системы имеют значение очаговые воспалительные явления (некротизирующий энцефалит), дисциркуляторные нарушения, связанные с васкулитом, обструкция ликворных путей, приводящая к гидро- и микроцефалии.
Наиболее грубые морфологические изменения нервной системы наблюдаются у детей. При макроскопическом исследовании выявляется расширение желудочков с перивентрикулярной зоной некроза. Обнаруживаются рубцы, замещающие участки некроза, облитерация межжелудочкового отверстия и латеральной апертуры IV желудочка. Гидроцефалия может быть выражена, приводя к истончению и деформации вещества полушарий.
Морфологические проявления токсоплазмоза мозга у взрослых многообразны. При микроскопическом исследовании наиболее характерны рассеянные по всему головному и спинному мозгу милиарные гранулемы, состоящие из больших эпителиоидных клеток, лимфоцитов, моноцитов, иногда эозинофилов. Гранулемы содержат многочисленных паразитов, окружены зоной отека с некротическими очажками, обусловленными васкулитом. Типично для токсоплазмоза обызвествление мелких очагов. При наличии токсоплазм в субарахноидальном пространстве возникает серозно-продуктивный лептоменингит.
У большинства зараженных нет клинических проявлений заболевания. У части больных наблюдается вялотекущие хронические формы и крайне редко - острые, с тяжелым течением заболевания. При внутриутробном заражении в первые месяцы беременности часто происходит выкидыш и гибель плода. Не исключается возможность внутриутробных уродств плода и рождения детей с дефектами развития. Если заражение произошло в поздние сроки беременности, рождается ребенок с генерализованным токсоплазмозом.
Симптомы Токсоплазмоза:
Токсоплазмозом заболевают лица любого возраста, однако наиболее часто - дети. Выделяют приобретенный и врожденный токсоплазмоз.
Приобретенный токсоплазмоз. Инкубационный период - от 3 до 14 дней. Продромальный период с общим недомоганием, мышечными и суставными болями - обычно несколько недель, иногда месяцев. Острая стадия заболевания проявляется повышением температуры, ознобом, лимфоаденопатией. Появляется генерализованная макулопапулезная сыпь, отсутствующая только на подошвах, ладонях, волосистой части головы. Наряду с общими признаками инфекционного заболевания имеется клиническая картина поражения различных органов: миокардит, пневмония, очаговый некротический нефрит, гепатит. Поражение нервной системы проявляется менингитом, энцефалитом, менингоэнцефалитом, энцефаломиелитом. Редко наблюдаются радикулоневритическая и малосимптомная формы (последняя может быть обнаружена лишь с помощью серологических реакций).
Наиболее типичной формой токсоплазмоза является менингоэнцефалит, в клинической картине которого имеются общемозговые и менингеальные симптомы, парезы конечностей, тонико-клонические судороги, глазодвигательные (диплопия) и координаторные нарушения. Иногда развиваются одиночные или множественные токсоплазмозные абсцессы в головном мозге. Характерны расстройства сознания, летаргия, утрата памяти и ориентировки в пространстве. В крови обнаруживаются лейкоцитоз со сдвигом формулы влево, увеличение СОЭ, в цереброспинальной жидкости - лимфоцитарный плеоцитоз, умеренное увеличение содержания белка.
Выделяют острую, хроническую и латентную формы с подразделением последней на первично-латентную, без клинических проявлений, и вторично-латентную, возникающую после острой формы или рецидива хронической.
Острый токсоплазмоз характеризуется внезапным началом, лихорадкой, явлениями общей интоксикации. У больных отмечаются лимфаденопатия, макулопапулезная сыпь, увеличиваются печень, селезенка. Могут развиться признаки энцефалита, менингоэнцефалита и миокардита.
В зависимости от преобладающего синдрома выделяют энцефалитическую, тифоподобную и смешанную формы острого токсоплазмоза.
После стихания процесса острый токсоплазмоз переходит во вторично-хроническую или, реже, вторично-латентную формы.
Хронический токсоплазмоз может развиться как первично-хроническое, так и вторично-хроническое заболевание. Он характеризуется торпидным, длительным течением, при котором наблюдаются периоды обострения и ремиссии. Основные клинические симптомы - интоксикация, субфебрилитет, миалгии, артралгии. У больных отмечаются раздражительность, снижение памяти, невротические реакции. Частым симптомом является генерализованная лимфаденопатия. Вследствие мезаденита возникают ноющие боли и вздутие живота, запор, тошнота. К числу важных симптомов заболевания относятся специфический миозит (в толще мышц иногда можно прощупать уплотнения и даже кальцификаты) и миокардит. У многих больных обнаруживают признаки вегето-сосудистой дистонии, эндокринные нарушения (расстройства менструального цикла, импотенция, вторичная надпочечниковая недостаточность и др.). Нередко встречается поражение глаз в форме хориоретинита, ретинита, увеита. В периферической крови - лейкопения, нейтропения, относительный лимфоцитоз, тенденция к эозинофилии. СОЭ в пределах нормы.
Однако преобладающей формой течения приобретенного заболевания является латентный токсоплазмоз. Он чаще имеет первично-латентный и, значительно реже, вторично-латентный характер. Латентный токсоплазмоз диагностируется только при серологическом исследовании. Латентная и хроническая формы болезни могут переходить в тяжелое генерализованное течение, что встречается при ВИЧ-инфекции и других состояниях, приводящих к иммунодефициту. Наиболее часто у больных ВИЧ/СПИДом встречаются менингоэнцефалит и абсцессы мозга, вызванные токсоплазмами. В диагностике большое значение имеет компьютерная томография. В процесс также вовлекаются легкие, сердце, миокард и другие органы. Токсоплазмоз - одна из причин гибели больных ВИЧ/СПИДом.
Врожденный токсоплазмоз. При заболевании матери токсоплазмозом в первой половине беременности плод, как правило, погибает вследствие несовместимых с жизнью пороков развития. При инфицировании матери во второй половине беременности ребенок рождается с тяжелым поражением мозга. Острая стадия заболевания протекает внутриутробно, рождается ребенок с активно текущим менингоэнцефалитом или его последствиями. Неврологические проявления менингоэнцефалита разнообразны: полиморфные эпилептические припадки, клонико-тонические судороги, спастические парезы, тремор, миоклонии, парезы глазных и мимических мышц, нистагм, контрактуры мышц, менингеальные явления. Иногда имеются симптомы поражения спинного мозга.
Для врожденного токсоплазмоза характерна триада признаков: гидроцефалия, хориоретинит и интрацеребральные кальцификаты. При гидроцефалии увеличиваются размеры головы, кости черепа истончаются, роднички напряжены. Гидроцефалии обычно сопутствует микрофтальмия. Если гидроцефалия развивается до рождения ребенка, то в родах приходится прибегать к краниотомии. Однако во многих случаях увеличение объема головы не обнаруживается и гидроцефалия выявляется только при пневмоэнцефалографии. Хориоретинит часто бывает двусторонним, фокальным, включающим макулярную область. Возможны также ирит, увеит, катаракта, первичная или вторичная атрофия зрительных нервов. Интрацеребральные кальцификаты диаметром 1-3 см располагаются в коре и базальных ганглиях и выявляются на краниограммах КТ и МРТ головного мозга.
Дети с врожденным токсоплазмозом отстают в умственном развитии вплоть до олигофрении. У них наблюдаются также разнообразные психотические состояния (депрессия, психомоторное возбуждение, галлюцинации, кататония). Иногда у детей с врожденным токсоплазмозом обнаруживаются желтуха, увеличенные печень и селезенка. Температура обычно остается нормальной. Ликворное давление при люмбальной пункции обычно нормальное. Отмечается высокое содержание белка и умеренный мононуклеарный плеоцитоз, иногда ксантохромия.
Осложнения врожденного токсоплазмоза - следствие поражения мозга и глаз, ведущего к истощению, параличам, умственной отсталости, слепоте. Присоединение вторичной инфекции обусловливает развитие гнойного менингоэнцефалита и пиоцефалии. Смерть наступает от прогрессирующего поражения головного мозга.
Течение токсоплазмоза
Ранее считалось, что врожденный токсоплазмоз приводит к смерти в течении первых лет жизни ребенка. В настоящее время возможны стабилизация инфекции и даже полное выздоровление с остаточными явлениями, выраженность которых зависит от степени поражения центральной нервной системы (кальцификаты, хореоретинит, эпилептический синдром, отставание в умственном развитии и др.). У взрослых наряду с острым течением часто отмечается подострое или даже хроническое развитие заболевания. Нередко приобретенный токсоплазмоз, особенно у взрослых, протекает без выраженных в той или иной степени клинических симптомов (инаппарантная форма).
Диагностика Токсоплазмоза:
Диагноз токсоплазмоза устанавливают на основании комплекса показателей, которые включают клинические данные и результаты лабораторного подтверждения. Относительное значение имеют эпидемиологические предпосылки, такие как контакт с кошками, условия общения с ними, особенности пищевых привычек (употребление сырого, полусырого мяса, проба сырого фарша, немытых овощей, фруктов), соблюдение личных гигиенических навыков, профессия и др.
Чрезвычайное многообразие клинических проявлений, отсутствие симптомов, характерных только для токсоплазмоза, затрудняет клиническую диагностику и позволяет в определенных случаях только предположить диагноз, который формируется при проведении полноценной дифференциальной диагностики и при анализе результатов лабораторного исследования.
Методы лабораторной диагностики токсоплазмоза делят на две группы: паразитологические и иммунологические.
Паразитологические методы основаны на возможности обнаружения возбудителя или выделении его при заражении восприимчивых животных - биопроба.
К ним относится прямая микроскопия мазков - отпечатков пораженных органов (миндалины, биоптат лимфоузлов, головного мозга, внутренние органы погибших эмбрионов или плодов) или мазков из осадка спинномозговой жидкости, крови, окрашенных по Романовскому - Гимзе. Можно исследовать гистологические препараты этих органов.
К сожалению, технические сложности обнаружения post mortum, а также редкие случаи обнаружения токсоплазм в крови, спинномозговой жидкости затрудняют использование этих методов.
Биологическая проба на белых мышах, хомяках, зараженных исследуемым материалом и проведением последующих 5-6 слепых пассажей, требует особых условий содержания животных, лабораторий со специальным режимом работы и применяется только в научных целях.
В широкой практике используют преимущественно иммунологические методы, которые включают серологические реакции и внутрикожную пробу. Эти методы, достаточно специфичные и чувствительные, определяют, прежде всего, состояние инфицированности, а серореакции - и заболеваемости. Эти понятия неоднозначны, ибо заболеваемость во много раз ниже инфицированности.
Из методов серологической диагностики используют реакцию связывания комплемента (РСК), реакцию непрямой иммунофлюоресценции (РНИФ) и иммуноферментный анализ (ИФА). Диагноз подтверждается достоверным нарастанием титра антител - динамикой титров в парных сывороротках, взятых с интервалом 2-4 недели.
РСК становится положительной со 2-й недели после заражения и наибольших титров - 1:16 - 1:320 достигает через 2-4 месяца. Через 1-3 года может стать отрицательной или сохраниться в низких титрах (1:5, 1:10), которые не имеют самостоятельного значения.
РНИФ становится положительной с 1-й недели инфекции и максимальных показателей (1:1280 - 1:5000) достигает на 2- 4 месяце. В низких титрах 1:10 - 1: 40 может сохраняться 15-20 лет.
ИФА в соответствии с ориентацией на международный стандарт ВОЗ является наиболее объективным методом. О положительной реакции свидетельствуют оптические показатели более 1,5, в иммуноферметных единицах - больше 60; в международных - больше 125, в титрах антител - 1:1600 и больше.
Диагностика врожденного токсоплазмоза у ребенка начинается с акушерского анамнеза матери, эпиданамнеза и показателей серологических реакций. Обязательны консультации специалистов для дифференциации с герпетической, цитомегаловирусной, листериозной, хламидийной инфекциями, а также рентгенография черепа и обследование в медикогенетическом центре.
Следует напомнить, что 20 - 30% женщин имеют антитела - это здоровые носители антител. Они не требуют лечения. 70 - 80%, показавших отрицательные серореакции, составляют группу риска и нуждаются в повторном обследовании.
На протяжении первого года жизни ребенка необходимо проводить параллельные серологические обследования матери и ребенка в динамике.
Лечение Токсоплазмоза:
При остром токсоплазмозе используются химиотерапевтические препараты.
Делагил (по 0,5г 2 раза в сутки) в сочетании с сульфаниламидами (по 0,5г 2 раза в сутки) в течение 10 дней. Фансидар назначается в количестве 5 таблеток на курс: по 1 табл. через 2 дня или в виде внутримышечных инъекций по 1 ампуле в 2,5 мг один раз в 2 дня в количестве 5 инъекций. Проводится один или два курса лечения.
Из антибиотиков назначаются: линкомицина гидрохлорид (по 0,5г 2 раза в сутки); метациклина гидрохлорид (по 0,3г 2 раза в сутки) в течение 5-7 дней в сочетании с сульфаниламидами; ровамицин.
Лечение хронического токсоплазмоза во много раз труднее, чем острого, так как химиопрепараты не оказывает значительного эффекта. Главное место занимает гипосенсибилизирующая и иммуномодулирующая терапия. В комплекс лечения включают витамины, десенсибилизирующие средства, лидазу, церебролизин и пр.
Имеются данные о положительном действии левамизола в терапии хронического токсоплазмоза. Левамизол назначается по 150 мг 3 дня подряд с перерывами 1 нед между циклами, всего 2 - 3 цикла.
Профилактика Токсоплазмоза:
Профилактика инфицирования токсоплазмами заключается в употреблении в пищу только хорошо термически обработанного мяса и мясопродуктов, чисто вымытых овощей, фруктов и ягод. В процессе приготовления пищи запрещается пробовать на вкус сырой мясной фарш. Необходимо тщательно мыть руки после обработки сырых мясопродуктов, работе в саду, огороде, детям после игры на детской площадке и, особенно, в песочнице. Следует тщательно соблюдать санитарно-гигиенические правила содержания в квартире домашних животных, не забывая мыть руки после контактов с ними.
При наступлении беременности каждая женщина должна быть обследована на токсоплазмоз в женской консультации. При выявлении у беременной клинических проявлений токсоплазмоза, а также обнаружение антител к токсоплазмам класса IgM, следует решить вопрос о необходимости лечения или прерывания беременности.
К каким докторам следует обращаться если у Вас Токсоплазмоз:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Токсоплазмоза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Токсоплазмоз при беременности – это паразитарное заболевание, вызванное проникновением T.gondii в организм беременной женщины. В большинстве случаев данная патология протекает бессимптомно, реже сопровождается гриппоподобным симптомокомплексом. Диагностика токсоплазмоза при беременности включает в себя серологическое исследование с определением IgM и IgG, ультразвуковое обследование плода и амниоцентез с последующим проведением ПЦР околоплодных вод. Вариант медикаментозного лечения зависит от инфицирования плода и может состоять из антибиотиков макролидного ряда или комбинации сульфаниламида и антагониста фолиевой кислоты.
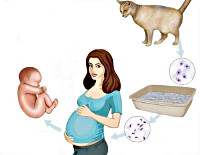
Общие сведения
Токсоплазмоз при беременности – это инфекционное заболевание, вызванное токсоплазмами, которое имеет большое значение в акушерстве и гинекологии за счет трансплацентарного пути передачи. Согласно статистике, порядка 15-25% женщин в возрасте от 15 до 45 лет инфицированы T.gondii. Общая частота врожденного токсоплазмоза составляет от 1 до 10 случаев на 10 000 новорожденных, из них 3-10% имеют тяжелые аномалии развития. При этом порядка 55% женщин, родивших инфицированных детей, не отмечали у себя каких-либо признаков заболевания. Как правило, более высокому риску развития токсоплазмоза при беременности подвержены женщины с иммунодефицитом и проживающие или путешествующие в эндемических зонах: Франции, Латинской Америке и южной Африке.

Причины токсоплазмоза при беременности
Возбудитель токсоплазмоза при беременности – Toxoplasma gondii. Она являет собой облигатного внутриклеточного паразита размером от 4 до 8 мкм. В зависимости от среды токсоплазма может находиться в трех формах: ооциста, тканевая циста и тахизоит. Первые две являются инвазивными для человека. Инфицирование цистами происходит при использовании зараженных мясных продуктов питания, ооцитами – при контакте с землей во время садовых работ или употреблении немытых овощей и фруктов. Токсоплазмы в форме ооцисты способны сохранять жизнеспособность длительное время, в особенности находясь в теплых и влажных условиях, что существенно повышает риск их передачами. При попадании в организм паразиты из инвазивных форм трансформируются в тахизоиты, которые обуславливают клинику заболевания и инфицирование плода на фоне токсоплазмоза при беременности.
Выделяют несколько вариантов пути заражения человека T.gondii – употребление в пищу сырого фарша или плохо термически обработанного мяса, контакт с испражнениями кошки или землей, содержащими ооцисты, трансплацентарная передача от матери к ребенку и переливание инфицированной крови. Значительная часть случаев (до 65%) токсоплазмоза при беременности возникает на фоне употребления инфицированных продуктов питания и воды, проходит в виде первичного инфицирования. При контакте с кошками основную опасность представляют питомцы, которые живут на улице или питаются сырым мясом.
Инфицированный человек может быть источником только в случае донорства крови или органов. Риск развития токсоплазмоза при беременности существенно возрастает при посещении регионов с высоким распространением токсоплазм: Франции, Латинской Америки и южной части Африки. Принято считать, что даже при единичном попадании в организм T.gondii человек остается инфицированным всю жизнь, а само заболевание протекает в субклинической форме. Однако только в отдельно взятых случаях токсоплазмоз при беременности вызывается активацией персистирующей инфекции.
Симптомы токсоплазмоза при беременности
Более чем 90% случаев токсоплазмоза при беременности протекает бессимптомно, в форме здорового носительства. Развитие выраженной клиники более вероятно у беременных с ослабленным иммунитетом – на фоне сопутствующих инфекционных или бактериальных заболеваний, употребления ГКС, ранних этапов СПИДа и т. д. Инкубационный период в таких случаях может колебаться от 1 до 3 недель после попадания паразита в организм. Для острого токсоплазмоза при беременности характерен гриппоподобный вариант течения: подъем температуры тела до 37,5-38°C, общая слабость и недомогание, головная боль, увеличение лимфатических узлов, реже – гепатоспленомегалия. У беременных редко возникает токсоплазмозный хориоретинит, еще реже – конъюнктивит, кератит или иридоциклит. Только на фоне выраженного дефицита иммунитета токсоплазмоз при беременности может вызывать тяжелые осложнения в виде энцефалита, гепатита, миокардита или пневмонии.
Токсоплазмоз относится к группе TORCH-инфекций, в которую входят инфекционные заболевания, способные оказывать тератогенное влияние. В основном опасность для плода представляет первичное заражение матери, хронический токсоплазмоз при беременности редко становится причиной внутриутробной передачи. Инфицирование происходит в промежутке от 1 до 4 месяцев после проникновения в плаценту тахизоитов, риск заражения возрастает со сроком гестации. Согласно статистике, частота передачи паразитов плоду на фоне отсутствия лечения токсоплазмоза при беременности в третьем триместре в 10-12 раз выше, чем в первом. Несмотря на это, чем раньше произошло инфицирование плода – тем хуже прогноз. При проникновении токсоплазм в организм плода в первом триместре могут наблюдаться спонтанные аборты, тяжелые аномалии развития. Более поздний врожденный токсоплазмоз проявляется тетрадой Сэбина: хориоретинит, водянка головного мозга, судорожный синдром, внутричерепная кальцификация. Также могут присутствовать выраженная задержка внутриутробного развития и микроцефалия. Их наличие свидетельствует о перенесенном остром токсоплазмозе при беременности.
Диагностика токсоплазмоза при беременности
Постановка диагноза токсоплазмоза при беременности основывается на анамнестических данных, выявленных симптомах, результатах лабораторных и инструментальных исследований. При сборе анамнеза акушером-гинекологом или инфекционистом выясняются все обстоятельства, при которых могло произойти инфицирование токсоплазмами: употребление сырого мяса, немытых овощей или фруктов, контакт с уличными кошками, работа с землей в саду, пребывание в эндемических зонах. Физикальный осмотр у женщин с токсоплазмозом при беременности может выявить гриппоподобный симптомокомплекс, но в подавляющем большинстве случаев он малоинформативен.
Ведущее место в диагностике токсоплазмоза при беременности играют серологические тесты, ультразвуковое сканирование и пункция амниотической оболочки плода. Лабораторная диагностика зачастую является первым шагом и реализуется она путем иммуноферментного анализа (ИФА) или специальных тест-систем. Суть этого исследования заключается в определении иммуноглобулинов класса М (IgM) и G (IgG). Их полное отсутствие опровергает диагноз токсоплазмоза при беременности. Наличие IgM и его нарастание в 4 раза и более указывает на первичное инфицирование T.gondii. Далее титр постепенно продолжает нарастать и достигает максимума через 5-20 дней после инвазии. Первое проявление IgG в крови матери наступает через 7-14 дней и достигает максимальной концентрации в промежутке от 3 до 6 месяцев. В большинстве случаев высокий уровень IgG свидетельствует о латентном течении токсоплазмоза при беременности. При получении позитивных результатов следует повторить исследование 3-4 раза в течение 2-3 недель.
Проведение УЗИ женщинам с подозрением на токсоплазмоз при беременности необходимо для оценки состояния плода. В большинстве случаев выявить какие-либо выраженные признаки врожденного токсоплазмоза не удается или присутствующих изменений недостаточно для подтверждения диагноза. К основным проявлениям инфицирования плода на фоне токсоплазмоза при беременности относятся общая задержка внутриутробного развития и нарушения структуры ЦНС – гидро- или микроцефалия, образование кальцификатов. Прерывание беременности рекомендуется только при обнаружении тяжелых морфологических аномалий.
Лечение токсоплазмоза при беременности
Лечение необходимо только в случаях острого токсоплазмоза при беременности, сопровождающегося клиническими проявлениями. При отсутствии клинических симптомов инфекции выздоровление наступает самостоятельно. В зависимости от поражения плода выделяют два направления медикаментозной терапии токсоплазмоза при беременности. При отсутствии признаков заражения плода по результатам ПЦР амниотической жидкости используются антибиотики макролидного ряда (спирамицин). Данные средства способны накапливаться в тканях плаценты и предотвращать вертикальный путь передачи.
При подтверждении или подозрении на инфицирование плода на фоне токсоплазмоза при беременности фармакотерапия должна состоять из антагониста фолиевой кислоты (пириметамин) и сульфаниламида (сульфадиазин). Первый способен подавлять деление клеток в костном мозге, поэтому его назначение всегда дополняется препаратами фолиевой кислоты. Также использование препарата противопоказано в I триместре беременности в связи с потенциальным тератогенным эффектом. Такой вариант лечения направлен на снижение тяжести заболевания у ребенка и улучшение общего прогноза.
Прогноз и профилактика токсоплазмоза при беременности
Прогноз для женщины на фоне токсоплазмоза при беременности благоприятный. Практически все случаи заканчиваются клиническим выздоровлением. Прогноз для будущего ребенка напрямую зависит от триместра, в котором произошло инфицирование – проникновение паразитов в организм плода в I триместре связано с высоким риском спонтанного аборта или тяжелых аномалий развития.
Профилактика токсоплазмоза при беременности подразумевает разрыв всех механизмов передачи инфекции и скрининг беременных. Первая часть превентивных мер включает в себя употребление только чистой воды и продуктов, прошедших качественную термическую обработку, ограничение работы с землей и контакта с кошками, тщательное мытье овощей и фруктов и т. д. Скрининг токсоплазмоза показан только беременным с высоким риском заражения и включает в себя ежемесячный серологический контроль.
Токсоплазмоз - зоонозная протозойная инфекция, имеющая длительное течение и приводящая к поражению нервной, лимфатической, зрительной, мышечной систем, миокарда, печени, селезенки. Острый токсоплазмоз протекает с лихорадочно-интоксикационным синдромом, лимфаденопатией, гепатоспленомегалией, кожными высыпаниями; в тяжелых случаях – с развитием миокардита, энцефалита, энцефаломиелита. Диагноз токсоплазмоза устанавливается с помощью бактериологического посева, ПЦР, ИФА. Лечение токсоплазмоза включает прием этиотропных антипаразитарных препаратов, десенсибилизирующих, общеукрепляющих средств, иммунотерапию токсоплазмином.
МКБ-10
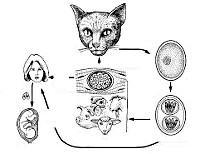
Общие сведения
Токсоплазмоз – хроническая паразитарная инвазия, вызываемая внутриклеточными простейшими (токсоплазмами) и сопровождающаяся развитием лимфаденита, гепатита, менингоэнцефалита, пневмонии, миокардита, миозита и др. Показатель инфицированности населения токсоплазмозом чрезвычайно высок: в Европе и Северной Америке он составляет 25-50%; в странах Африки, Южной и Латинской Америки – до 90%.
Огромную опасность токсоплазмоз представляет для беременных женщин и лиц со сниженным иммунитетом. В первом случае может происходить внутриутробное инфицирование плода с самопроизвольным прерыванием беременности, мертворождением или формированием эмбрио- и фетопатий; во втором - токсоплазмоз приобретает тяжелое манифестное течение. Учитывая множественные и разнообразные клинические проявления, токсоплазмоз актуален не только для инфекционных болезней, но также для неврологии, офтальмологии, пульмонологии, кардиологии.

Причины токсоплазмоза
Инфекционным агентом, приводящим к заболеванию, выступает Toxoplasma gondii (токосплазма), принадлежащая к роду облигатных внутриклеточных микроорганизмов, отряду кокцидий, классу споровиков. Токсоплазма имеет изогнутую форму полумесяца, один конец которого заострен, а другой более закруглен, длину 4-7мкм и ширину 2-5 мкм. В своем развитии возбудитель токсоплазмоза проходит фазы полового и бесполого размножения и стадии трофозоитов, цист и ооцист.
Половой цикл протекает в эпителиальных клетках кишечника представителей семейства кошачьих (домашних кошек, рыси, ягуара, пумы и др.), которые выступают окончательными хозяевами токсоплазм. Здесь образуются гаметоциты, которые затем дифференцируются в мужские и женские гаметы; при их слиянии формируется зигота, а затем ооциста. С испражнениями кошек ооцисты выделяются во внешнюю среду, где превращаются в инвазивные формы – спорозоиты.
Инфицирование токсоплазмозом чаще всего происходит алиментарным путем при употреблении в пищу продуктов, обсемененных ооцистами, а также сырого мяса инфицированных животных; реже – контактным путем через поврежденную кожу. При беременности возможна вертикальная передача инфекции плоду через плаценту. Реже заражение токсоплазмозом происходит парентеральным путем (при переливании крови или трансплантации органов).
Патогенез
Попав в организм человека через ЖКТ, ооцисты внедряются в энтероциты нижних отделов тонкой кишки, откуда проникают в мезентериальные лимфоузлы, вызывая их воспаление (мезаденит), некроз, кальцификацию и образование специфических гранулем. Из первичного лимфатического очага токсоплазмы попадают в кровь и гематогенным путем разносятся по организму, где фиксируются в органах-мишенях: печени, селезенке, миокарде, ЦНС, оболочках глаз, скелетной мускулатуре, вызывая формирование некрозов, гранулем, нарушение функции пораженных органов.
Жизнедеятельность токсоплазм сопровождается выделением аллергенов и токсинов, что находит выражение в развитии общеинфекционного и аллергического синдромов. По мере выработки специфических антител вегетативные формы токсоплазм инцистируются, что знаменуется переходом токсоплазмоза в хроническую форму. При снижении активности иммунной системы (у больных СПИДом, гематологических и онкологических больных) возможна реактивация инфекции с генерализованным течением.
Симптомы приобретенного токсоплазмоза
С учетом характера инфицирования различают врожденный и приобретенный токсоплазмоз. Приобретенная инфекция может протекать в острой, хронической и латентной форме; при этом латентная форма подразделяется на первичную и вторичную, развивающуюся после острого или рецидива хронического токсоплазмоза.
Латентная форма
Примерно у 95-99% людей токсоплазмоз протекает в виде латентной инфекции. При острой манифестной форме токсоплазмоза инкубационный период составляет 2-3 недели. Легкое и субклиническое течение токсоплазмоза обычно диагностируется ретроспективно по положительным результатам кожных проб с токсоплазмином, серологическим реакциям, кальцифицированным лимфоузлам и другим признакам.
Генерализованная форма
Хроническая форма
Хронический токсоплазмоз характеризуется длительным торпидным течением. Общие симптомы включают субфебрилитет, недомогание, похудание, генерализованные артралгии, лимфаденопатию. Проявлениями мезаденита служат диспепсические расстройства: тошнота, метеоризм, боли в животе, запор. Специфическими признаками хронического токсоплазмоза выступает поражение мышечной ткани, проявляющееся миозитом. Поражение сердца вызывает развитие очаговых или диффузных изменений миокарда или перикардита, проявляющихся утомляемостью, сердцебиением, одышкой, кардиалгиями.
Со стороны нервной системы отмечаются явления астении и вегето-сосудистой дистонии, неврастенические реакции и фобии. Многолетнее хроническое течение токсоплазмоза приводит к развитию эпилепсии, психических расстройств, снижению интеллекта. Эндокринные расстройства могут включать импотенцию, нарушение менструального цикла, вторичную надпочечниковую недостаточность. Поражение глаз при токсоплазмозе протекает в форме прогрессирующей близорукости, увеита, ретинита и хориоретинита с атрофией зрительного нерва.
Симптомы врожденного токсоплазмоза
Течение и исходы врожденного токсоплазмоза зависят от гестационного возраста плода. Инфицирование в I и II триместре приводит к внутриутробной гибели плода или формированию внутриутробных пороков – бластопатий, эмбрио- и фетопатий. В случае более позднего внутриутробного заражения (в III триместре) ребенок рождается с хронической, подострой или острой формой токсоплазмоза; при этом, чем позднее происходит инфицирование, тем тяжелее выражены симптомы на момент рождения.
Состояние новорожденных с острой формой токсоплазмоза тяжелое с первых дней. Отмечается фебрильная температура тела, выраженная интоксикация, обильные полиморфные высыпания на коже, генерализованная лимфоаденопатия, кровоизлияния в слизистые оболочки и склеры. Печень и селезенка обычно увеличены, часто развивается желтуха, диспепсические расстройства. Острый токсоплазмоз у новорожденных может приводить к развитию пневмонии, миокардита, энцефалита, менингоэнцефалита и летальному исходу. Подострое и хроническое течение токсоплазмоза характеризуется гидроцефалией, судорожным синдромом, длительной желтухой, субфебрилитетом, хориоретинитом.
В отдаленном периоде выявляются стойкие необратимые изменения, обусловленные внутриутробным инфицированием. Такими последствиями могут служить отставание в физическом развитии, задержка психического и речевого развития (ЗПР и ЗРР), микроцефалия, олигофрения, эпилепсия, микрофтальмия, слепота, тугоухость, глухота. Эти и другие нарушения расцениваются как резидуальный токсоплазмоз. Врожденный токсоплазмоз может иметь длительное латентное течение с клинической манифестацией на 2-7 году жизни ребенка.
Диагностика токсоплазмоза
В диагностике внутриутробного инфицирования большая роль отводится акушерскому анамнезу, результатам анализа на TORCH-инфекции у матери и серологических реакций у новорожденного, исследованию околоплодных вод и плаценты методом ПЦР. Дети нуждаются в наблюдении педиатра, детского офтальмолога, отоларинголога, невролога; проведении люмбальной пункции, КТ головного мозга, нейросонографии. Врожденный токсоплазмоз нужно дифференцировать с врожденной краснухой, герпесом, листериозом, цитомегалией, хламидийной инфекцией, внутричерепной родовой травмой.
Среди клинических проявлений наибольшее диагностическое значение при приобретенном токсоплазмозе имеет сочетание лимфаденопатии, гепатоспленомегалии, поражения глаз и ЦНС. Обязательно консультирование больного неврологом, офтальмологом, терапевтом или кардиологом. Основной перечень инструментальных исследований включает ЭЭГ, Эхо-ЭГ, рентгенографию или КТ черепа, офтальмоскопию, ЭКГ.
Для лабораторного подтверждения токсоплазмоза используются паразитологические и иммунологически методы. Первые предполагают микроскопическое выявление возбудителя в мазках-отпечатках пораженных органов, биоптате лимфоузлов, крови или спинномозговой жидкости. Возможно проведение биологической пробы с заражением лабораторных грызунов. Иммунологическая диагностика токсоплазмоза включает серологические методы (РСК, РНИФ, ИФА, РНГА), а также внутрикожную аллергическую пробу с токсоплазмином. В случае приобретенной инфекции в первую очередь исключается туберкулез, лимфогранулематоз, ревматизм, болезнь кошачьих царапин, инфекционный мононуклеоз, герпесвирусная инфекция.
Лечение токсоплазмоза
В зависимости от преимущественных органных поражений, лечение больных токсоплазмозом осуществляется в профильных отделениях: неврологических, терапевтических, кардиологических, офтальмологических и т. д. Этиотропная терапия при манифестном токсоплазмозе проводится препаратами противопаразитарного действия: чаще хлоридином в комбинации с сульфаниламидными препаратами или антибиотиками тетрациклинового ряда; при противопоказаниях - метронидазолом, хлорохином, аминохинолом. Обычно курс лечения токсоплазмоза состоит из 3-х 5-10-дневных циклов, повторяемых с интервалами 7-10 дней. Дополнительно назначаются антигистаминные и общеукрепляющие средства, поливитамины. При хроническом токсоплазмозе медикаментозный курс лечения дополняется иммунотерапией – внутрикожным введением токсоплазмина. Тактика ведения беременных с первично-хроническим или первично-латентным токсоплазмозом предполагает проведение химиопрофилактики спирамицином. При острой форме токсоплазмоза у беременной рекомендуется медицинский аборт.
Профилактика
Профилактика заражения человека токсоплазмозом включает комплекс ветеринарных (обследование и лечение домашних животных) и санитарно-гигиенических мероприятий. Последние предполагают избегание тесного контакта с кошками, тщательную термическую обработку мяса, защиту детских песочниц от испражнений безнадзорных животных, соблюдение мер личной гигиены. Обследование беременных на токсоплазмоз проводится трижды, в каждом триместре.
Врожденный токсоплазмоз – это паразитарная патология, которая возникает при трансплацентарном инфицировании ребенка Toxoplasma gondii. У большинства детей протекает бессимптомно. Возможные проявления заболевания: интоксикационный синдром, пятнисто-папулезная сыпь, лимфаденопатия, желтуха, гепатоспленомегалия, отеки нижних конечностей. Часто провоцирует развитие патологий органа зрения, слуха, ЦНС; реже – миокарда, легких и печени. Антенатальная диагностика базируется на проведении биопсии, постнатальная – на совокупности анамнестических и клинико-лабораторных данных (ИФА, ПЦР). Этиотропное лечение врожденного токсоплазмоза проводится при помощи схем на основе препаратов пириметамина и сульфадимезина или спирамицина.
МКБ-10
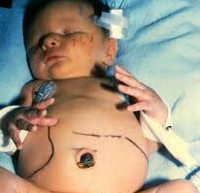
Общие сведения
Врожденный токсоплазмоз – заболевание в педиатрии и неонатологии, возникающее в результате трансплацентарного заражения плода на фоне острой формы токсоплазменной инфекции у матери. Впервые Toxoplasma gondii была описана французами К. Николь и Л. Монсо в 1908 году. В 1939 г. американцы Э. Вольф, Д. Кауэн и Б. Пэйдж подтвердили трансплацентарный механизм передачи возбудителя. Промежуточными хозяевами могут выступать более 400 видов животных. Согласно статистическим данным ВОЗ, число инфицированных токсоплазмой людей в мире составляет порядка 1,5 млрд. человек, в России – около 30% всего населения. Частота врожденной формы 1,5:1000 новорожденных. Даже на фоне лечения средний показатель смертности у детей до 5 лет составляет 12%, осложнения возникают почти у 90%.

Причины врожденного токсоплазмоза
Врожденный токсоплазмоз развивается только при инфицировании матери Toxoplasma gondii во время вынашивания ребенка. Механизм заражения беременной женщины – фекально-оральный. Наиболее распространенные причины: контакт с животными из семейства кошачьих и употребление термически необработанной пищи. Инвазивная форма возбудителя – ооциста – формируется в кишечнике животных и выделяется с калом, после чего может на протяжении 12 и больше месяцев сохранять контагиозность в условиях внешней среды. В крайне редких случаях этиологическим фактором может стать трансплантация контаминированных органов или переливание крови. Заражение плода T. gondii происходит трансплацентарным путем. После рождения ребенка развивается интенсивный гемолиз, возникают геморрагии на слизистых оболочках, расширение камер сердца, пневмония или интерстициальный отек легких, некроз печени и селезенки, увеличение лимфоузлов, воспаление и отек тканей головного мозга, некробиоз сетчатки. При гистологическом исследовании непосредственно пораженных тканей определяется некроз, гранулематозная или диффузная пролиферация ретикулоцитов, инфильтрация плазмоцитами и лимфоцитами, перифокально – множество токсоплазм. Впоследствии на месте некротизированных участков формируется фиброз, переходящий в кальциноз.
Классификация врожденного токсоплазмоза
В зависимости от периода инфицирования плода врожденный токсоплазмоз может протекать в трех формах:
- Хроническая форма. Заражение происходит в I-II триместрах беременности. Риск передачи возбудителя – 13-18%. При такой форме могут развиваться атрофия головного мозга, гидроцефалия, деформация желудочков мозга, анофтальмия, колобома, атрофия сетчатки, врожденные пороки сердца и других органов и систем.
- Подострая форма. Инфицирование – III триместр. Риск заражения ребенка – 75-85%. Проявления могут включать в себя энцефалит, менингоэнцефалит, очаговый некроз сетчатки, увеит.
- Острая форма. Токсоплазма попадает в организм ребенка непосредственно перед родами. Возможные симптомы: гипертермия, пятнисто-папулезная сыпь, интенсивная желтуха, гепатоспленомегалия, анемия, миокардит, пневмония.
Симптомы врожденного токсоплазмоза
Врожденный токсоплазмоз может проявляться в различные периоды жизни ребенка – от первых дней до нескольких месяцев. Специфических симптомов данное заболевание не имеет. Зачастую присутствующая клиника нечеткая и имитирует другие врожденные патологии. Наиболее вероятные проявления врожденного токсоплазмоза: ухудшение общего состояния, пятнисто-папулезная сыпь различной локализации, генерализованная лимфаденопатия, увеличение печени и селезенки, желтуха, отеки нижних конечностей, субфебрильное повышение температуры тела. Тяжесть симптомов зависит от степени инфицирования токсоплазмами, триместра беременности, в котором произошло инфицирование, и иммунных сил матери. Примерно 70-90% детей не имеют каких-либо проявлений в ранние периоды жизни, но почти у всех спустя некоторое время возникают осложнения. Классический врожденный токсоплазмоз проявляется триадой Сэбина – обструктивная гидроцефалия, хориоретинит и массивное внутричерепное обызвествление. Наблюдается данный комплекс не более чем у 3% детей. Помимо триады, часто возникают миокардит, миозит, гепатит и пневмония. Клинические проявления напрямую зависят от присутствующих патологических изменений. Вероятность развития поздних осложнений на фоне латентного врожденного токсоплазмоза составляет порядка 90%. Период возникновения может быть разным – от нескольких месяцев до нескольких лет. Наиболее часто наблюдается поражение глаз, органа слуха и ЦНС. Самое распространенное осложнение – ретинит (примерно 85% случаев). К другим последствиям перенесенного врожденного токсоплазмоза относят олигофрению, гидроцефалию, повышение внутричерепного давления, острый и хронический энцефалит, эпилепсию, полную глухоту и/или слепоту, микрофтальм, увеит, хроническую гипертермию, редко – шизофрению.
Диагностика врожденного токсоплазмоза
Диагностика врожденного токсоплазмоза может проводиться в антенатальном и постнатальном периоде. Антенатальное исследование подразумевает использование инвазивных методов с дальнейшими лабораторными анализами. Абсолютное показание к их проведению – острый токсоплазмоз матери в сумме с нарушениями развития плода по результатам акушерского УЗИ. Выбор методики исследования зависит от срока беременности. При гестации от 10 недель проводится биопсия хориона, от 16 недель – амниоцентез, от 18 – кордоцентез. Для верификации инфекции полученный материал исследуют при помощи ПЦР. Постнатальная диагностика включает в себя сбор анамнестических данных и проведение клинического и лабораторного исследования. Данная мера является обязательной для всех детей, входящих в группу риска внутриутробного инфицирования. Неспецифическая диагностика и ее результаты зависят от присутствующих симптомов и синдромов. Список исследований может включать в себя ОАК (анемия, тромбоцитопения, лейкоцитоз); рентгенографию ОГК (признаки инфильтрации легких); нейросонографию и КТ головного мозга; биохимическое исследование крови с измерением АЛТ и АСТ, определением СРБ, уровня билирубина и его фракций (все показатели выше нормы); офтальмоскопию (некроз сетчатки); спинномозговую пункцию (признаки воспаления). Специфические методы подразумевают серодиагностику биологических жидкостей методом ИФА, при котором наблюдается возрастание титра антител IgG в 4 и больше раз и высокий уровень IgM на протяжении 10-14 суток. При необходимости проводится ПЦР с целью идентификации ДНК токсоплазмы.
Лечение врожденного токсоплазмоза
Лечение новорожденного с выраженной клинической картиной врожденного токсоплазмоза проводится только в условиях стационара, в отделении патологии новорожденных. Соблюдение специфического режима и рациона не требуется, их коррекция проводится в соответствии с состоянием ребенка. При наличии отягощенного анамнеза матери этиотропную терапию начинают с момента постановки предварительного диагноза. В других случаях перед началом лечения требуется проведения лабораторных методов исследования. Используемые схемы: пириметамин и сульфадимезин на 1-1,5 месяца; спирамицин или другие макролиды на 4-6 недель. В некоторых случаях применяют системные глюкокортикостероиды – преднизолон. Симптоматическое лечение зависит от присутствующих симптомов и синдромов, выявленных педиатром или неонатологом. При стойком повышении внутричерепного давления или развитии гидроцефалии показано хирургическое лечение. При необходимости дальнейшее лечение может проводиться амбулаторно под контролем педиатра, инфекциониста и других специалистов. В таких же условиях проводится терапия субклинической и латентной формы врожденного токсоплазмоза. Решение об отказе от приема препаратов принимается на основе клинико-лабораторных показателей, находящихся в пределах возрастной нормы, и заключения всех лечащих врачей.
Прогноз и профилактика врожденного токсоплазмоза
Прогноз при врожденном токсоплазмозе зависит от триместра, в котором произошло инфицирование плода и тяжести клинических проявлений. При развитии патологии в I триместре может наблюдаться самопроизвольное прерывание беременности и выкидыш или дальнейшее развитие тяжелых форм заболевания, однако аномалии органов при этом не возникают. При адекватной и своевременной терапии прогноз для жизни благоприятный, для выздоровления – сомнительный. Неспецифическая профилактика врожденного токсоплазмоза включает в себя ограничение контакта домашних животных с беременной женщиной, соблюдение гигиенических норм, прием в пищу только термически обработанных продуктов, тщательное мытье овощей и фруктов. При наличии факторов, указывающих на возможное инфицирование матери, проводится специфическая диагностика, направленная на идентификацию T. gondii. При подтверждении диагноза показано немедленное проведение этиотропной терапии. Специфической профилактики врожденного токсоплазмоза не разработано.
Токсоплазмоз – это одна из TORCH-инфекций, инфекций которые связаны одним единственным признаком - возбудители могут передаваться внутриутробно: от матери к ребенку. Данные инфекции нередко являются причиной проблем с вынашиванием беременности и виновниками врожденных пороков развития у малыша.
Что провоцирует / Причины Токсоплазмоза у беременных:
Актуальность проблемы токсоплазмоза определяется высокой инфицированностью населения паразитом Toxoplasma gondii. Распространенность токсоплазмоза широко варьирует в зависимости от особенностей питания в тех или иных странах. Так, во Франции более 70 % женщин заражаются токсоплазмой до беременности и приобретают иммунитет еще до зачатия. Несмотря на это, подсчитано, что во Франции 1 из 140 женщин заболевает токсоплазмозом во время беременности, тогда как в Великобритании эта величина значительно ниже и составляет 1:400 женщин.
Токсоплазма является внутриклеточным паразитом из класса Sporozoa, основным хозяином которого являются животные семейства кошачьих. В эпителии кишечника кошек происходит половое размножение паразита с образованием ооцист, которые в острую фазу инфекции выделяются с испражнениями и длительно сохраняются в почве. Алиментарным путем ооцисты попадают в кишечник промежуточных хозяев - травоядных и плотоядных животных, в том числе и человека. В результате неполового деления образуется тахизоит - паразит размером 4-7 мкм, способный мигрировать и размножаться в клетках различных органов (ЦНС, лимфоидных, мышечных и др.), где быстро формируются псевдоцисты и цисты. В цистах паразит в форме брадизоита может находиться пожизненно в состоянии vita minima, активизируясь в случае значительного снижения иммунитета.
Патогенез (что происходит?) во время Токсоплазмоза у беременных:
Клеточный и гуморальный иммунитет обеспечивает надежную и пожизненную защиту от повторного инфицирования и активации брадизоитов, находящихся в цисте. Иммуногенез, в частности непрерывная продукция антител, индуцируется за счет контакта клеток иммунной системы с цистными антигенами паразита, такой иммунитет называется нестерильным. Состояние клеточного звена иммунитета учитывают только при манифестных формах заболевания.
Человек заражается тканевыми цистами при употреблении полусырого мяса или ооцистами - при употреблении немытых овощей либо непосредственно от кошек. Возможна трансплацентарная передача инфекции. До 80 % населения инфицированы токсоплазмами, они находятся в стадии латентной токсоплазменной инфекции. Риск инфекции в течение 9 мес беременности для серонегативных женщин составляет примерно 1 %.
Имеются 4 пути заражения человека токсоплазмозом.
- Прием через рот цист в мясе и колбасных изделиях, не подвергнутых достаточной термической обработке.
- Пероральное поступление ооцист в организм через продукты питания (например, салат), воду, а также через предметы и почву, которые загрязнены кошачьим калом (например, во время работы в саду); заразным кошачий кал становится только на 3-й день после экстракорпорального созревания.
- Трансплацентарная передача плоду во время острой токсоплазменной инфекции у будущей матери.
- Трансплантация органов и гемотрансфузии. Повреждение клетки паразитом приводит к ограниченному и/или генерализованному воспалению: лимфадениту, энцефалиту, гепатиту, миозиту, миокардиту. Выраженность воспалительных изменений бывает разной и, как правило, незначительной, но во всех случаях преобладает некроз с последующим фиброзом и кальцинацией ткани. В период острого процесса и цитолиза свободные формы (тахизоиты) находятся вне клеток, циркулируют в жидких средах организма, где атакуются фагоцитами с последующей быстрой элиминацией из крови.
Инфицирование и паразитемия в большинстве случаев бессимптомны, и только примерно у 10 % инфицированных людей отмечается малосимптомная картина заболевания: головная боль, небольшая лихорадка, локальный лимфаденит, легкий миозит. В редких, более тяжелых, случаях заболевание сопровождается генерализованной лимфаденопатией, пятнистой сыпью, мигрирующей артралгией и гепатоспленомегалией. Тяжелые варианты заболевания (миокардит, пневмония, увеит, хориоретинит) встречаются только у взрослых с иммунодефицитами и внутриутробно инфицированных детей.
Риск инфицирования плода значителен при первичном инфицировании беременной паразитом. Иммунитет женщины, инфицированной до беременности, надежно предохраняет плод при повторных контактах с токсоплазмой в случае возможной реинфекции в период беременности, за исключением редко встречающихся иммунодефицитных состояний. Число неиммунных беременных в России составляет 60-70 %. Во время беременности инфицируется около 11% женщин, которые в 30-40 % случаев передают инфекцию плоду. Таким образом, инфицируется 1 из 1000 плодов.
Для решения вопросов о профилактике и лечении токсоплазмоза плода и ребенка необходима своевременная диагностика инфицирования беременной, что возможно на основании результатов повторных серологических исследований, проведенных в определенные сроки беременности.
При заболевании в I и во II триместрах риск самопроизвольного аборта и преждевременных родов достигает 10-15 %. Риск врожденного токсоплазмоза и его тяжесть зависят от срока заражения беременной: чем раньше произошло заражение, тем меньше риск заболевания и больше выраженность проявлений. Так, при заражении матери в III триместре риск врожденного токсоплазмоза составляет 75-90 %, при этом у 90 % новорожденных заболевание протекает бессимптомно. При заражении же в I триместре риск врожденного токсоплазмоза всего 10-25 %, однако заболевание в 65 % случаев протекает в тяжелой форме. Если же женщина заразилась токсоплазмозом до беременности, то врожденный токсоплазмоз у ее будущего ребенка вообще маловероятен.
При внутриутробном заражении токсоплазмозом возможны смерть плода и преждевременные роды. Среди ранних проявлений врожденного токсоплазмоза следует отметить ЗВУР, микроцефалию, внутричерепные кальцификаты, гидроцефалию, хориоретинит, гепатоспленомегалию, желтуху и тромбоцитопению. Поздние проявления - задержка психического развития и эпилептические припадки. Лечение беременной снижает риск врожденного токсоплазмоза на 60 %.
При первичной инфекции у матери плод инфицируется или непосредственно, или косвенно от очагов токсоплазмоза в плаценте. После латентного периода инфекция может перейти от матери к плоду. Риск инфицирования и заболевания плода зависит от срока беременности. В ранние сроки беременности инфекция от матери к плоду переходит редко и медленно, в поздние сроки ребенок инфицируется быстрее и с более высокой вероятностью.
Только в редких случаях инфекция беременной ведет к инфицированию ребенка в I триместре. Хотя такие дети тяжело поражены, у них не отмечается аномалий закладки органов. Эмбриопатии, обусловленные токсоплазмой, у человека неизвестны, хотя имеются данные о токсическом нарушении эмбриогенеза в результате хорионита без непосредственного контакта паразита с эмбрионом. Для объяснения этого феномена есть две гипотезы: либо инфекция эмбриона ведет к выкидышу в ранние сроки, либо возбудитель переходит от матери к плоду из-за своего внутри-маточного латентного периода только после окончания периода эмбриогенеза и у ребенка есть возможность пережить инфекцию.
Симптомы Токсоплазмоза у беременных:
Заболевание часто протекает бессимптомно. Иногда по клиническому течению оно напоминает инфекционный мононуклеоз с появлением атипичных лимфоцитов в мазке крови и крайне редко приводит к скоротечно текущему пневмониту или летальному энцефаломиелиту. Как при врожденном, так и при приобретенном токсоплазмозе возможно поражение глаз в виде хориоретинита. Инфицирование детей и взрослых с недостаточностью иммунитета может вызвать генерализованный или локальный процесс с необратимыми последствиями. При ВИЧ-инфекции по мере нарастания иммунодефицита возможна реактивация токсоплазмоза, проявляющаяся множественными абсцессами головного мозга.
Размножение возбудителя ведет к воспалительным реакциям с некрозом и обызвествлением тканей. В более ранний период фетального развития при недостаточной собственной иммунокомпетентности ребенка или при массивной инфекции возможно очень сильное размножение возбудителя в плоде с гидроцефалией, асцитом, гепатозом. С тропизмом паразита к ЦНС связаны поражения мозга (менингоэнцефалит) и глаз (хориоретинит). Возможны генерализованный токсоплазмоз и поражение отдельных паренхиматозных органов (гепатит, миокардит). Если воспалительный процесс не приводит к выкидышу, то при рождении наблюдают остаточные явления: фиброзно-склеротические изменения в органах с их деформацией и нарушением функции - так называемые ложные пороки развития.
Поздняя фетопатия может проявляться широким спектром клинических признаков - от легких до крайне тяжелых вариантов. Клинически выраженные формы характеризуются лихорадкой, лимфаденитом, гепатоспленомегалией, желтухой, судорогами, анемией, тромбоцитопенией, экзантемой. Есть данные, что бессимптомные и субклинические формы также не проходят бесследно: у ряда детей спустя годы находят неврологические отклонения, последствия хориоретинита, глухоту, отставание в психическом развитии.
Диагностика Токсоплазмоза у беременных:
Если в крови беременной выявлены IgM-антитела, то это могут быть следующие ситуации:
- острая или недавно перенесенная инфекция, значимая для беременности;
- подъем специфических IgM-антител из-за нового интестинального контакта с токсоплазмой (локальная реинфекция?) или клинически значимое реактивирование;
- неспецифическая IgM-реакция (так называемые естественные IgM-антитела к токсоплазменным антигенам).
Нельзя оценивать позитивный IgM-тест при первом исследовании беременной без дальнейшего отбора признаков значимой для беременности инфекции. IgM-антитела персистируют, как правило, год, а часто даже 2-3 года. В каждом подобном случае необходимо исследование парных сывороток.
При сонографических данных, позволяющих предположить повреждение ребенка при токсоплазмозе в случае острой токсоплазменной инфекции у беременной, рекомендуется пренатальная диагностика. В большинстве случаев имеется относительное показание: при острой токсоплазменной инфекции у матери необходимо выяснить, не перешла ли инфекция на ребенка с нормальными данными сонографического исследования. При амниоцентезе исследуют околоплодные воды, при кордоцентезе - кровь.
Со времени инфицирования до момента исследования должно пройти не менее 4 нед (срок определяют по серологическим данным), потому что при более ранней пункции возбудитель, возможно, еще не достиг околоплодных вод и вероятен ложнонегативный результат. Пункцию делают не ранее 16 нед беременности. Нельзя до исследования проводить сочетанную терапию пириметамином и сульфадиазином, иначе возможны ложнонегативные результаты ПЦР. Если выявлена фетальная инфекция и одновременно имеются сонографические признаки повреждения у ребенка, с родителями следует обсудить возможность прерывания беременности. Если беременность без заметных отклонений со стороны плода не прервана, то проводят курсы терапии до родов и в течение первых 12 мес жизни ребенка (четырехнедельная комбинированная терапия пириметамином, сульфадиазином и фолиевой кислотой попеременно с четырехнедельной терапией ровамицином). После родов исследуют пуповинную кровь, плаценту методом ПЦР и сравнивают серологические пробы матери и ребенка.
Основные положения пренатальной диагностики токсоплазмоза следующие.
- Пренатальная диагностика необходима в следующих ситуациях:
- абсолютное показание: в случае острой токсоплазменной инфекции у беременной и данных УЗИ, позволяющих предположить повреждение плода;
- относительное показание: при острой токсоплазменной инфекции у беременной и "нормальных" данных УЗИ плода.
- со времени инфицирования до момента исследования должно пройти не менее 4 нед (для уменьшения количества ложноотрицательных результатов);
- амниоцентез проводят не ранее 16 нед беременности;
- нельзя до исследования проводить сочетанную терапию пириметамином и сульфадиазином (для уменьшения количества ложноотрицательных результатов).
Лечение Токсоплазмоза у беременных:
Лечение токсоплазмоза эффективно в периоды циркуляции в крови внецистных форм паразита, внутриклеточного деления тахизоитов с последующей паразитемией при остром и персистирующем процессе; на цистные формы (брадизоиты) препараты не действуют. В полной санации от паразита нет необходимости, так как цистные формы (носительство) обеспечивают нормальный нестерильный иммунитет.
Наиболее эффективны препараты пириметамина в комбинации с сульфаниламидами. Препараты блокируют функцию ферментов (редуктазы и синтетазы), участвующих в синтезе фолиевой кислоты паразита. Побочные действия всех антифолатов устраняют назначением фолиевой кислоты. На втором месте по эффективности стоят макролиды, тормозящие синтез белка на рибосомах возбудителя, учитывают также их меньшую токсичность и действие на внутриклеточные формы паразита.
При латентном токсоплазмозе (положительные результаты серологических проб в отсутствие клинических проявлений) лечение не проводят. Хотя при заражении в I триместре беременности риск врожденного токсоплазмоза невысок, в связи с возможностью тяжелого поражения плода показано прерывание беременности. Индивидуально решаются вопросы о прерывании беременности и предупреждении больной о потенциальной опасности химиотерапии, а также получения от нее письменного согласия на такое лечение.
В случае настойчивого желания женщины пролонгировать беременность в I триместре необходима терапия спирамицином. Начиная со II триместра при остром токсоплазмозе назначают пириметамин в сочетании с сульфаниламидами и чередуют их с курсами спирамицина. Терапию проводят до окончания беременности. В III триместре сульфаниламиды отменяют за 2 нед до предполагаемых родов во избежание конкурентозависимой гипербилирубинемии. Для устранения побочного действия пириметамина и сульфаниламидов (подавление функции костного мозга) назначают фолиевую кислоту до 5 мг/сут.
Схема лечения острого токсоплазмоза во время беременности следующая.
- С момента установления диагноза и до 15 нед: ровамицин 9 000000 ME в сутки.
- С 16 до 36 нед независимо от предшествующей терапии ровамицином проводят 4-недель-ную комбинированную терапию фолиевой кислоты: сульфаниламиды 4 г (по 1 г 4 раза в день), пириметамин - 1-й день 50 мг, затем 25 мг в день, лейковорин по 10-15 мг в день.
- С 36 нед и до конца беременности из-за опасности гемолиза и желтухи у новорожденного сульфадиазин заменяют ровамицином.
- Необходим еженедельный контроль клинического анализа крови и общего анализа мочи.
- Новорожденного обследуют (серология, клинические данные), при подтверждении врожденного токсоплазмоза проводят терапию чередующимися 4-недельными курсами под контролем неонатолога, офтальмолога, невропатолога, инфекциониста.
Профилактика Токсоплазмоза у беременных:
Профилактику внутриутробного токсоплазмоза следует проводить с учетом того факта, что только первичное заражение женщины во время беременности может привести к инфицированию плода. Методы профилактики подразделяют на санитарные и специальные методы. Первые включают информацию о соблюдении следующих правил: не пробовать сырой фарш, употреблять только термически хорошо обработанное мясо, тщательно вымытые фрукты, овощи, зелень, санировать кошачьи испражнения, следить за чистотой рук, работая в саду.
Специальные методы состоят в обследовании с использованием диагностического алгоритма всех женщин перед беременностью и во время беременности. При первом обращении беременной к врачу исследуют титр антител к Toxoplasma gondii. При положительном результате в том же образце сыворотки определяют содержание специфических IgM для исключения острой инфекции. При их обнаружении назначают лечение или рекомендуют прервать беременность. В отсутствие специфических антител обследование повторяют на 10-12-й неделе и 20-22-й неделе, так как серонегативные беременные будут составлять группу риска по острому токсоплазмозу.
За инфицированными, но "практически здоровыми детьми", родившимися от матерей с точно установленным первичным инфицированием во время беременности, необходимо диспансерное наблюдение до 10-летнего возраста, включающее регулярное клинико-лабораторное обследование для выявления возможной трансформации инфицирования в заболевание.
Основные положения профилактики врожденного токсоплазмоза следующие.
- Первичная профилактика - просвещение серонегативных по токсоплазмозу беременных:
- хорошая термическая обработка мяса и мясных изделий;
- тщательная обработка кипяченой водой салатов и фруктов;
- если у беременной дома есть кошка, необходимо применять консервированный или сухой корм, кошку держать в квартире, ящик для кала ежедневно чистить и ошпаривать кипятком;
- при припухании лимфатических узлов или жалобах, напоминающих грипп, для уточнения симптомов немедленно обратиться к врачу.
К каким докторам следует обращаться если у Вас Токсоплазмоз у беременных:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Токсоплазмоза у беременных, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Читайте также:

