Токсоплазмоз токсокароз фасциолез описторхоз эхинококкоз
Обновлено: 23.04.2024
Паразитарные поражения печени. Механизмы
Паразитарные болезни с поражением печени нередко вызывают трудности диагностики, в основном связанные с недостаточной информацией клиницистов. Представления об ареалах распространения заболеваний не учитывают миграционных процессов населения и риска завоза возбудителей в среднюю климатическую полосу. Примерами служат случаи малярии, амебиаза, стронгилоидоза, гименолипедоза.
Паразитарные болезни включают в себя заболевания, вызванные протозойной инфекцией и глистной инвазией. При большинстве таких заболеваний в патологигеский процесс вовлекается печень.
К протозойным инфекциям с поражением печени относятся прежде всего амебиаз, малярия, лейшманиоз, токсоплазмоз.
К гельминтозам относят нематодозы, трематодозы и цестодозы.
Нематодозы (паразиты — круглые черви): аскаридоз, токсокароз, стронгилоидоз, трихинеллез.
Трематодозы (сосальщики): описторхоз, клонорхоз и фасциолез. Цестодозы (ленточные черви): эхинококкоз и альвеококк.
Вариантность и динамика клинических проявлений болезней, вызванных гельминтами и простейшими, обусловлены многообразием стационарной локализации, циклами развития паразитов, стадиеспецифической локализацией мигрирующих личинок, а также иммунным ответом организма хозяина. Гельминтозы, поражающие печень, как правило, приводят к развитию механической желтухи. Синдромы поражения желгных протоков характерны для описторхоза, клонорхоза, фасциолеза. Сосальщики паразитируют в желчных протоках, желчном пузыре, протоках поджелудочной железы.
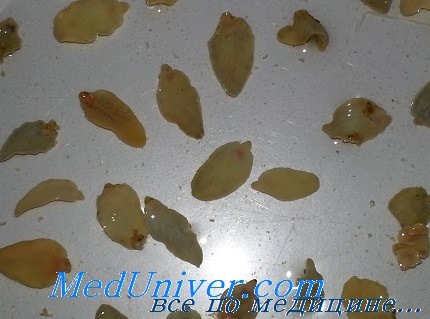
Вследствие механического повреждения стенок присосками образуются эрозии, железистая гиперплазия и кистозные изменения желчных протоков, холестаз, вторичное инфицирование с исходом в ангиохолит. Личинки фасциол прежде, чем проникнуть в гепатобилиарную систему, мигрируют двумя путями: по сосудам системы воротной вены и через брюшную полость в ткань печени, затем в желчные протоки, где превращаются во взрослых особей. В процессе дальнейшей миграции паразиты травмируют ткань печени и желчные протоки, вызывая микроабсцессы, микронекрозы, холестаз.
Поражением желчных путей может сопровождаться аскаридоз.
Объемные поражения печени образуют личиночная стадия эхинококков (киста печени), трофозоиты кишечной амебы.
Фиброз печени формируется при кишечных шистосомозах.
При малярии, висцеральном лейшманиозе, трипаносомозе наряду с гепатомегалией (гепатоспленомегалией), нарушением портального кровообращения, в тяжелых случаях манифестируют признаки поражения паренхимы печени, печеногной недостатогности.
Своеобразие поражений печени при паразитарных и протозойных болезнях определяется в первую очередь жизненным циклом паразита.
В целом поражения печени при большинстве гельминтозов и протозоозов имеют иммунную природу и свидетельствуют о неспецифигеской природе развивающегося процесса в виде лимфоидно-плазматигеской пролиферации, грануломатоза и своеобразных сосудистых поражений. Иммунологические реакции, переходя границы адекватного физиологического ответа, принимают характер иммунопатологических, приводящих к тяжелым органным поражениям. Ведущая роль в развитии иммунопатологических реакций принадлежит сенсибилизации организма ребенка соматическими, экскреторными и секреторными антигенами гельминтов.
В острой фазе гельминтозов происходит фиксация иммунных комплексов антиген — антитело на тучных клетках, что приводит к выделению биологически активных веществ: гистамина, гепарина, серотонинов и других. В результате наступают микроциркуляторные расстройства, нарушения проницаемости гистогематологических барьеров и клеточных мембран, что определяет развитие органной патологии.
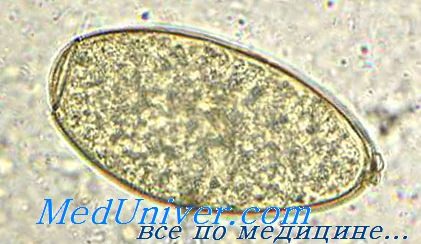
Иммунные комплексы фиксируются на мембранах тромбоцитов, вызывают лизис нейтрофилов, происходит освобождение лизосомальных ферментов, вазоактивных аминов, отложение фибрина и другие нарушения коагуляции, которые приводят к тяжелым сосудистым поражениям, нарушениям микроциркуляции, тромбозам, геморрагиям, отложению фибрина на базальной мембране сосудистых стенок с исходом в геалиноз или фибриноидный некроз. Повышенная проницаемость сосудистых стенок под действием вазоактивных аминов способствует проникновению иммунных комплексов в ткани и развитию органных поражений.
Личинки гельминтов оказывают также воздействие выделяемыми ими ферментами: гиалуронидазой, протеолитическими ферментами, способствующими активации системы комплемента, выделению простогландинов клетками окружающих гельминта тканей хозяина. Эти процессы провоцируют развитие воспалительных реакций. Таким образом, запускается каскадный механизм развития фиброза печени, начинающийся с регулярно повторяющегося повреждения ткани печени, следствием чего является преобладание процессов чрезмерного синтеза и накопления экстрацеллюлярного матрикса. В острой фазе фибриногенез контролируется и уравновешивается фибринолизом. В хронической фазе процессы фиброгенеза начинают превалировать.
Образование гранулем при гельминтозах обусловлено аллергической реакцией замедленного типа. Гранулемы появляются вокруг личиночных форм, а также вокруг взрослых паразитов, внедрившихся в ткани.
Кроме того, в патогенезе ряда инфекционных и паразитарных болезней существенная роль отводится системе цитокинов геловека. Цитокины — эндогенные биологически активные медиаторы, продуцируемые и секретируемые активированными клетками иммунной системы, в синтезе которых принимают участие фибробласты, эндотелиальные, эпителиальные и другие клетки. Клинически значимы интерлейкины (ИЛ 1-25), интерфероны (ИФН альфа, бета, гамма); факторы некроза опухоли (ФНО альфа, бета); колониостимулирующие факторы; факторы роста; хемокины.
В развитии и течении паразитарных болезней с поражением печени принимают активное участие следующие цитокины.
Интерлейкин 1 бета (ИЛ 1 бета) продуцируется макрофагами, моноцитами, лимфоцитами, фибробластами, эпителиоцитами.
ИЛ-1-бета регулирует синтез фактора роста гепатоцитов (ФРГ —HGF). Продуцируют HGF фибробласты, сосудистый эндотелий, активированный в результате повреждения печени, макрофагами и активированные Т-лимфоциты. Фактор является сильным митогеном для гепатоцитов и участвует в регенерации ткани печени. HGF супрессирует ген экспрессии тромбоцитарного фактора роста, повышает коллагеназную активность и угнетает апоптоз гепатоцитов, стимулирует их пролиферацию.
В повседневной клинической практике педиатра диагностика поражений печени при гельминтозах и протозоозах сопряжена с определенными трудностями. Задача усложнилась в последие годы в связи с миграцией детей из других регионов, эндемичных по различным контагиозным болезням, отсутствием информации об эпидемиологической ситуации в местах прежнего пребывания и посещаемых ребенком, отсутствием медицинской документации и достоверных анамнестических данных.
Категории МКБ: Амебиаз (A06), Анкилостомоз (B76.0), Аскаридоз (B77), Дикроцелиоз (B66.2), Дифиллоботриоз (B70.0), Другие инвазии, вызванные цестодами (B71), Инвазия, вызванная taenia saginata (B68.1), Инвазия, вызванная taenia solium (B68.0), Некатороз (B76.1), Описторхоз (B66.0), Стронгилоидоз неуточненный (B78.9), Токсоплазмоз (B58), Трихинеллез (B75), Трихуроз (B79), Фасциолез (B66.3), Цистицеркоз (B69), Энтеробиоз (B80)
Общая информация
Краткое описание
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ КЫРГЫЗСКОЙ РЕСПУБЛИКИ
ДЕПАРТАМЕНТ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ И ГОСУДАРСТВЕННОГО САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКОГО НАДЗОРА
КЫРГЫЗСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ ИНСТИТУТ ПЕРЕПОДГОТОВКИ И ПОВЫШЕНИЯ КВАЛИФИКАЦИИ
КЫРГЫЗСКО-РОССИЙСКИЙ СЛАВЯНСКИЙ УНИВЕРСИТЕТ им. Б.Н.ЕЛЬЦИНА
ДИАГНОСТИКА, ЛЕЧЕНИЕ И ПРОФИЛАКТИКА ПАРАЗИТАРНЫХ ЗАБОЛЕВАНИЙ
Клинические протоколы
Клинические протоколы (КП) по диагностике, профилактике и лечению паразитарных заболеваний приняты Экспертным советом по оценке качества клинических руководств/протоколов от 15.12.2017 г. и утверждены приказом Министерства здравоохранения Кыргызской Республики (МЗ КР) № 42 от 18 января 2017 г.
Клиническая проблема
Кишечные гельминтозы, протозоозы и тканевые паразитозы
Название документа
Диагностика, профилактика и лечение паразитарных заболеваний
Этапы оказания помощи
1-3 уровни медицинской помощи
Клинические протоколы применимы
к пациентам с кишечными гельминтозами, протозоозами и тканевыми паразитозами.
Целевые группы
Врачи-инфекционисты, семейные врачи, педиатры, аллергологи, окулисты, пульмонологи, эпидемиологи, паразитологи, лабораторные специалисты, организаторы здравоохранения, специалисты Фонда обязательного медицинского страхования (ФОМС), ординаторы, аспиранты, студенты и др.
Планируемая дата обновления
Проведение следующего пересмотра КП планируется в 2020 г., либо раньше, по мере появления новых ключевых доказательств по лабораторной, клинической диагностике и/или лечению паразитарных болезней.
В связи с тем, что новая стратегия по противорецидивной, консервативной терапии эхинококкоза и альвеококкоза находится на стадии разработки, клинические протоколы лечения данных личиночных гельминтозов исключены из данного сборника протоколов. После рассмотрения экспертным советом и утверждения МЗ КР, они будут изданы как дополнение к данному сборнику. В процессе апробации и рецензирования клинического протокола были получены комментарии и рекомендации, которые были учтены при его доработке.
Ожидаемый результат от внедрения данного клинического протокола
Внедрение в практическое здравоохранение профилактического лечения круглых червей – нематодов у всех членов семьи, включая беременных женщин с 3 триместра в эпидемиологически неблагополучных регионах (область, район, село), обеспечит оздоровление от нематодозов всей семьи и предупреждению риска постоянного перекрестного инвазирования членов семьи друг от друга, а также от других членов сообщества (в детских садах, школах, коллективах и тд). Лечение женщин во время беременности приведет к оздоровлению будущей мамы и снижению риска передачи инвазии детям грудного и раннего возраста.
Введение
Гельминтные инвазии в основном бывают двух типов: передаваемые через воду и передаваемые через почву ‒ геогельминты. Последние принадлежат к двум группам: нематодам (круглые черви) и платигельминтам (плоские черви) и живут в кишечнике человека, ежедневно выделяя тысячи яиц, которые попадают в почву с фекалиями инфицированных людей. При этом, яйца проглатываются детьми, которые берут грязные пальцы в рот после игр на земле (контакт с почвой); вместе с овощами, если овощи, не моются, не очищаются и не готовятся надлежащим образом; с водой из загрязненных источников и т. д. 1 .
После развития зрелых гельминтов в организме человека, они могут вызвать нарушение переваривания жиров, снижение абсорбции витаминов (особенно витамина А), временную непереносимость лактозы, снижение гемоглобина и железа, подавление аппетита и иммунной реакции, оказывают воздействие на рост, вес и познавательные функции инфицированных детей. Некоторые нематоды, в частности Trichuris trichiura, присасываются в слизистую оболочку кишечника и питаются кровью. Они выделяют антикоагулянты, вследствие чего повреждения кровоточат, что в итоге вызывает железодефицитную анемию.
Таким образом, паразиты могут быть опасными как для здоровья каждого человека, так и для всего сообщества в целом, в связи с чем большинство стран мира осуществляют различные программы, рекомендованные ВОЗ по профилактике и лечению паразитозов среди населения, особенно среди групп риска 1
Стратегия ВОЗ по борьбе с геогельминтами 1
ВОЗ рекомендует проводить ПЛ раз в год в случае, если распространенность гельминтозов, передаваемых через почву превышает 20% и дважды в год в случае, если этот показатель в сообществе превышает 50%.
Данная стратегия преследует глобальную цель – профилактическое лечение (ПЛ), по меньшей мере, 75% всех детей школьного возраста, подвергающихся риску заболевания геогельминтами. Направлена на профилактику и установление контроля над заболеваемостью геогельминтами путем проведения периодического ПЛ населения без предварительного индивидуального диагностического исследования всех людей из групп риска (дети дошкольного возраста, дети школьного возраста, включая подростков, а также беременные женщины со 2-го триместра) в эндемичных районах. Освобождение организма от гельминтов, путем ПЛ приводит к улучшению аппетита, что может способствовать увеличению роста и прибавки веса, также снижает заболеваемость и бремя болезни, вызванное наличием паразитов.
Важно отметить, что прием препаратов, используемых для ПЛ, детьми в возрасте до 12-месячного возраста не рекомендуется, так как безопасность и эффективность этих препаратов у детей данной возрастной группы не были подтверждены.
Профилактическое лечение однократной дозой альбендазола (400 мг) или мебендазола (500 мг) рекомендуется для беременных женщин после первого триместра, проживающих в районах, где распространенность нематодозов и/или трихоцефалеза составляет 20% или более (40% и более среди беременных женщин) и где анемия является серьезной проблемой общественного здравоохранения (условная рекомендация, среднее качество доказательств) 2 или в качестве лечения инфицированных беременных женщин в неэндемичных районах 3 .
Рекомендуемые ВОЗ лекарственные средства: альбендазол (400 мг) и мебендазол (500 мг) — эффективны, недороги и просты для распространения немедицинским персоналом (например, учителями). Они прошли экстенсивное тестирование на безопасность и использовались среди миллионов людей, при этом наблюдалось лишь незначительное количество умеренных побочных эффектов.
Паразитарные заболевания печени – группа разнородных болезней, вызываемых паразитами и гельминтами. Самые распространенные паразитозы печени: аскаридоз, эхинококкоз, амебиаз, описторхоз и др. К общим симптомам относят истощение, дистрофические изменения кожи и волос, повышенную утомляемость, нарушения сна, неприятный запах изо рта. В диагностике используют дуоденальное зондирование, исследование дуоденального содержимого, анализ кала на яйца гельминтов, УЗИ, КТ, сцинтиграфию печени. Лечение консервативное, заключающееся в назначении антипаразитарного препарата (специфического либо широкого спектра действия), либо оперативное.
Общие сведения
Паразитарные заболевания печени вызываются протозоозами и глистными инвазиями. Всемирная организация здравоохранения считает, что не менее 25% населения Земли заражено теми или иными паразитами. Паразитозы и гельминтозы занимают четвертое место среди заболеваний, приносящих наибольший вред здоровью человека. На данный момент не существует исследований, которые бы отражали истинную заболеваемость паразитарными болезнями и гельминтозами в России. По мнению экспертов в области инфекционных заболеваний и гастроэнтерологии, паразитарные инвазии могут быть выявлены не менее чем у двадцати миллионов россиян. Учитывая тот факт, что паразиты и глисты могут персистировать в организме долгие годы, заболевание нередко накладывает отпечаток на всю жизнь: вызывает задержку роста и развития в детском возрасте, ухудшает умственные способности школьников, провоцирует снижение работоспособности и активности взрослого населения.
Причины паразитарных заболеваний печени
Все паразитарные заболевания печени возникают либо при протозойном инфицировании, либо в результате глистной инвазии. Поражение печени в этой ситуации выступает одним из проявлений генерализованной инфекции. Среди протозойных инфекций печень чаще всего поражается при токсоплазмозе, амебиазе, лейшманиозе, малярии. Гельминтозы представлены нематодозами, цестодозами, трематодозами. Нематодозы вызываются круглыми червями (аскаридоз, стронгилоидоз, токсокароз, трихинеллез); трематодозы – сосальщиками (фасциолез, клонорхоз, описторхоз); цестодозы – ленточными глистами (альвеококкоз, эхинококкоз).
Разнообразие клинических проявлений паразитарных заболеваний печени обусловлены не только видом паразита либо гельминта, но и их жизненным циклом, местом внедрения в организм, локализацией различных жизненных форм, реакцией иммунитета на возбудителя.
Сосальщики обычно локализуются в желчевыводящих протоках, желчном пузыре. Присосками сосальщиков повреждается эпителий протоков, в которых образуются кисты, воспалительная реакция, формируется холангит и холестаз. При фасциолезе личинки с током крови проникают в ткань печени, затем мигрируют в желчевыводящие пути и там превращаются в половозрелого паразита. В дальнейшем гельминты повреждают ткань печени, формируя микроскопические гнойники в паренхиме и желчных ходах. Схожий патогенез заболевания имеет и аскаридоз.
При эхинококкозе и амебиазе в печени формируются объемные образования. Шистосомозы приводят к фиброзированию паренхимы печени. Заражение малярийным плазмодием, трипаносомами, шистосомами приводит к значительному увеличению размеров печени, воспалительному процессу, печеночной недостаточности.
Главную роль в поражении печеночной паренхимы играют патологические иммунные реакции. Паразиты и гельминты выделяют антигены, которые провоцируют избыточные иммунные реакции, приводящие к значительному поражению клеток и микрососудов печени. Личинки и взрослые особи глистов, находящиеся в ткани печени, выделяют ряд ферментов, повреждающих гепатоциты и стимулирующих синтез фибрина. Хроническое персистирование паразитов рано или поздно приводит к фиброзированию печени, хронической печеночной недостаточности. Ниже рассмотрены основные виды паразитарных заболеваний печени, встречающиеся в России.
Виды паразитарных заболеваний печени
Эхинококкоз печени
Эхинококкоз занимает ведущее место среди всех паразитарных заболеваний печени. В подавляющем большинстве случаев поражается правая половина печени, практически у половины пациентов эхинококковых кист несколько. У людей эхинококкоз печени может быть гидатидным (личиночная стадия, кистозная форма, человек является промежуточным хозяином) и альвеококковым. Основным хозяином являются псовые, в организме которых эхинококк созревает, а его терминальные членики с огромным количеством яиц попадают в окружающую среду, вызывая заражение человека фекально-оральным либо контактным путем. Попадая в желудок, оболочка яиц растворяется и гельминты проникают через стенку желудка или кишечника в кровь. С током крови возбудители мигрируют в печень, а затем и в другие органы, формируя в них кисты (изначально – около 1 мм диаметром). Эхинококковая киста печени имеет две оболочки, внутренняя продуцирует жидкую составляющую кисты, образует дочерние пузыри. Наружная оболочка может кальцифицироваться, содержимое ее может нагнаиваться. Кисты огромных размеров сдавливают паренхиму печени и сосуды, желчевыводящие пути.
Гидатидный эхинококкоз. В первые годы после заражения эхинококкоз может никак не проявляться. Первые клинические проявления обычно возникают по достижению кистой больших размеров – боли в правом боку, тошнота и рвота, слабость, исхудание, хроническая диарея, аллергические высыпания на коже, ломкость волос. Размеры печени увеличиваются, при поверхностном расположении кисты ее можно даже пропальпировать. Желтуха развивается только при сдавлении кистой протоков печени. Возможен прорыв кистозного образования в брюшную или грудную полость, сопровождающийся сильной болью, анафилактическим шоком (реакция на всасывание содержимого кисты). Нагнаивание содержимого кисты сопровождается болезненностью печени, лихорадкой, ухудшением общего состояния.
Диагностика эхинококкоза включает сбор анамнеза (контакт с собакой), пальпацию печени и выявление эхинококковой кисты. Специфическим методом диагностики является реакция Казони (положительна в 85% случаев), латекс-агглютинации (90%). Визуализировать паразита помогут УЗИ печени и желчного пузыря, ангиография чревного ствола, МРТ печени и желчевыводящих путей, статическая сцинтиграфия печени, диагностическая лапароскопия.
Лечение только оперативное. Производится иссечение эхинококковых кист печени, предварительно в кисту вводят формалин и отсасывают ее содержимое. Полость кисты ушивают наглухо. В последующем может сформироваться непаразитарная киста, гнойник. При маленьких размерах и краевом положении кисты возможна резекция печени вместе с кистой.
Альвеолярный эхинококкоз. Является более редкой формой паразитарного заболевания печени, вызываемого эхинококком. Возбудитель альвеококкоза отличается своей личиночной стадией. Заражение происходит при обработке шкур основного хозяина (лисы и др.), употреблении зараженных продуктов. Особенностью альвеококкоза является образование множества мелких кист, которые инфильтрируют паренхиму печени, плотно прилегая друг к другу и образуя опухолевидный узел в ткани печени. Пузырьки паразита способны прорастать в паренхиму печени, сосуды, желчные пути, соседние органы. В центре очага альвеококкоза формируется некроз, в дальнейшем альвеококковый очаг может обызвествляться. Дифференцировать заболевание следует с раком печени, циррозом печени.
Клиническая картина альвеококкоза сходна с гидатидной формой заболевания, однако имеет большую частоту механической желтухи. Лечение альвеококкоза печени имеет определенные особенности. Проведение операции затруднено инфильтративным ростом паразитов, прорастанием сосудов, желчных путей, круглой связки печени. Обычно операция назначается при значительном поражении печени, нагноении и прорыве кист. Чаще всего производится частичная резекция печени, оставшиеся кисты обрабатываются химиопрепаратами или формалином, подвергаются криодеструкции.
Аскаридоз печени и желчных путей
На сегодняшний день аскаридоз печени встречается достаточно редко. Человек заражается при употреблении в пищу зараженных яйцами аскарид продуктов. Попадая в кишечник, возбудители через кишечную стенку проникают в кровеносное русло, с током крови попадают в печень. В печени из-за персистирования паразитов формируются некрозы, микроабсцессы. В дальнейшем возбудители могут мигрировать по организму, попадая в другие органы и системы, а в кишечнике превращаясь в половозрелые формы.
Основными проявлениями аскаридоза являются холангиты, холестаз, абсцессы печени. Специфических симптомов аскаридоза не существует. Диагноз аскаридоза печени устанавливается на основании обнаружения аскарид и их яиц в рвотных массах, кале; также возможна визуализация гельминтов при УЗИ, КТ печени.
Лечение аскаридоза желчевыводящих путей только хирургическое. Применение противоаскаридозных средств при закупорке желчных путей противопоказано, так как приводит к кратковременной активизации паразитов и их дальнейшему проникновению в желчные пути и паренхиму печени. Для уточнения степени поражения протоков во время операции проводят РХПГ. Для профилактики персистирования аскаридоза, образования конкрементов желательно провести холецистэктомию. В послеоперационном периоде по дренажам вводят антиаскаридозные препараты для уничтожения оставшихся гельминтов.
Описторхоз печени
Данное паразитарное заболевание печени встречается достаточно редко, заражение человека происходит через сырую рыбу, зараженные водоемы. Размножение гельминта в желчных путях приводит к их расширению. Ткань печени становится очень плотной, расширенные внутрипеченочные протоки видны сквозь капсулу печени. Персистирование инвазии приводит к утолщению стенок желчных путей, формированию грубых рубцовых изменений вокруг них, которые напоминают цирроз печени, часто приводят к перфорации желчных протоков и перитониту. Закупорка желчных ходов благоприятствует застою и воспалительным изменениям в них. У пациентов с описторхозом часто в будущем развивает рак печени.
Описторхоз, как и другие паразитарные заболевания печени, не имеет специфической клиники. Частыми проявлениями являются увеличение и уплотнение печени, боли в правом подреберье, жидкий стул. В случае присоединения инфекции пациента беспокоят лихорадка, озноб, липкий пот.
Диагноз ставится на основании выявления особей и яиц гельминтов в кале и дуоденальном соке, полученном при зондировании. Лечение описторхоза печени хирургическое, заключается в дренировании протоков, введении антипаразитарных препаратов в дренажи.
Амебиаз печени
Заболевание часто встречается в тропических странах. Характеризуется преимущественным поражением толстого кишечника, диссеминацией возбудителя в паренхиматозные органы. Цисты амеб попадают в организм человека с зараженной водой, фруктами и овощами, зеленью.
Амебы вызывают образование язв в кишечнике, через которые возбудители попадают в кровоток, а затем в печень, приводя к формированию абсцессов печени примерно в 10% случаев. Особенность амебных абсцессов в том, что они не имеют капсулы, содержат в себе расплавленные ткани, кофейного цвета гной. Состояние пациентов обычно очень тяжелое, печень увеличена и болезненна. Кожные покровы иктерично-серые, сухие.
В диагностике абсцесса печени используют УЗИ гепатобилиарной системы, сцинтиграфию печени, КТ, пункционную биопсию печени (с целью выявления амеб). Лечение амебиаза обычно комплексное: антиамебные, антибактериальные и дезинтоксикационные препараты. Хирургическое лечение проводится при неэффективности консервативных мероприятий, возникновении осложнений.
Прогноз и профилактика паразитарных заболеваний печени
Прогноз при паразитарных заболеваниях печени зависит от многих факторов: длительности паразитарной инвазии, обширности поражения печени, наличия осложнений. При длительном течении паразитарного поражения печени с формированием фиброза, развитием печеночной недостаточности прогноз неблагоприятный.
Профилактика всех паразитарных заболеваний печени заключается в соблюдении правил личной гигиены (мыть руки после контакта с животными, пить только кипяченую воду, тщательно мыть овощи и фрукты перед употреблением в пищу, проводить термическую обработку мяса и рыбы), контроле за состоянием водоемов, из которых производится забор питьевой воды.
Токсокароз – это хроническое инфекционное заболевание, вызываемое личинками круглого червя токсокары. Для инвазии характерна лихорадка, рецидивирующие высыпания и увеличение размеров печени. Патология сопровождается поражением глазных яблок и внутренних органов: сердца, головного мозга, легких. Диагностика заключается в обнаружении специфических антител к возбудителю. Лечение этиотропное (антигельминтные препараты), также применяются средства симптоматической терапии, в некоторых случаях производятся хирургические вмешательства.
МКБ-10
B83.0 Висцеральная форма заболеваний, вызываемых миграцией личинок гельминтов [висцеральная Larva migrans]
Общие сведения

Причины токсокароза
Возбудитель – круглый червь Toxocara, наиболее часто встречаются инвазии видами Т. сanis (собачий) и T. сati (кошачий). Основной цикл развития паразита не включает в себя человеческий организм, поэтому люди оказываются случайными хозяевами гельминта, который в подобных условиях неспособен достигать половозрелой формы. Источником инфекции является больное животное (чаще собака), больной человек эпидемиологически не опасен. Считается, что доля зараженных токсокарозом среди взрослых собак варьирует от 15 до 50%, щенков – до 80%.
Больные животные выделяют яйца гельминтов с фекалиями, сами паразиты в половозрелой форме находятся у постоянного хозяина в пищеварительном тракте. Наиболее опасными считаются дворы, детские площадки, парки, поскольку контаминация земли яйцами паразита встречается в 10-40% почвенных проб. Инфицирование людей происходит контактным и пищевым путем – при поглаживании, играх со зверями, особенно бродячими, употреблении в пищу немытых ягод, фруктов и овощей. Отмечено, что тараканы могут поглощать яйца токсокар с последующим выделением до 25% потенциально жизнеспособных особей, что играет важную роль в распространении инфекции в быту.
Патогенез
После попадания яиц токсокары в тонкий кишечник человека (преимущественно двенадцатиперстную кишку) высвобождаются личинки, проникающие в системный кровоток через слизистую оболочку. Сначала токсокары заносятся в печень и правую половину сердца, затем в легочную артерию и левый желудочек, откуда выходят в большой круг кровообращения. Распространяясь по организму, личинки оседают в различных органах и тканях, вызывая геморрагические и некротические изменения, образование воспалительных очагов в виде гранулем, в центре которых находится некротизированная ткань и личинка, вокруг – воспалительный инфильтрат.
При попадании в кровеносное русло продуктов жизнедеятельности возникают аллергические реакции. Часть личинок гибнет, оставшиеся гельминты выделяют особую маскирующую субстанцию, которая позволяет им персистировать в организме до 10 лет, периодически мигрируя по кровеносной системе и поражая новые ткани. Характерной особенностью токсокар является формирование гранулем в поджелудочной железе, головном мозге, печени, легких, миокарде и мезентериальных лимфатических узлах. Патогенез поражения глаз до конца не изучен, имеются гипотезы о низкой активности инвазии и малой выраженности иммунного ответа.
Патогенез эпилепсии при токсокарозе окончательно не ясен. Предполагается, что поражение головного мозга может привести к формированию волокнистых рубцов после острого воспаления или хронических гранулем. Другая теория объясняет появление эпилептических припадков при повреждении нейронов усиленным образованием провоспалительных цитокинов из-за повышения проницаемости гематоэнцефалического барьера, вызываемого паразитами, а также аутоантителами к нейрональным элементам, которые нередко обнаруживаются у больных токсокарозом.
Классификация
Классификация токсокароза у человека основывается на глубине инвазии в организм человека. Гельминтоз практически всегда протекает с минимальной либо неспецифической клиникой (субклинически), бессимптомная форма встречается в 13% случаев заболевания, органные поражения более характерны для детей. Выделяют следующие виды токсокароза:
- Глазной.Типичен для детей старше 8 лет, подростков и молодых взрослых. Поражение зрительного аппарата обычно одностороннее, протекает в виде хронического эндофтальмита, увеита, абсцессов стекловидного тела, папиллитов, кератитов и косоглазия. При длительном течении возможна слепота.
- Висцеральный.Протекает остро или хронически с вовлечением дыхательной системы, сердца, кожи, лимфатических узлов, селезенки, печени, суставов и мышц. Часто наблюдается диарея, тошнота и рвота. Описаны поражения головного мозга: рецидивирующие головные боли, менингоэнцефалит, эпилептические припадки.
Симптомы токсокароза
Инкубационный период определить сложно, считается, что он может занимать несколько лет. При остром начале наблюдается лихорадка до 38,5°C и выше, поражения дыхательной системы – от заложенности носа, сухого кашля и першения в горле до тяжелой одышки и астматического статуса. На коже появляется зудящая сыпь в виде волдырей и пятен, при подкожном расположении личинок видны приподнятые над поверхностью прямые или извилистые красновато-коричневые ходы. У детей нередко выявляются увеличенные плотноэластические безболезненные лимфоузлы. Пациенты с токсокарозом часто предъявляют жалобы на боли в животе, тошноту, иногда – рвоту и срывы стула.
Осложнения
Наиболее частые осложнения висцерального токсокароза – бронхиальная астма, хронический бронхит и эпилепсия, глазного – отслойка сетчатки и односторонняя слепота. Подкожное расположение личинок токсокар приводит к присоединению вторичной бактериальной инфекции, образованию инфильтраов, абсцессов и флегмон, поражение легких – к тяжелым пневмониям смешанной этиологии с нарастающей дыхательной недостаточностью. Массивная инвазия гельминтов, полиорганное поражение могут стать причиной летального исхода. У беременных женщин токсокароз часто выявляется невынашивание, задержка внутриутробного развития плода.
Диагностика
Диагноз токсокароза подтверждается врачом-инфекционистом. Для исключения сочетания висцерального и глазного гельминтоза обязательным является осмотр офтальмолога, по показаниям назначаются консультации других специалистов. Диагностические методы, необходимые для верификации токсокарозного поражения, включают следующие методики:
Дифференциальную диагностику проводят с аскаридозом, при котором нередко наблюдаются кишечная непроходимость, острая обструкционная дыхательная недостаточность. Необходимо исключить описторхоз и стронгилоидоз, которые протекают с желтухой, болями в правом подреберье и срывами стула. Глазную форму токсокароза дифференцируют от ретинобластомы, проявляющейся лейкокорией, косоглазием, слезотечением, светобоязнью, вторичной глаукомой. Кожные проявления могут быть следствием укусов насекомых, воздействия аллергенов.
Лечение токсокароза
Показанием для стационарного лечения являются висцеральные формы болезни. Постельный режим назначается только при наличии лихорадки и рекомендуется до 2-4 дней устойчивого отсутствия высоких цифр температуры тела. Специальной диеты нет, однако, учитывая некоторые побочные эффекты применяемых препаратов, рекомендуется воздержаться от приема жирной, жареной пищи, алкоголя, специй, маринадов, сладостей. Важно соблюдение питьевого режима, исключение контакта с возможными пищевыми и бытовыми аллергенами. Недопустимо самовольное прекращение начатого медикаментозного лечения.
- Антигельминтная терапия. Высокоэффективными антигельминтными средствами для разрушения мигрирующих личинок считаются албендазол, мебендазол, диэтилкарбамазин, которые применяются в таблетированных формах. В отношении токсокар, находящихся в гранулемах, данные препараты не обладают выраженным нейтрализующим эффектом.
- Хирургические методы лечения применяются при глазном токсокарозе и включают в себя микрохирургическое удаление гранулем, лазерную коагуляцию для расщепления личинок в средах глаза и коррекции отслойки сетчатки.
- Симптоматическая терапия проводится по показаниям. Включает жаропонижающие (парацетамол, целекоксиб), дезинтоксикационные (хлосоль, глюкозо-солевые растворы), десенсибилизирующие (глюконат, хлорид кальция), антигистаминные (хлорапирамин, дезлоратадин), отхаркивающие (ацетилцистеин, мукалтин), ферментативные (панкреатин) и другие средства.
Прогноз и профилактика
Прогноз при неосложненных формах благоприятный, летальных случаев не описано. Длительность приема лекарственных средств может составлять до 3-4 недель и более, иногда требуются несколько курсов с перерывами в 2-4 месяца. Критериями эффективности считаются исчезновение клиники, снижение уровня антител и эозинофилии крови. Описаны случаи диссеминированного токсокароза среди ВИЧ-инфицированных лиц в стадии СПИДа, а также пациентов, длительно принимающих системные глюкокортикостероиды или проходящих лучевую терапию по поводу онкологических болезней.
Профилактические вакцины на основе ДНК показали положительный эффект в экспериментах на мышах, исследования в настоящее время продолжаются. Рекомендуется осуществлять контроль за популяцией бродячих животных, проводить выгул собак на специально отведенных территориях. Важными мерами неспецифической борьбы с заболеваемостью являются отучение детей от поедания земли, привитие навыков личной гигиены после игр на улице, песочнице, общения с животными; тщательное мытье ягод, зелени, овощей и фруктов перед едой; назначение антигельминтных препаратов беременным собакам, новорожденным щенкам.
2. Токсокароз. Клиника. Диагностика. Лечение. Профилактика. Информационно¬методическое пособие. – 2004.
4. Токсокароз у детей/ Глазунова Л.В., Артамонов Р.Г., Бекташянц Е.Г., Куйбышева Е.В., Шиц О.Л., Кирнус Н.И., Иванова Е.Ю. // Лечебное дело. – 2008.
Эхинококкоз – это паразитарная инвазия личиночной стадией ленточного гельминта эхинококка, протекающая с поражением внутренних органов (печени, легких, сердца, головного мозга и др.) и образованием в них эхинококковых кист. Неспецифические симптомы эхинококкоза включают слабость, крапивницу, преходящее повышение температуры; специфические зависят от места локализации паразита и могут быть представлены локальными болями, тошнотой, желтухой, кашлем, очаговой неврологической симптоматикой, кардиалгией, аритмией и пр. Диагностика эхинококкоза основывается на данных инструментальных исследований (рентгена, сцинтиграфии, УЗИ, КТ) и серологических проб. Лечение эхинококкоза хирургическое.
МКБ-10
Общие сведения
Эхинококкоз – гельминтное заболевание из группы цестодозов, вызываемое паразитированием в организме человека эхинококка в стадии онкосферы. В мире наибольшая заболеваемость эхинококкозом отмечается в Австралии, Новой Зеландии, Северной Африке, Южной Америке, Южной Европе, Центральной Азии. В России гельминтоз встречается в Поволжье, Приуралье, Ставропольском и Краснодарском крае, Западной Сибири, на Дальнем Востоке.
В эндемичных регионах заболеваемость населения эхинококкозом достигает 5-10%. Распространенность эхинококкоза тесно связана с развитием животноводства. Учитывая тот факт, что при эхинококкозе могут поражаться различные внутренние органы, а единственно радикальным методом лечения является операция, заболевание лежит в сфере интересов торакоабдоминальной хирургии, нейрохирургии, кардиохирургии.

Причины эхинококкоза
Эхинококкоз человека вызывается личиночной стадией ленточного гельминта Echinococcus granulosus - лавроцистой. Окончательными хозяевами половозрелых гельминтов выступают животные (собаки, лисицы, волки, львы, рыси и др.), в кишечнике которых паразитируют цестоды. Человек, домашние и дикие травоядные животные (рогатый скот, свиньи, лошади, олени, лоси и др.) являются промежуточными хозяевами личиночных стадий и одновременно биологическим тупиком, поскольку не выделяют яйца эхинококка в окружающую среду и не могут служить источником инвазии.
Взрослые особи эхинококка – это мелкие гельминты длиной 2,5-8 мм и шириной 0,5-10 мм, имеющие головку с четырьмя присосками и двумя рядами крючьев, шейку и несколько члеников. В зрелых члениках содержатся яйца эхинококка с онкосферами и шестикрючной личинкой-зародышем внутри. Онкосферы выживают в большом диапазоне температур (от -30°С до +30°С), несколько месяцев сохраняются в почве, но вскоре погибают под действием солнечного света.
Из кишечника окончательного хозяина яйца с испражнениями выделяются во внешнюю среду. Заражение людей эхинококкозом происходит алиментарным (при употреблении загрязненных фекалиями овощей и фруктов, воды) или контактным путем (при разделке туш или контакте с животными, инвазированными эхинококком). Высокий риск заболеваемости эхинококкозом имеют лица, занятые животноводством и уходом за животными (животноводы, охотники, работники скотобоен и др.).
Патогенез
В ЖКТ человека под действием пищеварительных ферментов оболочка яйца и онкосферы растворяется, и наружу выходит личинка. С помощью крючьев она внедряется в слизистую кишки, откуда попадает в венозный кровоток и в портальную систему. Большая часть онкосфер оседает в печени; иногда через нижнюю полую вену онкосферы попадают в правые отделы сердца, а оттуда – в малый круг кровообращения и легкие. Реже через легочные вены и левые отделы сердца зародыши оказываются в большом круге кровообращения и могут быть занесены в любой орган: головной мозг, селезенку, почки, мышцы и др. В результате инвазии примерно в 70-80% случаев развивается эхинококкоз печени, в 15% - эхинококкоз легких, в остальных случаях происходит поражение других органов.
После оседания зародыша эхинококка в том или ином органе начинается пузырчатая или гидатидозная стадия развития паразита. Эхинококковый пузырь представляет собой кисту, покрытую двухслойно оболочкой, состоящей из внутреннего (зародышевого) и наружного (хитинового) слоев. Киста медленно увеличивается в размерах (примерно на 1 мм в месяц), однако спустя годы может достигать гигантских размеров. Внутри эхинококкового пузыря содержится прозрачная или беловатая опалесцирующая жидкость, в которой плавают дочерние пузыри и сколексы. Дочерние пузыри эхинококка могут образовываться и снаружи хитиновой оболочки; их общее количество может достигать 1000.
Проявления эхинококкоза связаны с сенсибилизирующим влиянием паразитарных антигенов и механическим давлением кисты на органы и ткани. Паразитирование эхинококка сопровождается выделением продуктов обмена, что приводит к развитию интоксикации и аллергической реакции замедленного типа. В случае полного разрыва кисты происходит истечение ее содержимого в плевральную или брюшную полость, что может вызвать анафилактический шок. Увеличивающаяся в размерах эхинококковая киста давит на окружающие структуры, нарушая функции пораженного органа. В некоторых случаях развивается нагноение кисты; реже возможно самопроизвольная гибель эхинококка и выздоровление.
Симптомы эхинококкоза
Эхинококкоз может бессимптомно протекать годами и десятилетиями; в случае возникновения клинической симптоматики патогномоничные признаки отсутствуют. Независимо от локализации паразита в организме, эхинококкоз проходит в своем развитии три стадии:
- I - бессимптомную. Течение латентного периода начинается от момента внедрения онкосферы в ткани и продолжается до тех пор, пока не появляются первые клинические признаки эхинококкоза.
- II - стадию клинических проявлений. Во время II стадии больных беспокоят боли в месте локализации кисты, слабость, крапивница, кожный зуд, а также специфические симптомы, обусловленные паразитированием кистозной формы эхинококка в том или ином органе.
- III - стадию осложнений. В стадии осложненного эхинококкоза может произойти разрыв кисты и истечение содержимого в брюшную или плевральную полость с развитием перитонита, плеврита. При нагноении эхинококковой кисты присоединяются высокая лихорадка, тяжелая интоксикация. Сдавление кистой органов и тканей может вызывать развитие механической желтухи, асцита, вывихов, патологических переломов.
Эхинококкоз печени
Для эхинококкоза печени характерны жалобы на тошноту, снижение аппетита, периодически возникающую диарею, тяжесть и боли в правом подреберье. Объективно обнаруживается гепатоспленомегалия; иногда эхинококковая киста печени пальпируется в виде округлого плотного образования. В случае сдавления кистой желчных протоков развивается механическая желтуха; при компрессии воротной вены возникает асцит, портальная гипертензия. Присоединение вторичной бактериальной флоры может приводить к формированию абсцесса печени. Наиболее тяжелым осложнением эхинококкоза печени служит перфорация кисты с развитием клиники острого живота, перитонита и тяжелых аллергических реакций. При этом происходит диссеминация эхинококков, в результате чего развивается вторичный эхинококкоз с множественный локализацией.
Эхинококкоз легких
Эхинококкоз легких протекает с повышением температуры тела, интоксикационным синдромом, болью в груди, кашлем, кровохарканьем. Давление кисты на легочную ткань приводит к формированию ателектазов легких. При прорыве пузыря в бронхи развивается сильный кашель, цианоз, нередко - аспирационная пневмония. Крайне опасным осложнением легочного эхинококкоза является прорыв кисты в плевру и перикард, что может привести к анафилактическому шоку, резкому смещению средостения, тампонаде сердца и внезапной смерти. Инфицирование эхинококковой кисты сопровождается формированием абсцесса легкого.
Эхинококкоз сердца
При эхинококкозе сердца беспокоят загрудинные боли, напоминающие стенокардию. Компрессия кистами венечных артерий может вызвать развитие инфаркта миокарда. Часто возникают нарушения ритма и проводимости: желудочковая тахикардия, неполная и полная блокады ножек пучка Гиса, полная поперечная блокада сердца. Причинами гибели пациента с эхинококкозом сердца могут стать злокачественные аритмии, сердечная недостаточность, тампонада сердца, кардиогенный шок, ТЭЛА, постэмболическая легочная гипертензия и др.
Эхинококкоз головного мозга
Клинка эхинококкоза головного мозга характеризуется гипертензионным синдромом и очаговой неврологической симптоматикой (нарушением чувствительности, парезами конечностей, эпилептиформными приступами).
Диагностика
Правильной диагностике эхинококкоза способствует подробно собранный эпидемиологический анамнез, указывающий на тесный контакт человека с животными, эндемичность заражения. При подозрении на эхинококкоз любой локализации назначаются серологические исследования крови (ИФА, РНИФ, РНГА), позволяющие обнаружить специфические антитела к эхинококку. Специфичность и чувствительность тестов достигает 80-98%. Примерно в 2/3 случаев оказывается информативной кожно-аллергическая проба - реакция Казони.
Диапазон инструментальной диагностики эхинококкоза включает ультразвуковые, рентгеновские, томографические, радиоизотопные методы. Перечень исследований зависит от локализации поражения:
- При эхинококкозе печени информативны УЗИ гепатобилиарной системы, ангиография чревного ствола (целиакография), МРТ печени, сцинтиграфия, диагностическая лапароскопия и др.
- Распознать эхинококкоз легких позволяет проведение рентгенографии легких и КТ грудной клетки, бронхоскопии, диагностической торакоскопии.
- Ведущими методами диагностики эхинококкоза головного мозга служат КТ или МРТ.
- При подозрении на поражение сердца выполняется ЭхоКГ, коронарография, вентрикулография, МРТ сердца.
При прорыве эхинококковой кисты в просвет полых органов сколексы паразита могут быть обнаружены в исследуемом дуоденальном содержимом, мокроте. Также в этих случаях прибегают к выполнению бронхографии, холецистографии, пункционной холангиографии. Эхинококковую кисту необходимо дифференцировать от альвеококкоза, бактериальных абсцессов, кист непаразитарной этиологии, опухолей печени, легких, головного мозга и пр.
Лечение эхинококкоза
Радикальное излечение эхинококкоза возможно только хирургическим путем. Оптимальным способом является проведение эхинококкэктомии – вылущивания кисты без нарушения целостности хитиновой оболочки. При наличии крупного пузыря вначале производится его интраоперационная пункция с аспирацией содержимого. Остаточная полость тщательно обрабатывается антисептическими растворами, тампонируется, дренируется или ушивается наглухо. В процессе операции важно не допустить попадания содержимого пузыря на окружающие ткани во избежание диссеминации эхинококка.
В случае невозможности иссечения кисты при эхинококкозе легкого выполняется клиновидная резекция, лобэктомия, пневмонэктомия. Аналогичная тактика используется при эхинококкозе печени. Если иссечение эхинококковой кисты печени представляется технически невозможным, осуществляется краевая, сегментарная, долевая резекция, гемигепатэктомия. В до- и послеоперационном периоде назначается противопаразитарная терапия препаратами празиквантел, альбендазол, мебендазол.
Прогноз и профилактика
В случае радикального удаления эхинококковых кист и отсутствия повторного заражения прогноз благоприятный, рецидивов эхинококкоза не возникает. В случае интраоперационной диссеминации сколексов через 1-2 года может возникнуть рецидив заболевания с формированием множественных эхинококковых пузырей и неблагоприятным прогнозом.
Эхинококкоз - лечение в Москве
Комментарии к статье
Вы можете поделиться своей историей болезни, что Вам помогло при лечении эхинококкоза.
Читайте также:

