Транзиторная инфекция что это такое
Обновлено: 24.04.2024
НОРМАЛЬНАЯ МИКРОФЛОРА ВЛАГАЛИЩА ЖЕНЩИНЫ.
В основе нормального состояния влагалища лежат три основных фактора. Это: количество гликогена в эпителии влагалища; количество и состав нормальной микрофлоры; количество и состав транзиторной (временно присутствующей) условно-патогенной микрофлоры. Что происходит в норме? Под действием эстрогенов (женских половых гормонов) из продуктов распада поступающей в организм пищи в клетках влагалища происходит синтез особого вещества гликогена. Один из эстрогенов - прогестерон - вызывает слущивание и разрушение эпителиальных клеток влагалища с последующим высвобождением из них гликогена, который распадается на мальтозу и декстрозу, которые служат пищей для обитающих во влагалище лактобациллам, составляющим до 98% нормальной микрофлоры и бифидумбактериям. В процессе взаимодействия лактобацилл и гликогена образуется молочная кислота, которая придают влагалищу определенную кислотность, которая в норме равна рН 3.5-4.5. Кислая среда влагалища имеет 2 основные функции: уничтожение и создание неблагоприятной среды для размножения патогенной, в том числе и транзиторной (временно-присутствующей) условно-патогенной микрофлоры; определенная "эволюционная" функция - как известно кислая реакция является губительной для сперматозоидов, и прорваться через кислотный барьер и оплодотворить яйцеклетку может только самый здоровый и сильный сперматозоид.
Нормальная микрофлора женского влагалища, как было сказано выше, состоит в основном из ацидофильных лактобактерий, большинство из которых представлено перекись-образующими лактобациллами, небольшую часть микрофлоры составляют бифидумбактерии (до 10%) и пептострептококки (до 5%).Такая смесь микроорганизмов в норме носит название микрофлора Додерлейна. Помимо образования молочной кислоты лактобациллы выполняют несколько еще важных функций по защите влагалища: образование перекиси водорода, лизоцима и ряда ферментов, обладающих противомикробными свойствами, стимуляция местной иммунной защиты организма - активизация макрофагов, стимуляция выработки интерферона и секреторных иммуноглобулинов.
ТРАНЗИТОРНАЯ МИКРОФЛОРА ВЛАГАЛИЩА.
Влагалище является сообщающимся с внешней средой полым органом, поэтому инфицирование его различными микроорганизмами из внешней среды неизбежно. Часть микробов попадает во влагалище девочки во время родов, часть микроорганизмов попадает во влагалище взрослой женщины во время половых контактов, часть микроорганизмов заносится из внешней среды. Попавшие микробы уничтожаются сразу, либо временно находятся во влагалище, а затем уничтожаются кислой средой и лактобактериями, либо остаются во влагалище на неопределенное время, но их размножение также весьма ограничено механизмами защиты. Такая микрофлора была названа транзиторной (временной). В норме у здоровой женщины высокоточными методами исследования можно определить: гарднереллы, бактероиды, фузобактерии, мобилункус, лептотрикс, превотеллы и вейлонеллы, пептококки и пептострептококки, микоплазмы, но их количество крайне ничтожно и они не всегда присутствуют во влагалище здоровой женщины.
Таким образом, нормальное состояние влагалища представлено лактобациллярной микрофлорой Додерлейна, незначительным присутствием некоторых транзиторных условно-патогенных микроорганизмов и имеет, кислую среду (рН 3.5-4.5).
МЕХАНИЗМЫ РАЗВИТИЯ БАКТЕРИАЛЬНОГО ВАГИНОЗА.
Так почему же у женщины происходит угнетение нормальной микрофлоры и усиленное размножение транзиторной микрофлоры? На данный момент существует несколько теорий и версий. Нарушение синтеза гликогена: так как синтез гликогена регулируется эстрогенами (женскими половыми гормонами) то естественно снижение уровня гормонов или его повышение влияет на количество гликогена в эпителии.
При недостаточном уровне эстрогенов, а это бывает при эндокринных заболеваниях, гинекологических заболеваниях яичников, при нервных стрессах (нервная система участвует в регуляции гормонального обмена) количество гликогена в эпителии влагалища снижается, вследствие чего снижается и количество лактобацилл (проще говоря, им не хватает пищи). При повышении уровня эстрогенов (также эндокринные заболевания, прием гормональных контрацептивов, беременность) количества гликогена в клетках превышает норму, лактобациллы не успевают его перерабатывать и излишек гликогена достается транзиторной микрофлоре, которая начинает усиленно размножаться. Вполне вероятно и то, что снижение количества гликогена зависит и от вида принимаемой пищи, заболеваний печени и желудочно-кишечного тракта. Угнетение деятельности и (или) уничтожение лактобацилл:
лактобациллы такие же микробы, как и микробы, вызывающие заболевания у человека. Поэтому применение препаратов, уничтожающих болезнетворные микробы, также ведет к уничтожению и нормальных лактобацилл. Это, прежде всего прием антибиотиков по поводу различных заболеваний, местное применение антисептиков для профилактики венерических болезней - мирамистина, хлоргексидина, цидипола, применение местных противозачаточных препаратов, содержащих 9-нонксинол (следует не забывать, что этим веществом многие фирмы производители обрабатывают и поверхность презервативов). Патогенные микроорганизмы: при заражении женщины хламидиями, гонококками, вагинальной трихомонадой, уреаплазмой, микоплазмами в основном половым путем - внедрившиеся микробы ведут себя как завоеватели - уничтожая защитников влагалища - лактобациллы с помощью выработки различных экзотоксинов и освобождая себе жизненное пространство для размножения. Нередко в союзники к ним присоединяется транзиторная микрофлора - так как им, как и патогенной микрофлоре (хламидиям, гонококкам и уреаплазме) нужна не кислая, а щелочная среда во влагалище для дальнейшего размножения. Таким образом, под влиянием вышеизложенных факторов количество лактобацилл начинает уменьшаться вплоть до полного их исчезновения, в результате чего прекращается выработка молочной кислоты и происходит сдвиг рН в щелочную сторону. В более щелочной среде начинают усиленно размножаться представители транзиторной микрофлоры влагалища, вырабатывая в процессе своей деятельности вещества, которые еще более увеличивают сдвиг среды влагалища в щелочную сторону. Влагалище становиться беззащитным перед внедрением любой ацидофобной (не любящей кислоту инфекции). Развивается симптоматика бактериального вагиноза.
СИМПТОМЫ БАКТЕРИАЛЬНОГО ВАГИНОЗА.
Видимые клинические проявления: обильные выделения из половых путей белого или серого цвета, неприятный запах влагалищных выделений (тухлой рыбы), особенно после полового акта или во время менструации.
Лабораторные симптомы: незначительное количество или отсутствие нормальной микрофлоры; отсутствие воспалительной реакции (лейкоцитоза); повышенное количество кокковой микрофлоры; наличие так называемых "ключевых клеток" - эпителиальных клеток покрытых микроорганизмами; рН влагалища > 4.5; положительный аминотест - при добавлении 10% раствора КОН к выделениям - ощущается неприятный запах; обнаружение Gardnerella vaginalis, Mobiluncus species ,микоплазм.
Опасен ли для здоровья бактериальный вагиноз? Стоит ли его вообще лечить, если все дело в уменьшении нормальной микрофлоры? Ведь часто женщину, кроме будем называть "косметических проблем" - выделений с неприятным запахом, ничего не беспокоит. Мнение врачей и ученых - бактериальный вагиноз опасен для здоровья женщины, и его нужно лечить. С чем это связано? Есть несколько моментов, которые позволяют считать бактериальный вагиноз заболеванием, требующим лечения, а не особым состоянием влагалища с измененной микрофлорой
ОСЛОЖНЕНИЯ БАКТЕРИАЛЬНОГО ВАГИНОЗА
Патогенность транзиторной микрофлоры: до этого момента по отношению к транзиторной микрофлоре мы пользовались термином - условно-патогенная - т.е. условно-вредная для организма микрофлора. Под этим подразумевалось то, что эти микроорганизмы становятся вредными для организма только при определенных условиях. Вот как раз таким условием и является снижение кислотности влагалища и, вследствие этого, усиленное размножение транзиторных микробов. Соответственно эти микроорганизмы могут вызвать воспалительный процесс во влагалище - бактериальный вагинит и (или) проникнуть в вышележащие отделы половой системы - канал шейки матки, матку, яичники, маточные трубы. Снижение защитной функции влагалища: вследствие снижения кислотности влагалище женщины становиться легко доступным для инфицирования различными микроорганизмами. Прежде всего, это бактерии, вызывающие половые инфекции – гонококки, хламидии, трихомонада. Вероятность инфицирования ими у женщины с бактериальным вагинозом значительно выше, чем у здоровой женщины.
Дрожжеподобные грибы - частота кандидозных вагинитов у женщин с бактериальным вагинозом значительно выше, чем у здоровых женщин.
Инфицирование влагалища микроорганизмами, являющимися патогенной, условно-патогенной или нормальной микрофлорой для других органов организма: микроорганизмы, обитающие на коже человека (занос происходит контактным путем) - стрептококки, стафилококки, пропионбактерии; респираторные микроорганизмы - обитающие в верхних дыхательных путях (микоплазмы, хламидии, клебсиеллы, нейссерии) при оральном сексе (куннилингус) или гематогенным путем; кишечные бактерии (энтерококки, кишечная палочка) при контактном инфицировании - из-за анатомической близости влагалища к анусу или при чередующихся вагинальных и анальных контактах.
Все перечисленные микроорганизмы в большинстве случаев вызывают воспалительный процесс в различных отделах половой системы женщины. Потеря "эволюционной" функции влагалища:
как указывалась выше, кислая среда влагалища играет роль "эволюционного фильтра" т.е. преодолеть кислотный барьер может только самый подвижный и здоровый сперматозоид. В связи с ощелачиванием влагалища эта функция теряется и яйцеклетку может оплодотворить и неполноценный сперматозоид. Инфицирование транзиторной микрофлорой половых партнеров:
при определенных условиях мужчины - половые партнеры женщин больных бактериальным вагинозом могут инфицироваться от них транзиторной микрофлорой.
БАКТЕРИАЛЬНЫЙ ВАГИНОЗ КАК ПОЛОВАЯ ИНФЕКЦИЯ
Многолетние наблюдения и многочисленные результаты клинических и лабораторных исследований из личной практики убедительно доказывают инфицирование уретры мужчин (половых партнеров женщин больных бактериальным вагинозом) условно-патогенной транзиторной влагалищной микрофлорой. Мужская уретра, в отличие от здорового женского влагалища, имеет более щелочную среду, что является благоприятным фактором для обитания и размножения транзиторной влагалищной микрофлоры. Однако не все мужчины подвержены заражению. Среди инфицированных можно четко выделить три основные группы: лица, перенесшие в прошлом хламидийную и (или) гонококковую инфекцию; больные хроническим простатитом; лица, злоупотребляющие применением местных антисептиков для профилактики венерических болезней (мирамистин, хлоргексидин).
Видимо имеются какие-то факторы, связанные со снижением антибактериальной защиты (снижение содержания цинка в секрете простаты у больных хроническим простатитом), повреждением слизистой уретры, нарушением микроциркуляции крови, с изменением состава нормальной микрофлоры ладьевидной ямки уретры. Инфицирование уретры транзиторной микрофлорой влагалища протекает по следующим вариантам: носительство - наиболее частый вариант - при этом мужчину абсолютно ничего не беспокоит, носительство выявляется только при обследовании высокоточными лабораторными методами. Эти мужчины - переносчики транзиторной микрофлоры (у них, кстати, она тоже может находиться временно) и при частых случайных половых контактах они являются как бы основным резервуаром и распространителями транзиторных микроорганизмов среди женщин. Баланопостит - очень часто у больных бактериальным баланопоститом выявляются представители транзиторной влагалищной микрофлоры. Важен факт, что при назначении специфического лечения явления баланопостита исчезают. Уретрит - у определенной части больных транзиторная микрофлора вызывает воспалительный процесс в уретре. Симптомы аналогичны бактериальному вагинозу - обильные серо-белые выделения с неприятным рыбным запахом, но в отличие от вагиноза имеется лейкоцитарная реакция (до 15-30 лейкоцитов в поле зрения микроскопа), также у этих больных при микроскопии выявляются и "ключевые клетки".
ЛЕЧЕНИЕ БАКТЕРИАЛЬНОГО ВАГИНОЗА
Представляет чрезвычайно трудную задачу и требует большого терпения, как от врача, так и от больной. Уничтожить транзиторную микрофлору не представляет особой проблемы, гораздо сложнее восстановить нормальную лактофлору влагалища. Очень важно выявить и устранить предрасполагающие к вагинозу факторы.
You are using an outdated browser. Please upgrade your browser to improve your experience.
Правила обработки рук медперсонала – важнейший компонент безопасности оказания медицинской помощи
Инфекции, связанные с оказанием медицинской помощи (ИСМП), являются основной проблемой при обеспечении безопасности пациентов, именно поэтому предотвращение их возникновения должно быть приоритетной задачей для медицинских организаций любого профиля. По данным ВОЗ, из 100 госпитализированных пациентов как минимум 7 заражаются ИСМП. В связи с этим ВОЗ разработало руководство по гигиене рук в здравоохранении, направленное на профилактику инфекций, связанных с оказанием медицинской помощи.
Поверхностный слой эпидермиса (верхний слой кожи) полностью замещается каждые 2 недели. Ежедневно со здоровой кожи сшелушивается до 100 млн. кожных чешуек, из которых 10% содержат жизнеспособные бактерии. Микрофлору кожи можно разделить на две большие группы:
- Резидентная флора
- Транзиторная флора
Резидентная микрофлора - это те микроорганизмы, которые постоянно живут и размножаются на коже, не вызывая никаких заболеваний. То есть это нормальная флора. Численность резидентной флоры составляет примерно 10 2 -10 3 на 1 см 2 . Резидентная флора представлена преимущественно коагулазонегативными кокками (прежде всего Staphylococcus epidermidis) и дифтeроидами (Corinebacterium spp.). Несмотря на то, что Staphylococcus aureus обнаруживается в носу примерно 20% здоровых людей, он редко колонизирует кожу рук (если она не повреждена), однако в госпитальных условиях может обнаруживаться на коже рук медицинского персонала с не меньшей частотой, чем в носу.
Резидентную микрофлору невозможно уничтожить с помощью обычного мытья рук или даже антисептических процедур, хотя их численность при этом значительно снижается. Стерилизация кожи рук не только невозможна, но и нежелательна: потому что нормальная микрофлора препятствует колонизации кожи другими, гораздо более опасными микроорганизмами, прежде всего грамотрицательными бактериями.
Транзиторная микрофлора - это те микроорганизмы, которые приобретаются медицинским персоналом в результате контакта с инфицированными пациентами или загрязнёнными объектами окружающей среды. Транзиторная флора может быть представлена гораздо более опасными в эпидемиологическом отношении микроорганизмами (E.coli, Klebsiella spp., Pseudomonas spp., Salmonella spp. и другие грамотрицательные бактерии, S.aureus, C. albicans, ротавирусы и др.), в том числе госпитальными штаммами возбудителей внутрибольничных инфекций. Транзиторные микроорганизмы сохраняются на коже рук короткое время (редко более 24 часов). Они легко могут быть удалены с помощью обычного мытья рук или уничтожены при использовании антисептиков. Пока эти микробы сохраняются на коже, они могут передаваться пациентам при контакте и загрязнять различные объекты. Это обстоятельство делает руки персонала важнейшим фактором передачи внутрибольничной инфекции.
Наиболее загрязненные участки кожи рук:
Наиболее сложно промываемые участки кожи рук:
• выемка большого пальца
В медицинской практике того времени было широко распространено увлечение врачей препарированием трупов. При этом после посещения анатомического театра врачи шли к пациенткам, не обработав руки, а попросту протерев их носовым платком.
Существовало множество различных теорий происхождения родильной лихорадки, но открыть истинные причины ее распространения удалось лишь венскому врачу Игнацу Филиппу Земмельвейсу. 29-летний доктор предположил, что основной причиной послеродовых осложнений служит контаминация рук медицинского персонала трупным материалом.
Земмельвейс обратил внимание, что раствор хлорной извести устраняет запах гниения, а значит, может уничтожить и заразное начало, присутствующее в трупах. Наблюдательный доктор предложил осуществлять обработку рук акушеров хлорным раствором, что привело к снижению летальности в клинике в 10 раз. Несмотря на это, открытие Игнаца Земмельвейса было отвергнуто современниками и получило признание лишь после его смерти.
Виды обработки рук
Обработка рук делится на три уровня:
- Бытовой уровень (механическая обработка рук)
- Гигиенический уровень (обработка рук с применением кожных антисептиков)
- Хирургический уровень (особая последовательность манипуляций при обработке рук с последующим одеванием стерильных перчаток)
Цель бытового уровня обработки рук — механическое удаление с кожи большей части транзиторной микрофлоры (антисептики не применяются).
Подобная обработка рук проводится:
- после посещения туалета;
- перед едой или перед работой с продуктами питания;
- перед и после физического контакта с пациентом;
- при любом загрязнении рук.
Необходимое оснащение:
- Жидкое дозированное нейтральное мыло или индивидуальное одноразовое мыло в кусочках. Желательно, чтобы мыло не имело резкого запаха. Открытое жидкое или брусковое многоразовое неиндивидуальное мыло быстро инфицируется микробами.
- Салфетки размером 15х15 см одноразовые, чистые для промокания рук. Использование полотенца (даже индивидуального) не желательно, т. к. оно не успевает просохнуть и, кроме того, легко обсеменяется микробами.
Правила обработки рук:
Снимаются с рук все украшения, часы, поскольку они затрудняют удаление микроорганизмов. Руки намыливаются, затем ополаскиваются тёплой проточной водой и всё повторяется сначала. Считается, что при первом намыливании и ополаскивании тёплой водой микробы смываются с кожи рук. Под воздействием тёплой воды и самомассажа поры кожи открываются, поэтому при повторном намыливании и ополаскивании смываются микробы из раскрывшихся пор.
Тёплая вода способствует более эффективному воздействию антисептика или мыла, в то время как горячая вода удаляет с поверхности рук защитный жировой слой. В связи с этим следует избегать употребления слишком горячей воды для мытья рук.
Обработка рук — необходимая последовательность движений
1. Тереть одну ладонь о другую ладонь возвратно-поступательными движениями.
Каждое движение повторяется не менее 5 раз. Обработка рук осуществляется в течение 30 секунд - 1 минуты.
Очень важно соблюдать описанную технику мытья рук, поскольку специальные исследования показали, что при рутинном мытье рук определённые участки кожи (кончики пальцев и их внутренние поверхности) остаются загрязнёнными.
После последнего ополаскивания руки насухо вытираются салфеткой (15х15 см). Этой же салфеткой закрываются водопроводные краны. Салфетка сбрасывается в ёмкость с дезинфицирующим раствором для утилизации.
При отсутствии одноразовых салфеток возможно использование кусков чистой ткани, которые после каждого использования сбрасываются в специальные контейнеры и после дезинфекции отправляются в прачечную. Замена одноразовых салфеток на электрические сушилки нецелесообразна, т.к. при них не происходит растирания кожи, а значит не происходит удаление остатков моющего вещества и слущивания эпителия.
Цель гигиенической обработки — уничтожение микрофлоры кожи при помощи антисептиков (дезинфекция).
Подобная обработка рук проводится:
- перед одеванием перчаток и после их снятия;
- перед уходом за пациентом с ослабленным иммунитетом или при проведении обходов в палатах (когда нет возможности мыть руки после осмотра каждого больного);
- перед и после выполнения инвазивных процедур, малых хирургических манипуляций, ухода за раной или катетером;
- после контакта с биологическими жидкостями (например, аварийные ситуации с кровью).
Необходимое оснащение:
- Жидкое дозированное рН-нейтральное мыло или индивидуальное одноразовое мыло в кусочках.
- Салфетки размером 15х15 см одноразовые, чистые.
- Кожный антисептик. Целесообразно использовать спиртосодержащие кожные антисептики (70% раствор этилового спирта; 0,5% раствор хлоргексидина биглюконата в 70% этиловом спирте, АХД-2000 специаль, Стериллиум и др.)
Правила обработки рук:
Гигиеническая обработка рук состоит из двух этапов: механической очистки рук и дезинфекции рук кожным антисептиком.
После окончания этапа механической очистки (двукратное намыливание и ополаскивание) антисептик наносится на кисти рук в количестве не менее 3 мл и тщательно втирается в кожу до полного высыхания (вытирать руки не следует). Если руки не были загрязнены (например, отсутствовал контакт с пациентом), то первый этап пропускается и можно сразу наносить антисептик. Последовательность движений при обработке рук соответствует схеме EN-1500. Каждое движение повторяется не менее 5 раз. Обработка рук осуществляется в течение 30 секунд - 1 минуты.
Хирургическая обработка рук
Цель хирургического уровня обработки рук — минимизация рисканарушения операционной стерильности в случае повреждения перчаток.
Подобная обработка рук проводится:
- перед оперативными вмешательствами;
- перед серьёзными инвазивными процедурами (например, пункция крупных сосудов).
Необходимое оснащение:
- Жидкое дозированное рН-нейтральное мыло или индивидуальное одноразовое мыло в кусочках.
- Салфетки размером 15х15 см одноразовые, стерильные.
- Кожный антисептик.
- Перчатки одноразовые стерильные хирургические.
Правила обработки рук:
Хирургическая обработка рук состоит из трёх этапов: механической очистки рук, дезинфекции рук кожным антисептиком, закрытии рук стерильными одноразовыми перчатками.
1. В отличии от вышеописанного способа механической очистки на хирургическом уровне в обработку включаются предплечья, для промокания используются стерильные салфетки, а само мытьё рук длится не менее 2 минут. После высушивания дополнительно обрабатываются ногтевые ложа и околоногтевые валики одноразовыми стерильными деревянными палочками, смоченными в растворе антисептика.
Щётки применять не обязательно. Если щётки все же применяются, то следует применять стерильные мягкие щётки однократного применения или способные выдержать автоклавирование, при этом пользоваться щётками следует только для обработки околоногтевых областей и только для первой обработки в течение рабочей смены.
2. После окончания этапа механической очистки на кисти рук наносится антисептик порциями по 3 мл и, не допуская высыхания, втирается в кожу, строго соблюдая последовательность движений схемы EN-1500. Процедура нанесения кожного антисептика повторяется не менее двух раз, общий расход антисептика — 10 мл, общее время процедуры — 5 минут.
3. Стерильные перчатки надеваются только на сухие руки. При продолжительности работы в перчатках более 3 часов обработка повторяется со сменой перчаток.
4. После снятия перчаток руки вновь протираются салфеткой, смоченной кожным антисептиком, затем моются с мылом и увлажняются смягчающим кремом.


ТРАНЗИТОРНАЯ МИКРОФЛОРА МОЧЕПОЛОВЫХ ОРГАНОВ
Транзиторная микрофлора - это условно-патогенная микрофлора мочеполовых органов, постоянное присутствие которой нехарактерно для здорового человека и которая при определенных условиях может вызывать воспалительный процесс в мочеполовых органах и передаваться половым путем. Поэтому все состояния и заболевания, связанные с наличием транзиторной микрофлоры нужно определять как инфекцию.
В процессе эволюции часть микроорганизмов получила способность колонизировать мочеполовые органы человека, вызывая при этом у части людей заболевания. В большинстве случаев эти микроорганизмы жизнеспособны в мочеполовых органах только определенное время, а затем уничтожаются различными защитными механизмами. Поэтому такая микрофлора половых органов названа временной - транзиторной. Но у определенной части людей, которые имеют различные нарушения защитных механизмов мочеполовой системы, транзиторная микрофлора вызывает различные воспалительные процессы и заболевания.
КАКИЕ ИМЕЮТСЯ ГРУППЫ
ТРАНЗИТОРНОЙ МИКРОФЛОРЫ
Можно выделить несколько групп микроорганизмов, которые могут колонизировать мочеполовые органы человека:
Мочеполовые микроорганизмы
Для них обычной средой обитания являются мочеполовые органы человека, в которых при определенных условиях они могут размножаться.
Это, прежде всего генитальные микоплазмы : М.hominis,M.genitalium, М. fermentans, U.urealyticum , U.parvum
Респираторные микроорганизмы
Для микробов этой группы средой обитания являются полость рта, глотка и верхние дыхательные пути. Часть из них являются патогенными (вредными) для организма, часть нормальной микрофлорой. Инфицирование мочеполовых органов ими происходит во время орально-генитальных контакт ов. К ним относят:
Микоплазмы, патогенные - M.pneumoniae (пневмонийная), и являющиеся вариантом нормальной микрофлоры полости рта - M.orale, M.salivarum, M.buccalae (ротовая,слюнная,щечная)
Представители рода Neisseria species (sp. ) : N. meningitidis,N. sicca, N. subflava, N. flava, N. mucosa - так называемые негонококковые нейссерии.
Кишечные микроорганизмы
Для этих микробов средой обитания являются толстый кишечник и прямая кишка. Инфицирование происходит при анально-генитальных контактах или заносом женщинам из прямой кишки из-за анатомической близости ануса и влагалища либо гематогенным и лимфогенным путем (чаще у мужчин).
КАКОЙ МЕХАНИЗМ ЗАЩИТЫ
ПОЛОВЫХ ОРГАНОВ У ЖЕНЩИН
Состояние верхних отделов репродуктивного тракта во многом зависит от механизмов защиты влагалища:
Механическая защита
Слизистая пробка цервикального канала обеспечивает механическую преграду за счет вязкости, а также содержит антимикробные субстанции и антитела (секреторный IgА, лизоцим).
Менструация (отторжение функционального слоя эндометрия, формирование на его месте лимфоцитарного вала, препятствует длительному пребыванию патогенных микроорганизмов).
Также важную функцию механического удаления бактерий из влагалища осуществляют физиологические бели (секреция в норме 2 мл/сут) и физиологическая десквамация эпителия.
Иммунологические факторы
Локальная иммунологическая защита осуществляется макрофагами слизистой влагалища и локальными секреторными иммуноглобулинами IgA. происходит в клетках влагалища и лизоцимом слизистой оболочки
Нормальная микрофлора влагалища и кислотность влагалища
Нормальная лактобациллярная микрофлора влагалища играет ключевую роль в защите от транзиторной и патогенной микрофлоры. Помимо конкурирования за питательные вещества (гликоген влагалища), выделения бактерицинов и стимуляции местной иммунной системы, нормальная микрофлора создает кислую среду влагалища, которой многие исследователи придают определяющее значение в защите от условно-патогенных и патогенных бактерий.
КАКОЙ МЕХАНИЗМ ЗАЩИТЫ
ПОЛОВЫХ ОРГАНОВ У МУЖЧИН
Стафилококки уретры не являются защитными факторами мочеполовых органов как лактобациллы влагалища женщины, а в некоторых случаях сами являются причиной воспалительных процессов. Поэтому механизм защиты уретры у мужчин представлен иначе:
Механическая защита
Представлена заслонкой Герена, отделяющей ладьевидную ямку (вход в уретру) от передней уретры, уретральными железами Литтре, выделяющим уретральную слизь и бульбоуретральными железами Купера, выделяющим специфический секрет во время семяизвержения. Заслона Герена осуществляет частично барьерную функцию, а железы Литтре и Купера способствуют механическому удалению микроорганизмов из уретры.
Нейтральная или слабощелочная среда уретры
Создается уретральным секретом и секретом предстательной железы. Такая среда препятствует размножению ацидофильных бактерий в уретре (например, нормальных лактобацилл влагалища, кандид)
Локальная иммунологическая защита
Осуществляется макрофагами слизистой уретры и локальными секреторными иммуноглобулинами IgA, активная продукция которых происходит в клетках слизистой уретры и в предстательной железе, а также лизоцимом уретрального секрета.
Цинк-пептидный комплекс секрета простаты
Цинк-пептидный комплекс или противомикробный фактор простаты, который обладает выраженной противомикробной активностью и способствует поддержанию нейтрально-щелочной среды уретры. Концентрация цинка в секрете простаты у здорового мужчины более чем в 100 раз превышает концентрацию его в других органах.

Природой установлен защитный механизм противодействия - в кислой среде влагалища не приживаются микроорганизмы уретры мужчин, в нейтрально-щелочной среде уретры мужчины не приживаются микроорганизмы влагалища женщины. Нейтральная среда мочеполовых органов мужчины способствует выживанию всех сперматозоидов, кислая среда влагалища женщины осуществляет эволюционный контроль - уничтожая недоразвитых спермиев.
КАК ПРОТЕКАЮТ ТРАНЗИТОРНЫЕ ИНФЕКЦИИ
Временное носительство (транзит)
Наиболее часто встречающийся вариант - попавшая в мочеполовые органы транзитная микрофлора находится в них от нескольких часов до нескольких недель, после чего уничтожается защитными механизмами. Во время временного носительства-транзита носитель может передать инфекцию половым партнерам. Во время транзита возбудитель в мочеполовых органах можно определить высокоточными диагностическими исследованиями - полимеразной цепной реакцией - ПЦР.
Стойкое носительство (позитивность)
Довольно часто встречающийся вариант - транзитные микроорганизмы постоянно находится в мочеполовых органах, но в незначительном количестве - размножению препятствуют механизмы защиты и конкурирующая нормальная микрофлора. Полного уничтожения транзиторной микрофлоры нет - это должно настораживать в отношении наличия компенсированных форм бактериального вагиноза у женщин или умеренных изменений в простате у мужчин. При сбое защиты и (или) при снижении количества нормальных микробов возможно бурное размножение транзитной микрофлоры, которое организм пытается подавить лейкоцитарной реакцией - развивается воспалительный процесс. Носительство протекает бессимптомно (за исключением периодов обострения), возбудители определяются методом ПЦР. Носители передают инфекцию половым партнерам.
Развитие и проявление заболеваний
При определенных условиях организм не может сдерживать размножение транзиторной микрофлоры, в результате чего в мочеполовых органах развиваются воспалительные процессы типичные для половых инфекций ( уретрит , вагинит , цистит , эндоцервицит , простатит , орхоэпидидимит , ВЗОМТ ).
Основные причины активизации транзитной микрофлоры и превращения ее в патогенную для организма:
Перенесенные ранее половые инфекции - хламидийная и гонококковая инфекции, вследствие которых из-за рубцующихся процессов, часть слизистой оболочки мочеполовых органов не обеспечивает нужного уровня клеточного и гуморального местного иммунитета, что способствует колонизации транзитной микрофлоры.
Основными причинами колонизации и размножения транзитной микрофлоры в мочеполовых органах являются : снижение лактобацилл во влагалище у женщин при бактериальном вагинозе и, возможно, снижение уровня цинка в секрете простаты у мужчин при хроническом простатите.
КАК ПРОТЕКАЮТ ТРАНЗИТОРНЫЕ ИНФЕКЦИИ У ЖЕНЩИН

ТЕЧЕНИЕ ТРАНЗИТОРНЫХ ИНФЕКЦИЙ У ЖЕНЩИН
Для женщин характерно стойкое носительство транзиторной микрофлоры, инфицирование представителями транзитной микрофлоры происходит при половых контактах, чем больше половых контактов у женщины, тем больше риск ее инфицирования. Однако это представляет для женщины опасность только в эпидемиологическом плане (заражение половых партнёров) и при беременности (инфицирование плода и новорожденного).
КАК ПРОТЕКАЮТ ТРАНЗИТОРНЫЕ ИНФЕКЦИИ У МУЖЧИН
В подавляющем большинстве случаев у мужчин отмечается временное носительство транзиторной микрофлоры (от несколько часов до нескольких недель). В этот период они не предъявляют никаких жалоб и даже при пристальном клинико-лабораторном обследовании не выявляются признаки патологии, а представители транзиторной микрофлоры выявляются только при применении высокоточных методов диагностики. Однако в этот период они представляют опасность для инфицирования половых партнеров.
КАК ПЕРЕДАЮТСЯ ТРАНЗИТОРНЫЕ ИНФЕКЦИИ
Транзиторными инфекциями можно инфицироваться только тремя способами:
Половой контакт, в том числе и орально-генитальный и анально-генитальный самый частый путь инфицирования.
Вертикальный путь передачи от матери к плоду. Заражение происходит несколькими путями.
При наличии восходящей внутриматочной инфекции транзиторные микроорганизмы получают доступ к амниотическому мешочку, где они размножаются и переходят в легкие эмбриона. Это может произойти на ранних стадиях беременности, даже когда эмбриональные мембраны не повреждены, и инфекция может сохраняться в течение нескольких недель.
Внутриутробное проникновение транзиторных бактерий может также произойти гематогенным путем через инфицированную плаценту (через сосуды пуповины). Внутриматочная инфекция может привести к хориоамниониту, распространению на органы эмбриона и к развитию врожденных заболеваний.
Наконец, заражение транзиторными микроорганизмами новорождённых может произойти через инфицированные материнские родовые пути, что приводит к колонизации на коже, мембранах слизистой оболочки половых органов, конъюнктиве глаз, дыхательном тракте.
При трансплантации органов - редкий, но встречающийся путь инфицирования.
Основной резервуар транзиторных инфекций сексуально - активные женщины (более двух половых партнеров в год) со стойким носительством. В большинстве случаев мужчины являются временными носителями транзиторных инфекций, однако сохраняя способность во время транзита инфицировать женщин-половых партнеров.
Транзиторные иммунодефициты. Механизм развития транзиторных иммунодефицитов. Иммунотерапия. Иммунопрофилактика. Иммунобиологические препараты.
Многие инфекционные заболевания сопровождаются дефектами иммунной реактивности. Подобные нарушения известны ещё со времён фон Пирке (начало XX века), однако в большинстве случаев они носят временный характер и исчезают после выздоровления.
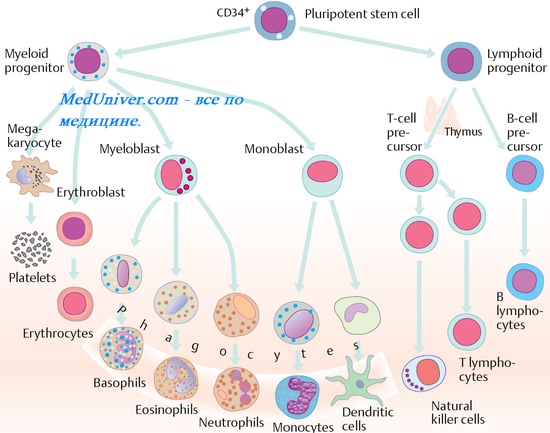
Основополагающий механизм развития транзиторных иммунодефицитов — повреждение или инфицирование иммунокомпетентных клеток с последующим нарушением их функций. Особенно часто транзиторные иммунодефицита наблюдают на фоне вирусных инфекций, что обусловлено облигатным внутриклеточным паразитизмом возбудителей. Наиболее яркий пример — ВИЧ, избирательно инфицирущий Т-хелперы. В результате развивается прогрессирующее разрушение иммунной системы — синдром приобретённого иммунодефицита (СПИД).
Иммунотерапия. Иммунопрофилактика. Иммунобиологические препараты
Иммунотерапия — введение с лечебными целями иммунных препаратов (например, AT, ИФН, цитокинов и др.). Иммунопрофилактика — введение иммунных препаратов с целью предотвращения развития инфекционных заболеваний (вакцины, сыворотки). На протяжении столетий практическая медицина применяла эмпирические методы искусственной защиты от инфекционных болезней (например, от оспы). Научные основы иммунопрофилактики были заложены исследованиями Пастера, открывшего феномен аттенуации (ослабления) микробов и создавшего вакцины против сибирской язвы и бешенства.
Все средства, применяемые для воздействия на иммунную систему, известны как иммунобиологические препараты. К ним относят разнообразные по природе и происхождению вещества.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Бессимптомные инфекции. Абортивная инфекция. Латентная ( скрытая ) инфекция. Инаппарантные инфекции. Дремлющие инфекции. Микробоносительство.
• Абортивная инфекция [от лат. aborto, не вынашивать, в данном контексте — не реализовывать патогенный потенциал] — одна из наиболее распространённых форм бессимптомных поражений. Такие процессы могут возникать при видовой или внутривидовой, естественной либо искусственной невосприимчивости (поэтому человек не болеет многими болезнями других животных). Механизмы невосприимчивости эффективно блокируют жизнедеятельность микроорганизмов, возбудитель не размножается в организме, инфекционный цикл возбудителя прерывается, он погибает и удаляется из макроорганизма.
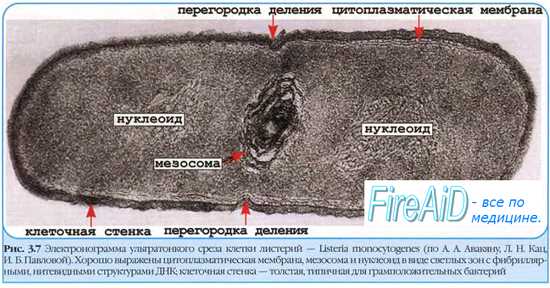
• Латентная, или скрытая, инфекция [от лат. latentis, спрятанный] — ограниченный процесс с длительной и циклической циркуляцией возбудителя, аналогичной наблюдаемой при явных формах инфекционного процесса. Возбудитель размножается в организме; вызывает развитие защитных реакций, выводится из организма, но никаких клинических проявлений не наблюдают. Подобные состояния также известны как инаппарантные инфекции (от англ. inapparent, неявный, неразличимый). Так, нередко в латентной форме протекают вирусные гепатиты, полиомиелит, герпетические инфекции и т.д. Лица с латентными инфекционными поражениями представляют эпидемическую опасность для окружающих.
• Дремлющие инфекции могут быть разновидностью латентных инфекций или состояниями после перенесённого и клинически выраженного заболевания. Обычно при этом устанавливается клинически не проявляемый баланс между патогенными потенциями возбудителя и защитными системами организма. Однако под влиянием различных факторов, понижающих резистентность (стрессы, переохлаждения, нарушения питания и т.д.), микроорганизмы приобретают возможность оказывать патогенное действие. Таким образом, лица, переносящие дремлющие инфекции, — резервуар и источник патогена.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

