Трава от астмы и туберкулез
Обновлено: 24.04.2024
Бронхиальная астма — заболевание, с которым все чаще сталкиваются врачи в последнее время. Это неудивительно, ибо, по данным международных исследований, в развитых странах мира около 5% взрослого населения и почти 10% детей страдают этим недугом.
Бронхиальная астма — заболевание, с которым все чаще сталкиваются врачи в последнее время. Это неудивительно, ибо, по данным международных исследований, в развитых странах мира около 5% взрослого населения и почти 10% детей страдают этим недугом. Кроме того, в последние десятилетия прослеживается четкая тенденция роста заболеваемости аллергическими болезнями, в том числе бронхиальной астмой.
В свою очередь, современная терапия бронхиальной астмы базируется на вышеупомянутой концепции, на основании которой определяются форма и степень тяжести заболевания.
Согласно современным представлениям, бронхиальная астма независимо от тяжести ее течения является хроническим воспалительным заболеванием дыхательных путей, в формировании которого участвуют многие клетки: тучные клетки, эозинофилы и Т-лимфоциты. При наличии предрасположенности это воспаление приводит к повторяющимся эпизодам хрипов, одышки, тяжести в грудной клетке и кашлю, особенно ночью и/или ранним утром. Эти симптомы обычно сопровождаются распространенной, но вариабельной обструкцией бронхов, которая по крайней мере частично обратима спонтанно или под влиянием лечения. Воспаление приводит к формированию повышенной чувствительности дыхательных путей к самым различным стимулам, которые у здоровых лиц никакой реакции не вызывают. Это состояние — бронхиальная гиперреактивность, которая может быть специфической и неспецифической. Специфическая гиперреактивность представляет собой повышенную чувствительность бронхов к определенным, специфическим аллергенам, вызвавшим развитие астмы. Под неспецифической гиперреактивностью понимают повышенную чувствительность к разнообразным неспецифическим стимулам неаллергенной природы: холодному воздуху, физической нагрузке, резким запахам, стрессам и пр. Одним из важных признаков гиперреактивности, используемых для оценки степени тяжести бронхиальной астмы, является суточная вариабельность пиковой скорости выдоха (ПСВ), составляющая 20% и более.
Установление формы бронхиальной астмы имеет принципиальное значение для ее терапии, ибо лечение любого аллергического заболевания начинается с мероприятий по элиминации аллергена (или аллергенов), виновного в развитии болезни. Можно полностью удалить аллерген, если речь идет о домашнем животном, пищевом продукте или лекарственном препарате, и уже только благодаря этому добиться ремиссии бронхиальной астмы. Но чаще развитие астмы провоцирует клещ домашней пыли, которого не удается удалить полностью. Однако количество пылевых клещей можно существенно сократить, используя специальные безаллергенные постельные принадлежности и акарицидные средства, проводя регулярную влажную уборку с помощью пылесоса с глубокой степенью очистки. Все эти мероприятия, равно как и меры по сокращению содержания пыльцы в воздухе жилых помещений в сезон цветения и меры, позволяющие минимизировать контакт со спорами внедомашних и внутридомашних непатогенных плесневых грибов, приводят к значительному ослаблению симптомов бронхиальной астмы у чувствительных к этим аллергенам пациентов.
Фармакотерапия — неотъемлемая и важнейшая составляющая комплексной лечебной программы бронхиальной астмы. Существует несколько ключевых положений в терапии бронхиальной астмы:
- астму можно эффективно контролировать у большинства пациентов, однако вылечить ее не удается;
- ингаляционный способ введения препаратов при астме наиболее предпочтителен и эффективен;
- базисная терапия астмы предполагает применение противовоспалительных препаратов, в частности ингаляционных глюкокортикостероидов, которые в настоящее время являются наиболее эффективными препаратами, контролирующими астму;
- бронходилататоры (β2-агонисты, ксантины, холинолитики) являются препаратами неотложной помощи, купирующими бронхоспазм.
Итак, все препараты, которые используются для лечения бронхиальной астмы, принято делить на две группы: базисные или лечебные, то есть обладающие противовоспалительным эффектом, и симптоматические, обладающие преимущественно быстрой бронхолитической активностью. Однако за последние годы на фармакологическом рынке появилась новая группа противоастматических препаратов, которые представляют собой комбинацию противовоспалительных и бронхолитических средств.
К базисным противовоспалительным препаратам относятся глюкокортикостероиды, стабилизаторы тучных клеток — кромоны и ингибиторы лейкотриенов.
Ингаляционные глюкокортикостероиды (беклометазон дипропионат, флютиказон пропионат, будесонид, флунизолид) в настоящее время являются препаратами выбора для лечения среднетяжелой и тяжелой астмы. Более того, согласно международным рекомендциям, ингаляционные глюкокортикостероиды (ИГКС) показаны всем больным с персистирующей астмой, в том числе и с легким течением, ибо даже при этой форме астмы в слизистой дыхательных путей присутствуют все элементы хронического аллергического воспаления. В отличие от системных стероидов, которые, в свою очередь, являются средством выбора при острой тяжелой астме, ИГКС не имеют тяжелых системных побочных эффектов, представляющих угрозу для больного. Лишь в высоких суточных дозах (выше 1000 мкг) они могут угнетать функцию коры надпочечников. Многофакторное противовоспалительное действие ингаляционных глюкокортикостероидов проявляется в их способности снижать или даже вовсе устранять бронхиальную гиперреактивность, восстанавливать и повышать чувствительность β2-адренорецепторов к катехоламинам, в том числе к препаратам β2-агонистам. Доказано, что противовоспалительная эффективность ИГКС зависит от дозы, поэтому целесообразно начинать лечение со средних и высоких доз (в зависимости от тяжести астмы). При достижении стабильного состояния больных (но не ранее чем через 1-3 месяца от начала терапии ИГКС) и улучшении показателей ФВД дозу ИГКС можно снизить, но не отменять! В случае ухудшения течения астмы и снижения функциональных легочных показателей доза ИГКС должна быть повышена. Возникновения таких неопасных, но нежелательных побочных эффектов ИГКС, как кандидоз ротовой полости, дисфония, раздражающий кашель, можно избежать благодаря применению спейсеров, а также полосканию ротовой полости и горла слабым раствором соды или просто теплой водой после каждой ингаляции препарата.
Кромогликат натрия и недокромил натрия (кромоны) подавляют выделение медиаторов из тучной клетки путем стабилизации ее мембраны. Эти препараты, назначенные до начала воздействия аллергена, способны угнетать раннюю и позднюю аллергические реакции. Их противовоспалительный эффект значительно уступает таковому у ИГКС. Снижение бронхиальной гиперреактивности происходит лишь после длительного (не менее 12 недель) лечения кромонами. Однако преимущество кромонов — в их безопасности. Эти препараты практически не дают побочных эффектов и поэтому с успехом применяются для лечения детской астмы и астмы у подростков. Атопическая астма легкого течения у взрослых иногда также хорошо контролируется кромогликатом или недокромилом натрия.
Таким образом, новые противоастматические препараты — антагонисты лейкотриеновых рецепторов могут использоваться для противовоспалительной (базисной) терапии астмы в следующих ситуациях [5]:
- легкая, персистирующая астма;
- детская астма;
- астма физических нагрузок;
- аспириновая астма;
- ночная астма;
- острая аллерген-индуцированная астма;
- средняя и тяжелая астма;
- ГКС-фобия;
- астма, которая неудовлетворительно контролируется безопасными дозами ГКС;
- лечение пациентов, у которых возникают трудности при пользовании ингалятором;
- лечение пациентов, у которых диагностирована астма в сочетании с аллергическим ринитом.
Препараты бронхолитического действия применяются как для купирования острого приступа астмы при хроническом ее течении, так и для профилактики астмы физических нагрузок, острой астмы, индуцированной аллергеном, а также для снятия тяжелого бронхоспазма при обострении бронхиальной астмы.
Ключевые положения в бронхолитической терапии бронхиальной астмы:
- β2-агонисты короткого действия являются наиболее эффективными бронхолитиками;
- ингаляционные формы бронхолитических препаратов предпочтительнее по сравнению с оральными и парентеральными формами.
Селективные β2-агонисты первой генерации [3]: албутерол (сальбутамол, вентолин), тербуталин (бриканил), фенотерол (беротек) и другие — представляют собой наиболее эффективные бронхолитики. Они способны быстро (в течение 3-5 мин) и на довольно долгий срок (до 4-5 ч) оказывать бронхолитическое действие после ингаляции в виде дозированного аэрозоля при легких и среднетяжелых приступах астмы, а при использовании растворов этих препаратов через небулайзер — и при тяжелых приступах в случае обострения астмы. Однако β2-агонисты короткого действия следует применять только для купирования приступа удушья. Они не рекомендуются для постоянной, базисной терапии, так как не способны уменьшать воспаление дыхательных путей и бронхиальную гиперреактивность. Более того, при постоянном и длительном их приеме степень бронхиальной гиперреактивности может возрастать, а показатели функции внешнего дыхания — ухудшаться [3]. Этих недостатков лишены β2-агонисты второй генерации, или β2-агонисты длительного действия: сальметерол и формотерол. В силу липофильности своих молекул эти препараты очень близки β2-адренорецепторам, чем прежде всего и определяется длительность их бронхолитического действия — до 12 ч после ингаляции 50 мкг или 100 мкг сальметерола и 6 мкг, 12 мкг или 24 мкг формотерола. При этом формотерол кроме длительного действия одновременно оказывает и быстрое бронхорасширяющее действие, сопоставимое со временем начала действия сальбутамола. Все препараты β2-адреномиметики обладают способностью ингибировать высвобождение медиаторов аллергического воспаления, таких, как гистамин, простагландины и лейкотриены, из тучных клеток, эозинофилов, причем максимально это свойство проявляется у β2-агонистов длительного действия. Кроме того, последние обладают способностью уменьшать проницаемость капилляров слизистой бронхиального дерева. Все это позволяет говорить о противовоспалительном эффекте β2-агонистов длительного действия. Они способны подавлять как раннюю, так и позднюю астматические реакции, возникающие после ингаляции аллергена, и снижать бронхиальную реактивность. Эти препараты являются средством выбора при легкой и среднетяжелой астме, а также у пациентов с ночными симптомами астмы; их можно использовать также для профилактики астмы физических нагрузок [1]. У пациентов со среднетяжелой и тяжелой астмой их целесообразно сочетать с ИГКС.
Теофиллины — основной вид метилксантинов, используемых в лечении астмы. Теофиллины обладают бронхолитическим и противовоспалительным действием. Блокируя фермент фосфодиэстеразу, теофиллин стабилизирует цАМФ и снижает концентрацию внутриклеточного кальция в клетках гладкой мускулатуры бронхов (и других внутренних органов), тучных клетках, Т-лимфоцитах, эозинофилах, нейтрофилах, макрофагах, эндотелиальных клетках. В результате происходят расслабление гладкой мускулатуры бронхов, подавление высвобождения медиаторов из клеток воспаления и снижение повышенной сосудистой проницаемости. Теофиллин в значительной степени подавляет как раннюю, так и позднюю фазы астматической реакции. Пролонгированные теофиллины успешно применяются для контроля ночных астматических проявлений. Однако эффективность теофиллина при острых приступах астмы уступает (как по скорости наступления эффекта, так и по его выраженности) β2-агонистам, применяемым ингаляционно, особенно через небулайзер. Поэтому внутривенное введение эуфиллина должно рассматриваться как резервное мероприятие для тех пациентов с острой тяжелой астмой, для которых прием β2-агонистов через небулайзер оказывается недостаточно эффективным [1]. Это ограничение обусловлено еще и высоким риском возникновения побочных реакций на теофиллин (сердечно-сосудистые и желудочно-кишечные расстройства, возбуждение ЦНС), развивающихся, как правило, при превышении концентрации 15 мкг/мл в периферической крови. Поэтому длительное применение теофиллина требует мониторинга его концентрации в крови.
Принципиально новым шагом в современной фармакотерапии бронхиальной астмы является создание комбинированных препаратов, обладающих выраженным противовоспалительным и длительным бронхолитическим действием. Речь идет о комбинации ингаляционных кортикостероидов и длительно действующих β2-агонистов. Сегодня на фармакологическом рынке Европы, и России в том числе, существуют два таких препарата: серетид, содержащий флютиказон пропионат и сальметерол, и симбикорт, имеющий в своем составе будесонид и формотерол. Оказалось, что в подобных соединениях кортикостероид и пролонгированный β2-агонист обладают комплементарным действием и их клинический эффект существенно превышает таковой в случае монотерапии ИГКС или β2-агонистом длительного действия. Назначение такой комбинации может служить альтернативой повышению дозы ИГКС у пациентов со среднетяжелой и тяжелой астмой. Пролонгированные β2-агонисты и кортикостероиды взаимодействуют на молекулярном уровне. Кортикостероиды увеличивают синтез β2-адренорецепторов в слизистой бронхов, снижают их десенситизацию и, напротив, повышают чувствительность этих рецепторов к действию β2-агонистов. С другой стороны, пролонгированные β2-агонисты стимулируют неактивный глюкокортикоидный рецептор, который в результате становится более чувствительным к действию ингаляционных глюкокортикостероидов [6]. Одновременное применение ИГКС и пролонгированного β2-агониста не только облегчает течение астмы, но и существенно улучшает функциональные показатели, снижает потребность в короткодействующих β2-агонистах, значительно эффективнее предупреждает обострения астмы по сравнению с терапией только ИГКС.
Безусловным преимуществом этих препаратов, особенно привлекающим пациентов-астматиков, является сочетание двух активно действующих субстанций в одном устройстве для ингаляций: дозированном аэрозольном ингаляторе (серетид ДАИ) или порошковом ингаляторе (серетид мультидиск) и турбухалере, содержащем препараты в виде пудры (симбикорт-турбухалер). Препараты имеют удобный двукратный режим дозирования, для симбикорта возможен также однократный прием. Серетид выпускается в формах, содержащих различные дозы ИГКС: 100, 250 или 500 мкг флютиказона пропионата при неизменной дозе сальметерола — 50 мкг. Симбикорт выпускается в дозировке 160 мкг будесонида и 4,5 мкг формотерола. Симбикорт можно назначать от 1 до 4 раз в сутки, что позволяет контролировать вариабельное течение астмы с помощью одного и того же ингалятора, уменьшая дозу препарата при достижении адекватного контроля астмы и увеличивая при ухудшении симптомов. Это обстоятельство позволяет подобрать адекватную терапию с учетом тяжести астмы для каждого конкретного больного. Кроме того, симбикорт за счет быстродействующего формотерола быстро облегчает симптомы астмы. Из этого вытекает повышение приверженности к терапии: видя, что лечение помогает быстро и эффективно, больной более охотно соблюдает предписание врача. Следует помнить, что комбинированные препараты (ИГКС + длительно действующие β2-агонисты) не должны использоваться для купирования острого приступа астмы. Для этой цели пациентам рекомендуются β2-агонисты короткого действия.
Таким образом, применение комбинированных препаратов ИГКС и пролонгированных β2-агонистов целесообразно во всех случаях персистирующей астмы, когда не удается достичь хорошего контроля над заболеванием только назначением ИГКС. Критериями хорошо контролируемой астмы являются отсутствие ночных симптомов, хорошая переносимость физической нагрузки, отсутствие потребности в неотложной помощи, суточная потребность в бронхолитиках менее 2 доз, пиковая скорость выдоха больше 80% и ее суточные колебания менее 20%, отсутствие побочных эффектов от проводимой терапии [7].
Безусловно, целесообразно начинать лечение ИГКС с комбинации их с сальметеролом или формотеролом, что позволит достичь быстрого клинического эффекта и заставит пациентов поверить в успех лечения.
Бронхиальная астма представляет собой воспалительный процесс, протекающий в хронической форме и локализующийся в органах дыхания. Заболевание вызывает не полную и обратимую закупорку бронхов, приступы удушья и кашля, а также усиленную реактивность бронхов.
Бронхиальная астма – хроническое заболевание, основой которого является постоянный неинфекционный воспалительный процесс в дыхательных путях. В развитии болезни играют роль внешние и внутренние факторы. Внешние факторы – это аллергены, инфекция (вирусы, грибы, некоторые виды бактерий), химические и механические раздражители, метеорологические факторы, стрессовые и физические перегрузки. Аллергия на пыль – самая распространенная форма. К внутренним факторам относятся дефекты иммунной, эндокринной систем, нарушение чувствительности и реактивности бронхов, которые могут носить наследственный характер, и др.
Симптомы астмы
Характерными проявлениями бронхиальной астмы являются приступы удушья, одышка с затрудненным выдохом, кашель с трудно отделяемой мокротой. Иногда повышается температура тела, что свидетельствует об усилении активности бронхолегочной инфекции.
При осмотре кожи больного можно увидеть сопутствующие аллергические проявления: крапивницу, экзему, псориаз.
Для одышки при приступе бронхиальной астмы характерны короткий вдох и удлиненный выдох, сопровождаемый свистящими хрипами, которые слышны на расстоянии. В дыхании принимают участие мышцы плечевого пояса, спины, живота. Грудная клетка при этом находится в положении максимального вдоха. Приступ заканчивается отделением вязкой мокроты.
Факторами, предрасполагающими к развитию астматического статуса, чаще всего являются бесконтрольный прием кортикостероидных и симпатомиметических препаратов, резкое прерывание длительно проводимой гормональной терапии, острые или обострение хронических заболеваний системы органов дыхания, злоупотребление снотворными и успокаивающими препаратами и др.
Выделяют несколько стадий развития астматического статуса
В первой стадии появляются боли в мышцах плечевого пояса, грудной клетки, живота, одышка и кашель с трудно отделяемой мокротой.
Для второй стадии характерно тяжелое состояние больного. Кожа приобретает бледно-серый оттенок, дыхание становится поверхностным и учащенным, артериальное давление снижается, пульс прощупывается с трудом. Периоды возбуждения сменяются безразличием.
В третьей стадии развития астматического статуса сознание может отсутствовать, кожные покровы синюшно-бледные, артериальное давление настолько низкое, что определяется с трудом, могут быть судороги.
Народные средства лечения бронхиальной астмы
Листья алоэ срезают в возрасте 3-5 лет, выдерживают в темноте 2 недели при температуре 4-8 °С, промывают, измельчают, заливают кипяченой водой в соотношении 1:3, настаивают 1–1,5 часа и отжимают сок. 0,5 стакана этого сока смешивают с 500 г измельченных грецких орехов и 300 г меда. Принимают по 1 столовой ложке 3 раза вдень за 30 минут до еды.
Состав лекарства: подорожник (листья) – 1 часть, бузина травянистая (цветки) – 1 часть, росянка (трава) – 1 часть, фиалка трехцветная (трава) – 1 часть. Четыре чайные ложки измельченной смеси заливают стаканом кипятка, 5 минут держат на водяной бане, после чего остужают и процеживают. Отвар выпивают в течение дня в 3 приема.
Столовую ложку сухих или свежих листьев подорожника большого залить стаканом кипятка, настоять в течение 15 минут, процедить. Принимать по 1 столовой ложке 4 раза в день до еды. Применяется как противокашельное средство при заболеваниях дыхательных путей с обильной мокротой, в том числе при бронхиальной астме, коклюше и туберкулезе.
Вымыть и очистить от кожуры 400 г корня имбиря, натереть его на терке, насыпать в бутылку и залить спиртом. Настаивать в тепле или на солнце в течение 14 дней, периодически встряхивая бутылку. Настойка должна приобрести желтый цвет. Процедить, отжать и дать отстояться. Пить 2 раза в день по 1 чайной ложке, запивая 3 глотками воды, после приема пищи.
Тщательно разомните 1 столовую ложку ягод калины и залейте стаканом теплой кипяченой воды, добавьте 1 столовую ложку меда и все хорошо перемешайте. Доведите смесь до кипения и варите на слабом огне 20 минут. Еще раз перемешайте и процедите. Смесь нужно выпить в течение дня, принимая по 1 столовой ложке каждые 1,5– 2 часа. Астматикам, склонным к гипертонии, лучше принимать сок из свежих ягод калины по 1 столовой ложке 6–8 раз в день. Эффективным бактерицидным и смягчающим средством при лечении бронхиальной астмы служит чесночное масло. Для его приготовления натрите на терке чеснок, смешайте его с солью и сливочным маслом (на 100 г масла – 5 крупных долек чеснока, соль по вкусу). Чесночное масло можно есть, намазывая на черный и белый хлеб или добавляя в картофельное пюре.
250 г молотого кофе залейте 0,5 кг меда и тщательно перемешайте. Принимайте маленькими порциями перед едой. Приготовленная смесь рассчитана на 20 дней лечения. Если вы почувствуете, что вам стало лучше, то лечение можно повторить еще раз. Можно также смешать 0,5 кг меда, 100 г сливочного масла, по 70. г кашицы хрена и чеснока. Принимайте по 1 столовой ложке за час до еды в течение 2 месяцев.
При приступах астмы очень помогает массаж верхней части тела – от головы вниз до груди. Можно делать массаж с использованием талька или маслянистого крема. Для разжижения мокроты во время приступов выпить немного кислого вина или принять соды на кончике ножа. Помогает также и настойка валерианы (15–20 капель на рюмку воды).
Дурман обыкновенный используют для лечения больных астмой. Это растение обладает противоспазматическим действием. Внутрь принимают настойку, которая готовится из 1 части толченых семян и 5 частей спирта, настаивают 7 часов. При приеме строго соблюдают дозировку: 2 капли на 3 столовые ложки воды. Принимать 3–5 раз в день, можно вдыхать ее пары по 15 минут 3 раза в день.
40 головок семенного лука залить кипятком и подождать, пока они не станут мягкими. Затем воду слить и потушить лук в 0,5 л оливкового масла. Тушить до готовности, после чего размять до консистенции пюре. Принимать утром и вечером по 1 столовой ложке.
2 головки чеснока и 5 лимонов натереть на терке, залить кипяченой водой комнатной температуры (1 л). Настаивать 5 дней, затем процедить и отжать. Принимать по 1 столовой ложке 3 раза в день за 20 минут до еды.
При бронхиальной астме, коклюше и хронических бронхитах как отхаркивающее с противоаллергическим эффектом средство употребляют отвар багульника. Столовую ложку измельченной травы заливают стаканом кипятка, кипятят 10 минут, остужают и принимают по столовой ложке 5–6 раз в день.
Плоды аниса обыкновенного, траву тимьяна ползучего, плоды фенхеля обыкновенного и семена льна посевного смешать поровну. Четыре чайные ложки сбора залить стаканом воды комнатной температуры, настоять 2 часа, прокипятить 5 минут, процедить. Принимать по 1/3 стакана 3 раза в день.
Плоды фенхеля обыкновенного, плоды аниса обыкновенного, корни солодки голой, почки сосны обыкновенной и траву тимьяна ползучего соединить в равных долях. 10 г сбора залить 200 мл воды, нагреть на кипящей водяной бане 15 минут, охлаждать 45 минут, процедить и довести количество настоя до первоначального объема. Принимать по 1/4–1/3 стакана 3 раза вдень.
Взять 4 чайные ложки измельченных листьев мать-и-мачехи, заварить стаканом кипятка, настоять 30 минут и процедить. Пить по 1/4 стакана 4 раза в день.
Траву тимьяна обыкновенного, лист мать-и-мачехи, траву фиалки трехцветной, корень девясила высокого, плоды аниса обыкновенного смешать в равных пропорциях. Столовую ложку смеси залить стаканом кипятка, настоять 30 минут. Принимать по 1/3 стакана 3 раза в день после еды при бронхите, бронхиальной астме.
150 г свежего тертого хрена смешать с соком 2–3 лимонов и принимать после еды по 1/2 чайной ложки утром и после обеда, не запивая. Это средство предназначено только для взрослых.
Смешать поровну траву тимьяна ползучего, почки сосны обыкновенной, плоды аниса обыкновенного, плоды фенхеля обыкновенного. Столовую ложку смеси залить стаканом горячей воды, нагревать на кипящей водяной бане 15 минут, охлаждать 45 минут. Процедить. Принимать по 1/4–1/3 стакана 3 раза вдень.
Скорлупу 10 сырых яиц освободить от внутренней пленки, просушить и растереть в порошок, который нужно залить соком 10 лимонов и поставить на 10 дней в темное место. Полученную смесь процедить через марлю и смешать с другим составом следующего приготовления: 10 желтков взбить с 10 столовыми ложками сахара и в образовавшийся гоголь-моголь влить бутылку коньяка. Полученную смесь (порошок скорлупы, лимонный сок, желтки, коньяк) тщательно перемешать и принимать по 30 г 3 раза в день за 30 минут до еды. Вскоре после приема должно наступить облегчение. При необходимости курс лечения можно повторить.
Рекомендуется принимать мумие по 0,2-0,3 г в сочетании с молоком или с коровьим жиром и медом (в соотношении 1:20) утром натощак и вечером перед сном. Курс лечения 25–28 дней. Необходимо провести 2-3 курса с 10-дневными перерывами.
Корень алтея лекарственного и траву тимьяна ползучего смешать поровну. Две столовые ложки смеси залить стаканом кипятка, настаивать 30 минут. Принимать по 1/3 стакана 3 раза в день после еды при кашле, коклюше, бронхите, бронхиальной астме.
Листья мать-и-мачехи, листья подорожника и почки сосны соединить всего поровну. Четыре, чайные ложки смеси настаивать 2 часа в холодной воде. Затем кипятить в закрытой посуде 5 минут. Процедить. Принимать по 1 столовой ложке 3 раза в день.
Приготовить настой следующих трав: корень аира – 50 г, корень девясила – 50 г, мать-и-мачеха – 100 г, багульник – 100 г, фиалка трехцветная – 100 г, цитварное семя – 150 г. Все травы измельчить, смешать. Столовую ложку сбора заварить на ночь в термосе 200 мл кипятка. Утром процедить и принимать по 2 столовых ложки 3 раза в день до еды и 4-й раз на ночь.
Традиционные средства лечения бронхиальной астмы
Для лечения больных применяют бронхорасширяющие препараты (?-адреномиметики, М-холиноблокаторы, ксантины), противоастматические противовоспалительные препараты (ингибиторы лейкотриенов, стабилизаторы тучных клеток). Стабилизаторы мембран тучных клеток и ингибиторы лейкотриенов относятся к базисной терапии. Эти препараты предупреждают развитие приступа бронхиальной астмы, уменьшают реактивность бронхов, снижают частоту и длительность приступов.
При некоторых формах заболевания назначают глюкокортикоиды, которые также входят в базисную терапию бронхиальной астмы. Эти препараты уменьшают воспалительную реакцию, отек слизистой оболочки бронхов, подавляют активность бронхиальных желез, а также, что очень важно при этом заболевании, снижают реактивность бронхов. Различают следующие виды глюкокортикостероидов: ингаляционные (беклометазон, флутиказон и др.) и системные (преднизолон, дексаметазон и др.). Преимущество ингаляционных препаратов заключается в том, что они оказывают преимущественно местное противовоспалительное действие, практически не оказывая системных побочных эффектов. Системные глюкокортикостероиды назначаются при тяжелых формах заболевания. Вводят их внутривенно или, что предпочтительнее, внутрь. Их желательно использовать только в крайних случаях, когда любая другая терапия не дала положительного эффекта.
Применяется и симптоматическая терапия. Это бронхорасширяющие препараты. Их существует огромное множество, но они дают лишь кратковременный эффект в виде быстрого снятия спазма бронхов. Частота применения бронхорасширяющих препаратов служит индикатором эффективности базисной терапии, т. е. чем чаще больному приходится использовать эти препараты, тем менее эффективно применение базисной терапии, и ее в срочном порядке необходимо корректировать в условиях стационара. Бронхорасширяющие препараты представлены самыми разнообразными ингаляторами, преимущество которых в том, что ими очень просто пользоваться даже вне дома. Одного-двух вдохов достаточно, чтобы снять бронхоспазм и предотвратить развитие приступа бронхиальной астмы.
Международно-принятым считается ступенчатое лечение бронхиальной астмы. Этот подход очень удобен в плане контроля симптомов бронхиальной астмы при применении минимального количества лекарственных препаратов. При усугублении симптомов, появлении новых признаков частота приемов лекарств увеличивается. Это ступень вверх. При адекватно подобранной терапии частота и количество приемов препаратов снижаются. Это говорит об эффективности лечения (ступень вниз). Однако не всегда усугубление симптомов заболевания связано с неадекватностью проводимой терапии. Прежде чем подниматься на ступень вверх, необходимо убедиться в правильности приема лекарств больным.
Физиотерапевтическое лечение больных бронхиальной астмой может проводиться и в периоды обострения, и в период ремиссии. Показаны УВЧ-терапия, индуктометрия, микроволновая терапия, ультразвуковая терапия, электрофорез, эритемотерапия.
Лечебная физкультура является обязательной частью комплексного лечения бронхиальной астмы у больных любой возрастной категории. Она помогает восстановить функцию дыхания, способствует дренажу бронхиального дерева, улучшая отхождение мокроты, предупреждает развитие эмфиземы легких, а также повышает сопротивляемость организма и укрепляет нервную систему.
Занятия показаны в межприступном периоде заболевания. Используются лечебная гимнастика, ходьба, игры и имитационные упражнения, особое внимание уделяется дыхательной гимнастике. Полезны также массаж грудной клетки, занятия плаванием, пешие прогулки перед сном, закаливание.
Туберкулезом невозможно заразиться, если пользуешься книгами, предметами быта, другими вещами больного, потребляешь пищу, которую приготовил или продавал больной, либо через пользование общей посудой.
На самом деле туберкулез передается через воздух, когда человек долго находится в закрытом помещении вместе с больным туберкулезом легких, который кашляет и не получает лечение.

Чтобы не заразиться туберкулезом, нужно чаще мыть руки и убирать дезинфицирующими растворами в местах, где находится много людей.
Опровержение: мыть руки и убирать действительно необходимо, чтобы предотвратить многие болезни, но таким образом от туберкулеза себя не защитишь. Ведь туберкулез передается через воздух, и единственный способ снизить риск - регулярно проветривать помещение. В медучреждениях, где лечатся больные туберкулезом, также постоянно облучают воздух ультрафиолетом.
Если среди вашего окружения есть человек, который кашляет более 2 недель - деликатно порекомендуйте ему обратиться к семейному врачу. В любом случае общаться с таким человеком лучше на открытом воздухе - там туберкулез не передается.
Туберкулезом болеть стыдно, потому что это болезнь людей с неправильным образом жизни.
Опровержение: риск заболеть увеличивается при определенных условиях. Туберкулезом чаще болеют безработные, бездомные, люди, которые живут за чертой бедности, заключенные, а также мигранты, военнослужащие, медики, шахтеры и металлурги. Риск подцепить туберкулез повышают ВИЧ-инфекция, злокачественные новообразования, сахарный диабет, аутоиммунные заболевания. Велик риск и у людей, переживших пересадку органов или костного мозга. Опасным является и длительный близкий контакт с больным, который не получает лечения. От большинства этих обстоятельств никто не застрахован.
Человек, который лечится или лечился от туберкулеза, очень опасен для своего окружения.
Опровержение: опасность представляет только человек с туберкулезом легких, который кашляет и при этом не лечится. Через несколько недель после начала лечения такой человек не может никого заразить, даже если в ее анализах еще остается возбудитель недуга. Однако больной должен ежедневно принимать лекарства, назначенные с учетом чувствительности.
Туберкулезом можно заразиться в общественном транспорте, кафе, супермаркете.
Опровержение: туберкулез не так быстро передается, как другие инфекции. Обычно заражаются люди, которые проводят много времени с больным туберкулезом легких. Это около 8 часов ежедневно в течение 3 месяцев до начала лечения. Поэтому на самом деле рискуют люди, которые живут или работают с лицом, которое долго кашляет, но не обследуется и не лечится.
При этом многие взрослые уже инфицированы туберкулезом. Однако 90% из них никогда не заболеют из-за очень сильного природного противотуберкулезного иммунитет.
Туберкулез лучше лечить в стационаре: там есть условия для изоляции пациента. Кроме того, в уколах лекарства лучше усваиваются.
Опровержение: лучшее лечение туберкулеза - когда человек находится дома и ежедневно принимает лекарства под контролем медработника. В зависимости от состояния пациента и обстоятельств его жизни, он или сам может приходить в медучреждение, или ему приносят лекарства. Человек с туберкулезом, который правильно лечится, не нуждается в изоляции.
Почти все противотуберкулезные лекарства лучше принимать в таблетках. А инъекции при необходимости делают на пункте амбулаторного лечения.
Переполненые пациентами больницы создают условия для обмена возбудителями среди больных и грозят тем, что человек может обрести устойчивости к лечению.
Лечение туберкулеза длительное - от 6 до 20 месяцев. Пережить это сложное время помогают пребывания в привычном окружении, поддержка семьи и друзей, посильная работа и увлечение.
Однако есть случаи, когда больные туберкулезом нуждаются в стационарном лечении. В больницах, которые не перегружены, легче создать достойные и безопасные условия для пациентов.
Если человек заболел туберкулезом - это навсегда.
Опровержение: в основном даже тяжелые случаи туберкулеза хорошо лечатся. Сегодня в Украине являются бесплатными вся своевременная диагностика туберкулеза и медикаменты для лечения разных форм болезни. Но, если человек принимает лекарства с перерывами, или вообще отказывается от лечения, возбудитель становится тренированным к действию лекарств - приобретает устойчивость. Тогда лечение продлится дольше и менее эффективно.
Более того, такой человек распространяет на свое окружение устойчивые формы инфекции. Поэтому близкие люди подвергаются не просто риску болезни, а риску развития наиболее неблагоприятной ее формы.
Лечение туберкулеза имеет побочные эффекты. Лучше лечиться народными методами.
Опровержение: лечение действительно может приводить к побочным реакциям, но за тяжестью их невозможно сравнить с туберкулезом. Единственное, что сделало туберкулез излечимым - это специальные антибактериальные лекарства. Все народные методы борьбы с туберкулезом (собачий или барсучий жир, сушеные насекомые, травы и т. п) люди применяли во времена, когда не было сильных антибиотиков. Так пытались компенсировать дефицит необходимых для выздоровления белков, микро- и макроэлементов. Но в те времена туберкулез все равно был смертельным недугом. Поэтому выздороветь без специального лечения нельзя.
Вакцинация против туберкулеза плохо переносится - место инъекции часто долго не заживает. К тому же, зачем она, если вакцинированные люди все равно болеют?
Опровержение: осложнения от вакцинации против туберкулеза (БЦЖ) случаются менее чем в 1% случаев. И большинство из этих осложнений не требует лечения. Нагноение и образование корочки, что немного кровит - нормальная реакция, которая может длиться до 6 месяцев и обеспечивает образование крепкого иммунитета.
Однако вакцинация не может полностью защитить от заражения и заболевания, а лишь снижает риск туберкулеза. Но именно благодаря вакцине дети сейчас болеют туберкулезом очень редко. В них практически нет тяжелых случаев туберкулеза, от которых раньше умирали или получали непоправимые последствия для здоровья.
Для цитирования: Бердникова Н.Г. Использование фитопрепаратов в терапии бронхолегочных заболеваний. РМЖ. 2014;6:440.
Применение лекарственных растений в медицине имеет многовековую историю. И несмотря на огромный выбор синтетических лекарственных препаратов, идея терапии фитопрепаратами не теряет своей актуальности. Известно, что использование лекарственных растений, в т. ч. в составе комплексной терапии, значительно расширяет терапевтические возможности и позволяет добиться лучших клинических результатов. ВОЗ призвала правительства всех стран сделать традиционную медицину, использующую лекарственные травы, частью государственных систем здравоохранения. По мнению экспертов ВОЗ, в лечении почти 75% больных возможно использовать препараты растительного происхождения, к тому же имеются определенные группы пациентов (дети, пожилые, беременные, кормящие), в терапии которых использование фитопрепаратов является целесообразным.
Вирусная инфекция может способствовать развитию таких осложнений, как бронхит, ларингит, трахеит, отит, пневмонии, энцефалит, бронхиальная астма. Также следует учитывать, что чем младше ребенок, тем выше вероятность осложнений. Пик заболеваемости острыми респираторными заболеваниями (ОРЗ) среди детей отмечается в возрасте от 6 мес. до 6 лет и составляет от 4 до 10 заболеваний в год. Этому способствуют незрелость анатомических структур, физиологические характеристики бронхолегочного дерева и особенности иммунной системы в детском возрасте. Так, бронхолегочная система у детей имеет свои возрастные характеристики: короткие носовые пути, незрелость сурфактанта, несостоятельность альвеол (окончательное формирование ацинусов происходит только к 5–9 годам). Все эти факторы вместе с транзиторными особенностями иммунной системы в детском возрасте (сниженное образование эндогенного интерферона, секреторного иммуноглобулина А, лизоцима носового секрета) могут приводить к образованию очагов хронической инфекции. Отмечено, что среди группы часто болеющих детей значительно чаще выявляются хронические заболевания носоглотки и легких, чаще встречается и тяжелее протекает бронхиальная астма (БА), аллергический ринит, выше частота гломерулонефрита и ряда других заболеваний [2].
Независимо от того, на какой уровень дыхательных путей (носоглотка, гортань, трахея, бронхи) вирусы оказывают воздействие, патофизиологический сценарий будет практически одинаковым. Воспалительный процесс слизистых различных отделов дыхательного тракта, индуцируемый вирусами, приводит к возникновению локальных (кашель, гиперсекреция слизи, образование мокроты) и общих симптомов интоксикации различной степени, которые зависят от вида вирусов [2, 3]. Кашель, различный по своему характеру, суточной вариабельности, длительности, сопровождает такие заболевания, как ларингит, трахеит, бронхит, пневмония, патология ЛОР-органов. Таким образом, кашель является самым распространенным симптомом и неизбежным спутником заболеваний дыхательных путей.
Как известно, кашель является сложной рефлекторной реакцией, направленной на защиту бронхолегочной системы. С одной стороны, кашель препятствует попаданию нежелательных частиц и веществ в бронхи, с другой, способствует эвакуации трахеобронхиального секрета. Обычно кашель расценивается как проявление бронхолегочных заболеваний, однако не следует забывать, что причина может быть связана и с внелегочной патологией: болезни придаточных пазух носа, сердца, желудочно-кишечного тракта, прием некоторых лекарственных препаратов также могут вызывать кашель (рис. 1).
- по характеру: непродуктивный (сухой) и продуктивный (влажный);
- по продолжительности: эпизодический, кратковременный, приступообразный и постоянный;
- по течению: острый (длящийся до 3-х нед.), подострый (от 3-х до 8 нед.), хронический (более 8 нед.).
При диагностике продуктивность, т. е. наличие мокроты, является важным показателем. Неэффективность кашля может быть обусловлена недостаточно выраженным кашлевым рефлексом, вязкостью мокроты, недостаточно глубоким дыханием, нарушением бронхиальной проходимости и другими причинами. При продуктивном кашле нужно обращать внимание на цвет, характер, количество мокроты, а также наличие крови, которые являются патогомоничными для того или иного заболевания.
При лечении инфекций вирусной природы, сопровождающихся продуктивным кашлем, обоснованным считается использование симптоматической терапии. Терапия должна быть направлена на устранение и/или уменьшение приступов кашля и облегчение отхождения мокроты, что влечет за собой укорочение сроков заболевания. У пациентов с бронхообструктивными заболеваниями (хроническая обструктивная болезнь легких (ХОБЛ), БА) или бронхоэктатической болезнью вирусная инфекция достаточно часто является инициатором обострения их основного заболевания. Структурная перестройка дыхательных путей и легочной ткани, изменение реологии мокроты и местной защиты бронхов – все эти патофизиологические особенности являются хорошим субстратом для возникновения обострения после дебюта вирусной инфекции.
Современная медицина имеет в своем арсенале большое количество химически синтезированных средств, однако препараты на основе растительных веществ остаются популярными. Фитотерапевтические препараты широко используются в отоларингологической и пульмонологической практике, особенно при острых и хронических заболеваниях дыхательных путей. Использование фитотерапевтических препаратов может приносить пользу пациенту, особенно в тех случаях, когда имеются противопоказания для назначения каких-либо синтезированных препаратов, фитопрепараты способны профилактировать обострения, дают возможность сократить использование других лекарств и/или длительность их приема, имеется возможность длительного и повторного использования. Фитотерапевтические препараты не используются как препараты неотложной терапии, при тяжелых состояниях пациентов, но рекомендованы при легкой и средней степени тяжести, а также в случаях хронических заболеваний. Использование фитопрепаратов также оправданно для профилактики рецидивов, в периоды реконвалесценции, совместно с другими химиотерапевтическими препаратами, что, несомненно, расширяет терапевтические возможности.
Фитопрепараты должны отвечать тем же критериям качества, эффективности и безопасности, что и химические лекарственные средства. В отличие от синтетических лекарственных средств они обладают более широким диапазоном, меньшим количеством побочных эффектов и меньшими рисками взаимодействия с другими препаратами.
Как было сказано выше, в терапии продуктивного кашля нетяжелой степени, который возникает при остром ларингите, трахеите и/или бронхите, как вариант терапии должны быть рассмотрены препараты растительного происхождения. Основные свойства, которыми они должны обладать, следующие: отхаркивающие, противовоспалительные, мукорегуляторные. Многие растительные препараты отвечают этим требованиям: эвкалипт, корень солодки, подорожник, мать-и-мачеха, тимьян, первоцвет, листья плюща, корень алтея, багульник, ромашка аптечная и др. Помимо использования при острых заболеваниях дыхательных путей растительные препараты находят место и в терапии хронических инфекций, позиционируются для профилактики обострений и в качестве комплексной терапии [4–6].
Анализируя медицинскую литературу, можно обнаружить достаточно данных об эффективности экстракта тимьяна в терапии продуктивного кашля. Эти данные подкреплены результатами зарубежных и отечественных исследований, а также широким использованием на фармацевтическом рынке экстракта тимьяна в составе фитокомпозиций. Это обусловлено тем, что в состав данного растения входят: эфирные масла (карвакрол и тимол), способствующие эвакуации мокроты, удалению слизи из легких, флавоноиды, обладающие бронхолитическим эффектом, и тимол, который помимо муколитического эффекта обладает и антисептическими свойствами. Удачными являются комбинации 2-х и более растительных препаратов, которые имеют однонаправленное действие. Так, биоактивными соединениями корня первоцвета являются сапонины и фенольные гликозиды (примеверин). Сапонины оказывают отхаркивающее действие путем стимуляции верхней части пищеварительного тракта, что рефлекторно индуцирует бронхиальную секрецию. Экстракт тимьяна и корень первоцвета имеют разные фармакологические свойства, которые в комбинации работают синергично, обеспечивая отхаркивающий, бронхоспазмолитический, секретолитический и противовоспалительный эффекты.
Заявленные эффекты были подкреплены серией достаточно популярных исследований. Это известное исследование B Kemmerich. (2007), переведенное на русский язык. Клиническое исследование было проспективным рандомизированным двойным слепым 11-дневным в параллельных группах для оценки эффективности и безопасности комбинации сухого экстракта травы тимьяна и корня первоцвета и плацебо при лечении пациентов, страдающих острым бронхитом с продуктивным кашлем. В исследование был включен 361 пациент. Результаты этого исследования показали, что среднее снижение приступов кашля на 7–9-й дни отмечалось в 67,1% случаев при использовании фитокомпозиции тимьян + первоцвет по сравнению с 51,3% в группе плацебо (р<0,0001). Симптомы острого бронхита быстро уменьшились в обеих группах (улучшение по шкале BSS), но регресс был быстрее и ответ лучше в группе комбинации тимьян + первоцвет по сравнению с плацебо к 4-му дню наблюдения (77,5% против 60,1%, р=0,0006) и на 10-й день (92,9% против 75,8%, р<0,0001). В целом нежелательные явления для комбинации тимьяна и первоцвета были редкими (1,6% пациентов), нетяжелыми и преходящими. Нарушения со стороны ЖКТ (тошнота, рвота) или аллергические реакции, которые отмечались при монотерапии корнем первоцвета и травой тимьяна, в данном исследовании не наблюдались [7].
Этим же автором также представлены результаты другой фитокомбинации – экстракт тимьяна и листьев плюща (сироп). В листьях плюща содержатся витамин Е, каротин, таниновая и олеиновая кислоты, хедерин. Препараты из листьев растения обладают вяжущим и антисептическим свойствами. В этом двойном слепом плацебо-контролируемом многоцентровом исследовании участвовали 363 пациента с острым бронхитом. Больные принимали комбинированный сироп тимьяна с листьями плюща (Бронхипрет, n=182) или плацебо-сироп (n=179). В результате было показано, что уменьшение приступов кашля с 7 по 9-й дни отмечено у 68,7% пациентов на фоне терапии тимьян + листья плюща по сравнению с 47,6% в группе плацебо (р<0,0001). Симптомы острого бронхита быстро уменьшились в обеих группах (улучшение по шкале BSS), но регресс симптомов был достоверно быстрее в группе пациентов, получающих сироп тимьяна + листья плюща (р <0,0001) по сравнению с плацебо [8]. Оба исследования демонстрируют эффективность сиропа и таблеток Бронхипрет в отношении более раннего снижения частоты приступов кашля, улучшения отхождения мокроты в дневное время, нормализации ночного сна (нарушения которого были связаны с ночным кашлем), динамики тяжести бронхита, доли лиц с положительным ответом на терапию.
При проведении систематического обзора с целью оценки эффективности и переносимости плюща при острых инфекциях верхних дыхательных путей было обнаружено 10 различных клинических исследований: рандомизированные, нерандомизированные, контролируемые и наблюдательные. Три исследования оценивали комбинацию плюща и тимьяна, 7 исследований посвящены использованию только плюща. Только одно плацебо-контролируемое исследование комбинации плюща и тимьяна показало статистически значимое превосходство в снижении частоты и продолжительности кашля.
В любом травнике всегда можно найти средства для лечения бронхиальной астмы (БА). Однако у некоторых врачей вызывает настороженность использование препаратов растительного происхождения у пациентов с БА и поллинозом, в связи с чем заслуживают внимания исследования и результаты наблюдения при использовании фитопрепаратов у пациентов с атопическими заболеваниями. Так, исследование эффективности и безопасности Бронхипрета у 50 детей (от 1 года до 3-х лет) с бронхитом или трахеитом на фоне ОРВИ продемонстрировало, что к 3-му дню отмечалась четкая положительная динамика в виде улучшения симптомов кашля. Препарат характеризовался хорошей переносимостью, даже у детей с атопическими дерматитами и аллергическими реакциями [9]. На основании 3-х исследований сделан вывод, что препараты экстракта листьев плюща улучшают дыхательные функции у детей с БА, при этом о развитии нежелательных побочных реакций или ухудшении течения астмы не сообщалось [10].
Также об эффективности и хорошей переносимости Бронхипрета свидетельствует исследование у детей (84 ребенка, возраст 7,25±3,8 года), находящихся на госпитализации с инфекциями верхних и нижних дыхательных путей. 42 ребенка в составе комплексной терапии получали Бронхипрет и 42 ребенка – стандартную терапию в соответствии со своим заболеванием. На фоне приема Бронхипрета кашель становился продуктивным уже к 3–му дню и полностью разрешался к 14-му дню лечения у 69% пациентов, в отличие от детей, которые Бронхипрет не принимали и у них кашель сохранялся до 14 дней (73,8%). Авторы приходят к выводу, что Бронхипрет оказывает положительное влияние на заболевания, сопровождающиеся кашлем: пневмонию, острый обструктивный бронхит, обострение хронического бронхита, бронхиальной астмы. У детей с БА аллергических реакций или ухудшения течения астмы не наблюдалось [11].
Несомненно, заслуживает внимания фундаментальное многоцентровое когортное исследование по изучению сравнительной эффективности и безопасности Бронхипрета (в форме таблеток, капель и сиропа) в сравнении с эталонными синтетическими отхаркивающими средствами (амброксол и ацетилцистеин). Число участников этого исследования составило более 7 тыс. человек с продуктивным кашлем, требующим лечения, в т. ч. 1490 детей. В соответствии с полученными данными, Бронхипрет продемонстрировал более высокую эффективность при лечении взрослых с острым неосложненным либо обострением хронического бронхита (по таким критериям, как аускультативная картина, частота кашля ночью и днем, болезненность и качество кашля, количество и вязкость мокроты). Заслуживает внимания и тот факт, что побочные эффекты (преимущественно со стороны пищеварительного тракта) при применении Бронхипрета отмечали существенно реже по сравнению с синтетическими муколитиками [12].
Как было отмечено выше, считается, что растительные препараты менее аллергенны, чем синтетические. При этом группу повышенного риска составляют люди с отягощенным аллергологическим анамнезом (БА, отек Квинке).
Подводя итоги, можно прийти к заключению, что комбинированный препарат Бронхипрет демонстрирует высокую эффективность как у взрослых, так и у детей, что подтверждено результатами крупных клинических отечественных и зарубежных исследований. Хорошая переносимость, отсутствие фармакокинетических взаимодействий, разнообразные формы выпуска (сироп, таблетки) позволяют выстраивать тактику лечения в соответствии с потребностями каждого больного, что обусловливает высокую приверженность пациентов лечению.
Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ? С чем связаны возможны
 |
| Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания |
Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ?
С чем связаны возможные ошибки в диагностике?
Какова основная роль b-агонистов в терапии бронхиальной астмы?
Как назначаются кортикостероиды?
Несмотря на возросшую компетентность врачей и доступность эффективных методов лечения, смертность от бронхиальной астмы остается высокой. Предотвратить многие смертельные исходы и даже избежать большинства случаев госпитализации можно было бы при проведении правильного лечения.
Необходимо помнить, что ведение больных астмой — процесс сложный и длительный.
Недооценка степени несостоятельности дыхания. Тяжесть состояния пациента и степень несостоятельности его дыхательной системы можно не распознать, если пренебречь тщательным выяснением всех проявлений болезни и построением диаграммы измерений максимальной скорости потока (МСП) выдыхаемого воздуха.
Зачастую у больных астмой снижены виды на будущее, хотя некоторые и склонны недооценивать серьезность симптомов своего заболевания. Чтобы выявить такую недооценку, нужно подробно расспросить пациента, бывает ли у него кашель или хриплое дыхание ночью или при физической нагрузке.
Если пациентам не удается достичь наилучшей возможной функции легких, то для коррекции этого состояния необходимо для начала вычислить нормальную МСП выдыхаемого воздуха для данного пациента, пользуясь диаграммой, прилагаемой к пикфлуометру.
Если измеренная МСП более чем на 20% меньше вычисленной, стоит провести исследование обратимости этого состояния, что делается путем сопоставления МСП или жизненной емкости легких (ЖЕЛ) до и после лечения.
Необходимая терапия может состоять всего лишь в однократном приеме бронходилятатора, но если это не увеличивает МСП на 20%, то есть до вычисленного уровня, могут понадобиться более серьезные меры, например трехнедельный курс системных кортикостероидов (30 мг преднизолона в день для взрослых). Таким образом выясняется наилучший достижимый уровень МСП, на который ориентируются в последующем лечении.
Иногда пациенты сообщают об уменьшении одышки, но при этом значения МСП не изменяются. В таких случаях необходимо провести измерение ЖЕЛ с помощью спирометра, которое может подтвердить улучшение, не определяемое по МСП (рис. 2). Спирометрами в настоящее время укомплектованы все врачебные приемные.
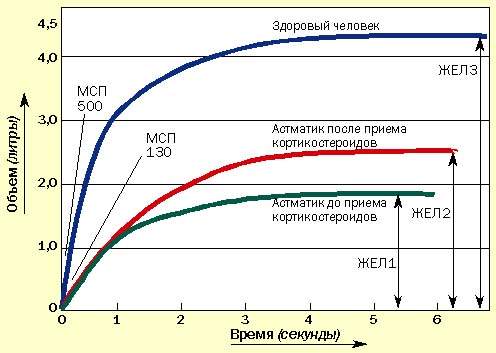 |
| Рисунок 2. Изменение ЖЕЛ под влиянием курса кортикостероидов. МСП может не измениться, но увеличение ЖЕЛ свидетельствует об улучшении состояния |
Бронхиальная астма, замаскированная под хроническое обструктивное заболевание легких (ХОЗЛ). Страдающие одышкой пациенты, которым поставлен диагноз ХОЗЛ или эмфизема, могут иметь скрытый бронхоспастический элемент, обусловленный бронхиальной астмой.
Таким пациентам необходимо провести исследование обратимости процесса, как описано выше. Любое улучшение функции легких можно поддержать, проводя адекватное лечение бронхиальной астмы. При отсутствии улучшения легочной функции назначение кортикостероидов ничем не оправдано, а только приводит к нежелательным побочным эффектам, таким как остеопороз.
Что должен помнить врач, наблюдающий больных с бронхиальной астмой
- Сказал ли я, что нужно применять спейсер при ингалировании кортикостероидов?
- Проверил ли я навыки ингаляции?
- Осмотрел ли я всех пациентов, недавно перенесших тяжелые приступы или госпитализацию?
- Все ли пациенты с повторными назначениями регулярно приходят на прием?
- Все ли я сделал, чтобы исключить астму у пациентов с ХОЗЛ?
- Проводятся ли регулярные проверки для достижения единообразного подхода к ведению астматиков?
Постоянный прием b-агонистов короткого действия. Показано, что лечение астмы постоянным приемом b-агонистов увеличивает гиперреактивность легких и утяжеляет бронхиальную астму [1]. Если пациент использует b-агонисты скорее регулярно, чем случайно, их применение должно сопровождаться назначением ингаляционных кортикостероидов или, если кортикостероиды уже применяются, увеличением их дозы до достаточной, чтобы контролировать астму. Таким образом, b-агонисты оставляют на случаи одышки и хрипов.
Последние методические указания по лечению бронхиальной астмы в Британии рекомендуют начинать с высокой дозы ингаляционных или системных кортикостероидов для достижения быстрого контроля, затем постепенно снижать дозу до минимальной, обеспечивающей нормальное самочувствие пациента и оптимальные значения МСП или ЖЕЛ на фоне минимального применения бронходилятатора (рис. 3). Быстрое облегчение состояния, достигаемое при применении кортикостероидов, улучшает настроение пациента и увеличивает его доверие к лечению.
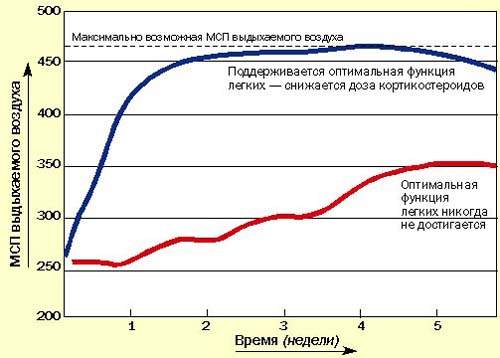 |
| Рисунок 3. Рекомендуется начинать с высоких доз кортикостероидов, а затем постепенно снижать дозу до минимальной (оптимальные значения МСП или ЖЕЛ) |
Последние данные свидетельствуют о том, что назначать кортикостероиды нужно как можно раньше всем астматикам, и не только для контролирования симптомов, но и для предотвращения прогрессирующих структурных повреждений легких, обусловленных хроническим воспалением [2,3]. Это означает, что кортикостероиды следует предпочесть b-агонистам, как только диагноз подтверждается МСП-диаграммой. b-агонисты остаются препаратами резерва на крайний случай.
Возможность альтернативного лечения. Хотя ингалируемые кортикостероиды должны быть краеугольным камнем в лечении астмы, в случаях, трудно поддающихся лечению, можно использовать и некоторые другие препараты. Доказано, что противовоспалительным эффектом обладают теофиллины в достаточно небольших дозах, но надо учитывать в каждом индивидуальном случае их возможное взаимодействие с другими препаратами.
Пожилым пациентам целесообразно назначать ипратропиум. Иногда оказываются эффективными недокромил и кромогликат.
Бронходилятаторы длительного действия, такие как сальметерол, могут облегчать состояние, особенно ночью, блокируя бронхоконстрикторные механизмы. Однако необходимо, чтобы все вышеперечисленные препараты сопровождались применением адекватных доз кортикостероидов.
Техника ингаляции. Нужно добиться, чтобы у пациентов выработались правильные навыки обращения с ингалятором. Врач должен помочь подобрать тот тип ингалятора, который наиболее удобен пациенту, и проверить его работоспособность. Для этого в кабинете врача должен быть полный набор ингаляторов.
Спейсеры. Применяемые вместе с аэрозольными ингаляторами, спейсеры облегчают проникновение препарата в легкие и снижают как накопление его в глотке, так и системное всасывание за счет проглатывания.
Спейсеры помогают координировать выброс препарата со вдохом. Это особенно важно при ингалировании кортикостероидов. Так как кортикостероиды применяются только дважды в день, громоздкий спейсер можно хранить дома.
Спейсеры обеспечивают лучшее накопление препарата в легких, чем распылители. Необходимо правильно их применять: встряхнуть ингалятор, чтобы лекарство смешалось с носителем, и однократно впрыснуть смесь с последующим скорейшим вдохом [4].
Триггерные факторы. Нераспознанные триггерные факторы могут быть и дома, и на работе, и на отдыхе, то есть практически в любом месте. Выявить источник поможет анамнез. Например, при профессиональной бронхиальной астме состояние улучшается во время отпуска и в выходные дни. Отсутствие раздражителя уменьшает или устраняет проявления болезни и снижает необходимость в лекарствах.
Проблемой, которую часто не принимают во внимание, может быть пассивное курение. Такие препараты, как b-блокаторы и нестероидные противовоспалительные средства (НПВС), также могут вызывать астму.
Использование распылителей (небулайзеров) без фоновой кортикостероидной терапии. При лечении острого астматического приступа без назначения пероральных кортикостероидов все еще используют распылители, которые обеспечивают проникновение более высокой дозы b-агонистов. Это действительно снимает бронхоспазм, но поскольку высокая доза b-агонистов не воздействует на сопутствующий воспалительный процесс, необходимо сразу же дать больному кортикостероиды внутрь, чтобы предотвратить нарастание приступа; эффект бронходилятаторов снижается по мере увеличения отека слизистой.
Если тяжесть приступа такова, что требуется небулайзер, необходимо назначить системные кортикостероиды. Даже при умеренном приступе бронходилятаторы сами по себе приносят лишь временное облегчение и есть опасность повторения приступа — возможно, глубокой ночью!
Несвоевременное назначение оральных кортикостероидов. Если не проводить противовоспалительной терапии, у больных нарастает отек слизистой, что приводит к повторению приступов. Такие пациенты часто нуждаются в госпитализации и назначении высоких доз кортикостероидов в течение нескольких дней, прежде чем у них наступит стабилизация состояния.
Пациенты, подверженные быстроразвивающимся приступам, нуждаются в как можно более раннем назначении кортикостероидов и бронходилятаторов. Они должны уметь распознавать ухудшение состояния, всегда иметь под рукой кортикостероиды и знать, как их использовать. Не следует заставлять этих пациентов дожидаться прихода к ним врача (рис. 4).
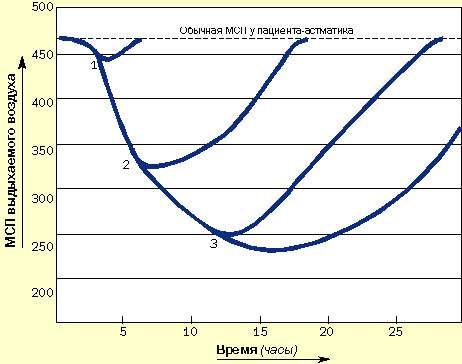 |
| Рисунок 4. Зависимость развития острых приступов от времени назначения кортикостероидов и как результат применения длительных курсов системной кортикостероидной терапии. (1) Кортикостероиды назначены сразу после возникновения приступа: выздоровление наступает быстро. (2) Кортикостероиды назначены через 6 часов: выздоровление замедлено. (3) Кортикостероиды назначены позже чем через 12 часов: приступ тяжелый и длительный, выздоровление наступает медленно |
Пациенты с постепенным развитием приступов могут подождать и посмотреть, помогает ли увеличенная доза ингаляционных кортикостероидов в сочетании с бронходилятаторами.
Неадекватный курс системных кортикостероидов. Иногда назначенные кортикостероиды отменяют до полного купирования приступа, что ведет к сохранению гиперреактивности бронхов и очередному приступу.
Подобная цепь событий может привести пациента к ложному заключению, что у него бронхиальная астма, трудно поддающаяся лечению.
Прекращение наблюдения за пациентом после острого приступа или госпитализации. Трудности возникают при отмене системного кортикостероида и назначении ингаляционного. В этот переходный период необходимо тщательное наблюдение; по достижении стабилизации состояния дозу ингалируемого кортикостероида постепенно снижают до минимально необходимой, чтобы заболевание никак себя не проявляло и функция легких была оптимальной.
Целью последующего лечения становится поддержание наивысшей МСП, достигнутой в больнице после курса системных кортикостероидов.
Консультация, проведенная через некоторое время после выписки, дает хорошую возможность проверить план ведения пациента, выяснить, что не так, и внести соответствующие поправки.
Кашель и хрипы с гнойной мокротой иногда принимают за легочную инфекцию. Однако мокрота больных астмой содержит гораздо больше эозинофилов, чем полиморфных клеток и бактерий. В пожилом возрасте левожелудочковая недостаточность и сердечная астма должны наводить на мысль о предшествующей бронхиальной астме. Будьте осторожны с b-блокаторами!
Внезапная одышка может быть обусловлена пневмотораксом или легочной эмболией. Хрипы встречаются при туберкулезе легких, бронхиальной карциноме или инородном теле и могут быть четко локализованы. Следовательно, у любого пациента с астмой, развившейся во взрослом возрасте, необходимо провести рентгенологическое исследование органов грудной клетки.
После установления диагноза основная цель врача — освободить пациента от проявлений болезни и оптимизировать функцию легких, а также установить контроль за болезнью. Для этого специально обученный медперсонал должен обучать больных и проверять правильность выполнения ими всех назначений.
Конечно, в некоторых случаях это может оказаться затруднительным, однако план предписанных действий способно усвоить абсолютное большинство больных.
Все пациенты должны:
- уметь распознать начало приступа
- знать, как применять высокие дозы b-агонистов;
- самостоятельно начать прием преднизолона внутрь;
- знать, когда звонить врачу или отправляться в больницу;
- все страдающие от приступов, должны быть обеспечены кортикостероидами.
Литература
1. Sears M. R., Taylor D. R. et al. Regular inhaled b-agonist treatment in bronchial asthma. Lancet 1990;336:1491–1396.
2. Tari Haahtela et al. Comparinson of terbutaline with budesonide in newly detected asthma. N Engl J Med 1991;325:388–392.
3. Redingon A. K., Howarth P. H. Airway remodelling in asthma. Thorax 1997;52:310–312.
4. O'Callaghan C., Barry P. Spacer devices in the treatment of asthma. BMJ 1997;314:1061–1062.
Спирометрия при хронической бронхиальной астме
Бочкообразная грудная клетка при хронической бронхиальной астме возникает из-за задержки воздуха в периферических отделах легких, что приводит к постоянному поддержанию грудной клетки в состоянии вдоха. Задержанный воздух не выдыхается и бесполезно занимает большую часть легких (остаточный объем). Это снижает объем воздуха (жизненную емкость легких), входящего в легкое.
Воздух задерживается из-за хронического воспаления, вызывающего отек слизистой периферических бронхиол. При лечении кортикостероидами отек спадает и воздух высвобождается. Это доказывается увеличением ЖЕЛ, определенной спирометрически. МСП может не изменяться (см. рис. 2.)
Читайте также:

