Туберкулез и заболевания желудочно-кишечного тракта
Обновлено: 18.04.2024
Туберкулез пищеварительной системы — Туберкулез пищевода представляет одну из редких локализаций этого заболевания и в большинстве случаев наблюдается у лиц с далеко зашедшими его легочными формами незадолго до смерти.
Этиология, патогенез
Туберкулезные микобактерии попадают в пищевод при заглатывании инфицированной мокроты, при активном туберкулезе гортани, надгортанника и глотки, реже лимфогенным или гематогенным путем, а также в результате непосредственного перехода туберкулезного процесса с окружающих органов: бифуркационных лимфатичес-ких узлов, позвоночника, щитовидной железы, гортани, глотки. Туберкулезные язвы возникают в результате казеозного распада туберкулезных бугорков. Встречаются также милиарная и стенозирующая формы туберкулезного поражения пищевода.
Симптомы, течение
Заболевание может протекать бессимптомно, однако чаще его симптомы затушевываются более выраженными проявлениями туберкулезного поражения других органов (прежде всего легких и гортани) и тяжелым общим состоянием больного.
Наиболее ярким симптомом является дисфагия, которая при наличии изъязвлений слизистой может сопровождаться резкой болью.
Рентгенологическое исследование выявляет крупные туберкулезные язвы и рубцовое сужение просвета пищевода.
Диагноз
Облегчает эзофагоскопия, биопсия, бактериологическое исследование материала, полученного из язвы.
Прогноз

Симптомы, течение. Заболевание может протекать бессимптомно или же сопровождаться болью в эпигастральной области, отрыжкой, рвотой, резким снижением аппетита; как правило, наблюдаются общее истощение, лихорадка, повышенная потливость.
Диагноз туберкулеза желудка подтверждается рентгенологическим исследованием и гастрофиброскопией. Поэтому особую ценность имеет прицельная биопсия. При исследовании желудочного сока часто выявляется ахилия, в желудочном содержимом (чаще в промывных водах) обнаруживают микобактерии туберкулеза.
Течение и прогноз в большинстве случаев определяются тяжестью легочной и других локализаций туберкулеза. Редкими осложнениями являются перфорация туберкулезной язвы желудка, желудочное кровотечение, рубцовый стеноз привратника.
![]()
Туберкулез поджелудочной железы встречается очень редко. Даже у больных активным туберкулезом легких он выявляется лишь в 0,5–2% случаев.
Симптомы, течение. Больные предъявляют жалобы на отрыжку, понижение аппетита, тошноту, боль в верхнем левом квадранте живота, нередко опоясывающего характера, поносы, усиленную жажду (при нарушении инкреторной функции поджелудочной железы), прогрессирующее истощение, повышенную потливость, недомогание, лихорадку. Кожа иногда приобретает темноватую окраску, как при аддисоновой болезни. При пальпации поджелудочной железы отмечается болезненность в месте ее расположения.
Диагноз. Для подтверждения диагноза проводят эхографию, ретроградную панкреатохолангиографию, вирсунгографию, сканирование поджелудочной железы, исследование ее внешней и внутренней секреции (характерна недостаточность функции). Дифференциальный диагноз проводят с неспецифическими панкреатитами, злокачественными и доброкачественными опухолями поджелудочной железы.
Туберкулез печени сопровождает туберкулез кишечника в 79–99% случаев. Туберкулезные микобактерии проникают в печень гематогенным или лимфогеннным путем, возможно также распространение процесса по желчным ходам. Чаще всего наблюдаются милиарная форма или множественные туберкуломы печени с казеозным распадом в центре. Встречаются также неспецифические изменения в печени при туберкулезе легких в виде реактивного гепатита, жировой дистрофии, амилоидоза или лекарственного гепатита (при длительном применении туберкулостатических средств).
Симптомы, течение. Анорексия, общее недомогание, слабость, повышенная потливость, субфебрилитет, боль в правом подреберье. Печень увеличена, край ее плотный, в ряде случаев поверхность неровная (при гранулематозной форме) или удается прощупать узел на ее поверхности (ту-беркулому). Нередко увеличена селезенка. Заподозрить туберкулезное поражение печени можно в том случае, если у больного легочным туберкулезом обнаруживается увеличение печени, отмечается боль в правом подреберье.
Диагноз подтверждается лапароскопией, пункционной биопсией печени, эхографией и сканированием.
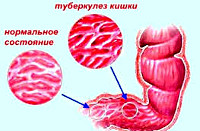
Туберкулез кишечника обнаруживают у 60–90% лиц, умерших от туберкулеза. Туберкулезные микобактерии попадают в кишечник чаще всего гематогенным или лимфоген-ным путем либо при заглатывании инфицированной мокроты, слюны и слизи, особенно при туберкулезном поражении гортани и глотки. Чаще всего поражаются дистальные отделы подвздошной и слепой кишки, аппендикс, реже- восходящая, поперечная, ободочная кишка.
Симптомы, течение. Вначале туберкулезное поражение кишечника может протекать бессимптомно или с общими симптомами — нарушением аппетита, тошнотой и тяжестью в животе после еды, слабостью, недомоганием, субфебрильной лихорадкой, повышенной потливостью, вздутием кишечника. Неустойчивым стулом, малохарактерными болями в животе. В дальнейшем боль становится более постоянной, локализуется чаще в правой подвздошной области и около пупка, при пальпации определяются плотные болезненные утолщения стенок слепой кишки и конечной части подвздошной кишки. При поражении прямой кишки наблюдаются тенезмы и ложные позывы. При туберкулезном мезадените боль локализуется в глубине живота несколько влево и книзу от пупка или по ходу брыжейки тонкой кишки. Во время рентгенологического исследования кишечника обнаруживают изъязвления слизистой оболочки, дискинетические явления, рубцовые стенозы, иногда дефекты наполнения слепой кишки. Поражение толстой кишки может быть уточнено при колоноскопии. При исследовании кала отмечают положительные реакции на скрытую кровь и пробу ребунале на растворимый белок. В крови — гипохромная анемия, лейкопения с относительным лимфоцитозом, при обострении — нейтрофильный лейкоцитоз, увеличение СОЭ.

Течение туберкулеза кишечника при отсутствии соответствующего лечения обычно прогрессирующее. Прогноз в значительной степени определяется тяжестью туберкулезного поражения легких и других органов. Осложнения: сужение просвета кишки, перфорация туберкулезных язв, перитонит и кишечное кровотечение.
Диференциальный диагноз проводят с неспецифическим энтероколитом, болезнью Крона, неспецифическим язвенным колитом, раком слепой кишки.
Лечение проводят в специализированных противотуберкулезных больницах. При туберкулезных язвах пищевода внутрь, дополнительно назначают медицинские препараты. Назначают щадящую диету с ограниченным содержанием жиров, исключением острых продуктов и повышенным содержанием белка. При признаках внешнесекреторной недостаточности поджелудочной железы назначают ферментные препараты.
Туберкулез кишечника – хроническое инфекционное заболевание, вызванное микобактериями; характеризующееся формированием в кишечной стенке специфических гранулем с дальнейшим расплавлением очага, образованием полости и фиброзированием при санации. Клиническая картина характеризуется отсутствием специфических симптомов; типичен болевой синдром, диспепсические явления, интоксикация. Для диагностики проводится рентгенологическое исследование кишечника, эндоскопия с биопсией, туберкулиновые пробы, УЗИ органов брюшной полости, КТ. Терапия включает использование туберкулостатических препаратов, при наличии осложнений – лечение хирургическое.
МКБ-10
Общие сведения
Туберкулез кишечника - относительно редкий вид внелегочной локализации туберкулеза. В настоящее время распространенность данной патологии составляет около 45 случаев на 100 тысяч населения. Несмотря на достижения современной фтизиатрии, рост заболеваемости как легочным, так и абдоминальным туберкулезом продолжается. Актуальность проблемы заключается и в том, что отсутствуют методики скринингового обследования и ранние клинические симптомы туберкулеза кишечника. Малосимптомность данной формы, ее протекание под маской других заболеваний приводит к неуклонному росту выявления уже запущенных форм. Изучением туберкулеза кишечника занимаются специалисты в области гастроэнтерологии, фтизиатрии, хирургии.

Причины
Причиной развития данной патологии является попадание микобактерий туберкулеза непосредственно в слизистую оболочку кишечника. В зависимости от пути проникновения микроорганизмов выделяют первичный и вторичный туберкулез кишечника. Крайне редко регистрируется первый тип, который характеризуется формированием первичного очага специфического воспаления в слизистой как результата попадания микроорганизмов в ЖКТ извне (например, при употреблении инфицированного молока).
Реализация инфицирования при вторичном туберкулезе кишечника возможна тремя путями: гематогенным, лимфогенным и деглютационным. Деглютационный механизм инфицирования заключается в заглатывании содержащей большое количество бактерий мокроты при наличии легочного туберкулеза с очагами распада. Ранее данный путь развития патологии считался основным, и туберкулез кишечника рассматривался как завершающий этап общего заболевания. В настоящее время важная роль в формировании туберкулеза кишечника отводится гематогенному и лимфогенному путям (очаги поражения в кишечнике диагностируются у пациентов с туберкулезом мочеполовой, костно-суставной систем).
Для формирования очага специфического туберкулезного воспаления в кишечнике недостаточно только попадания микроорганизмов. Патология развивается при нарушении местной и общей сопротивляемости (риск повышается при неспецифических заболеваниях слизистой желудочно-кишечного тракта, воспалительно-дегенеративных изменениях нервного аппарата стенки кишечника).
Симптомы туберкулеза кишечника
Особенностью клинической картины туберкулеза кишечника является отсутствие специфических симптомов. Возможно и бессимптомное течение, когда диагноз устанавливается по результатам аутопсии. Первые признаки патологии могут проявляться спустя длительное время после инфицирования (от года до 10-15 лет). Симптоматика определяется стадией процесса, распространенностью и локализацией поражения.
На первом этапе развития заболевания под эпителием слизистой оболочки формируются гранулемы. В этот период клиническая картина характеризуется болями в животе слабой интенсивности, не имеющими четкой локализации. Возможны диспепсические явления: тошнота, нарушения стула (запоры, сменяющиеся поносами). Дальнейшее развитие патологического процесса сопровождается казеозным распадом очагов; болевой синдром становится более выраженным, боль постоянная, чаще всего локализуется в правой подвздошной области (туберкулез кишечника в большинстве случаев поражает илеоцекальную область), не связана с приемом пищи.
Присоединяются признаки интоксикации: пациент отмечает выраженную общую слабость, недомогание, температура повышается до субфебрильных цифр, снижается вес. Клиническая картина туберкулеза кишечника характеризуется сменой фаз обострения и затихания: периодически возникают эпизоды гипертермии, усиления диспепсических явлений.
Осложнения
При отсутствии адекватного лечения и прогрессировании специфического процесса возможна перфорация пораженного участка кишечника, развитие ограниченного или разлитого перитонита. При поражении червеобразного отростка возникает симптоматика острого аппендицита. При прорыве очага в полость кишечника отмечается обильная диарея с примесью крови, не поддающаяся противовоспалительному и антидиарейному лечению. Если в патологический процесс вовлекаются мезентериальные лимфоузлы, пациент отмечает появление постоянных интенсивных тупых болей в области пупка, которые усиливаются при смене положения тела, физической нагрузке. Симптомы интоксикации нарастают.
Диагностика
В выявлении данной патологии важную роль играет настороженность специалистов в отношении туберкулеза кишечника, детальное обследование пациентов с неопределенной симптоматикой поражения кишечника, болями в правой подвздошной области. Консультация гастроэнтеролога позволяет предположить наличие специфического воспаления. В начале заболевания диагностика затруднительна, поскольку нет специфических исследований, позволяющих верифицировать туберкулез кишечника. В то же время, скудность симптоматики приводит к тому, что пациенты обращаются уже на поздних этапах, когда имеет место казеозный некроз.
Для уточнения диагноза и локализации процесса могут проводиться КТ, УЗИ органов брюшной полости, но данные методы самостоятельного значения не имеют. Дифференциальная диагностика туберкулеза кишечника проводится с неспецифическим язвенным колитом, болезнью Крона, аппендицитом, злокачественными новообразованиями, амилоидозом кишечника.
Лечение туберкулеза кишечника
Лечение пациентов с верифицированным туберкулезом кишечника проводится в специализированных отделениях противотуберкулезных диспансеров. Применяются препараты: изониазид, рифампицин, ПАСК, фтивазид. В связи с распространенностью устойчивых форм микобактерий целесообразно одновременное назначение двух препаратов. При отсутствии эффективности назначаются препараты второго ряда: циклосерин, этамбутол, этионамид. Лечение туберкулостатическими препаратами проводится в течение полутора-двух лет до полного исчезновения клинической симптоматики.
Лечение туберкулеза кишечника также включает диетотерапию. Назначается питание с достаточным количеством белков, углеводов, жиров, высокой питательной ценностью. Дополнительно проводится витаминотерапия. При развитии осложнений (перфорация кишечника, кровотечение, формирование свищей, кишечная непроходимость, перитонит) проводится хирургическое лечение.
Прогноз и профилактика
Прогноз при данном заболевании неблагоприятный. Это связано с преимущественным выявлением запущенных форм туберкулеза кишечника, высоким процентом пациентов, которые самостоятельно прекращают лечение в связи с побочными эффектами или недисциплинированностью, большим количеством осложнений, в том числе сужений просвета кишечника с непроходимостью, наличием устойчивости микобактерий к химиопрепаратам. Более благоприятный прогноз при поражении толстого отдела кишечника, поскольку возможно выполнение обширной резекции.
Специфическая профилактика туберкулеза, в том числе и абдоминальной локализации, заключается в вакцинировании BCG (эффективность достигает 80%). Под наблюдением фтизиатров должны находиться лица, имеющие иммунодефицит или получающие иммуносупрессивную терапию. Специфическая химиопрофилактика (пероральный прием изониазида в течение года) назначается людям, имеющим контакт с больным открытой формой туберкулеза, а также с положительным результатом туберкулиновых проб.
Туберкулез легких – это инфекционная патология, вызываемая бациллой Коха, характеризующаяся различными в клинико-морфологическом отношении вариантами поражения легочной ткани. Многообразие форм туберкулеза легких обусловливает вариабельность симптоматики. Наиболее типичны для туберкулеза легких респираторные нарушения (кашель, кровохарканье, одышка) и симптомы интоксикации (длительный субфебрилитет, потливость, слабость). Для подтверждения диагноза используются лучевые, лабораторные исследования, туберкулинодиагностика. Химиотерапия туберкулеза легких проводится специальными туберкулостатическими препаратами; при деструктивных формах показано хирургическое лечение.
МКБ-10

Общие сведения
На сегодняшний день туберкулез легких представляет не только медико-биологическую, но и серьезную социально-экономическую проблему. По данным ВОЗ, туберкулезом инфицирован каждый третий житель планеты, смертность от инфекции превышает 3 млн. человек в год. Легочный туберкулез является самой частой формой туберкулезной инфекции. Удельный вес туберкулеза других локализаций (суставов, костей и позвоночника, гениталий, кишечника, серозных оболочек, ЦНС, глаз, кожи) в структуре заболеваемости значительно ниже.

Причины
Характеристика возбудителя
Отличительной чертой МБТ является их высокая устойчивость к внешним воздействиям (высоким и низким температурам, влажности, воздействию кислот, щелочей, дезинфектантов). Наименьшую стойкость возбудители туберкулеза легких демонстрируют к солнечному свету. Для человека опасность представляют туберкулезные бактерии человеческого и бычьего типа; случаи инфицирования птичьим типом микобактерий крайне редки.
Пути заражения
Основной путь заражения при первичном туберкулезе легких – аэрогенный: от больного открытой формой человека микобактерии распространяются с частичками слизи, выделяемыми в окружающую среду при разговоре, чихании, кашле; могут высыхать и разноситься с пылью на значительные расстояния. В дыхательные пути здорового человека инфекция чаще попадает воздушно-капельным или пылевым путем.
Меньшую роль в инфицировании играют алиментарный (при употреблении зараженных продуктов), контактный (при использовании общих предметов гигиены и посуды) и трансплацентарный (внутриутробный) пути. Причиной вторичного туберкулеза легких выступает повторная активация ранее перенесенной инфекции либо повторное заражение.
Факторы риска
Однако попадание МБТ в организм не всегда приводит к заболеванию. Факторами, на фоне которых туберкулез легких развивается особенно часто, считаются:
- неблагоприятные социально-бытовые условия
- курение и другие химические зависимости
- недостаточное питание
- иммуносупрессия (ВИЧ-инфекция, прием глюкокортикоидов, состояние после трансплантации органов)
- онкологические заболевания и др.
В группе риска по развитию туберкулеза легких находятся мигранты, заключенные, лица, страдающие наркотической и алкогольной зависимостью. Также имеет значение вирулентность инфекции и длительность контакта с больным человеком.
Патогенез
При снижении местных и общих факторов защиты микобактерии беспрепятственно проникают в бронхиолы, а затем в альвеолы, вызывая специфическое воспаление в виде отдельных или множественных туберкулезных бугорков или очагов творожистого некроза. В этот период появляется положительная реакция на туберкулин - вираж туберкулиновой пробы. Клинические проявления туберкулеза легких на этой стадии часто остаются нераспознанными. Небольшие очажки могут самостоятельно рассасываться, рубцеваться или обызвествляться, однако МБТ в них длительно сохраняются.
Классификация
Первичный туберкулез легких - это впервые развившаяся инфильтрация легочной ткани у лиц, не имеющих специфического иммунитета. Диагностируется преимущественно в детском и подростковом возрасте; реже возникает у лиц старшего и пожилого возраста, которые в прошлом перенесли первичную инфекцию, закончившуюся полным излечением. Первичный туберкулез легких может принимать форму:
- первичного туберкулезного комплекса (ПТК)
- туберкулеза внутригрудных лимфоузлов (ВГЛУ)
- хронически текущего туберкулеза.
Вторичный туберкулез легких развивается при повторном контакте с МБТ или в результате реактивации инфекции в первичном очаге. Основные вторичные клинические формы представлены:
Отдельно различают кониотуберкулез (туберкулез, развивающийся на фоне пневмокониозов), туберкулез верхних дыхательных путей, трахеи, бронхов; туберкулезный плеврит. При выделении больным МБТ в окружающую среду с мокротой говорят об открытой форме (ВК+) туберкулеза легких; при отсутствии бацилловыделения – о закрытой форме (ВК–). Также возможно периодическое бацилловыделение (ВК±).
Течение туберкулеза легких характеризуется последовательной сменной фаз развития:
- 1) инфильтративной
- 2) распада и обсеменения
- 3) рассасывания очага
- 4) уплотнения и обызвествления.
Симптомы туберкулеза легких
Первичный туберкулезный комплекс
Первичный туберкулезный комплекс сочетает в себе признаки специфического воспаления в легком и регионарный бронхоаденит. Может протекать бессимптомно или под маской простудных заболеваний, поэтому выявлению первичного туберкулеза легких способствуют массовые скрининги детей (проба Манту) и взрослых (профилактическая флюорография).
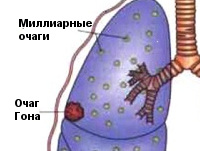
Чаще возникает подостро: больного беспокоит сухой кашель, субфебрилитет, утомляемость, потливость. При острой манифестации клиника напоминает неспецифическую пневмонию (высокая лихорадка, кашель, боль в груди, одышка). В результате лечения происходит рассасывание или обызвествление ПТК (очаг Гона). В неблагоприятных случаях может осложняться казеозной пневмонией, образованием каверн, туберкулезным плевритом, милиарным туберкулезом, диссеминацией микобактерий с поражением почек, костей, мозговых оболочек.
Туберкулез внутригрудных лимфоузлов
Признаки туберкулезной интоксикации включают отсутствие аппетита, снижение массы тела, утомляемость, бледность кожи, темные круги под глазами. На венозный застой в грудной полости может указывать расширение венозной сети на коже грудной клетки. Данная форма нередко осложняется туберкулезом бронхов, сегментарными или долевыми ателектазами легких, хронической пневмонией, экссудативным плевритом. При прорыве казеозных масс из лимфоузлов через стенку бронхов могут формироваться легочные очаги туберкулеза.
Очаговый туберкулез легких
Клиническая картина очагового туберкулеза малосимптомна. Кашель отсутствует или возникает редко, иногда сопровождается выделением скудной мокроты, болями в боку. В редких случаях отмечается кровохарканье. Чаще больные обращают внимание на симптомы интоксикации: непостоянный субфебрилитет, недомогание, апатию, пониженную работоспособность. В зависимости от давности туберкулезного процесса различают свежий и хронический очаговый туберкулез легких.
Течение очагового туберкулеза легких относительно доброкачественное. У больных с нарушенной иммунной реактивностью заболевание может прогрессировать в деструктивные формы туберкулеза легких.
Инфильтративный туберкулез легких
Клиническая картина инфильтративного туберкулеза легких зависит от величины инфильтрата и может варьировать от нерезко выраженных симптомов до острого лихорадочного состояния, напоминающего грипп или пневмонию. В последнем случае отмечается выраженная высокая температура тела, ознобы, ночная потливость, общая слабость. Со стороны органов дыхания беспокоит кашель с мокротой и прожилками крови.
В воспалительный процесс при инфильтративной форме туберкулеза легких часто вовлекается плевра, что обусловливает появление болей в боку, плеврального выпота, отставание пораженной половины грудной клетки при дыхании. Осложнениями инфильтративного туберкулеза легких могут стать казеозная пневмония, ателектаз легкого, легочное кровотечение и др.
Диссеминированный туберкулез легких
Может манифестировать в острой (милиарной), подострой и хронической форме. Тифоидная форма милиарного туберкулеза легких отличается преобладанием интоксикационного синдрома над бронхолегочной симптоматикой. Начинается остро, с нарастания температуры до 39-40 °С, головной боли, диспепсических расстройств, резкой слабости, тахикардии. При усилении токсикоза может возникать нарушение сознания, бред.
При легочной форме милиарного туберкулеза легких с самого начала более выражены дыхательные нарушения, включающие сухой кашель, одышку, цианоз. В тяжелых случаях развивается острая сердечно-легочная недостаточность. Менингеальной форме соответствуют симптомы поражения мозговых оболочек.
Подострое течение диссеминированного туберкулеза легких сопровождается умеренной слабостью, понижением работоспособности, ухудшением аппетита, похуданием. Эпизодически возникают подъемы температуры. Кашель продуктивный, не сильно беспокоит больного. Иногда первым признаком заболевания становится легочное кровотечение.
Хронический диссеминированный туберкулез легких при отсутствии обострения бессимптомен. Во время вспышки процесса клиническая картина близка к подострой форме. Диссеминированный туберкулеза легких опасен развитием внелегочного туберкулеза, спонтанного пневмоторакса, тяжелых легочных кровотечений, амилоидоза внутренних органов.
Кавернозный и фиброзно-кавернозный туберкулез легких
Характер течения кавернозного туберкулезного процесса волнообразный. В фазу распада нарастают интоксикационные симптомы, гипертермия, усиливается кашель и увеличивается количество мокроты, возникает кровохарканье. Часто присоединяется туберкулез бронхов и неспецифический бронхит.
Фиброзно-кавернозный туберкулез легких отличается формированием каверн с выраженным фиброзным слоем и фиброзными изменениями легочной ткани вокруг каверны. Протекает длительно, с периодическими обострениями общеинфекционной симптоматики. При частых вспышках развивается дыхательная недостаточность II-III степени.
Осложнениями, связанными с деструкцией легочной ткани, являются профузное легочное кровотечение, бронхоплевральный свищ, гнойный плеврит. Прогрессирование кавернозного туберкулеза легких сопровождается эндокринными расстройствами, кахексией, амилоидозом почек, туберкулезным менингитом, сердечно-легочной недостаточностью – в этом случае прогноз становится неблагоприятным.
Цирротический туберкулез легких
Является исходом различных форм туберкулеза легких при неполной инволюции специфического процесса и развитии на его месте фиброзно-склеротических изменений. При пневмоциррозе бронхи деформированы, легкое резко уменьшено в размерах, плевра утолщена и нередко обызвествлена.
Изменения, происходящие при цирротическом туберкулезе легких, обусловливают ведущие симптомы: выраженную одышку, тянущую боль в груди, кашель с гнойной мокротой, кровохарканье. При обострении присоединятся признаки туберкулезной интоксикации и бацилловыделение. Характерным внешним признаком пневмоцирроза служит уплощение грудной клетки на стороне поражения, сужение и втянутость межреберных промежутков. При прогрессирующем течении постепенно развивается легочное сердце. Цирротические изменения в легких необратимы.
Туберкулома легкого
Представляет собой инкапсулированный казеозный очаг, сформировавшийся в исходе инфильтративного, очагового или диссеминированного процесса. При стабильном течении симптомы не возникают, образование выявляется при рентгенографии легких случайно. В случае прогрессирующей туберкуломы легкого нарастает интоксикация, появляется субфебрилитет, боль в груди, кашель с отделением мокроты, возможно кровохарканье. При распаде очага туберкулома может трансформироваться в кавернозный или фиброзно-кавернозный туберкулез легких. Реже отмечается регрессирующее течение туберкуломы.
Диагностика
Диагноз той или иной формы туберкулеза легких выставляется врачом-фтизиатром на основании совокупности клинических, лучевых, лабораторных и иммунологических данных. Для распознавания вторичного туберкулеза большое значение имеет подробный сбор анамнеза. Для подтверждения диагноза проводится:
- Лучевая диагностика.Рентгенография легких является обязательным диагностической процедурой, позволяющей выявить характер изменений в легочной ткани (инфильтративный, очаговый, кавернозный, диссеминированный и т. д.), определить локализацию и распространенность патологического процесса. Выявление кальцинированных очагов указывает на ранее перенесенный туберкулезный процесс и требует уточнения данных с помощью КТ или МРТ легких.
- Анализы. Обнаружение МБТ достигается неоднократным исследованием мокроты (в т. ч. с помощью ПЦР), промывных вод бронхов, плеврального экссудата. Но сам по себе факт отсутствия бацилловыделения не является основанием для исключения туберкулеза легких. Современные иммунологические тесты позволяют выявить туберкулезную инфекцию почти со 100%-ной вероятностью. К ним относятся QuantiFERON и Т-спот. ТБ.
- Туберкулинодиагностика. К методам туберкулинодиагностики относятся диаскин-тест, пробы Пирке и Манту, однако сами по себе данные методы могут давать ложные результаты. Иногда для подтверждения туберкулеза легких приходится прибегать к пробному лечению противотуберкулезными препаратами с оценкой динамики рентгенологической картины.
По результатам проведенной диагностики туберкулез легких дифференцируют с пневмонией, саркоидозом легких, периферическим раком легкого, доброкачественными и метастатическими опухолями, пневмомикозами, кистами легких, абсцессом, силикозом, аномалиями развития легких и сосудов. Дополнительные методы диагностического поиска могут включать бронхоскопию, плевральную пункцию, биопсию легкого.

Лечение туберкулеза легких
Во фтизиатрической практике сформировался комплексный подход к лечению туберкулеза легких, включающий медикаментозную терапию, при необходимости - хирургическое вмешательство и реабилитационные мероприятия. Лечение проводится поэтапно: сначала в тубстационаре, затем в санаториях и, наконец, амбулаторно. Режимные моменты требуют организации лечебного питания, физического и эмоционального покоя.
- Противотуберкулезная терапия. Ведущая роль отводится специфической химиотерапии с помощью препаратов с противотуберкулезной активностью. Для терапии различных форм туберкулеза легких разработаны и применяются 3-х, 4-х и 5-тикомпонентные схемы (в зависимости от количества используемых препаратов). К туберкулостатикам первой линии (обязательным) относятся изониазид и его производные, пиразинамид, стрептомицин, рифампицин, этамбутол; средствами второго ряда (дополнительными) служат аминогликозиды, фторхинолоны, циклосерин, этионамид и др. Способы введения препаратов различны: перорально, внутримышечно, внутривенно, эндобронхиально, внутриплеврально, ингаляторно. Курсы противотуберкулезной терапии проводят длительно (в среднем 1 год и дольше).
- Патогенетическая терапия. При туберкулезе легких включает прием противовоспалительных средств, витаминов, гепатопротекторов, инфузионную терапию и пр. В случае лекарственной резистентности, непереносимости противотуберкулезных средств, при легочных кровотечениях используется коллапсотерапия.
- Хирургическое лечение. При соответствующих показаниях (деструктивных формах туберкулеза легких, эмпиеме, циррозе и ряде др.) применяются различные оперативные вмешательства: кавернотомию, торакопластику, плеврэктомию, резекцию легких.
Профилактика
Профилактика туберкулеза легких является важнейшей социальной проблемой и приоритетной государственной задачей. Первым шагом на этом пути является обязательная вакцинация новорожденных, детей и подростков. При массовых обследованиях в дошкольных и школьных учреждениях используется постановка внутрикожных туберкулиновых проб Манту. Скрининг взрослого населения осуществляется путем проведения профилактической флюорографии.
Заболеваемость туберкулезом легких среди больных язвенной болезнью желудка и двенадцатиперстной кишки и у лиц, перенесших резекцию желудка по поводу язвенной болезни, в 3-4 раза выше, чем в общей популяции. Наиболее часто сочетание язвенной болезни и туберкулеза легких встречается у мужчин молодого и среднего возраста, т.е. у наиболее трудоспособной части населения.
В настоящее время туберкулез в России приобрел значение глобальной проблемы, создающей угрозу национальной безопасности. Как и ранее, основными причинами роста заболеваемости туберкулезом остаются социальные факторы: снижение уровня жизни, миграция больших групп населения, алкоголизм и различные виды наркомании.
В настоящей статье мы хотим обсудить еще одну из причин, повышающих риск заболевания туберкулезом - тяжелую хроническую патологию внутренних органов и, в частности, язвенную болезнь желудка и двенадцатиперстной кишки. Научно доказано, что лица с сопутствующими заболеваниями внутренних органов: хроническими неспецифическими заболеваниями легких, врожденными и приобретенными иммунодефицитами, сахарным диабетом, патологией желудочно-кишечного тракта - являются одной из основных групп риска заболевания туберкулезом. Отмечено, что у больных туберкулезом легких пожилого возраста преобладает сопутствующая патология сердечно-сосудистой системы и сахарный диабет, а в молодом возрасте более актуальны патология желудочно-кишечного тракта и хронический алкоголизм.
Болезни желудочно-кишечного тракта занимают второе место среди всех сопутствующих заболеваний при туберкулезе легких и, по данным исследований, составляют до 30% случаев. Чаще всего туберкулезу легких сопутствуют вирусные гепатиты и патология верхних отделов желудочно-кишечного тракта.
Изучение состояния желудка у больных туберкулезом легких имеет длительную историю. Еще в конце XIX в. появилось понятие "претуберкулезной диспепсии". Это было связано с тем, что у части больных с неясным диагнозом, предъявлявших жалобы на стойкое отсутствие аппетита, похудание, неприятные ощущения в эпигастральной области, годами посещавших врачей, впоследствии выявлялся туберкулез легких. Уже в то время было сделано предположение, что диспептические явления у больных туберкулезом связаны с функциональными нарушениями желудка. Однако основные достижения в изучении данной проблемы относятся к более позднему периоду, когда появившиеся новые технические средства позволили проводить прижизненную диагностику язвенной болезни и хронического гастрита у больных туберкулезом.
Почему больные язвенной болезнью чаще страдают туберкулезом легких? Предполагается, что длительное использование малокалорийной противоязвенной диеты, дисбаланс в работе нервной системы организма, частые обострения с расстройствами пищеварения снижают сопротивляемость организма к инфекционным заболеваниям, в том числе к туберкулезу. У больных, перенесших резекцию желудка по поводу язвенной болезни, нарушается всасывание жиров, белков, углеводов, минеральных солей, витаминов, что еще в большей мере повышает риск развития туберкулеза легких. Туберкулез легких обычно развивается в первые 5 лет после заболевания язвенной болезнью или резекции желудка.
Туберкулез легких при сопутствующей язвенной болезни характеризуется неблагоприятным течением, чаще выявляются формы с большим объемом поражения и распадом легочной ткани. Нередко обострение язвенной болезни ведет к прогрессированию туберкулезного процесса. Характерны высокая частота рецидивов и низкая эффективность лечения, реже удается добиться прекращения бактериовыделения и закрытия полостей распада. Сочетание язвенной болезни и туберкулеза легких характеризуется длительной потерей трудоспособности, частой инвалидизацией. Еще хуже результаты лечения больных туберкулезом, перенесших резекцию желудка по поводу язвенной болезни. У повторно поступающих в стационар больных с сочетанной патологией в половине случаев отмечается лекарственная устойчивость выделяемых микобактерий туберкулеза.
Предотвратить обострение язвенной болезни и хронического гастрита на фоне приема противотуберкулезных препаратов можно только учитывая современные представления о причинах и механизмах развития этих заболеваний.
Повреждения слизистой оболочки желудка и двенадцатиперстной кишки развиваются вследствие нарушения равновесия между факторами агрессии и факторами защиты. К основным факторам агрессии относятся повышение выработки соляной кислоты и пепсина, сбои в регуляции желудочной секреции, нарушение механизмов обновления клеток слизистой оболочки, повышение выработки стимуляторов желудочной секреции, повреждающее действие некоторых лекарственных препаратов. При туберкулезе легких, кроме выше перечисленных факторов, актуальны воздействие специфической интоксикации и длительный прием противотуберкулезных препаратов.
Открытый в 1983 году жгутиковый микроорганизм, паразитирующий в толще слизистой оболочки желудка, названный позже Helicobacter pylori, пополнил список известных факторов риска развития гастродуоденальной патологии. Более того, некоторые исследователи считают Helicobacter pylori главной причиной развития хронического гастрита и главным фактором патогенеза язвенной болезни двенадцатиперстной кишки.
В клинике фтизиатрии Военно-Медицинской академии было проведено исследование, посвященное изучению морфологического и функционального состояния желудка у больных туберкулезом легких молодого возраста.
Исследование показало, что 90% больных, поступающих в противотуберкулезные стационары, имеют различной степени выраженности воспалительно-дистрофические изменения слизистой оболочки желудка, частота и интенсивность обсеменения Helicobacter pylori у больных туберкулезом достоверно выше, чем у здоровых лиц такого же возраста. На фоне длительного приема противотуберкулезных препаратов отмечено нарастание интенсивности обсеменения слизистой оболочки желудка Helicobacter pylori и связанной с этим выраженности гастритических изменений.
Для профилактики и раннего выявления сопутствующей патологии желудка и двенадцатиперстной кишки у больных туберкулезом легких при поступлении в стационар необходимо проводить опрос, целью которого является обнаружение факторов риска развития гастрита и язвенной болезни. При появлении жалоб на пищеварительные расстройства больного необходимо углубленно обследовать.
Для лечения обострений язвенной болезни и хронического гастрита у больных туберкулезом мы используем преимущественно препараты, создающие защитный барьер, препятствующий повреждению слизистой оболочки желудка, при этом не снижающие в значительной степени кислотность желудочного сока. К таким препаратам относятся вентер, де-нол, викалин. Наиболее быстро и эффективно больным туберкулезом с сопутствующим гастритом и язвенной болезнью помогает де-нол, обладающий выраженной активностью в отношении Helicobacter pylori.
В заключение мы хотим обратить внимание на тот факт, что нередко больные язвенной болезнью при малосимптомном начале туберкулеза принимают общие симптомы интоксикации (слабость, похудание, потерю аппетита) за проявления основного заболевания и длительное время не обращаются к врачу, что приводит к развитию распространенных деструктивных форм туберкулеза легких. Врачи-гастроэнтерологи, наблюдающие больных язвенной болезнью, должны рекомендовать им регулярно проходить флюорографическое обследование легких, а при появлении симптомов туберкулезной интоксикации и поражения органов дыхания направлять на микроскопическое исследование мокроты и консультацию фтизиатра.
Для врачей-фтизиатров основные проблемы лечения больных с сочетанием язвенной болезни и туберкулеза легких связаны с часто возникающими обострениями язвы на фоне терапии, что существенно ухудшает переносимость лекарственных препаратов, а в ряде случаев является причиной их отмены. В условиях все большего распространения лекарственной устойчивости микобактерий туберкулеза отмена резервных препаратов вследствие их непереносимости может сыграть трагическую роль в судьбе больного! Вот почему так важно прогнозировать и своевременно выявлять обострение гастродуоденальной патологии на фоне туберкулостатической терапии.
Представлен обзор отечественных и зарубежных исследований, посвященных применению на фоне противотуберкулезной терапии гепатопротекторов, в том числе препаратов производных метионина и содержащих янтарную кислоту.
Ключевые слова: гепатопротекторы, полихимиотерапия, туберкулез, нежелательные явления, препараты янтарной кислоты, производные метионина
Use of hepatoprotectors during tuberculosis chemotherapy: review of the russian and international studies
А. А. Stаrshinovа 1,2 , E. N. Belyaevа 1,3 , А. M. Рanteleev 3,4 , M. V Pаvlovа 1
1 St. Petersburg Research Institute of Phthisiopulmonology, St. Petersburg, Russia
2 St. Petersburg University, St. Petersburg, Russia
3 Tuberculosis Hospital no. 2, St. Petersburg
4 Pavlov First Saint Petersburg State Medical University, St. Petersburg, Russia
The article presents the review of the Russian and international studies devoted to the use of hepatoprotectors during anti-tuberculosis treatment, including methionine derivatives and agents containing succinic acid.
Key words: hepatoprotectors, polychemotherapy, tuberculosis, adverse events, drugs containing succinic acid, methionine derivatives
Основными причинами распространения туберкулеза с лекарственной устойчивостью возбудителя являются проблемы в организации лечения: прерывание лечения пациентами, невыполнение стандартных режимов химиотерапии. Этому способствует высокая частота возникновения нежелательных явлений на прием отдельных противотуберкулезных препаратов (ПТП) и их сочетаний [1, 20, 25].
При лечении туберкулеза, оказывая влияние на жизнедеятельность микобактерий туберкулеза, ПТП одновременно влияют на макроорганизм, вызывая функциональные нарушения многих систем организма пациента [1, 2, 14, 20, 25].
Систематизации нежелательных явлений на препараты уделяется значительное внимание с момента появления химиотерапии, что привело к созданию нескольких классификаций, одни разработаны на основе повреждения определенных органов и систем, другие - с учетом особенностей патогенеза нежелательных воздействий препаратов [3, 6].
Гепатотоксические реакции на фоне ПТП отмечаются, по данным разных авторов, в 44-60% случаев и связаны с образованием метаболитов, вызывающих в 60% случаев токсическое повреждение печени, что проявляется нарушением дезинтоксикационной, белковосинтетической и других функций. Лекарственные гепатиты могут сопровождаться синдромом цитолиза в 34,1%, явлениями холестаза - в 50% и их сочетанием - в 15,9% случаев [3, 5, 8, 28].
Механизмы гепатотоксичности бывают разными, что доказано в экспериментальных исследованиях [13] (рис.).
Рис. Механизмы гепатотоксичности (фармакотерапия лекарственных поражений печени при туберкулезе [13])
Fig. Mechanisms of hepatotoxicity (pharmacotherapy of drug-induced liver damage in case of tuberculosis [13])
Основными виновниками развития гепатотоксических реакций являлись рифампицин (67% случаев), пиразинамид (30%) и изониазид (7%) [3, 4, 8, 23, 27]. По данным ряда авторов, гепатотоксические реакции вызывают протионамид, парааминосалициловая кислота, линезолид, бедаквилин и тиоуреидоиминометилпиридиния перхлорат. Как правило, наряду с ними, развиваются гиперурикемия, артралгия, поражение желудочно-кишечного тракта, центральной нервной системы, полинейропатия, кардио- и нефропатические реакции [10, 16].
Поражение печени при туберкулезе может быть обусловлено не только токсическим влиянием препаратов, но и интоксикационным воздействием самого инфекционного процесса, а также развитием системного воспалительного ответа. При этом факторами риска развития гепатотоксических реакций являются хронические заболевания печени и желчевыводящих путей [4, 11, 26].
В клинической практике встречаются от 1,7 до 90,0% случаев, когда нежелательные явления на фоне противотуберкулезной терапии носят как токсический, так и аллергический характер (токсико-аллергические проявления) [2, 3, 12].
По данным немногочисленных исследований, риск развития лекарственно-индуцированных нарушений органов и систем, а также электролитного обмена на фоне полихимиотерапии туберкулеза у больных с множественной лекарственной устойчивостью возбудителя отмечается в 86-90% случаев, что в несколько раз чаще, чем у больных с лекарственно-чувствительным к изониазиду и рифампицину возбудителем [1, 2, 5, 10].
Отечественные и международные подходы по ведению больных туберкулезом на фоне полихимиотерапии различаются в отношении применения терапии сопровождения. В международной практике возможно проведение коррекции нежелательных явлений при их возникновении, тогда как в отечественной практике рекомендуют назначение корригирующей терапии одновременно с началом химиотерапии для предотвращения нежелательных явлений, особенно со стороны печени и желудочно-кишечного тракта. Вопрос применения гепатопротекторов остается нерешенным, что связано с отсутствием достаточной доказательной базы, а также клинических исследований по определению эффективности их применения.
Согласно результатам доклинических исследований, на крысах гепатотоксическое влияние изониазида в дозе 100 мг/кг отмечалось уже через 21 день. При приеме ежедневной комбинации изониазида (50 мг/кг) и рифампицина (100 мг/кг) у мышей происходили нарушения окислительно-восстановительной функции печени с апоптотическим повреждением ее клеток. В исследовании не было найдено доказательств того, что прием данных препаратов три раза в неделю снижает риск развития этих реакций [21].
Поскольку изониазид и рифампицин являются высокоэффективными препаратами, их применение при лечении латентной или активной туберкулезной инфекции является оптимальным. Только у пациентов с нестабильным или прогрессирующим заболеванием печени, если уровень аланина аминотрансферазы в сыворотке крови более чем в 3 раза выше нормы уже на исходном уровне, не следует рассматривать совместное применение данных препаратов. Авторами сделан вывод о необходимости сокращения количества гепатотоксических препаратов и длительности их применения в зависимости от тяжести течения заболевания печени [24].
В одном из проспективных исследований, проведенном в Китае на когорте больных туберкулезом (n = 4 488), оценена эффективность применения гепатопротективных препаратов (силимарина, глюкуроновой кислоты, инозина) для предотвращения развития гепатотоксических реакций на фоне противотуберкулезной терапии. Пациенты принимали гепатопротекторы в течение 183 дней и более. Согласно мониторингу биохимических показателей крови, характеризующих функциональное состояние печени, значимых отличий с группой контроля не получавших эти препараты, не обнаружено [27].
Интересны данные метаанализа [19], проведенного по публикациям 1970-2011 гг., обнаруженным в информационных системах, соответствующим обозначенным требованиям. Описаны результаты лечения 40 034 пациентов с туберкулезом легких, из которых у 1 208 (3,1%) были проявления гепатотоксичности на прием препаратов, из них 339 пациентов имели возраст старше 60 лет. Было доказано, что у пациентов старше 60 лет гепатотоксическая реакция чаще всего связана с приемом пиразинамида и несколько реже - рифампицина и изониазида. Однако различия в уровнях трансаминаз на прием каждого из этих препаратов не были статистически значимыми. Полученные данные потребовали пересмотра нормативных документов по лечению туберкулеза в США и улучшения мониторинга проявлений гепатотоксичности у пациентов от 60 лет и старше. Обозначена необходимость проведения мониторинга клинической симптоматики и биохимических показателей каждые две недели у лиц данной категории, чего ранее не проводилось.
Сопоставимые данные были в исследовании Суханова Д. С. и др. (2013), которые показали, что применение сукцинатсодержащих инфузионных растворов [меглюмина натрия сукцината (в виде препарата реамберина) и комбинации N-метилглюкамина (меглумина) - 8,725 г; янтарной кислоты -5,280 г; инозина - 2,0 г; метионина - 0,75 г; никотинамида - 0,25 г (в виде препарата ремаксола)] эффективно снимает гепатотоксические реакции, индуцированные применением ПТП у больных туберкулезом легких [14].
В проведенном Д. А. Ивановой исследовании получены данные о факторах риска лекарственного поражения печени, которыми являются: женский пол, лекарственная аллергия в анамнезе, дефицит питания. Ею доказано, что первые две недели противотуберкулезной химиотерапии являются периодом наибольшего риска развития неблагоприятных вариантов лекарственного поражения печени (40,9% всех случаев лекарственного поражения печени, 95%-ный ДИ 33,2-50,3%) [4].
Причины возникновения нежелательных явлений во многом обусловлены не только непосредственным действием лекарственного средства, возрастом и полом больного, но и тяжестью его состояния и спектром сопутствующих заболеваний, длительностью приема и способом введения лекарственного средства, а также взаимодействием препарата в организме (фармакодинамические и фармакокинетические аспекты). Нежелательные явления различной степени тяжести развиваются в 10-30% случаев у пациентов стационара и в 40% - при амбулаторном лечении, а также являются причиной госпитализации от 6 до 16% пациентов. В странах Европы 10-25% бюджета стационаров расходуется на лечение осложнений лекарственной терапии [17, 20].
Аналогичные результаты получены и в других исследованиях. При этом появление нежелательных явлений в виде лекарственного поражения печени являлось основной причиной, препятствующей получению хорошего эффекта противотуберкулезной терапии из-за ее прерывания и коррекции [8, 19].
Положительный эффект применения гепатопротекторов при противотуберкулезной химиотерапии чаще подтверждается по результатам отечественных исследований.
Среди препаратов, применяемых для фармакотерапии различных поражений печени, выделяют относительно небольшую группу лекарственных средств, для которых гепатотропное действие является основным, преобладающим или имеющим самостоятельное клиническое значение. Фармакологическое действие данных препаратов заключается в повышении резистентности печени к повреждающему действию различных патогенов, в восстановлении функциональной активности гепатоцитов и регуляции репаративно-регенераторных процессов [6]. В патогенезе повреждения гепатоцитов при хронических поражениях печени важную роль играет развитие тканевой гипоксии, которая приводит к нарушению функций митохондрий и, как следствие, снижению запасов АТФ с активацией высвобождения свободных радикалов [7, 11].
Сегодня на медицинском рынке представлено большое количество гепатопротекторов различных групп: эссенциальные фосфолипиды, производные метионина, препараты на основе расторопши и других растений, холелитолитики, производные део- и урсоксихолевой кислот. Исследования, доказывающие их эффективность, проведены только по некоторым из них.
Ремаксол является раствором, его наиболее активный компонент янтарная кислота - универсальный энергообеспечивающий интермедиат цикла Кребса. В физиологических условиях она диссоциирована, являясь продуктом пятой и субстратом шестой реакции цикла трикарбоновых кислот Кребса, поэтому название ее аниона - сукцинат - часто используют как синоним янтарной кислоты. При этом мощность системы энергопродукции, использующей сукцинат, в сотни раз превосходит все другие системы энергообразования организма [6, 7].
При проведении рандомизированного многоцентрового плацебо контролируемого клинического исследования на базе 7 клинических центров с включением 494 пациентов с хроническим гепатитом С и В различной степени активности отмечено, что у них после курсового приема ремаксола (раствор для инфузий) зафиксировано снижение уровня трансаминаз в 1,8 раза по сравнению с группой контроля, в том числе за счет антихолестатического эффекта препарата [11].
В исследованиях показано, что, обладая выраженным гепатопротекторным действием, ремаксол улучшает энергетическое обеспечение гепатоцитов, повышая устойчивость мембран клеток к перекисному окислению липидов и восстанавливая активность ферментов антиоксидантной защиты. Это позволяет применять его в качестве терапии сопровождения при различных патологических состояниях. Детоксицирующая активность препарата обеспечивается стимуляцией оттока желчных кислот, предотвращая застой желчи и отравление организма желчными кислотами, в результате чего восстанавливается функция печени, нет влияния на реологические свойства крови. Происходит нормализация показателей, характеризующих степень поражения гепатоцитов (АлТ, АсТ, ЩФ, ГГТП) и функциональное состояние печени за счет уменьшения цитолитического и холестатического синдромов [7, 12].
В исследовании Д. С. Суханова получены доказательства эффективности препаратов ремаксола и реамберина в эксперименте [13]. Так, зафиксировано их положительное влияние на показатели липидного обмена: уровень триглицеридов статистически значимо уменьшился, нормализовались показатели АлАТ и АсАТ. При морфологическом исследовании печени установлено, что параллельно с улучшением биохимических показателей уменьшался некробиоз гепатоцитов с сокращением распространенности жировой дистрофии, которая регистрировалась только на периферии долек и в междольковом пространстве. При применении адеметионина (независимо от способа введения и дозы) в 45,5% случаев обнаруживали очаги некроза различной величины, что свидетельствовало о стимуляции альтерации печеночной ткани, это связано с процессом карбоксиметилирования белков, продуктами которого являются метанол, формальдегид и муравьиная кислота, обладающие цитотоксическим действием [14, 13].
В детской практике на фоне полихимиотерапии в 72,2% случаев отмечалось нарушение функции печени, которое отражалось в биохимических показателях крови (повышение уровня общего билирубина, трансаминаз, тимоловой пробы, уровня щелочной и кислой фосфатаз) [9]. Нормализация биохимических показателей на фоне применения гепатопротекторов (Лив 52) отмечалась через 1 мес. в 23% случаев, через 2 мес. - в 67% случаев, к концу 3-го мес. - в 100% случаев, что обусловлено стимулирующим действием на регенерацию гепатоцитов, а также мембраностабилизирующим действием, что особенно ценно при длительной противотуберкулезной терапии. Снижение активности щелочной и кислой фосфатаз свидетельствовало о нормализации функциональной активности печени и функции желчеобразования [15].
Следовательно, применение гепатопротекторов является желательным на фоне лечения туберкулеза, в особенности при появлении нежелательных явлений, связанных с нарушением функции печени. Согласно международным рекомендациям, коррекция нежелательных явлений со стороны печени и желчевыводящих путей должна осуществляться только после появления функциональных нарушений третей и четвертой степени тяжести [17]. Однако отечественные исследователи считают необходимым назначение гепатопротекторов одновременно с применением ПТП не только при появлении нарушений функции печени, но и при тяжелом течении процесса для снятия интоксикационного воздействия на печень [3, 4, 12].
Назначение корригирующей терапии при возникновении нежелательных явлений на фоне лечения туберкулеза (в том числе при сочетании с ВИЧ-инфекцией) в настоящее время является обоснованным [4, 14].
При оценке нежелательных явлений, развивающихся в ходе химиотерапии туберкулеза, следует учитывать, что возможна суммация побочного действия разных ПТП, если они направлены на одни и те же органы-мишени (например, на печень). При серьезных нежелательных явлениях необходима временная отмена и/или замена всей схемы химиотерапии [4, 18].
Согласно проведенным исследованиям, назначение и выбор гепатопротективных препаратов должны проводиться в зависимости от степени повышения биохимических показателей (АЛТ, щелочной фосфатазы и билирубина), а также на основании оценки факторов риска развития нежелательных явлений со стороны печени [4].
Современная фармакотерапия заболеваний печени строится на комплексном использовании нескольких направлений [3, 5-7]:
1) профилактического, призванного обеспечить первичную защиту печени от различных повреждений;
2) этиотропного, направленного на элиминацию патологического возбудителя из организма;
3) патогенетического, нацеленного на коррекцию универсальных мультифакторных звеньев патогенеза заболевания;
4) симптоматического.
Основной целью лечения болезней печени является восстановление морфологической и функциональной полноценности органа.
Заключение
Повышение эффективности лечения туберкулеза легких является одной из важнейших задач в борьбе с туберкулезом. Современные схемы противотуберкулезной терапии включают прием нескольких ПТП, обладающих выраженным токсическим эффектом, вызывающим нарушения функции печени в 70-80% случаев. Применение эффективных гепатопротекторов для профилактики и устранения лекарственного поражения печени при лечении туберкулеза является необходимым и обоснованным.
Препаратом выбора для купирования гепатотоксичности является инфузионный гепатотропный препарат ремаксол, обладающий мультимодальным фармакологическим действием на патогенетические механизмы развития лекарственных и токсических поражений печени.
Конфликт интересов. Авторы заявляют об отсутствии у них конфликта интересов.
Conflict of Interests. The authors state that they have no conflict of interests.
ЛИТЕРАТУРА
Читайте также:

