Туберкулез легких и рак желудка
Обновлено: 25.04.2024
Представлен обзор отечественных и зарубежных исследований, посвященных применению на фоне противотуберкулезной терапии гепатопротекторов, в том числе препаратов производных метионина и содержащих янтарную кислоту.
Ключевые слова: гепатопротекторы, полихимиотерапия, туберкулез, нежелательные явления, препараты янтарной кислоты, производные метионина
Use of hepatoprotectors during tuberculosis chemotherapy: review of the russian and international studies
А. А. Stаrshinovа 1,2 , E. N. Belyaevа 1,3 , А. M. Рanteleev 3,4 , M. V Pаvlovа 1
1 St. Petersburg Research Institute of Phthisiopulmonology, St. Petersburg, Russia
2 St. Petersburg University, St. Petersburg, Russia
3 Tuberculosis Hospital no. 2, St. Petersburg
4 Pavlov First Saint Petersburg State Medical University, St. Petersburg, Russia
The article presents the review of the Russian and international studies devoted to the use of hepatoprotectors during anti-tuberculosis treatment, including methionine derivatives and agents containing succinic acid.
Key words: hepatoprotectors, polychemotherapy, tuberculosis, adverse events, drugs containing succinic acid, methionine derivatives
Основными причинами распространения туберкулеза с лекарственной устойчивостью возбудителя являются проблемы в организации лечения: прерывание лечения пациентами, невыполнение стандартных режимов химиотерапии. Этому способствует высокая частота возникновения нежелательных явлений на прием отдельных противотуберкулезных препаратов (ПТП) и их сочетаний [1, 20, 25].
При лечении туберкулеза, оказывая влияние на жизнедеятельность микобактерий туберкулеза, ПТП одновременно влияют на макроорганизм, вызывая функциональные нарушения многих систем организма пациента [1, 2, 14, 20, 25].
Систематизации нежелательных явлений на препараты уделяется значительное внимание с момента появления химиотерапии, что привело к созданию нескольких классификаций, одни разработаны на основе повреждения определенных органов и систем, другие - с учетом особенностей патогенеза нежелательных воздействий препаратов [3, 6].
Гепатотоксические реакции на фоне ПТП отмечаются, по данным разных авторов, в 44-60% случаев и связаны с образованием метаболитов, вызывающих в 60% случаев токсическое повреждение печени, что проявляется нарушением дезинтоксикационной, белковосинтетической и других функций. Лекарственные гепатиты могут сопровождаться синдромом цитолиза в 34,1%, явлениями холестаза - в 50% и их сочетанием - в 15,9% случаев [3, 5, 8, 28].
Механизмы гепатотоксичности бывают разными, что доказано в экспериментальных исследованиях [13] (рис.).
Рис. Механизмы гепатотоксичности (фармакотерапия лекарственных поражений печени при туберкулезе [13])
Fig. Mechanisms of hepatotoxicity (pharmacotherapy of drug-induced liver damage in case of tuberculosis [13])
Основными виновниками развития гепатотоксических реакций являлись рифампицин (67% случаев), пиразинамид (30%) и изониазид (7%) [3, 4, 8, 23, 27]. По данным ряда авторов, гепатотоксические реакции вызывают протионамид, парааминосалициловая кислота, линезолид, бедаквилин и тиоуреидоиминометилпиридиния перхлорат. Как правило, наряду с ними, развиваются гиперурикемия, артралгия, поражение желудочно-кишечного тракта, центральной нервной системы, полинейропатия, кардио- и нефропатические реакции [10, 16].
Поражение печени при туберкулезе может быть обусловлено не только токсическим влиянием препаратов, но и интоксикационным воздействием самого инфекционного процесса, а также развитием системного воспалительного ответа. При этом факторами риска развития гепатотоксических реакций являются хронические заболевания печени и желчевыводящих путей [4, 11, 26].
В клинической практике встречаются от 1,7 до 90,0% случаев, когда нежелательные явления на фоне противотуберкулезной терапии носят как токсический, так и аллергический характер (токсико-аллергические проявления) [2, 3, 12].
По данным немногочисленных исследований, риск развития лекарственно-индуцированных нарушений органов и систем, а также электролитного обмена на фоне полихимиотерапии туберкулеза у больных с множественной лекарственной устойчивостью возбудителя отмечается в 86-90% случаев, что в несколько раз чаще, чем у больных с лекарственно-чувствительным к изониазиду и рифампицину возбудителем [1, 2, 5, 10].
Отечественные и международные подходы по ведению больных туберкулезом на фоне полихимиотерапии различаются в отношении применения терапии сопровождения. В международной практике возможно проведение коррекции нежелательных явлений при их возникновении, тогда как в отечественной практике рекомендуют назначение корригирующей терапии одновременно с началом химиотерапии для предотвращения нежелательных явлений, особенно со стороны печени и желудочно-кишечного тракта. Вопрос применения гепатопротекторов остается нерешенным, что связано с отсутствием достаточной доказательной базы, а также клинических исследований по определению эффективности их применения.
Согласно результатам доклинических исследований, на крысах гепатотоксическое влияние изониазида в дозе 100 мг/кг отмечалось уже через 21 день. При приеме ежедневной комбинации изониазида (50 мг/кг) и рифампицина (100 мг/кг) у мышей происходили нарушения окислительно-восстановительной функции печени с апоптотическим повреждением ее клеток. В исследовании не было найдено доказательств того, что прием данных препаратов три раза в неделю снижает риск развития этих реакций [21].
Поскольку изониазид и рифампицин являются высокоэффективными препаратами, их применение при лечении латентной или активной туберкулезной инфекции является оптимальным. Только у пациентов с нестабильным или прогрессирующим заболеванием печени, если уровень аланина аминотрансферазы в сыворотке крови более чем в 3 раза выше нормы уже на исходном уровне, не следует рассматривать совместное применение данных препаратов. Авторами сделан вывод о необходимости сокращения количества гепатотоксических препаратов и длительности их применения в зависимости от тяжести течения заболевания печени [24].
В одном из проспективных исследований, проведенном в Китае на когорте больных туберкулезом (n = 4 488), оценена эффективность применения гепатопротективных препаратов (силимарина, глюкуроновой кислоты, инозина) для предотвращения развития гепатотоксических реакций на фоне противотуберкулезной терапии. Пациенты принимали гепатопротекторы в течение 183 дней и более. Согласно мониторингу биохимических показателей крови, характеризующих функциональное состояние печени, значимых отличий с группой контроля не получавших эти препараты, не обнаружено [27].
Интересны данные метаанализа [19], проведенного по публикациям 1970-2011 гг., обнаруженным в информационных системах, соответствующим обозначенным требованиям. Описаны результаты лечения 40 034 пациентов с туберкулезом легких, из которых у 1 208 (3,1%) были проявления гепатотоксичности на прием препаратов, из них 339 пациентов имели возраст старше 60 лет. Было доказано, что у пациентов старше 60 лет гепатотоксическая реакция чаще всего связана с приемом пиразинамида и несколько реже - рифампицина и изониазида. Однако различия в уровнях трансаминаз на прием каждого из этих препаратов не были статистически значимыми. Полученные данные потребовали пересмотра нормативных документов по лечению туберкулеза в США и улучшения мониторинга проявлений гепатотоксичности у пациентов от 60 лет и старше. Обозначена необходимость проведения мониторинга клинической симптоматики и биохимических показателей каждые две недели у лиц данной категории, чего ранее не проводилось.
Сопоставимые данные были в исследовании Суханова Д. С. и др. (2013), которые показали, что применение сукцинатсодержащих инфузионных растворов [меглюмина натрия сукцината (в виде препарата реамберина) и комбинации N-метилглюкамина (меглумина) - 8,725 г; янтарной кислоты -5,280 г; инозина - 2,0 г; метионина - 0,75 г; никотинамида - 0,25 г (в виде препарата ремаксола)] эффективно снимает гепатотоксические реакции, индуцированные применением ПТП у больных туберкулезом легких [14].
В проведенном Д. А. Ивановой исследовании получены данные о факторах риска лекарственного поражения печени, которыми являются: женский пол, лекарственная аллергия в анамнезе, дефицит питания. Ею доказано, что первые две недели противотуберкулезной химиотерапии являются периодом наибольшего риска развития неблагоприятных вариантов лекарственного поражения печени (40,9% всех случаев лекарственного поражения печени, 95%-ный ДИ 33,2-50,3%) [4].
Причины возникновения нежелательных явлений во многом обусловлены не только непосредственным действием лекарственного средства, возрастом и полом больного, но и тяжестью его состояния и спектром сопутствующих заболеваний, длительностью приема и способом введения лекарственного средства, а также взаимодействием препарата в организме (фармакодинамические и фармакокинетические аспекты). Нежелательные явления различной степени тяжести развиваются в 10-30% случаев у пациентов стационара и в 40% - при амбулаторном лечении, а также являются причиной госпитализации от 6 до 16% пациентов. В странах Европы 10-25% бюджета стационаров расходуется на лечение осложнений лекарственной терапии [17, 20].
Аналогичные результаты получены и в других исследованиях. При этом появление нежелательных явлений в виде лекарственного поражения печени являлось основной причиной, препятствующей получению хорошего эффекта противотуберкулезной терапии из-за ее прерывания и коррекции [8, 19].
Положительный эффект применения гепатопротекторов при противотуберкулезной химиотерапии чаще подтверждается по результатам отечественных исследований.
Среди препаратов, применяемых для фармакотерапии различных поражений печени, выделяют относительно небольшую группу лекарственных средств, для которых гепатотропное действие является основным, преобладающим или имеющим самостоятельное клиническое значение. Фармакологическое действие данных препаратов заключается в повышении резистентности печени к повреждающему действию различных патогенов, в восстановлении функциональной активности гепатоцитов и регуляции репаративно-регенераторных процессов [6]. В патогенезе повреждения гепатоцитов при хронических поражениях печени важную роль играет развитие тканевой гипоксии, которая приводит к нарушению функций митохондрий и, как следствие, снижению запасов АТФ с активацией высвобождения свободных радикалов [7, 11].
Сегодня на медицинском рынке представлено большое количество гепатопротекторов различных групп: эссенциальные фосфолипиды, производные метионина, препараты на основе расторопши и других растений, холелитолитики, производные део- и урсоксихолевой кислот. Исследования, доказывающие их эффективность, проведены только по некоторым из них.
Ремаксол является раствором, его наиболее активный компонент янтарная кислота - универсальный энергообеспечивающий интермедиат цикла Кребса. В физиологических условиях она диссоциирована, являясь продуктом пятой и субстратом шестой реакции цикла трикарбоновых кислот Кребса, поэтому название ее аниона - сукцинат - часто используют как синоним янтарной кислоты. При этом мощность системы энергопродукции, использующей сукцинат, в сотни раз превосходит все другие системы энергообразования организма [6, 7].
При проведении рандомизированного многоцентрового плацебо контролируемого клинического исследования на базе 7 клинических центров с включением 494 пациентов с хроническим гепатитом С и В различной степени активности отмечено, что у них после курсового приема ремаксола (раствор для инфузий) зафиксировано снижение уровня трансаминаз в 1,8 раза по сравнению с группой контроля, в том числе за счет антихолестатического эффекта препарата [11].
В исследованиях показано, что, обладая выраженным гепатопротекторным действием, ремаксол улучшает энергетическое обеспечение гепатоцитов, повышая устойчивость мембран клеток к перекисному окислению липидов и восстанавливая активность ферментов антиоксидантной защиты. Это позволяет применять его в качестве терапии сопровождения при различных патологических состояниях. Детоксицирующая активность препарата обеспечивается стимуляцией оттока желчных кислот, предотвращая застой желчи и отравление организма желчными кислотами, в результате чего восстанавливается функция печени, нет влияния на реологические свойства крови. Происходит нормализация показателей, характеризующих степень поражения гепатоцитов (АлТ, АсТ, ЩФ, ГГТП) и функциональное состояние печени за счет уменьшения цитолитического и холестатического синдромов [7, 12].
В исследовании Д. С. Суханова получены доказательства эффективности препаратов ремаксола и реамберина в эксперименте [13]. Так, зафиксировано их положительное влияние на показатели липидного обмена: уровень триглицеридов статистически значимо уменьшился, нормализовались показатели АлАТ и АсАТ. При морфологическом исследовании печени установлено, что параллельно с улучшением биохимических показателей уменьшался некробиоз гепатоцитов с сокращением распространенности жировой дистрофии, которая регистрировалась только на периферии долек и в междольковом пространстве. При применении адеметионина (независимо от способа введения и дозы) в 45,5% случаев обнаруживали очаги некроза различной величины, что свидетельствовало о стимуляции альтерации печеночной ткани, это связано с процессом карбоксиметилирования белков, продуктами которого являются метанол, формальдегид и муравьиная кислота, обладающие цитотоксическим действием [14, 13].
В детской практике на фоне полихимиотерапии в 72,2% случаев отмечалось нарушение функции печени, которое отражалось в биохимических показателях крови (повышение уровня общего билирубина, трансаминаз, тимоловой пробы, уровня щелочной и кислой фосфатаз) [9]. Нормализация биохимических показателей на фоне применения гепатопротекторов (Лив 52) отмечалась через 1 мес. в 23% случаев, через 2 мес. - в 67% случаев, к концу 3-го мес. - в 100% случаев, что обусловлено стимулирующим действием на регенерацию гепатоцитов, а также мембраностабилизирующим действием, что особенно ценно при длительной противотуберкулезной терапии. Снижение активности щелочной и кислой фосфатаз свидетельствовало о нормализации функциональной активности печени и функции желчеобразования [15].
Следовательно, применение гепатопротекторов является желательным на фоне лечения туберкулеза, в особенности при появлении нежелательных явлений, связанных с нарушением функции печени. Согласно международным рекомендациям, коррекция нежелательных явлений со стороны печени и желчевыводящих путей должна осуществляться только после появления функциональных нарушений третей и четвертой степени тяжести [17]. Однако отечественные исследователи считают необходимым назначение гепатопротекторов одновременно с применением ПТП не только при появлении нарушений функции печени, но и при тяжелом течении процесса для снятия интоксикационного воздействия на печень [3, 4, 12].
Назначение корригирующей терапии при возникновении нежелательных явлений на фоне лечения туберкулеза (в том числе при сочетании с ВИЧ-инфекцией) в настоящее время является обоснованным [4, 14].
При оценке нежелательных явлений, развивающихся в ходе химиотерапии туберкулеза, следует учитывать, что возможна суммация побочного действия разных ПТП, если они направлены на одни и те же органы-мишени (например, на печень). При серьезных нежелательных явлениях необходима временная отмена и/или замена всей схемы химиотерапии [4, 18].
Согласно проведенным исследованиям, назначение и выбор гепатопротективных препаратов должны проводиться в зависимости от степени повышения биохимических показателей (АЛТ, щелочной фосфатазы и билирубина), а также на основании оценки факторов риска развития нежелательных явлений со стороны печени [4].
Современная фармакотерапия заболеваний печени строится на комплексном использовании нескольких направлений [3, 5-7]:
1) профилактического, призванного обеспечить первичную защиту печени от различных повреждений;
2) этиотропного, направленного на элиминацию патологического возбудителя из организма;
3) патогенетического, нацеленного на коррекцию универсальных мультифакторных звеньев патогенеза заболевания;
4) симптоматического.
Основной целью лечения болезней печени является восстановление морфологической и функциональной полноценности органа.
Заключение
Повышение эффективности лечения туберкулеза легких является одной из важнейших задач в борьбе с туберкулезом. Современные схемы противотуберкулезной терапии включают прием нескольких ПТП, обладающих выраженным токсическим эффектом, вызывающим нарушения функции печени в 70-80% случаев. Применение эффективных гепатопротекторов для профилактики и устранения лекарственного поражения печени при лечении туберкулеза является необходимым и обоснованным.
Препаратом выбора для купирования гепатотоксичности является инфузионный гепатотропный препарат ремаксол, обладающий мультимодальным фармакологическим действием на патогенетические механизмы развития лекарственных и токсических поражений печени.
Конфликт интересов. Авторы заявляют об отсутствии у них конфликта интересов.
Conflict of Interests. The authors state that they have no conflict of interests.
ЛИТЕРАТУРА
Различия рака и туберкуломы. Диагностические особенности рака и туберкуломы.
По мере прогрессирования размеры периферического рака достигают значительной величины (6—8—10 см). Подрастая к корню легкого, он нередко теряет шаровидную форму и принимает характер центрально расположенной опухоли. При этом он сравнительно редко распространяется в соседнюю долю легкого, хотя край тени опухоли может образовать прогибающуюся книзу линию (симптом Ленка).
У 20—30% больных в раковом узле отмечаются мелкие полости распада. У 10—13% образуются более крупные полости, характерные для так называемого кавернозного рака. В этих случаях мелкие или щелевидные полости постепенно объединяются и превращаются в единую обширную полость, иногда достигающую 6—8 см в диаметре. Она имеет неправильные ландкартообразные очертания и содержит обычно небольшое количество жидкости. Наружные контуры распавшегося периферического рака сохраняют характерные для него признаки, а стенка остается довольно толстой (более 5 мм). При этом в окружающей легочной ткапи отсутствуют очаги обсеменения. К важным диагностическим признакам прогрессирования раковой опухоли относятся появление ее метастазов в лимфатических узлах корня легкого и средостения, развитие плеврита, прорастание тканей грудной стенки, диафрагмы и т. д.
Определенное значение приобретают результаты бронхографии, при которой удается установить симптомы, характерные для рака: признак культи (ампутации) бронха в зоне опухоли, деструкцию и перавномерное сужение мелких бронхов. При опухолях больших размеров, кроме того, может наблюдаться оттеснение и смещение соседних бронхов. При ангиопульмонографии определяются характерные изменения в виде обеднения сосудов вокруг опухоли или симптом культи на границе с нею. Скиалогическая картина периферического рака легкого, таким образом, заметно отличается от таковой при туберкуломе.
При бронхоскопии у большинства больных периферическим раком легкого не удается обнаружить патологические изменения из-за недоступности непосредственному осмотру субсегментарных и мелких бронхов. Только в части случаев можно отметить гиперемию и отечность слизистой оболочки сегментарных, долевых и главных бронхов или косвенные признаки бластоматозного процесса. У больных туберкулезом нередко выявляется специфический эндобронхит в виде инфильтрации или язвенного поражения слизистой оболочки сегментарных и более крупных бронхов.
Важную роль в дифференциальной диагностике рака и туберкуломы играют лабораторные методы исследования. Более чем у 1/2 больных периферическим раком легких в мокроте или в промывных водах бронхов при цитологическом исследовании находят опухолевые клетки, а у 3/4 — эритроциты. Обнаруживаемые иногда при этом бациллы являются кислотоустойчивыми сапрофитами, реже микобактериями туберкулеза. В последнем случае их обнаруживают в мокроте однократно, и выделяются они обычно в результате обострения и распада латентного туберкулезного очага в зоне опухоли.
Такой же случайной находкой становятся в свою очередь атипичные клетки цилиндрического эпителия у больных туберкулезом легких, страдающих одновременно хроническим бронхитом, пневмосклерозом.
Обращают на себя внимание некоторые отличия в гемограмме: тенденция к лейкоцитозу и лимфопении при раке и к лимфоцитозу при туберкулезе. При раке в большей мере снижено содержание в сыворотке крови альбуминов и повышен уровень глобулинов, главным образом за счет фракций. При туберкул омах состав белков в этих случаях обычно мало изменен.
После впрыскивания под кожу туберкулина у части больных туберкулезом (у 43% —по данным И. П. Жингеля, 1974) уменьшается содержание альбуминов и увеличивается уровень глобулиновых фракций. При раке таких сдвигов не наблюдается. Этот феномен является отображением более высокой чувствительности организма больных туберкулезом к данному аллергену, чем у страдающих раком. Среди последних у 1/3 мы отмечали отрицательные реакции на 1 ТЕ, а среди больных туберкуломой легких—у 19%.
Однако даже с помощью всех указанных методов исследования не всегда удается дифференцировать периферический рак и туберкулому легких. В таких случаях производят катетеризацию периферических бронхов с аспирационной биопсией и цитологическим исследованием извлеченного аспирата. С помощью этого метода удается верифицировать диагноз в среднем у 60—70% больных раком. Однако при расположении опухоли в кортикальных отделах легкого разрешающая диагностическая способность данного способа исследования уменьшается. Более эффективной в этих случаях может оказаться игловая биопсия леткого, посредством которой удается не только установить наличие опухоли, но и определить ее гистологический характер. При отрицательных результатах всех этих методов исследования или невозможности применить их по каким-либо причинам следует прибегать к торакотомии, если для этого нет противопоказаний.
Необходимо подчеркнуть, что весь объем диагностических приемов должен выполняться по определенному плану и по возможности в ограниченные сроки. В связи с этим нельзя считать оправданным длительное применение туберкулостатических средств как метода дифференциальной диагностики ex juvantibus. При такой тактике могут быть упущены возможности для эффективного хирургического вмешательства при периферическом раке легкого.
Среди опухолевых процессов, которые могут походить на туберкулому, следует иметь в виду узловатую форму бронхиоло-альвеолярного ракач или аденоматоза. В отличие от первичного рака бронхов адсноматоз сравнительно часто встречается у людей более молодого возраста и нередко у женщин. Так, из 29 таких больных, которых наблюдали на протяжении 1947 — 1970 гг. Galy и Marcq (1973), было 12 женщин и 17 мужчин. Их средний возраст составлял 50 лет, а некоторым было 25—30 лет Клинико-рентгенологическая картина болезни, по данным указанных авторов, протекает в виде 3 типов. У части больных в одной из долей легких, преимущественно нижней, появляется крупнофокусное образование, напоминающее туберкулезный инфильтрат или туберкулому.
В этих случаях обычно нет признаков метастазирования в плевру и лимфатические узлы. В других случаях в пределах доли обнаруживают несколько изолированных или сливающихся между собой очагов, причем у части больных при этом выявляется поражение внутригрудных лимфатических узлов и плевры. Третью группу составляют больные с более распространенными очаговыми и сливными фокусными изменениями в одном или обоих легких обычно уже с признаками метастазирования.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Патогенез взаимодействия туберкулеза и рака легкого. Диагностика рака при туберкулезе.
Но как ни важны и интересны патогенетические аспекты взаимоотношения между этими заболеваниями, наибольшее практическое значение в настоящее время приобретают их дифференциальная диагностика, а также своевременное распознавание сочетанных форм процесса. Актуальность этой проблемы значительно возросла с тех пор, как было установлено, что начальной формой часто является периферический рак легкого, который по своим рентгенологическим признакам может походить на туберкулезный процесс.
Вместе с тем встречаются такие формы туберкулеза, которые по клинико-рентгенологической картине весьма напоминают рак легкого. Очевидно, только с помощью комплекса различных диагностических методов можно своевременно распознать сочетание рака и туберкулеза. С этой целью предложены многие способы клинического, инструментального, лабораторного и иммунологического исследования. Пользуясь ими, мы могли установить, что сочетание этих заболеваний в подавляющем большинстве случаев встречается у мужчин обычно старше 50 лет (в 89,5%).
Средний возраст этих больных составляет 58,5 года и приближается к соответствующему показателю для больных только ракам (61,4 года), но в то же время отличается от более молодого возрастного состава больных туберкулезом.
Характерно, что интервал между сроком выявления или затихания активного туберкулеза и моментом установления диагноза рака оказывается довольно длительным. Только у 23,3% больных оба заболевания выявлены одновременно и лишь в исключительных случаях (у 1,3%) туберкулез развивался на фоне рака легких. Таким образом, у подавляющего большинства больных (75,4%) туберкулез предшествует раку. У этих больных период между выявлением туберкулеза и рака легкого составляет в среднем 8,8—10,8 года, а между затиханием туберкулеза и возникновением рака — около 7 лет.
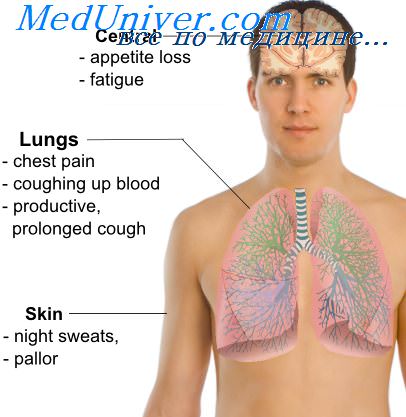
При всей общности отдельных клинических признаков, характерных для рака и туберкулеза органов дыхания, при сочетании этих заболеваний обращают на себя внимание появление или учащение и утяжеление таких симптомов, как общая слабость, длительный и нередко надсадный сухой кашель, упорные кровохарканья, стойкие и нарастающие боли в груди, одышка, потеря в весе, лихорадка неправильного типа. Такое состояние особенно отмечается при центральной форме броихогенного рака, присоединяющегося к туберкулезу.
В подобных случаях, кроме того, отсутствуют признаки обострения туберкулеза в виде появления бацилловыделения, увеличения размеров каверн, образования перифокалыюго воспаления вокруг старых очагов и свежей бронхогенной или гематогенной диссеминации. Характерно, что у большинства больных, несмотря на присоединение рака, туберкулезный процесс не только не обостряется, но под влиянием химиотерапии даже затихает и лишь в части случаев, главным образом в терминальной фазе рака, прогрессирует.
Наряду с правильной интерпретацией симптоматики болезни некоторую роль имеют туберкулиновые тесты (отрицательные кожные реакции и белково-туберкулиновая проба и др.). Значительно большее диагностическое значение приобретают результаты бронхоскопии, цитологического исследования мокроты и смывов со слизистой оболочки бронхов, а также изучение биоптического материала, полученного при пункции легкого или путем аспирации при зондировании бронхов. Но ведущую роль в выявлении этих сочетанпых заболеваний играет, конечно, комплексный рентгенологический метод исследования. Правда, раннее рентгенологическое распознавание броихогенного рака при одновременном наличии туберкулеза встречает определенные затруднения.
Тем не менее в этих случаях можно отметить некоторые признаки, характерные для такого вида поражения легких. Так, если туберкулез не сопровождается обострением, а вне зоны специфических изменений или в противоположном легком возникает одиночная, изолированная, крупноочаговая или фокусная тень со слегка волнистыми контурами и однородной структуры, то в первую очередь следует предположить присоединение периферического рака к туберкулезу легких. Подозрение на развитие опухолевого процесса вызывает появление такой же тени в зоне расположения старых фиброзных очагов, особенно при отсутствии их обострения.
При развитии рака в зоне активных туберкулезных изменений правильный диагноз может быть установлен иногда в результате короткого курса специфической химиотерапии. При сочетании периферического рака и активного туберкулеза последний при этом подвергается инволюции, а изменения, отображающие опухолевый процесс, увеличиваются в объеме и прогрессируют.
Иногда рак может развиваться в стенке туберкулезной каверны или в дренирующем ее бронхе. В этих случаях рентгенологически можно отметить появление выраженного асимметричного утолщения стенки каверны, ранее тонкостенной и равномерно утолщенной, или образование полипообразных разрастаний в ее просвете. Значительные трудности возникают при выявлении рака, образующегося в зоне туберкуломы или в заполненной каверне. Важнейшими рентгенологическими признаками, которые позволяют заподозрить озлокачествление этих туберкулезных образований, являются постепенное увеличение их объема и появление бугристости контуров, но без перифокалыюго воспаления вокруг них, а также формирование в патологическом фокусе обширного центрального ландкартообразного или множественного распада, не сопровождающегося бронхогенной диссеминацией и бацилловыделением.
При присоединении к туберкулезу центрального рака легкого наиболее ранними рентгенологическими признаками являются перемещающиеся гиповентиляция и эмфизема сегмента или доли легкого и нередкое одновременное появление в них дольковых ателектазов и пневмоиита. При применении антибиотиков широкого спектра действия воспалительные изменения в этих случаях подвергаются быстрой инволюции, что не свойственно туберкулезу. Иногда присоединение центрального рака отображается появлением ограниченных, груботяжистых, перибронхиальных, интерстициальных или стелющихся по междолевой плевре уплотнений, исходящих из корня легкого. Наиболее убедительными, хотя и запоздалыми, рентгенологическими признаками центрального рака, развивающегося при туберкулезе, являются ателектаз сегмента или доли, одностороннее увеличение и изменение структуры тени корня легких, который может содержать увеличенные лимфатические узлы. Такие изменения не характерны для туберкулеза легких у взрослых.
Косвенными рентгенологическими признаками присоединившегося к туберкулезу центрального рака и его метастазов во внутригрудные лимфатические узлы являются, кроме того, симптом Гольцкнехта — Якобсона, не вызванное туберкулезом стойкое смещение средостения, подъем купола диафрагмы, его неподвижность или парадоксальное перемещение.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Трудности диагностики сочетания туберкулеза и рака легкого. Лечение туберкулеза при раке легкого.
При рентгенологическом исследовании больных туберкулезом и раком легкого лишь у 7,9% картина патологического процесса не давала основакий заподозрить присоединение рака легкого к имеющемуся туберкулезу. У 15,2% больных ее можно было расценить двояко: либо как обострение туберкулеза, либо как присоединение к нему рака. У остальных 76,9% обнаруживались рентгенологические признаки, характерные для периферического или центрального рака, а нередко и для его осложнений или метастазов во внутригрудные лимфатические узлы, легкие и кости. При ретроспективной оценке данных у динамически прослеженных больных рентгенологическое отображение опухоли или ее осложнений у 92,1 % имело место до поступления в клинику и было документировано рентгенограммами у 53,9% больных за 3 мес, у 16,6% — за 6, у 17,3% — за 12 мес и у 12,2% — за 1—2 года и более до установления диагноза рака легкого.
Анализ этих материалов показал, что имевшаяся у большинства больных клиническая и рентгенологическая симптоматология легочного процесса часто истолковывалась неправильно и оценивалась как проявление только туберкулезного процесса (28%), его рецидива (38,1%) или неопухолевых и нетуберкулезных заболеваний (13,9%). Уверенное предположение о наличии сочетания рака и туберкулеза было высказано лишь у 12,2% больных. В результате этого больные раком легкого при его сочетании с туберкулезом поступали в клинику в 54,4% при наличии уже III и IV стадий опухолевого процесса, что, естественно, резко затрудняло или делало невозможным хирургическое лечение. В то же время ретроспективная оценка клинико-рентгеиологических данных показала, что при более тщательном их изучении можно было во многих случаях избежать запоздалой диагностики.
Анализируя причины позднего выявления рака у наблюдавшихся больных туберкулезом, мы убедились, что они связаны с недостаточно внимательным изучением клинико-рентгено-лабораторных материалов и неполным использованием современных инструментальных и биопсических методов исследования. Применение последних у поступивших в клинику больных позволило установить, что высокорезультативными при выявлении рака являются: бронхоскопия в сочетании с биопсией преимущественно при центральной его форме (70,2%); катетеризация периферических бронхов с аспирационной биопсией главным образом при периферической его форме (80%) и другие биопсические методы (55,1%). Нередко их использование являлось основным средством верификации рака и его гистологической структуры. Лишь у 4,3% больных из-за объективных трудностей диагноз первичного рака, сочетающегося с туберкулезом легких, был установлен только в результате операции (3,6%) или на секций (0,7%).
В остальных случаях клиническая диагностика этих заболеваний оказалась возможной еще до операции или летального исхода.
Приведенные данные свидетельствуют о большом значении обсуждаемой проблемы, в разрешении которой должны сыграть роль дальнейшее усовершенствование и практическое освоение различных способов ранней диагностики рака.
Тем самым открываются пути и для успешного лечения больных, страдающих одновременно раком и туберкулезом органов дыхания. Еще не так давно многим таким больным отказывали в оперативном вмешательстве или даже в паллиативных методах терапии, опасаясь возможного обострения и быстрого прогрессирования туберкулеза. Однако с течением времени ситуация в этом отношении существенно изменилась. При ограниченном распространении опухолевого процесса, особенно при периферическом раке, теперь все чаще производят более экономные операции, которые не вызывают выраженных нарушений дыхания и кровообращения.
Вместе с тем при своевременно и правильно примененной антибактериальной терапии, как мы убедились на нашем опыте, во многих случаях можно не только предупредить обострение или рецидив туберкулеза, но и достигнуть его затихания или даже излечения. Непременным условием при этом должна быть достаточно длительная и контролируемая туберкулостатическая терапия как в до-, так и в послеоперационном периоде.
Тот же принцип следует реализовать в целях профилактики вспышки туберкулеза при применении лучевого или противоопухолевого химиотерапевтического лечения независимо от того, назначается ли оно как самостоятельный метод терапии, или как дополнительный к оперативному вмешательству.
Очевидно, что только при согласованной лечебной тактике фтизиатра, онколога, хирурга и радиолога может быть достигнут должный эффект и тем самым сохранена или продлена на длительный срок жизнь больных, страдающих раком и туберкулезом органов дыхания. Наряду с этим выявление больных с наиболее ранними и ограниченными формами туберкулеза легких и их полноценное лечение будут, несомненно, способствовать выздоровлению с минимальными остаточными морфологическими изменениями, что следует расценивать как одно из условий профилактики рака органов дыхания.
Итак, нами изложены основные вопросы этиологии, патогенеза, клиники, а также принципы терапии и профилактики туберкулеза органов дыхания. Каждый из них — весьма важная и в сущности самостоятельная проблема. И все же наибольшее значение, на наш взгляд, приобретает диагностика и дифференциальная диагностика этой болезни. Ведь навсегда сохранится в силе основной постулат медицинской науки и практики — кто хорошо и, добавим, своевременно распознает болезнь, тот хорошо ее лечит. Однако в современную эпоху, когда изменилась и осложнилась клиническая картина туберкулеза, при решении этой задачи нередко встречаются определенные затруднения. Они усугубляются еще и тем, что из почти 500 известных заболеваний органов дыхания многие весьма походят на туберкулез. Конечно, даже высококвалифицированному и опытному интернисту нелегко разобраться в этой мозаичной и многообразной патологии, которая стала предметом современной пульмонологии.
Но к этому следует стремиться каждому терапевту, педиатру, рентгенологу и прежде всего фтизиатру, который весьма часто встречается с разнообразной легочной патологией. Вот почему формирование нового профиля врача — фтизиопульмонолога — веление времени. Недаром к этому стремятся многие практические работники диспансеров, больниц, клиник и санаториев. Если данная книга окажется им в какой-то мере полезной, автор будет считать свою задачу выполненной.
- Вернуться в оглавление раздела "Пульмонология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Заболеваемость туберкулезом легких среди больных язвенной болезнью желудка и двенадцатиперстной кишки и у лиц, перенесших резекцию желудка по поводу язвенной болезни, в 3-4 раза выше, чем в общей популяции. Наиболее часто сочетание язвенной болезни и туберкулеза легких встречается у мужчин молодого и среднего возраста, т.е. у наиболее трудоспособной части населения.
В настоящее время туберкулез в России приобрел значение глобальной проблемы, создающей угрозу национальной безопасности. Как и ранее, основными причинами роста заболеваемости туберкулезом остаются социальные факторы: снижение уровня жизни, миграция больших групп населения, алкоголизм и различные виды наркомании.
В настоящей статье мы хотим обсудить еще одну из причин, повышающих риск заболевания туберкулезом - тяжелую хроническую патологию внутренних органов и, в частности, язвенную болезнь желудка и двенадцатиперстной кишки. Научно доказано, что лица с сопутствующими заболеваниями внутренних органов: хроническими неспецифическими заболеваниями легких, врожденными и приобретенными иммунодефицитами, сахарным диабетом, патологией желудочно-кишечного тракта - являются одной из основных групп риска заболевания туберкулезом. Отмечено, что у больных туберкулезом легких пожилого возраста преобладает сопутствующая патология сердечно-сосудистой системы и сахарный диабет, а в молодом возрасте более актуальны патология желудочно-кишечного тракта и хронический алкоголизм.
Болезни желудочно-кишечного тракта занимают второе место среди всех сопутствующих заболеваний при туберкулезе легких и, по данным исследований, составляют до 30% случаев. Чаще всего туберкулезу легких сопутствуют вирусные гепатиты и патология верхних отделов желудочно-кишечного тракта.
Изучение состояния желудка у больных туберкулезом легких имеет длительную историю. Еще в конце XIX в. появилось понятие "претуберкулезной диспепсии". Это было связано с тем, что у части больных с неясным диагнозом, предъявлявших жалобы на стойкое отсутствие аппетита, похудание, неприятные ощущения в эпигастральной области, годами посещавших врачей, впоследствии выявлялся туберкулез легких. Уже в то время было сделано предположение, что диспептические явления у больных туберкулезом связаны с функциональными нарушениями желудка. Однако основные достижения в изучении данной проблемы относятся к более позднему периоду, когда появившиеся новые технические средства позволили проводить прижизненную диагностику язвенной болезни и хронического гастрита у больных туберкулезом.
Почему больные язвенной болезнью чаще страдают туберкулезом легких? Предполагается, что длительное использование малокалорийной противоязвенной диеты, дисбаланс в работе нервной системы организма, частые обострения с расстройствами пищеварения снижают сопротивляемость организма к инфекционным заболеваниям, в том числе к туберкулезу. У больных, перенесших резекцию желудка по поводу язвенной болезни, нарушается всасывание жиров, белков, углеводов, минеральных солей, витаминов, что еще в большей мере повышает риск развития туберкулеза легких. Туберкулез легких обычно развивается в первые 5 лет после заболевания язвенной болезнью или резекции желудка.
Туберкулез легких при сопутствующей язвенной болезни характеризуется неблагоприятным течением, чаще выявляются формы с большим объемом поражения и распадом легочной ткани. Нередко обострение язвенной болезни ведет к прогрессированию туберкулезного процесса. Характерны высокая частота рецидивов и низкая эффективность лечения, реже удается добиться прекращения бактериовыделения и закрытия полостей распада. Сочетание язвенной болезни и туберкулеза легких характеризуется длительной потерей трудоспособности, частой инвалидизацией. Еще хуже результаты лечения больных туберкулезом, перенесших резекцию желудка по поводу язвенной болезни. У повторно поступающих в стационар больных с сочетанной патологией в половине случаев отмечается лекарственная устойчивость выделяемых микобактерий туберкулеза.
Предотвратить обострение язвенной болезни и хронического гастрита на фоне приема противотуберкулезных препаратов можно только учитывая современные представления о причинах и механизмах развития этих заболеваний.
Повреждения слизистой оболочки желудка и двенадцатиперстной кишки развиваются вследствие нарушения равновесия между факторами агрессии и факторами защиты. К основным факторам агрессии относятся повышение выработки соляной кислоты и пепсина, сбои в регуляции желудочной секреции, нарушение механизмов обновления клеток слизистой оболочки, повышение выработки стимуляторов желудочной секреции, повреждающее действие некоторых лекарственных препаратов. При туберкулезе легких, кроме выше перечисленных факторов, актуальны воздействие специфической интоксикации и длительный прием противотуберкулезных препаратов.
Открытый в 1983 году жгутиковый микроорганизм, паразитирующий в толще слизистой оболочки желудка, названный позже Helicobacter pylori, пополнил список известных факторов риска развития гастродуоденальной патологии. Более того, некоторые исследователи считают Helicobacter pylori главной причиной развития хронического гастрита и главным фактором патогенеза язвенной болезни двенадцатиперстной кишки.
В клинике фтизиатрии Военно-Медицинской академии было проведено исследование, посвященное изучению морфологического и функционального состояния желудка у больных туберкулезом легких молодого возраста.
Исследование показало, что 90% больных, поступающих в противотуберкулезные стационары, имеют различной степени выраженности воспалительно-дистрофические изменения слизистой оболочки желудка, частота и интенсивность обсеменения Helicobacter pylori у больных туберкулезом достоверно выше, чем у здоровых лиц такого же возраста. На фоне длительного приема противотуберкулезных препаратов отмечено нарастание интенсивности обсеменения слизистой оболочки желудка Helicobacter pylori и связанной с этим выраженности гастритических изменений.
Для профилактики и раннего выявления сопутствующей патологии желудка и двенадцатиперстной кишки у больных туберкулезом легких при поступлении в стационар необходимо проводить опрос, целью которого является обнаружение факторов риска развития гастрита и язвенной болезни. При появлении жалоб на пищеварительные расстройства больного необходимо углубленно обследовать.
Для лечения обострений язвенной болезни и хронического гастрита у больных туберкулезом мы используем преимущественно препараты, создающие защитный барьер, препятствующий повреждению слизистой оболочки желудка, при этом не снижающие в значительной степени кислотность желудочного сока. К таким препаратам относятся вентер, де-нол, викалин. Наиболее быстро и эффективно больным туберкулезом с сопутствующим гастритом и язвенной болезнью помогает де-нол, обладающий выраженной активностью в отношении Helicobacter pylori.
В заключение мы хотим обратить внимание на тот факт, что нередко больные язвенной болезнью при малосимптомном начале туберкулеза принимают общие симптомы интоксикации (слабость, похудание, потерю аппетита) за проявления основного заболевания и длительное время не обращаются к врачу, что приводит к развитию распространенных деструктивных форм туберкулеза легких. Врачи-гастроэнтерологи, наблюдающие больных язвенной болезнью, должны рекомендовать им регулярно проходить флюорографическое обследование легких, а при появлении симптомов туберкулезной интоксикации и поражения органов дыхания направлять на микроскопическое исследование мокроты и консультацию фтизиатра.
Для врачей-фтизиатров основные проблемы лечения больных с сочетанием язвенной болезни и туберкулеза легких связаны с часто возникающими обострениями язвы на фоне терапии, что существенно ухудшает переносимость лекарственных препаратов, а в ряде случаев является причиной их отмены. В условиях все большего распространения лекарственной устойчивости микобактерий туберкулеза отмена резервных препаратов вследствие их непереносимости может сыграть трагическую роль в судьбе больного! Вот почему так важно прогнозировать и своевременно выявлять обострение гастродуоденальной патологии на фоне туберкулостатической терапии.
Читайте также:

