Туберкулезный склероз что это такое
Обновлено: 13.05.2024
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению? Какова роль фторхинолонов в лечении туберкулеза легких?
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению?
Какова роль фторхинолонов в лечении туберкулеза легких?
Таблица. Стандартные концентрации ПТП, используемые для выявления лекарственной устойчивости МБТ
Первый этап характеризуется проведением интенсивной насыщенной химиотерапии четырьмя-пятью ПТП в течение 2-3 месяцев, что ведет к подавлению размножающейся микобактериальной популяции, уменьшению ее количества и предотвращению развития лекарственной резистентности. На первом этапе используется комбинация препаратов, состоящая из изониазида, рифампицина, пиразинамида, стрептомицина и/или этамбутола.
Второй этап — менее интенсивной химиотерапии — проводится, как правило, двумя-тремя ПТП. Цель второго этапа — воздействие на оставшуюся бактериальную популяцию, в большинстве своем находящуюся внутриклеточно в виде персистирующих форм микобактерий. Здесь главной задачей является предупреждение размножения оставшихся микобактерий, а также стимуляция репаративных процессов в легких с помощью различных патогенетических средств и методов лечения.
Такой методический подход к лечению ЛЧТЛ позволяет к концу первого этапа комбинированной химиотерапии под непосредственным медицинским наблюдением абациллировать 100%, а к завершению всего курса лечения — закрыть каверны в легких у более чем 80% больных с впервые выявленным и рецидивным туберкулезом легких [5].
Намного сложнее вопрос о проведении этиотропного лечения второго варианта, к которому мы относим ЛУТЛ, вызванный лекарственно резистентными (ЛР) МБТ к одному и более ПТП и/или их сочетанию. Особенно тяжело протекает ЛУТЛ у больных с множественной ЛР МБТ к изониазиду и рифампицину, то есть к основным и самым эффективным ПТП. Поэтому поиск новых концептуальных путей повышения эффективности лечения ЛУТЛ и разработка современной методологии специфического воздействия на ЛР МБТ является одним из важнейших и приоритетных направлений современной фтизиатрии.
Развитие ЛР у МБТ к ПТП — одна из главных причин недостаточно эффективной этиотропной химиотерапии. Больные туберкулезом, выделяющие ЛР-штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих ЛР-возбудителем. Чем больше число больных, выделяющих ЛР МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной резистентностью не только к основным, но и к резервным ПТП.
Феномен ЛР МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является ЛР. В активно размножающейся бактериальной популяции всегда имеется небольшое количество ЛР-мутантов, которые практического значения не имеют, но по мере уменьшения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством ЛР и устойчивых МБТ [5]. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. Следовательно, в клинической практике необходимо исследовать ЛР МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких [5].
По определению экспертов ВОЗ [3], ЛУТЛ — это случай туберкулеза легких с выделением МБТ, резистентных к одному и более ПТП. По данным Центрального НИИ туберкулеза РАМН, у каждого второго впервые выявленного и ранее не леченного противотуберкулезными препаратами больного в мокроте выявлялись ЛР к ПТП МБТ, при этом у 27,7% из них наблюдалась устойчивость к двум основным противотуберкулезным препаратам — изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота вторичной ЛР МБТ возрастает до 95,5%.
По нашему мнению, и это составляет основу нашей концепции, для повышения эффективности лечения туберкулеза, вызванного ЛР МБТ, необходимо в первую очередь использовать ускоренные методы выявления ЛР МБТ, что позволяет своевременно изменять режим химиотерапии.
Исследование лекарственной устойчивости МБТ в настоящее время возможно по прямому и непрямому методам.
Непрямой метод определения лекарственной чувствительности МБТ требует от 30 до 60, а иногда до 90 суток, ввиду того что вначале производится посев мокроты на твердые питательные среды и только после получения культуры МБТ производят ее пересев уже на среды с добавлением ПТП. При этом коррекция химиотерапии носит отсроченный характер, как правило, уже на конечном этапе интенсивной фазы химиотерапии.
В последнее время для ускоренного определения лекарственной устойчивости нами применялся радиометрический метод с использованием автоматической системы ВАСТЕС-460 ТВ (Becton Dickinson Diagnostic Systems, Sparks, MD), которая позволяет выявлять лекарственную резистентность МБТ на жидкой среде Middlebrook 7H10 через 6-8 дней.
Не менее важно правильное лечение впервые выявленных больных туберкулезом легких и применение современных режимов химиотерапии с использованием в начале лечения комбинации из четырех-пяти основных противотуберкулезных препаратов до получения результатов лекарственной устойчивости МБТ [2]. В этих случаях существенно повышается вероятность того, что даже при наличии первичной ЛР МБТ бактериостатическое действие окажут два или три химиопрепарата, к которым чувствительность сохранена. Именно несоблюдение фтизиатрами научно обоснованных комбинированных режимов химиотерапии при лечении впервые выявленных и рецидивных больных и назначение ими только трех ПТП является грубой врачебной ошибкой, что в конечном счете ведет к формированию наиболее трудно поддающейся лечению вторичной ЛР МБТ.
Наличие у больного туберкулезом легких ЛР МБТ существенно снижает эффективность лечения, приводит к появлению хронических и неизлечимых форм, а в ряде случаев и летальных исходов. Особенно тяжело протекают специфические поражения легких у больных с полирезистентными МБТ, которые обладают множественной ЛР, как минимум к изониазиду и рифампицину, т. е. к основным и самым активным противотуберкулезным препаратам. ЛР МБТ имеет не только чисто клиническое и эпидемиологическое, но и экономическое значение, так как лечение таких больных резервными ПТП обходится намного дороже, чем больных с чувствительными МБТ к основным химиопрепаратам.
В этих условиях расширение списка резервных ПТП, воздействующих на ЛР МБТ, является актуальным и крайне важным для повышения эффективности лечения больных с ЛУТЛ. Кроме того, присоединение к ЛУТЛ неспецифической бронхолегочной инфекции существенным образом утяжеляет течение специфического процесса в легких, требуя назначения дополнительных антибиотиков широкого спектра. В этом плане применение антибиотиков, воздействующих как на МБТ, так и на неспецифическую патогенную бронхолегочную микрофлору, является научнообоснованным и целесообразным.
В этом плане хорошо себя зарекомендовал в России такой препарат из группы фторхинолонов, как офлоксацин (таривид) [3]. Мы же свой выбор остановили на ломефлоксацине, как препарате, который еще не столь широко применяется при лечении туберкулеза и у которого, судя по имеющимся данным, практически не выявляются побочные эффекты и крайне редко формируется ЛР возбудителей инфекционных заболеваний [2].
Ломефлоксацин (максаквин) — антибактериальный препарат из группы фторхинолонов. Как и все представители производных оксихинолонкарбоновой кислоты, максаквин обладает высокой активностью против грамположительных (включая метициллин-устойчивые штаммы Staphylococcus aureus и Staphylococcus epidermidis) и грамотрицательных (включая Pseudomonas) микроорганизмов, в том числе по отношению к различным типам Micobacterium tuberculosis).
Механизм действия максаквина заключается в ингибировании хромосомной и плазмидной ДНК-гиразы, фермента, ответственного за стабильность пространственной структуры микробной ДНК. Вызывая деспирилизацию ДНК микробной клетки, максаквин ведет к гибели последней.
Максаквин обладает иным механизмом действия, нежели другие антибактериальные средства, поэтому к нему не существует перекрестной устойчивости с другими антибиотиками и химиотерапевтическими препаратами [2].
Основной целью настоящего исследования явилось изучение клинической и микробиологической эффективности максаквина при комплексном лечении больных деструктивным ЛУТЛ, выделяющих ЛР МБТ к изониазиду, рифампицину и другим ПТП, а также при сочетании туберкулеза с неспецифической бронхолегочной инфекцией.
Под наблюдением находилось 50 больных деструктивным ЛУТЛ, выделяющих с мокротой ЛР МБТ к изониазиду, рифампицину и ряду других ПТП. Эти люди в возрасте от 20 до 60 лет составили основную группу.
В контрольную группу вошли также 50 больных деструктивным ЛУТЛ легких в той же возрастной группе, выделяющие ЛР МБТ к изониазиду, рифампицину и другим ПТП. Эти пациенты лечились только протионамидом, амикацином, пиразинамидом и этамбутолом.
У 47 больных основной группы и 49 контрольной в мокроте микробиологическими методами были выявлены различные возбудители неспецифической бронхолегочной инфекции.
Среди больных основной группы диссеминированный туберкулез был установлен у 5 человек, инфильтративный — у 12, казеозная пневмония — у 7, кавернозный — у 7 и фиброзно-кавернозный туберкулез — у 17 человек. Большинство больных (45 пациентов) имели распространенный туберкулез легких с поражением более двух долей, у 34 больных был двусторонний процесс. У всех больных основной группы в мокроте были обнаружены МБТ, как методом микроскопии по Цилю — Нильсену, так и методом посева на питательные среды. При этом у них МБТ были устойчивы как минимум к изониазиду и рифампицину. Необходимо отметить, что все пациенты уже ранее неоднократно и неэффективно лечились основными ПТП, и специфический процесс у них приобрел рецидивирующий и хронический характер.
В клинической картине преобладали симптомы интоксикации с высокой температурой тела, потливостью, адинамией, изменениями в крови воспалительного характера, лимфопенией, увеличенной СОЭ до 40-50 мм в час. Следует отметить наличие грудных проявлений болезни — кашель с выделением мокроты, подчас значительного количества, слизисто-гнойной, а у половины больных — гнойной, с неприятным запахом. В легких выслушивались обильные катаральные явления по типу мелко-, средне-, а подчас и крупнопузырчатых влажных хрипов.
У большинства больных преобладали клинические проявления, которые скорее укладывались в картину неспецифического бронхолегочного поражения (бронхита, острой пневмонии, абсцедирования) с частыми и практически не стихающими обострениями.
Основным возбудителем неспецифической инфекции был Streptococcus hemoliticus — у 15,3% и Staphilococcus aureus — у 15% больных. Среди грамотрицательной микрофлоры преобладал Enterobacter cloacae в 7,6% случаев. Следует отметить высокую частоту ассоциации возбудителей неспецифической бронхолегочной инфекции.
МБТ были обнаружены у всех 50 больных. У 42 человек определялось обильное бактериовыделение. У всех пациентов выделенные штаммы МБТ были устойчивы к изониазиду и рифампицину. При этом у 31 больного лекарственная устойчивость МБТ к изониазиду и рифампицину сочеталась с другими ПТП.
Определение минимальной ингибирующей концентрации (МИК) максаквина проводили на лабораторных штаммах H37Rv и Academia, а также клинических штаммах (изолятах), выделенных от 30 больных, из которых 12 изолятов были чувствительны ко всем основным химиопрепаратам и 8 обладали резистентностью к изониазиду, рифампицину и стрептомицину. В опытах in vitro подавление роста лабораторных штаммов МБТ наблюдалось в зоне 57,6±0,04 до 61,8±0,02 мкн/мл, что почти в семь раз больше, чем показатели, характерные для остальных ПТП .
Таким образом, в ходе микробиологических исследований было установлено выраженное бактериологическое действие максаквина на МБТ, при этом более выраженный эффект наблюдался при его воздействии на лекарственно чувствительные штаммы и изоляты. Однако при повышенных концентрациях максаквина эффект также заметен при воздействии на полирезистентные МБТ, устойчивые к основным ППТ.
Лечение максаквином проводилось у всех 50 больных основной группы в разработанной нами комбинации с другими резервными препаратами: протионамидом, амикацином, пиразинамидом и этамбутолом.
Максаквин назначали в дозе 800 мг в сутки перорально однократно в утренние часы сразу вместе с другими противотуберкулезными препаратами для создания максимальной суммарной бактериостатической концентрации в крови и очагах поражения. Доза максаквина выбрана с учетом микробиологических исследований и соответствовала МИК, при которой отмечалось существенное подавление роста МБТ. Терапевтический эффект определяли через месяц — для оценки воздействия его на неспецифическую патогенную бронхолегочную микрофлору и через два месяца — для оценки воздействия на полирезистентные МБТ. Длительность курса лечения резервными химиопрепаратами в сочетании с максаквином составляла два месяца.
Через месяц комплексного лечения было отмечено значительное улучшение состояния больных основной группы, что проявлялось в уменьшении количества мокроты, кашля и катаральных явлений в легких, снижении температуры тела, при этом более чем у двух третей больных — до нормальных цифр.
У всех больных к этому сроку в мокроте перестал определяться рост вторичной патогенной бронхолегочной микрофлоры. К тому же у 34 больных значительно уменьшилась массивность выделения микобактерий туберкулеза. Практически у всех больных нормализовались анализы крови.
Следует отметить, что у 28 пациентов рентгенологически через месяц лечения максаквином в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом отмечалось частичное рассасывание специфических инфильтративных изменений в легких, а также существенное уменьшение перикавитарной воспалительной реакции. Это позволило применить на данном этапе искусственный пневмоторакс, который является обязательным методом в лечении ЛУТЛ и составляет вторую и не менее важную часть нашей концепции повышения эффективности лечения больных деструктивным туберкулезом легких, выделяющих полилекарственнорезистентные МБТ.
При анализе эффективности специфического действия комбинации резервных противотуберкулезных препаратов в сочетании с максаквином на полирезистентные МБТ при лечении 50 больных основной группы мы делали основной акцент на показатель прекращения бактериовыделения, как по микроскопии мокроты по Цилю — Нильсену, так и по посеву на питательные среды через два месяца после химиотерапии.
Анализ частоты прекращения бактериовыделения у больных основной и контрольной группы через два месяца лечения показал, что у пациентов, получавших максаквин в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом, прекращение бактериовыделения было достигнуто в 56% случаях. В контрольной группе больных, не получавших максаквина, — только в 30% случаев.
Следует отметить, что у остальных больных основной группы за этот период времени существенно уменьшилась массивность выделения МБТ.
Инволюция локальных изменений в легких у 50 больных контрольной группы также шла более замедленными темпами, и только у 25 больных к концу второго месяца удалось достичь частичного рассасывания перикавитарной инфильтрации и применить к ним искусственный пневмоторакс. К 39 из 50 пациентов основной группы был применен искусственный пневмоторакс в течение 1,5-2 месяцев, и 17 из них удалось достигнуть закрытия каверн в легких. 11 оставшихся больных, имеющих противопоказания к проведению искусственного пневмоторакса, в этот период были подготовлены к плановому оперативному вмешательству.
При определении лекарственной устойчивости МБТ к максаквину через два месяца лечения у больных основной группы только в 4% случаев была получена вторичная лекарственная устойчивость, сформировавшаяся в процессе двухмесячной химиотерапии, что в конечном итоге потребовало его отмены и замены на другой химиопрепарат, к которому МБТ сохранили свою чувствительность.
К концу второго месяца у 4% больных отмечались явления непереносимости максаквина — в виде диспепсических явлений и диареи, связанной с дисбактериозом, аллергических кожных проявлений и эозинофилии до 32%, что привело к полной отмене препарата. Во всех остальных случаях при двухмесячном ежедневном применении максаквина в суточной дозе 800 мг побочных явлений не отмечалось.
Проведенная после окончания курса лечения максаквином комбинированная химиотерапия резервными препаратами и динамическое наблюдение за этими же больными показали, что достигнутый ко второму месяцу положительный результат в абациллировании мокроты оказал положительное влияние и на конечный результат излечения больных с ЛУТЛ.
Таким образом, применение максаквина в дозе 800 мг в сутки в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом у больных деструктивным ЛУТЛ с сопутствующей неспецифической бронхолегочной инфекцией показало его достаточную эффективность как антибиотика широкого спектра, воздействующего на грамотрицательную и грамположительную микрофлору, и препарата, действующего на туберкулезное воспаление.
Максаквин с полной уверенностью может быть отнесен к группе резервных ПТП. Он эффективно действует не только на МБТ, чувствительные ко всем ПТП, но и на ЛУ МБТ к изониазиду и рифампицину, что и обусловливает целесообразность его назначения таким больным. Тем не менее максаквин не следует рассматривать как основной препарат в схемах лечения больных с впервые выявленным туберкулезом легких, он должен оставаться в резерве и применяться только при ЛУТЛ и сопутствующей неспецифической бронхолегочной инфекции.
Для изониазида это составляет 1 мкг/мл, для рифампицина — 40 мкг/мл, стрептомицина — 10 мкг/мл, этамбутола — 2 мкг/мл, канамицина — 30 мкг/мл, амикацина — 8 мкг/мл, протионамида (этионамида) — 30 мкг/мл, офлоксацина (таривида) — 5 мкг/мл, циклосерина — 30 мкг/мл и для пиразинамида — 100 мкг/мл.
Литература
1. Лечение туберкулеза. Рекомендации для национальных программ. ВОЗ. 1998. 77 с.
2. Мишин. В. Ю., Степанян И. Э. Фторхинолоны в лечении туберкулеза органов дыхания // Русский медицинский журнал. 1999. № 5. С. 234-236.
3. Рекомендации по лечению резистентных форм туберкулеза. ВОЗ. 1998. 47 с.
4. Хоменко А. Г., Мишин В. Ю., Чуканов В. И. и др. Эффективность применения офлоксацина в комплексном лечении больных туберкулезом легких, осложненным неспецифической бронхолегочной инфекцией // Новые лекарственные препараты. 1995. Вып. 11. С. 13-20.
5. Хоменко А. Г. Современная химиотерапия туберкулеза // Клиническая фармакология и терапия. 1998. № 4. С. 16-20.
Туберозный склероз — генное заболевание, характеризующееся поражением нервной системы в виде эпилепсии и олигофрении, полиморфными кожными симптомами, опухолевыми и неопухолевыми процессами в соматических органах. Диагностический алгоритм состоит из обследования нервной системы (МРТ, КТ головного мозга, ЭЭГ), офтальмологического исследования, обследования внутренних органов (УЗИ, МРТ сердца, КТ почек, рентгенография легких, ректороманоскопия). Главными направлениями лечения являются: противоэпилептическая терапия, нейропсихологическая коррекция, наблюдение и своевременное хирургическое лечение новообразований.
МКБ-10
Общие сведения
Туберозный склероз (ТС) — наследственная нейроэктодермальная патология, проявляющаяся изменениями кожи, эпилептическими приступами, олигофренией (умственной отсталостью) и возникновением новообразований различной локализации. Наряду с нейрофиброматозом, болезнью Гиппеля-Линдау, синдромом Луи-Бар, болезнью Стерджа-Вебера и др., ТС относится к факоматозам. Заболеваемость составляет 1 случай на 30 тыс. населения, среди новорожденных — 1 случай на 6-10 тыс. Известны не только семейные, но и спорадические случаи. Причем последние составляют до 70%.

Причины туберозного склероза
Заболевание имеет генетическую природу. Большинство случаев обусловлено возникновением новых мутаций и лишь 30% аутосомно-доминантным наследованием генных аберраций, имеющихся у родителей. Выделяют туберозный склероз тип 1, развитие которого обусловлено мутациями в гене 34 локуса 9-й хромосомы, ответственном за кодирование гамартина, и туберозный склероз тип 2, связанный с нарушениями в 13-ом участке 16-й хромосомы, отвечающем за кодирование туберина.
Биохимические аспекты патогенеза до конца не изучены. Известно только, что в норме гамартин и туберин являются факторами подавления опухолевого роста. Морфологическим субстратом выступают разросшиеся глиальные элементы церебральной ткани, гистологически представленные гигантскими клетками с атипично увеличенными ядрами и большим числом отростков. Глиальные разрастания формируют субэпендимальные узлы, корковые туберы и специфические островки в белом веществе. Все эти образования имеют тенденцию к обызвествлению. Субэпендимальные узлы зачастую дают начало образованию гигантоклеточной астроцитомы. В 10% случаев отмечается поражение тканей мозжечка. Глиальные разрастания наблюдаются также на диске зрительного нерва и в периферических отделах сетчатки.
Симптомы туберозного склероза
Клиника, которую имеет туберозный склероз, очень вариабельна. Она включает поражение центральной нервной системы (ЦНС), дерматологические и офтальмологические проявления, новообразования внутренних органов. Дебют приходится на различные возрастные периоды, но чаще туберозный склероз манифестирует в течение первых 5-ти лет жизни. Возможны различные по тяжести варианты течения. В легких случаях пациенты имеют ряд факультативных неспецифических симптомов и зачастую не проходят диагностику на наличие ТС. Туберозный склероз в стертой форме протекает без эпиприступов, олигофрении и расстройств поведения.
Поражение ЦНС
Изменения в ЦНС выступают доминирующими проявлениями ТС. Среди них наиболее часто (в 80-90% случаев) встречается судорожный синдром, с которого обычно манифестирует заболевание. Для эписиндрома, дебютирующего на первом году жизни, характерны инфантильные спазмы (синдром Веста), затем трансформирующиеся в синдром Леннокса-Гасто. Возможны атипичные абсансы, сомато- и сенсомоторные пароксизмы, вторично-генерализованные приступы. Возникновение в возрасте до года, высокая частота и гетерогенность приступов сопровождаются их резистентностью к антиконвульсантной (противоэпилептической) терапии. Эпилептические пароксизмы являются причиной задержки психического развития и нарушений поведения (агрессивности, аутизма, СДВГ) у детей.
В половине случаев туберозный склероз сопровождается выраженной в различной степени олигофренией. Наряду с эпилепсией, причиной ее развития считается наличие корковых туберов. Уже в младшем возрасте у детей отмечается анормальное поведение: общее беспокойство, капризность и недовольство наряду с медлительностью, затруднениями переключаемости внимания. Степень этих нарушений тем выше, чем раньше возник туберозный склероз. У большинства пациентов также наблюдаются нарушения сна. Они характеризуются ночными пробуждениями, инсомнией, сомнамбулизмом, ранним утренним переходом от сна к бодрствованию.
Дерматологические симптомы
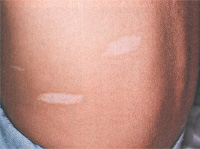
Изменения со стороны кожи сопровождают туберозный склероз практически в 100% случаев. Они характеризуются большим полиморфизмом элементов и их сочетаний. Чаще всего (в 90% случаев) наблюдаются пятна гипопигментации, которые возникают обычно в первые 3 года жизни и в дальнейшем увеличивают свое количество. Они асимметрично разбросаны по ягодицам, туловищу и на передне-латеральных поверхностях конечностей. Возможна депигментация ресниц, бровей и волос. В 14% случаев выявляются участки гиперпигментации в виде пятен, более характерных для нейрофиброматоза. Как правило, их насчитывается не более 5 штук.
В 25% случаев туберозный склероз сопровождается образованием фиброзных бляшек, в 30% случаев — мягких дерматофибром. До 50% больных после пубертата имеют склонные к прогредиентному росту околоногтевые фибромы. Последние более часто располагаются на ступнях. Имеют вид тусклых красных узелков или папул, окружающих ногтевую пластинку.
Офтальмологические симптомы
Отмечаются редко, хотя почти у половины больных ТС выявляется наличие гамартом зрительного нерва и/или гамартом сетчатки. Гамартомы могут иметь плоскую гладкую, незначительно возвышающуюся поверхность или представляют собой узловатое образование, иногда встречаются гамартомы смешанного типа — узловатые в центре. Основным проявлением гамартом является прогрессирующее падение зрения, но зачастую наблюдается их субклиническое течение. Возможны и другие офтальмологические расстройства: депигментация радужки, отек диска зрительного нерва, колобома, косоглазие, ангиофибромы век, катаракта.
Поражение внутренних органов
Новообразования соматических органов, сопровождающие туберозный склероз, отличаются множественностью и частым двусторонним поражением парных органов, длительно протекают субклинически. Период их манифестации колеблется от 5 до 40 лет. К наиболее патогномоничным для ТС новообразованиям относятся: рабдомиома сердца, кисты легких, поликистоз почек, гамартомы печени, ректальные полипы. В 4,5% случаев при ТС наблюдаются злокачественные опухоли, чаще почечно-клеточный рак.
Со стороны сердечно-сосудистой системы выявляются опухоли сердца. В 30-60% случаев это рабдомиомы. При их внутриутробном развитии может наблюдаться антенатальная гибель плода. У половины новорожденных с ТС рабдомиомы выявляются случайно при выполнении ЭхоКГ. У маленьких детей они проявляются аритмией, синдромом WPW, тахикардией, фибрилляцией желудочков. Интрамуральное положение рабдомиомы влечет за собой расстройство сократимости; обтурация опухолевой массой сердечных камер приводит к сердечной недостаточности. У старших детей рабдомиомы преимущественно бессимптомны; возможна блокада ножки пучка Гиса, псевдоишемические отклонения на ЭКГ. Зачастую наблюдается регресс и даже полное исчезновение рабдомиомы к 6-летнему возрасту.
Диагностика
Диагностировать туберозный склероз возможно лишь совместными усилиями нескольких специалистов (невролога, офтальмолога, дерматолога, кардиолога, нефролога) с проведением широкого аппаратного обследования пациента. Церебральная эпилептическая активность регистрируется при помощи ЭЭГ и ЭЭГ с пробами. У детей до года возможно проведение нейросонографии. Наибольшую значимость в диагностике поражений ЦНС имеют КТ и МРТ. КТ головного мозга более информативно в отношении кальцифицированных туберов и субэпендимальных узлов, а МРТ головного мозга — в выявлении некальцифицированных туберов. С целью своевременной диагностики астроцитомы детям, имеющим туберозный склероз, рекомендовано прохождение МРТ или КТ-исследования не реже чем раз в 2 года.
Проводится комплексное обследование соматических органов: ЭКГ, УЗИ и МРТ сердца, УЗИ брюшной полости, УЗИ и КТ почек, урография, обзорная рентгенография грудной клетки, ректороманоскопия, колоноскопия. Диагностика офтальмологических поражений осуществляется путем прямой и непрямой офтальмоскопии, сканирующей томографии сетчатки.
В связи с большой полиморфностью сопровождающих туберозный склероз проявлений, для установления диагноза используют диагностические критерии, разработанные в 1998 г. в Швеции. Они включают первичные, вторичные и третичные признаки. Туберозный склероз достоверен, когда имеет место 1 первичный признак в сочетании с 2 вторичными или третичными. Туберозный склероз вероятен при наличии 1 вторичного и 1 третичного или 3 третичных признаков. Окончательную точку в вопросе диагностики туберозного склероза помогает поставить генетический анализ.
Лечение туберозного склероза
Основополагающим направлением в лечении ТС является антиконвульсантная терапия, поскольку степень олигофрении и ЗПР напрямую коррелирует с частотой эпиприступов, а эпилептический статус может стать причиной смертельного исхода. Выбор препарата зависит от вида пароксизмов, при недостаточной эффективности монотерапии, назначается комбинированное лечение. При синдроме Веста применяют вигабатрин и тетракозактид. Препаратами второй очереди выступают вальпроаты. Если туберозный склероз протекает с парциальными эпиприступами, то базовой терапией считается сочетание вальпроатов с карбамазепином. При отсутствии эффекта в эту схему лечения включают ламотриджин. При генерализованных эпиприступах и парциальных пароксизмах в качестве монопрепарата и в комбинации с другими противоэпилептическими средствами могут применяться современные антиконвульсанты топирамат и леветирацетам.
Терапия олигофрении проводится преимущественно путем нейропсихологической коррекции и комплексного психологического сопровождения ребенка. Назначение ноотропов и прочих стимулирующих нейропрепаратов противопоказано из-за наличия эписиндрома. При выявлении астроцитомы проводится динамическое наблюдение. Хирургическое удаление внутримозговой опухоли показано только при резком увеличении ее размеров с подъемом внутричерепного давления. Операцию проводят нейрохирурги.
В отношении новообразований соматических органов применяется преимущественно выжидательная тактика. Хирургическое лечение проводится по показаниям, в основном в случаях, когда опухоль вызывает существенную дисфункцию органа или имеется угроза ее злокачественного течения.
Туберозный склероз — редкое (1 случай на 30 000 человек) генетическое заболевание, вызывающее образование опухолей в органах по всему телу. Поражаются чаще всего внутренние органы (почки, сердце, легкие), но на начальной стадии заболевание может проявлять себя внешне: на коже лица появляются множественные новообразования.
Лечение и прогноз туберозного склероза — задача не из легких: здесь нужен целый ряд грамотных специалистов и проведение множества обследований. При этом прогноз будет зависеть от здоровья пациента в целом, как быстро ему поставили правильный диагноз и как скоро начали лечение. В лучшем случае пациенты с ТС могут прожить довольно долгую жизнь.

Причины туберозного склероза
Болезнь Бурневилля имеет генетическую природу и обусловлена мутациями в генах TSC1 и TSC2, в связи с чем у больных наблюдается неконтролируемый рост опухолевых тканей.
Выделяют 2 типа туберозного склероза в зависимости от локализации:
- Мутация гена 34 локуса девятой хромосомы. В этом случае происходит нарушение кодирования гематина — антионкогена, обеспечивающего профилактику опухолевой трансформации клеток;
- Мутация в 13 участке шестнадцатой хромосомы приводит к сбоям в работе туберина — белка, блокирующего неконтролируемый рост клеток.
Мнение эксперта

Автор: Андрей Игоревич Волков
Врач-невролог, кандидат медицинских наук
Туберозный склероз — очень редкое заболевание, генетическое, характеризуется развитием доброкачественных опухолей в различных органах. ТС диагностируется в период полового созревания. Примерная частота — 1 на 6000. Если один из родителей имеет такое заболевание, то шанс того, что оно обнаружится у ребенка, составляет 50%. В то же время есть статистика, показывающая что 2/3 случаев — это новые мутации.
Клинические проявления заболевания очень разнообразны и зависят от локализации опухолей. Поражения ЦНС перекрывают поток нервных импульсов, приводят к задержке когнитивного развития, провоцируют судороги, спазмы. Туберомы могут разрастаться и перекрывать поток спинномозговой жидкости, что становится причиной односторонней гидроцефалии. Ангиолипомы (опухоли почек) и поликистоз почек провоцируют развитие артериальной гипертензии. Очень часто встречаются поражения кожи.
Для диагностики используются большие и малые признаки. Чтобы поставить диагноз туберозный склероз, достаточно двух больших признаков или одного большого признака в сочетании с двумя (и более) малыми. Обязательно нужны анализы крови и мочи, УЗД почек, ЭКГ, ЭЭГ, КТ, МРТ, генетические исследования.
Формы заболевания
ТС имеет два основные формы:
- Семейная — обнаруживается в семьях, где был больной родственник. У ребенка, чей родитель болен ТС, шанс заболевания — до 50%.
- Спорадическая — не носит наследственный характер, возникает спонтанно.
Симптомы туберозного склероза
Болезнь Бурневилля имеет довольно вариабельную клиническую картину, но в целом все признаки протекания болезни можно разделить на первичные и вторичные.
- ангиофибромы (новообразования с волокнистым и сосудистым типом ткани) лица или фиброзные бляшки (плотные округлые белые образования) на лбу;
- новообразования возле ногтей;
- нарушение пигментации кожи: появление трех и более гипопигментных пятен;
- выраженная сухость кожных покровов, так называемая шагреневая кожа;
- множественные новообразования на сетчатке (гемартомы);
- туберсы на головном мозге на границе белого и серого вещества;
- опухоль ЦНС;
- гиганто-клеточная астроцитома;
- рабдомиома (узел) сердца;
- кистозная деструкция легочной ткани;
- множественные новообразования на почках.
- многочисленные углубления в эмали зубов;
- полипы в кишечнике;
- разрушение костной ткани (костные кисты);
- фибромы полости рта;
- доброкачественные опухоли (гамартомы) внутренних органов;
- изменение цвета сетчатки глаза;
- нарушение пигментации кожных покровов;
- кисты в почках.
Для точного диагностирования туберозного склероза специалисту нужно подтверждение, как минимум двух первичных признаков или одного первичного признака и двух вторичных признаков.
У детей симптоматика следующая:
- головокружение и замедленная речь;
- временное ухудшение зрения, боль в глазах;
- понижение мышечного тонуса;
- дрожь конечностей (при поражении мозжечка);
- недержание мочи (при сложном протекании болезни);
- тошнота и рвота.
Поражение ЦНС
Поражение центральной нервной системы может проявляться по-разному. У пациента могут наблюдаться:
- приступы судорог (встречаются уже на первом году жизни ребенка, больного туберозным склерозом);
- изменение поведенческих реакций (аутизм, синдром гиперподвижности и дефицита внимания, агрессия и аутоагрессия);
- нарушение интеллекта (умственная отсталость) — отмечается в 50% случаев (варьируется от умеренной до глубокой);
- нарушение сна (бессонницы, снохождение, раннее пробуждение и пр.).
При поражении ЦНС на мозге появляются:
- Корковые туберсы (единичные и множественные) — выступы над бороздами головного мозга. Наблюдаются у больных в 50% случаев;
- Субэпендимарные узлы локализуются в желудочках головного мозга. В 10-15% случаев могут перерасти в гигантоклеточные астроцитомы. В этом случае у пациентов наблюдаются сильная головная боль, тошнота и рвота.
Дерматологические симптомы
Данное заболевание довольно активно проявляет себя внешне. Так, у больного могут обнаруживаться следующие симптомы:
Офтальмологические симптомы
У 50% пациентов наблюдаются офтальмологические симптомы, сложность заключается лишь в том, что их трудно обнаружить на ранних этапах. Проявляется заболевание на этом уровне в появлении доброкачественной опухоли (гамартома, нередко — множественных) сетчатки и зрительного нерва. Обычно опухоль локализуется рядом с оптическим диском.
Проявляет себя гамартома падением зрения, депигментацией радужки, отеком диска зрительного нерва, косоглазием, катарактой и пр.
Поражение внутренних органов
Новообразования внутренних органов при ТС часто бывают множественными и поражают парные органы. Какое-то время течение болезни может быть бессимптомным. Чаще других при ТС поражаются следующие органы:
- сердце (рабдомиома) — при внутриутробном развитии рабдомиомы — вероятна гибель плода. У маленьких детей о наличии рабдомиомы могут свидетельствовать тахикардия, аритмия, фибрилляция желудочков. У детей постарше симптомов вообще может не быть, а к 5-6-летнему возрасту рабдомиома может исчезнуть совсем);
- легкие (кисты) поражаются уже в сознательном возрасте, обычно подростковом, приводит к дыхательной недостаточности;
- почки (поликистоз) — симптом характерен для половины больных и выступает вторым, приводящим к смерти (после поражения ЦНС). Данная проблема обнаруживается обычно у больных после 30 лет;
- печень (гамартома — доброкачественная опухоль, которая сопровождается одышкой, рвотой, дыхательной дисфункцией);
- кишечник (полипы — доброкачественные новообразования на ножке, свисающие со стенок органа. Возможны приступы схваткообразных болей и кровотечение).
Два последних нарушения приводят также к образованию дефектов зубов (углубления на эмали).
Диагностика туберозного склероза
ТС довольно трудно диагностировать. Как уже говорилось выше, иногда заболевание может протекать бессимптомно. Так как болезнь проявляет себя в разных органах (от глаз до кишечника), необходимы будут совместные усилия нескольких специалистов и проведение обширного обследования. Для начала специалистами проводится опрос пациента, который обычно содержит следующие вопросы:
- Какие симптомы?
- Как давно они появились?
- С какой частотой повторяются?
- Были ли в семье случаи данного заболевания?
Невролог осматривает пациента с целью найти какие-либо неврологические патологии (приступы эпилепсии, расстройства интеллекта и пр.).
Дерматологический осмотр нацелен на нахождение бугорков на коже или признаков ее обесцвечивания.
Офтальмолог осматривает глазное дно, сетчатку, зрительный нерв.
Также проводятся следующие обследования:
- Анализ крови на наличие повышенного уровня креатина, мочевины (наблюдается при поражении почек);
- Анализ мочи на наличие крови в ней (также симптом нарушения работы почек);
- Эхокардиография призвана показать бугорки на сердце;
- ЭЭГ с пробами поможет зарегистрировать церебральную эпилептическую активность.
- Чтобы оценить силу поражения ЦНС необходимо провести КТ и МРТ головного мозга. В случае туберозного склероза здесь будут видны бугорки на поверхности головного мозга, а также увеличение количества ликвора.
- При подозрении на локализацию ТС в конкретном органе проводится УЗИ, КТ и МРТ этого органа или совокупности (например, УЗИ брюшной полости), при подозрении поражения кишечника проводится ректороманоскопия и колоноскопия. Диагностика офтальмологических поражений происходит путем проведения офтальмоскопии (осмотр глазного дна с целью оценки состояния сетчатки).
- Генетическое обследование на наличие изменений в генах TSC1 и TSC2.
Лечение туберозного склероза
Полностью вылечиться от ТС на данный момент невозможно, так как заболевание является генетическим. Курс терапии призван прервать признаки болезни и улучшить общее состояние пациента.
Антиконвульсантная терапия является основной в лечении ТС, так как данное заболевание сопровождается частыми припадками эпилепсии, а степень олигофрении напрямую связана с частотой эпиприступов.
Врачами обычно назначаются препараты следующего рода:
- Гипотензивные — призваны понизить давление;
- Сердечно-сосудистые — в случае нарушения работы сердца;
- Кортикостероиды, противосудорожные средства и антидепрессанты — для ликвидации приступов эпилепсии и пр.
Пациентам с ТС также важно правильно питаться: необходимо увеличить потребление жиров и уменьшить — белков и углеводов.
В случае тяжелого протекания болезни пациентам назначается операция (в зависимости от места локализации опухоли): удаляют опухоли в головном мозге, почках, органах ЖКТ и пр. Если опухоли множественные, нередко удаляется орган целиком. Бугорки на коже удаляют лазером или методом криодеструкции.
Для детей также необходима консультация психотерапевта для предупреждения олигофрении. Лечение в детском возрасте призвано устранить нервные судороги. При локализации опухолей в сердце или почках лечат сердечную и почечную недостаточность. Внутричерепные опухоли подлежат удалению, так как они провоцируют рост внутричерепного давления. Вовремя поставленный диагноз и грамотное лечение дает шансы ребенку прожить довольно долгую жизнь.
Осложнения
ТС — заболевание довольно опасное: диагностировать его трудно, вылечить практически невозможно, так еще и встречается ряд осложнений, а именно:
- Гемианопсия — поражение зрительной системы. Человек с таким диагнозом видит мир будто наполовину;
- Водянка головного мозга (гидроцефалия) опасна сильными головными болями, снижением слуха и зрения;
- Почечная недостаточность ведет к задержке шлаков в организме, нарушению кислотно-щелочного баланса, сбоям в работе сердца;
- Стойкая эпилепсия — это невозможность для пациента прийти в сознание даже на время между приступами. Эпилептический статус (затянувшийся приступ) может привести к летальному исходу.
ТС опасен целым рядом осложнений, каждое из которых, в свою очередь, требует отдельного лечения, именно поэтому так важно вовремя поставить правильный диагноз и приступить к лечению ТС.
Прогноз заболевания
Полностью данное заболевание устранить невозможно, но вот облегчить симптомы — вполне. Поэтому так важно диагностировать ТС на ранних этапах: возможно для борьбы с признаками еще будет достаточно традиционной терапии без хирургического вмешательства.
Поэтому при обнаружении ряда вышеописанных симптомов (особенно у детей) сразу необходимо проконсультироваться с врачом, сдать необходимые анализы и пройти обследование. Так как ТС — нарушение генетическое, то людям, в чьих семьях оно встречалось, на стадии планирования беременности рекомендуется консультация медицинского генетика.
Менингит характеризуется воспалением мозговых оболочек спинного и головного мозга. Заболевание относится к числу инфекционных. Менингитом болеют взрослые и дети. У детей менингит нередко проходит в молниеносной или острой форме. Взрослые чаще болеют

Причины менингита
Менингит может иметь инфекционное и неинфекционное происхождение. Инфекционная форма заболевания развивается в результате проникновения в организм микроорганизмов: бактерий, вирусов, грибков и паразитов. Неинфекционный менингит развивается у больных в результате приема некоторых медикаментов и формирования опухолей.
В медицине используется классификация по типу микроорганизмов-возбудителей. Современному человеку важно знать, как распознать менингит и какие разновидности заболевания существуют:
- бактериальный менингит наиболее часто вызывают стрептококки, менингококки, пневмококки и гемофильные палочки, которые передаются воздушно-капельным путем;
- вирусный менингит. Наиболее распространенная форма заболевания. Данный тип характеризуется наименьшей тяжестью. Возбудителями вирусного менингита являются энтеровирусы;
- грибковый менингит развивается в результате жизнедеятельности определенных видов грибковых микроорганизмов;
- паразитические менингиты.
Перечень терапевтических мероприятий при менингите определяется тем, в результате действия каких факторов началось развитие заболевания. Так, при лечении бактериального менингита назначаются антибиотики, которые являются неэффективными при вирусном менингите. Если человеку известно, как распознать менингит, то вероятность диагностирования заболевания на начальной стадии и эффективность терапевтических мероприятий высоки.
Определить менингит самостоятельно не представляется возможным. Клиническая картина заболевания имеет разнообразный характер. Признаки отличаются в соответствии с этиологическим фактором. Начальные проявления менингита часто принимают за симптомы простуды. По мере распространения инфекционного процесса состояние резко ухудшается. Высокий риск летального исхода вследствие менингита сохраняется на протяжении 1-2 суток с момента появления первых патологических симптомов. Несвоевременная диагностика и терапия приводят к развитию тяжелых, угрожающих жизни осложнений.
Группа риска
В группу риска по менингиту входят дети и пожилые люди. Кроме того, данное заболевание часто диагностируется у людей с отсутствием селезенки и иммунодефицитом.
Распространение менингита, как и всех других инфекционных заболеваний, активнее в местах большого скопления людей, закрытых группах, например, в детских садах, школах, студенческих общежитиях, казармах, так как заболеть менингитом легче, оказавшись в компании с бессимптомными носителями.

Чаще всего менингит передается воздушно-капельным путем. Этот механизм передачи инфекции считается самым распространенным и свойственным для менингита вирусного происхождения. Возбудитель инфекции передается через кашель, чихание, поцелуи и сексуальные контакты.
Новорожденные дети могут заразиться от зараженной матери через родовые пути. Особенно велика вероятность заражения у детей, появляющихся на свет с помощью кесарева сечения. Таким путем может передаваться бактериальный и вирусный менингит.
Заражение менингитом может произойти орально-фекальным путем: через грязную пищу или неочищенную воду.
Кроме того, менингит может развиться в результате укуса насекомого или животного – носителя инфекционного агента.
Симптомы менингита у взрослых
Менингит, как правило, отличается внезапным началом. Первыми симптомами менингита у взрослых являются: повышение температуры тела, головные боли, рвота (так называемая, менингальная триада). Однако данные патологические признаки менингита сопровождают и другие инфекционные заболевания, поэтому важно знать особенности проявления менингита.
Менингит отличается стремительным развитием с ярко выраженными признаками интоксикации:
- головной болью;
- высокой температурой и ознобом;
- спутанностью и потерей сознания;
- судорогами;
- кожной сыпью;
- мышечной слабостью;
- сонливостью;
- светобоязнью, повышенной чувствительностью кожи, реакцией на звук;
- ригидностью затылочных мышц;
- потерей аппетита, тошнотой, рвотой;
- конъюнктивитом;
- повышением частоты сердечных сокращений.
У больных менингитом часто первым признаком заболевания являются высыпания на коже и слизистых оболочках. Сыпь изначально носит геморрагический характер, иногда на кожных покровах появляются пятна и папулы. Высыпания расценивают как аллергическую реакцию на приём лекарственных средств.
Головная боль
Насторожить должна сильная головная боль. Головные боли, вызванные менингитом, по ощущениям отличаются от других видов болей. Их интенсивность гораздо выше, чем у головных болей, связанных с обезвоживанием или с мигренями. Прием безрецептурных обезболивающих препаратов не приносит облегчения.
Тошнота и рвота
Тошнота и рвота, появившиеся при головной боли, не являются абсолютными признаками менингита. Данные симптомы могут сопровождать и другие заболевания, например, мигрень. Пристальное внимание необходимо обратить на другие состояния, которые возникают наряду с рвотой и тошнотой.
Рвота при менингите редко бывает однократной, чаще всего она многократная, повторяющаяся, и не связана с приемом пищи.
Высокая температура
Повышение температуры тела, как и другие симптомы, может свидетельствовать о развитии менингита. При данном заболевании температура обычно гораздо выше, чем при ОРЗ. К тому же прием жаропонижающих средств при менингите малоэффективен – температура снижается очень сложно и кратковременно.
Температура при менингите может быть умеренной, высокой и сверхвысокой. Умеренная температура держится в пределах от 38 0 до 39 0 С, высокая от 39 0 до 42 0 С, сверхвысокая от 42 0 Си выше.
Менингит у ребенка без температуры встречается в нескольких случаях:
- если у ребенка есть сопутствующая инфекция носоглотки, менингит в данном случае считается вторичным заболеванием.
- если ребенок недоношенный, заражение инфекцией произошло внутриутробно, во время родов, после родов, то нередко заболевание не проявляется повышением температуры – симптомы менингита сглажены. Такое состояние связано с плохой работой иммунной системы малыша, морфофункциональной незрелостью организма.
- если менингит развился у новорожденного после рождения, то первые симптомы заболевания появятся через 20-25 дней. К этому моменту снижается в крови ребенка уровень антител, полученных от матери. Очень часто такой менингит протекает на начальных стадиях без температуры.
- нередко без температуры протекает вирусный менингит. Он проходит в легкой форме за несколько дней.
Независимо от того, есть у ребенка повышенная температура или нет, при появлении первых симптомов менингита следует срочно обратиться к врачу.
Болевые ощущения в шее
Довольно часто больные с менингитом жалуются на болезненность и чувство напряжения в шее, им трудно повернуть или поднять голову. Это связано с давлением от воспаленных оболочек мозга. Данный симптом может наблюдаться также при растяжении мышц шеи или травме от резкого движения головой.
Подтвердить подозрение на менингит может сгибание бедер в горизонтальном положении больного – возникновение болей в шее во время выполнения данного движения является признаком менингита.
Затрудненная концентрация внимания
Воспаление мозговых оболочек при менингите сопряжено с возникновением у больных трудностей восприятия. Им сложно дочитать до конца статью, сосредоточиться на разговоре, завершить выполняемое задание. Степень спутанности сознания может усугубляться по мере нарастания отека головного мозга. Кроме вялости и спутанности сознания у больных наблюдается падение артериального давления, появление одышки, шумного поверхностного дыхания.
Вялость, сонливость
Больные становятся не способными к самостоятельным действиям, у них появляется сонливость и вялость. Данное состояние возникает как следствие общей интоксикации организма или отека головного мозга. Бактериальные менингиты могут сопровождаться резким угнетением сознания и даже комой.
Светобоязнь
Проявлением светобоязни у больных менингитом является сильная боль, возникающая при ярком свете. Появление болевых ощущений и чувствительности глаз, как реакции на свет, считается тревожным сигналом, так как является характерным признаком менингита.

Судороги
Судороги, иногда с непроизвольным мочеиспусканием и дезориентацией в пространстве, наблюдаются у 20% больных менингитом. Их течение схоже с эпилептическим, либо наблюдается появление тремора отдельных мышц и отдельных частей тела. Возникновение судорог (генерализованных и локальных) связано с раздражением коры и подкорковых структур головного мозга.
Характерная сыпь
Сыпь геморрагического характера на кожных покровах и слизистой не является специфическим симптомом менингита. Она появляется у 25% больных с бактериальным менингитом и чаще всего наблюдается при заболевании менингококковой природы, так как именно менингококк вызывает повреждение внутренних стенок сосудов. Появление кожных высыпаний отмечается, как правило, через 15-20 часов от начала болезни. При этом сыпь является полиморфной – может быть розеолезной, папулезной, в виде узелков или петехий. Высыпания имеют неправильную форму, могут выступать над уровнем кожи.
Психомоторное возбуждение, беспокойство
Беспокойство, возбуждение и дезориентация возникают у больных с такой формой заболевания, как менингоэнцефалит, в начале заболевания. При бактериальной форме менингита подобные симптомы могут появляться на 4-5 день от начала болезни. После психомоторного возбуждения у больных может произойти потеря сознания или кома.
В начале заболевания, как и в более поздних стадиях у больных менингитом может развиться симптоматический психоз, проявляющийся возбуждением либо наоборот, заторможенностью, бредом, зрительными и звуковыми галлюцинациями.
Бред и галлюцинации могут возникать у больных с лимфоцитарным хориоменингитом и менингитом, который вызывает вирус клещевого энцефалита.
Среди этиологических факторов менингита выделяют гайморит. Скопление гнойного содержимого в области носовых пазух без корректного лечения может привести к распространению инфекции на мозговые оболочки. В подобных случаях менингит рассматривается в качестве осложнения гайморита. От качества проводимой диагностики зависит эффективность лечения воспаления носовых пазух.
Гайморит и менингит: взаимосвязь заболеваний
Менингит развивается как самостоятельное заболевание, так и может являться осложнением при патологических процессах. Гайморит и менингит взаимосвязаны, так как скопление гноя в гайморовых пазухах может стать причиной воспаления оболочки мозга. Людям, относящимся к группе риска, важно знать, как гайморит переходит в менингит, какие симптомы при этом отмечаются у больного.
Развитие осложнений при гайморите наблюдается редко, так как современные специалисты используют эффективные методы лечения. Однако при несвоевременном и неэффективном лечении на фоне сниженного иммунитета у пациента может развиваться менингит. Если у больного существуют подозрения на менингит или резко ухудшилось самочувствие, необходимо обратиться к врачу-терапевту или неврологу, который назначит обследование и установит причину проблемы.
Самым главным и показательным анализом при подозрении на наличие воспалительного процесса в оболочках головного и спинного мозга является люмбальная пункция. Исследовать спинномозговую жидкость необходимо для выявления причины воспаления и назначения адекватной терапии.
Боли при менингите
Наиболее характерным признаком патологии является головная боль. Она имеет место при любой форме менингита и появляется с первых дней заболевания. Головные боли могут иметь различный характер, но, как правило, пациенты жалуются на то, что болит вся голова. Также на фоне головных болей нередко наблюдаются приступы тошноты и рвоты.
Какие боли возникают
Проявление болевых ощущений напрямую зависит от локализации зоны поражения мозга, природы возникновения менингита (вирусной либо инфекционной, либо же как следствие развития заболевания по причине сужения сосудов и нарушений позвоночника).
Во всех случаях характер головной боли будет отличаться. Боли зависят от области расположения воспаления, его распространенности, а также от степени влияния на работу мозга.
Головная боль при серозном менингите
При серозном менингите во всем черепе наблюдается умеренное проявление боли. При этом жара и повышения температуры тела не наблюдается. У больного на фоне постоянных головных болей также появляется озноб, тошнота и рвота. При этом после рвоты облегчения больной не ощущает.
Как болит голова при гнойном менингите
При данной форме менингита у больного появляются сильные головные боли, имеющие распирающий характер. Болевые ощущения то стихают, то вновь нарастают. Характерными в данном случае являются тошнота, рвота, жар, озноб.
Боли при субарахноидальном кровоизлиянии
В данной ситуации головные боли имеют постоянный характер, то есть они не утихают ни днем, ни ночью, ни летом, ни зимой. Головная боль характеризуется интенсивным, резким и острым проявлением.
Как болит голова при туберкулезном менингите
Это самая слабая по своим проявлениям форма менингита, отличающаяся нарастающим характером проявления симптоматики. У пациентов наблюдается постоянная слабость, повышенное потоотделение, депрессия. Тошнота и рвота появляются очень редко.
При любой форме менингита головные боли приводят к ухудшению зрения. Нередко у пациентов развивается непереносимость громких звуков и светобоязнь. Боли в несколько раз усиливаются при нажатии на область висков или глаз.
Диагностика менингита
- развернутого анализа крови;
- осмотра глазного дна;
- рентгенологического исследования черепа;
- электрокардиограммы сердца;
- электроэнцефалографии;
- компьютерной и магнитно-резонансной томографии.
Для подтверждения диагноза менингита врачи используют бактериологическое исследование слизи из носоглотки и спинномозговой жидкости. При бактериоскопическом исследовании спинномозговой жидкости проводят окраску мазков по Граму или метиленовым синим. Для исключения грибкового менингита окрашивают препарат со спинномозговой жидкостью тушью. Лаборанты выделяют чистую культуру на средах с добавлением нормальной лошадиной сыворотки или сыворотки крупного рогатого скота и проводят её идентификацию по биохимической активности, антигенной структуре.
При вирусных менингитах в препаратах, которые приготовлены с окрашиванием по Граму и тушью, невозможно идентифицировать возбудитель инфекции. Культивирование бактерий и грибов также даёт отрицательные результаты. При культивировании клеточного материала со стандартными лабораторными клеточными линиями можно выделить возбудителя, серологически идентичного вирусу кори. С помощью метода кокультивирования выделяют вирус краснухи.
Для выявления олигоклональных иммуноглобулинов используют метод электрофореза в агарозном геле или изоэлектрофокусирования гамма-глобулинов спинномозговой жидкости. Иммуноглобулины появляются при целом ряде вирусных инфекций. В результате иммунологических исследований в цереброспинальной жидкости обнаруживают антигены вирусов или антитела, методом полимеразной цепной реакции—нуклеиновую кислоту вируса. Методом иммуноферментного анализа выявляют антигены возбудителя в кале, моче или слюне. Экспресс-методы позволяют быстро и в ранние сроки определить наличие антигена вируса простого герпеса в ликворе и крови или ДНК вируса (методом полимеразной цепной реакции).
Цитоз ликвора при менингите
Анализ спинномозговой жидкости позволяет не только подтвердить диагноз, а также и дифференцировать гнойный и серозный менингит, выявить возбудителя заболевания, определить степень интоксикации, а также дает возможность проводить контроль эффективности лечения.
Бактериологическое исследование спинномозговой жидкости в случае туберкулезного менингита может давать ложноотрицательный результат. Выявление туберкулезной палочки в ликворе зависит от тщательности проведения исследований. В Юсуповской больнице все диагностические процедуры выполняют с использованием современной медицинской аппаратуры и применением новых препаратов и методик. Результаты исследований, проведенных в Юсуповской больнице, являются достоверными и максимально информативными.
Как лечится менингит
В Юсуповской больнице пациенты могут получить полный спектр медицинских услуг по выявлению и лечению менингита, реабилитации после перенесенного заболевания и профилактике. Пациенты с менингитами могут обратиться в клинику неврологи Юсуповской больницы ежедневно в течение 24 часов для получения экстренной помощи.
При поступлении пациентов в Юсуповскую больницу проводится комплексная диагностика, включающая ряд обследований для выявления причин менингита, сбор жалоб и симптоматики. Больные менингитом нуждаются в стационарном лечении, поэтому в Юсуповской больнице созданы комфортные условия пребывания и обеспечивается взаимодействие с квалифицированным персоналом.
Последствия менингита
Так как мужчины реже своевременно обращаются к врачу и чаще, чем женщины, болеют цереброспинальным менингитом, у них нередко развиваются осложнения во время болезни. К легким осложнениям относится головная боль при перемене погоды или переутомлении, незначительное снижение слуха, концентрации внимания, памяти. В зависимости от тяжести течения менингита и своевременности обращения к врачу могут развиться следующие осложнения:
- резкое снижение остроты зрения;
- заикание;
- косоглазие;
- значительная потеря слуха;
- снижение интеллекта;
- водянка мозга;
- эпилепсия;
- нарушение психики;
- развитие шизофрении;
- деменция.
Больной может впасть в кому, у него может развиться паралич, при осложненном течении менингита возможен летальный исход.
В Юсуповской больнице проводят эффективную диагностику заболевания. Больной проходит обследование в диагностическом центре больницы, который оснащен современным оборудованием ведущих мировых производителей. Записаться на консультацию к врачу можно по телефону Юсуповской больницы.
Читайте также:

