Тяжелая травма и инфекция
Обновлено: 19.04.2024
6628 12 Августа
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Ушиб: причины появления, симптомы, диагностика и способы лечения.
Определение
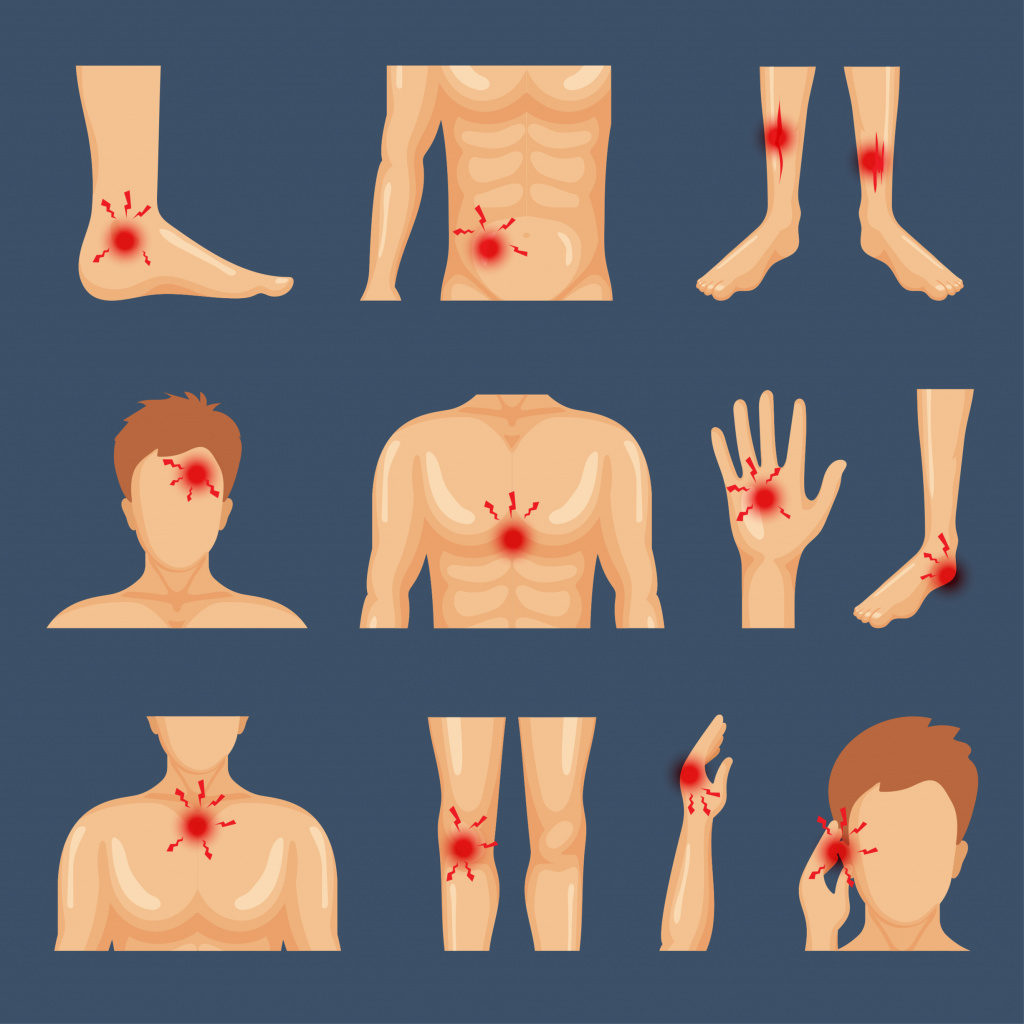
Ушиб — закрытое механическое повреждение внутренних тканей или органов без значительного нарушения их структуры. Для ушибов характерна внезапность, быстрота и кратковременность действия травмирующего фактора. Ушибы носят большей частью местный характер. Наиболее уязвимы дерма и расположенные под ней сосуды, что приводит к образованию гематом и отеков. В результате сильного ушиба могут быть травмированы внутренние органы. Тяжесть процесса определяется видом поврежденной ткани или органа, на которые воздействует травмирующий агент (кожа, подкожная клетчатка, мышцы, паренхиматозные или полые органы, головной или спинной мозг и др.).
В тех случаях, когда повреждение носит тяжелый характер, происходят множественные разрывы мелких сосудов с последующим кровоизлиянием и нарушением функции органа.
Причины появления ушибов
Ушиб считается наиболее распространенным видом бытовых травм и возникает, как правило, при падении или ударе о твердые предметы. У детей первых лет жизни преобладают бытовые, игровые травмы, ушиб мягких тканей лица и шеи. В более старшем возрасте основными считаются транспортные, спортивные и уличные травмы.
Ушиб легкого и/или ушиб сердца в результате механического воздействия на грудную клетку является потенциально опасной травмой - подавляющее большинство пострадавших составляют водители, ударившиеся грудью о рулевую колонку автомобиля.
Ушиб поверхностных мягких тканей всегда сопровождается отеком места повреждения в результате пропитывания кожи лимфой, кровью и местного асептического воспаления. Выраженность отека зависит от площади повреждения подкожной клетчатки в месте ушиба. Так, например, в области свода черепа ввиду тонкого слоя подкожной жировой клетчатки отек незначительный, тогда как даже слабые ушибы лица сопровождаются сильным отеком.
В результате ушиба головы может развиться сотрясение мозга.
Сильное глубокое кровотечение нередко приводит к дополнительной травме соседних тканей в результате их сдавливания, что сопровождается постепенным усилением боли и нарушением функции травмированного органа.
Нередко в месте травмы наблюдаются ссадины и неглубокие раны, которые служат входными воротами для возбудителей инфекции.
Классификация заболевания
Ушибы различаются по степени тяжести:
- первая — легкое повреждение без нарушения целостности кожного покрова либо с незначительными царапинами и ссадинами, практически безболезненное, самостоятельно заживающее на протяжении нескольких дней;
- вторая — ушиб мышц, сопровождающийся сильной болью, образованием отеков и гематом;
- третья — в результате ушиба могут быть повреждены связки и сухожилия;
- четвертая — ушиб внутренних органов с сильным отеком и болезненными ощущениями, с возможностью нарушения работы поврежденных органов.
Кровоизлияние в месте ушиба проявляется сине-багровым пятном, цвет которого постепенно меняется на зеленоватый и желтый. В зависимости от локализации ушиба синяк и припухлость могут проявиться незамедлительно, как происходит в случае повреждения подкожной клетчатки и верхних слоев кожи. В случае ушибов глубоко расположенных тканей гематома формируется спустя несколько часов и даже суток.

Травмы мягких тканей сопровождаются болью различной интенсивности. Так, при ушибах крупных нервов и их окончаний боль всегда резкая, простреливающая. При ушибах туловища и конечностей могут возникать напряженные гематомы с распирающими болями, иногда с поверхностным онемением.
Отек, сопровождающий ушиб, снижает подвижность травмированных тканей, создавая дискомфорт во время движения или поворота туловища (например, при ушибе ребер). Самую сильную боль пострадавший испытывает сразу после ушиба мягких тканей, а через пару часов она стихает. При надавливании болезненность увеличивается.
При ушибе сустава через несколько часов после травмы его объем увеличивается, нарушается функция, усиливается боль (особенно при движении).
Сильная боль возникает при ушибе надкостницы, наружных половых органов, крупных нервных стволов.
Симптомы ушиба и закрытого перелома очень схожи между собой: сильная боль, отек, ограничение подвижности. Но если в случае ушиба боль стихает в течение 2–3 часов, то при переломе она, напротив, может усиливаться.
Общее состояние больных при ограниченных, поверхностных ушибах обычно не страдает. Но при множественных ушибах тела, больших или нагноившихся гематомах, гемартрозе (кровоизлиянии в полость сустава) возможна лихорадка с температурой до 38°С и выше, обусловленная всасыванием продуктов распада крови.
Симптомы ушиба легких включают повышенную чувствительность и болевые ощущения в области грудной клетки, ребер и в некоторых случаях одышку. Другие физические признаки могут наблюдаться по причине сочетанных повреждений.
Диагностика ушиба
Основные методы диагностики:
-
рентгенография грудной клетки;
Рентгенологическое исследование структуры легких с целью диагностики различных патологий.
Травматическая болезнь – общий ответ организма на травматическое воздействие. Включает в себя ряд приспособительных и патологических реакций, а также местных и общих изменений, происходящих в организме с момента травмы до выздоровления или смерти больного. Влияет на исход травмы, в значительной степени определяет прогноз в отношении жизни и трудоспособности. Включает в себя изменения в психоэмоциональной сфере, процессах метаболизма и гемостаза, состоянии иммунной системы, работе сердца, легких, органов пищеварения и ЦНС. Имеет стадийное течение.
МКБ-10
Общие сведения
Травматическая болезнь – относительно новая концепция в травматологии, позволившая пересмотреть отношение к травме. Ранее как в практической медицине, так и в научных работах доминировал взгляд на травму, как на изолированное поражение определенного органа. Формирование концепции травматической болезни дало возможность рассмотреть изменения, происходящие в организме больного, как единую систему взаимосвязанных процессов. В настоящее время данная концепция считается общепризнанной и широко используется практическими врачами: травматологами, реаниматологами, терапевтами, хирургами, психологами, иммунологами, кардиологами, физиотерапевтами и другими специалистами, которые принимают участие в лечении больного на стационарном и поликлиническом этапах.

Первый период травматической болезни
Начинается сразу после травматического воздействия и продолжается 6-12 часов. Может проявляться в виде терминального состояния или травматического шока. При повреждении груди возможно развитие острой сердечной или дыхательной недостаточности, при черепно-мозговых травмах – травматическая кома. В этом периоде пациенты находятся либо на догоспитальном этапе, либо на этапе поступления и обследования. На догоспитальном этапе проводят временную иммобилизацию, инфузионную терапию, искусственное дыхание, обезболивание и т. д.
При поступлении в стационар на фоне продолжающихся реанимационных мероприятий осуществляют неотложные инвазивные манипуляции интенсивной терапии (трахеостомию, катетеризацию подключичной артерии, катетеризацию мочевого пузыря и т. д.). Выполняют диагностические манипуляции (люмбальную пункцию, лапароцентез), а также манипуляции и операции, направленные на устранение состояний, представляющих непосредственную угрозу для жизни пациента (плевральную пункцию, торакоскопию, лапароскопию и т. д.).
При благоприятном развитии событий этап завершается постановкой диагноза, устранением жизнеугрожающих состояний, относительной стабилизацией показателей дыхания и кровообращения и возмещением кровопотери. Из противошоковой палаты или операционной больных переводят в отделение реанимации. Основной причиной смерти пациентов в этом периоде являются несовместимые с жизнью повреждения, тяжелый шок и массивная кровопотеря с развитием ДВС-синдрома.
Второй период травматической болезни
Продолжается 12-48 часов. На этом этапе пульс, артериальное давление и другие показатели сохраняются в пределах нормы или приближаются к своим нормальным значениям, но организм функционирует неустойчиво. Пациенты находятся в отделении реанимации, им проводят интенсивную терапию. При необходимости в этом периоде осуществляют срочные хирургические вмешательства: операции на спинном мозге, позвоночнике, костях, магистральных сосудах конечностей и т. д.
План лечения, объем и способ оперативных вмешательств определяют индивидуально, с учетом характера травм, вероятности развития опасных осложнений, возраста и общего состояния больного, наличия острых и хронических заболеваний. В одних ситуациях оказывается целесообразным отложить операцию на более поздний срок, чтобы не увеличить опасность для жизни пациента. В других, напротив, может быть показано одновременное вмешательство на нескольких областях тела. Основной причиной гибели пострадавших в этом периоде является полиорганная недостаточность.
Третий период травматической болезни
Начинается на третьи сутки, может продолжаться до двух недель. На этом этапе наиболее высока вероятность развития осложнений. Во время предыдущих периодов организм пациента страдал от кровопотери, ДВС-синдрома и эндотоксикоза. Все перечисленное стало причиной формирования множественных очагов микротромбозов во внутренних органах: почках, кишечнике, печени, селезенке, легких и сердце. Теперь микроорганизмы, попадающие в кровь из ран, кишечника и верхних дыхательных путей, начали оседать в пострадавших участках, провоцируя образование очагов воспаления, отрыв тромбов и их миграцию по сосудистому руслу и т. д.
Особенно часто страдают легкие. Из-за воспаления базальная мембрана альвеол теряет способность пропускать кислород, в таких случаях возникает респираторный дистресс-синдром, заканчивающийся смертью в 90% случаев. У больных, перенесших тяжелый шок, на 3-6 сутки может развиться очаговая пневмония или синдром шокового легкого, также завершающийся летальным исходом. Возможна тромбоэмболия, а при тяжелой скелетной травме (например, переломе таза или переломе бедра) – и жировая эмболия.
Осложнения возникают с определенной периодичностью. Так, нарушения со стороны легких при травматической болезни обычно выявляются на 3-4 сутки, перитониты, гнойные трахеобронхиты, менингоэнцефалиты, а также местные инфекционные осложнения (миозиты, анаэробные целлюлиты, флегмоны и абсцессы) – на 6-10 сутки. Тактика лечения определяется индивидуально. Проводится антибиотикотерапия и дезинтоксикационная терапия, в ряде случаев требуются оперативные вмешательства.
Четвертый период травматической болезни
Продолжительность четвертого периода травматической болезни сильно колеблется в зависимости от локализации и тяжести травмы, а также от наличия и характера осложнений. Состояние организма постепенно улучшается, все жизненно важные функции нормализуются. В этом периоде осуществляются плановые операции по восстановлению поврежденных органов и тканей, назначается консервативное лечение, проводятся реабилитационные мероприятия. Степень восстановления органов, пострадавших в результате травмы или осложнений, может сильно варьировать.
Наряду с традиционными медицинскими мероприятиями на этом этапе большое значение приобретает работа по нормализации психологического состояния пациентов. Травма, сопровождающаяся утратой способности к самообслуживанию, изменением условий жизни и социального статуса, является тяжелейшим стрессом не только для тела, но и для психики. А продолжительное лечение еще больше усугубляет эти изменения. Может наблюдаться утрата мотивации, повышенная агрессивность, эмоциональная лабильность, депрессия, наличие эффекта вторичной выгоды и т. д. Поэтому современные ученые и практические врачи, специализирующиеся на лечении травматической болезни, рекомендуют проводить реабилитацию с участием психологов и психотерапевтов.
2. Шокогенная травма и травматическая болезнь (лекция) / Шапот Ю.Б., Селезнев С.А., Куршакова И.В., Карташкин В.Л. // Бюллетень ВСНЦ СО РАМН - 2005 - №3
3. Патологическая физиология и современные принципы лечения тяжелых сочетанных травм / Штейнле А.В. // Сибирский медицинский журнал (Томск) - 2009 - №3
Проведен анализ методов лечения и обследования 913 больных с множественной и сочетанной травмой. Выявлена высокая вероятность развития местных и висцеральных инфекционных осложнений у этих больных на фоне развития травматической болезни и её декомпенсации. Рассмотрены этапы хирургического лечения и сроки окончательной стабилизации костных отломков. Непосредственные результаты лечения изучены у всех 913 больных, отдалённые у 868 (95 %) больных с применением интегральной оценки результатов лечения пострадавших с использованием балльной шкалы Neer-Grantham-Shelton. При анализе причин инфекционных осложнений у больных в контрольной группе (315) выявилось отсутствие понимания развития травматической болезни у больных с множественной и сочетанной травмой, опасности первичной декомпенсации травматической болезни. Лечение больных с множественной и сочетанной травмой требует весь период интенсивных противошоковых мероприятий лечения травматической болезни. При этом необходимо выбирать наиболее щадящий способ стабилизации отломков в качестве первичного остеосинтеза. Окончательный остеосинтез у больных с открытыми переломами длинных трубчатых костей с множественной и сочетанной травмой выполняется после стабилизации общего и местного статуса.

1. Агаджанян В.В., Пронских А.А. К вопросу о тактике лечения больных с политравмой // Политравма. – 2010. – № 1. – С. 5–9.
2. Гиршин С.Г. Клинические лекции по неотложной травматологии / С.Г. Гиршин. – М.: Азбука, 2004. – С. 17.
3. Костюченко Ф.Д. Интенсивная терапия послеоперационной раневой инфекции и сепсиса / Ф.Д. Костюченко, Ф.Н. Вельских, Ф.Н. Тулупов. – СПб.: Фолиант, 2000. – 448 с.
4. Соколов В.А. Множественные и сочетанные травмы / В.А. Соколов. – М.: ГЭОТАР-Медиа, 2006. – С. 141.
5. Шапошников Ю.Г. Концепция травматической болезни на современном этапе // Ортопедия, травматология и протезирование. – 1989. – № 9. – С. 65–70.
6. Matthes G. et al. Early death of the severely injured patient – a retrospective analysis // Z. Blatt. Chir. – 2001. – Bd 126, H 12. – Р. 995–999.
7. Sckalea T.M., Boswell S.A., Scott I. External fixations as a bridge to intra-medullary nailing for patients with multiple injuries and with femur fractures: damage control orthopedics // J. Trauma. – 2000. – Vol. 48, № 4. – P. 613–624.
8. Yokoyama K., ltoman M., Shindo M. Deep infection and fracture healing in immediate and delayed locked intramedullary nailing for open femoral fractures // Orthopedics. – 1999. – Vol. 22, № 5. – P. 485–490.
Лечение пострадавших с множественной и сочетанной травмой представляет одну из наиболее трудных задач в травматологии, характеризуется высокой летальностью – 33,89 %, длительной нетрудоспособностью и высоким уровнем инвалидности – 43,4 % [1, 4, 5, 6]. Для них характерно развитие жизнеугрожающих состояний; наличие синдрома взаимного отягощения; высокая частота развития общих осложнений, более тяжелое протекание раневого процесса, нарушение консолидации отломков и неудовлетворительный результат восстановления функции поврежденных конечностей. В настоящее время происходит широкое распространение современных технологий малоинвазивного внутреннего остеосинтеза. Взамен классического внутреннего и внешнего остеосинтеза они широко применяются в травматологических отделениях многопрофильных стационаров, что значительно расширяет показания для хирургического лечения больных с множественной и сочетанной травмой [2, 3, 7, 8].
Целью данного исследования являлся анализ причин инфекционных осложнений при лечении больных с множественной и сочетанной травмой. Изучение этапов хирургического лечения и сроков окончательной стабилизации костных отломков с целью профилактики инфекционных осложнений и снижения количества неудовлетворительных результатов.
Материалы и методы исследования
Клинический материал исследования составил 913 пострадавших с множественной и сочетанной травмой. Началу работы предшествовал ретроспективный анализ результатов лечения 329 пострадавших с множественными и сочетанными повреждениями, находившихся в стационаре с 2001 по 2006 г. (контрольная группа), у которых были использованы традиционная тактика лечения данной патологии. При лечении повреждений опорно-двигательного аппарата в этой группе преобладал консервативный метод. На первом этапе большинству пострадавшим была выполнена иммобилизация гипсовой повязкой или наложено скелетное вытяжение. Выполнение окончательного остеосинтеза значительно задерживалось в связи с необходимостью лечения осложнений, развившихся из-за неадекватной и недостаточно активной травматологической хирургической тактики на реанимационном этапе, включающей в себя преимущественно консервативные методы стабилизации отломков.
Собственные клинические наблюдения основаны на результатах лечения 584 пострадавших с множественными и сочетанными повреждениями, лечившихся на клинических базах СЗГМУ им. И.И. Мечникова с 2007 по 2013 г. (основная группа). В этой группе при лечении пострадавших использовалась усовершенствованная тактика оказания травматологической хирургической помощи, основанная на объективных критериях тяжести травм и состояния пострадавших, а также широком применении предложенных нами методов и устройств, с целью создания условий для раннего восстановления функций конечностей. Распределение пострадавших с множественной и сочетанной травмой в основной и контрольной группах представлено в табл. 1.
Результаты исследования и их обсуждение
Проведённый анализ показал, что в контрольной группе у пострадавших с сочетанной травмой для стабилизации отломков на реанимационном этапе чаще всего (в 131 случае, или 60,4 %) применяли консервативные методики. Из оперативных методов чаще всего использовали внеочаговый остеосинтез, который применили у 41 пострадавшего (18,8 %). Данный вид остеосинтеза использовался, как правило, в качестве временной фиксации отломков до стабилизации состояния больного. После оказания медицинской помощи на реанимационном этапе больные были переведены на профильное отделение. Основным способом остеосинтеза на профильном отделении был внутренний остеосинтез в 49 случаях (59 %) в отдалённом периоде травмы после использования консервативных методов иммобилизации.
При переводе на профильное отделение часть пострадавших с сочетанной травмой имела различного рода осложнения.
Помимо постгеморрагической анемии у 45 пострадавших (20,7 %), имелись осложнения инфекционного характера: местные – пролежни, нагноения в области спиц в 12 случаях (5,5 %); висцеральные – пневмонии, циститы, тромбофлебиты в 16 случаях (7,4 %). Осложнения ортопедического характера: смещение костных фрагментов в гипсовой повязке, неустранённое смещение в аппарате внешней фиксации, несостоятельность внешней фиксации, контрактуры в смежных суставах в 37 случаях (17 %). Подробная характеристика общих осложнений приведена в табл. 2.
У пострадавших с множественными повреждениями структура осложнений была иной. В этой группе было всего 16 пострадавших (14,3 %), находившихся в тяжёлом состоянии и состоянии средней тяжести (ВПХ-СП – от 18 и выше). В основном с нестабильными переломами костей таза – 9 случаев (8 %). Подробная характеристика общих осложнений приведена в табл. 3.
Проведённый анализ выявил значительное влияние развившихся осложнений на сроки и методы выполнения окончательного остеосинтеза. Средние сроки подготовки к операциям окончательного остеосинтеза для пострадавших с множественными повреждениями составили 13,4 суток после травмы. Для пострадавших с тяжёлыми сочетанными травмами и переломами костей таза время предоперационной подготовки составило 32,5 суток.
У 88 пострадавших (56,2 %), получивших тяжёлую сочетанную или множественную травму, окончательный остеосинтез на профильном отделении выполняли после лечения общих осложнений и коррекции основных показателей гомеостаза, что, несомненно, отрицательно сказалось на сроках консолидации и функциональных результатах лечения.
Интегральная оценка результатов лечения пострадавших производилась с использованием балльной шкалы Neer-Grantham-Shelton. Отдалённые результаты лечения больных с сочетанной травмой удалось проследить у 209, с множественной травмой у 106 пострадавших, и они представлены в табл. 4.
Для улучшения результатов лечения пострадавших с множественной и сочетанной травмой были проведены экспериментальные исследования и предложены новые устройства и методы хирургического лечения, ставшие основой усовершенствованной тактики запрограммированного многоэтапного хирургического лечения (ЗМХЛ) или damage control пострадавших с множественной и сочетанной травмой. С целью оценки эффективности предложенной тактики проведён сравнительный анализ основных лечебных мероприятий, осложнений, результатов и сроков лечения пострадавших в основной и контрольной группах.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
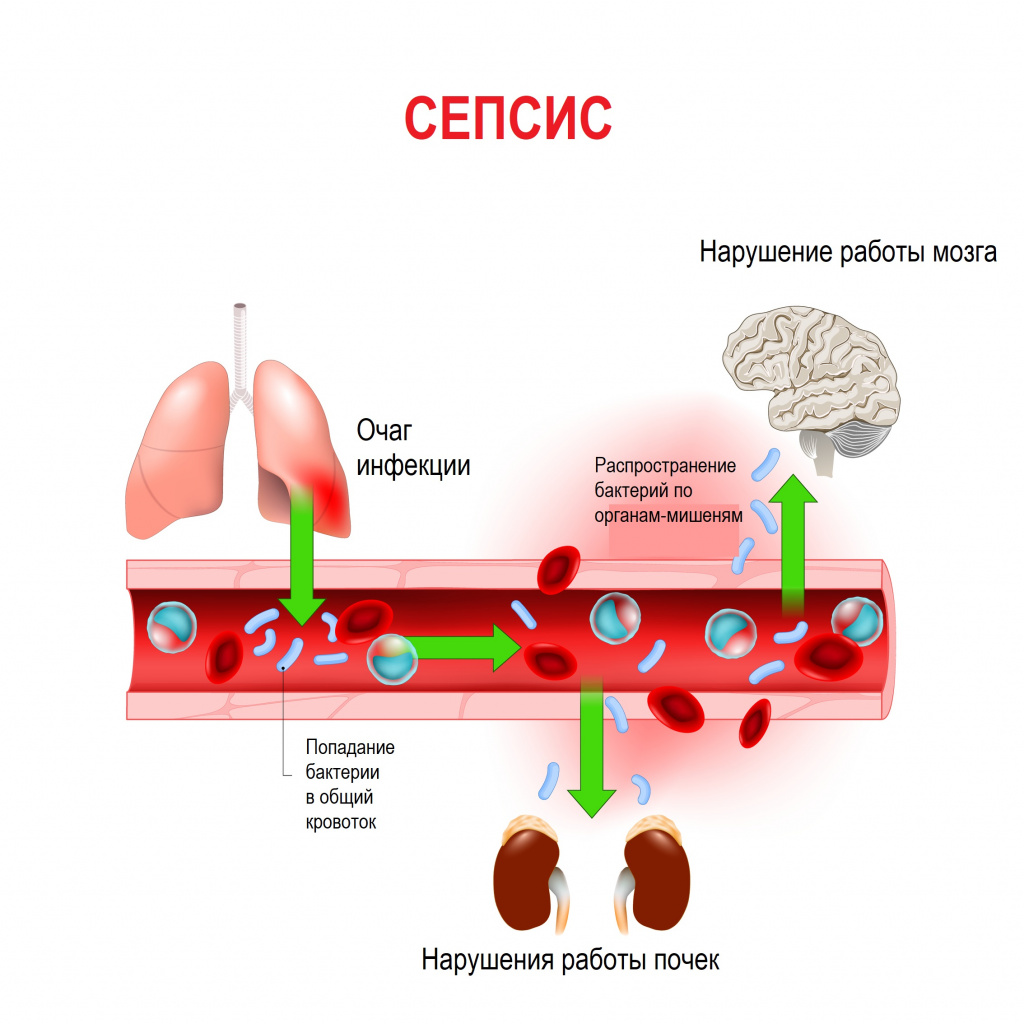
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
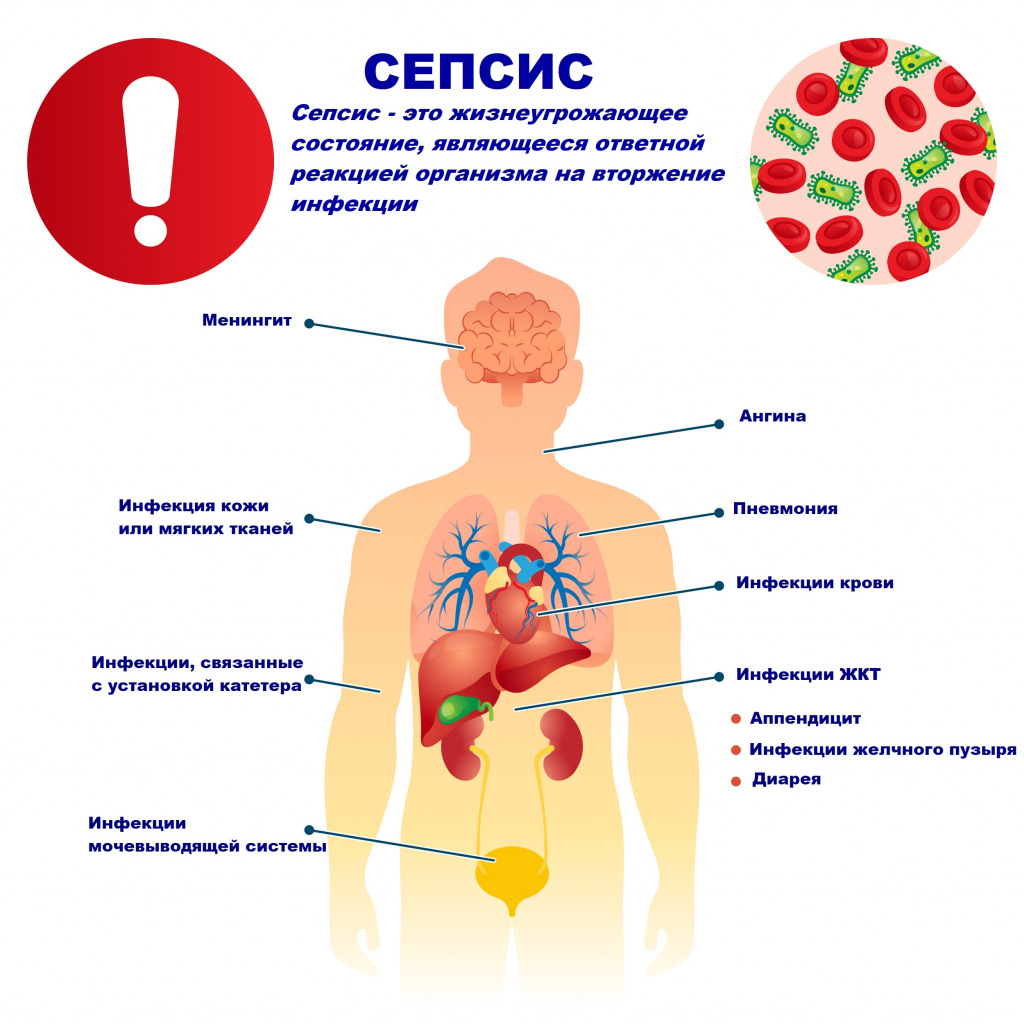
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Читайте также:

