У больных с хламидийным цервицитом вне беременности наиболее эффективен
Обновлено: 12.05.2024
Статья содержит данные об эпидемиологии и этиологии урогенитального хламидиоза. Подробно рассмотрены вопросы лечения инфекции, приведены схемы назначения препаратов различных фармакологических групп. Представлены общие соображения, касающиеся профилактики хламидийной инфекции.
Инфекции, вызываемые микроорганизмом Chlamydia Trachomatis (СТ), в настоящее время признаны одними из наиболее распространенных заболеваний, передаваемых половым путем.
Инфекции, вызванные СТ, - самые распространенные и самые "дорогостоящие" из бактериальных заболеваний, передающихся половым путем. Последствия невыявленной и нелеченной инфекции наносят обществу демографический и экономический ущерб, оцениваемый астрономическими суммами. Например, в США регистрируется примерно 4 млн новых случаев в год. При этом экономические потери от хламидиоза оценены в 1 млрд долларов, а потери от нелеченной хламидийной инфекции достигают 4 млрд долларов ежегодно [1].
В отечественной литературе приводятся весьма разноречивые данные о распространенности хламидиоза. При этом надо принимать во внимание, что регистрация урогенитального хламидиоза (УХ) в России началась лишь с декабря 1993 г. По этим данным, заболеваемость УХ в 2 - 3 раза выше, чем гонореей [2].
В большом числе исследований показано, что распространение хламидийной инфекции (ХИ) среди сексуально активных девушек-подростков обычно составляет 10 - 12%, а среди женщин молодого возраста (до 25 лет) - 20 - 22%.
Клинический спектр урогенитальных ХИ включает в себя уретриты, проктиты, цервициты, эпидидимиты, воспалительные заболевания органов малого таза. По данным клиники им. Гельмгольца (Москва), за последние 5 лет от 10 до 30 % от общего числа конъюнктивитов - паратрахомного происхождения. Возрастает частота болезни Рейтера у детей, атипичных пневмоний. В настоящее время насчитывается более 20 нозологических форм, связанных с ХИ. Использование современных методов диагностики позволяет выявить хламидии у каждой второй женщины с хроническим воспалением урогенитальной сферы, у 57% женщин, страдающих бесплодием, у 87% женщин с невынашиванием беременности. Частота ХИ при трубном бесплодии составляет 41 - 51%. Большую роль ХИ играет в развитии фоновых и предраковых заболеваний шейки матки. 50% случаев внематочной беременности, являющейся основной причиной смерти в I триместре беременности среди чернокожих женщин (по данным ВОЗ), - результат осложнений, связанных с УХ. Вовремя не диагностированная и не леченная инфекция у беременных приводит к заражению новорожденных. По данным различных авторов, у 20 - 30% новорожденных развивается конъюнктивит, а у 10 - 20% - пневмония. По данным экспертов ВОЗ (1993 г.), 40 - 50% детей, рожденных от матерей с хламидийным цервицитом, имеют те или иные клинические признаки ХИ. Это свидетельствует о том, что ХИ является "семейным заболеванием", передающимся не только половым путем. УХ у женщин характеризуется рядом особенностей, определяющих клиническое течение и тактику лечения: преобладание латентных, асимптомных форм течения (85 - 70%) и большое количество смешанных форм (сочетание с гарднереллезом встречается в 14 - 24% случаев, с кандидозом - в 13 - 15%, с трихомониазом - в 5 - 10%, с гонореей - в 3 - 5%, с вирусом простого герпеса - в 18 - 20% случаев).
В настоящее время известны 3 вида хламидий: Chlamydia psittaci, преобладающая у животных, особенно распространена у птиц, поражает человека только случайно; Chlamidia pneumoniae, вызывающая у взрослых пневмонии, и наиболее важная группа, встречающаяся только у человека - Chlamidia trachomadis (СТ), в которой известно много серотипов, вызывающих у человека совершенно различные картины болезни. Среди СТ различают серотипы от А до С, которые являются возбудителями трахомы. Серотипы L1, 2, 3 характеризуются размножением прежде всего в лимфатической ткани и являются возбудителями тропической венерической болезни lymphogranulema venereum. Инфицирование СТ серотипов от D до К происходит при половом контакте, новорожденный заражается от матери при родах.
Хламидии являются облигатными внутриклеточными паразитами и имеют вид мелких грамотрицательных кокков. Это очень маленькие (диаметром 0,2 - 0,15 мкм) неподвижные сферические паразитические микроорганизмы, которые напоминают бактерии, но, как и вирусы, неспособные к размножению вне клетки хозяина. Жизнедеятельность хламидий осуществляется за счет двух стадий жизненного цикла: инфекционных внеклеточных форм и неинфекционных внутриклеточных форм. Элементарные (инфекционные) тельца инфицируют главным образом клетки цилиндрического эпителия, после чего реструктурируются с образованием метаболически активных ретикулярных телец и, пройдя стадию промежуточных форм, замещаются элементарными тельцами. Полный цикл репродукции хламидий равен 48 - 72 ч.
Клинические проявления хламидиоза
Как и при других заболеваниях мочеполовых органов, различают свежий (острый, подострый, торпидный) и хронический хламидиоз. Поскольку инкубационный период при хламидиозе колеблется от 15 до 35 дней, острые формы заболевания встречаются только как казуистика. Значительно чаще встречаются подострые и торпидные формы, около 75% составляют хронические формы.
Приблизительно в 80% случаев на начальных этапах хламидиоз протекает бессимптомно. Отсутствие клинических симптомов заболевания лишь указывает на временное равновесие между паразитом и хозяином в условиях, ограничивающих размножение паразита, но не препятствующих ему. ХИ с клинически бессимптомным течением является не менее опасной, чем ее манифестные формы, и обязательно требует проведения лечебных и профилактических мероприятий, воздействующих на возбудителя и повышающих защитные силы организма.
По топографии поражения можно выделить хламидийное поражение нижнего отдела урогенитального тракта и восходящую ХИ.
К поражениям нижнего отдела урогенитального тракта можно отнести хламидийный уретрит, парауретрит, бартолинит, кольпит, эндоцервицит.
Хламидийные уретриты не имеют специфических проявлений, и больные редко предъявляют жалобы на дизурию.
Первичные кольпиты при ХИ встречаются редко. Это связано с тем, что хламидии у взрослых неспособны размножаться в многослойном плоском эпителии, а вне клетки они высокочувствительны к кислой реакции влагалища.
Первичные хламидийные кольпиты возможны лишь в случаях значительно измененной гормональной активности, в частности, у пожилых женщин, беременных и девочек.
Цервициты наблюдаются как первичное и наиболее частое проявление ХИ.
гематогенно, о чем свидетельствует наличие экстрагенитальных очагов (глотка - хламидийный фарингит, суставные сумки - артрит);
"Восходящая ХИ" - поражение слизистой оболочки матки, труб, яичников, брюшины. Описаны осложнения в форме перигепатита (синдром Фитц-Хью - Куртиса), периколита и периаппендицита.
Хотелось бы еще раз подчеркнуть, что поскольку в 80% случаев УХ протекает мало- или асимптомно, к наиболее частым осложнениям хламидийного процесса относятся хламидийный сальпингит и перисальпингит, следствием которых является трубное бесплодие.
В рекомендациях Центрального научно-исследовательского кожно-венерологического института от 1996 г. предлагается использовать термин "семейный хламидиоз"[3]. Примерно 30 - 35% детей в семьях, где родители больны УХ, также поражены этим заболеванием, причем в 7% случаев это экстрагенитальные формы (конъюнктивиты, артриты и т. д. ). Заражение детей происходит либо при прохождении через родовые пути, либо бытовым путем при использовании предметов туалета (полотенце, мочалка).
Малосимптомное течение приводит к поздней обращаемости уже при наличии сформированного патологического процесса. Авторами подчеркивается мысль о возможности развития впоследствии бесплодия у детей вследствие рубцовых изменений фаллопиевых труб у девочек и перенесенного хламидийного орхоэпидидимита у мальчиков.
Учитывая клинические особенности течения хламидиоза, тяжелые последствия несвоевременного и неправильно проводимого лечения, особую важность приобретают лабораторные методы диагностики этой инфекции.
больные с воспалительными заболеваниями гениталий, особенно с наличием поражения шейки матки (цервициты, эрозии и т. д. );
беременные с отягощенным акушерским анамнезом (неразвивающаяся беременность, самопроизвольные выкидыши, преждевременные роды, рождение детей с низкой массой тела, многоводие) и с осложненным течением данной беременности - угроза прерывания, многоводие, плацентит и т. д.
В Германии, например, с 1 апреля 1995 г. обследование на хламидиоз включено в программу обследования всех беременных. При этом важно подчеркнуть, что исследования на хламидии надо проводить независимо от картины влагалищного мазка и наличия сопутствующей условно-патогенной флоры в половых путях, так как доказано, что в 80% случаев генитальный хламидиоз протекает при нормальной картине влагалищного мазка.
Существующие методы диагностики хламидиоза можно разделить на три группы: цитологические, выделение хламидий на культуре тканей и серологические. Неоднократно проводился сравнительный анализ диагностической ценности этих методов.
Наиболее чувствительным и специфичным оказался метод выделения хламидий на культуре тканей ("золотой стандарт"). Однако в силу трудоемкости, высокой стоимости и необходимости большого времени для постановки реакции этот метод в настоящее время применяется ограниченно.
Цитологический метод диагностики - это бактериоскопия соскобов со слизистых после их окраски по Романовскому - Гимзе или раствором Люголя. По данным разных авторов, этот метод позволяет идентифицировать хламидийные включения лишь в 40 - 60% случаев, результат зависит от опыта исследователя и требуется много времени на просмотр каждого препарата.
Наиболее объективными методами диагностики хламидиоза являются серологические методы: метод гибридизации ДНК, полимеразная цепная реакция (ПЦР), иммуноферментный анализ, методы прямой и непрямой иммунофлюоресценции с использованием отечественных (Хламислайд, Хламискан, Хламимоноскрин) и импортных (Микротран, Хламиген, США; Хламисет, Финляндия) и др. тест-систем.
Все хламидии имеют общий групповой антиген, что используется при диагностике хламидиоза иммунофлюоресцентными методами.
Отмечено, что чувствительность ПЦР в 5 - 10 раз выше чувствительности метода прямой иммунофлюоресценции.
Очень важным для диагностики хламидиоза является правильное взятие материала для исследования.
Больные не должны принимать антибиотики тетрациклинового ряда в течение 3 - 4 нед до исследования. Перед взятием материала больные не должны мочиться в течение 1 - 1, 5 ч.
При взятии материала следует помнить, что хламидии в основном персистируют в цилиндрическом эпителии мочеполовых путей (передняя уретра на глубине 2,5 - 4 см у мужчин и слизистая цервикального канала на глубине 1,5 см у женщин). При взятии материала из цервикального канала ключевым моментом является удаление слизистой пробки, которую удаляют ватным тампоном и пинцетом, а затем берут материал. Преимущество имеет взятие материала щеточкой фирмы "Rovers" (Голландия), так как для получения репрезентативного результата важно присутствие в соскобе клеток со всей поверхности шейки матки, цервикального канала, зоны трансформации .
Наиболее точно диагноз УХ можно поставить путем сопоставления данных о наличии возбудителя в соскобах тканей из очагов поражения и обнаружения антител в крови. Так, в исследованиях П. А. Мэрд [4] указывается, что диагноз хламидийного сальпингита может быть поставлен при наличии антихламидийных антител в титре 1:256 или при 4-кратном увеличении титра антихламидийных IgG-антител в парных сыворотках. По результатам серологического скрининга, проведенного в СССР и Франции, авторы делают вывод о том, что диагностировать заболевание можно и при выявлении антихламидийных антител в разведении 1:128.
При лечении УХ приходится сталкиваться со многими проблемами. Это и полимикробная этиология симптомокомплекса, и высокая частота рецидивов (по данным разных авторов, она колеблется от 2 до 30%), и наличие резистентных форм хламидий к существующим препаратам, и особенности состояния иммунитета больных.
Поскольку хламидия - внутриклеточный паразит, то выбор препаратов, активных в отношении этого микроорганизма, ограничивается только теми, которые накапливаются внутриклеточно.
При лечении УХ используются следующие группы препаратов : тетрациклины, макролиды, фторхинолоны.
Группа тетрациклинов. Тетрациклин при свежем неосложненном хламидиозе назначают по 500 мг после еды 4 раза в сутки в течение 7 дней, при остальных формах продолжительность лечения составляет 14 - 21 день.
Доксициклин при свежем неосложненном хламидиозе назначают по 100 мг после еды 2 раза в сутки в течение 7 дней, при остальных формах - в течение 14 - 21 дня.
Препараты данной группы противопоказаны при беременности.
Эритромицин применяют начиная с второй половины беременности в дозе 500 мг 4 раза в сутки в течение 14 дней. Небеременным женщинам в острой фазе назначают эритромицин по 500 мг каждые 6 ч в течение 7 - 10 дней. Курсовая доза - 12 г.
Рокситромицин назначают по 0,15 г за 15 мин до еды 2 раза в день в течение 10 дней.
Джозамицин назначают по 500 мг 2 раза в сутки в течение 10 - 14 дней. В настоящее время проводятся исследования по применению джозамицина у беременных.
Азитромицин является кислотоустойчивым, усваивается при пероральном применении, способен достигать высоких концентраций в тканях, особенно воспаленных, и сохраняться в них в терапевтических концентрациях в течение нескольких суток. Азитромицин оказался первым антибиотиком, который после однократного приема излечивает ХИ, однако это касается лишь острых свежих процессов. Исследования показали неприемлемость одноразового лечения при длительно существующей ХИ.
Рекомендуется следующая схема лечения: 1-й день - 1 г, в последующие - по 500 мг/сут в течение 5 дней или по 250 мг в течение 9 дней. В многочисленных исследованиях отмечена хорошая переносимость препарата, побочные явления возникают редко.
Группа фторхинолонов. Фторхинолоны являются синтетическими антибактериальными препаратами с широким спектром действия, характеризуются высокой биологической доступностью и длительным периодом полувыведения, что позволяет назначать их 1 - 2 раза в сутки, эффективны при гонорее, хламидиозе, уреаплазмозе.
Рекомендуются следующие схемы лечения этими препаратами: пефлоксацин - по 0, 6 г 1 раз в сутки в течение 14 дней, на курс 8,4 г, или по 400 мг во время еды 2 раза в сутки в течение 10 дней; ломефлоксацин - по 0,6 г 1 раз в сутки, на курс 8,4 г; ципрофлоксацин - по 500 мг 2 раза в сутки в течение 12 дней; офлоксацин - по 200 мг 2 раза в сутки в течение 15 дней.
При лечении УХ необходимо помнить, что моноинфекция встречается лишь в 20 - 25% случаев, в остальных случаях имеют место сочетания с гарднереллезом, уреаплазмозом, кандидозом, трихомониазом.
Учитывая это обстоятельство, имеет смысл в схему лечения УХ добавлять метронидазол и противомикотические препараты.
При хронической хламидийной инфекции значительно изменяется иммуннитет. Во многих исследованиях было показано, что при данной инфекции иммунная система функционирует неадекватно, ответ формируется поздно и над защитными реакциями преобладают иммунопатологические. Однако повсеместное, широкое и бесконтрольное применение иммуномодуляторов не показано, особенно при отсутствии тщательного динамического контроля за состоянием иммунной системы.
При хронической форме УХ целесообразно назначение препаратов, воздействующих на неспецифическую реактивность организма, активизирующих репаративно-восстановительные процессы (экстракт алоэ, ФИБС, стекловидное тело, трипсин, рибонуклеаза, витамины группы В, фолиевая кислота, аскорбиновая кислота). Препараты назначают в обычных терапевтических дозах.
Рекомендуется применение протеолитических ферментов: ораза - внутрь по 1 чайной ложке 3 раза в день во время еды в течение всего курса антибактериальной терапии, вагинально вводится несколько гранул оразы в свечах "Апилак"; химотрипсин - внутримышечно по 5 - 10 мг 1 - 2 раза в день в течение 10 дней. Уретру, цервикальный канал и влагалище обрабатывают 5 % раствором химотрипсина, всего 10 - 15 процедур; химопсин используется только местно, 25 мг препарата растворяют в 10 - 25 мл воды или изотонического раствора, инстиллируют в уретру, обрабатывают цервикальный канал, во влагалище на 2 ч вводят тампон, который потом больная самостоятельно удаляет.
При отсутствии противопоказаний (гипертоническая болезнь, нарушения сердечно-сосудистой деятельности, гиперкинезы) при проведении антибиотикотерапии показано применение адаптогенов: сапарал - внутрь после еды по 0,05 г (1 таблетка) 2 - 3 раза в день; экстракт элеутерококка жидкий - по 20 - 30 капель за полчаса до еды 2 - 3 раза в день; настойка аралии - по 30 - 40 капель за полчаса до еды 2 - 3 раза в день; пантокрин - по 30 - 40 капель или 1 - 2 таблетки за полчаса до еды 2 - 3 раза в день; экстракт левзеи - по 30 капель за полчаса до еды 2 - 3 раза в день; настойка лимонника - по 20 - 30 капель 2 - 3 раза в день за полчаса до еды; настойка женьшеня - по 20 капель 2 - 3 раза в день за полчаса до еды.
С целью восстановления микробиоценоза влагалища и коррекции местного иммунитета рекомендуются эубиотики - бифидумбактерин, ацилакт - в свечах для вагинального и ректального применения.
В связи с изложенным необходимо проводить обязательное контрольное обследование больных через 4 нед и через 3 мес после проведения терапии.
Профилактика осложнений ХИ привлекает особое внимание, так как больные, у которых отсутствуют симптомы, не обращаются за помощью.
Профилактика хламидиоза успешно осуществляется в Норвегии и Дании, где отмечена тенденция к уменьшению частоты заболевания хламидиозом. Профилактика хламидиоза в этих странах включает следующие основные меры: создание сети диагностических лабораторий по всей стране; обязательное обследование женщин до 25 лет 1 - 2 раза в год; обязательное обследование женщин после прерывания беременности; бесплатное лечение хламидиоза; повышение моральной ответственности партнеров за распространение ХИ.
1. Машкиллейсон А.Л., Гомберг М.А. Конгресс Международного союза по венерическим заболеваниям и трепонематозам 1995. – Вестн. дерматологии. – 1995. – №6. – C. 57–60.
2. Машкиллейсон, Гомберг М.А., Соловьев А.М. К проблеме урогенитального хламидиоза. Заболевания, передающиеся половым путем. – 1995. – №5. – С. 28–33.
3. Хламидиоз. Клиника, диагностика, лечение. // Методические рекомендации. – М., – 1996. – С. 20.
4. Мэрд П.А. Репродуктивное здоровье. // Под ред. Л.Г. Кейта и др. – М. – 1988. – Т. 1. – С. 354–65.
Прилепская В.Н., Абуд И.Ю.
В. Н. Прилепская - проф., д.м.н., зав. поликлиническим отделом
И. Ю. Абуд - врач отделения, к. м. н. Научный центр акушерства, гинекологии и перинатологии (директор - академик РАМН проф. В.И. Кулаков), РАМН, Москва
Что такое цервицит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Батаршиной О. И., гинеколога со стажем в 18 лет.
Над статьей доктора Батаршиной О. И. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Цервицит — это воспалительное заболевание шейки матки, которое развивается под влиянием различных агентов (как инфекционных, так и неинфекционных) [2] .
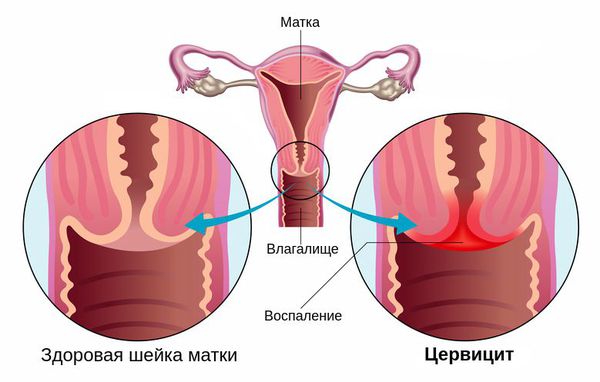
Распространённость цервицита у женщин достигает 10-45 %. Наиболее часто его вызывают возбудители, передаваемые половым путём, такие как гонокок, хламидия, трихомонада, вирус герпеса, бледная трепонема и др. [7] [8] [11] . Также причиной возникновения цервицита являются различные заболевания, аллергические реакции на противозачаточные спермициды, латекс в составе презервативов или продукты женской гигиены, такие как мыла, гели для душа или дезодоранты.
Длительный и вялотекущий дисбиоз влагалища (бактериальный вагиноз) также рассматривается как одна из возможных причин цервицита, поскольку на фоне изменения уровня кислотности влагалища меняется и соотношение видов влагалищной микрофлоры.
В зоне риска по возникновению цервицита находятся женщины, которые:
Также доказано, что фоном для развития воспаления шейки матки и его хронизации является местный иммунодефицит, связанный с нарушением защитной функции слизистой оболочки.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цервицита
Возможно как симптомное, так и бессимптомное течение заболевания [31] .
При бессимптомном процессе диагноз "цервицит" может быть поставлен:
- при неудовлетворительных результатах мазков — повышенном уровне лейкоцитов (клеток крови, отвечающих за иммунный ответ на внедрение инфекционных агентов);
- на основан ии визуального осмотра шейки матки врачом-гинекологом — покраснения и отёка шейки матки.
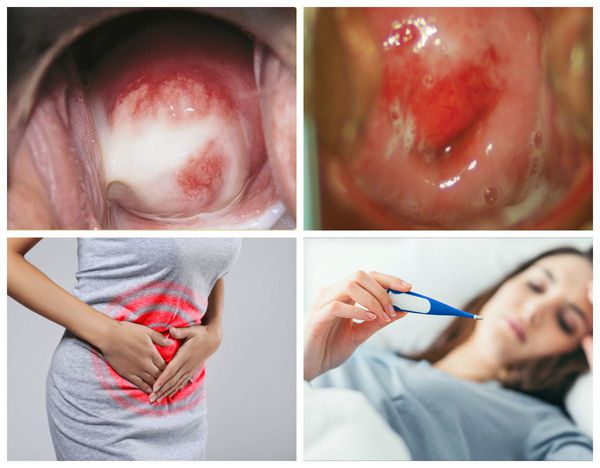
При симптомном течении заболевания женщину могут беспокоить:
- сероватые или бледно-жёлтые выделения из влагалища;
- аномальные кровянистые выделения во время или после полового контакта, а также в перерывах между менструациями [31] ;
- боль во время секса;
- затруднённое, болезненное или частое мочеиспускание;
- тазовая боль или, в редких случаях, лихорадка.
Патогенез цервицита
Когда речь идет о патогенезе цервицита, прежде всего необходимо обозначить понятия, о которых пойдёт речь.
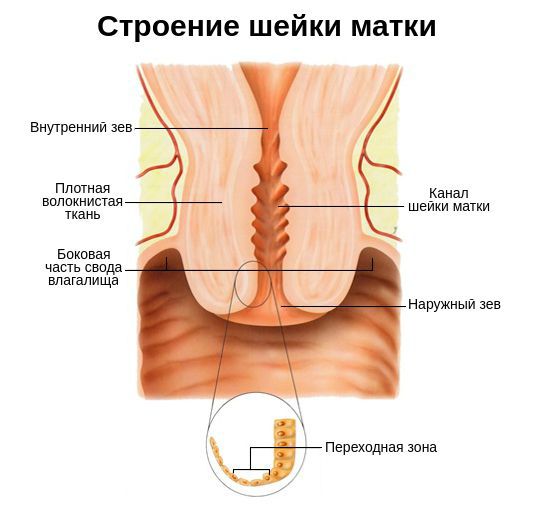
Шейка матки представляет собой гладкомышечный орган длиной 2-3 см, образованный соединительной тканью. Основная функция данной части матки — барьерная. Она реализуется за счёт секрета (выделений) слизистой , которая препятствует попаданию патогенных возбудителей в матку, маточные трубы и малый таз. В состав секрета входят как иммуноглобулины всех классов ( IgG, IgM, IgA и др. ), так и вещества, обладающие высокой расщепляющей и бактерицидной активностью.
Также шейку матки защищает микрофлора влагалища . Она состоит из анаэробных и аэробных бактерий, причём первых в десять раз больше, чем вторых. Такое соотношение создаёт определённый уровень кислотности слизистой, который не позволяет патогенным микроорганизмам внедряться в полость матки [8] .
Циклическое воздействие половых гормонов на женский организм позволяет сохранять микрофлору влагалища в норме, тем самым защищать шейку матки:
- в первой фазе менструального цикла под воздействием эстрогенов синтезируется гликоген, стимулируется выработка слизистого секрета, выполняющего барьерную функцию [4][17][27] ;
- во второй фазе цикла под воздействием прогестерона происходит подкисление среды влагалища и размножение лактобактерий.
При снижении барьерных свойств микрофлоры влагалища и слизистой шейки матки в организм женщины проникают различные патогенные возбудители, которые приводят к развитию цервицита. Их активному проникновению и распространению в полости малого таза способствуют сперматозоиды в качестве клеток-переносчиков инфекционных агентов, а также трихомонады и установка внутриматочной спирали на фоне воспалительного процесса.
Острый цервицит
Чаще возникает при поражении шейки матки специфическими возбудителями (например, гонококком), а также после искусственного прерывания беременности, в осложнённом послеродовом периоде (возбудителями чаще становятся стафилококковая и стрептококковая инфекции) и при вирусном поражении шейки матки. На ранней стадии заболевания возникают:
- полнокровие сосудов;
- повышение уровня лейкоцитов (лейкоцитарная инфильтрация);
- просачивание крови сквозь стенки сосудов в зону воспаления (экссудация);
- дистрофические изменения с вакуолизацией цитоплазмы и ядер клеток.
В результате дистрофических изменений клеток на поверхности слизистой оболочки шейки матки появляется гнойный и серозно-гнойный экссудат — сероватые или бледно-жёлтые выделения.
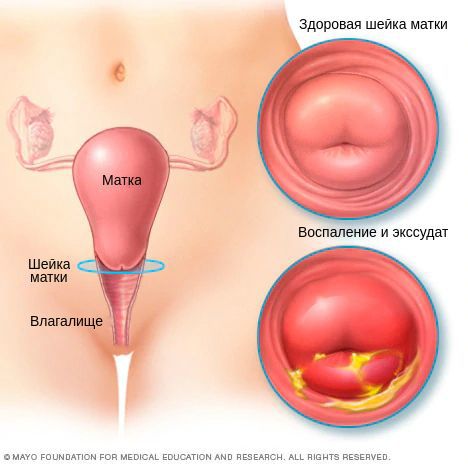
Хронический цервицит
При проникновении возбудителей в межклеточное пространство крипт шейки матки (небольших трубчатых углублений), труднодоступных для лечения, возникает хронический цервицит. Причиной хронизации заболевания нередко является поражение шейки матки хламидийной инфекцией. В 24-40 % случаев хронический цервицит возникает на фоне длительного и вялотекущего бактериального вагиноза. При осмотре гинекологом шейка матки выглядит покрасневшей, отёчной, легко травмируется. Микроскопически наблюдается инфильтрация подэпителиальной ткани лимфоцитами, плазмоцитами, полнокровие сосудов. Наряду с дистрофическими процессами в ткани преобладают процессы непрямого деления клеток, разрастания ткани и замещения одного вида клеток другим. Часто при хроническом цервиците нарушаются процессы ороговения клеток, что проявляется уплотнением тканей и изменением процесса гликогенизации клеток [6] [11] .
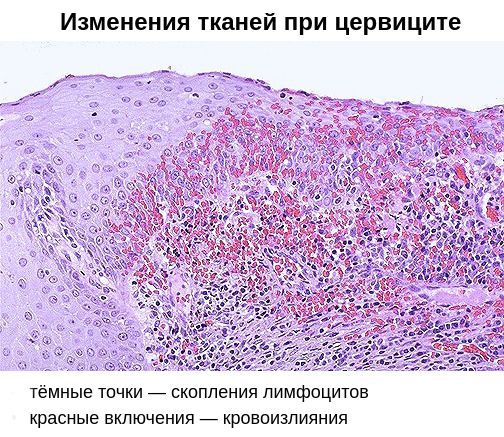
Помимо специфического возбудителя, немалую роль в возникновении хронического цервицита играет вторичный иммунодефицит. Он заключается в неполноценности клеточного и гуморального иммунитета. На клеточном уровне снижается количество Т- и В-лимфоцитов, а также нарушается фагоцитарная активности клеток, позволяющая им поглощать и переваривать патогенные микроорганизмы. В результате возбудители остаются в организме, снижается содержание антител IgG и IgM, увеличивается выработка антител IgA, что ведёт к изменению качества цервикальной слизи.
Послеродовой цервицит
Отдельно такую форму не выделяют, цервицит после родов ничем не отличается от обычного. Разница может быть лишь в лечении: не все антибиотики можно принимать при грудном вскармливании.
Классификация и стадии развития цервицита
Классификация цервицита зависит от типа возбудителей, локализации и давности патологических процессов. Так, в зависимости от типа возбудителя цервициты подразделяют на инфекционные и неинфекционные. Инфекционные цервициты бывают:
- гонококковыми;
- хламидийными;
- трихомонадными;
- кандидозными;
- вирусными.
Неинфекционные цервициты рассматриваются и классифицируется в зависимости от причины, вызвавшей воспаление. Они бывают аллергическими, атрофическими (сенильными) и др. [8] .
Кроме того, по локализации цервицит подразделяют на:
- экзоцервицит — протекает преимущественно на поверхности шейки матки;
- эндоцервицит — в основном затрагивает эпителий канала шейки матки (цервикальный канал).
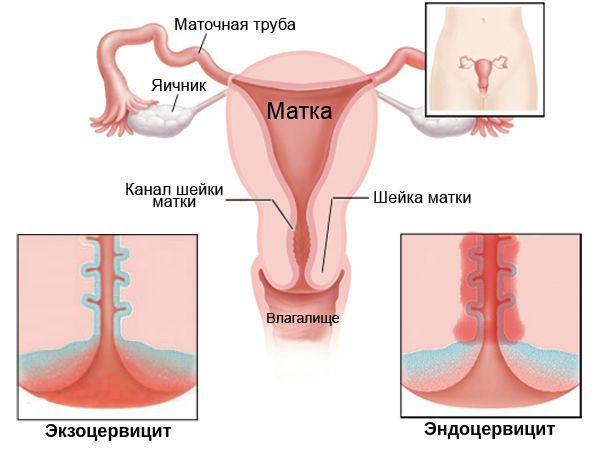
По длительности протекания процесса цервицит может быть:
- острым — процесс воспаления длится не более шести недель;
- хроническим — болезнь протекает с периодическими ремиссиями и обострениями.
Осложнения цервицита
Выявление причины цервицита имеет важное значение, поскольку при наличии инфекционного агента возбудитель способен распространяться за пределы шейк и матки и вызывать эндометрит , а также воспаление в теле матки, маточных трубах и малом тазе. В ряде случаев это приводит к бесплодию или препятствует вынашиванию плода [25] [27] .
Цервицит и беременность
Если беременность возникла на фоне цервицита, возбудитель заболевания может привести к преждевременному прерыванию беременности в связи с проникновением инфекции в водную оболочку, обращённую к плоду, затем в хорион (плаценту), околоплодные воды и сам плод.
При инфицировании ребёнка на ранних сроках беременности могут сформироваться врождённые пороки развития, возникает риск первичной плацентарной недостаточности и внутриутробной гибели плода. При позднем инфицировании наблюдаются следующие осложнения беременности:
- внутриутробная задержка развития плода;
- вторичная плацентарная недостаточность (часто на фоне плацентита — воспаления плаценты);
- локальные и генерализованные (распространённые) инфекционные поражения плода.
Генерализованные формы внутриутробной инфекции чаще развиваются в первом триместре беременности, так как плод ещё не может препятствовать распространению воспалительного процесса. В третьем триместре воспалительные изменения вызывают сужение или обтурацию (закрытие просвета) каналов и отверстий, что ведёт к аномальному развитию уже сформировавшегося органа — псевдоуродствам ( гидроцефалии , гидронефрозу и др.) [29] .
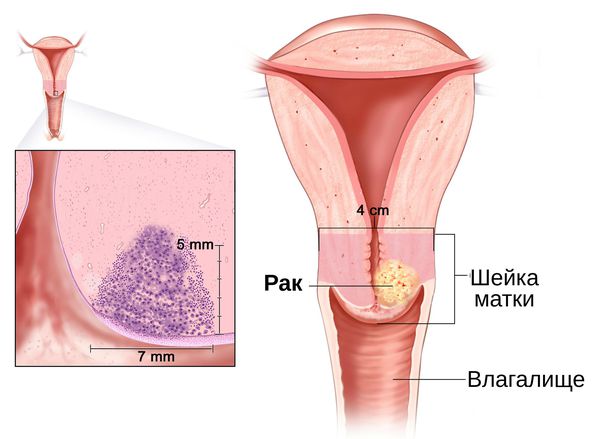
Длительное воспаление шейки матки становится фоном для развития злокачественных процессов . Это связано с нарушением регенерации слизистой оболочки шейки матки, которое наблюдается при хроническом цервиците. Наиболее значимыми факторами, влияющими на регенерацию, являются вирусы и хламидии [10] . Учёные доказали, что формирование рака шейки матки происходит только на фоне сохранившейся в криптах вирусной инфекции, которая активируется более чем через год после первичного обнаружения возбудителя [30] .
Диагностика цервицита
Диагностическими критериями цервицита при осмотре в зеркалах являются:
- покраснение слизистой, отёк;
- обильные выделения грязно-серого или зеленоватого цвета;
- творожистое отделяемое (при грибковом поражении шейки матки и влагалища).
При микроскопическом исследовании наблюдается увеличение количества лейкоцитов, также можно обнаружить возбудителей трихомониаза и гонореи.
Однозначными признаками цервицита при вульвоцервикоскопии служат:
- фолликулярный кольпит, "лунный ландшафт" — для хламидиоза;
- очаговый кольпит — для трихомониаза;
- диффузный кольпит — для неспецифической бактериальной инфекции;
- симптом "манной крупы" — для герпетической инфекции [17] .
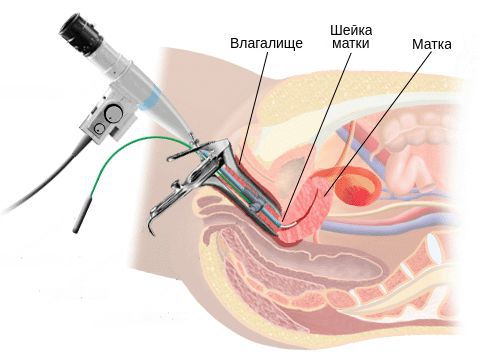
Бактериологическое исследование с поверхности шейки матки и заднего свода влагалища позволяет оценить не только соотношение лактофлоры, создающей нормальную кислотность влагалища, но и выявить рост условно-патогенных возбудител ей, таких как кишечные палочки, стрептококки, стафилококки, анаэробные кокки и др. Причём клинически значимым является рост микроорганизмов в колич естве более чем 10 4 КОЕ/мл.
ПЦР-диагностика позволяет обнаружить специфических возбудителей, вызвавших воспалительный процесс, таких как микоплаз мы, уреаплазмы, гарднереллы, хламидии, вирус герпеса и др. [31] . Для этого исследования врач-гинеколог должен взять мазок из шейки матки.
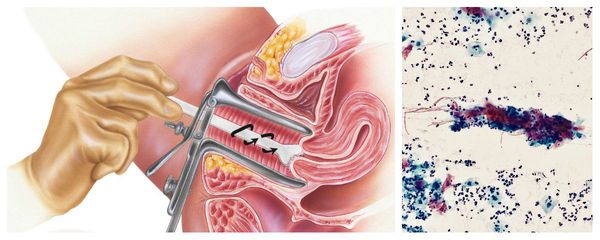
Цитологическое исследование клеточного материала позволяет оценить структуру клеток, характер и уровень их повреждения, а также эффективность лечения в динамике. При длительно текущем воспалении шейки матки в цитограмме преобладают гистиоциты, плазмациты, фибробласты и лимфоидные элементы. При продуктивном воспалении (защитной реакции организма) преобладают клеточные инфильтраты — макрофагальные, г игантоклеточные, плазмоклеточные, лимфоцитарно-моноцитарные. В 40 % случаев цитологическая диагностика позволяет выявить возбудителя заболевания (хламидии, кандиды, трихомонады, цитомегаловирус), более чем в 50 % случаев диагностируется папилломавирус и вирус простого герпеса.
При ультразвуковом исследовании признаками эндоцервицита являются увеличение толщины М-эхо шейки матки более 4 мм и реактивный отёк подэпителиальных о тделов УЗИ. рекомендуется выполнять на 5-7 день менструального цикла.
Следует помнить, что обследование гинекологом и взятие мазков проводятся перед началом менструации или через несколько дней после её окончания: оптимальный срок — пятый день, когда нет мажущих кровянистых выделений. Накануне и в день процедуры не следует использовать вагинальные свечи, тампоны, мази, средства интимной гигиены, поскольку это может стать причиной получения недостоверных данных. Кроме того, необходимо отказаться от спринцевания и воздержаться от половых контактов в течение одного-двух дней до сдачи анализа.
Лечение цервицита
Препараты для лечения цервицита
Определяющим звеном при выборе тактики лечения является природа возбудителя цервицита: вирусные воспаления шейки матки предполагают использование противовирусных препаратов, бактериальные воспаления — приём антибактериальных средств. При этом важно учитывать чувствительность выявленных инфекционных агентов к антибиотикам [1] [2] [3] .
Главной проблемой лечения цервицита шейки матки являются наличие нескольких возбудителей (микст-инфекции) и устойчивость возбудителей к антибактериальным препаратам. В таких случаях необходимо прибегнуть к приёму комбинации антибиотиков. Конкретные препараты назначает врач.
Иногда антибиотикотерапия сопровождается назначением фитопрепаратов, биологически активных добавок. Также рекомендуются общеукрепляющие физические нагрузки, нормализация режима труда и отдыха [9] [24] .
Помимо лечения пациентки параллельно в обязательном порядке проводится лечение её полового партнёра. Во время терапии необходимо пользоваться барьерной контрацепцией.
Нормали зация микробиоценоза влагалища с помощью пробиотиков [15] в сочетании с иммунокоррекцией (с учётом данных иммунограммы) [5] [16] [19] также целесообразны, поскольку изменённый уровень кислотности среды и возникающий дефицит иммунных факторов способствуют частым рецидивам воспалительного процесса [40] [43] [44] .
Физиотерапия
Кроме того, в ряде случаев назначается физиолечение:
- ДМВ-терапия — лечение дециметровыми волнами частотой от 300 МГц до 3 ГГц, проводится каждый день, предполагает 10-15 процедур продолжительностью 10 минут;
- магнитотерапия — воздействие магнитного поля низкой или высокой частоты, проводится каждый день, предполагает 10-20 процедур продолжительностью 10-20 минут;
- диадинамотерапия — лечение высокочастотным электрическим током, проводится каждый день до появления ощущения болезненной вибрации, предполагает 12-15 процедур;
- СМТ-терапия — лечение низкочастотным электрическим током, проводится каждый день, предполагает 12-15 процедур;
- электрофорез с солями магния — воздействует на область малого таза, проводится каждый день, предполагает 10-15 процедур продолжительностью 20 минут;
- дарсонвализация и лазеротерапия с использованием влагалищных датчиков — проводятся каждый день, предполагает 10-12 процедур [32] .
Деструктивные методы лечения цервицита
Цервицит — это воспалительный процесс, поэтому его лечат медикаментозно. Физические или химические методы применяются при атипии в клетках, покрывающих шейку матки или выстилающих цервикальный канал. Прижигание кислотами, жидким азотом, лазерная вапоризация, аргоноплазменная абляция, электрохирургическая эксцизия для лечения цервицита не используются .
Прогноз. Профилактика
Прогноз заболевания при своевременно начатом лечении благоприятный. При бессимптомном цервиците и отсутствии инфекций, передаваемых половым путём, у пациенток остаётся риск появления выраженных клинических признаков заболевания [30] .
Помимо основного лечения назначаются консультации других специалистов для коррекции различных нарушений (нейроэндокринных, гормональных, иммунных), выявления соматических заболеваний и факторов риска. Это позволит предотвратить повторное развитие цервицита [28] .
С целью профилактики воспаления шейки матки рекомендуется:
- один раз в шесть месяцев посещать гинеколога;
- использовать барьерные средства контрацепции;
- не допускать хронизации заболеваний мочеполовой системы.
Рассмотрен цервицит у женщин, развивающийся вследствие симптомной урогенитальной хламидийной инфекции, подходы к диагностике урогенитальной хламидийной инфекции у женщин. Приведены современные международные и российские рекомендации по лечению хламидийной
Chlamydia infection in gynecology and midwifery: the tactics of conducting patients in accordance with the contemporary recommendations in Russia and abroad
Cervicitis Is examined in women, developing as a result of the symptomal uro genital chlamydia infection, approaches to diagnostics of uro genital chlamydia infection in women. Contemporary international and Russian recommendations regarding treatment of chlamydia infection in midwifery and gynaecology are also provided.
При развитии симптомной урогенитальной хламидийной инфекции у женщин чаще всего возникает цервицит. В случае бессимптомного течения нелеченная хламидийная инфекция может привести к поражению верхних отделов генитального тракта и возникновению воспалительных заболеваний органов малого таза (ВЗОМТ). Ежегодно в США диагностируется около 750 000 случаев ВЗОМТ [11]. Как клинически диагностированные случаи ВЗОМТ, так и субклинические варианты поражения органов малого таза могут привести к фиброзу, образованию рубцов и нарушению проходимости маточных труб, что нередко является причиной серьезных нарушений репродуктивной функции, включая трубное бесплодие, эктопическую беременность и развитие синдрома хронической тазовой боли [3].
Около 10–15% нелеченных случаев хламидийной инфекции приводят к клинически диагностируемым случаям ВЗОМТ, из которых 15% могут привести к развитию трубного бесплодия [12, 13]. Доля трубного бесплодия среди всех других видов бесплодия варьирует от 10% до 40% [14, 15]. Хламидийная инфекция является лидирующей предотвращаемой причиной трубного бесплодия [14]. Прямые медицинские затраты на хламидийную инфекцию, включая диагностику и лечение бесплодия, вызванного хламидийной инфекцией, составляют 701 млн долларов ежегодно (2010 г.) [3].
Что касается хламидийной инфекции у беременных, то, по данным ВОЗ, частота обнаружения C. trachomatis у беременных колеблется в очень широких пределах (от 2% до 37%), в среднем составляя 6–8% и достигая 70% у пациенток с хроническими ВЗОМТ и отягощенным акушерско-гинекологическим анамнезом [16–18). Ежегодно в США у 100 000 беременных женщин диагностируется хламидийная инфекция [19].
Данные о влиянии хламидийной инфекции на течение и исход беременности неоднозначны. Результаты ряда исследований свидетельствуют о том, что наличие хламидийной инфекции половых путей у матери может приводить к повышению частоты случаев невынашивания беременности, мертворождения, преждевременных родов, преждевременного разрыва плодных оболочек, к развитию эндометрита и сальпингита в послеродовом периоде, а также к рождению детей с низкой массой тела [20–25]. Так, например, в ходе проспективного исследования, выполненного в США, показано, что инфицирование C. trachomatis во время беременности приводит к задержке внутриутробного развития плода, а также повышает риск преждевременных родов [23]. В других исследованиях связь хламидийной инфекции с неблагоприятными исходами беременности не была доказана [26].
С другой стороны, не подлежит сомнению, что урогенитальный хламидиоз у беременных является фактором риска развития хламидийной инфекции у новорожденных. Инфицирование происходит в 23–70% случаев, преимущественно во время родов при прохождении плода через инфицированные родовые пути. При этом у 11–50% детей, рожденных женщинами с хламидиозом, в первые две недели жизни развивается конъюнктивит, а у 3–16% на 1–3 месяц жизни хламидийная пневмония [26, 27].
Подходы к диагностике урогенитальной хламидийной инфекции у женщин
Диагноз урогенитальной хламидийной инфекции устанавливается на основании клинической картины заболевания и выявления C. trachomatis при проведении лабораторных исследований [28]. Как отмечено выше, наиболее частой клинической формой локализованной хламидийной инфекции у женщин является цервицит [6, 28]. Симптомы заболевания обычно возникают спустя 1–3 недели после инфицирования. Пациентки могут предъявлять жалобы на выделения из половых органов слизисто-гнойного характера, зуд, жжение, дискомфорт в области наружных половых органов, боль в нижней части живота, межменструальные или посткоитальные кровянистые выделения. При гинекологическом обследовании у пациенток с хламидийным цервицитом выявляются гиперемия и отечность в области наружного зева цервикального канала и слизисто-гнойные выделения, нередко — цирцинарная эрозия [6, 28]. Но — нельзя не подчеркнуть данный факт еще раз — у большинства пациенток с хламидийным цервицитом отмечается отсутствие субъективных симптомов заболевания [6, 28, 29].
К основным методам лабораторной диагностики хламидийной инфекции относятся:
- молекулярно-биологические методы (методы амплификации нуклеиновых кислот или ПЦР-диагностика);
- культуральное исследование;
- метод прямой иммунофлюоресценции.
Метод прямой иммунофлюоресценции (ПИФ) с моноклональными антителами отличается высокой степенью субъективной оценки результатов и низкой воспроизводимостью. Чувствительность и специфичность данного метода составляет не более 60–80%, что зависит от качества получения материала для исследования и квалификации персонала лаборатории [10, 28].
Современные международные и российские рекомендации по лечению хламидийной инфекции в акушерстве и гинекологии
В опубликованных в 2010 г. Рекомендациях по лечению заболеваний, передаваемым половым путем (Sexually Transmitted Diseases Treatment Guidelines), CDC [29] и Европейском руководстве по ведению пациентов с инфекцией, вызванной C. trachomatis (European guideline for the management of Chlamydia trachomatis infections) [6] основными препаратами в лечении хламидийной инфекции у небеременных пациенток являются азитромицин и доксициклин, у беременных женщин — азитромицин (табл. 1).
По данным метаанализа 12 рандомизированных исследований, в котором проводилось сравнение азитромицина и доксициклина в лечении урогенитальной хламидийной инфекции, оказалось, что сравниваемые режимы лечения эквивалентны по эффективности с достигнутой частотой эрадикации патогена, которая составила 97% и 98% соответственно [31].
Существенным преимуществом азитромицина в терапии урогенитального хламидиоза является возможность однократного приема внутрь 1 г препарата, что делает азитромицин наиболее целесообразным антибиотиком (в том числе и с экономической точки зрения) в лечении всех пациенток, особенно женщин с рискованным сексуальным поведением, недостаточной комплаентностью назначенному лечению или с невозможностью проведения оценки излеченности во время последующих визитов к врачу [29]. Как показали исследования, комплаентность лечения значительно выше в случае однократного применения азитромицина как пациентками, так и их партнерами [32–34].
Указанный в Рекомендациях CDC эритромицин рассматривается (по сравнению с азитромицином или доксициклином) как менее эффективный препарат, что, в первую очередь, связано с достаточно часто возникающими нежелательными явлениями со стороны ЖКТ, в значительной степени влияющими на комплаентность [29]. Левофлоксацин и офлоксацин являются эффективной альтернативной, однако не имеют преимуществ по режимам дозирования и длительности использования [29].
В российских схемах терапии хламидийной инфекции у небеременных пациенток, помимо азитромицина, доксициклина, эритромицина, левофлоксацина, офлоксацина и джозамицина, указаны и другие антибиотики (в частности, в Клинических рекомендациях Российского общества акушеров и гинекологов, 2009 г., указаны макролиды спирамицин, рокситромицин и кларитромицин, что не противоречит Европейскому руководству по ведению пациентов с инфекцией, вызванной C. trachomatis, а также ломефлоксацин, отсутствующий во всех других рекомендациях и протоколах ведения больных).
Кроме того, нельзя не остановиться на крайне широком диапазоне дозирования джозамицина и рекомендуемой длительности использования. По данным исследований, приведенным в табл. 3, дозирование джозамицина при урогенитальной хламидийной инфекции варьировало от 500 мг 2 раза в сутки до 500 мг 3 раза в сутки, длительность исследования — от 7 до 14–15 дней.
Что касается терапии хламидийной инфекции у беременных пациенток, то и в Рекомендациях по лечению заболеваний, передаваемым половым путем, CDC, 2010 г. и в Европейском руководстве по ведению пациентов с инфекцией, вызванной C. trachomatis, основным препаратом является азитромицин, также используются амоксициллин и эритромицин (табл. 1) [6, 29].
В настоящее время наиболее оптимальным препаратом для лечения урогенитального хламидиоза во время беременности представляется азитромицин. Первые сведения о возможности применения азитромицина при хламидийной инфекции у беременных были получены еще в 1996 г., когда в сравнительном исследовании было установлено, что по клинической и бактериологической эффективности при цервиците, вызванном C. trachomatis, азитромицин в дозе 1 г однократно не уступает эритромицину, назначаемому в дозе 500 мг 4 раза в сутки в течение 10 дней. Никаких различий между группами по исходам беременности выявлено не было [49].
Для подтверждения эффективности и безопасности применения азитромицина при лечении хламидийной инфекции во время беременности при поддержке CDC в США было инициировано ретроспективное когортное исследование. При анализе результатов лечения 277 беременных женщин с хламидийной инфекцией оказалось, что эффективность азитромицина в данной популяции составила 97%, амоксициллина — 95% и эритромицина — 64%. Таким образом, в данном исследовании эффективность азитромицина оказалась достоверно (p < 0,0001) выше, чем эритромицина. Различий в исходах беременности (как в отношении самих пациенток, так и их потомства) при лечении указанными препаратами выявлено не было [50].
На основании результатов данного исследования в 2006 г. впервые в Рекомендациях CDC по лечению ИППП азитромицин (1 г внутрь однократно), наряду с амоксициллином (по 500 мг 3 раза в сутки в течение 7 дней) стал рассматриваться в качестве препарата выбора для лечения хламидийной инфекции у беременных женщин [51].
По данным метаанализа 8 рандомизированных контролируемых исследований [52–59], сравнивавших эффективность и безопасность применения однократной дозы азитромицина (1 г) с эритромицином или амоксициллином при лечении хламидийной инфекции у беременных женщин [60], азитромицин по эффективности не уступал 7-дневным курсам лечения препаратами сравнения (отношение шансов 1,45 в популяции пациенток, пригодных для клинической оценки, n = 344). В то же время в сравнении с лечением эритромицином применение азитромицина сопровождалось достоверно меньшей частотой нежелательных реакций со стороны ЖКТ (отношение шансов 0,11), а также достоверно более редким преждевременным прекращением участия пациенток в исследовании (отношение шансов 0,12) и лучшей комплаентностью (отношение шансов 23,7) [60].
Перечисленный во всех рекомендациях эритромицин характеризуется достаточно высокой эффективностью при лечении урогенитального хламидиоза во время беременности (72–95%) [62, 60], однако у 30–50% пациенток [60] (а в одном исследовании у всех беременных женщин [59]) были отмечены нежелательные реакции со стороны ЖКТ, что нередко приводило к отказу от приема этого препарата. Амоксициллин отличается лучшей переносимостью (частота нежелательных реакций составляет 1,5–12,8%) и приемлемой эффективностью, которая по данным различных авторов варьирует от 58–80% [60] до 85–99% [63, 64]. В то же время необходимость длительного многократного приема эритромицина и амоксициллина может существенно снижать комплаентность пациенток [60]. Кроме того, по данным недавних исследований у эритромицина выявлено тератогенное действие — у детей, чьи матери принимали эритромицин на ранних сроках беременности (3546 детей), отмечался повышенный риск возникновения врожденных аномалий развития (отношение шансов 1,24). Увеличение риска было обусловлено повышением частоты возникновения аномалий сердечно-сосудистой системы (отношение шансов — 1,92). Кроме того, было выявлено повышение риска возникновения пилоростеноза у новорожденных, матери которых принимали эритромицин на ранних сроках беременности (относительный риск 3,0) [65].
Кроме этого, при рассмотрении аспекта дозирования джозамицина согласно Клиническим рекомендациям Российского общества акушеров и гинекологов, в которых рекомендуется применять препарат по 500 мг 2 раза в сутки на протяжении 12 дней, нельзя не упомянуть исследование, которое продемонстрировало достаточно высокую неэффективность (17%) при использовании именно этой схемы применения джозамицина [48].
Заключение
На настоящий момент согласно российским и зарубежным руководствам наиболее эффективными антимикробными препаратами, применяемыми для лечения урогенитальной хламидийной инфекции у небеременных пациенток являются азитромицин, применяемый в дозе 1 г внутрь однократно, и доксициклин, назначаемый 7-дневным курсом по 100 мг 2 раза в сутки. Что касается терапии беременных пациенток с данной патологией, то наиболее оптимальным препаратом с точки зрения безопасности и эффективности лечения, рекомендуемым и зарубежными, и российскими руководствами, является азитромицин.
Литература
За остальным списком литературы обращайтесь в редакцию.
А. А. Хрянин*, доктор медицинских наук, профессор
О. У. Стецюк**, кандидат медицинских наук
И. В. Андреева**, кандидат медицинских наук, доцент
* ГБОУ ВПО НГМУ Минздравсоцразвития России, Новосибирск
** НИИ антимикробной химиотерапии ГБОУ ВПО СГМА Минздравсоцразвития России, Смоленск
Урогенитальная хламидийная инфекция, по данным ВОЗ, является одной из самых распространенных инфекций, передаваемых половым путем. Особенности клинического течения (скудная симптоматика или ее полное отсутствие как у мужчин
Урогенитальная хламидийная инфекция, по данным ВОЗ, является одной из самых распространенных инфекций, передаваемых половым путем. Особенности клинического течения (скудная симптоматика или ее полное отсутствие как у мужчин, так и у женщин) и трудности лабораторной диагностики приводят к тому, что инфицированные лица обращаются к специалистам несвоевременно. Это затрудняет лечение и увеличивает риск развития осложнений.
Профессор А. Л. Машкиллейсон еще в 80-х гг. прошлого века указывал на необходимость выбора терапевтической тактики с учетом клинической формы хламидиоза. Это положение не потеряло своей актуальности до сегодняшнего дня. Современная классификация урогенитального хламидиоза, согласно МКБ-Х, подразумевает деление на хламидийную инфекцию нижних отделов (неосложненную) и инфекцию верхних отделов мочеполового тракта (осложненную). Терапевтический подход к лечению каждой из этих форм различается.
- наличие инфекции в организме (в течение многих месяцев и даже лет);
- многократное неэффективное лечение различными антибиотиками;
- иммунологические нарушения;
- высокие титры сывороточных и местно-секретируемых противохламидийных антител (в особенности IgA);
- возможное отсутствие хламидийной инфекции у половых партнеров больных хламидиозом, несмотря на половые контакты без использования презерватива.
Таким образом, терапевтические подходы к лечению урогенитального хламидиоза можно разделить на три основные группы:
1) лечение больных с хламидийной инфекцией нижних отделов урогенитального тракта;
2) лечение больных с хламидийной инфекцией верхних отделов урогенитального тракта;
3) лечение больных персистирующим и рецидивирующим урогенитальным хламидиозом.
Во всех этих изданиях для антибактериальной терапии хламидийной инфекции рекомендуются антибиотики следующих фармакологических групп: тетрациклины, макролиды и фторхинолоны. Ниже мы постараемся пояснить различия в терапевтических подходах к лечению различных форм урогенитальной хламидийной инфекции.
Лечение больных хламидийной инфекцией нижних отделов урогенитального тракта
При лечении этой формы инфекции, как правило, достаточно одной лишь антибактериальной терапии и нет необходимости в дополнительных терапевтических мероприятиях.
Антибиотики тетрациклинового ряда
Препараты тетрациклинового ряда — это основные лекарственные средства, применяемые для лечения больных хламидиозом. Согласно всем упоминавшимся выше рекомендациям, для лечения больных урогенитальным хламидиозом препаратом выбора является доксициклин. Он назначается в дозе 100 мг два раза в сутки не менее семи дней. Первая доза составляет 200 мг. Преимущество использования доксициклина в его достаточно высокой эффективности (по данным литературы, 95—100%) и относительно небольшой стоимости лечения. У больных хламидиозом можно использовать другие препараты этой группы: тетрациклин (препарат рекомендуется ФР в качестве альтернативного) — по 500 мг четыре раза в сутки 7—10 дней, метациклин — по 300 мг четыре раза в сутки 7—10 дней.
У доксициклина, по сравнению с тетрациклином, выше биодоступность, он имеет более длительный период полувыведения и лучше переносится. Кроме того, при использовании доксициклина, и в этом его отличие от других тетрациклинов, нет необходимости соблюдать диету, назначаемую из-за связывания тетрациклинов с ионами Са. Следует помнить, что все препараты тетрациклинового ряда противопоказаны при почечной недостаточности, беременности и для лечения детей до восьми лет. Наиболее частыми побочными эффектами при приеме лекарственных средств тетрациклинового ряда являются тошнота, рвота, диарея, аллергические реакции. В период лечения препаратами этой группы больным необходимо избегать инсоляции из-за возможности фотосенсибилизации.
Макролиды
К числу наиболее активных противохламидийных препаратов принадлежат макролиды. К препаратам выбора при лечении хламидиоза относят азитромицин. Высокая терапевтическая концентрация азитромицина в тканях достигается после однократного приема стандартной дозы антибиотика и сохраняется в местах воспаления не менее семи суток. ФР и другие руководства рекомендуют для лечения больных хламидиозом нижних отделов мочеполового тракта однократный прием 1,0 г азитромицина за 1 ч до еды или через 2 ч после.
В качестве альтернативных препаратов в ФР представлены: спирамицин который назначается по 3 млн МЕ три раза в сутки в течение 10 дней; рокситромицин — по 150 мг два раза в сутки 10 дней; эритромицин — по 500 мг четыре раза в сутки 10 дней. Также при лечении больных хламидийной инфекцией используют другие препараты группы макролидов: джозамицин — по 500 мг два раза в сутки 10 дней, кларитромицин — по 250 мг два раза в сутки 10 дней, мидекамицин — по 400 мг три раза в сутки 10 дней. Преимуществами всех современных макролидных антибиотиков перед эритромицином являются улучшенная фармакокинетика, хорошая переносимость и меньшая кратность приема.
При приеме макролидов могут наблюдаться побочные эффекты со стороны желудочно-кишечного тракта (тошнота, рвота, диарея) и печени (повышение активности трансаминаз, холестаз, желтуха). Разумеется, возможны и аллергические реакции.
Фторхинолоны
Следующую группу препаратов, обладающих противохламидийной активностью, составляют фторхинолоны. Препаратам той группы свойственна различная, в том числе и достаточно высокая, чтобы излечивать эту инфекцию, активность in vitro в отношении Chlamydia trachomatis. Однако единственным препаратом данной группы, который современные руководства рекомендуют для лечения хламидиоза, да и то в качестве альтернативного, является офлоксацин. Его назначают по 400 мг два раза в день в течение 10 дней. Преимуществом офлоксацина перед другими фторхинолонами можно считать его практически 100-процентную биодоступность.
Из других препаратов этой группы применяют пефлоксацин — по 400 мг два раза в сутки 10 дней и ломефлоксацин — по 400 мг один-два раза в сутки 10 дней.
Такие ограничения в использовании фторхинолонов для лечения хламидийной инфекции связаны с тем, что в сравнении с антибиотиками других вышеперечисленных групп после подобной терапии слишком высок процент рецидивов.
Показанием к использованию фторхинолонов при хламидиозе может быть смешанная гонорейно-хламидийная инфекция или сочетание Chlamydia trachomatis с другими микроорганизмами, демонстрирующими чувствительность к этим антибиотикам (требующая терапии сопутствующая кокковая или палочковая флора).
Группа фторхинолонов является сегодня одним из наиболее активно развивающихся классов противомикробных препаратов. Появляются все новые и новые поколения фторхинолонов. Хинолоны последних поколений (III и IV) превосходят предшествующие препараты этой группы по активности в отношении хламидий и кратности применения.
Препараты из группы фторхинолонов противопоказаны беременным и детям до 12 лет, больным с нарушением функции печени и почек. Из побочных реакций после приема фторхинолонов могут наблюдаться диспептические расстройства, тошнота, рвота, головокружение, аллергические реакции, тендиниты. Для всех препаратов этой группы, за исключением моксифлоксацина, характерен фотосенсибилизирующий эффект, о чем необходимо напоминать больному.
Лечение хламидиоза у беременных и новорожденных
В огромном числе наблюдений, проводившихся за почти 50 лет существования эритромицина, показана его безопасность, благодаря чему этот антибиотик можно считать едва ли не единственным лекарственным средством, разрешенным к применению у беременных и новорожденных.
По всем существующим сегодня рекомендациям, включая рекомендации ФР, беременным женщинам эритромицин назначают по 500 мг четыре раза в сутки 7 дней или по 250 мг четыре раза в сутки 14 дней. Для детей до 8 лет (с массой тела до 45 кг) разовая доза составляет 50 мг на 1 кг массы тела, кратность — каждые 6 ч в течение 10—14 дней. Детям старше 8 лет назначают такой же курс эритромицина, как и взрослым.
Достаточно высокой терапевтической эффективностью и лучшей, чем у эритромицина, переносимостью обладает еще один давно известный представитель макролидов — спирамицин. Его назначают по 3 млн МЕ три раза в сутки 7—10 дней.
Лечение больных с хламидийной инфекцией верхних отделов урогенитального тракта
При лечении больных с данной клинической формой хламидийной инфекции используют все перечисленные выше антибиотики, но менее продолжительными курсами (до трех недель), чем при неосложненных формах заболевания. Более удобен в этих случаях азитромицин, который ФР рекомендует назначать курсами: три курса по 1 г один раз в неделю.
В многоцентровом исследовании, проведенном в различных регионах России (г. Екатеринбург, Ставрополь и Москва), была показана высокая эффективность такой схемы применения азитромицина при осложненных формах хламидиоза (применялся препарат сумамед фирмы ПЛИВА, Хорватия), что и позволило внести соответствующие дополнения в рекомендации.
Лечение больных с осложненной формой хламидийной инфекции должно быть комплексным, поскольку процесс связан не только с наличием инфекции, но и с теми неблагоприятными последствиями, которые она вызывает при длительном течении болезни. Поэтому для достижения клинического излечения назначение антибактериальных препаратов в таких случаях должно сочетаться с комплексом противовоспалительных, симптоматических и физиотерапевтических мероприятий, выбор которых зависит от характера патологии.
Лечение больных с персистирующим и рецидивирующим урогенитальным хламидиозом
Персистенция хламидий требует особого подхода к больному. Применения одних антибиотиков при этой форме инфекции, как правило, недостаточно, поскольку все эффективные в отношении хламидий антибиотики обладают бактериостатическим действием и способны оказывать эффект только в процессе осуществления жизненного цикла хламидий. Поскольку при персистенции данный жизненный цикл приостанавливается на неопределенное время, использование антибиотиков в этот период не способно привести к гибели микроорганизмов, остановившихся в своем развитии. Однако лечить данную инфекцию необходимо, так как сохранение хламидий в организме может сопровождаться иммунными нарушениями, что ведет к различным осложнениям, в частности бесплодию.
При лечении таких состояний обычно рекомендуют сочетанную терапию антибиотиками и иммунокорректорами. Были предложения назначать антибиотики в различных сочетаниях длительными курсами. Последний подход имеет существенные отрицательные стороны: длительный прием антибиотиков неблагоприятно воздействует на работу всех систем организма: желудочно-кишечный тракт (нарушая работу печени и микроэкологию кишечника), нервную, мочевыделительную, иммунную (угнетая иммунитет и аллергизируя организм больного) системы. Кроме того, при персистирующей инфекции антибиотики в качестве монотерапии вообще могут быть неэффективны, исходя из особых биологических свойств возбудителя, о чем уже говорилось выше.
Наши исследования показали, что примерно у 75% больных персистирующим хламидиозом встречаются различные нарушения иммунного статуса. Они выражаются, в первую очередь, в изменении числа CD4+ и CD8+ Т-клеток и нарушении их соотношения примерно у 50% больных. По сравнению с контрольной группой, у больных наблюдается статистически достоверное снижение относительных и абсолютных показателей естественных киллеров (CD16+) (что очень важно с точки зрения продукции интерферона), HLA DR-клеток, В-клеток (CD72+ и CD21+).
Наши наблюдения, основанные на лечении более 1000 больных персистирующим хламидиозом, показывают, что наиболее оптимальна в этих случаях комбинированная терапия, основанная на сочетании антибиотиков и иммунных препаратов. При антибиотикотерапии используют стандартные для осложненной инфекции курсы и дозировки перечисленных выше антибиотиков. Но начинать лечение желательно с курса иммунотерапии. Из иммунных препаратов наибольшей эффективности можно добиться, применяя полиоксидоний и a-интерферон. На основании собственных исследований мы предлагаем следующие варианты предшествующей назначению антибиотиков иммунотерапии:
- полиоксидоний назначается по 6 мг в/м один раз в сутки; первые две инъекции ежедневно, затем три инъекции через день, остальные два раза в неделю, всего на курс 10 инъекций. После четвертой инъекции начинают курс антибактериальной терапии;
- интерферон альфа-2b назначается в виде ректальных суппозиториев двумя 5-ти дневными циклами с интервалом в две недели между ними в суммарной дозе 10 млн МЕ на курс. После окончания иммунотерапии проводится курс антибактериальной терапии. Причем оптимальным в этой ситуации оказался курс азитромицина по схеме лечения осложненных форм (по 1,0 г на 1-й, 7-й и 14-й дни).
Указанные подходы позволяют повысить эффективность лечения персистирующей и рецидивирующей хламидийной инфекции до 90%.
В ближайшие две недели после окончания лечения следует использовать метод выделения хламидий в культуре клеток, потому что только он дает возможность определить наличие в организме пациента жизнеспособных форм хламидий. Положительный результат остальных методов, включая полимеразую цепную реакцию (ПЦР) или прямую иммунофлюоресценцию (ПИФ), не обязательно говорит о том, что лечение было неэффективным, а может рассматриваться лишь как свидетельство того, что не произошла полная элиминация хламидий или их фрагментов. Следовательно, эти методы позволяют судить об эффективности проведенного лечения не ранее чем через 30 дней после окончания антибиотикотерапии.
Таким образом, соблюдение определенных правил ведения больных с урогенитальным хламидиозом позволяет добиваться полного излечения даже в тех ситуациях, когда хламидии сохраняются у пациента в течение продолжительного времени, а сам инфекционный агент оказывается устойчив к обычной антибактериальной терапии.
М. А. Гомберг, доктор медицинских наук
А. М. Соловьев, кандидат медицинских наук
ЦНИКВИ, МГМСУ, г. Москва
Читайте также:

