Убивает ли спирт кишечную палочку
Обновлено: 23.04.2024
Спирты давно и прочно обосновались в нашей повседневной жизни, причём не только на праздничном столе. ВОЗ считает антисептические средства на спиртовой основе единственными известными, которые способны быстро и эффективно уничтожить потенциально патогенные микроорганизмы на руках человека.
Спирты – виды и особенности
Спирты – обширная химическая группа веществ со своей строгой классификацией, в основе которой лежат особенности строения молекулы.
- Существует классификация, разделяющая спирты по количеству молекул углерода – одноатомные, двухатомные, трёхатомные, четырёхатомные или многоатомные.
- В зависимости от насыщенности углеводородного заместителя делятся на предельные или насыщенные, непредельные (или ненасыщенные) и ароматические – такие, в которых содержится ароматическая система, зацикленный участок молекулы с двойными сопряжёнными связями, придающий всей молекуле аномально высокую стабильность.
- По признаку наличия или отсутствия цикла в углеводородном заместителе разделяют на ациклические (или алифатические), которые не имеют цикла, и алициклические – у которых есть цикл.
- Количество заместителей при α-углеродном атоме делит спирты на первичные, вторичные и третичные.
Производить спирт в промышленных масштабах несложно, это не требует крупных финансовых затрат, а конечный продукт отличается простотой использования – вот основные причины того, почему эта химическая группа соединений обрела заслуженную популярность в сфере дезинфекции.
Какой спирт эффективен в борьбе с вирусами и бактериями
Бактерицидному и вирулицидному действию спирты обязаны своей способности к денатурации.
Денатурация – изменение структуры молекул, которое приводит к потере их естественных свойств. Денатурация мембран бактерий и защитной белковой оболочки вирусов приводит к их естественному разрушению и потере способности размножаться. Денатурация – универсальный процесс, которому подвержены многие молекулы, и именно это свойство лежит в основе широкого спектра их действия.
Спиртовые соединения эффективны против грамположительных и грамотрицательных бактерий, включая возбудителей туберкулёза, эффективны против многих распространённых вирусов, вызывающих респираторные вирусные инфекции, герпес, все виды гепатитов. Спектр действия включает также вирус иммунодефицита человека (ВИЧ) и возбудителей некоторых грибковых инфекций, предупредить которые своевременной дезинфекцией гораздо проще и быстрее, чем лечить.
В борьбе против инфекционных агентов лучше всего проявили себя три представителя: этиловый, пропиловый и его изомер изопропиловый. Все они классифицируются как одноатомные предельные ациклические первичные спирты.
Самый известный из этой тройки – этанол, потому что он, как и вода, служит основным компонентом алкогольных напитков. Этанол нашёл широкое распространение в медицине, где используется как антисептик, экстрагент и растворитель.
Пропил и изопропил менее известны, но это не делает их хуже. Оба изомера обладают высокой дезинфицирующей активностью, которая превосходит таковую у этанола, что благодаря чему концентрация действующего вещества в антисептике может быть ниже. Пропил и изопропил также безопаснее этанола – несмотря на то, что они токсичные, алкогольное опьянение наступает гораздо раньше и выражено оно сильнее, поэтому человек, по ошибке выпивший антисептик на основе пропила или изопропила, не успеет выпить летальную дозу.
Пропил и изопропил, в отличие от этанола, обладают меньшей летучестью. Для достижения опасной концентрации их паров необходима площадь разлива и испарения значительно большая, чем у этанола, что делает эти два изомера более безопасными в отношении отравления парами.
Спиртовые кожный санитайзеры и антисептики
Всемирная Организация Здравоохранения рекомендует использовать антисептики и санитайзеры, которые содержат не меньше 60% этанола и 75% изопропила. Наиболее эффективен этанол в концентрации от 70%, в некоторых случаях концентрация его может составлять до 96% включительно. Эти значения верны для антисептических средств, в составе которых спирт – основной и единственный дезинфицирующий компонент.
Кожные санитайзеры и антисептики могут содержать и другие антисептические вещества, например, четвертичные аммонийные соединения (ЧАС). Добавление позволяет снизить концентрацию спирта в составе, удешевить производство и сделать дезинфектанты доступнее для всех слоёв населения.
Любые кожные антисептические средства должны отвечать следующим требованиям:
- Эффективность.
- Простота использования.
- Дешевизна производства.
- Максимальная доступность.
- Хорошая переносимость.
В условиях пандемии пользоваться спиртовыми санитайзерами приходится чаще, чем обычно, поэтому при выборе антисептика стоит обратить внимание на состав – в нём должны быть смягчающие и увлажняющие кожу рук вещества. Спиртсодержащие средства сушат кожу, а сухие кожные покровы в большей степени подвержены микротравматизации; любая травма, даже самая маленькая и невидимая глазу подобна широко распахнутым воротам для инфекции, особенно вирусной, потому что вирусы очень маленького размера. Увлажнение кожи послужит дополнительной защитой.
Согласно историческим источникам, в III веке до нашей эры римские генералы рекомендовали своим солдатам пить вино, чтобы предотвратить дизентерию. А во время эпидемий холеры в XIX веке считалось, что бренди может предотвратить заражение инфекцией. В 2011 году в журнале Королевского медицинского общества вышла статья шотландских ученых Джэнет С. Гатри и Даррелла О. Хо-Йена, которые проверили эту теорию.

Исследователи обнаружили, что холерный вибрион полностью погибает в 20%-ном джине через час, в 18,75%-ном джине — через 6 часов, а в 15%-ном джине — через 26 часов. Оказалось, что еще быстрее справляется с бактериями красное вино: в 6,25%-ном вине их не стало уже через 30 минут. Тем не менее, авторы исследования подчеркивают, что большая часть возбудителей холеры погибает в кислой среде желудка, а при злоупотреблении алкоголем кислотность желудка понижается. Поэтому те, кто страдает алкоголизмом, рискуют заболеть при меньшем количестве бактерий, чем непьющие люди.
Какие еще исследования подтверждают антибактериальный эффект алкоголя?
Исследование, проведенное в 1988 году Медицинским колледжем штата Висконсин, показало, что сальмонелла и кишечная палочка хуже всего себя чувствуют в красном вине. Также антибактериальный эффект оказало пиво — спустя 48 часов выжило лишь небольшое количество бактерий.
Считается, что бактерицидное действие красного вина обусловлено его высокой кислотностью и концентрацией спирта. В 1998 году в Журнале клинической гастроэнтерологии вышла статья, которая частично опровергла эту гипотезу. В ходе лабораторного исследования сравнивалось влияние на сальмонеллу красного вина и раствора, содержащего такую же концентрацию алкоголя и уровень pH. Оказалось, что вино активнее подавляет инфекцию, что доказывало, что его антибактериальный эффект обусловлен не только кислотным pH и наличием алкоголя.
Между тем, концентрация алкоголя имеет значение при воздействии на микробов. В частности, в информационном бюллетене минздрава Южной Австралии приводится информация, что обработка рук спиртовым раствором с концентрацией алкоголя в диапазоне 60-80% активнее удаляет микроорганизмы с рук, чем мыло. Кроме того, сотрудники стоматологической исследовательской группы из Новой Зеландии выяснили, что 40%-ный этанол оказывает бактерицидный эффект на группы микроорганизмов во рту в течение 1-2 минут, при этом 10%-ный этанол практически не оказывал никакого воздействия.
Почему нельзя лечиться алкоголем?
Несмотря на исследования, доказывающие эффективность красного вина и этанола в борьбе с инфекцией, врачи не советуют прибегать к такому методу профилактики и лечения.

Некоторые исследования доказывают, что алкоголь оказывает негативное влияние на органы пищеварения. В 1996 году немецкие гастроэнтерологи провели эндоскопическое исследование, в котором выяснили действие чистого этанола и некоторых алкогольных напитков на слизистую оболочку желудка. 47 здоровых людей-добровольцев выпили 100 мл пива, белого вина, виски или сопоставимого раствора чистого этанола (4%,10%, 40%). Оказалось, что наибольшие поражения слизистой получили участники эксперимента, которые принимали чистый этанол: типичным повреждением была эрозия, сопровождаемая кровью. Причем, чем выше была концентрация алкоголя, тем большие повреждения он вызывал: поражения от этанола более 10% заживали более 24 часов. Пиво, вино и виски вызывали повреждения слизистой оболочки желудка в меньшей степени, что могло быть связано с защитным действием безалкогольных ингредиентов напитков.
Исследование 2017 года, проведенное под руководством доктора медицинских наук Фараза Бишехсари из Медицинского центра университета Раша в Чикаго, выявило влияние алкоголя на воспаление кишечника. После употребления алкоголь абсорбируется главным образом в верхних отделах кишечного тракта, а уже затем попадает в печень и другие органы. Поэтому желудочно-кишечный тракт особенно подвержен риску повреждения токсинами. Алкоголь, особенно если его употреблять хронически или в больших количествах, способен вызывать воспаление кишечника различными способами: изменяя состав и функции микрофлоры, увеличивая проницаемость слизистой оболочки и нарушая ее иммунную систему. По мнению авторов исследования, эти процессы впоследствии могут привести к воспалению и дисфункции различных органов и хроническим нарушениям, включая заболевания печени, неврологические заболевания, рак желудочно-кишечного тракта и синдром раздраженного кишечника.
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С.,
врач – клинический фармаколог
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Микробиологические аспекты
E.coli относится к типичным представителям семейства Enterobacteriaceae, являясь грамотрицательной бактерией, факультативным анаэробом в составе нормальной кишечной микрофлоры человека. Но тут же становится патогеном, выбравшись из среды нормального обитания, хотя отдельные штаммы являются патогенными и для желудочно-кишечного тракта. То есть кишечная палочка относится к кишечным комменсалам, кишечным патогенам и внекишечным патогенам, каждый из которых мы кратко разберем.
К штаммам E.coli, действующим как кишечные патогены и встречающимся чаще других, относятся:
- Штамм серотипа O157:H7 (STEC O157) или так называемый энтерогеморрагический штамм E.coli, который является причиной 90% случаев геморрагических колитов и 10% случаев гемолитико-уремического синдрома. Встречается достаточно часто, а если вы работаете в стационарах плановой помощи, то это один из обязательных анализов для принятия решения о госпитализации, так что так или иначе он на слуху. Проблема инфицирования этим возбудителем связана с употреблением плохо термически обработанной пищи и передачи штамма контактным путем от человека к человеку, проще говоря, через руки.
- Второй крайне опасный высоко-патогенный штамм кишечной палочки – O104:H4, вызвавший в Германии 2011 году эпидемию с высоким уровнем смертности среди пациентов с пищевыми токсико-инфекциями вследствие развития гемолитико-уремического синдрома. Если помните, это была очень громкая история с перекрытиями границ для испанских огурцов, потом вообще для всей плодоовощной продукции из Европы в Россию, пока искали хотя бы источник, не говоря уж о виновнике тех событий. Окончательно виновными тогда были обозначены листья салата, в поливе которых использовалась вода с признаками фекального заражения, а затем речь пошла уже о пророщенных семенах, которые так же полили фекально-зараженной водичкой. Так вышли на конкретный штамм E.coli – O104:H4, который, подвергшись санации антибиотиком, выплескивает эндотоксин, вызывающий гемолиз и острую почечную недостаточность. В итоге – массовая летальность пациентов, получавших антибиотики.
Затем тот же штамм обнаружился при вспышке ПТИ в Финляндии, но к тому времени пациентов с диареями до появления микробиологических результатов перестали лечить бактерицидными антибиотиками и ситуация была купирована в зародыше.
И третий громкий (для нашей страны) случай – это массовое заболевание питерских школьников в Грузии, где так же был выявлен этот штамм (пресс-релиз Роспотребнадзора по данному случаю лежит здесь).
Когда кишечная палочка выступает внекишечным патогенном? Почти всегда, когда обнаруживается вне места своего нормального обитания.
- Заболевания мочевыводящий путей. Здесь E.coli является абсолютным лидером и играет ведущую роль в развитии:
- Острых циститов
- Пиелонефритов
- Абсцессов почек и
- Простатитов
Этот факт объясняется близким анатомическим расположением двух систем и огрехами в личной гигиене, что позволяет на этапе эмпирической терапии вышеперечисленных заболеваний сразу же назначать препараты, активные в отношении кишечной палочки.
- Заболевания желудочно-кишечного тракта:
- Диарея путешественников
- Интраабдоминальные абсцессы и перитониты, чаще всего носящие вторичный характер (прободение кишки в результате первичного заболевания, либо при дефектах оперативного вмешательства)
- Инфекции центральной нервной системы у очень ослабленных пациентов, результатом чего будет развитие менингитов. Встречается в основном у лиц старческого возраста и новорожденных. Кроме того, в случае внутрибольничного заражения менингит может развиться в результате плохой обработки рук медицинского персонала перед оперативным вмешательством или перевязками.
- Инфекции кровотока, а именно сепсис, как продолжение развития заболеваний мочевыводящих путей, ЖКТ и билиарного тракта вследствие метастазирования очага инфекции. Лечению поддается крайне тяжело, особенно если задействованы внутрибольничные штаммы, летальность чрезвычайно высокая.
- Инфекции кожи и мягких тканейкак следствие раневых инфекций после вмешательств на органах брюшной полости.
- Внутрибольничные пневмонии, вызванные устойчивыми штаммами кишечной палочки, целиком связаны с дефектами ухода за пациентом и фактором чистоты, точнее ее отсутствия, рук медицинского персонала или ухаживающих родственников. Факт внутрибольничного заражения доказывается элементарно, что будет наглядно продемонстрировано в следующем разделе.
- Послеродовые (и не только) эндометриты. Вынуждены упомянуть и эту патологию, так как инфицирование кишечной палочкой встречается все чаще и чаще, а большой настороженности нет. Как результат, можно очень сильно промахнуться с антибактериальной терапией и, как следствие, прийти к экстирпации органа в виду неэффективности антибиотикотерапии. Натолкнуть на мысль может более позднее, чем обычно, поступление и более агрессивное, чем обычно течение. Дополнительный осмотр прианальной области так же может натолкнуть на вероятность развития именно такого инфицирования.
(часть вторая) Практические вопросы диагностики и лечения.
Когда мы можем заподозрить, что перед нами пациент с инфекцией, вызванной кишечной палочкой?
- Пациенты с диареей, приехавшие из отпуска и все-таки смогшие прийти на прием (диарея путешественников или энтеротоксигенные штаммы E.coli).
- Пациенты со всеми заболеваниями мочевыделительной системы, в том числе беременные, но строго с наличием симптоматики (не надо лечить бессимптомную бактериурию, иначе вырастите резистентные штаммы и создадите проблему и себе, и женщине, и роддому в последующем).
- В стационарах – нозокомиальные пневмонии, послеоперационные менингиты, перитониты, сепсисы и т. д., носящие вторичный характер.
Подтвердить или полностью исключить кишечную палочку из возбудителей может только микробиологическое исследование. Конечно, в современных условиях микробиология уже становится практически эксклюзивом, но мы пришли учиться, а учится надо на правильных примерах, поэтому далее будет рассмотрен ряд антибиотикограмм, выполненных автоматизированными системами тестирования. Вдруг вам повезет, и в вашем лечебном учреждении все уже есть или в ближайшее время будет, а вы уже умеете с этим всем работать?
Если вы читаете данный цикл по порядку, то в базовом разделе по микробиологии был выложен ряд антибиотикограмм некоего микроорганизма в контексте нарастания антибиотикорезистентности, и это была наша сегодняшняя героиня – кишечная палочка.
- Начнем с дикого и крайне симпатичного штамма E.coli, который живет в кишечнике и обеспечивает синтез витамина К. С ним сталкиваются доктора амбулаторной службы у пациентов с инфекциями мочевыводящих путей или в случае госпитализации у пациентов, которые не получали антибиотики около года. И именно такую чувствительность мы имеем в виду, когда назначаем эмпирическую антибиотикотерапию
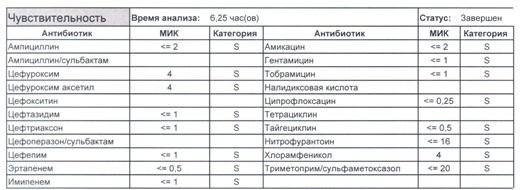
- Как видите, зверь чувствителен абсолютно ко всему, и это как раз тот случай, когда можно свободно пользоваться табличными материалами справочников или клинических рекомендаций, так как механизмы резистентности полностью отсутствуют.
- Если в ваши руки попал пациент, которого в течение последнего полугодия лечили антибиотиками пенициллинового ряда, то антибиотикограмма может выглядеть следующим образом.
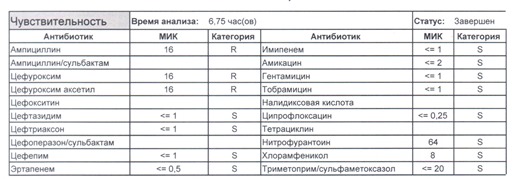
Если такая кишечная палочка окажется внекишечным патогенном, и перед вами будет беременная и ИМП (самый частый случай), то нам необходимо преодолеть резистентность к пенициллинам, то есть подавить деятельность пенициллиназ. Соответственно высокую эффективность продемонстрируют препараты с ингибиторами бета-лактамаз, чаще всего амоксициллина/клавуланат, как наиболее безопасный и эффективный. Единственное, пациентку необходимо предупредить, что в результате стимуляции рецепторов кишечника может развиться антибиотик-ассоциированная диарея.
- Отдельно хотелось бы обратить внимание на следующий штамм E.coli, как типичного обладателя бета-лактамаз расширенного спектра. И эти БЛРС чаще всего вырабатываются в результате неуемного использования цефалоспоринов третьего поколения и совершенно конкретного его представителя – цефтриаксона.
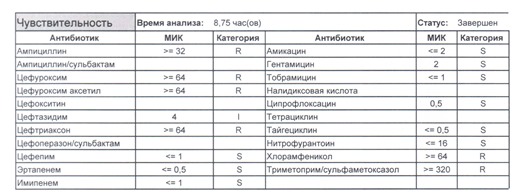
В каких ситуациях мы можем увидеть (или подумать) о таком звере:
- Пациент сам рассказывает, что получал цефтриаксон в промежутке полугодия
- Пациент был переведен из другого стационара (хотя там можно будет и следующую картинку обнаружить)
- Пациент ничего не получал, и вообще в больнице не лежал, но возбудитель попал с рук медицинского персонала, вызвав внутрибольничную инфекцию
- И самый простой случай – посев был взят в момент проведения терапии цефтриаксоном
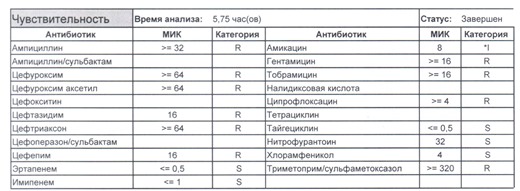
Подобный пациент не придет к вам своими ногами, его не увидит амбулаторная служба, это абсолютно стационарные больные, и если их привезут, то только из другого лечебного учреждения. Чаще всего это пациенты палат интенсивной терапии или реанимации, и такой возбудитель носит на 100% нозокомиальный характер.
Когда можем его обнаружить:
- вторичные перитониты,
- нозокомиальные пневмонии,
- пиелонефриты,
- послеоперационные менингиты,
- сепсис и т. п.
- Для эрадикации такого возбудителя нужен не просто отдельный обученный специалист и имеющая весь набор препаратов резерва аптека, но и напряженная работа эпидемиологической службы, так как подобный пациент должен быть изолирован в отдельную палату, а лучше изолятор (не подумайте, что бред – при правильной организации такие вещи вполне реальны) с проведением карантинных мероприятий, так как основная проблема появления подобного рода возбудителей в том, что они очень быстро разбегаются по всему корпусу (или стационару, если корпуса не изолированы) и обсеменяют все и вся, нанося вред другим ослабленным тяжелой болезнью пациентам и заселяя кишечники всего медицинского персонала.
- И еще одно крайне мерзкое свойство таких возбудителей – они умеют осуществлять горизонтальный перенос механизмов резистентности с другой флорой семейства Enterobacteriaceae, и даже если вы избавились от E.coli, неприятным сюрпризом может стать ее подруга клебсиелла, наносящая еще больший вред и по сути добивающая больного. Избавится полностью от этих возбудителей невозможно, для этого надо избавится от медицинского персонала как основных носителей, но контролировать можно – мероприятия подробно расписаны в действующих СанПиН 2.1.3.2630-10. Так что в случае выявления подобного возбудителя речь пойдет не только о лечении того пациента, у которого он обнаружен, но и проведения мероприятий по недопущению инфицирования всех остальных пациентов (а это, напомню, почти всегда ПИТ или ОРИТ), находящихся рядом.
- И в заключение необходимо упомянуть о панрезистентной E.coli, вооруженной полным спектром механизмов резистентности. В антибиотикограмме будут тотальные R, а МПК возбудителей пробьют все возможные потолки. К счастью для автора, она с таким зверем пока не сталкивалась, что связано с наличием работающей системы эпиднадзора, поэтому картинки не будет, хотя ее несложно представить. Такие пациенты, если кишечная палочка окажется патогеном, а не колонизатором (мало ли с чьих рук, например, в рану упала), к сожалению, почти не выживают, так как изначально являются крайне тяжелыми соматически, а кишечная палочка обычно подводит черту к их существования на бренной земле.
- Не допускать развития такой, не побоюсь этого слова, зверюги в ваших стационарах, а если появилась – гонять эпидемиологическую службу, чтобы избавляла руки и поверхности от такого рода заражения, что возможно только при условии наличия достаточного количества расходных материалов, перчаток и дезинфицирующих средств.
А теперь подведем небольшой итог нашего непростого разговора:
- Кишечная палочка – возбудитель очень серьезный и не следует его недооценивать. В ее типах также необходимо четко ориентироваться.
- В первую очередь о ней мы думаем при лечении инфекций мочевыводящих путей, особенно у беременных.
- Если перед нами пациент с признаками кишечной инфекции, то подход к терапии антибиотиками должен быть сугубо индивидуальным, и если состояние позволяет, то до получения микробиологии – вообще без антибиотиков. Если не позволяет – это должны быть бактериостатики.
- Мы никогда не лечим только анализ, и даже микробиологическое заключение, мы всегда лечим пациента со всем комплексом его симптомов и синдромов. Но микробиология помогает решить как дифференциально-диагностические задачи, что и позволяет отделить безусловный патоген от мирно живущего комменсала.
- Микробиологическая диагностика носит ключевое значение как для подтверждения самого возбудителя, так и для выбора необходимого антибиотика
- В случае выявления резистентных и панрезистентных возбудителей, помимо лечения самого пациента должна в полной мере задействоваться эпидемиологическая служба лечебного учреждения
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Врага, как известно, надо знать в лицо. Просторы интернета принесли вот такое симпатичное фото нашего противника.
Данного возбудителя невозможно перепутать ни с чем, особенно, когда процесс зашел далеко. Практически все отделение будет в курсе наличия такого больного из-за непередаваемого аромата, разносящегося из его пораженных областей.
Pseudomonas aeruginosa бывает дикой, ее нам приносят пациенты из внешнего мира и нашей, госпитальной, которая живет внутри больничных отделений (чаще хирургических и реанимационных) и вызывает тот самый суеверный ужас практически у всех, обремененных медицинским образованием.
Синегнойная палочка является вольным жителем тех мест, где тепло и влажно. Она живет в прудах (дикая), в раковинах, в банках с фурацилином и другими дезенфектантами, диализных жидкостях и наркозных аппаратах в стационарах.
А потому, если в отделение что-то такое выросло, борьба с синегнойной инфекцией должна начинаться со смены сантехники (старой на новую) и линолеума вокруг раковины. С отказа от фурацилина, со сроком изготовления более суток и с просушивания трубок аппаратуры для вентиляции легких.
Больной у нас тоже теплый и, как и любой человек, на 70% состоит из воды. А еще у него множество вольных открытых пространства – мокнущие раневые поверхности, ожоговые раны, свищевые ходы, пролежни, цистостомы, трахеостомы, катетеры. То есть все те условия, которые палочка очень любит. А еще теплой и влажной поверхностью у нас является роговица глаза и если промедлить с лечением – этот самый глаз можно потерять за несколько часов.
- Гангренозную пневмонию
- Эмпиему
- Наружный отит
- Инфекции глаз (особенно после травм и хирургических вмешательств)
- Фурункулез (после горячих ванн)
- Септицемию
- Эндокардит
- Менингит
- Часто инфицирует ожоговые поверхности, свищевые ходы, изъязвленные пролежни.
Синегнойная инфекция развивается чаще всего на фоне иммуносупрессии или массированной антимикробной терапии, так как сам возбудитель природно устойчив абсолютному большинству антибактериальных препаратов, а массовая гибель конкурентов, дает ей селективное преимущество. Кстати, основными препаратами, селектирующими в отделениях Pseudomonas aeruginosa являются цефалоспорины третьего и четвертого поколений.
- на руках
- на общих полотенцах в ординаторских, процедурных и манипуляционных (многоразовых)
- на фонендоскопах
- на мобильных телефонах
- на авторучках, которые у нас торчат из карманов и т.д.
И достаточно в отделении появиться одному пациенту с этим возбудителем, а персоналу забыть о путях распространения – к вечеру все 100% пациентов будут обсеменены этим возбудителем. А дальше как повезет… пациентам…
Если инфицирование все-таки произошло, и у пациента возникла синегнойная инфекция, чем же мы будем ее лечить?
В этом списке нет цефоперазона и цефоперазона/сульбактама, о которых нам с института говорят, что они антисинегнойные. Дело в том, что единственным действительно антисинегнойным цефалоспорином является цефтазидим, а данные о якобы высокой чувствительности к цефоперазону и цефоперазону сульбактаму существуют только в России, так как нет ни одной рекомендации по использованию этих препаратов ни в США, ни на medscape.com, ни на EUCAST. Более того, эти источники не дают даже критериев определения чувствительности Pseudomonas aeruginosa к этим препаратам. И откуда взялись наши российские выводы о высокой чувствительности вообще не понятно. Более того, комбинация Цефоперазон/сульбактам существует только в 2-х странах – России и Турции. FDA в свое время очень быстро отменила его регистрацию.
Цефалоспорин третьего поколения. Препарат с явной и очень высокой антисинегнойной активностью. Первые несколько лет после появления он был самым мощным препаратом против грам(-) флоры. Однако в связи с увеличением количества как госпитальных, так и внебольничных беталактамаз расширенного спектра (БЛРС), его значение было пересмотрено и сейчас он используется в качестве индикатора для выявления БЛРС у грам(-) бактерий. Проще говоря, если кишечная палочка или клебсиелла устойчивы к цефтаздиму, то любой, сколь угодно большой диаметр зоны на чашке Петри вокруг диска с цефотаксимом или цефтриаксоном в расчет уже не принимаются.
Если антибиотикограммы еще нет, но есть пациент предлеченный цефтазидимом без эффекта, то не нужно выбирать ему препарат среди III генерации цефалоспоринов, по причине того, что использование их будет бесполезным, при этом, если пациента с грамотрицательной инфекцией лечили цефалоспоринами 2-3-й генерации, то вполне допустима терапия цефтазидимом, потому что, во-первых, он активен против синегнойки, а во вторых бета-лактамаза цефуроксимаза, рушит все цефалоспорины, но не цефтазидим.
Еще одной особенностью цефтазидима является его возможность создавать высокие концентрации в ликворе, проникая через гематоэнцефалический барьер, поэтому его используют для лечения менингитов, вызванных грамотрицательной микрофлорой, при условии чувствительности к нему возбудителей.
3. Карбопенемы обладают антисинегнойной активностью, но она слабее чем у цефтазидима и анисинегнойными они стали только из-за того, что существует Эртапенем, у которого нет никакой антисинегнойной активности. Да, применять можно, но только в комбинации с другими антисинегнойными препаратами.
4. Амикацин, как и все аминогликозиды, обладает более мощным бактерицидным действием, чем бета-лактамы и минимальным количеством аллергических реакций. Но он должен нами рассматриваться, как и другие антисинегнойные препараты, как препарат резерва и не использоваться широко в стационаре. Другие аминогликозиды прекрасно отработают Гр (-) флору и без него, нам важно сохранить чувствительность нашей, местной синегнойки к нему как можно дольше.
Дозируем амикацин, как вы помните, на килограмм массы тела и детям и взрослым и обязательно с учетом клиренса креатинина. (подробнее о дозировании смотрите обзорную статью по аминогликозидам, которая располагается по этой ссылке /vracham/Informatsiya-dlya-spetsialistov/Antibiotikoterapiya/Obzory-antibiotikov-razlichnyh-grupp/Obzory-antibiotikov-razlichnyh-grupp_411.html)
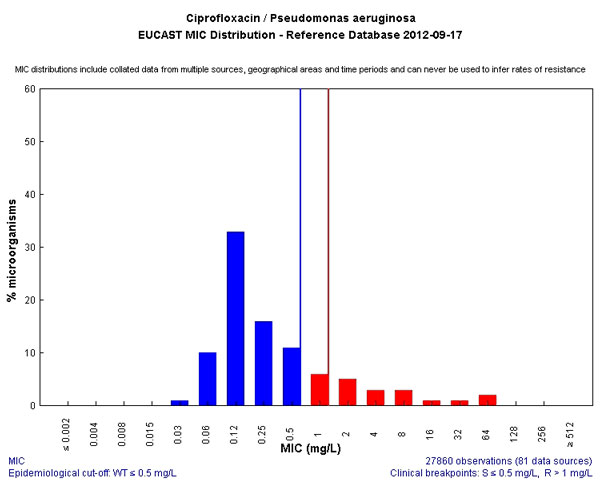
И, к сожалению, препарат, который нам скоро уничтожат коллеги из поликлинического звена, потому что назначают его направо и налево. Да и в стационарах коллеги грешат его необоснованным назначением, так как он относительно дешев и более чем доступен из-за огромного количества дженериков. Как результат, нам уже приходится использовать дозировки не 400 мг в сутки, а 800-1200 мг. И, слава богу, что механизм резистентности нам это еще позволяет. Является одним из самых безопасных антисинегнойных препаратов, а потому беречь его мы должны как самое дорогое.
Он может использоваться в стационаре в случаях не синегнойной инфекции только тогда, когда другим способом помочь пациенту невозможно.
Это препарат такого же глубокого резерва как амикацин. И может использоваться только под контролем клинического фармаколога в отличие от других фторхинолонов.
И один из самых страшных моих, и не только моих, кошмаров – это панрезистентная синегнойная палочка. Это та палочка которая устойчива абсолютно ко всем известным на данный момент антимикробным средствам и здесь мы совершенно бессильны. А потому наша основная цель состоит в том, чтобы не дать ей у нас в стационаре появиться. Для этого требуется соблюдать несложные правила асептики, а именно, мыть и обрабатывать руки после каждого пациента, менять перчатки, обрабатывать фонендоскопы и к пациентам с гнойным воспалением не заходить с мобильниками и чем либо еще, что мы можем схватить руками, сами того не замечая. Ну и никаких общих полотенец в ординаторских и сестренских.
Кишечная палочка — разновидность грамотрицательных палочковидных бактерий, которые присутствуют в нормальной микрофлоре ЖКТ человека. Тем не менее, некоторые её виды вызывают заболевания, преимущественно желудочно-кишечные. Отдельные штаммы способны поражать органы мочеполовой системы, вызывать пневмонию, перитонит, мастит и сепсис.

Общие сведения о Escherichia coli
Кишечная палочка — это нормальный обитатель кишечника человека и важная часть естественной кишечной микрофлоры. Она появляется у человека с первых дней после рождения.
Характерная особенность этой бактерии — устойчивость к действию внешних факторов. Она может в течение долгого времени сохраняться в воде и земле, размножается в продуктах питания (особенно в молоке), переносит высушивание. На палочку губительно воздействуют прямые солнечные лучи (воздействие — несколько минут), раствор карболовой кислоты (1%) и температура +60 градусов (воздействие в течение 15 минут).
Escherichia coli — условно-патогенный штамм. Основным резервуаром его обитания является кишечник.
В большинстве случаев эта палочка не наносит вреда организму, но, под действием определенных факторов, непатогенная микрофлора замещается патогенной.
Норма кишечной палочки в организме составляет 107–108 КОЕ/г на 1 г фекалий. Недостаток этой бактерии приводит к дисбиозу, который проявляется в метеоризме, нарушениях стула, болях в животе.
Иногда в организм проникают патогенные микроорганизмы — кишечные и внекишечные. Они могут вызывать расстройство желудка, инфекции мочевыводящих путей, менингит.

Как происходит заражение?
Патогенные штаммы Escherichia coli передаются преимущественно орально-фекальным путем, реже — контактно-бытовым.
- В первом случае палочка попадает в почву и воду вместе с каловыми массами. Здесь она сохраняется в течение долгого времени, так как устойчива ко внешним факторам. Инфицирование человека происходит при заглатывании зараженной воды (не только при питье, но и при купании в водоемах), контакте с загрязненной почвой или растениями.
- Контактно-бытовой путь заражения менее распространен. Чаще всего передача палочки таким способом происходит в коллективах (больницы, школы, детские сады). Это связано с недостаточной гигиеной.
Симптомы заражения
Патогенные кишечные палочки бывают разными. В зависимости от их типа проявляются характерные симптомы заражения.
- Энтеропатогенная кишечная палочка. Основное проявление заражения — диарея. В каловых массах не наблюдаются включения крови, но присутствует слизь. Иногда поднимается температура. Чаще всего такой тип палочки выявляют у детей.
- Энтеротоксигенная. Эта бактерия прикрепляется к стенкам кишечника и выделяет токсины. Помимо диареи, заражение проявляется в симптомах интоксикации (головная боль, тошнота, общая слабость, повышение температуры).
- Энтерогеморрагическая. Это наиболее опасный вид кишечной палочки: он вызывает геморрагический колит, который осложняется гемолитико-уремическим синдромом (сочетание анемии с почечной недостаточностью). К симптомам заражения относят схваткообразные боли в животе, диарею с кровью, рвоту, лихорадку.
Кишечная палочка поражает не только кишечник, но и мочеполовую систему как женщин, так и мужчин. У женщин эта бактерия провоцирует развитие пиелонефрита, цистита, кольпита, вульвовагинита. У мужчин патогенные кишечные палочки вызывают острый уретрит. Из уретры они могут проникать в предстательную железу и яички, вызывая простатит, орхит и эпидидимит.

Лечение
Для устранения симптомов кишечной палочки назначают такие группы препаратов:
- Антибактериальные средства. Это традиционные препараты при выявлении Escherichia coli в моче, кале, а также во влагалище у женщин. Конкретный вид антибиотика определяют в зависимости от степени тяжести поражения.
- Спазмолитики и обезболивающие. Они назначаются при выраженном болевом синдроме.
- Пробиотики. Препараты этой группы восстанавливают баланс нормальной микрофлоры кишечника.
При кишечных инфекциях также показано соблюдение диеты. Целью являются:
- щадящее воздействие на желудочно-кишечный тракт (как механическое, так и химическое);
- уменьшение воспалительного процесса;
- снижение выраженности брожения и гнилостных процессов в организме;
- восстановление работоспособности кишечника.
Основные правила лечебной диеты:
- легкоусвояемость блюд, отсутствие в рационе продуктов, раздражающих слизистую оболочку желудка и нагружающих поджелудочную железу;
- допустимые способы приготовления еды — варка (обычная и на пару);
- допустимая температура еды — от 33 до 36 градусов.
В рацион можно включать:
- некрепкий чай, свежевыжатые соки из фруктов и ягод, немного разбавленные водой;
- молочные и кисломолочные продукты с низким содержанием жира;
- нежирные супы;
- нежирные сорта мяса и рыбы (отваренные либо приготовленные на пару);
- тушеные и вареные овощи;
- крупяные гарниры на воде.
При выявлении кишечной палочки Escherichia coli нельзя употреблять:
- жирные сорта рыбы и мяса;
- колбасы, копчености;
- консервы;
- бобовые;
- грибы;
- соленья и маринады;
- свежие хлебобулочные изделия;
- кондитерские изделия, шоколад;
- газированные напитки и алкоголь.
Все перечисленные продукты раздражают слизистую оболочку желудка и тяжело перевариваются.
Лечение при симптомах заражения кишечной палочкой обязательно, так как при его отсутствии процесс осложняется обезвоживанием, интоксикацией, перитонитом, сепсисом. Эти состояния угрожают не только здоровью, но и жизни.

Профилактика
Для того, чтобы снизить риск заражения инфекцией, нужно соблюдать такие правила:
Читайте также:

