Укажите признаки отличающие пти и холеру
Обновлено: 22.04.2024
Эшерихиозы — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечной палочки, протекающих с симптомами общей интоксикации и поражением ЖКТ.
Классификация
Этиология и патогенез
Эшерихии — подвижные грамотрицательные палочки, аэробы, относящиеся к виду Escherichia coli, роду Escherichia, семейству Enterobacteriaceae. Растут на обычных питательных средах, выделяют бактерицидные вещества-колицины. Морфологически серотипы не отличаются друг от друга. Эшерихии содержат соматические (О-Аг — 173 серотипа), капсульные (К-Аг — 80 серотипов) и жгутиковые (Н-Аг — 56 серотипов) антигены. Диареегенные кишечные палочки подразделяются на пять типов:
Факторы патогенности ЭТКП (пили, или фимбриальные факторы) определяют склонность к адгезии и колонизации нижних отделов тонкой кишки, а также к токсинообразованию. Термолабильный и термостабильный энтеротоксины ответственны за повышенную экскрецию жидкости в просвет кишки. Патогенность ЭПКП обусловлена способностью к адгезии. ЭИКП способны, имея плазмиды, проникать в клетки кишечного эпителия и размножаться в них. ЭГКП выделяют цитотоксин, шигоподобные токсины 1-го и 2-го типов, содержат плазмиды, которые облегчают адгезию к энтероцитам. Факторы патогенности энтероадгезивных кишечных палочек изучены недостаточно.
Эшерихии устойчивы в окружающей среде, могут месяцами сохраняться в воде, почве, испражнениях. Сохраняют жизнеспособность в молоке до 34 дней, в детских питательных смесях — до 92 дней, на игрушках — до 3-5 мес. Хорошо переносят высушивание. Обладают способностью размножаться в пищевых продуктах, особенно в молоке. Быстро погибают при воздействии дезинфицирующих средств и при кипячении. У многих штаммов Е. coli отмечают полирезистентность к антибиотикам.
Эшерихии проникают через рот, минуя желудочный барьер, и в зависимости от типовой принадлежности оказывают патогенное действие.
Энтеротоксигенные штаммы способны вырабатывать энтеротоксины и фактор колонизации, посредством которого осуществляются прикрепление к энтероцитам и колонизация тонкой кишки.
Энтеротоксины — термолабильные или термостабильные белки, которые воздействуют на биохимические функции эпителия крипт, не вызывая видимых морфологических изменений. Энтеротоксины усиливают активность аденилатциклазы и гуанилатциклазы. При их участии и в результате стимулирующего действия простагландинов увеличивается образование цАМФ, вследствие чего в просвет кишки секретируется большое количество воды и электролитов, которые не успевают реабсорбироваться в толстой кишке, — развивается водянистая диарея с последующими нарушениями водно-электролитного баланса. Инфицирующая доза ЭТКП — 10х10 10 микробных клеток.
ЭИКП обладают свойством внедряться в клетки эпителия толстой кишки. Проникая в слизистую оболочку, они вызывают развитие воспалительной реакции и образование эрозий кишечной стенки. Из-за повреждения эпителия усиливается всасывание в кровь эндотоксинов. У больных в испражнениях появляются слизь, кровь и полиморфно-ядерные лейкоциты. Инфицирующая доза ЭИКП — 5х10 5 микробных клеток.
Механизм патогенности ЭПКП изучен недостаточно. У штаммов (055,086,0111 и др.) выявлен фактор адгезии к клеткам Нер-2, за счёт которого происходит колонизация тонкого кишечника. У других штаммов (018, 044, 0112 и др.) этот фактор не обнаружен. Инфицирующая доза ЭПКП — 10х10 10 микробных клеток.
ЭГКП выделяют цитотоксин (SLT — shiga-like toxin), который разрушает клетки эндотелия, выстилающего мелкие кровеносные сосуды кишечной стенки проксимальных отделов толстой кишки. Сгустки крови и фибрин препятствуют кровоснабжению кишки — в кале появляется кровь. Развивается ишемия кишечной стенки, вплоть до некроза. У некоторых больных наблюдают осложнения с развитием синдрома диссеминированного внутрисосудистого свёртывания (ДВС), ИТШ и ОПН.
ЭАКП способны к колонизации эпителия тонкой кишки. Вызванные ими заболевания взрослых и детей протекают длительно, но легко. Это связано с тем, что бактерии прочно закрепляются на поверхности эпителиальных клеток.
Эпидемиология
Основной источник эшерихиозов — больные со стёртыми формами заболевания, меньшую роль играют реконвалесценты и носители. Значимость последних возрастает, если они работают на предприятиях по приготовлению и реализации пищевых продуктов. По некоторым данным, источник возбудителя при энтерогеморрагических эшерихиозах (0157) — крупный рогатый скот. Инфицирование людей происходит при употреблении продуктов, которые были недостаточно термически обработаны. Механизм передачи — фекально-оральный, который осуществляется пищевым, реже — водным и бытовым путём. По данным ВОЗ, для энтеротоксигенных и энтероинвазивных эшерихии характерен пищевой, а для энтеропатогенных — бытовой путь.
Из пищевых продуктов чаще фактором передачи служат молочные изделия, готовые мясные продукты, напитки (квас, компот и др.).
В детских коллективах инфекция может распространяться через игрушки, загрязнённые предметы обихода, руки больных матерей и персонала. Реже регистрируют водный путь передачи эшерихиозов. Наиболее опасно загрязнение открытых водоёмов, которое происходит в результате сброса необезвреженных хозяйственно-бытовых сточных вод, особенно из детских учреждений и инфекционных больниц.
Основу профилактики эшерихиозов составляют меры по пресечению путей передачи возбудителя. Особенно важно соблюдать санитарно-гигиенические требования на объектах общественного питания, водоснабжения; предупреждать контактно-бытовой путь заражения в детских учреждениях, родильных домах, стационарах (использование индивидуальных стерильных пелёнок, обработка рук дезинфицирующими растворами после работы с каждым ребёнком, дезинфекция посуды, пастеризация, кипячение молока, молочных смесей). Продукты, готовые к употреблению, и сырые, нужно разделывать на разных досках отдельными ножами. Посуду, в которой транспортируют пищу, необходимо обрабатывать кипятком.
При подозрении на эшерихиоз необходимо обследовать беременных до родов, рожениц, родильниц и новорождённых.
Контактных в очаге заболевания наблюдают 7 дней. Детей, контактных с больным эшерихиозом по месту жительства, допускают в детские учреждения после разобщения с больным и трёхкратных отрицательных результатов бактериологического исследования кала.
При выявлении больных эшерихиозом в детских учреждениях и родильных домах прекращают приём поступающих детей и рожениц. Персонал, матери, дети, бывшие в контакте с больным, а также дети, выписанные домой незадолго до заболевания, обследуются трёхкратно (проводят бактериологическое исследование кала). При выявлении лиц с положительными результатами обследования их изолируют. Больных, перенёсших эшерихиоз, наблюдают в течение 3 мес с ежемесячным клиническим и бактериологическим обследованием в КИЗ. Перед снятием с учёта — двукратное бактериологическое исследование кала с интервалом в 1 день.
Клиническая картина
Cимптомы, течение
Клинические проявления эшерихиозов зависят от типа возбудителя, возраста больного, иммунного статуса.
Заболевание начинается остро, больных беспокоят слабость, головокружение. Температура тела нормальная или субфебрильная. Появляются тошнота, повторная рвота, разлитые схваткообразные боли в животе. Стул частый (до 10-15 раз в сутки), жидкий, обильный, водянистый, нередко напоминающий рисовый отвар. Живот вздут, при пальпации определяют урчание, небольшую разлитую болезненность. Тяжесть течения определяется степенью дегидратации. Возможна молниеносная форма заболевания с быстрым развитием эксикоза. Длительность болезни 5-10 дней.
Особенности эшерихиоза, вызванного энтероадгезивными штаммами, изучены мало. Заболевание регистрируют у пациентов с ослабленной иммунной системой. Чаще выявляют внекишечные формы — поражение мочевыводящих (пиелонефрит, цистит) и желчевыводящих (холецистит, холангит) путей. Возможны септические формы (коли-сепсис, менингит).
Диагностика
Клиническая картина эшерихиозов сходна с клинической картиной других диарейных инфекций. Поэтому диагноз подтверждают на основании бактериологического метода исследования. Материал (испражнения, рвотные массы, промывные воды желудка, кровь, моча, ликвор, жёлчь) следует брать в первые дни болезни до назначения больным этиотропной терапии. Посевы производят на среды Эндо, Левина, Плоскирева, а также на среду обогащения Мюллера.
Используют иммунологические методы исследования РА, РИГА в парных сыворотках, но они не убедительны, так как возможны ложноположительные результаты из-за антигенного сходства с другими энтеробактериями. Эти методы используют для ретроспективной диагностики, особенно во время вспышки.
Перспективным методом диагностики служит ПЦР. Инструментальные методы исследования (ректороманоскопия, колоноскопия) при эшерихиозах малоинформативны.
Дифференциальный диагноз
Дифференциальную диагностику эшерихиозов проводят с другими острыми диарейными инфекциями: холерой, шигеллёзом, сальмонеллёзом, кампилобактериозом, ПТИ стафилококковой этиологии и вирусными диареями: ротавирусной, энтеровирусной, Норволк-вирусной инфекцией и др.
В отличие от эшерихиозов, холера характеризуется отсутствием интоксикации, лихорадки, болевого синдрома, наличием многократной рвоты, быстрым развитием дегидратации III-IV степени. Помогает в постановке диагноза эпидемиологический анамнез — пребывание в эндемичных для холеры регионах.
Сальмонеллёз, в отличие от эшерихиозов, характеризуется более выраженной интоксикацией, разлитыми болями в животе, болезненностью при пальпации в эпигастральной и околопупочной областях, урчанием. Характерен зловонный стул зеленоватого цвета.
Для ПТИ стафилококковой этиологии, в отличие от эшерихиозов, характерны острое, бурное начало заболевания, короткий инкубационный период (30-60 мин), более выражены симптомы интоксикации, рвота неукротимая. Боли в животе режущего характера, с локализацией в эпигастральной и околопупочной областях. Характерны групповой характер заболевания, связь заболевания с пищевым фактором, быстрый регресс болезни.
Осложнения
Чаще эшерихиозы протекают доброкачественно, но возможны осложнения: ИТШ, гиповолемический шок с дегидратацией III-IV степени, ОПН, сепсис, пневмония, пиелоцистит, пиелонефрит, холецистит, холангит, менингит, менингоэнцефалит. Летальный исход в результате ОПН (синдром Гассера) регистрируют у детей до 5 лет в 3-7% случаев. В Москве за последние 10 лет летальных исходов не было.
Лечение
В остром периоде болезни больным рекомендуют щадящую терапию (стол № 4, при нормализации стула — № 2, в период реконвалесценции — № 13).
В лёгких случаях заболевания достаточно назначения оральной регидратационной терапии (регидрон и другие растворы, количество которых должно в 1,5 раза превышать потери воды с испражнениями).
Показаны ферменты (панзинорм-форте, мезим-форте), энтеросорбенты (полисорб, энтеросгель, энтеродез в течение 1-3 дней). При лёгком течении болезни целесообразно использование кишечных антисептиков (интетрикс по две капсулы три раза в день, неоинтестопан после каждого акта дефекации по две таблетки, до 14 в сутки, энтерол по две капсулы два раза в день) в течение 5-7 дней. Лёгкие и стёртые формы эшерихиозов не требуют назначения этиотропных препаратов.
При лечении больных в условиях стационара показан постельный режим в первые 2-3 дня. Назначают этиотропную терапию. С этой целью при среднетяжёлых формах используют один из следующих препаратов: ко-тримоксазол по две таблетки два раза в день или препараты фторхинолонового ряда (ципрофлоксацин по 500 мг два раза в сутки перорально, пефлоксацин по 400 мг два раза в сутки, офлоксацин по 200 мг два раза в сутки), длительность терапии 5-7 дней.
В тяжёлых случаях фторхинолоны применяют вместе с цефалоспоринами 2-го (цефуроксим по 750 мг четыре раза в сутки внутривенно или внутримышечно; цефаклор по 750 мг три раза в сутки внутримышечно; цефтриаксон 1,0 г один раз в сутки внутривенно) и 3-го поколения (цефоперазон по 1,0 г два раза в сутки внутривенно или внутримышечно; цефтазидим по 2,0 г два раза в сутки внутривенно или внутримышечно).
При дегидратации II-III степени назначают регидратационную терапию внутривенно кристаллоидными растворами (хлосоль, ацесоль и пр.), которую проводят по общим правилам.
При выраженных симптомах интоксикации используют коллоидные растворы (декстран и др.) в объёме 400-800 мл/сут.
После приёма антибактериальных препаратов при продолжающейся диарее используют эубиотики для коррекции дисбактериозов (бифидумбактерин-форте, хилак-форте и др.) в течение 7-10 дней. Больных выписывают после полного клинического выздоровления, нормализации стула и температуры тела, а также однократного бактериологического исследования кала, которое проводят не ранее чем через 2 дня после окончания лечения.
При лёгкой форме заболевания 5-7 дней, при среднетяжёлой 12-14 дней, при тяжёлой — 3-4 нед. Диспансеризация не регламентирована.
Госпитализация
Госпитализацию больных с эшерихиозами проводят по клиническим и эпидемиологическим показаниям. Больных при среднетяжёлом и тяжёлом течении заболевания госпитализируют в инфекционные больницы. В лёгких случаях больные могут лечиться амбулаторно при наличии благоприятных бытовых, санитарно-гигиенических условий.
По эпидемиологическим показаниям госпитализации подлежат лица из декретированных групп, больные из организованных коллективов, а также пациенты, проживающие в коммунальных квартирах, общежитиях.
В данной теме рассматриваются вопросы этиологии, патогенеза, клиники и лечения наиболее распространенных пищевых токсикоинфекций и ботулизма.
Пищевые токсикоинфекции (ПТИ) — острые, кратковременные заболевания, вызываемые условно-патогенными бактериями, способными продуцировать экзотоксины вне организма человека (в продуктах питания), протекающие с симптомами поражения верхних отделов ЖКТ (гастрит, гастроэнтерит) и нарушениями водно-солевого обмена и КЩС.
Этиология пищевых токсикоинфекций
ПТИ вызываются возбудителями, принадлежащими к родам Proteus, Clostridium, Citrobacter, Serratia, Klebsiella, Salmonella, Pseudomonas, Vibrio и др. Энтеротоксины этих бактерий термолабильны. Отдельной группой среди возбудителей ПТИ стоит Staphylococcus aureus. Культуры стафилококков обладают большой устойчивостью во внешней среде и длительно сохраняются в пищевых продуктах, переносят высокие концентрации соли (до 10%), погибают при прогревании до 80°С, а энтеротоксины данного возбудителя сохраняются даже при прогревании до 100°С.

Патогенез пищевых токсикоинфекций ( пти )
Патогенетические механизмы и тяжесть клиники зависят от вида и дозы энтеротоксина и наличия цитотоксина. Среди возбудителей, вырабатывающих кроме энтеротоксинов и цито-токсины, выделяют Clostridium perfringens, Clostridium difficile, Staphylococcus aureus, Klebsiella pneumoniae и ряд других микробов. ПТИ, вызываемые этими бактериями, протекают более тяжело.
Механизм действия энтеротоксина. Энтеротоксин взаимодействует с эпителием желудка и кишечника и активирует ферментные системы этих клеток, в частности, гуанилциклазу и аденилциклазу. Это приводит к увеличению в клетках кишечного и желудочного эпителия циклического аденозинмонофосфата (цАМФ) и циклического гуанидинмонофосфата (цГМФ). Также увеличивается синтез гистамина, простагландинов, кишечных гормонов и др. Все эти вещества вызывают увеличение секреции жидкости (и соответственно солей) в просвет ЖКТ. Вследствие этого развивается обильная рвота и диарея, приводящие к выраженной гиповолемии и нарушению электролитного баланса. Действие токсинов прекращается после отторжения клеток кишечного эпителия, с этим связана кратковременность течения ПТИ.
Цитотоксины, в отличие от энтеротоксина, вызывают повреждение мембраны клеток кишечного эпителия. Это приводит к увеличению секреции жидкости в просвет ЖКТ и снижает функцию всасывания. Кроме этого, увеличивается проницаемость кишечной стенки для токсинов, которые попадают в кровь, проникают в различные органы, связываются с митохондриями клеток печени, почек, селезенки, легких. Возникает повреждение эндотелия сосудов, что приводит к развитию геморрагических явлений. Все это вызывает развитие интоксикации, нарушение микроциркуляции и местные воспалительные изменения слизистой оболочки кишки. Иногда возбудитель проникает непосредственно в кровь, в результате чего может развиться сепсис.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Пищевые токсикоинфекции - острые кишечные инфекции, вызванные употреблением в пищу продуктов, содержащих микроорганизмы и их токсины. Пищевые токсикоинфекции характеризуются внезапным началом, приступами тошноты и многократной рвоты, диареей, схваткообразными болями в животе, повышением температуры и симптомами интоксикации. Диагностика пищевых токсикоинфекций производится путем бактериологического исследования рвотных масс, промывных вод желудка, испражнений, пищевых продуктов. При пищевых токсикоинфекциях необходимо промывание желудка, прием энтеросорбентов, ферментов, пробиотиков, проведение оральной или парентеральной регидратации.

Общие сведения
Пищевые токсикоинфекции (пищевой бактериотоксикоз) – это группа острых инфекционных заболеваний, возникающих в результате отравления человека пищевыми продуктами, содержащими производимые условно-патогенной флорой экзотоксины. Пищевые отравления протекают с явлениями острого гастроэнтерита, интоксикации и дегидратации. Восприимчивость к пищевым токсикоинфекциям всеобщая (80-100%); заболеваемость - повсеместная, по частоте уступающая лишь ОРВИ. Опасность пищевых токсикоинфекций обусловлена частотой возникновения массовых вспышек, сложностью обнаружения источника инфекции, возможностью развития инфекционно-токсического, дегидратационного шока и даже летального исхода, особенно среди детей и лиц пожилого возраста.

Причины
Возбудителем пищевой инфекции могут быть микроорганизмы различных родов: Klebsiella, Enterobacter, Citrobacter, Serratia, Enterococcus и др. Эти бактерии весьма распространены в природе, в подавляющем большинстве они входят в состав нормального биоценоза кишечника человека. Поскольку клиническая картина токсикоинфекции развивается в результате воздействия не самих микроорганизмов, а токсических продуктов их жизнедеятельности, возбудитель как таковой, нередко, не выделяется. Условно-патогенные бактерии способны изменять свои биологические свойства (устойчивость к антибиотикам и дезинфицирующим средствам, вирулентные характеристики) в результате воздействия факторов окружающей среды.
Источником и резервуаром инфекции, обычно, являются люди и сельскохозяйственные животные, птица. Чаще всего это лица, страдающие заболеваниями бактериальной природы с активным выделением возбудителя (гнойные заболевания, ангины, фурункулез), молочный скот, больной маститом. Стать источником заражения может и здоровый носитель. Для некоторых родов бактерий, способных вызвать пищевую токсикоинфекцию, резервуаром может служить почва и вода, загрязненные фекалиями животных и человека объекты окружающей среды.
Токсикоинфекции передаются по фекально-оральному механизму преимущественно пищевым путем. Микроорганизмы попадают в пищевые продукты, где происходит их активное размножение и накопление. Пищевая токсикоинфекция развивается тогда, когда человек употребляет в пищу продукты, в которых образовалась высокая концентрация микроорганизмов. Токсикоинфекции в подавляющем большинстве случаев возникают при употреблении продуктов животного происхождения: мяса, молочных продуктов, кондитерских изделий с жирными кремами, рыбы. Мясо и полуфабрикаты из него (фарш) являются основным источником клостридиальной инфекции. Некоторые способы изготовления полуфабрикатов и блюд, условия хранения и транспортировки способствуют прорастанию спор и размножению бактерий. Для продуктов, пораженных стафилококками, характерно отсутствие видимых и вкусовых отличий от нормальной пищи. В передаче инфекции могут принимать участие различные объекты и предметы, источники воды, почва, пыль. Для заболевания характерна сезонность: в теплое время года частота токсикоинфекций увеличивается, поскольку температура воздуха способствует активному размножению бактерий. Токсикоинфекции могут возникать как в виде отдельных случаев в быту, так и вспышками при организованном питании в коллективах.
Естественная восприимчивость у людей к данным инфекциям высокая, как правило, все, употреблявшие в пищу пораженные микроорганизмами продукты, заболевают с той или иной степенью тяжести. Лица с ослабленными защитными свойствами организма (дети первых лет жизни, старики, больные после хирургических вмешательств или прошедшие длительный курс антибиотикотерапии) входят в группу особого риска, токсикоинфекции у них могут протекать наиболее тяжело. В патогенезе токсикоинфекций основную роль играют токсины, выделяемые возбудителями. В зависимости от преимущественного типа токсинов различаются и особенности клинического течения.
Симптомы пищевых токсикоинфекций
Инкубационный период токсикоинфекции редко превышает несколько часов, но в некоторых случаях может укорачиваться до получаса или удлиняться до суток. Хотя возбудители токсикоинфекции довольно многообразны, клиническая картина при заражении, как правило, сходная. Заболевание обычно начинается остро, с приступов тошноты и многократной рвоты. Характерна энтеритная диарея с частотой дефекаций 10 раз в сутки и более. Могут наблюдаться боли в животе схваткообразного характера, повышение температуры (обычно длится не более суток), признаки интоксикации (озноб, ломота в теле, слабость, головная боль). Быстрая потеря жидкости с рвотой и калом приводит к развитию синдрома дегидратации. Больные, как правило, бледны, кожные покровы сухие, конечности холодные. Отмечается болезненность при пальпации в эпигастрии и около пупка, тахикардия, артериальная гипотензия. Заболевание обычно длится не более 1-3 дней, после чего клиническая симптоматика стихает.
Существуют некоторые особенности протекания токсикоинфекции в зависимости от характера возбудителя. При поражении стафилококками отмечается быстрое острое начало, преобладает желудочно-кишечная симптоматика, температура может оставаться нормальной или достигать субфебрильных цифр, диарея может отсутствовать. С первых же часов заболевания могут отмечаться судороги и цианотичность кожных покровов, но чаще всего острая клиника продолжается не более 1-2 дней и не вызывает серьезных нарушений водно-электролитного гомеостаза. Клостридиальное поражение похоже на таковое при стафилококковой инфекции, но для него более характерно поражение толстого кишечника с диареей, в кале может присутствовать кровь. Лихорадка обычно не отмечается. Протейная токсикоинфекция отличается зловонными каловыми массами.
Токсикоинфекции обычно протекают достаточно кратковременно и не оставляют последствий. В редких случаях: при тяжелом течении у лиц с ослабленным организмом, может развиваться дегидратационный шок, сепсис, острая сердечно-сосудистая недостаточность.
Диагностика
При диагностировании пищевых токсикоинфекций производят выделение возбудителя из рвотных масс, испражнений, промывных вод желудка. При выявлении возбудителя производят бакпосев на питательные среды и определяют его токсигенные свойства. Однако во многих случаях выявление невозможно. Кроме того, не всегда выявленные микроорганизмы являются непосредственной причиной токсикоинфекции. Связь возбудителя с заболеванием определяют либо посредством серологических тестов, либо, выделив его из пищевых продуктов и у лиц, употреблявших ту же пищу, что и больной.
Лечение пищевых токсикоинфекций
Первостепенным лечебным мероприятием при пищевой токсикоинфекции является максимально быстрое зондирование и промывание желудка (в первые же часы возникновения клинических признаков отравления). Если тошнота и рвота затягиваются, эту процедуру можно провести и позднее. Для освобождения от токсинов кишечника применяют энтеросорбенты и производят сифонную клизму. Для предупреждения дегидратации больному дают дробно небольшими порциями регидратационные растворы, сладкий чай. Количество жидкости, принимаемой больным, должно компенсировать ее потерю с рвотой и калом.
При развитии тяжелой степени дегидратации производят внутривенное введение регидратационных смесей. Больным с токсикоинфекцией на время острого периода рекомендовано лечебное питание. При тяжелом течении могут назначаться антибактериальные средства. После прекращения рвоты и диареи нередко рекомендуют ферментные препараты (панкреатин, трипсин, липаза, амилаза) для скорейшего восстановления пищеварения и пробиотики или продукты, содержащие необходимые для нормализации кишечного биоценоза бактерии.
Прогноз и профилактика
В подавляющем большинстве случаев прогноз благоприятный, выздоровление наступает на 2-3 день. Ухудшается прогноз при развитии осложнений, инфекционно-токсического шока. Общая профилактика токсикоинфекций заключается в мерах санитарно-гигиенического контроля на предприятиях и хозяйствах, чья деятельность связана с изготовлением, хранением, транспортировкой продуктов питания, а так же в учреждениях общественного питания, столовых детских и производственных коллективов. Кроме того, осуществляется ветеринарный контроль над состоянием здоровья сельскохозяйственных животных. Индивидуальная профилактика заключается в соблюдении правил личной гигиены, хранения и кулинарной обработки пищевых продуктов. Специфической профилактики, в силу многочисленности видов возбудителя и широкого распространения его в природе, не предусмотрено.
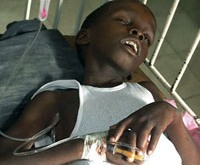
Холера – это острая кишечная инфекция, возникающая при поражении человека холерным вибрионом. Холера проявляется выраженной частой диареей, обильной многократной рвотой, что приводит к значительной потере жидкости и обезвоживанию организма. Признаками дегидратации служат сухость кожных покровов и слизистых, снижением тургора тканей и сморщивание кожи, заострение черт лица, олигоанурия. Диагноз холеры подтверждается результатами бактериологического посева каловых и рвотных масс, серологическими методиками. Лечение включает изоляцию холерного больного, парентеральную регидратацию, терапию тетрациклиновыми антибиотиками.
МКБ-10
Общие сведения
Холера – особо опасная инфекция, вызываемая энтеропатогенной бактерией Vibrio cholerae, протекающая с развитием тяжелого гастроэнтерита и выраженным обезвоживанием вплоть до развития дигидратационного шока. Холера имеет тенденцию к эпидемическому распространению и высокую летальность, поэтому отнесена ВОЗ к высокопатогенным карантинным инфекциям.
Наиболее часто эпидемические вспышки холеры регистрируются в странах Африки, Латинской Америки, Юго-Восточной Азии. По оценкам ВОЗ, ежегодно холерой заражается 3-5 млн. человек, около 100-120 тыс. случаев заболевания заканчивается смертельно. Т. о., на сегодняшний день холера остается глобальной проблемой мирового здравоохранения.

Причины холеры
Характеристика возбудителя
На сегодняшний день обнаружено более 150 типов холерных вибрионов, различающихся по серологическим признакам. Холерные вибрионы разделяют на две группы: А и В. Холеру вызывают вибрионы группы А. Холерный вибрион представляет собой грамотрицательную подвижную бактерию, выделяющую в процессе жизнедеятельности термостабильный эндотоксин, а также термолабильный энтеротоксин (холероген).
Возбудитель устойчив к действию окружающей среды, сохраняет жизнеспособность в проточном водоеме до нескольких месяцев, до 30 часов в сточных водах. Хорошей питательной средой является молоко, мясо. Холерный вибрион погибает при химическом дезинфицировании, кипячении, высушивании и воздействии солнечного света. Отмечается чувствительность к тетрациклинам и фторхинолонам.
Пути передачи
Резервуаром и источником инфекции является больной человек или транзиторный носитель инфекции. Наиболее активно выделяются бактерии в первые дни с рвотными и фекальными массами. Тяжело выявить инфицированных лиц с легко протекающей холерой, однако они представляют опасность в плане заражения. В очаге обнаружения холеры обследованию подвергаются все контактировавшие, вне зависимости от клинических проявлений. Заразность с течением времени уменьшается, и обычно к 3-й неделе происходит выздоровление и освобождение от бактерий. Однако в некоторых случаях носительство продолжается до года и более. Удлинению срока носительства способствуют сопутствующие инфекции.
Холера передается бытовым (грязные руки, предметы, посуда), пищевым и водным путем по фекально-оральному механизму. В настоящее время особое место в передаче холеры отводится мухам. Водный путь (загрязненный источник воды) является наиболее распространенным. Холера является инфекцией с высокой восприимчивостью, наиболее легко происходит заражение людей с гипоацидозом, некоторыми анемиями, зараженных гельминтами, злоупотребляющих алкоголем.
Симптомы холеры
Диспепсия
Инкубационный период при заражении холерным вибрионом продолжается от нескольких часов до 5 дней. Начало заболевания острое, обычно ночью или утром. Первым симптомом выступает интенсивный безболезненный позыв к дефекации, сопровождающийся дискомфортным ощущением в животе. Первоначально стул имеет разжиженную консистенцию, но сохраняет каловый характер. Довольно быстро частота дефекаций увеличивается, достигает 10 и более раз за сутки, при этом стул становится бесцветным, водянистым.
При холере испражнения обычно не зловонны в отличие от других инфекционных заболеваний кишечника. Повышенная секреция воды в просвет кишечника способствует заметному увеличению количества выделяемых каловых масс. В 20-40% случаев кал приобретает консистенцию рисового отвара. Обычно испражнения имеют вид зеленоватой жидкости с белыми рыхлыми хлопьями, похожими на рисовые.
Нередко отмечается урчание, бурление в животе, дискомфорт, переливание жидкости в кишечнике. Прогрессирующая потеря жидкости организмом приводит к проявлению симптомов обезвоживания: сухость во рту, жажда, затем появляется ощущение похолодания конечностей, звон в ушах, головокружение. Эти симптомы говорят о значительном обезвоживании и требуют экстренных мер по восстановлению водно-солевого гомеостаза организма.
Поскольку к диарее зачастую присоединяется частая рвота, потеря жидкости усугубляется. Рвота возникает обычно спустя несколько часов, иногда на следующие сутки после начала диареи. Рвота обильная, многократная, начинается внезапно и сопровождается интенсивным ощущением тошноты и болью в верхней части живота под грудиной. Первоначально в рвотных массах отмечаются остатки непереваренной пищи, затем желчь. Со временем, рвотные массы также становятся водянистыми, приобретая иногда вид рисового отвара.
При рвоте происходит быстрая потеря организмом ионов натрия и хлора, что приводит к развитию мышечных судорог, сначала в мышцах пальцев, затем всех конечностей. При прогрессировании дефицита электролитов мышечные судороги могут распространиться на спину, диафрагму, брюшную стенку. Мышечная слабость и головокружение нарастает вплоть до невозможности подняться и дойти до туалета. При этом сознание полностью сохраняется.
Выраженной болезненности в животе, в отличие от большинства кишечных инфекций, при холере не отмечается. 20-30% больных жалуются на умеренную боль. Не характерна и лихорадка, температура тела остается в нормальных пределах, иногда достигает субфебрильных цифр. Выраженная дегидратация проявляется снижением температуры тела.
Дегидратация
Дегидратация организма различается по стадиям:
- на первой стадии потеря жидкости не превышает 3% от массы тела;
- на второй - 3-6%;
- на третьей - 6-9%;
- на четвертой стадии потеря жидкости превышает 9% массы тела.
При потере более 10% массы тела и ионов происходит прогрессирование дегидратации. Возникает анурия, значительная гипотермия, пульс в лучевой артерии не прощупывается, периферическое артериальное давление не определяется. При этом диарея и рвота становятся менее частыми в связи с параличом кишечной мускулатуры. Данное состояние называют дегидратационным шоком.
Нарастание клинических проявлений холеры может прекратиться на любом этапе, течение может быть стертым. В зависимости от тяжести дегидратации и скорости нарастания потери жидкости различают холеру легкого, среднетяжелого и тяжелого течения. Тяжелая форма холеры отмечается у 10-12% пациентов. В случаях молниеносного течения развитие дегидратационного шока возможно в течение первых 10-12 часов.
Осложнения
Холера может осложняться присоединением других инфекций, развитием пневмонии, тромбофлебита и гнойного воспаления (абсцесс, флегмона), тромбозом сосудов брыжейки и ишемией кишечника. Значительная потеря жидкости может способствовать возникновению расстройств мозгового кровообращения, инфарктом миокарда.
Диагностика
Тяжело протекающая холера диагностируется на основании данных клинической картины и физикального обследования. Окончательный диагноз устанавливают на основании бактериологического посева каловых или рвотных масс, кишечного содержимого (секционный анализ). Материал для посева необходимо доставить в лабораторию не позднее 3-х часов с момента получения, результат будет готов через 3-4 суток.
Существуют серологические методики выявления заражения холерным вибрионом (РА, РНГА, виброцидный тест, ИФА, РКА), но они не являются достаточными для окончательной диагностики, считаясь методами ускоренного ориентировочного определения возбудителя. Ускоренными методиками для подтверждения предварительного диагноза можно считать люминисцентно-серологический анализ, микроскопию в темном поле иммобилизованных О-сывороткой вибрионов.
Лечение холеры
Поскольку основную опасность при холере представляет прогрессирующая потеря жидкости, ее восполнение в организме является основной задачей лечения этой инфекции. Лечение холеры производится в специализированном инфекционном отделении с изолированной палате (боксе), оборудованной специальной койкой (койка Филипса) с весами и посудой для сбора испражнений. Для точного определения степени дегидратации ведут учет их объема, регулярно определяют гематокрит, уровень ионов в сыворотке, кислотно-щелочной показатель.
Первичные регидратационные мероприятия включают восполнение имеющегося дефицита жидкости и электролитов. В тяжелых случаях производится внутривенное введение полиионных растворов. После этого производят компенсаторную регидратацию. Введение жидкости происходит в соответствии с ее потерями. Возникновение рвоты не является противопоказанием к продолжению регидратации. После восстановления водно-солевого баланса и прекращения рвоты начинают антибиотикотерапию. При холере назначают курс препаратов тетрациклинового ряда, а в случае повторного выделения бактерий – хлорамфеникол.
Специфической диеты при холере нет, в первые дни могут рекомендовать стол №4, а после стихания выраженной симптоматики и восстановления кишечной деятельности (3-5-й день лечения) - питание без особенностей. Перенесшим холеру рекомендовано увеличить в рационе содержащие калия продукты (курага, томатный и апельсиновый соки, бананы).
Прогноз и профилактика
При своевременном и полном лечении после подавления инфекции наступает выздоровление. В настоящее время современные препараты эффективно действуют на холерный вибрион, а регидратационная терапия способствует профилактике осложнений.
Специфическая профилактика холеры заключается в однократной вакцинации холерным токсином перед посещением регионов с высоким уровнем распространения этого заболевания. При необходимости через 3 месяца производят ревакцинацию. Неспецифические меры профилактики холеры подразумевают соблюдение санитарно-гигиенических норм в населенных местах, на предприятиях питания, в районах забора вод для нужд населения. Индивидуальная профилактика заключается в соблюдении гигиены, кипячении употребляемой воды, мытье продуктов питания и их правильной кулинарной обработке. При обнаружении случая холеры эпидемиологический очаг подлежит дезинфекции, больные изолируются, все контактные лица наблюдаются в течение 5-ти дней на предмет выявления возможного заражения.
Читайте также:

