Урологический сепсис что это такое
Обновлено: 22.04.2024
Уросепсис — это генерализованный неспецифический инфекционно-воспалительный процесс, вызванный проникновением в кровяное русло уроинфекционных патогенов и их токсинов. Проявляется внезапным ухудшением состояния, гипертермией, ознобами, тахикардией, олигурией, симптомами общей интоксикации, усугубляющими основную уропатологию. Диагностируется с помощью общего и биохимического анализов крови и мочи, УЗИ, КТ мочевыводящих органов, экскреторной урографии, микробиологических методов исследования. Для лечения уросепсиса проводится хирургическая санация очага инфекции в комбинации с антибактериальной, инфузионной, дезинтоксикационной, иммуномодулирующей терапией.
МКБ-10
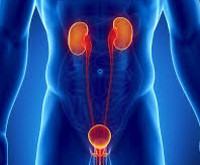
Общие сведения
Впервые о лихорадочных приступах, возникших после катетеризации и операций на уретре, в 1833-1837 годах сообщили французские хирурги А. Вельпо и Ж. Сивиаль. В 1899 году были описаны острая и хроническая формы мочевой лихорадки. В настоящее время распространенность уросепсиса в индустриально развитых европейских странах достигает 16,5-33 случаев на 100 тысяч населения, показатель продолжает ежегодно увеличиваться, при этом возрастает количество заболеваний, вызванных грамположительной флорой и кандидами.
По данным российских исследований, летальность при урогенной форме сепсиса остается стабильно высокой и составляет от 35 до 65%. Заболевание больше распространено у мужчин, что связано с более частым проведением эндоскопических инвазивных вмешательств у пациентов мужского пола.

Причины уросепсиса
Возбудителями заболевания являются те же микроорганизмы, которые обычно высеиваются у пациентов, страдающих острыми и хроническими инфекционными болезнями мочевыделительных органов. В 79-80% случаев уросепсис вызывается грамотрицательной условно-патогенной микрофлорой, в первую очередь – кишечной палочкой, реже — протеем, синегнойной палочкой, клебсиеллой, серратией, у 10-10,5% больных — грамположительными бактериями (энтерококками, эпидермальным стафилококком), в 0,75% наблюдений — кандидами. У 9% пациентов определяются полимикробные ассоциации. По мнению специалистов в сфере урологии и нефрологии, предпосылками, способствующими генерализации уроинфекции, являются:
- Воспалительные урологические заболевания. Обычно септическое состояние осложняет уже существующий инфекционный процесс. Более чем у половины больных уросепсис развивается на фоне острого и хронического пиелонефрита, особенно их апостематозных форм. Основной для генерализации инфекции также могут стать пионефроз, карбункул почки, паранефрит, острый абсцедирующий простатит, эпидидимит, гангрена Фурнье и др.
- Уростаз. Провоцирующим фактором активного размножения патогенной флоры является нарушение естественного пассажа мочи, обусловленное ренальными и постренальными причинами. Наиболее высок риск возникновения уросепсиса у пациентов с мочекаменной болезнью и обструкцией камнем мочеточника. Застой мочи возможен при стриктурах уретры, сморщенном мочевом пузыре, мочеточниково-влагалищных свищах, других обтурационных процессах.
- Медицинские манипуляции. Распространению инфекции способствует недостаточная санация мочевыводящих путей перед урологическими вмешательствами и нарушение техники их выполнения. Уросепсис может диагностироваться после грубой катетеризации мочевого пузыря, уретроскопии, цистоскопии, трансуретральной резекции простаты, мочевого пузыря, чрескожной нефролитотомии, других диагностических и лечебных вмешательств.
- Сопутствующая патология. Условно-патогенная микрофлора чаще активируется и бурно размножается у больных сахарным диабетом, хронической печеночной недостаточностью, кардиопатологией. Снижению иммунитета способствует прием иммуносупрессивных препаратов, применяемых для лечения аутоиммунных заболеваний, злокачественных опухолей, предотвращения отторжения трансплантированной почки или других органов.
Патогенез
По результатам последних исследований в области иммунологии и генетики, при уросепсисе бактериальный агент играет роль пускового фактора, запускающего каскадную гиперергическую воспалительную реакцию. В ответ на действие микробных эндотоксинов происходит активация комплемента, стимулирующая выделение гистамина. На фоне эндотоксемии повышается активность свертывающей системы крови, усиливаются адгезивные свойства тромбоцитов и нейтрофилов, в больших количествах выделяются медиаторы воспаления, кислородные радикалы, протеазы. В конечном итоге это приводит к множественному повреждению сосудистого эндотелия с последующим развитием полиорганной недостаточности. У части больных на фоне септицемии формируются вторичные гнойные метастазы в других органах.
Классификация
При выделении различных форм уросепсиса учитывают тип возбудителя, механизм его проникновения в кровоток, фазу и особенности клинического течения септического процесса. Различают бактериальные, вирусные, грибковые варианты заболевания. При наличии источника инфекции в органах мочевыводящего тракта уросепсис называют эндогенным, при инфицировании во время инвазивных процедур — экзогенным. Наиболее значимой для прогнозирования исхода и разработки оптимальной врачебной тактики является классификация процесса по динамике нарастания и выраженности симптоматики. Существуют следующие клинические формы септического состояния:
- Бактериемический уросептический шок. Самый неблагоприятный вариант течения расстройства. Отличается молниеносным нарастанием симптомов, выраженной полиорганной недостаточностью, высокими (до 60-65%) показателями летальности. Выявляется у 9,1% пациентов.
- Острый уросепсис. Обычно проявляется 2-3 общетоксическими атаками с ознобом и выраженной гипертермической реакцией. Хорошо поддается лечению. У некоторых больных принимает затяжной характер. Диагностируется в 56,6% случаев урогенных септических процессов.
- Подострый уросепсис. Интоксикационная симптоматика менее выражена. Заболевание имеет затяжной характер без четко ограниченных атак. Ведущим клиническим проявлением является стойкая гипертермия, сохраняющаяся до 2-3 месяцев. Определяется у 30% больных.
- Хронический уросепсис. Встречается у 4,3% пациентов. Не имеет острого периода. Симптоматика нарастает постепенно или проявляется волнообразно в виде обострений. Температура обычно повышается до субфебрильных цифр. Часто возникает почечная недостаточность.
Септический процесс развивается поэтапно и может быть стабилизирован на любой стадии. Начальная токсемическая фаза уросепсиса (синдром системной воспалительной реакции) характеризуется циркулированием в крови бактериальных эндотоксинов и развитием гиперергического воспаления. В септицемической фазе отмечается бактериемия, которая в дальнейшем может осложниться формированием гнойных метастазов (фаза септикопиемии).
Симптомы уросепсиса
Основными клиническими проявлениями молниеносной и острой форм заболевания являются резкое ухудшение состояния больного, длительно страдающего урологическим заболеванием либо перенесшего инвазивное вмешательство на мочевыводящих органах, высокая температура тела, сильный озноб, судороги, значительная тахикардия. Прогностически неблагоприятным симптомом считается гипотермия ниже 35,5° С. При уросепсисе часто наблюдается нарушение оттока мочи, уменьшение ее количества. Появляются и нарастают признаки общей интоксикации в виде головных болей, слабости, тошноты.
При присоединении сосудистых нарушений отмечается падение артериального давления, побледнение кожных покровов, оглушенность, спутанность, потеря сознания, мелкоточечные кровоизлияния. Для подострой и хронической форм уросепсиса характерен длительный субфебрилитет, который периодически можно сменяться кратковременными подъемами температуры до фебрильных цифр. У таких пациентов на фоне клинической симптоматики основного урологического расстройства сильно выражены интоксикационные астеновегетативные нарушения — быстрая утомляемость, слабость, головокружения, потливость, сердцебиение.
Осложнения
При стремительном прогрессировании симптомов, неадекватной терапии, нарастании коагулопатических расстройств уросепсис осложняется ДВС-синдромом. У 58,7% пациентов выявляется почечная недостаточность, у 55,5% появляются метастатические гнойные очаги в различных органах, у 42,2% поражается печень — возникает токсический гепатит, острая печеночная недостаточность, гепаторенальный синдром. В 14,8% случаев наблюдаются кровотечения разной локализации, в том числе из стрессовых язв желудка. На фоне полиорганной недостаточности повышается риск развития респираторного дистресс-синдрома, тяжелой энцефалопатии вплоть до септического психоза и мозговой комы. Уровень смертности при тяжелых септических процессах достигает 65%.
Диагностика
О возможном начале уросепсиса свидетельствует связь общетоксической реакции с предшествующим урологическим заболеванием или инвазивным вмешательством на органах мочевыделительной системы. Диагностический поиск направлен на выявление признаков системного воспаления, первичного инфекционного очага, определение возбудителя инфекционного процесса и его чувствительности к антибиотикам, оценку функциональной состоятельности почек. Рекомендованными методами обследований при подозрении на уросепсис являются:
- Общий анализ мочи. При наличии бактериальной уроинфекции определяется лейкоцитурия, бактериурия, возможна протеинурия. У пациентов, которые страдают мочекаменной болезнью, при микроскопии выявляют кристаллы солей (оксалатов, фосфатов, уратов). Присутствие неизмененных эритроцитов может указывать на травматическое повреждение слизистых при эндоскопии.
- Общий анализ крови. О развитии уросепсиса свидетельствуют выраженные воспалительные изменения показателей. Диагностически значимым является лейкоцитоз до 12х10 9 /л и более, лейкопения менее 4х10 9 /л, выявление более 10% незрелых форм лейкоцитов. СОЭ обычно ускоряется до 20 мм/ч и выше. При тяжелом течении снижаются уровни тромбоцитов и лимфоцитов.
- Сонография. УЗИ забрюшинного пространства позволяет обнаружить морфологические изменения почечной паренхимы, конкременты, обструкцию, скопления гноя. Преимуществами сонографии являются неинвазивность и возможность использования в качестве скринингового метода диагностики уропатологии. При необходимости УЗИ дополняют УЗДГ почек.
- Контрастная рентгенография. На основании данных о естественном пассаже рентгеноконтрастного вещества по мочевыводящему тракту оценивают особенности строения и функциональную активность почечной паренхимы, определяют конкременты в чашечно-лоханочной системе. В ходе экскреторной урографии выявляют обтурацию мочеточников и другие причины застоя мочи.
- КТ-урография. Благодаря созданию послойных изображений органов и тканей КТ мочевыделительных органов позволяет визуализировать абсцессы, кисты, опухоли, расширение чашечек и лоханок, другие морфологические нарушения в почках, забрюшинном пространстве. С учетом возможного нарушения фильтрации предпочтительным является бесконтрастное сканирование.
В качестве альтернативных или дополнительных методов диагностики могут быть рекомендованы МСКТ почек, МСКТ цистоуретрография, МРТ урография. Для определения возбудителя выполняется посев мочи на микрофлору и трехкратный бактериологический посев крови. Поскольку даже при самом тщательном проведении исследования микробиологическая верификация уросепсиса возможна лишь у половины пациентов, для выявления системного воспаления оценивают содержание в сыворотке крови прокальцитонина — суррогатного маркера генерализованной инфекционно-воспалительной реакции.
Меньшей специфичностью отличается повышение концентрации С-реактивного белка, альбуминов, отдельных фракций глобулинов. Для обнаружения возможной почечной дисфункции применяют биохимический анализ крови на креатинин, азот мочевины, мочевую кислоту, калий, назначают нефрологический комплекс. Дифференциальную диагностику уросепсиса проводят с хирургическими, акушерскими септическими состояниями, перитонитом, тяжелыми формами пиелонефрита, пионефроза, паранефрита, карбункулом и абсцессом почки, эндогенными интоксикациями (уремической, раковой). Диагностику и лечение осуществляет специалист-уролог или нефролог, по показаниям назначаются консультации других специалистов.
Лечение уросепсиса
Основными задачами при урогенных септических состояниях являются элиминация возбудителя, коррекция полиорганных расстройств, восстановление гомеостаза. С учетом тяжести состояния пациента рекомендуется госпитализация в палату интенсивной терапии урологического или реанимационного отделения и соблюдение строгого постельного режима. Этиотропное лечение уросепсиса предполагает эффективную санацию инфекционного очага и проведение адекватной антибактериальной терапии. Антибиотики назначают в два этапа:
- Эмпирическая антибиотикотерапия. Осуществляется до получения результатов бактериологического исследования. Схема лечения обычно включает комбинацию цефалоспоринов IV поколения с аминогликозидами или карбапенемы. При возможном инфицировании грамположительными микроорганизмами терапию дополняют трициклическими гликопептидами.
- Целенаправленная антибиотикотерапия. После получения данных о чувствительности возбудителя уросепсиса применяют соответствующий антибактериальный препарат узконаправленного действия. Во избежание формирования терапевтически резистентных штаммов микроорганизмов противомикробную терапию продолжают до 4-6 дня нормализации температуры.
Чтобы восстановить адекватную тканевую и органную перфузию, корректировать расстройства гомеостаза, уменьшить токсемию, проводят активную инфузионную и противошоковую терапию. При значительной артериальной гипотензии и дефиците ОЦК под контролем диуреза вводят кристаллоидные и коллоидные растворы, плазмозаменители, альбумин, прямые антикоагулянты, ксантиновые ингибиторы фосфодиэстеразы, селективные β₁-адреномиметики.
Пациенту с уросепсисом обеспечивают адекватное энтеральное питание специальными сбалансированными смесями. Для усиления иммунитета назначают заместительную терапию специфическими иммуноглобулинами, используют иммуномодуляторы. Эффективность лечения существенно возрастает при хирургической санации очага инфекции не позднее двух часов после диагностирования уросепсиса. С учетом состояния пациента выполняют чрескожную пункционную или классическую открытую нефростомию.
Для нормализации пассажа мочи при обструктивных состояниях может применяться эпицистостомия, уретеролитотомия, уретеролитоэкстракция. При значительной деструкции печеночной паренхимы показана экстренная нефрэктомия. С детоксикационной целью в предоперационном периоде и после операции рекомендованы экстракорпоральные методы: плазмаферез, плазмосорбция, гемофильтрация, гемодиафильтрация.
Прогноз и профилактика
Хотя при поздней диагностике и неэффективной терапии уросепсис характеризуется высокой вероятностью летального исхода, выявление расстройства на стадии токсемии позволяет снизить смертность с 65% до 7,5%. Профилактика основана на грамотной санации очагов уроинфекции, устранении обструкции мочевыводящих путей, проведении превентивной антибиотикотерапии перед диагностическими и лечебными урологическими вмешательствами, соблюдении техники выполнения медицинских процедур. Важную роль в предупреждении уросепсиса играют контроль своевременного опорожнения мочевого пузыря, снижающий риск избыточного накопления патогенов, укрепление иммунитета, исключение переохлаждений.
2. Уросепсис - актуальная проблема современной урологии/ Учваткин Г.В., Гайворонский Е.А. // Урологические ведомости. – 2017.
3. Этиопатогенетические аспекты развития гнойно-септических осложнений и уросепсиса у пациентов с урологическими заболеваниями до и после трансплантации почки: современный взгляд на проблему/ Крстич М., Зулькарнаев А.Б.// Альманах клинической медицины. - 2013 - №28.
4. Патогенетическое обоснование коррекции нарушений системного кровообращения в периоперационном периоде у больных с уросепсисом: Автореферат диссертации/ Адилбеков Е.А. – 2006.
Акушерский сепсис – это системное осложнение инфекций женской мочеполовой системы и молочной железы, развившееся во время беременности, изгнания плода и в послеродовом (послеабортном) периоде. Проявляется тяжёлым общим состоянием, нарастающей слабостью, лихорадкой, сердцебиением, одышкой, снижением артериального давления. По мере прогрессирования присоединяются помутнение сознания, выраженное затруднение дыхания, резкое уменьшение объёма отделяемой мочи. Диагноз устанавливается на основании данных физикального осмотра, УЗИ, лабораторных исследований крови. Лечение комплексное: хирургическая санация гнойников, антибиотикотерапия, интенсивная терапия.
МКБ-10
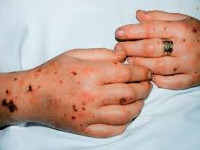
Общие сведения

Причины
Акушерский сепсис всегда вторичен, его источником является локальная инфекция. Основные возбудители гнойно-воспалительных заболеваний – представители оппортунистической флоры (пиогенный стрептококк, стрептококк группы B, золотистый стафилококк, кишечная палочка, клебсиелла, протей, пептококк, пептострептококк, бактероид, грибок кандида), чаще всего населяют нижние отделы мочеполовой сферы и кишечника и приводят к патологии только под воздействием определённых факторов. К основным причинам и источникам инфицирования относятся:
- Хирургические операции и травмы тканей. Раневая поверхность служит воротами инфекции и способствует значительному снижению местного иммунитета. Гнойный процесс может стать исходом кесарева сечения, раннего отхождения околоплодных вод (при неправильном положении плода, многоплодии), полученных в родах разрывов и оперативных вмешательств на промежности.
- Лечебно-диагностические манипуляции. Возбудитель передаётся при контакте с обсеменённым инструментом, кроме того, микротравмы, полученные при исследовании, создают благоприятные условия для лимфо- и гематогенного заражения. В группе факторов риска - цервикальный серкляж, амниоцентез, кордоцентез, уретральная катетеризация, экстракорпоральное оплодотворение, многократные влагалищные исследования в ходе родов.
- Физиологические изменения, вызванные беременностью. Растущая матка сдавливает и смещает окружающие анатомические структуры, а прогестерон снижает тонус гладкой мускулатуры. Эти факторы приводят к нарушению уродинамики и создают предпосылки для развития гестационного пиелонефрита и уросепсиса.
- Застой грудного молока. В результате лактостаза происходит активный рост стафилококков, вызывающих мастит. Нарушение оттока молока – основная причина послеродовых абсцессов и флегмон.
С другой стороны, гнойные процессы могут осложниться сепсисом лишь при условии гипо- или гиперреактивности иммунного ответа. Функциональные расстройства иммунной системы приводят к усилению активности оппортунистических микроорганизмов и формированию патологической реакции на гнойное воспаление. К факторам риска относятся ожирение, сахарный диабет, анемия, острые и хронические воспаления (генитальные и экстрагенитальные), недостаток питания, возраст старше 35 лет.
Патогенез
Массивное поражение ткани инфекцией сопровождается перманентным или периодическим выбросом в кровоток медиаторов воспалительного ответа, что истощает регуляторную функцию иммунной системы и запускает ряд неконтролируемых реакций в дистантных органах и тканях. В результате повреждается эндотелий, ухудшается микроциркуляция (перфузия), снижается транспорт кислорода. Эти изменения приводят к нарушениям гомеостатической регуляции, развитию синдрома острой полиорганной недостаточности (СПОН) и ДВС-синдрома.
Желудочки сердца расширяются, происходит снижение сердечного выброса, нарушается сосудистый тонус. В лёгких образуются ателектазы, развивается респираторный дистресс-синдром. В результате снижения объёма циркулирующей крови (ОЦК) и гемостатических нарушений ухудшается микроциркуляция почечной ткани и кровоснабжение коркового слоя с последующей острой функциональной недостаточностью. В печени нарушаются обменные процессы, а недостаток кровоснабжения влечёт формирование некротических участков. Гипоперфузия приводит к патологической проницаемости слизистой оболочки кишечника с выбросом токсинов и микроорганизмов в лимфатическую систему, в результате ишемии на стенках органов ЖКТ образуются стрессовые язвы. Нарушение обменных процессов и микроциркуляции головного мозга обусловливает неврологические расстройства.
Классификация
Акушерский сепсис классифицируют по разным критериям: по возбудителю, по метастатическому распространению (септицемия, характеризующаяся наличием лишь первичного очага, и септикопиемия – наличие гнойных отсевов в других тканях и органах) или по клиническому течению. В современном акушерстве принята классификация, отражающая последовательные этапы формирования системной воспалительной реакции:
- Синдром системного воспалительного ответа (ССВО). Предвестник септического состояния – системная реакция на воспалительный процесс любой этиологии. Устанавливается при наличии воспалительного заболевания и на основании не менее двух клинических проявлений ССВО: тахикардии, тахипноэ или гипервентиляции, гипо- или гипертермии, лейкоцитоза (лейкопении) или повышения доли незрелых нейтрофилов. У 12% больных сепсисом признаки ССВО отсутствуют.
- Сепсис. Патологический системный ответ на первичную или присоединившуюся инфекцию. Диагноз выставляется при наличии инфекционного очага или на основании верифицированной бактериемии и остро развившихся признаков функциональной недостаточности двух и более органов (СПОН).
- Септический шок. Крайняя форма патологической реакции. Сопровождается выраженными, стойкими, плохо поддающимися медикаментозной коррекции гипотензией и нарушением перфузии.
Симптомы акушерского сепсиса
Послеродовый сепсис манифестирует на второй-третий день после изгнания плода сукровично-гнойными выделениями, явлениями общей интоксикации (тахикардией, одышкой, слабостью, потерей аппетита, иногда рвотой и диареей) и повышением температуры до 39-40°C с ознобами. Гипертермия обычно устойчивая, однако могут наблюдаться формы с постепенным повышением или большим разбросом суточной температуры и редкими приступами ознобов. Отмечаются боли в животе или молочных железах, могут регистрироваться генерализованные высыпания. Выраженность симптомов и длительность заболевания различны в зависимости от формы клинического течения.
Для молниеносного акушерского сепсиса нарастание симптоматики характерно в течение суток, при острой форме клиническая картина разворачивается в течение нескольких дней. При подострой форме признаки выражены менее ярко, процесс развивается неделями. Хрониосепсис характеризуется слабо выраженными изменениями (субфебрилитетом, повышенным потоотделением, головной болью и головокружениями, сонливостью, диареей) и вялым течением в течение многих месяцев. Рецидивирующая форма представляет череду затуханий (периодов ремиссии без заметных проявлений) и обострений (периодов с яркой симптоматикой) и характерна для септикопиемии, когда ухудшение состояния обусловлено повторными эпизодами образования вторичных гнойников.
Особенно тяжёлым течением и рядом специфических признаков отличается анаэробный сепсис, ассоциированный с гангреной матки. Заболевание протекает молниеносно или остро, сопровождается интенсивной некупируемой болью внизу живота, крепитацией и усилением боли при пальпации матки, выделением из влагалища газа и зловонной жидкости с пузырьками воздуха, бронзовой окраской кожи, бурым цветом мочи. Явления септического шока проявляются уже в самом начале болезни.
Осложнения
У больных, переживших острый период, может развиться тяжёлое, нередко летальное осложнение – суперинфекция. Значительное ухудшение качества жизни или гибель пациентки часто влекут другие последствия сепсиса: сопряжённые с ишемией или гнойным метастазированием необратимые органные изменения почек, печени, лёгких, сердца, головного мозга, прободение и кровотечения из гастроэнтеральных стресс-язв, артериальная тромбоэмболия и флеботромбоз. Сепсис у беременных может вызвать преждевременные роды, гибель плода, энцефалопатию и ДЦП рожденного ребенка.
Диагностика
В диагностике акушерского сепсиса участвуют акушер-гинеколог, терапевт, реаниматолог, микробиолог, осложнённые формы требуют привлечения нефролога, кардиолога, невролога, гепатолога. В ходе гинекологического исследования и общего осмотра по наличию очага гнойного воспаления в органах малого таза или молочной железе, а также признакам ССВО можно заподозрить септическое состояние. Проводятся следующие исследования:
- Определение возбудителя. Культуральный анализ крови и влагалищного мазка позволяют выявить инфекционный агент и подобрать эффективный препарат для лечения инфекции. Бактериемия подтверждает наличие септического процесса. При отсутствии бактериемии для дифференцирования локальной и генерализованной инфекции проводится тест на прокальцитонин.
- Инструментальные исследования. УЗИ малого таза и почек подтверждает (выявляет) наличие первичного гнойного очага в мочеполовых органах. УЗИ органов брюшной полости, рентгенография органов грудной клетки, ЭхоКГ позволяют обнаружить вторичные абсцессы в печени, лёгких, сердце.
- Клинико-биохимические анализы крови. Общий анализ крови обнаруживает лейкоцитоз, лейкопению, сдвиг лейкоцитарной формулы влево – значения, косвенно подтверждающие септическое состояние. Данные биохимического исследования говорят о нарушениях водно-электролитного баланса и функций почек, печени. Анализ газов крови выявляет нарушения КЩС и дыхательную недостаточность. По результатам коагулограммы определяются нарушения свёртывания крови. Тестирование уровня лактата в плазме позволяет обнаружить тканевую гипоперфузию и оценить тяжесть шока. Иммунограмма свидетельствует о расстройствах иммунной активности.
Акушерский сепсис следует дифференцировать с гестозами, амниотической эмболией и тромбоэмболией лёгочной артерии, острыми инфекциями (тяжёлым гриппом, бруцеллёзом, тифом, малярией, милиарным туберкулёзом), острым панкреатитом, лейкозами, лимфогранулематозом. Для дифференциальной диагностики может потребоваться консультация кардиохирурга, инфекциониста, фтизиатра, онкогематолога.
Лечение акушерского сепсиса
Лечебные мероприятия проводятся в условиях гинекологического или обсервационного акушерского отделения, больные с тяжёлыми формами сепсиса переводятся в отделение реанимации и интенсивной терапии. Лечение комплексное, включает хирургические и консервативные методы и направлено на борьбу с инфекцией и коррекцию витальных функций:
- Инфузионная терапия. Лечение предусматривает коррекцию гомеостатических расстройств (гипотонии, коагулопатии, нарушений кислотно-щелочного и водно-солевого и обмена, дефицита ОЦК), восстановление тканевой перфузии, дезинтоксикацию. С этими целями вводятся солевые и коллоидные растворы, альбумин, криоплазма, инотропы и вазопрессоры.
- Антибактериальная терапия. Направлена на уничтожение инфекционного агента с целью блокировки воспалительного каскада. Стартовое лечение включает внутривенное введение комбинации препаратов широкого спектра. После выделения возбудителя приступают к этиотропной антибиотикотерапии.
- Хирургическое лечение. Ликвидация гнойных очагов повышает эффективность интенсивной терапии и улучшает прогноз. Лечение предполагает санацию первичного и вторичных очагов – вскрытие и опорожнение абсцессов, кюретаж, вакуум-аспирацию или удаление матки (гистерэктомию).
В случае необходимости проводится искусственная вентиляция лёгких, энтеральное питание пациентки. Дополнительные методы интенсивной терапии включают применение кортикостероидов, выполнение хирургической детоксикации (плазмаферез, гемосорбция, гемофильтрация) после оперативного лечения нагноений, иммунотерапию.
Прогноз и профилактика
На ранних стадиях, когда не развились выраженные признаки СПОН, устойчивая гипотензия и ДВС-синдром, прогноз благоприятный. При развитии септического шока смертность может достигать 65% (в среднем – 45%). Профилактические мероприятия состоят в своевременном лечении воспалительных заболеваний (как на этапе планирования, так и в течение беременности), борьбе с внебольничными вмешательствами (внутриматочными и вагинальными манипуляциями, криминальными абортами, домашними родами), рациональной превентивной антибиотикотерапии при оперативных вмешательствах, полноценном питании, стабилизации уровня глюкозы в крови при сахарном диабете.
3. Клинические рекомендации по диагностике и лечению тяжелого сепсиса и септического шока в лечебно-профилактических организациях Санкт-Петербурга. – 2016.
4. Гнойно-воспалительные заболевания и сепсис в акушерстве. Клинические рекомендации (протокол лечения)/ Коллектив авторов. – 2015.
Что такое абсцесс простаты? Причины возникновения, диагностику и методы лечения разберем в статье доктора Лелявина Кирилла Борисовича, уролога со стажем в 29 лет.
Над статьей доктора Лелявина Кирилла Борисовича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Абсцесс предстательной железы — это жизненно опасное полиэтиологическое гнойно-некротическое воспалительное заболевание, при котором происходит гнойное расплавление железистых тканей простаты с последующим формированием одиночной или множественных гнойных полостей. Возникший абсцесс в предстательной железе требует безотлагательного, незамедлительного стационарного лечения.
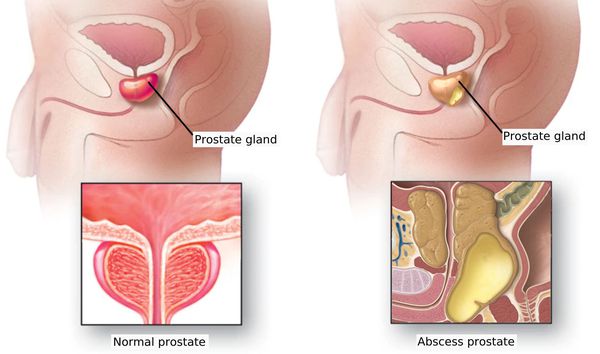
Простатический абсцесс в большинстве случаев является серьёзным осложнением острой или хронической инфекции нижних мочевых путей и возникает в результате очагового скопления гноя в предстательной железе.
В современную эпоху широко применения антибактериальных препаратов частота возникновения абсцесса простаты существенно снизилась. На сегодняшний день распространенность данной патологии составляет около 0,5-2,5% от всех заболеваний предстательной железы и 0,2% от всех урологических болезней. [1]
Заболевание стало достаточно редким явлением особенно в развитых странах. На существенное снижение частоты возникновения абсцесса простаты повлияло уменьшение заболеваемости гонококковым уретритом, так как до появления современной антибиотикотерапии 75% абсцессов предстательной железы были вызваны именно гонококком, а уровень смертности от патологии составлял от 6 до 30%. [2] В то же время, несмотря на небольшую распространённость заболевания, своевременная диагностика и адекватное лечение абсцессов простаты остаются серьёзными проблемами для врачей-урологов.
С момента появления антибиотикотерапии бактериология абсцессов простаты изменилась. Исторически возбудителями абсцесса простаты являлись гонококк, золотистый стафилококк и палочка Коха. В настоящее время наиболее часто встречающимися возбудителями заболевания являются грамотрицательные бактерии, такие как кишечная палочка и стафилококк. [3]
Предрасполагающие факторы возникновения заболевания:
- различные инструментальные манипуляции на уретре;
- использование постоянных уретральных катетеров;
- хроническая почечная недостаточность (длительный гемодиализ);
- иммуносупрессия (ВИЧ-инфекция);
- трансплантация органов.
Большинство простатических абсцессов развивается в результате или на фоне острого и хронического простатита, а также после проведения биопсии простаты. Так, по данным литературы, абсцесс предстательной железы осложняет течение острого простатита примерно в 5% случаев и является результатом прогрессирования острого паренхиматозного воспаления в предстательной железе. [8]
У пожилых пациентов абсцесс предстательной железы может осложнить течение доброкачественной гиперплазии простаты. У более молодых мужчин абсцесс предстательной железы может быть первоначальным проявлением таких хронических состояний, как сахарный диабет, ВИЧ-инфекция и цирроз печени. Так, более 50% мужчин, страдающих от абсцесса предстательной железы, имеют сахарный диабет.
В специализированной литературе были описаны случаи гематогенного бактериального распространения инфекции из отдалённых очагов (например, пищеварительного тракта и дыхательных путей). [5]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы абсцесса простаты
На фоне широкого использования антибиотиков простатический абсцесс стало достаточно сложно своевременно диагностировать, поскольку он имитирует и скрывается под маской других заболеваний нижних мочевых путей. [5]
Наиболее выраженными клиническими проявлениями заболевания являются признаки тяжёлого септического состояния:
- повышение температуры тела (гектического характера, т.е. в форме изнуряющей лихорадки) с ознобами;
- интоксикация;
- повышенная потливость и сердцебиение;
- возможно присоединение нарушения сознания.
Со стороны органов мочевыводящей системы может развиться:
- учащённое мочеиспускание;
- дизурия (например, болезненность и затруднение при выделении мочи);
- иногда острая задержка мочеиспускания и гематурия (присутствие крови в моче). [4][5]
Пациентов беспокоит боль в поясничной области и промежности. Отличительной чертой является то, что болевой синдром имеет одностороннюю локализацию, которая соответствует поражённой воспалительным процессом доле простаты.
По характеру болевой синдром — интенсивный, резкий, с пульсацией, как правило, распространяющийся на прямую кишку. В некоторых случаях отмечается нарушение, вплоть до задержки мочеиспускания и дефекации, иногда затруднено отхождение газов.
Вышеперечисленные клинические проявления заболевания характерны для стадии инфильтрации. После перехода патологического процесса происходящего в простате в стадию гнойной деструкции или в период отграничения абсцесса наступает некоторое "улучшение" состояния пациента:
- уменьшается интенсивность болевого синдрома;
- понижается температура тела.
Однако такое благополучие — мнимое, так как именно в этот период может произойти прорыв сформировавшегося гнойника в клетчатку, расположенную вокруг уретры или паравезикальное клетчаточное пространство, которое находится вокруг мочевого пузыря, с последующим развитием грозных осложнений (например, флегмоны).
После того, как произошёл спонтанный прорыв абсцесса в клетчатку, расположенную вокруг уретры (мочеиспускательного канала), возможно:
- появление гноя в моче;
- изменение цвета и характера мочи (она становится мутной, появляются хлопья);
- присоединение неприятного резкого запаха.
В некоторых случает происходит вскрытие гнойника простаты в просвет прямой кишки с последующем формированием прямокишечного свища. В данной ситуации пациенты отмечают появление примеси слизи и гноя в кале.
Следует обратить внимание, что после прорыва гнойника не происходит полное опорожнение полости абсцесса, поэтому в дальнейшем возможен рецидив заболевания.
Абсцесс простаты на фоне иммунодефицита (ВИЧ-инфекции) имеет свои характерные особенности. У данной категории пациентов существенно преобладают симптомы интоксикации:
- слабость;
- мышечные боли;
- длительное повышение температуры тела до субфебрильных цифр;
- боли в суставах. [4][5]
В тоже время локальные проявления простатического абсцесса менее выражены. Иногда только при подробном расспросе удаётся выявить незначительное ухудшение мочеиспускания и появление тянущих болей в области промежности.
У ВИЧ-инфицированных пациентов абсцесс простаты может протекать на фоне септикопиемии (особенно у героиновых наркоманов).
Патогенез абсцесса простаты
Предстательная железа имеет довольно высокую природную устойчивость к экзогенному и эндогенному инфицированию. Поэтому воспалительный процесс возникает только при угнетении или снижении локального (местного) иммунитета и при очень высокой вирулентности микроорганизмов.
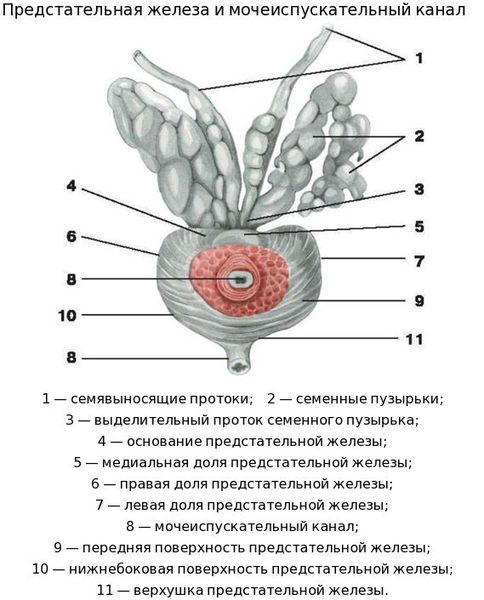
При абсцессе простаты инфекционные агенты попадают в ткань железы тремя способами:
- через выводные отверстия протоков, располагающиеся на задней части мочеиспускательного канала;
- лимфогенным путём (при длительном нахождении мочевого катетера);
- гематогенным путём, т. е. через кровь (при бактериемии).
Воспаление в предстательной железе сопровождается выделением большого количества лейкоцитов и микроорганизмов. Далее в результате лечения или мобилизации собственных защитных сил организма происходит отграничение очага острого или хронического воспаления.
Некоторые авторы предполагают, что абсцесс простаты в основном является осложнением бактериального простатита, острого или хронического, чаще всего наблюдаемого у мужчин в 50-60 лет, однако абсцесс может возникать в любом возрасте. [6]
В настоящее время энтеробактерии, особенно кишечная палочка, являются основными возбудителями острого бактериального простатита и абсцесса предстательной железы. Реже встречаются Klebsiella sp., Proteus mirabilis, Enterococcus faecalis и Pseudomonas aeruginosa. [7] В последнее время в литературе отмечается рост числа случаев метициллинрезистентного золотистого стафилококка в качестве возбудителя абсцесса простаты.
В таблице представлены возбудители острого простатита и абсцесса предстательной железы.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
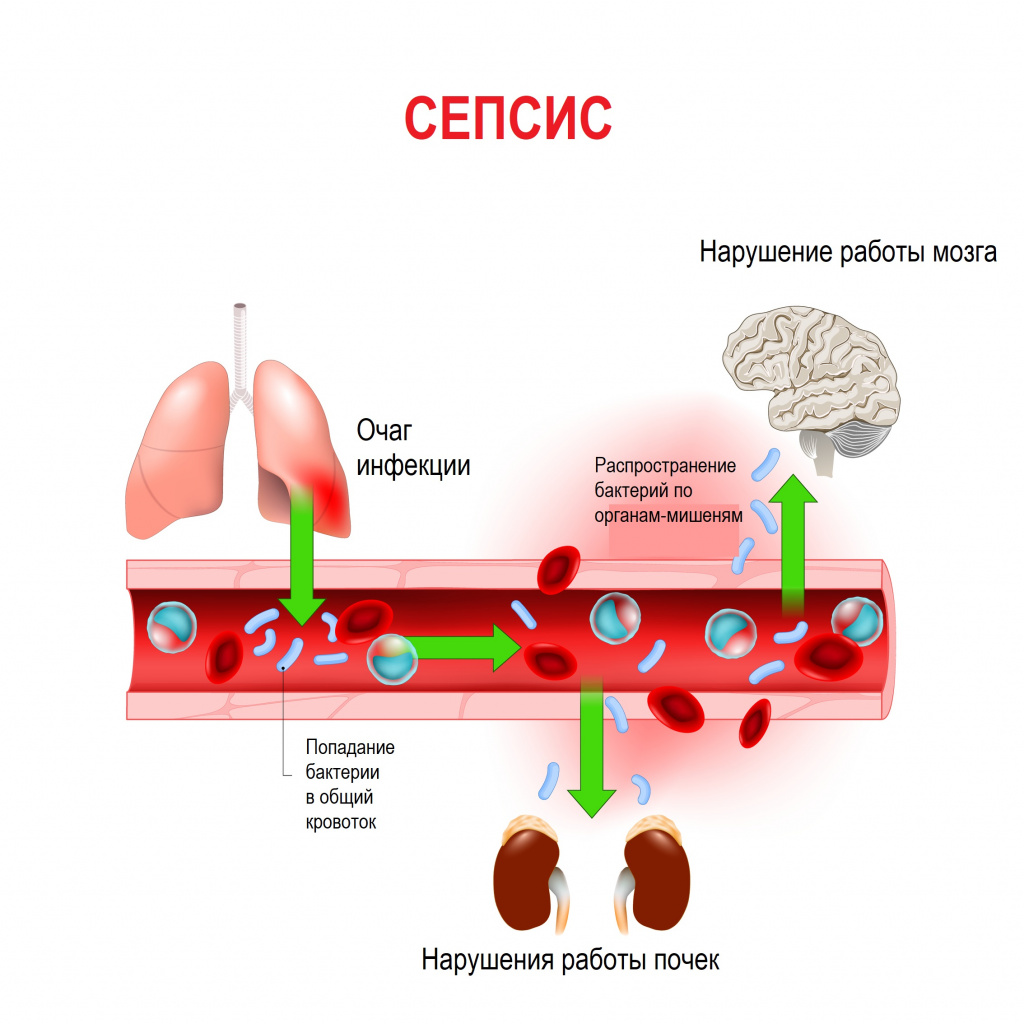
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
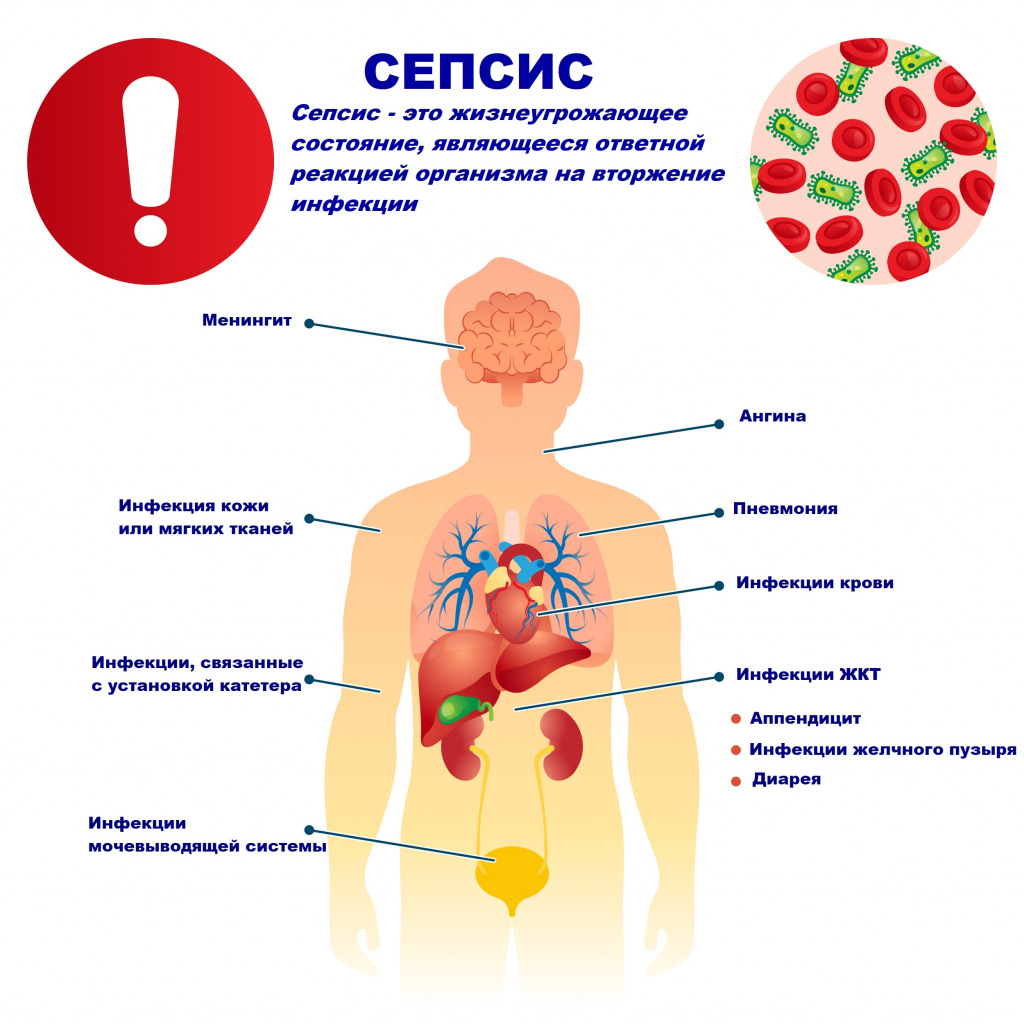
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Читайте также:

