Устойчивый штамм при туберкулезе
Обновлено: 13.05.2024
Лекарственно устойчивые штаммы туберкулёза возникают естественным путём в ходе спонтанного мутагенеза как ответная реакция на введение антибиотиков. Они, как правило, обладают слабым фитнесом, т.е. они медленнее растут, слабее размножаются, у них нет других преимуществ, за исключением устойчивости к антибиотикам. И, соответственно, первоначальная стратегия при столкновении с лекарственно устойчивыми штаммами заключалась в том, чтобы, во-первых, антибиотики, направленные на лечение туберкулёза, были изъяты из широкой сети обращения и использовались только в специализированных учреждениях и, во-вторых, курс лечения проводился особым образом: сначала больного лечили антибиотиками, потом делали перерыв, за это время оставшиеся лекарственно чувствительные штаммы начинали доминировать, соответственно вытесняя лекарственно устойчивые варианты, затем опять проводили химиотерапию, достигали хороших результатов, что снова приводило к появлению лекарственно устойчивых штаммов, снова делали перерыв и так до полного излечения. Но потом оказалось, и обнаружили это, прежде всего в Африке, что такие проблемы как СПИД, который поражает иммунную систему, приводят к значительному росту числа лекарственно устойчивых штаммов. Причём если раньше эти штаммы были в основном в лечебных учреждениях, то теперь они стали обнаруживаться во всей популяции. И наиболее распространённая на сегодняшний день теория, для которой находится всё больше и больше подтверждений, заключается в том, что для того, чтобы лекарственно устойчивые штаммы вырвались в популяцию, они должны пройти несколько циклов размножения в организме со слабой иммунной системой, а именно такими объектами являются, прежде всего, больные СПИДом. Далее обнаружилось, что в странах, где происходят колоссальные социальные пертурбации, где всё рушится, возникает большая прослойка бедных, социально дезориентированных людей, у которых доходы ниже прожиточного реального минимума и иммунная система ослаблена, и такие люди тоже становятся тем резервуаром, в котором лекарственно устойчивые штаммы могут адаптироваться и приобрести такие преимущества, которые позволяют им конкурировать с лекарственно чувствительными штаммами. Таким образом с появлением и распространением СПИДа в мире, а также с началом таких крупных социальных потрясений, как в бывших странах СНГ, появились две большие зоны, включающие Африку, Азию, страны СНГ, где лекарственно устойчивые штаммы стали стремительно распространяться.
И тогда первыми забеспокоились международные организации, потому что эпидемия любого заболевания, в том числе и туберкулёза, в одной стране, является проблемой многих. В данном случае это было связано и усугублялось миграцией, поскольку открылись все ворота, люди стали эмигрировать из бывшего Советского Союза, и в Западной Европе вдруг стали обнаруживать те генотипы туберкулёза, которые раньше там не регистрировались.
Несмотря на то, что со дня открытия туберкулёза прошло уже больше ста лет, микобактерия хорошо изучена, известен и расшифрован её геном, но, тем не менее, мы пока не имеем надёжных средств вакцинации от туберкулёза. Спектр имеющихся лекарственных препаратов из-за проблемы лекарственной устойчивости приходится постоянно расширять и модифицировать, и ещё одна большая проблема – это проблема ранней диагностики туберкулёза.
В России Т-клеточные технологии пока не внедрены. А в мире эти технологии уже внедрены в Германии и США, в специализированных крупных центрах, что надо делать и нам. Там не только есть центры, но действует система иммунологического мониторинга и система мониторинга генотипов микобактерии туберкулёза. Это позволяет реально оценивать эффективность всех противотуберкулёзных мероприятий, позволяет изучать процессы, которые реально происходят с микобактерией туберкулёза, вовремя выявлять эпидемические очаги, а не работать, как это делали раньше, по территориям в целом.
Рисунок 1. У пациентов могут быть неспецифические или атипичные симптомы. Исследования необходимо проводить при малейшем подозрении на туберкулез Как сегодня проявляется туберкулез? Каковы общие проблемы ведения больных? Как можно с
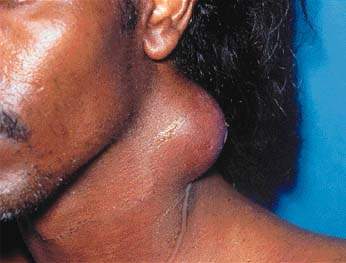 |
| Рисунок 1. У пациентов могут быть неспецифические или атипичные симптомы. Исследования необходимо проводить при малейшем подозрении на туберкулез |
Как сегодня проявляется туберкулез?
Каковы общие проблемы ведения больных?
Как можно свести к минимуму частоту развития множественной резистентности при туберкулезе?
Во всем мире, в особенности в развивающихся странах, ТБ представляет огромную проблему. Смертность при туберкулезе занимает первое место, если говорить об общей смертности взрослых от инфекционных болезней. Регистрируется примерно восемь миллионов новых случае заболевания и три миллиона смертей ежегодно. При правильном подходе ТБ излечим, причем зачастую пациенты выздоравливают достаточно быстро.
Таблица 1. Важные моменты анамнеза и симптомы
- Симптомы, ассоциированные с находками на рентгенограмме: кашель, боль в груди и кровохарканье
- Лихорадка и ночные поты
- Потеря веса
- Социоэкономическая депривация
- Пациент относится к этнической группе, в которой высока заболеваемость ТБ
- Пациенты с внутривенным введением лекарств или наркоманией в анамнезе
- ТБ в семейном или индивидуальном анамнезе
- Вторичный иммунодефицит из-за ВИЧ-инфекции, лекарственных препаратов или гематологических злокачественных заболеваний
- Недавняя поездка в регион с высокой заболеваемостью
В противном случае можно ожидать самого худшего, в том числе смертельного исхода. К сожалению, ТБ так и не стал достоянием истории, и в наше время он встречается достаточно часто; можно сказать, что особенности течения заболевания бросают сегодня вызов всем нашим клиническим приемам.
Пациенты могут поступать в клинику с неспецифическими или атипичными проявлениями, поэтому необходимо постоянно иметь в виду ТБ и при малейшем подозрении проводить обследование.
Классическими симптомами легочного ТБ являются кашель, лихорадка, потеря веса, кровохарканье и ночные поты. Однако у пациента может вообще не быть симптомов данного заболевания или оказывается налицо всего один-два из них. Ключ к решению проблемы дает анамнез, особенно анализ социальных условий (табл. 1).
Частые жалобы на инфекции дыхательных путей, боли в спине или дизурия должны насторожить врача. Особое внимание следует проявить, если эти жалобы хронические и связаны с системными симптомами, такими как лихорадка или потеря веса, или пациент принадлежит к группе повышенного риска (например, к группе лиц, контактировавших с больным ТБ, или входящих в этническую группу, в которой выявлена повышенная заболеваемость) (табл. 2).
Таблица 2. Атипичные проявления
 |
| Рисунок 2. Рентгенограмма: туберкулезная каверна в левом легком у женщины с диабетом, у которой наблюдалась лихорадка и потеря веса в течение нескольких месяцев |
Помните, что мокрота, моча, гной и любая ткань, отправляемая на анализ, не проходит автоматически исследования на туберкулез — об этом надо попросить особо.
Департамент здравоохранения рекомендует проводить лекарственную терапию ТБ независимо от того, какой орган поражен, под руководством соответствующего клинического специалиста. Как правило, это консультант по респираторным инфекциям. Если затронуты и другие органы, привлекают соответствующих специалистов, например нейрохирургов, гастроэнтерологов и урологов.
Таблица 3. Препараты, воздействующие на Mycobacterium tuberculosis
Несмотря на необходимость вмешательства специалиста, роль врача общей практики трудно переоценить. По меньшей мере в течение шести месяцев необходимо соблюдать сложный режим лечения (табл. 3), жизненно важным оказывается сотрудничество и работа в одной команде врача общей практики, пациента, фтизиатра и специализированной медицинской сестры.
 |
| Рисунок 3. Внутривенная урография: расширенные и измененные за счет почечного ТБ лоханки. Пациент имеет симптомы цистита и лейкоциты в моче |
К сожалению, часто лекарственная терапия, проводимая без контроля фтизиатра, способствует увеличению заболеваемости, смертности, ведет к частым рецидивам и возникновению лекарственной устойчивости.
Лекарства и дозы устанавливает специалист. Однако как при назначении, так и при выдаче лекарств очень часты ошибки: назначают один рифампицин, забывая о существовании рифинаха или римактацида (комбинированные рифампицин и изониазид), и ошибочно приравнивают две таблетки рифинаха 150 к одной таблетке рифинаха 300 (они отличаются содержанием изониазида).
Важно помнить, что использование неадекватных лекарственных схем ведет к развитию множественной лекарственной резистентности.
Не стоит забывать и о побочном действии лекарств. Большинство антитуберкулезных препаратов вызывают лекарственный гепатит, поэтому в ТБ-отделении тщательно исследуется функция печени, особенно в первые шесть недель лечения.
Этамбутол может вызывать неврит глазного нерва, поэтому в начале лечения пациента должен осмотреть офтальмолог. Нужно попросить больного сообщать о всех изменениях в зрении.
Сыпь сопровождает прием большинства противотуберкулезных препаратов, а артралгии — обычный побочный эффект пиразинамида. Большинство реакций преходящи, но в тяжелых случаях нужно отменить все препараты и обратиться за помощью к специалисту. Отмена одного или двух препаратов, особенно на длительное время, может приводить к лекарственной устойчивости.
 |
| Рисунок 4. Компьютерная томограмма: большие зоны разрушения тела позвонка. Пациент поступил с параплегией и данными анамнеза о боли в спине, лихорадке и потере веса в течение года |
 |
| Рисунок 5. Компьютерная томограмма головы молодого человека, поступившего с жалобами на давно мучившие его головные боли, относимые за счет перенапряжения. Кольцевидные тени — это туберкулемы |
Изоляция пациентов. Пациенты с открытой, или ТБ+, формой заболевания (то есть микобактерии обнаруживаются при микроскопическом исследовании мазков мокроты) действительно могут быть госпитализированы на первые две недели лечения, в особенности если дома есть маленькие дети. Однако большинству пациентов достаточно лечиться амбулаторно при постоянном контроле функции печени.
Уведомление и выявление контактов. Согласно закону, обо всех случаях ТБ докладывается в местное отделение Контроля за заразными болезнями.
После уведомления автоматически отслеживаются все контакты больного. Значительному риску подвергаются члены семьи больного, хотя к врачу часто обращаются и его обеспокоенные знакомые. Лица, не находившиеся в постоянном и тесном контакте с пациентом, не относятся к группе риска, однако некоторые все же нуждаются в направлении на рентгенографию грудной клетки.
Множественная лекарственная устойчивость микобактерий, обнаруживающаяся в 2% бактериологически подтвержденных случаев ТБ в Великобритании, в последние годы стала, возможно, наиболее серьезной проблемой, когда речь идет о ТБ.
Чаще всего такая устойчивость наблюдается у больных с иммунодефицитом, но также встречается и у пациентов, подвергшихся ошибочному лечению одним или двумя препаратами или не следовавших схеме лечения.
Как правило, монорезистентность к изониазиду не представляет глобальной проблемы, но при этом в курс лечения необходимо включать дополнительный препарат, например этамбутол. Однако множественная резистентность, скажем, к изониазиду и рифампицину требует иных, более сложных схем лечения.
О множественной устойчивости штамма врач зачастую узнает через много недель после установления диагноза, так как микобактерии медленно растут в культуре и для выяснения их чувствительности требуется время. Такие пациенты должны находиться под пристальным наблюдением специалиста по ТБ, имеющего опыт борьбы с множественно устойчивыми штаммами.
Рекомендуемое чтение
1. Chemotherapy and managment of tuberculosis in the United Kingdom: recommendations of the Joint Tuberculosis Committee of the British Thoracic Society. Thorax 1990; 45:403–408.
2. Control and prevention of tuberculosis in the UK: code of practice 1994. Thorax 1994; 49:1193-1200.
3. Kumar D et al. Tuberculosis in England and Wales 1993: results of a national survey. Thorax 1997; 52:1060-1067.
4. The prevention and control of tuberculosis in the UK: guidance on tuberculosis control 1996. Department of Health and Welsh Office.
5. Davies PDO (Ed). Clinical Tuberculosis. Chapman & Hall, London 1994.
6. Moore-Gillon J. Tuberculosis. In: Horizons in Medicine, No 8. Ed Farthing MJG. Royal College Physicians, London 1997.
Убийца бедных, бездомных и страдающих иммунодефицитом
Даже в начале и середине нашего века заболевшие ТБ представители всех слоев общества, несмотря на длительное лечение в санатории, в большинстве своем все еще умирали. Торакальные хирурги производили разнообразные операции, но без особого
Однако в 70-х годах прошлого века, то есть задолго до появления противотуберкулезных препаратов, заболеваемость ТБ в Великобритании начала снижаться. Эта тенденция сохранялась в течение века.
Такое положение было частично обусловлено улучшением условий жизни, а также повышением качества питания. Со временем появилась прививка БЦЖ и эффективные лекарственные препараты, и заболеваемость начала снижаться еще более быстрыми темпами. В начале 80-х казалось, что туберкулез, подобно оспе, вскоре будет ликвидирован.
Однако стало ясно, что надеяться на это не приходится. С середины 80-х годов по середину 90-х число случаев ТБ в Великобритании возросло на 11% — и это вместо ожидаемого спада!
Наибольший прирост заболеваемости наблюдается в крупных городах, особенно среди нищих всех этнических групп. Пациенты с иммунодефицитом, включая обусловленный ВИЧ-инфекцией, также принадлежат к группе повышенного риска. Разразившаяся эпидемия СПИДа, несомненно, подогрела интерес к лечению ТБ, особенно случаев атипических микобактерий. Повышенный интерес представляет появление множественной лекарственной резистентности микобактерий, которая часто встречается в группе ВИЧ-инфицированных.
Процентное соотношение случаев ТБ, вызванных СПИДом, в Великобритании, по сравнению с другими странами мира, крайне невелико.
При ненарушенном иммунитете ведущими факторами, которыми обусловлена предрасположенность к ТБ, остаются перенаселенность и недостаточное питание.
Бездомные, особенно страдающие алкоголизмом и наркоманией, составляют группу повышенного риска. Реальную заболеваемость в этой группе оценить нелегко.
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению? Какова роль фторхинолонов в лечении туберкулеза легких?
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению?
Какова роль фторхинолонов в лечении туберкулеза легких?
Таблица. Стандартные концентрации ПТП, используемые для выявления лекарственной устойчивости МБТ
Первый этап характеризуется проведением интенсивной насыщенной химиотерапии четырьмя-пятью ПТП в течение 2-3 месяцев, что ведет к подавлению размножающейся микобактериальной популяции, уменьшению ее количества и предотвращению развития лекарственной резистентности. На первом этапе используется комбинация препаратов, состоящая из изониазида, рифампицина, пиразинамида, стрептомицина и/или этамбутола.
Второй этап — менее интенсивной химиотерапии — проводится, как правило, двумя-тремя ПТП. Цель второго этапа — воздействие на оставшуюся бактериальную популяцию, в большинстве своем находящуюся внутриклеточно в виде персистирующих форм микобактерий. Здесь главной задачей является предупреждение размножения оставшихся микобактерий, а также стимуляция репаративных процессов в легких с помощью различных патогенетических средств и методов лечения.
Такой методический подход к лечению ЛЧТЛ позволяет к концу первого этапа комбинированной химиотерапии под непосредственным медицинским наблюдением абациллировать 100%, а к завершению всего курса лечения — закрыть каверны в легких у более чем 80% больных с впервые выявленным и рецидивным туберкулезом легких [5].
Намного сложнее вопрос о проведении этиотропного лечения второго варианта, к которому мы относим ЛУТЛ, вызванный лекарственно резистентными (ЛР) МБТ к одному и более ПТП и/или их сочетанию. Особенно тяжело протекает ЛУТЛ у больных с множественной ЛР МБТ к изониазиду и рифампицину, то есть к основным и самым эффективным ПТП. Поэтому поиск новых концептуальных путей повышения эффективности лечения ЛУТЛ и разработка современной методологии специфического воздействия на ЛР МБТ является одним из важнейших и приоритетных направлений современной фтизиатрии.
Развитие ЛР у МБТ к ПТП — одна из главных причин недостаточно эффективной этиотропной химиотерапии. Больные туберкулезом, выделяющие ЛР-штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих ЛР-возбудителем. Чем больше число больных, выделяющих ЛР МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной резистентностью не только к основным, но и к резервным ПТП.
Феномен ЛР МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является ЛР. В активно размножающейся бактериальной популяции всегда имеется небольшое количество ЛР-мутантов, которые практического значения не имеют, но по мере уменьшения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством ЛР и устойчивых МБТ [5]. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. Следовательно, в клинической практике необходимо исследовать ЛР МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких [5].
По определению экспертов ВОЗ [3], ЛУТЛ — это случай туберкулеза легких с выделением МБТ, резистентных к одному и более ПТП. По данным Центрального НИИ туберкулеза РАМН, у каждого второго впервые выявленного и ранее не леченного противотуберкулезными препаратами больного в мокроте выявлялись ЛР к ПТП МБТ, при этом у 27,7% из них наблюдалась устойчивость к двум основным противотуберкулезным препаратам — изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота вторичной ЛР МБТ возрастает до 95,5%.
По нашему мнению, и это составляет основу нашей концепции, для повышения эффективности лечения туберкулеза, вызванного ЛР МБТ, необходимо в первую очередь использовать ускоренные методы выявления ЛР МБТ, что позволяет своевременно изменять режим химиотерапии.
Исследование лекарственной устойчивости МБТ в настоящее время возможно по прямому и непрямому методам.
Непрямой метод определения лекарственной чувствительности МБТ требует от 30 до 60, а иногда до 90 суток, ввиду того что вначале производится посев мокроты на твердые питательные среды и только после получения культуры МБТ производят ее пересев уже на среды с добавлением ПТП. При этом коррекция химиотерапии носит отсроченный характер, как правило, уже на конечном этапе интенсивной фазы химиотерапии.
В последнее время для ускоренного определения лекарственной устойчивости нами применялся радиометрический метод с использованием автоматической системы ВАСТЕС-460 ТВ (Becton Dickinson Diagnostic Systems, Sparks, MD), которая позволяет выявлять лекарственную резистентность МБТ на жидкой среде Middlebrook 7H10 через 6-8 дней.
Не менее важно правильное лечение впервые выявленных больных туберкулезом легких и применение современных режимов химиотерапии с использованием в начале лечения комбинации из четырех-пяти основных противотуберкулезных препаратов до получения результатов лекарственной устойчивости МБТ [2]. В этих случаях существенно повышается вероятность того, что даже при наличии первичной ЛР МБТ бактериостатическое действие окажут два или три химиопрепарата, к которым чувствительность сохранена. Именно несоблюдение фтизиатрами научно обоснованных комбинированных режимов химиотерапии при лечении впервые выявленных и рецидивных больных и назначение ими только трех ПТП является грубой врачебной ошибкой, что в конечном счете ведет к формированию наиболее трудно поддающейся лечению вторичной ЛР МБТ.
Наличие у больного туберкулезом легких ЛР МБТ существенно снижает эффективность лечения, приводит к появлению хронических и неизлечимых форм, а в ряде случаев и летальных исходов. Особенно тяжело протекают специфические поражения легких у больных с полирезистентными МБТ, которые обладают множественной ЛР, как минимум к изониазиду и рифампицину, т. е. к основным и самым активным противотуберкулезным препаратам. ЛР МБТ имеет не только чисто клиническое и эпидемиологическое, но и экономическое значение, так как лечение таких больных резервными ПТП обходится намного дороже, чем больных с чувствительными МБТ к основным химиопрепаратам.
В этих условиях расширение списка резервных ПТП, воздействующих на ЛР МБТ, является актуальным и крайне важным для повышения эффективности лечения больных с ЛУТЛ. Кроме того, присоединение к ЛУТЛ неспецифической бронхолегочной инфекции существенным образом утяжеляет течение специфического процесса в легких, требуя назначения дополнительных антибиотиков широкого спектра. В этом плане применение антибиотиков, воздействующих как на МБТ, так и на неспецифическую патогенную бронхолегочную микрофлору, является научнообоснованным и целесообразным.
В этом плане хорошо себя зарекомендовал в России такой препарат из группы фторхинолонов, как офлоксацин (таривид) [3]. Мы же свой выбор остановили на ломефлоксацине, как препарате, который еще не столь широко применяется при лечении туберкулеза и у которого, судя по имеющимся данным, практически не выявляются побочные эффекты и крайне редко формируется ЛР возбудителей инфекционных заболеваний [2].
Ломефлоксацин (максаквин) — антибактериальный препарат из группы фторхинолонов. Как и все представители производных оксихинолонкарбоновой кислоты, максаквин обладает высокой активностью против грамположительных (включая метициллин-устойчивые штаммы Staphylococcus aureus и Staphylococcus epidermidis) и грамотрицательных (включая Pseudomonas) микроорганизмов, в том числе по отношению к различным типам Micobacterium tuberculosis).
Механизм действия максаквина заключается в ингибировании хромосомной и плазмидной ДНК-гиразы, фермента, ответственного за стабильность пространственной структуры микробной ДНК. Вызывая деспирилизацию ДНК микробной клетки, максаквин ведет к гибели последней.
Максаквин обладает иным механизмом действия, нежели другие антибактериальные средства, поэтому к нему не существует перекрестной устойчивости с другими антибиотиками и химиотерапевтическими препаратами [2].
Основной целью настоящего исследования явилось изучение клинической и микробиологической эффективности максаквина при комплексном лечении больных деструктивным ЛУТЛ, выделяющих ЛР МБТ к изониазиду, рифампицину и другим ПТП, а также при сочетании туберкулеза с неспецифической бронхолегочной инфекцией.
Под наблюдением находилось 50 больных деструктивным ЛУТЛ, выделяющих с мокротой ЛР МБТ к изониазиду, рифампицину и ряду других ПТП. Эти люди в возрасте от 20 до 60 лет составили основную группу.
В контрольную группу вошли также 50 больных деструктивным ЛУТЛ легких в той же возрастной группе, выделяющие ЛР МБТ к изониазиду, рифампицину и другим ПТП. Эти пациенты лечились только протионамидом, амикацином, пиразинамидом и этамбутолом.
У 47 больных основной группы и 49 контрольной в мокроте микробиологическими методами были выявлены различные возбудители неспецифической бронхолегочной инфекции.
Среди больных основной группы диссеминированный туберкулез был установлен у 5 человек, инфильтративный — у 12, казеозная пневмония — у 7, кавернозный — у 7 и фиброзно-кавернозный туберкулез — у 17 человек. Большинство больных (45 пациентов) имели распространенный туберкулез легких с поражением более двух долей, у 34 больных был двусторонний процесс. У всех больных основной группы в мокроте были обнаружены МБТ, как методом микроскопии по Цилю — Нильсену, так и методом посева на питательные среды. При этом у них МБТ были устойчивы как минимум к изониазиду и рифампицину. Необходимо отметить, что все пациенты уже ранее неоднократно и неэффективно лечились основными ПТП, и специфический процесс у них приобрел рецидивирующий и хронический характер.
В клинической картине преобладали симптомы интоксикации с высокой температурой тела, потливостью, адинамией, изменениями в крови воспалительного характера, лимфопенией, увеличенной СОЭ до 40-50 мм в час. Следует отметить наличие грудных проявлений болезни — кашель с выделением мокроты, подчас значительного количества, слизисто-гнойной, а у половины больных — гнойной, с неприятным запахом. В легких выслушивались обильные катаральные явления по типу мелко-, средне-, а подчас и крупнопузырчатых влажных хрипов.
У большинства больных преобладали клинические проявления, которые скорее укладывались в картину неспецифического бронхолегочного поражения (бронхита, острой пневмонии, абсцедирования) с частыми и практически не стихающими обострениями.
Основным возбудителем неспецифической инфекции был Streptococcus hemoliticus — у 15,3% и Staphilococcus aureus — у 15% больных. Среди грамотрицательной микрофлоры преобладал Enterobacter cloacae в 7,6% случаев. Следует отметить высокую частоту ассоциации возбудителей неспецифической бронхолегочной инфекции.
МБТ были обнаружены у всех 50 больных. У 42 человек определялось обильное бактериовыделение. У всех пациентов выделенные штаммы МБТ были устойчивы к изониазиду и рифампицину. При этом у 31 больного лекарственная устойчивость МБТ к изониазиду и рифампицину сочеталась с другими ПТП.
Определение минимальной ингибирующей концентрации (МИК) максаквина проводили на лабораторных штаммах H37Rv и Academia, а также клинических штаммах (изолятах), выделенных от 30 больных, из которых 12 изолятов были чувствительны ко всем основным химиопрепаратам и 8 обладали резистентностью к изониазиду, рифампицину и стрептомицину. В опытах in vitro подавление роста лабораторных штаммов МБТ наблюдалось в зоне 57,6±0,04 до 61,8±0,02 мкн/мл, что почти в семь раз больше, чем показатели, характерные для остальных ПТП .
Таким образом, в ходе микробиологических исследований было установлено выраженное бактериологическое действие максаквина на МБТ, при этом более выраженный эффект наблюдался при его воздействии на лекарственно чувствительные штаммы и изоляты. Однако при повышенных концентрациях максаквина эффект также заметен при воздействии на полирезистентные МБТ, устойчивые к основным ППТ.
Лечение максаквином проводилось у всех 50 больных основной группы в разработанной нами комбинации с другими резервными препаратами: протионамидом, амикацином, пиразинамидом и этамбутолом.
Максаквин назначали в дозе 800 мг в сутки перорально однократно в утренние часы сразу вместе с другими противотуберкулезными препаратами для создания максимальной суммарной бактериостатической концентрации в крови и очагах поражения. Доза максаквина выбрана с учетом микробиологических исследований и соответствовала МИК, при которой отмечалось существенное подавление роста МБТ. Терапевтический эффект определяли через месяц — для оценки воздействия его на неспецифическую патогенную бронхолегочную микрофлору и через два месяца — для оценки воздействия на полирезистентные МБТ. Длительность курса лечения резервными химиопрепаратами в сочетании с максаквином составляла два месяца.
Через месяц комплексного лечения было отмечено значительное улучшение состояния больных основной группы, что проявлялось в уменьшении количества мокроты, кашля и катаральных явлений в легких, снижении температуры тела, при этом более чем у двух третей больных — до нормальных цифр.
У всех больных к этому сроку в мокроте перестал определяться рост вторичной патогенной бронхолегочной микрофлоры. К тому же у 34 больных значительно уменьшилась массивность выделения микобактерий туберкулеза. Практически у всех больных нормализовались анализы крови.
Следует отметить, что у 28 пациентов рентгенологически через месяц лечения максаквином в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом отмечалось частичное рассасывание специфических инфильтративных изменений в легких, а также существенное уменьшение перикавитарной воспалительной реакции. Это позволило применить на данном этапе искусственный пневмоторакс, который является обязательным методом в лечении ЛУТЛ и составляет вторую и не менее важную часть нашей концепции повышения эффективности лечения больных деструктивным туберкулезом легких, выделяющих полилекарственнорезистентные МБТ.
При анализе эффективности специфического действия комбинации резервных противотуберкулезных препаратов в сочетании с максаквином на полирезистентные МБТ при лечении 50 больных основной группы мы делали основной акцент на показатель прекращения бактериовыделения, как по микроскопии мокроты по Цилю — Нильсену, так и по посеву на питательные среды через два месяца после химиотерапии.
Анализ частоты прекращения бактериовыделения у больных основной и контрольной группы через два месяца лечения показал, что у пациентов, получавших максаквин в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом, прекращение бактериовыделения было достигнуто в 56% случаях. В контрольной группе больных, не получавших максаквина, — только в 30% случаев.
Следует отметить, что у остальных больных основной группы за этот период времени существенно уменьшилась массивность выделения МБТ.
Инволюция локальных изменений в легких у 50 больных контрольной группы также шла более замедленными темпами, и только у 25 больных к концу второго месяца удалось достичь частичного рассасывания перикавитарной инфильтрации и применить к ним искусственный пневмоторакс. К 39 из 50 пациентов основной группы был применен искусственный пневмоторакс в течение 1,5-2 месяцев, и 17 из них удалось достигнуть закрытия каверн в легких. 11 оставшихся больных, имеющих противопоказания к проведению искусственного пневмоторакса, в этот период были подготовлены к плановому оперативному вмешательству.
При определении лекарственной устойчивости МБТ к максаквину через два месяца лечения у больных основной группы только в 4% случаев была получена вторичная лекарственная устойчивость, сформировавшаяся в процессе двухмесячной химиотерапии, что в конечном итоге потребовало его отмены и замены на другой химиопрепарат, к которому МБТ сохранили свою чувствительность.
К концу второго месяца у 4% больных отмечались явления непереносимости максаквина — в виде диспепсических явлений и диареи, связанной с дисбактериозом, аллергических кожных проявлений и эозинофилии до 32%, что привело к полной отмене препарата. Во всех остальных случаях при двухмесячном ежедневном применении максаквина в суточной дозе 800 мг побочных явлений не отмечалось.
Проведенная после окончания курса лечения максаквином комбинированная химиотерапия резервными препаратами и динамическое наблюдение за этими же больными показали, что достигнутый ко второму месяцу положительный результат в абациллировании мокроты оказал положительное влияние и на конечный результат излечения больных с ЛУТЛ.
Таким образом, применение максаквина в дозе 800 мг в сутки в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом у больных деструктивным ЛУТЛ с сопутствующей неспецифической бронхолегочной инфекцией показало его достаточную эффективность как антибиотика широкого спектра, воздействующего на грамотрицательную и грамположительную микрофлору, и препарата, действующего на туберкулезное воспаление.
Максаквин с полной уверенностью может быть отнесен к группе резервных ПТП. Он эффективно действует не только на МБТ, чувствительные ко всем ПТП, но и на ЛУ МБТ к изониазиду и рифампицину, что и обусловливает целесообразность его назначения таким больным. Тем не менее максаквин не следует рассматривать как основной препарат в схемах лечения больных с впервые выявленным туберкулезом легких, он должен оставаться в резерве и применяться только при ЛУТЛ и сопутствующей неспецифической бронхолегочной инфекции.
Для изониазида это составляет 1 мкг/мл, для рифампицина — 40 мкг/мл, стрептомицина — 10 мкг/мл, этамбутола — 2 мкг/мл, канамицина — 30 мкг/мл, амикацина — 8 мкг/мл, протионамида (этионамида) — 30 мкг/мл, офлоксацина (таривида) — 5 мкг/мл, циклосерина — 30 мкг/мл и для пиразинамида — 100 мкг/мл.
Литература
1. Лечение туберкулеза. Рекомендации для национальных программ. ВОЗ. 1998. 77 с.
2. Мишин. В. Ю., Степанян И. Э. Фторхинолоны в лечении туберкулеза органов дыхания // Русский медицинский журнал. 1999. № 5. С. 234-236.
3. Рекомендации по лечению резистентных форм туберкулеза. ВОЗ. 1998. 47 с.
4. Хоменко А. Г., Мишин В. Ю., Чуканов В. И. и др. Эффективность применения офлоксацина в комплексном лечении больных туберкулезом легких, осложненным неспецифической бронхолегочной инфекцией // Новые лекарственные препараты. 1995. Вып. 11. С. 13-20.
5. Хоменко А. Г. Современная химиотерапия туберкулеза // Клиническая фармакология и терапия. 1998. № 4. С. 16-20.
В чем преимущество многокомпонентных противотуберкулезных препаратов? Каковы показания к применению четырехкомпонентных противотуберкулезных препаратов? Какова эффективность использования многокомпонентных препаратов? Комбинированные противотуберкулезны
В чем преимущество многокомпонентных противотуберкулезных препаратов? Каковы показания к применению четырехкомпонентных противотуберкулезных препаратов? Какова эффективность использования многокомпонентных препаратов?
Комбинированные противотуберкулезные препараты с фиксированными дозами применяются в отечественной фтизиатрии с 60-х годов (пасомицин — комплекс ПАСК + дигидрострептомицин и стрептосалюзид — комплекс стрептомицин + салюзид).
Всемирный союз по борьбе с туберкулезом и заболеваниями органов дыхания в своих рекомендациях по химиотерапии считает целесообразным использование комбинаций препаратов в фиксированных дозах, поскольку такой подход исключает монотерапию и неточность дозирования. Комбинированные препараты удобны для больных, а также медицинского персонала и являются надежным способом проведения контролируемой комбинированной химиотерапии туберкулеза. Лечение больных туберкулезом многокомпонентными лекарственными формами позволяет значительно снизить количество таблеток, прописываемых на курс лечения, что способствует улучшению переносимости лекарств.
Один из четырехкомпонентных препаратов — майрин-п — подробно изучен в клинике НИИ фтизиопульмонологии ММА им. И. М. Сеченова.
Показания к применению майрина-п в терапии туберкулеза:
- впервые выявленные больные с ограниченными формами туберкулеза легких (с наличием или отсутствием бактериовыделения);
- впервые выявленные больные с распространенными формами туберкулеза (с наличием или отсутствием бактериовыделения).
- лицам с гиперчувствительностью к изониазиду, рифампицину, пиразинамиду, этамбутолу;
- беременным и кормящим женщинам;
- лицам с заболеваниями печени и желудочно-кишечного тракта в острой фазе;
- лицам с заболеваниями центральной нервной системы (эпилепсия и другие заболевания со склонностью к судорожным припадкам), органов зрения.
Майрин-п представляет собой комбинированный противотуберкулезный препарат, в состав которого входят четыре компонента: этамбутол HCl USP — 225 мг; рифампицин USP — 120 мг; изониазид USP — 60 мг; пиразинамид USP — 300 мг.
Майрин-п — таблетки, покрытые оболочкой (10 таблеток в блистере, в одной упаковке — 100 таблеток).
Продолжительность лечения препаратом майрин-п — 4-6 месяцев. Он дозируется по рифампицину из расчета 10 мг/кг массы тела, но не более 6 таблеток. Препарат принимают один раз в сутки натощак. Одновременно с майрином-п при распространенных формах туберкулеза назначается на 2-3 месяца стрептомицин. Больным с быстрым типом ацетилирования изониазида назначается дополнительно 5 мг/кг этого препарата, общая суточная доза изониазида составляет 10 мг/кг. При умеренно выраженной лекарственной резистентности микобактерий туберкулеза (МБТ) одновременно с майрин-п применяют протионамид — (12,5 мг/кг на три приема) и канамицин (16 мг/кг один раз в сутки). На весь курс лечения майрином-п назначают витамин В6 по 30 мг на два приема. При заболевании желчевыводящих путей в анамнезе применяют желчегонные средства.
Клинические исследования эффективности майрина-п проведены у 277 больных с впервые выявленным туберкулезом легких (основная группа). Возраст пациентов колебался от 18 до 50 лет.
У большинства получавших майрин-п [226 (81,6%)] диагностировался распространенный туберкулез: у 34 (12,3%) человек — двусторонний процесс, у 41 (14,8%) — поражение всего легкого, у 151 (54,5%) — поражение доли легкого. У 167 (60,3%) человек в легких были обнаружены полости распада. Все больные с распространенным туберкулезом выделяли МБТ; у 19 (6,9%) из них обнаружены лекарственно-устойчивые штаммы (у 16 — к 5-10 мкг/мл стрептомицина, у 13 — к 25-50 мкг/мл рифампицина и у 14 — к 5-25 мкг/мл изониазида). Множественная лекарственная устойчивость наблюдалась в 11(57,9%) случаях. Ограниченный процесс с поражением до двух сегментов выявился у 51(18,4%) больного. Двадцать из них выделяли лекарственно-чувствительные МБТ, у 11(3,9%) обнаружены мелкие единичные полости распада.
В группе сравнения было 197 пациентов, получавших лечение противотуберкулезными препаратами, входящими в майрин-п и выпускающимися в свободных лекарственных формах. Из них 110 (55,8%) больных выделяли МБТ, чувствительные к противотуберкулезным препаратам первой линии. У 92 (46,7%) человек выявили распространенный туберкулез, у 18 (9,1%) — ограниченный (с поражением до двух сегментов), у 59 (29,9%) пациентов в легких обнаружены полости распада. У 87 (44,1%) больных с распространенным туберкулезом легких в мокроте были обнаружены лекарственно-резистентные штаммы МБТ. У 43 (21,8%) из них наблюдалось поражение доли легкого, у 24 (12,1%) — поражение всего легкого, у 20 (10,2%) — двух легких. Наиболее часто выявлялась устойчивость к стрептомицину (48,6%), изониазиду (37,4%), рифампицину (27,6%); к канамицину и этамбутолу устойчивость МБТ встречалась значительно реже (8,9% и 5% соответственно). Устойчивость МБТ к изониазиду и рифампицину отмечена в 22% случаев, лекарственная полирезистентность к трем и четырем препаратам — в 27,2%.
Майрин-п и аналогичные препараты в свободных лекарственных формах назначали в терапевтических режимах, представленных в табл. 1 и 2.
Результаты лечения больных туберкулезом легких с использованием комбинированного препарата майрин-п
Туберкулезная интоксикация (повышение температуры тела, изменения гемограммы, дефицит веса) среди больных с лекарственно-чувствительным туберкулезом легких наблюдалась у 207 (84%) из 245 человек основной группы и у 93 (84,5%) из 110 человек из группы сравнения. Динамика исчезновения симптомов интоксикации среди больных этих групп дана в табл. 3.
Как видно из табл. 3, применение майрина-п у больных с распространенным лекарственно-чувствительным туберкулезом позволяет за 2 месяца ликвидировать симптомы интоксикации в 72,5% случаев. У больных с ограниченным туберкулезом легких из основной группы уже к третьему месяцу лечения интоксикация исчезла в 100% случаев. В группе сравнения полное исчезновение симптомов интоксикации было достигнуто к четвертому месяцу.
Среди больных с распространенным лекарственно-резистентным туберкулезом клинические признаки туберкулезной интоксикации наблюдались у 17 (90,8%) человек из опытной группы и у 80 (91,6%) из группы сравнения. Динамика исчезновения симптомов интоксикации у больных этих групп приведена в табл. 4.
В табл. 5 представлены частота и сроки прекращения бактериовыделения у больных с лекарственно-чувствительным туберкулезом легких.
Частота и сроки прекращения бактериовыделения у больных лекарственно-резистентным туберкулезом представлены в табл. 6.
Как видно из табл. 6, при лекарственно-резистентном туберкулезе негативация мокроты за 4 месяца наблюдалась у 79,3% больных основной группы и у 65,5% пациентов из группы сравнения. Достаточно высокий процент прекращения бактериовыделения при резистентных формах туберкулеза обусловлен полученными в ходе эксперимента данными о выраженном синергизме изониазида, рифампицина, пиразинамида и протионамида.
Закрытие каверн за 4 месяца лечения у больных с распространенным лекарственно-чувствительным туберкулезом при использовании майрина-п наблюдалось в 44,5% случаев. Этот результат можно считать достаточно эффективным, если учесть большую протяженность процесса. У больных с ограниченным процессом без бактериовыделения за 4 месяца лечения деструктивные изменения в легких перестали определяться во всех случаях. В группах сравнения закрытие полостей распада при ограниченных формах туберкулеза легких наблюдалось в 89% случаев, при распространенном туберкулезе — в 38% за те же сроки лечения.
Значительно меньшей (21,1%) была частота закрытия полостей распада у больных основной группы с лекарственно-резистентным туберкулезом. Но и этот показатель оказался выше, чем в группе сравнения (16,2%), где применялись противотуберкулезные препараты в свободных лекарственных формах. Терапия майрином-п в комбинации с протионамидом и канамицином позволила за 4 месяца подготовить большинство больных с сохранившимися полостями распада к хирургическому лечению и успешно прооперировать их.
Нежелательные явления в процессе лечения майрином-п возникли у 28 (10,1%) больных, причем чаще всего встречались медикаментозный гепатит и обострение хронического гастрита. В 53,6% случаев нарушения носили устранимый характер и исчезали без отмены майрина-п. Для 13 из 17 больных с нежелательными явлениями со стороны ЖКТ и печени препарат был отменен.
При стандартной химиотерапии нежелательные явления наблюдались значительно чаще (40,2%); более чем в половине случаев (23,5%) они были неустранимы и требовали изменения режима терапии.
Читайте также:

