В россии синтезировали вещество убивающее вич
Обновлено: 24.04.2024
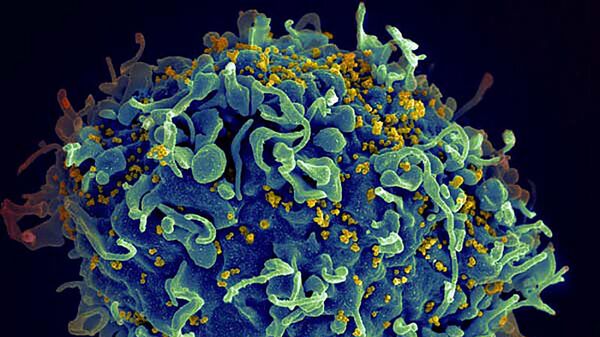
Заражение ВИЧ и многими другими опасными вирусами обычно протекает в два этапа. Сначала вирус активно размножается в организме новой жертвы, что приводит к активации иммунитета и появлению недомогания, похожего по симптомам на грипп. Когда организм начинает бороться с вирусом, инфекция переходит в хроническую стадию, постепенно истощая иммунитет.
Сегодня больные ВИЧ могут прожить десятки лет благодаря приему антиретровирусных препаратов – веществ, подавляющих различные этапы репликации вируса в клетках тела. Так как они часто обладают сильными побочными эффектами, медики часто вынуждены прекращать их прием на несколько недель.

При прекращении их приема ВИЧ "вылезает из окопов" и начинает интенсивно копировать себя, зачастую возвращаясь к начальным масштабам инфекции за три или две недели. В последние годы ученые активно пытаются найти лекарства или антитела, которые помогали бы избежать подобной "контратаки" вируса, или позволяли бы "выгнать" вирус из клеток.
Крайне малое число носителей ВИЧ, примерно 0,3% больных, не нуждается в подобной терапии - их иммунитет по пока неизвестным причинам более эффективно борется с инфекцией и сдерживает ее распространение без помощи лекарств. Многие подобные люди, так называемые "нонпрогрессоры", живут с инфекцией уже более трех десятков лет, не страдая от резкого снижения в уровне CD4-клеток.
Генетики, вирусологи и молекулярные биологи уже много лет изучают их лимфоциты и ДНК в надежде понять, что защищает их иммунитет от истощения, и трансплантировать эти уникальные особенности в организм других больных, которым повезло меньше.
Кауфманн и его коллеги провели одно из самых масштабных исследований такого рода, организовав своеобразную "перепись" среди Т-клеток и прочих иммунных телец, присутствующих в образцах крови у обычных носителей ВИЧ и людей, на которых вирус почти не действует.
Ученых интересовало то, работа каких генов в этих клетках у них отличалась и как эти отличия могли влиять на взаимодействия между вирусом и организмом человека. Дополнительно биологи проанализировали то, как изменилась работа тех же самых генов у больных, проходивших антиретровирусную терапию.
Это позволило им проследить за тем, как лекарства влияли на иммунные клетки, а также тем, было ли их действие похоже на то, что происходит в организме "нонпрогрессоров". Этот анализ раскрыл несколько важных сходств и различий в работе лимфоцитов у всех трех категорий больных.
К примеру, в иммунных тельцах людей, необычно хорошо сопротивлявшихся ВИЧ, а также в немногочисленных выживших лимфоцитах "обычных" больных были активны гены, связанные с работой и ростом трех подтипов Т-клеток –TH-1, TH-17 и TH-22. Они, как отмечают ученые, особенно активно распознавали вирусные частицы и уничтожали их, что, вероятно, помогает "нонпрогрессорам" сдерживать инфекцию.
Что интересно, подобные клетки чаще встречаются не в крови, а в кишечнике человека, где, как сегодня считают исследователи, протекает острая фаза заражения ВИЧ и его фактическое проникновение в организм. Скорее всего, они играют ведущую роль в сдерживании инфекции, так как снижение активности связанных с ними генов или пониженное число этих телец ведет к ускоренному развитию инфекции.
Антиретровирусная терапия, как обнаружили Кауфманн и его коллеги, тоже воздействует на эти участки ДНК, но не так, как это происходит в организме "нонпрогрессоров". Активность части генов вырастает, тогда как другие оказались подавлены, что заметно ослабило способность иммунитета сопротивляться инфекции.
Соответственно, если понять, как "переключить" гены в нужное положение, то можно создать средство, которое не излечит человека от ВИЧ, но переведет инфекцию в такое состояние, что она перестанет прогрессировать. Что для этого надо сделать, ученые планируют выяснить в ближайшее время.
Более 20 лет наука пытается победить ВИЧ. Борьбу ведут самые авторитетные лаборатории мира, вкладываются многие миллионы долларов, но безуспешно. И вот только что ученые России и США объявили о прорыве. О сути исследования корреспонденту "РГ" рассказал доктор фармацевтических наук, заведующий лабораторией ФИЦ Биотехнологии РАН Вадим Макаров.

Главное - уничтожить вирус ВИЧ во всем организме, в том числе в нейронах мозга. Очистка - полная. Фото: Reuters
Если еще недавно страшный диагноз был приговором, то в последние годы созданы препараты, которые позволяют инфицированным жить достаточно долго. Хотя вирус в организме и остается. Почему эти лекарства не могут выбить его окончательно?
Вадим Макаров: В этом специфика вируса. Кстати, аналогичная картина с герпесом. Ведь он живет в организме каждого, кто им хотя бы раз переболел. Герпес не излечивается, а переходит в спящую форму, затаившись в нейронах мозга. Может там отсиживаться десятки лет, а потом вдруг неожиданно выскочить на губах.
Так же и вирус ВИЧ. Он тоже прячется в нейронах. Самые лучшие препараты не могут до него добраться, они всего лишь переводят острую фазу болезни в хроническую, но до самого вируса не добираются.

Но как этот вирус сумел создать столь изощренную систему защиты? Что за такой эффективный щит?
Вадим Макаров: Это произошло в процессе естественного отбора. Все живые существа ищут способ выжить, ищут наиболее безопасное место. И вирус ВИЧ нашел очень удачное - нейроны мозга. Почему оно безопасное? Дело в том, что в нейроны крайне сложно проникнуть извне, так как надежно защищены от всех внешних воздействий специальным барьером. Он называется гематоэнцефалический барьер.
И вы сумели пробить эту стену. Создали новые лекарства, которые работают принципиально иначе, чем все существующие?
Вадим Макаров: Нет, нового киллера мы не придумывали, а применили уже хорошо известный метод убийства вируса. Задача была в другом - протащить эту киллер-молекулу через защитный барьер в нейроны. В чем здесь главная сложность? Требовалось придать молекуле новые функции, оставив старые. Так ее модернизировать, чтобы она и киллером осталась, и могла разрушить щит. Эту задачу и решала наша объединенная команда российских и американских ученых.
И как удалось?
Вадим Макаров: Если совсем просто, то мы меняли одни части молекулы на другие и проверяли эффект. На самом деле исследование сложнейшее. Каждый вариант моделировался на компьютере, отбирались лучшие, на их основе синтезировались варианты препарата, которые проверялись на мышах. Такой поиск продолжался четыре года. За это время на компьютере перебрали десятки тысяч разных вариантов модернизированной молекулы, а реально синтезировали и проверили на мышах несколько сотен.
В итоге наша команда создала вещество, которое будет уничтожать вирус ВИЧ во всем организме, в том числе и в нейронах. Очистка будет полной. Не останется никакой "хроники". Что и показано в экспериментах на мышах.

Но мышь не человек. У нас препарат, вполне вероятно, будет работать иначе, может и не пробиться в нейроны?
Вадим Макаров: В том-то и дело, что опыты проводились на так называемых гуманизированных мышах. Кстати, очень дорогих, они есть только в США. У них с помощью генных технологий создана иммунная система, полностью идентичная человеческой. Поэтому на них можно понять, как препарат будет работать в организме человека.
Понятно, мыши были американские. А как вообще в этой научной команде поделили сферы исследований?
Вадим Макаров: Кроме мышей американцы занимались компьютерным моделированием и биологической частью. Наша сфера - химия, синтез препарата и его дизайн.
Жизнь научила медицину быть консервативной: много раз проверить, прежде чем выпустить новое лекарство в жизнь
Американцы пытаются все делать сами, особенно стремятся не делить ни с кем прорывные исследования. Почему, на ваш взгляд, пошли на контакт с российской наукой?

Вадим Макаров: Во-первых, это очень дорогое исследование, его не потянет ни одна частная фирма. У нас работы финансировал РФФИ, в США - Национальный институт здоровья. Во-вторых, наша наука в области тонкого химического синтеза признана во всем мире. Более того, считается ведущей. Так что у нас сложился взаимовыгодный тандем.
Понятно, что от экспериментов на мышах до внедрения препарата в медицинскую практику путь не близкий. Когда можно ожидать его появление аптеках?
Вадим Макаров: Здесь ситуация стандартная. Жизнь научила медицину быть консервативной, много раз проверить, прежде чем выпустить новое лекарство в жизнь. Обычно на это уходит минимум 10 лет. Такова практика практически во всех странах мира.
— Какие на данный момент существуют разработки препаратов против ВИЧ? Насколько в этом направлении продвинулись зарубежные коллеги?
Есть еще обширный пласт просто химиопрепаратов, которые разрабатываются для ВИЧ-пациентов. Этими препаратами кормят пациентов на протяжении всей жизни со всеми вытекающими последствиями.
— Самые перспективные исследования сейчас с чем связаны?
— Связаны с генной терапией, в первую очередь, когда вводятся гены, которые разным способом действуют на инфекцию. В нашем случае мы говорим о так называемой внутриклеточной иммунизации, когда гены вводят в клетку и эта клетка становится устойчивой к вирусу: он не может в нее зайти или не может в клетке размножаться. Варианты зависят от гена. Делаем такую вот иммунизированную клетку, которая для вируса недоступна.
— Можете немного подробнее рассказать, как это работает?
— Есть доказательства, что этот механизм эффективен?

— Как можно повторить такой случай излечения?
— В чем принципиальная разница между нашей разработкой и американской?
— Комплексным подходом?
— Совершенно верно. Аналогичный подход используется сейчас при терапии ВИЧ — антиретровирусная терапия комбинированная, и она помогает. В генной терапии такой же подход — недостаточно перекрыть один какой-то путь вирусу. Мы сейчас задумываемся о том, что мы к этому препарату будем добавлять еще один ген, который еще дополнительно подстрахует. Мы считаем, что в генной терапии тоже три гена будут успешны.
— По доклиническим испытаниям есть два основных направления: мы должны показать эффективность и безопасность этого лекарственного препарата. С безопасностью тут все понятно: есть серия тестов, они одинаковые для химических препаратов и для биологических, таких как наш, мы их все успешно прошли, доказали, что препарат безопасен и в больших дозах не вызывает никаких побочных эффектов. В том, что касается эффективности, сложнее, потому что для каждого препарата нужна своя модель. Например, животные, которые болеют этой болезнью, чтобы мы их вылечили и показали, что препарат работает. С ВИЧ сложно, поскольку моделей готовых нет, а на человеке не можем проводить.
— Но на клетках уже есть результаты?
— На данный момент мы показали эффективность препарата на клетках. Есть клетки, их можно заразить.
Можно у человека взять его лимфоциты, посадить в пробирку. Если к ним добавить вирус, вирус начинает размножаться — клетки дохнут. На такой системе in vitro мы показали, что когда мы обрабатываем препаратом клетки, то потом на них вирус практически не растет.
— Может быть, не 100% сейчас, но очень сильное снижение вируса, практически до нуля. При этом есть еще некоторые моменты, которые мы могли бы улучшить, а именно — доставку препарата. Поскольку когда мы обрабатываем препаратом клетки, то он попадает не во все клетки. Поэтому мы сейчас работаем над улучшением доставки, поскольку от этого улучшится и эффективность препарата.
— На какой стадии сейчас исследования на животных?
— Второй вопрос в том, что нужно все-таки провести исследования in vivo, то есть на каких-нибудь животных. Тут проблема такая, что в принципе есть модель мышей, специально разработанная, так называемые гуманизированные мыши. Их можно заразить вирусом, и он будет себя вести в них, как в теле человека, потому что у этих мышей — человеческие клетки крови, лимфоциты и так далее. Но в нашей стране их, к сожалению, нет. Их можно привезти, но их транспортировка требует особых условий, потому что они изначально не имеют иммунной системы. Если все это сложить, то получается, что мыши стоят очень и очень дорого.
— А сколько таких мышей надо?
— Необходимо не менее 50 животных и отлаженная методика гуманизации. Каждая мышь стоит 300—500 евро, но еще больше стоит работа по гуманизации, содержанию мышей, заражению их вирусом.
— То есть сейчас все уперлось в отсутствие возможности провести доклинические исследования на животных моделях?
— Конечно, прежде чем выйти на клинические испытания, хотелось бы больше быть уверенными, что он у нас in vivo работает. На тех тестах, которые мы уже провели, видно, что он хорошо себя ведет, хотелось бы еще убедиться в этом на животных моделях. Кроме того, мы сейчас подали проект на совместное финансирование с немецкими коллегами, которые работают с такими мышами. Ждем сейчас, будет им это интересно или нет. Если будет интересно, то со следующего года мы начнем проверять уже на этих мышах. С другой стороны, идет строительство собственного вивария в ЦНИИ эпидемиологии, где будут созданы все условия для содержания таких мышей, для их гуманизации, чтобы мы могли сами уже это делать, не зависеть ни от кого, потому что на самом деле заказ таких исследований за рубежом — это очень дорого.
— На какой стадии сейчас исследования по редактированию генома?
— Это более безопасное, хотя и пока менее эффективное воздействие. Тем не менее у нас сейчас более или менее хорошо работает система изменения генома CRISPR-Cas. Есть еще вторая система, которая может что-то прицельно в геноме вырезать, что-то прицельно вставлять и делать уже направленные изменения. Тут более или менее все ясно, потому что изменять надо ген CCR5, и это мы уже делаем. Но поскольку препарат нам нужен комплексный, мы ищем способы, как бы нам вместо этого CCR5 встроить гены, которых нам не хватает для того, чтобы клетка была полностью защищена. Уже работы идут, но есть нюансы. Я думаю, что к тому моменту, когда у нас появятся собственные мыши в виварии, мы уже будем готовы испытывать, и сразу выберем лучшее, и с ним уже будем готовиться к клиническим испытаниям.
— Когда нам ожидать регистрации препарата?
— То есть это через несколько лет?
— Это не следующий год, это лет через пять, по оптимистичным прогнозам. В среднем до 10 лет проходит. Опять-таки клинические испытания — это деньги, производство препарата — это тоже деньги. С другой стороны, мы рассчитываем, что это будет революция, потому что с химиопрепаратами для антиретровирусной терапии уже более или менее все понятно — они работают, но это пожизненно, дорого и токсично для организма.
Обнаружение белка CARD8 открыло возможность использования его для уничтожения всех "спящих" копий ВИЧ в организме пациента вне зависимости от того, насколько сильно мутировал вирус, атакуя ту его часть, которая является одинаковой для всех его версий

ТАСС, 4 февраля. Биологи из США выяснили, что один из белков врожденной иммунной системы CARD8 способен распознавать следы присутствия одного из ключевых белков ВИЧ внутри клеток и оповещать об этом остальной организм. Это позволяет использовать его для очистки тела от "спящего" ВИЧ, сообщила в четверг пресс-служба Университета Вашингтона в Сент-Луисе (WUSTL) со ссылкой на статью в журнале Science.

"Обнаружение белка CARD8 открыло возможность использования его для уничтожения всех "спящих" копий ВИЧ в организме пациента вне зависимости от того, насколько сильно мутировал вирус, атакуя ту его часть, которая является одинаковой для всех его версий. Подобная терапия радикально улучшит жизнь даже тех пациентов, в чьем организме ВИЧ остается подавленным благодаря антиретровирусной терапии", - заявил Шань Лян, доцент WUSTL, чьи слова приводит пресс-служба вуза.
ВИЧ проникает в иммунные клетки человека, используя белки, которыми покрыта его оболочка. Структура этих молекул, а также связанных с ними нитей сахаров быстро меняется по мере размножения вируса, что вынуждает иммунитет постоянно вырабатывать новые наборы антител. В конечном итоге в этой гонке почти всегда побеждает вирус, если пациент не принимает антиретровирусных лекарств.
В свою очередь их прием ведет к тому, что вирус переходит в своеобразную спячку, не формирует новых вирусных частиц и не проявляет себя в жизни клетки. Это позволяет ему избегать внимания иммунитета и быстро восстанавливать прежние масштабы инфекции после того, как прием лекарств прекращается. Ученые уже два десятилетия пытаются создать способы уничтожения всех следов "спящего" вируса или зараженных им клеток, но пока существенных успехов достичь не удалось.
Шань Лян и его коллеги сделали большой шаг к решению этой задачи, изучая реакцию врожденной иммунной системы клеток на проникновение и размножение частиц ВИЧ внутри них.
Помощь врожденного иммунитета
В частности, их интересовало то, взаимодействуют ли какие-то белки или молекулы РНК, производимые клеткой, с различными компонентами вирусных частиц, из которых собираются новые копии ВИЧ во время активной фазы инфекции. Подобным образом клетки защищают организм от дальнейшего распространения бактериальных инфекций, начиная вырабатывать сигналы опасности при появлении токсинов микробов внутри них, что привлекает внимание иммунитета.
Оказалось, что подобную роль в случае с вирусом иммунодефицита может исполнять белок CARD8, распознающий молекулы ВИЧ-протеазы - белка, играющего ключевую роль в сборке новых вирусных частиц. Этот фермент разрезает на части заготовки белков вируса, из которых формируются его оболочка, и его вывод из строя лишает ВИЧ способности заражать другие клетки.
Как обнаружили Шань Лян и его коллеги, CARD8 похож по устройству на некоторые компоненты вируса, что заставляет ВИЧ-протеазу захватывать и разрезать его. Это запускает цепочку реакций, которая одновременно заставляет клетку самоуничтожиться и выработать большое количество сигнальных молекул, привлекающих внимание иммунных телец, специализирующихся на уничтожении зараженных клеток.
Проблема заключается в том, что для этого необходимо вывести вирус из "спящего режима", так как в противном случае ВИЧ-протеаза находится в неактивной форме и не взаимодействует с CARD8. Этого, как выяснили ученые, можно добиться, если обработать зараженные клетки большими дозами эфавиренца, одного из первых лекарств от ВИЧ, которое сейчас почти не применяется в клинической практике.
"Мы намерены найти или создать вещества, которые бы еще лучше справлялись с этой задачей, чем эфавиренц или другие препараты, блокирующие работу обратной транскриптазы ВИЧ. Данные, которые мы собрали в рамках этого исследования, помогут нам создать препараты, способные полностью очистить организм больных от вируса", - подытожил Шань Лян.
Читайте также:

