Вич 1 типа ненуклеозидного происхождения
Обновлено: 05.05.2024
Морфология вируса иммунодефицита человека. Антигены вируса иммунодефицита человека.
Зрелые вирионы вируса иммунодефицита человека имеют сферическую форму, их размеры не превышают 100-120 им в диаметре. Геном вируса иммунодефицита человека образуют две нити +РНК; их связывают белки рб и р7 (цифра соответствует молекулярному весу в кД).
Капсид вируса иммунодефицита человека образует белок р24. Сердцевина вириона вируса иммунодефицита человека имеет цилиндрическую или конусовидную формы; её формируют белки р18 и р24.
В сердцевине вируса иммунодефицита человека располагаются РНК, внутренние белки (р7 и р9), обратная транскриптаза (димер из белков р66 и p51) и эндонуклсаза (р31). Матричный белок р17 формирует прослойку между сердцевиной вириона и внешней оболочкой.
Суперкапсид вируса иммунодефицита человека образован двойным липидным слоем, который пронизывают гликопротсиновыс шипы. Каждый шип состоит из белков gp41 и gp 120. Гликопротеины gpl20 локализованы в выступающей части шипа и взаимодействуют с молекулами CD4 на мембранах клеток.
Гликопротеины gp41 (белки слияния) вируса иммунодефицита человека располагаются внутри оболочки и обеспечивают её слияние с клеточной мембраной.
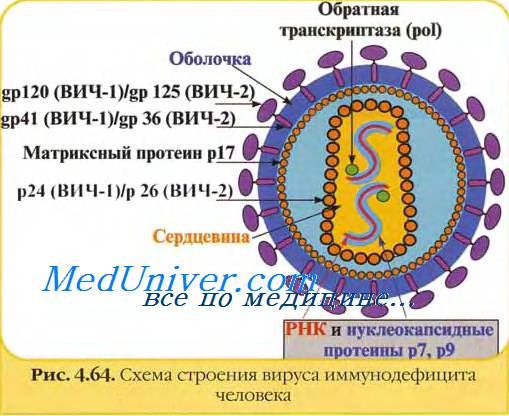
Антигенная структура вируса иммунодефицита человека
У вируса иммунодефицита человека главными антигенами выступают группо- и видоспецифичные антигены [сердцевинные (gag-) белки p24; типоспецифичные антигены [оболочечные (env-) белки gp41 и gp120].
В соответствии с их структурой выделяют два типа и более 10 сероваров вируса иммунодефицита человека. Вирус иммунодефицита человека отличается высокой антигенной изменчивостью, и в результате сбоев обратной транскриптазы из организма больного можно выделить серологически различные вирусы.
Главные антигены вируса иммунодефицита человека — поверхностные gp41 и gpl20, a также сердцевинный (ядерный) gp24.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Категории МКБ: Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде других состояний (B23), Болезнь, вызванная вирусом иммунодефицита человека [вич], неуточненная (B24), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде других уточненных болезней (B22), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде злокачественных новообразований (B21), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде инфекционных и паразитарных болезней (B20), Острый ВИЧ-инфекционный синдром (B23.0)
Общая информация
Краткое описание
ВИЧ-инфекция - инфекционная болезнь, развивающаяся в результате многолетнего персистирования в лимфоцитах, макрофагах и клетках нервной ткани вируса иммунодефицита человека (далее - ВИЧ), характеризующаяся медленно прогрессирующим дефектом иммунной системы, который приводит к гибели больного от вторичных поражений, описанных как синдром приобретенного иммунодефицита (далее - СПИД) [1].
B20 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде инфекционных и паразитарных болезней;
B21 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде злокачественных новообразований;
B22 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде других уточненных болезней;
Пользователи протокола: инфекционисты, терапевты, врачи общей практики, клинической лабораторной диагностики, фтизиатры.
Класс I - польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс III - имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.
Классификация
• нейтропения (
• хронический герпес (оролабиальный, генитальный или аноректальный длительностью более месяца или висцеральный любой локализации);
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
• число лимфоцитов CD4 (абсолютное и процентное содержание) - двукратное измерение с интервалом не менее 7 дней;
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: не проводится.
Заболевание начинается постепенно.
• половые контакты (гетеро- или гомосексуальные; тип контактов: оральный, вагинальный, анальный) с ВИЧ-статус партнерами (если известно);
• патологическое увеличение лимфатических узлов, персистирующая генерализованная лимфоаденопатия.
Ротоглотка: стоматит, язвенно-некротические поражения, разрастание слизистой полости рта, преимущественно боковой поверхности языка.
Мочеполовая система и перианальная область: признаки следующих заболеваний: нефропатия, инфекция, вызванная вирусом папилломы человека (остроконечные кондиломы половых органов и заднего прохода, рак шейки матки).
Неврологический и психический статус: нарушение когнитивных функций (Приложение 1), парезы, симптомы нейропатии, нарушение сознания, менингеальные синдром.
Биохимический анализ крови: повышение уровня креатинина и мочевины в крови, гипонатриемия, гипокалиемия (при развитии ОПП).
• полимеразная цепная реакция РНК ВИЧ: определяемая вирусная нагрузка.
МРТ/КТ головного мозга: отек головного мозга, признаки менингоэнцефалита, дисциркуляторная энцефалопатия, объемные процессы;
• консультация невропатолога: при признаках/подозрении на криптококковый менингит, ВИЧ-энфефалопатию, токсоплазмоз ЦНС, ПМЛ, лимфомы головного мозга, периферической полинейропатии;
• консультация психиатра: при признаках/подозрении психического расстройства. ВИЧ-энцефалопатии/деменции;
Дифференциальный диагноз
Дифференциальный диагноз: проводится с оппортунистическими инфекциями и другими вторичными заболеваниями по результатам консультаций специалистов.
Лечение
Курс лечения АРТ – пожизненный, применяется тройная схема, кратность приема АРВ препаратов зависит от формы выпуска.
• эмтрицитабин (FTC) 200 мг, капсула; 200 мг 1 раз в сутки.
• рилпивирин* (RPV) 25 мг таблетка; 25 мг 1 раз в сутки.
• дарунавир (DRV) 400 мг, 600 мг, 800 мг таблетка; 600 мг 2 раза в сутки в комбинации с ритонавиром в дозе 100 мг 2 раза в сутки;
• типранавир* (TPV) 250 мг капсула; применяется усиленный ритонавиром, 2 раза в сутки 500 мг+200 мг ритонавира.
ИИ с целью: блокирования фермента ВИЧ, участвующий во встраивании провирусной ДНК в геном клетки-мишени.
• долутегравир (DTG) 50 мг таблетка; 50 мг 1 раз в сутки.
• элвитегравир 150 мг/кобицистат 150 мг /эмтрицитабин 200 мг /тенофовир 300 мг* 1 таблетка 1 раз в сутки;
* При регистрации в Республике Казахстан.
В приоритетном порядке АРТ назначается всем пациентам в 3-4 стадии ВИЧ-инфекции или пациентам с количеством CD4+ лимфоцитов ≤ 350 кл/мкл.
− ВИЧ-позитивным лицам в дискордантных парах (для снижения риска трансмиссии ВИЧ неинфицированным партнерам), при условии предварительного консультирования обоих партнеров;
− при подготовке ВИЧ-инфицированного пациента к применению вспомогательных репродуктивных технологий.
Схема АРТ состоит не менее, чем из трех антиретровирусных препаратов. Предпочтение отдается комбинированным препаратам в фиксированных дозировках.
b NVP использовать у лиц с низким числом лимфоцитов CD4 (у женщин с СД4 менее 250/мкл, у мужчин с СД4 менее 400/мкл)
с вместо AZT при умеренной анемии или гранулоцитопении (уровень гемоглобина> 90 г/л или количество нейтрофилов> 1000 клеток/мкл) рекомендуется назначать ABC, или TDF, а при более выраженной анемии или гранулоцитопении – АВС или TDF.
d использование комбинированного препарата фиксированной дозировки DRV/c (при регистрации)
При невозможности использования вышеперечисленных препаратов ddI может быть назначен в качестве НИОТ в комбинации 3TC/FTC +EFV.
• пациенты, получающие противотуберкулезные препараты.
− при количестве CD4+ лимфоцитов от 50 до 250 клеток/мкл и нормальном уровне АЛТ или АСТ – NVP в сочетании с АВС, или TDF, или AZT + 3ТС, или FTC;
− при любом количестве CD4+ лимфоцитов – LPV/r или DRV/r или ATV/r в сочетании с АВС, или TDF, или AZT + 3ТС, или FTC.
Рекомендуемые схемы АРТ: назначается схема из предпочтительных АРВП – 2 НИОТ + 1 ИП/r, или 2НИОТ + 1 ННИОТ, или 2 НИОТ + 1 ИИ.
LPV/r в сочетании с AZT/3TC. В качестве третьего компонента схемы АРТ являются LPV/r в таблетках (400/100 мг 2 раза в сутки).
При непереносимости LPV/r можно использовать (в порядке приоритетности) – DRV/r (600/100 мг 2 раза в сутки), NVP (при CD4 < 250 клеток/мкл и нормальном уровне АЛТ и АСТ). Частота назначения LPV/r и DRV/r – не реже 2 раз в сутки.
При непереносимости LPV/r и DRV/r, можно назначить ATV/r или другие ИП/р. В качестве нуклеозидной основы рекомендуется ZDV/3TC. Применение EFV не рекомендуется в I триместрe беременности.
Для лечения пациентов с низким уровнем CD4+-лимфоцитов рекомендуется применять схемы, включающие бустированный ИП.
В качестве нуклеозидной основы рекомендуется применять комбинацию ABC с 3TC или TDF с 3TC в стандартных дозах (или комбинированный препарат TDF/FTC). Однако у пациентов с ВН более 100 000 копий/мл препараты, содержащие ABC, применять не рекомендуется.
В качестве альтернативы третьим препаратом можно назначить FPV/r из-за минимального влияния на функцию почек либо LPV/r.
ТDF не рекомендуется больным с почечной недостаточностью.
более чем в 2,5 раза выше верхней границы нормы (ВГН) – EFV или RPV (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ < 100000 копий/мл) в сочетании с TDF+3TC или TDF/FTC;
• при уровне активности АЛТ или АСТ более чем в 2,5 раза выше ВГН – DTG, бустированный RTV ИП (DRV/r или LPV/r) в сочетании с TDF+3TC или TDF/FTC.
При снижении числа CD4+ лимфоцитов менее 500 клеток/мкл рекомендуют начать АРТ одновременно с терапией ХГС.
При количестве CD4+лимфоцитов менее 350 клеток/мкл начинают лечение ВИЧ-инфекции, а затем присоединяют терапию ХГС.
Не рекомендуется сочетание рибавирина с зидовудином (увеличивается частота развития анемии), диданозином (повышается вероятность декомпенсации заболевания печени).
Оптимальным сочетанием НИОТ является TDF + 3TC или FTC в стандартных дозировках. При невозможности применять TDF назначают АВС.
• при нормальном уровне активности АЛТ/АСТ или повышении его не более чем в 2,5 раза выше ВГН – EFV, RPV (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ < 100000 копий/мл) или DTG (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ >100000 копий/мл) в сочетании с АВС или TDF + 3TC или TDF/FTC.
• при уровне активности АЛТ/АСТ более чем в 2,5 раза выше ВГН – DTG или бустированный ИП (LPV/r или DRV/r) в сочетании с АВС или TDF + 3TC или TDF/FTC.
У больных при сочетании ВИЧ-инфекции и ХГС, не получающих лечения ХГС, в состав схемы АРТ может быть включено сочетание ZDV+3TC.
Все ЛЖВ с диагностированным туберкулезом нуждаются в лечении ТБ и ВИЧ-инфекции, независимо от числа лимфоцитов CD4.
Первым начинают противотуберкулезное лечение, а затем как можно быстрее (в первые 8 недель лечения) назначают АРТ.
Больным ВИЧ/ТБ, имеющим выраженный иммунодефицит (число лимфоцитов CD4 менее 50 клеток/мкл), необходимо начать АРТ немедленно – в течение первых 2 недель после начала лечения ТБ.
При наличии туберкулезного менингита начало АРТ следует отложить до завершения фазы интенсивной терапии ТБ.
В начале АРТ у больных, получающих противотуберкулезное лечение, предпочтительным ННИОТ является EFV, который назначают вместе с двумя НИОТ.
При отсутствии EFV рекомендована схема лечения - 3TC (или FTC) + ZDV + ABC (или TDF).
В таблице 3 представлены варианты замены антиретровирусных препаратов при развитии нежелательныхэффектов.
Неудача лечения определяется как постоянно выявляемая вирусная нагрузка более 1000 копий/мл по результатам двух последовательных измерений, проведенных с интервалом в 2-4 недели, но не ранее, чем через шесть месяцев после начала использования АРВ-препаратов.
Основные лекарственные средства, имеющие 100% вероятность применения: см пункт Медикаментозное лечение, оказываемое на амбулаторном уровне.
• эмтрицитабин (FTC) 200 мг, капсула;
• рилпивирин* (RPV) 25 мг таблетка;
• дарунавир (DRV) 400 мг, 600 мг, 800 мг таблетка; 600 мг в комбинации с ритонавиром в дозе 100 мг 2 раза в сутки;
• типранавир* (TPV) 250 мг капсула; применяется усиленный ритонавиром, 2 раза в сутки 500 мг+200 мг ритонавира.
• элвитегравир 150 мг/кобицистат 150 мг /эмтрицитабин 200 мг /тенофовир 300 мг* 1 таблетка 1 раз в сутки;
• элвитегравир 150 мг/кобицистат 150 мг* 1 таблетка 1 раз в сутки.
Хирургические вмешательства: нет.
• туберкулеза (при исключении у пациента активного туберкулеза) –однократно изониазид (5 мг/кг), но не более 0,3 г в сутки + пиридоксин (при наличии) в дозе 25 мг/сут не менее 6 месяцев;
• пневмоцистной пневмонии в случае CD4 < 200 клеток/мкл, токсоплазмоза, в случае CD4 < 100 клеток/мкл – котримоксазол (960 мг 3 раза/неделю). Отменить профилактику если у пациента более 3 месяцев количество CD4+ - лимфоцитов стабильно превышает 200 кл/мкл, возобновить при падении количества CD4+ - лимфоцитов
• Диспансерное наблюдение пациентов получающих АРТ осуществляется совместно ПМСП и территориальным центром СПИД с кратностью посещений не менее 1 раза в 3 месяца.
• Вирусная нагрузка определяется перед началом АРТ. В дальнейшем следует измерять ВН первый раз не позднее 3 месяцев, затем 1 раз в 6 месяцев, при достижении неопределяемого уровня ВН.
• В случае отсутствия снижения ВН через 6 месяцев от начала лечения на 1 lоg10 или последовательного двукратного повышения ВН после исходной супрессии, следует провести генотипический тест на определение резистентности ВИЧ к антиретровирусным препаратам.
• Число лимфоцитов CD4 нужно измерять через 3 месяца, затем каждые 6 месяцев, при необходимости чаще в течение 1-го года АРТ, далее не реже 1 раз в год (за исключением случаев неэффективности лечения).
• Лабораторные исследования необходимо проводить не менее одного раза в 6 месяцев.
Таблица 4. Сроки проведения лабораторных исследований
х - лабораторное исследование показано независимо от используемых АРВ-препаратов;
x (АРВ-препарат) - исследование показано пациентам, которые получают указанный в скобках препарат.
b Пациентам с хроническими гепатитами биохимические показатели определяют согласно клиническому протоколу диагностики и лечения хронического вирусного гепатита В и С у взрослых в РК.
Через 3 месяца после начала приема АРВ-препарата клинически проявляющиеся побочные эффекты должны отсутствовать (а также субклинические, которые со временем могут проявиться клинически )
b Вирусная нагрузка уменьшается постепенно: у большинства пациентов (за исключением имеющих изначально высокую вирусную нагрузку) через 24 недели АРТ она должна быть < 50 копий/мл либо демонстрировать выраженную тенденцию снижения до этого уровня.
При расхождении между вирусологическими и иммунологическими показателями, приоритет за вирусологическими.
Число лимфоцитов CD4 необходимо определять каждые 3 месяца, по стабилизации СД4 лимфоцитов на фоне АРТ - 1 раз в 6 месяцев.
Цель АРТ - снижение ВН до неопределяемого уровня (пороговый уровень
При показателях ВН от 200 до 400 коп/мл – развитие резистентности возможно, необходимо усилить работу по соблюдению приверженности к АРТ.
Госпитализация
III степень (тяжелая) - повседневная жизнь существенно нарушена, часто требуется дополнительная помощь близких, медицинская помощь и лечение, возможно в стационаре;
IV степень (крайне тяжелая, жизнеугрожающая) - нормальная повседневная жизнь невозможна, требуется постоянная помощь посторонних, серьезное лечение, чаще всего в стационаре.
Информация
Источники и литература
Информация
5) Трумова Жанна Зиапеденовна – доктор медицинских наук, профессор РГП на ПХВ «Казахский национальный медицинский университет имени С.Д.
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Оценку нарушений познавательной деятельности (когнитивных функций) целесообразно проводить у всех ВИЧ-инфицированных пациентов без отягощающих факторов(тяжелые психиатрические заболевания, злоупотребление психоактивными веществами, в том числе алкоголем, текущие оппортунистические инфекции центральной нервной системы, другие неврологические заболевания) в течение 6 мес. со времени постановки диагноза. Данный подход позволяет точно определить исходные показатели и, соответственно, более точно оценить дальнейшие изменения. Для раннего скрининга когнитивных функций необходимо задать пациенту 3 вопроса (S.Simionietal. AIDS 2009, EACS 2012):
1. Часто ли у Вас бывают случаи потери памяти (например, Вы забываете значительные события, даже самые недавние, назначенные встречи и т.д.)?
Нейропсихологическое обследование должно включать в себя тесты для изучения следующих характеристик познавательной деятельности: слухоречевая и зрительная память, счет, скорость восприятия информации, внимание, , двигательные навыки. (Antinorietal.Neurology, 2007). В случае выявления патологии требуется обследование пациента у невролога, проведение МРТ головного мозга и исследовании спинномозговой жидкости (СМЖ) на вирусную нагрузку и, если есть к тому показания, провести исследование генотипической резистентности к препаратам в двойной пробе СМЖ и плазмы крови. Если у пациента выявлена патология нейрокогнитивных функций на этапе скрининга или при дальнейшем нейропсихологическом обследовании, необходимо рассмотреть возможность включения в схему препаратов, потенциально воздействующих на центральную нервную систему. К ним относятся либо те препараты, проникновение которых в СМЖ было продемонстрировано в исследованиях, проведенных у здоровых ВИЧ-инфицированных пациентов(концентрация выше IC90 у более чем 90% обследуемых пациентов), либо те, для которых доказана краткосрочная (3–6 мес.) эффективность воздействия на когнитивные функции или на снижение ВН на СМЖ, при условии, что оценка проводится в отсутствие каких-либо других совместно принимаемых препаратов или в рамках контролируемых исследований, результаты которых рецензируются экспертами (EACS 2012).
За более, чем тридцатилетний период изучения ВИЧ-инфекции и СПИДа, было создано немало трудов по этиологии, диагностике и лечению болезни. До сих пор совершенствуются клинические рекомендации по комбинации антиретровирусных препаратов, а также по лечению различных форм резистентности к АРВТ.
Разрабатываются организационные основы профилактической помощи и противоэпидемические мероприятия. В социальной работе с заражёнными людьми акцент смещается в сторону их психологической поддержки, особенно после впервые установленного диагноза. Итак, рассмотрим подробнее, что такое ВИЧ-инфекция, ее пути передачи, особенности лабораторной диагностики и лечения.
1. Эпидемия ВИЧ в мире
В настоящее время ВИЧ-инфекция стала убиквитарным заболеванием: она существует везде, где есть источник инфекции – человек.
Период с 1981 г. по 2000 г. характеризуется стремительным развитием эпидемии. В этот временной интервал эпидемия вышла за границы контроля и приобрела статус пандемии. Так, за эти годы число инфицированных достигло 26,5 миллионов человек.
В 2014 году во всём мире насчитывалось 36,9 млн. человек с положительным ВИЧ статусом. В этом же году охват лекарственной терапией больных составил около 40%.
Инфекция распространена неравномерно по континентальным регионам и отдельным странам. В мировой статистике для оценки пандемии пользовались числом диагностированных случаев ВИЧ и СПИДа. Однако этот показатель недостоверен и не даёт глубокой оценки современного распространения инфекции.
Это обусловлено тем, что для установления диагноза СПИД необходимо наличие оппортунистических инфекций (заболеваний, которые не встречаются у человека с нормальным иммунным статусом). Их диагностика продолжительна и сложна технически.
Эти факторы совместно с длительным промежутком времени развития СПИД вносят своеобразные коррективы в настоящую статистику ВИЧ-инфекции на всей планете. Истинная картина заболеваемости на разных континентах и в разных странах представлена плохо.
Например, наибольшее число человек, больных СПИДом (за всё время наблюдения) выявлено в США, но на самом деле страна отличается невысоким уровнем распространённости инфекции. Центральная Африка изобилует такими больными. В настоящее время на этот континент направлено множество сил уполномоченных организаций по борьбе с инфекцией.
Статистика эпидемиологических данных (заболеваемость, распространённость, поражённость) не отражает реальность ситуации по заболеванию в Африке, поскольку случаи там регистрируются плохо или не регистрируются вовсе.
Восточная Европа характеризуется значительно более поздним началом эпидемии, нежели в Западном полушарии, поэтому людей, имеющих СПИД - относительно мало, опять же из-за длительного развития ВИЧ-инфекции в СПИД.
Региональная статистика в 2014 году указана в таблице 1.

Таблица 1 - Региональная статистика по ВИЧ-инфекции, данные за 2014 г. Для просмотра кликните по таблице
Обобщая данные, можно сказать, что в мире, в 2014 году насчитывается:
- 1 36,9 миллионов человек с положительным статусом;
- 2 70% (приблизительно) больных из этой цифры приходится на Африканский регион;
- 3 40% инфицированных охвачены антиретровирусной терапией.
1.1. Ситуация в Российской Федерации
Распространённость инфекции в России оценивается с помощью специализированных учреждений по профилактике этих заболеваний.
Именно такие медицинские организации в каждом субъекте РФ несут полную информацию об эпидемиологической ситуации в регионе. Полученные сведения репрезентативны для всеобщей оценки ситуации по стране. Основная статистика представлена в ежегодном отчёте Управления Роспотребнадзора РФ.
В таблице 2 представлена заболеваемость в субъектах РФ в 2016 году, в показателе на 100 тысяч населения.
| Краевые, областные, автономные субъекты РФ | Показатель на 100 000 человек |
|---|---|
| В целом по России | 70,6 |
| Кемеровская | 228,9 |
| Иркутская | 163,7 |
| Самарская | 161,6 |
| Свердловская | 156,8 |
| Ленинградская | 1086,6 |
| Оренбургская | 117,5 |
| Тюменская | 150,7 |
| Челябинская | 154,1 |
| Ульяновская | 97,3 |
| Пермский | 125,0 |
| Тверская | 74,1 |
| Алтайский | 114,2 |
| Ивановская | 72,6 |
| Новосибирская | 137,0 |
| Томская | 138,2 |
| Красноярский | 129,6 |
| Ханты-Мансийский А.О. | 124,5 |
| Омская | 110,2 |
| Курганская | 110,0 |
| Нижегородская | 71,2 |
| Республика Крым | 83,3 |
| Хакасия | 82,5 |
| Удмуртия | 75,2 |
| Башкортостан | 68,5 |
Таким образом, в стране наблюдается положительная динамика относительно роста заболеваемости инфекцией. Сохраняется уровень заболеваемости, несмотря на снижение темпов прироста в отдельных регионах РФ. Важной проблемой в России стал выход эпидемии из групп риска в общую популяцию.
Сложившаяся ситуация в стране требует проактивного вмешательства со стороны органов здравоохранения и вовлечённых в проблему организаций.
2. Вирус иммунодефицита человека
Вирус иммунодефицита человека (ВИЧ, HIV) относят к подсемейству лентивирусов, семейству ретровирусов. Первенство в открытии принадлежит двум группам учёных. Впервые он был выделен в 1983 году французским исследователем. Материалом послужили лейкоциты француза-гомосексуалиста.
Первым названием стал синдром лимфаденопатии того самого француза – вирус, ассоциированный с лимфаденопатией (LAV). Одновременно, американская группа под руководством R. Gallo сообщила о выделении вируса от больного с такими же симптомами лимаденопатии. Впоследствии его обозначили как человеческий лимфотропный вирус 3-го типа.
В настоящее время различают два типа вируса. Это ВИЧ 1 и ВИЧ 2. Они отличаются антигенной структурой и генетическим материалом. Каждый из видов имеет свои особенности строения. ВИЧ 2 был выделен в 1985 году и считается менее контагиозным. Это объясняется более длительным временем репликации РНК, соответственно, вероятность его передачи на ранних стадиях болезни снижается в разы.
3. Строение вирусной частицы
Вирус диаметром около 100 нм, имеет генетический материал, находящийся внутри капсида (рисунок 1). Он представлен 2 молекулами РНК. РНК состоит из 9749 нуклеотидных пар, которые способны кодировать белки и ферменты. Капсид, окружающий РНК, представлен 2000 молекул белка р24 (основной структурный белок капсида).
ВИЧ 1 внутри нуклеокапсида содержит три фермента:
- 1 Обратная транскриптаза.
- 2 Протеаза.
- 3 Интеграза.
Капсид, в свою очередь, окружен матриксом. В состав его входит белок р17 (основной структурный белок матрикса). Матрикс и нуклеокапсид окружены липидной оболочкой (наружная оболочка).
Липидная оболочка состоит из фосфолипидов, в которые встроены гликопротеиновые комплексы (комплекс gp41- gp120). Gp120 соединяется с CD4-рецепторами при проникновении вируса в организм человека.

Рисунок 1 - Строение вириона вируса иммунодефицита человека. Источник иллюстрации - Википедия
ВИЧ 2 схож по строению с ВИЧ 1. Вместе с тем, отличается генетическим материалом, молекулярной массой белков и антигенными свойствами.
4. Источник инфекции
В настоящее время заболевание считается антропонозом. Источником ВИЧ 1-го типа предположительно являются шимпанзе. Однако полноценным звеном эпидемического процесса этот вид обезьян быть не может, ввиду низкого потенциала передачи вируса от обезьяны к человеку и их сравнительно малой численностью по сравнению с населением Земли.
Природным резервуаром ВИЧ 2 является вид обезьян, так называемые дымчатые мангобеи. Особи этих обезьян более многочисленны, поэтому в литературе можно встретить указание на антропозоонозный характер передачи вируса ВИЧ 2.
5. Локализация возбудителя
Вирус иммунодефицита и его частицы обнаруживаются в полном спектре человеческих клеток. В Т- и В-лимфоцитах, лейкоцитах, в макрофагах, в неспецифических клетках нервной ткани и т.д.
6. Механизм и пути передачи
Для поддержания и развития эпидпроцесса нужны специальные условия, обеспечивающие сохранность вируса.
Эпидемиологические исследования доказали возможность передачи в следующих ситуациях:
- 1 При прямом контакте (половой путь);
- 2 От инфицированной матери плоду в процессе естественных родов;
- 3 При грудном вскармливании;
- 4 При переливании инфицированной крови;
- 5 Парентерально, при вмешательствах инфицированными инструментами.
Важнейшую роль в передачи инфекции играет тропность вируса к клеточному рецептору CD4⁺. Лимфоциты и макрофаги, несущие на своей поверхности этот рецептор, локализуются в основном в ротовой полости, во влагалище и в кишечнике. Это ограничивает заражение потенциального восприимчивого хозяина.
Наличие дефектов на слизистой рта, воспалительных очагов в половых путях увеличивает риск заражения в несколько раз. То есть, любые нарушения целостности слизистой способствуют проникновению инфицированного вирусом биологического материала в ткани и восприимчивые клетки.
Достоверные исследования свидетельствуют о 30 – 40 % заразившихся половых партнеров, имеющих гетеросексуальные контакты на протяжении одного года с инфицированными.
7. Патогенез
Вирус обеспечивает себе длительное существование и выживание в организме человека. Циркуляция вируса происходит во внутренних жидких средах организма. Вирион живёт около 3 часов от момента прикрепления к клетке-мишени до репликации.
После прикрепления вириона к рецепторам CD4⁺ РНК проникает в клетку. Фермент обратная транскриптаза является вспомогательным фактором для образования ДНК ВИЧ. Образовавшаяся ДНК встраивается в геном клетки.
8. Классификация
Выделяют 5 стадий заболевания. Стадии определяются клинической картиной. Основные симптомы и синдромы ВИЧ-инфекции представлены в таблице 3.
Таблица 3 - Стадии ВИЧ-инфекции
9. Диагностика инфекции
В настоящее время для диагностики заболевания пользуются стандартным лабораторным методом обнаружения Ат/Аг ВИЧ с последующим подтверждением с помощью иммуноблота.
9.1. Иммуноферментный анализ
9.2. Быстрые тесты
Это тесты, выполняемые менее, чем за час. Их используют в трансплантологии, при срочном родоразрешении беременных с неизвестным ВИЧ статусом, в эпидемиологическом надзоре, при постконтактной профилактики заражения. В качестве материала используют слюну, кровь, плазму крови, соскоб со слизистой дёсен. Результаты быстрых тестов предварительные и должны быть подтверждены классическими методами.
9.3. Иммуноблот
Сам метод заключается в проведении ИФА с антигенами ВИЧ. Аг вируса фракционировано распределены на нитроцеллюлозной мембране в зависимости от молекулярного веса. Таким образом, антигенные детерминанты на белковых частицах вируса под действием иммуноферментного анализа проявляются в виде отдельных полос.
Интерпретация полученных в ходе иммуноблоттинга результатов зависит от разных критериев.
- 1 Для отрицательного результата характерно отсутствие всех полос или слабое реагирование с p18.
- 2 Положительный результат выводится, если в ИБ реагируют p25, gp41,gp120/160 (рекомендации CDC).
- 3 О неопределенном результате свидетельствует присутствие одного, либо нескольких антигенов, не удовлетворяющих критериям положительного результата.
Альтернативой ИБ является линейный анализ. Отличием от иммуноблоттинга является отсутствие проведения электрофореза полоски нитроцеллюлозы. В линейном анализе используются рекомбинантные антигены вирусов иммунодефицита двух типов.
10. Лекарственная терапия
Лечение болезни заключается в базисной терапии и терапии вторичных и сопутствующих состояний. Основная терапия определяется стадией, фазой заболевания, уровнем CD4⁺ - лимфоцитов, РНК ВИЧ.
Лекарственные препараты этиотропны. Однако, искоренить вирус из организма пока невозможно, поэтому действие химических веществ только подавляет размножение вируса.
Первые рекомендации по лечению ВИЧ-инфекции были изданы в 1993 году, но применение, например, зидовудина упоминается и в 1987 году.
С появлением новых лекарств происходит периодический пересмотр схем лечения практикующими врачами, научными сотрудниками в пользу безопасности и эффективности в течение длительного срока применения.
АРВТ действует на звенья жизненного цикла ВИЧ:
- 1 Присоединение к лимфоциту вируса с помощью соединения gp41 и 120 к хемокиновым рецепторам и рецепторам CD4⁺ .
- 2 Синтез ДНК вируса на матричной РНК под действием ОТ.
- 3 Встраивание провирусной ДНК в человеческую ДНК.
- 4 Формирование новых частиц.
В настоящее время разработаны и внедрены в практику химические препараты, блокирующие действие ферментов вируса.
Выделяют пять основных групп препаратов для лечения ВИЧ инфекции (см. таблицу 4).
Таблица 4 - Препараты для лечения ВИЧ-инфекции (АВРТ). Для просмотра кликните по таблице
АРВТ назначается больным на любой стадии, особенно при неблагоприятных показателях крови. Оправданность назначения АРВТ по эпидемиологическим показаниям закреплена правовыми документами.
11. Профилактические мероприятия
Предупреждение заражения ВИЧ-инфекцией населения страны в целом будет эффективным и достигнет наибольших успехов только при объединении всех мер противодействия на разных организационных уровнях. Велика роль и поддержки других стран.
Направления профилактики сводятся к двум основным постулатам:
- 1 Не дать заразиться здоровым людям;
- 2 Снизить вирусную нагрузку у инфицированных и ограничить возможность заражения других лиц источником инфекции.
Первый пункт подразумевает информирование населения об опасности инфекции, её путях передачи и исходе заболевания.
Второй пункт рассматривает возможности применения эффективных средств терапии, адаптированных возрасту и другим особенностям пациентов.
Инфекция вируса иммунодефицита человека (ВИЧ): диагностика, лечение, профилактика
Вирус иммунодефицита человека (ВИЧ) — сферический оболочечный РНК-ретровирус, образующий при помощи обратной транскриптазы ДНК-копию вирусной РНК. Последняя встраивается в ядро клетки хозяина и служит шаблоном для производства последующих вирусных РНК. Для репликации возбудителя необходимы три гена: gag, pol и env. ВИЧ определяют как лентивирус.
Патогенными для человека считают ВИЧ-1 (наиболее распространённый) и ВИЧ-2 (регистрируют в основном на территории Западной Африки), которому свойственна меньшая вирулентность.
Эпидемиология ВИЧ-инфекции. ВИЧ-инфекция распространена во всём мире. Передача вируса осуществляется парентеральным и половым путём. В группу риска входят пациенты, ведущие беспорядочную половую жизнь (особенно при наличии изъязвлений на слизистой оболочке половых органов). В развитых странах чаще всего жертвами ВИЧ становятся мужчины (гомосексуалисты и наркоманы).
Передачу вируса между гетеросексуальными партнёрами встречают реже. В развивающихся странах ВИЧ обычно распространяется при гетеросексуальных связях, переливании неисследованной заражённой крови и использовании инфицированного медицинского инструментария. Возможна передача инфекции от матери к плоду.
Патогенез инфекции вируса иммунодефицита человека. Сначала вирус поражает клетки, обладающие СD4-рецепторами (например, Т-лимфоциты, макрофаги). Затем следует репликация, приводящая к сокращению количества здоровых Т-лимфоцитов и снижению клеточного иммунитета. Различные штаммы вируса имеют разное сродство к клеткам с различными хемокиновыми рецепторами.
При снижении Т-клеточного иммунитета также уменьшается активность В-лимфоцитов. Кроме того, ВИЧ поражает нейроны, стимулирует выделение большого количества цитокинов, способствующих дальнейшему повреждению нервной системы. Большинство клинических признаков при ВИЧ-инфекции связано со вторичными инфекционными заболеваниями, возникающими вследствие снижения иммунитета (уменьшение СD4-клеток).
Клинические признаки инфекции вируса иммунодефицита человека. Через несколько недель после заражения возникает мононуклеозоподобный синдром, сопровождающийся появлением сыпи, лихорадки и лимфаденопатии. Затем следует латентный период, который может продолжаться 10—15 лет.
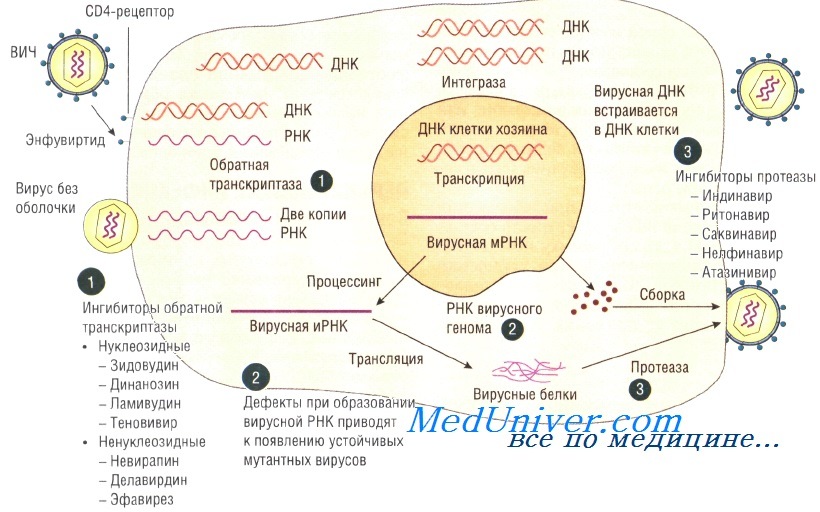
ВИЧ-инфекция
Диагностика инфекции вируса иммунодефицита человека. Диагноз ВИЧ-инфекции подтверждают двумя серологическими методами: ИФА и постановкой иммуноблоттинга (вестерн-блоттинга), направленных на определение специфических антител. РНК вируса определяют с помощью ПЦР.
При обследовании пациенты с подозрением на ВИЧ должны получать исчерпывающую консультацию врача. Поскольку сероконверсия может продолжаться в течение 3 мес, при первоначальном отрицательном результате необходимо провести повторный анализ.
Лечение необходимо сопровождать регулярным измерением вирусной нагрузки. Вирус может расти в лимфоцитах, но это не используют в диагностических целях.
Лечение инфекции вируса иммунодефицита человека
Для лечения ВИЧ-инфекции применяют:
• нуклеозидные ингибиторы обратной транскриптазы (например, зидовудин);
• ненуклеозидные ингибиторы обратной транскриптазы (например, невирапин);
• ингибиторы протеаз (например, индинавир). Основные три направления лечения:
• торможение вирусной репликации;
• предупреждение появления устойчивых форм;
• повышение иммунитета пациента.
Терапию начинают проводить пациентам с выраженными симптомами, при развитии заболеваний, вызванных условно-патогенной микрофлорой, а также при снижении количества клеток с CD4-рецепторами ниже 0,2x10 9 /л. При показателях выше 0,2x10 9 /л и ниже 0,35x10 9 /л необходимо тщательно продумать тактику лечения (с учётом риска развития побочных эффектов и состояния пациента).
Существуют разнообразные режимы лечения ВИЧ-инфекции. На начальном этапе обычно применяют:
• ненуклеозидный ингибитор обратной транскриптазы + два препарата из группы нуклеозидных ингибиторов обратной транскриптазы;
• ингибитор протеазы + нуклеозидный ингибитор обратной транскриптазы.
При заражении устойчивыми штаммами слудует соблюдать осторожность и применять нестандартные методы, основанные на индивидуальном подходе. В связи с тем что РНК-вирусы не имеют достаточно эффективных генетических механизмов коррекции, мутации, приводящие к образованию устойчивых штаммов, происходят достаточно быстро.
В начале лечения происходит повышение иммунитета, поэтому в связи с усилением иммунного ответа симптомы сопутствующих заболеваний могут усилиться.
Профилактика ВИЧ-инфекции. Для профилактики заражения необходимо избегать половых контактов с лицами, входящими в группу риска, и незащищённых половых связей (без использования барьерной контрацепции). Кроме того, необходимо тщательно исследовать донорскую кровь и уничтожать её образцы, подозрительные на ВИЧ-инфекцию.
Снижению риска заражения среди наркоманов способствуют программы медицинского просвещения и пропаганда использования одноразовых шприцев и игл. К сожалению, разнообразие антигенов вируса делает невозможным создание эффективной вакцины. При случайных проколах кожи медицинскими иглами необходимо проходить профилактический курс антиретровирусной терапии. Риск передачи инфекции от матери к плоду можно снизить с помощью проведения эффективной антиретровирусной терапии, правильно выполненного кесарева сечения и отказа от кормления грудью.
При отсутствии возможности проведения высокоактивной антиретровирусной терапии (в развивающихся странах) лечение проводят коротким курсом для снижения риска передачи инфекции.
У пациентов с ВИЧ-инфекцией развиваются тяжёлые кандидозы кожи и слизистых оболочек, сопровождающиеся изъязвлением слизистой оболочки ротовой полости и поражением пищевода, что приводит к дисфагии и существенной потере массы тела. Для лечения острой инфекции назначают приём внутрь флуконазола, но при длительной терапии часто развивается устойчивость возбудителей. Кроме того, очень серьёзной проблемой считают криптококковый менингит.
Инфекция Toxoplasma gondii у ВИЧ инфицированных. Инфекция персистирует в организме на протяжении длительного времени. Снижение иммунитета приводит к активации возбудителя и развитию различных патологических процессов (объёмные образования головного мозга, сопровождающиеся энцефалитом и др.).
При энцефалите отмечают высокую температуру, головные боли, судороги, неврологические расстройства. Возможно развитие комы. При компьютерной томографии обнаруживают множественные фокальные очаги кольцевидной формы. Исследуемый материал — биоптат мозга. Методы диагностики — культивирование возбудителя, полимеразная цепная реакция. Для лечения энцефалита применяют пириметамин + сульфадиазин. После выздоровления необходимо проведение курса поддерживающей терапии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
ВИЧ. Вирус иммунодефицита человека. СПИД. Эпидемиология вич-инфекции.
Вирус иммунодефицита человека (ВИЧ) — возбудитель своеобразной инфекции, проявляющейся развитием прогрессирующих нарушений иммунного реагирования в результате длительного циркулирования вируса в лимфоцитах, макрофагах и клетках нервной ткани.
Следствие ВИЧ-инфекции — синдром приобретённого иммунодефицита (СПИД). ВИЧ входит в состав подсемейства Lentivirinae семейства Retroviridae. Характерные особенности ретровирусов — уникальное строение генома и наличие обратной транскриптазы (РНК-зависимая ДНК-полимераза). Обратная транскриптаза (или ревертаза) обеспечивает обратную направленность потока генетической информации — не от ДНК к РНК, а наоборот, от РНК к ДНК, в связи с чем семейство и получило своё название 1от англ. retro, обратно].
Геном вич образует две идентичные молекулы однонитевой несегментированной +РНК. Репродуктивный цикл вич уникален, так как при его реализации образуются промежуточные продукты-интермедиаты ДНК.
В настоящее время выделяют два типа вирусов: ВИЧ-1 (HIV-1)— основной возбудитель ВИЧ-инфекции, ВИЧ-2 (HIV-2) — менее вирулентный аналог ВИЧ-I, редко вызывающий типичные проявления СПИДа; его выделяют преимущественно в Западной Африке.
Впервые ВИЧ выделили французский вирусолог Л. Монтаньё (1983) под названием LAV [от англ. tymphoadenopathy associated virus] и американский вирусолог Р. Гэлло (1984) под названием вирус HTLV-III [Т-лимфотропный вирус человека III типа]. После установления идентичности HTLV-III и LAV во избежание путаницы вирусу было присвоено название HIV [англ. human immunedeficiency virus, вирус иммунодефицита человека], или ВИЧ.
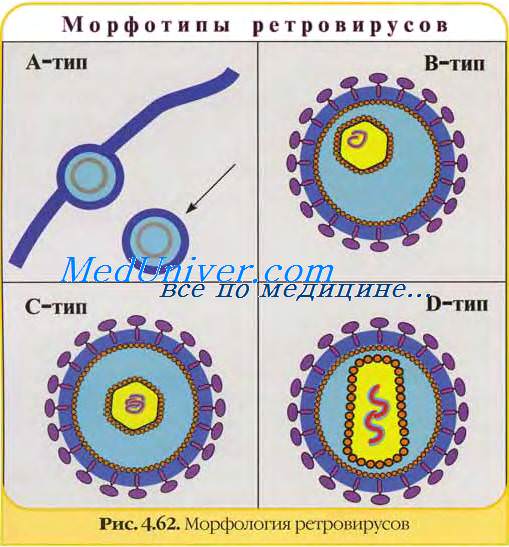
Эпидемиология вич-инфекции
ВИЧ-инфекция — типичный антропоноз, у животных воспроизвести заболевание не удаётся. Резервуар вируса вич-инфекции — инфицированный человек. Возбудитель передаётся трансмиссивно.
Основной фактор передачи вич-инфекции — половые контакты (вирус проникает в кровь через повреждения слизистых оболочек). Второй по значимости фактор передачи вируса вич-инфекции — использование одних и тех же игл и шприцев наркоманами.
ВИЧ чувствителен к действию высоких температур (при 56 X инактивируется за 30 мин, при 70-80 °С — через 10 мин), этанола, эфира, ацетона и многих дезинфектантов. В крови и других биологических материалах при комнатной температуре вирус сохраняет жизнеспособность в течение нескольких суток.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

