Вич энцефалит у детей
Обновлено: 18.04.2024
ВИЧ-энцефалопатия (ВИЧ-энцефалит) у ребенка
ВИЧ-1 является ретровирусом, который инфицирует клетки, несущие CD4-рецепторы и хемокиновые рецепторы (например, CCR5, CXCR4), включая Т-хелперы (CD4-клетки) и моноциты. Новорожденные могут быть инфицированы внутриутробно, при рождении или при кормлении грудью, но в большинстве случаев инфицирование происходит во время родов. Нагрузка материнской плазмы вирусами ВИЧ — наиболее важный прогностический фактор ВИЧ-инфекции новорожденных, но риск передачи повышается при преждевременных родах, длительном безводном периоде, других инфекциях, передающихся половым путем, при хориоамнионите и родах через естественные родовые пути с оперативным пособием (Abrams et al, 1995; Peckham и Gibb, 1995). В группах без грудного вскармливания выявлено 15-20% инфицированных по сравнению с 30-40% в популяции с грудным вскармливанием (European Collaborative Study, 1991,1994; Newell et al, 2004).
Вмешательства, включая антиретровирусную терапию во время беременности, во время родов и в послеродовом периоде; кесарево сечение до начала родовой деятельности и воздержание от кормления грудью может уменьшить передачу вирусов от матери к плоду до уровня менее 1% (Hawkins et al., 2005).
Вирус иммунодефицита человека относится к нейротропным вирусам, хотя продуктивная инфекция в ЦНС, вероятно, ограничивается макрофагами и микроглией. Вовлечение ткани головного мозга происходит вскоре после инфицирования инфицированность микроглии определяется уже через семь дней после переливания зараженной крови. In vitro ВИЧ инфекция приводит к активации эндотелия сосудов мозга, повышая риск проникновения клеток и частиц вируса в ЦНС.
ВИЧ-индуцированная экспрессия ICAM-1 (англ. Inter-Cellular Adhesion Molecule 1 — молекула межклеточной адгезии) на эндотелиальных клетках микрососудов головного мозга человека увеличивает краевое скопления лейкоцитов в сосудистом русле мозга, приводя тем самым к появлению большего количества мишеней ВИЧ-инфекции в пределах ЦНС (Stins et al, 2003). Небольшое педиатрическое исследование продемонстрировало связь между воспалительными медиаторами Т-клеток в ликворе и вирусной нагрузкой ВИЧ-инфекцией в СМЖ (McCoig et al., 2004). ВИЧ в ЦНС способствует воспалительному процессу, который со временем приводит к смерти клеток и выпадению нейронов, возможно, посредством апоптоза (Epstein и Gendelman, 1993). Патологические данные (Sharer et al., 1986) включают уменьшение веса мозга с возрастом.
Воспалительный клеточный инфильтрат, состоящий из микроглии, лимфоцитов, плазматических клеток и особенно из многоядерных гигантских клеток, распределяется по всему мозгу, но особенно заметен в глубинных структурах, таких как базальные ганглии и стволе мозга. Присутствуют выраженные воспалительные изменения и кальцификация мелких или средних сосудов, особенно в глубоких структурах мозга. Это может объяснить возникновение ишемических инфарктов и инсультов у детей с ВИЧ-инфекцией (Frank et al., 1989; Parketal, 1990). В спинном мозге только в редких случаях развивается вакуолярная миелопатия, частая у взрослых (Dickson et al., 1989).
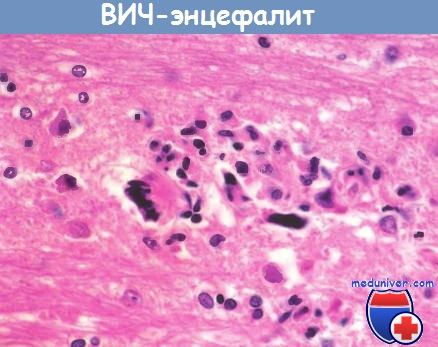
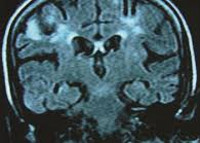
ВИЧ-энцефалит.
Обратите внимание на микроглиальные узелки
и многоядерные гигантские клетки.
Более тонкие когнитивные расстройства встречаются по крайней мере у 30% детей с ВИЧ-инфекцией, и у многих возникают сложности языкового и речевого характера и проблемы при обучении в школе (Tardieu et al., 1995; Pearson et al., 2000). В классических случаях у новорожденных представлены задержка в развитии, микроцефалия и двусторонний двигательный дефицит. Данная патология часто сочетается с другими оппортунистическими инфекциями, включающими в себя цитомегаловирусную и пневмоцистную пневмонии. В одном детальном исследовании, проведенном в США, у детей инфицированных как ВИЧ, так и ЦМВ отмечалось существенное повышение риска развития заболевания ЦНС с худшим отдаленным неврологическим прогнозом (Kovacs et al., 1999). У этих новорожденных клиническая картина напоминает таковую у детей со стойкими неврологическими повреждениями и проблемами развития; для них не характерна картина деменции, наблюдаемая у инфицированных взрослых или детей старшего возраста с более зрелой тканью мозга (Tardieu et al., 2000).
Более чем в двух третях случаев симптоматического течения на КТ выявляется атрофия мозга, повышенное размягчение белого вещества и примерно в четверти случаев кальцификация базальных ядер (Belman et al., 1986, DeCarli et al., 1993; Pearson et al., 2000). В большинстве случаев при MPT выявляются усиление сигнала в области белого вещества и признаки дегенеративных изменений коры головного мозга (Chamberlain et al., 1991; Pavlakis etal., 1995).
У маленьких детей в связи с персистентностью трансплацентарных материнских антител требуются прямые методы определения, включая либо ВИЧ РНК ПЦР, bДНК ВИЧ ПЦР, либо провирусную амплификацию ДНК ВИЧ. Прогрессирование ВИЧ заболевания и потребность в антиретровирусной терапии определяется клинической оценкой и подсчетом количества CD4 и вирусной нагрузки ВИЧ в плазме.
До эпохи успешного лечения ВИЧ инфекции лишь около 50% зараженных детей доживали до 10-летнего возраста, а при наличии неврологических признаков и симптомов присутствовал очень высокий риск стремительного прогрессирования заболевания во всех возрастных группах (Pearson et al., 2000). С появлением комбинированной антиретровирусной терапии (APT), большинство ВИЧ-инфицированных детей, вероятно, имеют больше шансов (Gibb et al., 2003).
Решающим является раннее выявление ВИЧ-инфицированных новорожденных с риском развития энцефалопатии, поэтому лечение может быть начато достаточно рано, чтобы предотвратить необратимое нейротоксическое повреждение, если это возможно (Sanchez-Ramon et al., 2003). По данным французского исследования, у 40 детей с APT до 6-месячного возраста не отмечено раннего начала тяжелой ВИЧ-инфекции, включая энцефалопатию на протяжении первых 24 месяцев жизни, тогда как в группе с отсроченной терапией (n=43) у 3 пациентов развилась энцефалопатия (Faye et al., 2004).
Хотя эти показатели незначительны, лечение в младенческом возрасте целесообразно для предотвращения необратимых неврологических осложнений. Однако в случаях, когда нейротоксическое повреждение двигательных нейронов уже произошло в детском возрасте, неудивительно, что оно не может восстановиться при комбинации APT (Foster et al., 2006). Тем не менее было подтверждено, что APT может предупредить или улучшить более тонкие нейропсихологические проблемы (Sanchez-Ramon et al., 2003). На данной стадии можно лишь предполагать, будут ли выжившие при вертикальной инфекции ВИЧ (с APT или без нее) иметь повышенный риск раннего развития ВИЧ-деменции или других неврологических синдромов во взрослом возрасте.
КТ-исследование ребенка с ВИЧ-энцефалопатией: кальцификация базальных ядер. Нейропатогенез ВИЧ.
Предположительно вирус инфицирует эндотелиальные клетки капилляров мозга и проникает через базолатеральную поверхность этих клеток к астроцитам, выстилающим гематоэнцефалический барьер (ГЭБ).
Инфицирование обоих типов клеток приводит к нарушению целостности ГЭБ и проникновению в мозг инфицированных Т-клеток и макрофагов.
В результате этого осуществляется ВИЧ-инфицирование других клеток мозга (например, олигодендроцитов и микроглии).
Затем начинается продукция ВИЧ и вирусных белков, а также высвобождение различных цитокинов (в частности, TNF и низкомолекулярных веществ).
Эти вещества могут вызывать нарушение межклеточной передачи сигнала, блокируя действие нейротропных факторов.
Прямое инфицирование клеток, а также высокая концентрация вирусных белков (например, гликопротеинов оболочки, Tat, Nef) и цитокинов оказывают прямое токсическое действие на нервные клетки, повреждая их мембрану.
Диагностика приобретенного ВИЧ-энцефалита по КТ, МРТ
а) Определения:
• ВИЧ-1-энцефалит/ВИЧ-1-энцефалопатия (ВИЧЭ)
• Прямое ВИЧ-инфицирование головного мозга:
о Отсутствие оппортунистических инфекционных заболеваний
о Когнитивные, поведенческие и двигательные аномалии в 25-70% случаев
о Наиболее частая неврологическая манифестация ВИЧ-инфекции
• Умеренные когнитивные нарушения, несмотря на хороший вирусологический ответ на терапию
б) Визуализация:
1. Общие характеристики приобретенного ВИЧ-энцефалита:
• Лучший диагностический критерий:
о Атрофия головного мозга + двустороннее диффузное изменение белого вещества (БВ):
- Картина при диагностической визуализации/патологоанато-мическом исследовании варьирует в зависимости от возраста пациента и остроты симптомов заболевания
• Локализация:
о Перивентрикулярное БВ/БВ полуовального центра с двух сторон, базальные ганглии, мозжечок, ствол мозга
• Размеры:
о Вариабельны, часто диффузный характер поражений
• Морфология:
о Распространяется до границы между серым и белым веществом
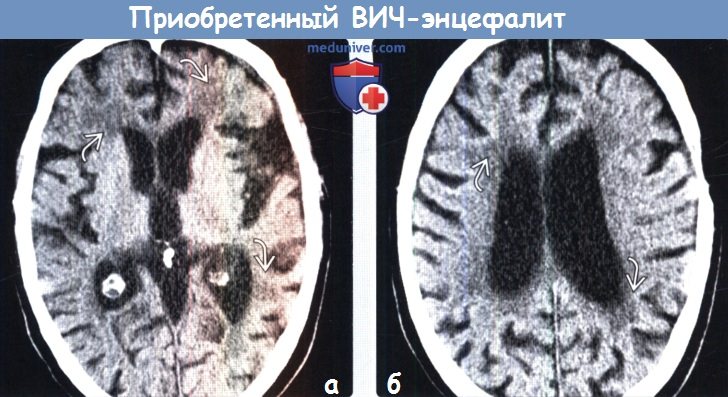
(а) Бесконтрастная КТ, проведенная по поводу снижения когнитивной функции у мужчины 38 лет с длительным анамнезом ВИЧ/СПИД, который получал ВААРТ, аксиальный срез: обратите внимание на выраженную атрофию головного мозга, а также зоны низкой плотности в структуре субкортикального белого вещества.
(б) Бесконтрастная КТ, аксиальный срез: у этого же пациента определяется характерное снижение плотности перивентрикулярного белого вещества в сочетании с диффузным расширением борозд и боковых желудочков.
2. КТ признаки приобретенного ВИЧ-энцефалита:
• Бесконтрастная КТ:
о Дети: атрофия и диффузное снижение плотности белого вещества:
- Внутриутробное инфицирование ВИЧ: характерны двусторонние и симметричные кальцификаты в базальных ганглиях и БВ лобных областей с возможным контрастным усилением
о Взрослые: умеренная атрофия или ее отсутствие, снижение плотности БВ
о Масс-эффект отсутствует
• КТ с контрастированием:
о Отсутствие накопления контрастного вещества
3. МРТ признаки приобретенного ВИЧ-энцефалита:
• Т1-ВИ:
о Изменений в БВ может не наблюдаться
• Т2-ВИ:
о Два визуализационных паттерна:
- фокальные участки гиперинтенсивного сигнала
- Диффузное усиление сигнала от БВ от умеренной до высокой степени выраженности
о Распространенность и протяженность поражения БВ не всегда коррелирует с клинической картиной
• FLAIR:
о Тот же визуализационный паттерн, что и на Т2-ВИ
о Обеспечивает раннее выявление мелких патологических очагов, локализованных в кортикальном/субкортикальном и глубоком БВ
о Большая заметность изменений (по сравнению с Т2-ВИ)
• Постконтратсное Т1-ВИ:
о В вовлеченных областях контрастное усиление отсутствует
• МР-спектроскопия:
о СПИД-дементный комплекс
- ↑ пиков миоинозитола, холина, в белом веществе и базальных ганглиях
- ↓ пика N-ацетиласпартата (NAA) в белом веществе
о Пациенты без симптомов с сохранным сознанием
- Умеренное ↑ пика миоинозитола
• Два основных последствия ВИЧ-инфекции мозговой ткани
о Атрофия мозговой ткани, обусловленная смертью нейронов
о Изменения в глубоком БВ (обычно перивентрикулярные области) → повышение сигнала на Т2-ВИ
• Отношение переноса намагниченности (ОПН):
о ОПН позволяет дифференцировать ВИЧЭ от прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ):
- При ПМЛ наблюдается значительное ↓ ОПН в пораженных областях (по сравнению с таковыми при ВИЧЭ), вероятно обусловленное демиелинизацией
• Диффузионно-тензорная визуализация
о При ВИЧ-ассоциированных когнитивных нарушениях возможно ↓ фракционной анизотропии в раннем периоде заболевания
4. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о МРТ по сравнению с КТ более информативна в обнаружении патологии БВ
о МР-спектроскопия позволяет обнаружить изменения БВ даже на бессимптомной стадии заболевания
• Советы по протоколу исследования:
о КТ исследование должно быть проведено при:
- Впервые возникших судорожном синдроме, головных болях, депрессии или нарушении ориентации
о МРТ исследование должно быть проведено при:
- Обнаружении методом КТ фокального объемного образования
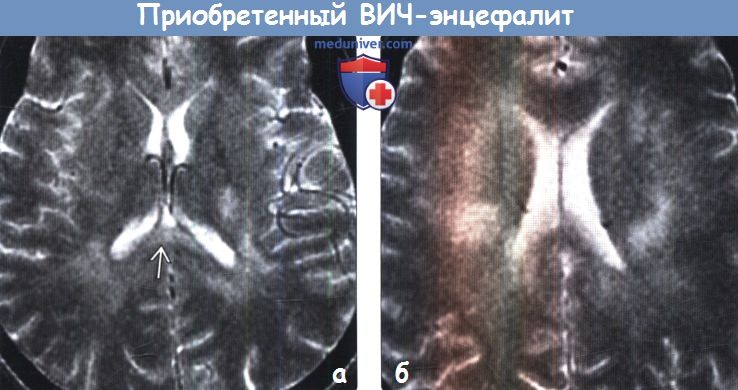
(а) Изменения белого вещества могут появляться в головном мозге пациентов с ВИЧ/СПИД до развития его атрофии и деменции, что и наблюдается у данного ВИЧ-положительного мужчины 34 лет с головными болями. Желудочки имеют нормальный внешний вид, визуализируются двусторонние облаковидные зоны повышения интенсивности сигнала от белого вещества, включая мозолистое тело.
(б) МРТ, Т2-ВИ, аксиальный срез: у этого же пациента неотчетливо определяется мультифокальное двустороннее асимметричное облаковидное повышение сигнала от белого вещества.
в) Дифференциальная диагностика приобретенного ВИЧ-энцефалита:
1. Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ):
• Мультифокальное поражения БВ
о Может быть односторонним, но гораздо чаще имеет двусторонний, асимметричный характер
о Наиболее часто локализуются в теменно-затылочных областях
о Поражение субкортикальных U-волокон (в отличие от ВИЧ-инфекции или ЦМВИ)
• Отсутствие накопления контрастного вещества; при наличии контрастирования предполагайте воспалительный синдром восстановления иммунитета (ВСВИ)
2. ЦМВ-ассоциированное поражение ЦНС:
• Энцефалит (диффузное повышение интенсивности сигнала от БВ на Т2-ВИ)
• Вентрикулит (контрастирование эпендимы)
3. Герпетический энцефалит:
• Вирус простого герпеса (ВПГ), вирус герпеса человека 6 типа (ВГЧ-6): на ранних стадиях зоны поражения локализуются в гиппокампе и медиальных отделах височных областей
4. Токсоплазмоз:
• Объемное образование(я) с кольцевым характером накопления контрастного вещества
• Гиперинтенсивные поражения на T2-ВИ/FLAIR, ДВИ
5. Первичная лимфома ЦНС:
• Одиночные/мультифокальные поражения, локализованы в глубоком > субкортикальном БВ
• Выраженная склонность к поражению базальных ганглиев, полушарий мозжечка, таламуса, ствола мозга, мозолистого тела и субэпендимальных отделов
• КТ с контрастированием: у ВИЧ-положительных пациентов обычно наблюдается краевой характер накопления контрастного вещества
• Положительные результаты ОФЭКТ-исследования с таллием-201
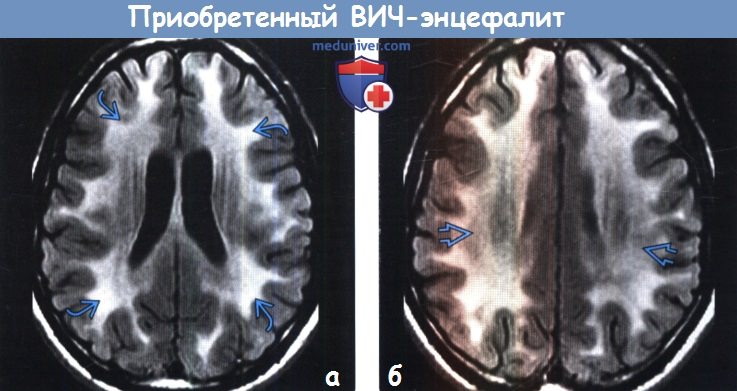
(а) МРТ, FAIR, аксиальный срез: у ВИЧ-позитивного мужчины 25 лет с когнитивными и поведенческими нарушениями определяются протяженные сливные относительно симметричные зоны повышения интенсивности сигнала от белого вещества в сочетании с легкой атрофией.
(б) МРТ, FAIR, аксиальный срез: у этого же пациента определяются схожие диффузные зоны повышения интенсивности сигнала от белого вещества. Данные изменения характерны для ВИЧ-энцефалита. Такие патологические изменения не оказывают масс-эффект на окружающие структуры и не накапливают контрастное вещество. При наличии любого из этих признаков необходимо предполагать иной диагноз.
г) Патология:
1. Общие характеристики приобретенного ВИЧ-энцефалита:
• Этиология:
о При первичной ВИЧ-инфекции вирус проникает в мозг через моноцитарную/макрофагальную систему
о ВИЧ способен вызывать неврологические заболевания, но он не реплицируется в нейронах и клетках глии
о Воспалительные (Т-клеточные) реакции с развитием васкулита, лептоменингита
• Генетика:
о Геномика ВИЧ → более нейровирулентные штаммы
о Деменция развивается лишь у пациентов, инфицированных штаммами ВИЧ, в которых произошли критические мутации
• Ассоциированные аномалии:
о ВИЧЭ может развиваться в сочетании с другими ВИЧ-ассоциированными аномалиями (например, другими инфекциями)
о Прогрессирующая энцефалопатия у детей часто сочетается с миелопатией
• Отличительный признак ВИЧЭ: микроглиальные узелки с гигантскими многоядерными клетками (ГМК)
• Реактивный глиоз, фокальный некроз и демиелинизация
• Умеренная потеря нейронов; минимальные воспалительные изменения
• Проникновение вируса в мозг происходит на самых ранних этапах после системной инфекции
2. Стадирование и классификация приобретенного ВИЧ-энцефалита:
• Три типа нейропатологоанатомических изменений:
о 1 тип: ВИЧ-энцефалит:
- Множественные диссеминированные очаги микроглии, макрофагов и ГМК; если ГМК не обнаружены, необходимо провести исследование на ВИЧ-антиген/нуклеиновые кислоты
о 2 тип: ВИЧ-лейкоэнцефалопатия:
- Диффузное и симметричное поражение БВ (потеря миелина, реактивный астроглиоз, макрофаги и ГМК); если ГМК не обнаружены, необходимо провести исследование на ВИЧ-ан-тиген/нуклеиновые кислоты
о 3 тип: ВИЧ-ассоциированные гигантские клетки:
- PAS(+) одно- или многоядерные макрофаги
• Легкая ВИЧЭ: тип 1 без МГК
• Умеренная ВИЧЭ: тип 1, 2 или 3
• Выраженная ВИЧЭ: атрофия головного мозга + тип 1 или 2
3. Макроскопические и хирургические особенности:
• Ранняя стадия: бледность окраски БВ
• Поздняя стадия: инфицирование неокортекса, атрофия
4. Микроскопия:
• ВИЧЭ:
о Инфицированные клетки: преимущественно макрофаги и микроглия; малая часть астроглии; редко олигодендроциты
о Вторичное повреждение нейронов
о Минимальные воспалительные изменения: периваскулярные макрофагальные инфильтраты и микроглиальные узелки
• Прогрессирующая энцефалопатия у ВИЧ-инфицированных детей:
о Воспалительные инфильтраты с ГМК
о Протяженная кальцифицирующая васкулопатия с преимущественным поражением мелких сосудов базальных ганглиев, а также БВ головного мозга и моста
о Атрофия, обусловленная нарушением созревания миелина или потерей миелина
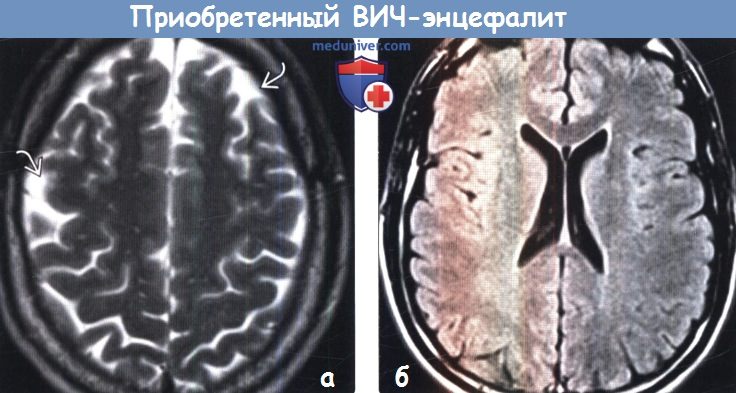
(а) МРТ, Т2-ВИ, аксиальный срез: у ВИЧ-положительного пациента с ранними признаками субкортикальной деменции определяется вариант картины ВИЧ-энцефалита. Атрофические изменения очевидны на уровне верхних отделов полушарий головного мозга, вокруг которых отмечается расширение ликворных пространств ВИЧ-энцефалит при диагностической визуализации наиболее часто проявляется в виде диффузных облако-видных зон поражения белого вещества головного мозга в сочетании с его атрофическими изменениями. Тем не менее, в некоторых случаях (в том числе и здесь) атрофия головного мозга может быть доминирующим признаком.
(б) MPT, FLAIR: у этого же пациента определяется легкая атрофия без значимого изменения белого вещества.
д) Клиническая картина:
1. Проявления приобретенного ВИЧ-энцефалита:
• Наиболее частые признаки/симптомы:
о Субкортикальная деменция с когнитивными, моторными и поведенческими нарушениями
• Клинический профиль:
о ВИЧ-ассоциированный когнитивный синдром: невыраженный или выраженный (деменция)
о Нарушения центральной моторной функции
о Поведенческие нарушения: псевдодеменция (депрессия), делирий и спутанность сознания
о В педиатрической практике: микроцефалия, когнитивные нарушения, слабость, пирамидные знаки, атаксия и судорожные признаки
2. Демография:
• Возраст:
о ВИЧ-положительные пациенты как взрослого, так и детского возраста
• Пол:
о Преобладание патологии у какого-либо пола не выявлено; половая структура распространения ВИЧЭ отражает таковую для ВИЧ инфекции
• Эпидемиология:
о У 33-67% ВИЧ-положительных взрослых и 40-50% ВИЧ- положительных детей развивается ВИЧЭ
о ВИЧЭ развивается до развития оппортунистических инфекций и опухолей; распространенность не связана со стадией заболевания
3. Течение и прогноз:
• Когнитивные нарушения возникают тогда, когда пациент становится иммунокомпрометированным
• Медленно прогрессирующее нарушение контроля мелкой моторики, вербальной беглости и кратковременной памяти
• Через несколько месяцев: выраженное ухудшение и субкортикальная деменция с развитием на поздних стадиях состояний, близких к вегетативному
4. Лечение:
• Высокоактивная антиретровирусная терапия (ВААРТ) не позволяет избежать развития ВИЧЭ, но позволяет ↓ ее выраженность:
о Эра ВААРТ: ↓ частоты встречаемости выраженной ВИЧЭ, но ↑ частоты встречаемости ВИЧЭ легкой-умеренной степени
Инфекции с осложнением в виде энцефалита у ребенка
а) Микоплазменный энцефалит. Микоплазма, хотя и не является вирусом, также нуждается в механизме репликации клетки-хозяина. Энцефалит микоплазменной этиологии иногда может иметь острое начало одновременно с респираторными симптомами или чаще в виде вторичного явления с атипичным иммунным ответом на инфекцию в ЦНС (Abramovitz с соавт., 1987). В одном из исследований были представлены плохие продолжительные неврологические последствия у пациентов с микоплазменным энцефалитом (Koskiniemi et al., 1991). Диагноз ставится при выделении ДНК из ликвора и/или серологическим методом определения продукции IgM, IgG и IgA к микоплазме в крови и/или СМЖ (Bencina et al., 2000).
Несмотря на то, что макролидные антибиотики эффективны против микоплазменного агента и должны использоваться при острой системной инфекции, в отдельных случаях трудно установить, является ли энцефалит первичным или иммунной реакцией. Однако проникновение макролидов в ЦНС недостаточно, и эффективность в преодолении гематоэнцефалического барьера не определена.
б) Респираторные вирусные инфекции:
1. Гриппозный энцефалит (грипп А и В). Несмотря на то, что у большинства новорожденных и детей, зараженных вирусом гриппа, развивается легкая респираторная инфекция, могут встречаться более тяжелые проявления болезни, включая неврологические симптомы (Wang et al., 2003; Maricich et al., 2004). Неврологическое поражение часто стойкое с серьезными последствиями или смертельным исходом, и включает острый энцефалит, синдром Рейе, острую некротическую энцефалопатию и миелит, а также аутоиммунные состояния типа синдрома Гийена-Барре. Вирусологическая диагностика основана на выделении вируса или определении антигенов в носоглоточном секрете, а так же на выявлении РНК в ликворе с помощью ПЦР или сероконверсией (Studahl, 2003).
Первоначально о повышенном уровне заболеваемости грипп-ассоциированным энцефалитом/энцефалопатией было заявлено у японских детей. В одном исследовании у 89 детей со средним возрастом 3,8 лет, ни один из которых не получал аспирин, заболевание отмечалось в течение восьми сезонов гриппа (1994-2002 гг.) (Togashi et al., 2004). После короткого респираторного продромального периода у большинства пациентов быстро развилось коматозное состояние с (или без) судорогами; 37% умерли, 19% имели неврологические последствия. В образцах плазмы и ликвора у двоих пациентов, которые умерли от молниеносного течения болезни, отмечалось значительное повышение уровня интерлейкина-6 (ИЛ-6) и фактора некроза опухоли-α (ФНО-α).
При посмертном исследовании одного летального случая выявлен вазогенный отек мозга с генерализованной васкулопатией, подтверждая повреждение эндотелия сосудов, вероятно, за счет высокой активности цитокинов. Другие исследования показали повышенный уровень системных и ликворных цитокинов при гриппозном энцефалите (ИЛ-6 и ФНО-а), так же как увеличение цитохрома С, свидетельствующего о вторичной смерти клеток путем апоптоза в результате гиперцитокинемии (Hosoya et al., 2005, Nunoi et al., 2005). Наиболее высокий уровень отмечен у пациентов с летальным исходом.
2. Энцефалит птичьего гриппа. На сегодняшний день птичий грипп A (H5N1) возникает у небольшой группы лиц, обычно там, где имеется контакт с больными птицами (de Jong et al., 2006). Как и при тяжелой респираторной инфекции, возможно сочетанное поражение многих органов с комой, в большинстве случаев с летальным исходом.
3. Аденовирусный энцефалит. Чаще встречается у детей, обычно проявляясь в виде легкой простудной или гастроинтестинальной болезни. К более тяжелым осложнениям относятся дыхательная недостаточность, энцефалопатия и хронические последствия, включая облитерирующий бронхиолит и продолжительное повреждение ЦНС (Chuang et al., 2003). Аденовирус может быть причиной асептического менингита, однако некоторые штаммы, такие как аденовирус 7 типа, часто вызывают менингоэнцефалит с более тяжелым течением. Другие неврологические синдромы, связанные с аденовирусом — миелит, подострый очаговый аденовирусный энцефалит и Рейе-подобный синдром (Straussberg et al., 2001).
У детей с ослабленным иммунитетом аденовирус может быть причиной полиорганной недостаточности с энцефалитом, печеночной коагулопатией и смертью. Диагноз выставляется на основе изоляции вируса или определения антигенов в носоглоточном секрете или стуле, так же как определение ДНК методом ПЦР в спинномозговой жидкости.
Редкие проявления энцефалопатии возникали при ротавирусных гастроэнтеритах, но, вероятно, это не связано с проникновением вирусов в ткани ЦНС (Nakagomi и Nakagomi, 2005). Энцефалитные проявления с припадками и расстройствами сознания могут быть осложнением других невирусных диарейных заболеваний, включая энтеритные инфекции Shigella (Mulligan et al., 1992) и C. jejuni (Nasralla et al., 1993).
г) Постинфекционные энцефалиты. Постинфекционные энцефалиты, вероятно, самый распространенный тип острых энцефалитов в европейских странах. Поскольку ни в одном из этих случаев не обнаруживают вирус, они скорей всего не являются результатом прямого вирусного вторжения в ЦНС, а вероятно возникают благодаря ответу иммунной системы на инфекционный агент в тканях хозяина посредством механизмов, обсуждаемых в отдельной статье на сайте при остром диссеминированном энцефаломиелите (ADEM).
Большинство случаев постинфекционного энцефалита являются осложнением заболеваний, сопровождающихся экзантематозной сыпью. Однако многие случаи возникают вследствие недиагностированных инфекционных заболеваний. Частота постинфекционных энцефалитов оценивается приблизительно, так как во многих случаях не доступны данные патогенеза и механизма острой энцефалитной картины. Так, при свинке менингит возникает очень часто, но доказательства перивенозного энцефалита представлены лишь в некоторых случаях (Johnson, 1982а). В ряде случаев болезнь, предшествующая началу энцефалита, не диагностируется и не идентифицируется ни один вирус, даже ретроспективно. Диагноз вирусной инфекции основывается на клинических проявлениях и течении продромального периода.
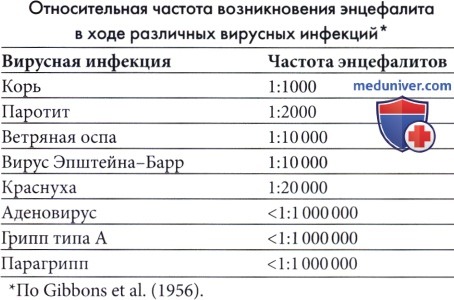
Корь — наиболее частая причина экзантематозной сыпи; таким образом, заболеваемость энцефалитом будет зависеть от заболеваемости корью и уровня иммунизации против кори среди населения. Острый коревой энцефалит начинается через 6-8 дней после первых высыпаний и встречается в 1 из 1000 случаев (Johnson et al, 1984). Несмотря на вариабельность интенсивности, заболевание часто протекает тяжело, со смертельными исходами в 10% случаев и частыми осложнениями, включая припадки, двигательные нарушения и умственную отсталость. Трудности в обучении и поведенческие расстройства характерны для детей с очевидным полным выздоровлением. Описаны редкие случаи постинфекционного энцефалита вследствие вакцинации против кори, но их частота значительно меньше, чем энцефалиты, связанные с диким вирусом кори (Landrigan и Witte, 1973). Постинфекционный энцефалит, ассоциированный с пятой болезнью (парвовирус В19) и внезапной сыпью (HHV-6 и 7) встречается очень редко.
В странах с вакцинацией против кори, свинки и краснухи, rubella (коревая краснуха) в настоящее время является редким заболеванием и случаи острого краснушного энцефаломиелита, следовательно, крайне редки. Постинфекционный краснушный энцефалит — тяжелое заболевание со смертностью примерно в 20% случаев, возникающее в 1 из 5000 острых случаев краснухи. Может развиваться одновременно с сыпью или даже через неделю или позже.
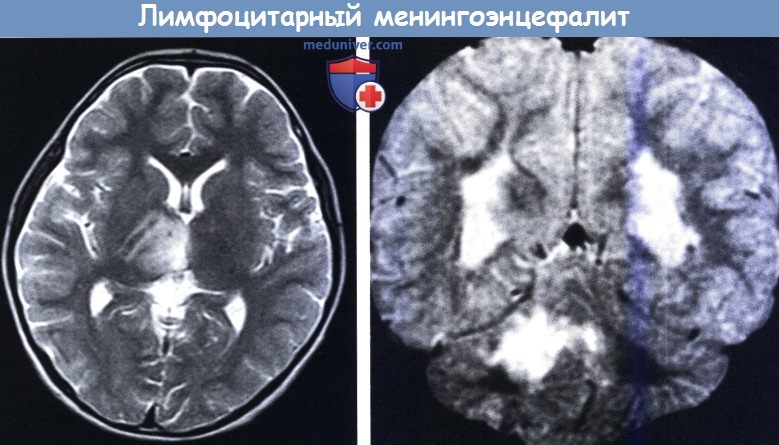
MPT (слева): патологический сигнал от правого таламуса и среднего мозга, вызванный параинфекционным лимфоцитарным менингоэнцефалитом.
12-последовательность (справа): более обширная зона интенсивного сигнала от правого полушария мозжечка и двусторонний интенсивный сигнал от супратенториального белого вещества полушарий (четырехлетняя девочка с мозжечковой атаксией с внезапным началом,
продолжающейся несколько недель, с легким ступором, который исчез через несколько дней).
1. Патология. Патогенез постинфекционного энцефалита имеет отличительные черты. Представлен множественными очагами перивенозной демиелинизации. Осевые цилиндры обычно лучше сохраняются, чем миелин. Определяются лейкоцитарные муфты вокруг вен и венул из мононуклеарных клеток, в демиелинизированных участках видны клетки микроглии и макрофаги.
2. Клинические проявления. Клинические проявления те же, что и при уже описанных типах энцефаломиелита. В большинстве случаев имеется внезапное начало с расстройствами сознания и припадками. Эти симптомы появляются в среднем через шесть дней (до 21 дня) после появления инфекции верхних дыхательных путей или экзантемы, в большинстве случаев у детей в возрасте старше двух лет. Могут быть представлены различные неврологические проявления, включая гемипарез, экстрапирамидные симптомы, атаксию, лицевые параличи, нистагм и поражение черепных нервов (Kennard и Swash, 1981; Marks et al, 1988). Результаты нейровизуализации могут быть отрицательными, а при МРТ обычно выявляются участки повышения сигнала преимущественно в белом веществе полушарий и иногда с вовлечением мозжечка. Характерны вовлечение зрительного бугра и базальных ганглиев. Течение заболевания варьирует от случая к случаю и зависит от причинных факторов. Уровень смертности низкий. Три четверти случаев протекают быстро, с выздоровлением в течение двух недель.
Другим вариантом постинфекционного энцефалита является острый геморрагический лейкоэнцефалит. Это фульминантное заболевание, которое характеризуется быстрой прогрессией очаговых неврологических симптомов и признаков, особенно гемиплегии, сопровождающейся беспокойством, комой и лихорадкой. Ликвор при этом ксантохромный в 20% случаев и показывает полиморфноядерный плеоцитоз. В периферической крови часто представлен выраженный лейкоцитоз. Возможно бифазное течение. Демиелинизирующие повреждения имеют геморрагический характер из-за некротизирующего ангиита венул и капилляров. В постановке диагноза может помочь КТ и МРТ, указывая на наличие больших гиподенсных участках иногда с геморрагическим компонентом (Watson et al., 1984, Huang et al., 1988). При некоторых случаях острого геморрагического лейкоэнцефалита удавалось выделить ДНК и РНК герпесвирусов, но до сих пор неясно, вовлекаются ли эти вирусы в патологический процесс (An et al., 2002).
Лечение постинфекционного энцефалита в основном такое же, как при всех острых энцефалитных заболеваниях. Значение стероидной терапии остается неясным, несмотря на весьма впечатляющее немедленное действие в отдельных случаях (Pasternak et al, 1980). В некоторых случаях применяли внутривенное введение иммуноглобулинов (Kleiman и Brunquell, 1995).
д) Энцефалит ствола мозга и мозжечка. При рентгенографии в случаях острого диссеминированного энцефалита может выявляться вовлечение ствола мозга. Ограниченное вовлечение ствола мозга не характерно и может встречаться при первичных энцефалитах (Kaplan и Koveleski, 1978; North et al., 1993; Duarte et al., 1994) и реже, при постинфекционных типах.
Среди клинических проявлений выделяют лихорадку, системные симптомы и асептический менингит вместе с симптомами и признаками дисфункции ствола головного мозга. Заметно поражение глазодвигательных нервов и нижней лицевой пары, что может сопровождаться заторможенностью и признаками вовлечения длинных нервных путей, что приводит к пирамидальным и мозжечковым проявлениям. Участие черепных нервов и атаксия могут имитировать синдром Миллера-Фишера, который некоторыми авторами рассматривается в качестве формы энцефалита ствола мозга. МРТ может продемонстрировать повышенный сигнал в ножках мозга, в мосте, мозжечке и продолговатом мозге (Ormerod et al., 1986, Hosoda et al., 1987) и энцефалит следует отличать от опухоли ствола мозга, абсцесса или других нейрохирургических проблем. Всегда следует помнить о возможности ромбэнцефалита, вызванного L. monocytogenes, при эффективности антибиотикотерапии (Frith et al., 1987).
е) Острый очаговый энцефалит. Острый очаговый энцефалит, поражающий ограниченный участок при инфекции коксаки-вирусом А9 (Roden et al., 1975) и ЕСНО-вирусом 25 (Peters et al., 1979), может привести к острой гемиплегии или гемихорее. Лакунарные повреждения в центральном сером веществе или внутренней капсуле могут быть результатом сосудистых инфарктов или очаговых церебритов.
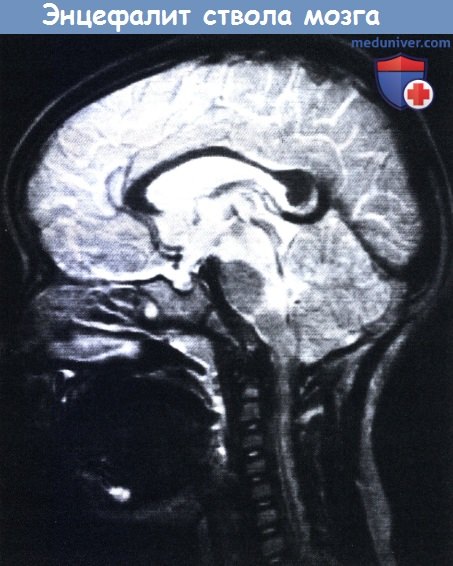
Энцефалит ствола мозга у четырехлетней девочки с клиникой ступора и множественными параличами черепных нервов.
При МРТ выявлено усиление сигнала от ножек мозга и дорсальной части моста.
При повторной МРТ через два месяца патологических изменений не обнаружено.
Неврологические проявления ВИЧ-инфекции (нейроСПИД) — обобщенное клиническое понятие, включающее многообразные первичные и вторичные синдромы и заболевания нервной системы, обусловленные ВИЧ. Проявлениями нейроСПИДа могут выступать менингоэнцефалит, полиневропатия, энцефало- и миелопатия, оппортунистические нейроинфекции, опухоли ЦНС, церебральные сосудистые нарушения и т. п. Диагностируется нейроСПИД при сопоставлении результатов анализов на ВИЧ, данных неврологического осмотра, нейропсихологического тестирования, ликворологических и томографических исследований, ЭФИ нервно-мышечного аппарата. Лечение нейроСПИДа осуществляется в рамках терапии ВИЧ-инфекции с назначением специфической и симптоматической терапии имеющихся неврологических проявлений.
Общие сведения

Причины возникновения нейроСПИДа
Несмотря на общепризнанность нейротропности ВИЧ, конкретные патогенетические механизмы его воздействия на нервную систему (НС) до конца не ясны. Предполагается, что нейроСПИД обусловлен как прямым, так опосредованным воздействием вируса на НС. Прямое влияние связывают с тропностью ВИЧ к CD4-рецепторам, которые имеются не только в мембране лимфоцитов, но и в глиальных клетках мозговой ткани.
Опосредованное воздействие ВИЧ реализуется несколькими путями. Во-первых, это развитие оппортунистических инфекций и опухолевых процессов за счет резкого снижения иммунного статуса организма. Во-вторых, предполагают наличие аутоиммунных механизмов (например, в развитии асептического менингита и полиневропатии при нейроСПИДе), связанных с синтезом антител к нервным клеткам, имеющим встроенный ВИЧ-антиген. Существует также гипотеза о нейротоксическом действии продуцируемых ВИЧ химических веществ. Кроме того, развитие нейроСПИДа возможно вследствие повреждения эндотелия мозговых сосудов провоспалительными цитокинами, приводящего к расстройству микроциркуляции и гипоксии, обуславливающей гибель нейронов.
Следует отметить, что отсутствие полной ясности в этиопатогенезе ВИЧ-инфекции и нейроСПИДа в частности, наличие существенного количества ложноположительных реакций на ВИЧ при его лабораторной диагностике, а также сложности с выделением вируса привели к появлению среди медиков и специалистов в области иммунологии лиц, считающих неправомочным само понятие ВИЧ-инфекция. При этом сторонники ВИЧ-отрицания признают существование синдрома иммунодефицита как такового, но опасаются, что с введением понятий ВИЧ-инфекция и нейроСПИД под эти диагнозы массово попадают пациенты с различными другими заболеваниями.
Классификация нейроСПИДа
В соответствии с прямым или опосредованным воздействием ВИЧ на нервную систему принято различать первичный и вторичный нейроСПИД. К базовым клиническим формам, которые включает первичный нейроСПИД, относят: острый асептический менингит, ВИЧ-энцефалопатию (СПИД-деменцию), ВИЧ-миелопатию (вакуолярную миелопатию), васкулярный нейроСПИД, поражения периферической НС (дистальная симметричная невропатия, синдром Гийена-Барре, множественная мононевропатия, хроническая воспалительная демиелинизирующая полинейропатия, синдром конского хвоста), поражение мышц (миопатии).
Вторичный нейроСПИД включает оппортунистические нейроинфекции и опухоли. Первые отличаются большим многообразием: церебральный токсоплазмоз, криптококковый менингит, герпесвирусная нейроинфекция (опоясывающий герпес, цитомегаловирусный и герпесвирусный энцефалиты, цитомегаловирусная полирадикулопатия, герпесвирусный миелит и ганглионевриты), прогрессирующая мультифокальная лейкоэнцефалопатия, туберкулезные поражения НС, нейросифилис. Наиболее часто встречающимися опухолями центральной НС при нейроСПИДе являются: первичная лимфома головного мозга, лимфома Беркитта, глионейробластома, диссеминированная саркома Капоши.
Симптомы нейроСПИДа
Первичный нейроСПИД зачастую имеет бессимптомное субклиническое течение. В 10-20% случаев неврологические симптомы дебютируют в первые 2-6 недель от заражения ВИЧ (период сероконверсии). В этот период на фоне фебрилитета, лимфаденопатии и кожных высыпаний у части пациентов манифестируют признаки асептического менингита и острой радикулоневропатии. Другие клинические формы первичного нейроСПИДа (ВИЧ-энцефалопатия, ВИЧ-миелопатия) возникают преимущественно в развернутой стадии ВИЧ-инфекции на фоне системных проявлений и выраженной иммуносупрессии. Вторичный нейроСПИД развивается в фазе симптомной хронической ВИЧ-инфекции (стадия вторичных заболеваний), которая наступает в период от 2 до 15 лет с момента первых клинических проявлений. Отдельные неврологические симптомы (головная боль, полиневропатия, нарушения сна, астения, депрессия, миопатия) могут быть вызваны токсичной антиретровирусной терапией.
Острая радикулоневропатия связана с острой воспалительной демиелинизацией корешков спинномозговых и черепных нервов. Характерны вялый тетрапарез, полиневритический тип нарушений чувствительности, корешковый синдром, поражение лицевого (реже глазодвигательного) нервов, бульбарные расстройства. Фаза нарастания симптомов может длиться от нескольких дней до месяца, затем после 2-4 недель стабильного состояния начинается регресс симптоматики. У 70% пациентов с этой формой нейроСПИДа отмечается полное восстановление, у 15% - выраженные остаточные парезы.
ВИЧ-энцефалопатия является самым частым проявлением первичного нейроСПИДа. Включает когнитивные, поведенческие и двигательные расстройства. Последние бывают представлены мозжечковой атаксией, тремором, пирамидной недостаточностью, вторичным паркинсонизмом, гиперкинезами. Отдельные симптомы и умеренный когнитивный дефицит отмечаются примерно у 75% пациентов со СПИДом. У 3-5% больных энцефалопатия выступает начальным синдромом нейроСПИДа. Морфологическим субстратом является мультифокальный гигантоклеточный энцефалит с поражением преимущественно лобных и височных долей, подкорковых структур, моста и мозжечка.
ВИЧ-миелопатия проявляется нижним спастическим парапарезом и тазовыми расстройствами. Отличается медленным течением и вариативностью тяжести клинических симптомов от легкого пареза до грубой плегии с недержанием мочи и кала. Это проявление нейроСПИДа отмечается у 20% пациентов с ВИЧ. Морфологически выявляется вакуолизация белого спинномозгового вещества, наиболее выраженная в грудных сегментах. Однако на МРТ позвоночника изменения зачастую не фиксируются.
Васкулярный нейроСПИД обусловлен васкулитом церебральных сосудов и зачастую приводит к развитию ишемического инсульта, отличительной чертой которого является волнообразное течение и частая трансформация в геморрагический инсульт. Характерны предшествующие инсульту ТИА, а также повторные инсульты, вследствие мультифокального поражения сосудов.
Диагностика нейроСПИДа
Учитывая частую встречаемость нейроСПИДа, консультация невролога рекомендована всем больным ВИЧ-инфекцией. В связи с тем, что первыми симптомами ВИЧ-энцефалопатии зачастую выступают когнитивные нарушения, исследование неврологического статуса целесообразно дополнять нейропсихологическим обследованием. Среди практических неврологов должна существовать определенная настороженность в отношении впервые обратившихся пациентов из групп риска, поскольку неврологические проявления у них могут являться симптомами первичного нейроСПИДа. В таких случаях следует обращать внимание на наличие у больного признаков иммуносупрессии и системных симптомов (снижения массы тела, лимфаденопатии, выпадения волос и т. п.).
Наряду с обязательными в диагностике ВИЧ-инфекции исследованиями крови путем ИФА, иммуноблоттинга и определения вирусной нагрузки при помощи ПЦР, в диагностике нейроСПИДа широко используются электрофизиологические, томографические и ликворологические методы. При необходимости проводятся консультации психиатра, нейрохирурга и др. специалистов. Диагностика и анализ результатов лечения поражений периферической НС при нейроСПИДе осуществляются преимущественно с помощью ЭФИ нервно-мышечной системы (ЭМГ, ЭНМГ, исследование ВП).
С целью диагностики поражений центральной НС при нейроСПИДе, для анализа их течения и эффективности проводимой терапии широко используются методы компьютерной томографии и магнитно-резонансной томографии. КТ головного мозга особенно информативна в диагностике вторичных объемных процессов церебральной локализации. МРТ головного мозга более эффективно визуализирует диффузные и мелкоочаговые изменения (участки атрофии и демиелинизации), расположенные в глубинных отделах мозга патологические очаги. Однако результаты аутопсии показывают, что современные методы нейровизуализации способны отображать не все морфологические изменения, происходящие в мозговой ткани при нейроСПИДе.
Немаловажное значение в диагностике нейроСПИДа имеет исследование цереброспинальной жидкости, полученной при люмбальной пункции. У серопозитивных пациентов даже при отсутствии неврологической симптоматики в ликворе зачастую наблюдается умеренный лимфоцитоз, повышение уровня белка и снижение концентрации глюкозы. При наличии неврологических проявлении эти изменения, наряду со снижением уровня CD4-лимфоцитов, говорят о возможном развитии нейроСПИДа. Иммунологические исследования ликвора, как правило, выявляют повышенное содержание IgG.
Лечение нейроСПИДа
Основу терапии и профилактики развития нейроСПИДа составляет лечение ВИЧ-инфекции. Эффективная антиретровирусная терапия (АРТ) фармпрепаратами, способными проходить через ГЭБ, позволяет блокировать репликацию ВИЧ, остановить нарастание иммунодефицита и таким образом уменьшить тяжесть клинических проявлений нейроСПИДа, снизить риск возникновения оппортунистических нейроинфекций и повысить эффективность их терапии. К наиболее апробированным средствам, применяемым при нейроСПИДе, относятся зидовудин, ставудин, абакавир. Учитывая токсичность большинства антиретровирусных препаратов, АРТ назначается по индивидуально подобранной схеме только при наличии показаний и с согласия пациента.
Параллельно с АРТ осуществляется специфическая и симптоматическая терапия возникшей клинической формы нейроСПИДа. Так, при ВИЧ-энцефалопатии применяют холина альфосцерат и мягкие ноотропы (мебикар, цитиколин, пирацетам, фенибут), при инсульте — антикоагулянты и пентоксифиллин, при полиневропатии — цитиколин, комбинированные препараты витаминов группы В, при острых психических нарушениях — антипсихотические средства (клозапин). При поражениях периферической НС отмечена эффективность плазмафереза. В лечении миопатий используют плазмаферез и кортикостероидную терапию.
При оппортунистических нейроинфекциях применяют этиотропные препараты: при криптококовых менингитах — фторцитозин с амфотерицином, токсоплазменных энцефалитах — кларитромицин, азитромицин, спирамицин, при герпетических поражениях — ацикловир, валацикловир, ганцикловир, абакавир, саквинавир. Лечение опухолей, возникающих как проявление вторичного нейроСПИДа, может потребовать хирургического вмешательства. Вопрос о необходимости операции рассматривается совместно с нейрохирургом.
ВИЧ-инфекция у детей – это патологическое состояние, вызванное вирусом иммунодефицита человека (ВИЧ) и характеризующееся прогрессирующим снижением иммунитета ребенка. Специфических клинических симптомов нет, основные проявления – лихорадка, диарея неясной этиологии, лимфаденопатия, частые инфекционные и бактериальные заболевания, СПИД-ассоциированные и оппортунистические патологии. Основные методы лабораторной диагностики ВИЧ-инфекции у детей – ИФА, иммуноблоттинг, ПЦР. Специфическое лечение включает в себя схемы антиретровирусных препаратов (ингибиторов обратной транскриптазы и протеазы).

Общие сведения
ВИЧ-инфекция у детей – это заболевание, которое развивается в результате длительной персистенции вируса иммунодефицита человека в лимфоцитах и клетках нервной системы и характеризуется медленно прогрессирующей дисфункцией иммунной системы. Впервые данный вирус был описан французским вирусологом профессором Люком Монтанье в 1983 году. ВИЧ – это РНК-содержащий ретровирус, имеющий сложное строение и высокую изменчивость, что обеспечивает его выраженную способность к репликации и стойкости в организме человека. Распространенность ВИЧ-инфекции у детей за последние 15 лет уменьшилась более чем на 50%. Ежегодно в мире фиксируется порядка 250 тысяч случаев, из них в России около 6,5-7,5 тысяч. Правильное проведение профилактики вертикальной трансмиссии вируса позволило снизить частоту инфицирования с 30% до 1-3% беременностей ВИЧ-позитивных матерей.

Причины ВИЧ-инфекции у детей
ВИЧ-инфекция у детей имеет несколько механизмов передачи. Вирус может быть получен ребенком гематогенным путем от матери во время беременности. Также инфицирование может произойти во время использования необработанного медицинского инструментария, гемотрансфузий, трансплантации органов, у старших детей – при незащищенном половом акте. Все эти пути реализуются за счет содержания вируса в биологических жидкостях (кровь, спинномозговая жидкость, сперма, влагалищные выделения), тканях и органах инфицированного человека.
Основная причина (примерно 80%) ВИЧ-инфекции у детей – вертикальная передача вируса от матери к ребенку. Выделяют 3 периода, в которых потенциально возможно заражение – перинатальный (через систему плацентарного кровообращения), интранатальный (при контакте кожных покровов ребенка с кровью и секретом влагалища матери) и постнатальный (через грудное молоко). Риск инфицирования указанными путями составляет 20%, 60% и 20% соответственно. К факторам, повышающим риск передачи, относятся отсутствие профилактического лечения матери во время вынашивания ребенка, многоплодная беременность, преждевременные роды и роды через естественные половые пути, маточные кровотечения и аспирация крови ребенком, прием наркотических веществ и алкоголя во время беременности, вскармливание грудным молоком, экстрагенитальная патология и коинфекция.
Патогенез ВИЧ-инфекции у детей основан на связывании вируса с CD4+ Т-лимфоцитами, в которых он модифицирует ДНК клетки. В результате этого начинается синтез новых вирусных частичек, а затем – вирионов. После полной репродукции вируса происходит гибель Т-лимфоцитов, однако инфицированные клетки остаются в системном кровотоке, служа резервуаром. Как результат отсутствия функционально полноценных иммунокомпетентных клеток развивается иммунодефицит. Характерной особенностью ВИЧ-инфекции у детей является сопутствующий дефицит В-лимфоцитов и тропность вируса к тканям ЦНС. Проходя сквозь гематоэнцефалический барьер, вирус вызывает аномалию расположения глиальных клеток, задержку развития головного мозга, дистрофию и атрофию нервной ткани и определенных нервов (чаще всего – зрительного). В педиатрии поражение ЦНС является одним из первых маркеров наличия ВИЧ.
Симптомы ВИЧ-инфекции у детей
Клиническая картина ВИЧ-инфекции у детей может существенно отличаться в зависимости от периода и способа передачи вируса. При инфицировании парентеральным или половым путем присутствует острый ретровирусный синдром, после чего заболевание протекает в 4 стадии: два латентных этапа и два периода развернутых клинических симптомов. При вертикальном пути заражения острый ретровирусный синдром и бессимптомная стадия не выявляются. Острый ретровирусный синдром наблюдается у 30-35% детей после окончания инкубационного периода (от 2 недель до 3 месяцев с момента инфицирования). Клинически ВИЧ-инфекция у детей на этом этапе может проявляться фарингитом, лимфоаденопатией, гепатоспленомегалией, субфебрилитетом, уртикарной или папулезной сыпью, редко – менингеальными симптомами. Ее длительность колеблется от 2 суток до 2 месяцев, в среднем составляет 21 день.
Следующая стадия – бессимптомного носительства и персистирующей лимфаденопатии. Возможное проявление ВИЧ-инфекции у детей на этой стадии – увеличение двух групп лимфоузлов. Ее длительность – от 2 до 10 лет. Вторая стадия характеризуется потерей массы тела (порядка 10%), поражением кожных покровов и слизистых оболочек (дерматиты, микозы придатков кожи, рецидивные заболевания слизистых ротовой полости и губ), рецидивирующим опоясывающим герпесом. Общее состояние, как правило, не нарушается. Третья стадия включает в себя выраженные проявления иммунодефицита: общее недомогание, диарею невыясненной этиологии, анорексию, лихорадку, головную боль, потливость по ночам, спленомегалию. ВИЧ-инфекция у детей на данном этапе сопровождается неврологическими нарушениями, отмечаются периферическая невропатия, ухудшение памяти. Также она характеризуется рецидивирующим кандидозом полости рта, простым и опоясывающим герпесом, ЦМВ-паротитом. При четвертой стадии (стадия СПИДа) на первый план выходят клинические проявления тяжелых оппортунистических заболеваний и опухолей.
У младенцев и детей в возрасте до 3 лет типичной особенностью является высокая частота тяжелых бактериальных инфекций. Практически в 50% случаев ВИЧ-инфекции у детей возникают гнойные отиты, менингиты, поражения кожи, бактериальные пневмонии со склонностью к абсцедированию и появлению плеврального выпота, бактериальный сепсис, поражения суставов и костей. Как правило, в роли возбудителей выступают S. pneumoniae, S. aureus, H. influenzae, E. coli и некоторые виды сальмонелл.
Диагностика ВИЧ-инфекции у детей
Диагностика ВИЧ-инфекции у детей основывается на данных анамнеза и лабораторных тестах. Объективный осмотр и инструментальные методы исследования информативны только в случае развития бактериальных инфекций или СПИД-ассоциированных заболеваний. Подозрение на ВИЧ-инфекцию у детей возникает при выявлении педиатром хотя бы четырех из следующих симптомов: отягощенный эпидемиологический анамнез, генерализованная гиперплазия лимфоузлов, потеря массы тела (свыше 10% от исходной), необоснованная диарея (более 1 месяца), стойкая или перемежающаяся гипертермия (более 1 месяца), частые бактериальные, вирусные, грибковые или паразитарные заболевания, СПИД-ассоциированные и оппортунистические патологии и т. д.
Ведущее место в диагностике ВИЧ-инфекции у детей занимают лабораторные тесты. Среди неспецифических изменений в общем и биохимическом анализах крови могут присутствовать анемия, лейкопения, тромбоцитоз или тромбоцитопения, повышение уровня АлТ и/или АсТ. При иммунологических исследованиях у таких детей можно выявить повышение уровня иммуноглобулинов, падение уровня CD4 и соотношения CD4/CD8, уменьшение продукции цитокинов, повышение уровня циркулирующих иммунокомплексов, у новорожденных возможна гипо-γ-глобулинемия. Специфическая диагностика ВИЧ-инфекции у детей подразумевает проведение ИФА с определением антител к вирусу. При его позитивном результате осуществляется иммуноблоттинг с идентификацией иммуноглобулинов к некоторым белкам вируса (gp 41, gp 120, gp 160). В последнее время широко используются тесты для определения вирусной нагрузки (количества копий вирусной РНК).
Лечение ВИЧ-инфекции у детей
Лечение ВИЧ-инфекции у детей заключается в проведении специфической антиретровирусной терапии, профилактике или лечении оппортунистических заболеваний и устранении симптомов патологии. В современной медицинской практике используются противовирусные препараты, ингибирующие обратную транскриптазу (нуклеозидные и ненуклеозидные аналоги) и протеазу. Наиболее эффективной считается схема, состоящая их трех препаратов – два нуклеозидных аналога и один ингибитор протеазы. Выбор конкретных медикаментов, схема их употребления подбираются индивидуально для каждого ребенка. В зависимости от имеющихся оппортунистических заболеваний используются специфические этиотропные (антибиотики, противотуберкулезные, противовирусные, противогрибковые препараты и пр.) и симптоматические (жаропонижающие, антигистаминные, пробиотики, витаминные комплексы, дезинтоксикационная терапия) средства.
Прогноз и профилактика ВИЧ-инфекции у детей
Прогноз при ВИЧ-инфекции у детей серьезный. Как правило, правильно подобранная антиретровирусная терапия позволяет добиться замедления репликации вируса на долгие годы, однако на данный момент ВИЧ остается неизлечимым заболеванием. На фоне проводимого лечения удается достичь высокого качества и удовлетворительной продолжительности жизни и полной адаптации ребенка в социуме.
Профилактика ВИЧ-инфекции у детей включает в себя исключение всех возможных путей передачи вируса: контроль переливаемой крови и трансплантируемых органов, медицинского инструментария, избежание незащищенных половых актов. Отдельное место занимает профилактика вертикальной трансмиссии. Согласно рекомендациям UNICEF, она включает в себя помещение беременной ВИЧ-позитивной женщины на учет у гинеколога, прием противовирусных средств с 24-28 недели, рациональный выбор способа родоразрешения, исключение грудного вскармливания, назначение противовирусных средств ребенку с момента рождения. Данные меры позволяют снизить риск развития ВИЧ-инфекции у детей до 1-3%.
Читайте также:

