Вич и вилочковая железа
Обновлено: 24.04.2024
Американские ученые выяснили механизм, позволяющий иммунной системе некоторых пациентов подавлять размножение вируса иммунодефицита на протяжении практически неограниченного времени. По данным исследователей, подобная неуязвимость для ВИЧ-инфекции связана с особенностями созревания T-лимфоцитов в вилочковой железе.
Американские ученые выяснили механизм, позволяющий иммунной системе некоторых пациентов подавлять размножение вируса иммунодефицита на протяжении практически неограниченного времени. По данным исследователей, подобная неуязвимость для ВИЧ-инфекции связана с особенностями созревания T-лимфоцитов в вилочковой железе.
У большинства людей заражение ВИЧ при отсутствии лечения неизбежно приводит к разрушению иммунной системы и развитию синдрома приобретенного иммунодефицита (СПИДа). Однако иммунная система очень небольшой группы больных способна самостоятельно бороться с вирусом. СПИД у этих людей не развивается на протяжении многих лет и даже десятилетий после заражения. Предыдущие исследования показали, что большинство таких пациентов обладают особым вариантом гена из группы человеческих лейкоцитарных антигенов HLA B57. Наличие этого гена также связано с повышенным риском развития аутоиммунных заболеваний.
Учитывая эти данные, сотрудники Массачусетского технологического института построили компьютерную модель, описывающую особенности созревания T-лимфоцитов у носителей гена HLA B57, а также влияние этих особенностей на способность иммунной системы выявлять и уничтожать клетки, пораженные вирусом иммунодефицита. Достоверность результатов такого моделирования была подвержена исследованием с участием 1900 ВИЧ-инфицированных, 1000 из которых обладали устойчивостью к развитию СПИДа.
В процессе созревания T-лимфоцитов в вилочковой железе эти клетки подвергаются воздействию различных антигенов, образующих комплекс с протеинами, кодируемыми генами HLA. Клетки, слишком активно реагирующие на эти антигены, получают сигнал к самоуничтожению. Таким образом происходит отсев Т-лимфоцитов, которые способны атаковать собственные ткани организма.
По данным американских ученых, наличие варианта гена HLA B57 приводит к тому, что созревающим в вилочковой железе лимфоцитам предлагается меньшее число "контрольных" антигенов. В результате в организм поступают более "агрессивные" T-лимфоциты, способные взаимодействовать с большим числом антигенов. Эта особенность позволяет иммунной системе носителей гена HLA B57 быстро опознавать мутировавшие формы ВИЧ, которые остаются незаметными для иммунной системы других людей. По данным исследователей, аналогичным защитным эффектом при ВИЧ-инфекции обладает еще один вариант человеческого лейкоцитарного антигена – HLA B27.
По словам одного из соавторов исследования Брюса Уолкера, выводы ученых, возможно, окажутся полезными при разработке новых методов лечения ВИЧ-инфекции. В частности, возможно создание вакцин, искусственно увеличивающих число агрессивных Т-лимфоцитов у зараженных ВИЧ пациентов.
Инфекционные болезни:
Популярные разделы сайта:
Влияние ВИЧ на тимус
ВИЧ может инфицировать и повреждать клетки-предшественники в тимусе, в результате чего в нем происходит уменьшение пролиферации клеток.
Тимоциты сначала обычно характеризуются как CD4+/CD8+ и несут оба типа хемокиновых рецепторов для ВИЧ, хотя и слабо экспрессируемых; количество CCR5 на них ниже по сравнению с CD4+-Т-клетками периферической крови.
Внутритимусные CD4+-предшественники Т-клеток, из которых затем дифференцируются дважды позитивные тимоциты (CD4+/CD8+), наиболее чувствительны к ВИЧ-инфицированию Х4-вирусами, поскольку такие клетки экспрессируют CXCR4, но не экспрессируют CCR5. Дендритные клетки тимуса также могут продуцировать большие количества ВИЧ, особенно R5-вирусов.
Инфицирование предшественников Т-клеток и тимоцитов может приводить к нарушению образования и высвобождения новых Т-лимфоцитов, в особенности неиммунных клеток, которые затем заселяют периферические лимфоидные органы и ткани организма. Эти клетки обеспечивают реакции иммунной системы на новые антигены.
Исследования на мышиной модели SCID/hu Thy/Liv подтвердили предположение о том, что ВИЧ-инфекция вызывает снижение количества гемопоэтических клеток-предшественников, а также тимоцитов. Токсические эффекты в тимусе при ВИЧ-инфекции, по-видимому, вызываются преимущественно попутно возникающими клеточными факторами, а не собственно вирусом, проникшим в клетки тимуса.
Тимус взрослого человека может продуцировать новые Т-лимфоциты для пополнения их периферического пула. Таким образом, как отмечали выше, уменьшение количества Т-клеток может быть связано с повреждением тимуса.
Ранее считали, что вилочковая железа у взрослых людей находится в неактивном состоянии и поэтому не может принимать участие в восстановлении Т-клеток после лечения ВИЧ-инфекции. Результаты некоторых исследований позволили в настоящее время изменить эту точку зрения.
В одной из первых работ было показано, что в ткани тимуса, особенно у молодых людей, количество CD4+-клеток составляет около 300-500 клеток/мкл. У пожилых инфицированных людей без клинических признаков заболевания железа увеличивается в размере на фоне положительной реакции на антиретровирусное лечение.
Продуцирование лимфоцитов тимусом определяется по количеству новых клеток, вышедших из тимуса, которые несут эписомные кольца ДНК, образовавшиеся в результате перестройки генов TCR. Такие кольцевые ДНК, выщепленные из хромосомной ДНК генов вариабельных участков TCR, (TREC - TCR rearranged excision circles), не дуплицируются при делении тимоцитов и, соответственно, их количество в клетке уменьшается с каждым последующим циклом пролиферации.
Таким образом, TREC являются индикаторами клеток, недавно вышедших из тимуса. У кур время полувыведения TREC составляет около 2 недель; однако время полувыведения TREC у человека до сих пор неизвестно. В активной вилочковой железе, в которой идет лимфопоэз Т-лимфоцитов, обнаруживают наличие TREC в сочетании с разнообразием b-цепей TCR. При ВИЧ-инфекции уменьшение количества неиммунных CD4+- и CD8+-Т-клеток можно определить по уменьшению числа циркулирующих Т-лимфоцитов, содержащих TREC.
О восстановлении функций тимуса можно судить по его увеличению в размере и восстановлению пролиферации тимоцитов, а также по наличию TREC в циркулирующих лимфоцитах. TRЕС+-клетки обнаруживаются во время проведения противоретровирусной терапии. Количество циркулирующих TREC-содержащих клеток, однако, может изменяться за счет других процессов, таких, как перераспределение лимфоцитов в органах и тканях, пролиферация и апоптоз лимфоцитов.
Эти факторы необходимо учитывать при проведении исследований процессов апоптоза и клеточного цикла. После частичной регенерации функций тимуса возможно частичное восстановление иммунной системы. Некоторые исследования показали, что функция тимуса зависит от степени восстановления Т-клеток после начала эффективной противоретровирусной терапии. Другие исследования позволили предположить, что использование гормона роста может помочь в восстановлении ткани тимуса.
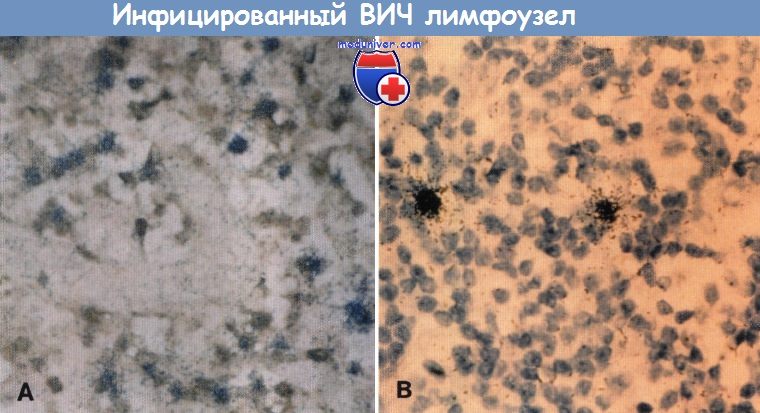
ВИЧ-инфицирование лимфоидной ткани.
Присутствие ВИЧ-инфекции в клетках лимфатического узла было показано с помощью метода ПЦР in situ ДНК и РНК.
(А) Большое количество клеток поражено инфекцией, как показано с помощью in situ ДНК ПЦР.
Отмечается зеленая зернистость (обозначающая реакцию с ВИЧ) вокруг ВИЧ-инфицированных клеток.
(В) В том же лимфатическом узле, как показано с помощью in situ РНК ПЦР, обнаруживаются только две клетки с реплицирующимися вирусными частицами (темная зернистость показывает вирусную РНК).
Примерно от 1 на 300 до 1 на 400 инфицированных клеток в лимфатическом узле продуцируют вирус.
Изучение морфологических изменений органов гемиммунопоэза при воздействии ВИЧ-инфекции имеет первостепенное значение поскольку именно они являются основными органами-мишенями при данной патологии.
Цель исследования - изучение морфологии центральных (костный мозг, тимус) и периферических (селезёнка, лимфатические узлы) органов гемиммунопоэза у больных, погибших на терминальной стадии ВИЧ-инфицирования.
Изучены гистологические препараты секционного материала, окрашенные гематоксилином и эозином, по ван Гизону. ВИЧ-инфекция была подтверждена с помощью иммуноблоттинга, а туберкулёз - бактериоскопическим и бактериологическим методами. Проанализированы результаты 261 вскрытия умерших от туберкулёза. Статистическая обработка данных проводилась с применением критерия Стьюдента.
В результате исследования выявлены следующие изменения в исследуемых органов. В красном костном мозге выявляется миелодисплазия. Отмечается нормальное и несколько увеличенное число ядерных клеток при нормальном соотношении миелоидных и эритроцитарных клеток, умеренный плазмоцитоз и некоторое увеличение ретикулина. Количество лимфоцитов снижено. В пунктате костного мозга находятся гистиоциты, многие из которых поглощены ядерными эритроидными клетками или гранулоцитами. Наблюдается увеличение объёма жировой ткани костного мозга. Эти данные свидетельствуют о том, что при ВИЧ-инфекции структурные изменения костного мозга затрагивают как гемопоэтическую ткань, так и стромальные элементы костного мозга.
Изменения тимуса при СПИДе и врождённом иммунодефиците связаны с поражением Т-системы. В вилочковой железе у умерших при злокачественном течении СПИД отсутствует деление на корковое и мозговое вещество, не выявляются тельца Гассаля и скопления эпителиальных клеток. Ткань тимуса инфильтрирована плазматическими и тучными клетками. Пролиферативная активность лимфоцитов при стимуляции их растворимыми антигенами снижена. При этом уровни иммуноглобулинов (IgM, IgG, IgA) повышены. Происходят изменения периферической картины крови: нейтропения, анемия, тромбоцитопения.
Выявляются очаговые поражения паренхимы селезёнки. Они представлены мелкими и крупными гипоэхогенными очагами, зонами некроза, кальцинатами, кистами, гематомами, метастазами и инфарктом селезёнки. У большей части больных селезёнка увеличена в размерах.
Изменения в лимфоузлах выражаются множественными, часто симметричными аденопатиями, наиболее часто локализующимися в шейной, подмышечной и подчелюстной областях. Особенно типичной является персистирующая генерализованная лимфаденопатия.

Обзор
Автор
Редакторы



Спонсором приза зрительских симпатий выступила компания BioVitrum.
Все явления, изучаемые биологией,
образуют непрерывную цепь событий,
и каждое последующее звено нельзя объяснить,
не принимая в расчет предыдущее.
Дж. Бернал. Возникновение жизни
Будем знакомы, меня зовут Тимус!
Зарождаюсь я, еще когда вы находитесь в утробе своей мамы и постепенно там развиваетесь. Моя главная задача — успеть развиться до вашего рождения, чтобы потом, в ваши ранние годы, приготовить для вас гормоны, обучить тимоцитов, чтобы оградить вас от вирусов, бактерий и прочих врагов. Мне надо очень многое успеть сделать для вас за короткий срок, так как, увы, мой век не долог. (. Я очень быстро старею и поэтому стараюсь за свою короткую жизнь сделать очень многое.) Попробую вам интересно и кратко рассказать о своей жизни. Итак, начнем-с.
Когда вы появляетесь на свет, я молод и полон сил для работы. Я красноватого цвета и работаю, не покладая рук (точнее, клеток). Из красного костного мозга ко мне на обучение приходят клетки, которые после обучения у меня приобретают профессию и выходят на защиту вашего организма. Эти обученные мной клетки называются Т-лимфоцитами (Т — это потому, что я, Тимус, их обучил) и получают после обучения мною три профессии:
- Т-хелпер — активирует Т-киллеров, то есть при обнаружении врага дает сигнал и зовет на помощь.
- Т-киллер — уничтожает врагов и ликвидирует поврежденные клетки своего организма.
- Т-супрессор — исполняет роль регулировщика военных действий. Он сдерживает атаку Т-киллеров и не допускает развития аутоиммунных заболеваний (когда свои собственные клетки организм принимает за чужие и начинает уничтожать их, как врагов).
Также я готовлю для вас необходимые гормоны. Что они делают. Ооо, да всего не перечислишь.
Гормоны — это вещества, которые вырабатываются в вашем организме органами; попадая в кровь, они разносятся по всему организму и сообща с другими работниками нашей системы помогают обмену углеводов, кальция в крови, регулируют развитие и рост вашего скелета. Гормоны также нужны для регенерации (восстановления) и кроветворения (образования и созревания кровяных клеток), они следят за соотношением Т- и В-лимфоцитов (если соотношение будет нарушено, то могут появится болезни) и делают много другого необходимого для вашего организма.
Зная о том, что вскоре я превращусь в жировую ткань, я делаю все возможное, чтобы даже после моего превращения мои выпускники Т-лимфоциты продолжали заботиться о вас. Когда вы маленькие, я нахожусь в самом расцвете сил и вырабатываю много Т-клеток, которые запоминают всех врагов (бактерий, вирусов и прочих), которые пытались проникнуть к вам в организм, и в будущем при встрече с ними вы уже защищены от них, так как Т-лимфоциты их запоминают и знают как с ними бороться. Когда вас в детстве вакцинируют от всех наиболее опасных болезней: туберкулеза, коклюша, кори и других инфекций, я выпускаю своих выпускников Т-лимфоцитов в бой, и они активно сражаются, запоминая навсегда врага, чтобы в следующий раз при встрече с ним быть во всеоружии и не дать ему проникнуть в организм.
С вашим взрослением потребность организма в новых Т-лимфоцитах снижается потому, что первые контакты с инфекциями и вирусами у человека происходят в основном в первые годы жизни (болезни, прививки), и когда вы вырастаете, Т-лимфоциты уже знают основных врагов вашего организма и вовсю работают, защищая вас! Я все меньше и меньше обучаю клетки. Моя работа заканчивается, я старею и перерождаюсь в жировую ткань. Когда вы повзрослеете, конечно же, будут встречаться незнакомые вашему организму инфекции, но их будет намного меньше, чем уже знакомых врагов организма. К тому же Т-лимфоциты могут жить долго и защищать вас (но эта их способность не вечна. ). Наш организм — (как я и говорил в начале) единая система! Если часто подвергаться болезням, нервничать, испытывать стресс, то Т-лимфоциты тратятся намного быстрее и в итоге их становится меньше и меньше, и тогда они не успевают ловить врагов. И если не беречь свое здоровье, то они не будут успевать выполнять свою работу!
Берегите себя! Будьте здоровы!
Ваш Тимус
Словарик

Обзор
Автор
Редактор
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Всегда ли можно дать сорокалетнему мужчине его сорок? А пятидесятилетнему? А скольким тридцатилетним женщинам вы бы не дали двадцати? Определять возраст человека по внешней составляющей не самая лёгкая задача. Однако, людям, перешагнувшим определённый порог, различный для мужчин и женщин, когда репродуктивная функция начинает стремительно угасать, становится сложнее скрывать свой возраст.

Рисунок 1. Сравнение размеров тимуса у новорождённого (а) и взрослого (б). К 50 годам тимус уменьшается в 5-7 раз по сравнению с первоначальным размером. Рисунок с сайта my.bpcc.edu.
Тимус — военная база иммунной системы

Рисунок 2. Соматическая рекомбинация на примере β цепи TCR. Исходная последовательность в гене, кодирующем β цепь TCR содержит V (variable), D (diversity), J (Joining) и C (constant) сегменты. Сначала один из двух D-сегментов соединятеся с одним из 13 J-сегментов. Получившийся DJ-сегмент присоединяется к одному из 50 V-сегментов. Сегменты выбираются случайным образом, и механизм их сшивки также предполагает случайное варьирование количества пар оснований, это обеспечивает разнообразие TCR. Аналогичный процесс происходит c последовательностью, кодирующей α-цепь только без D-сегмента. Рисунок с сайта Slideshare.

Рисунок 3. Взаимодействие TCR и антиген-презентирующей клетки. а — Т-клетка (фиолетовая) взаимодействует с антиген-презентирующей клеткой (APC, синяя). б — APC презентирует антиген в составе MHC. Гетеродимер TCR состоит из α и β цепей, охватывающих MHC с антигеном. С антигеном главным образом взаимодействуют области CDR3 — это домены, отвечающие за специфичность TCR к данному антигену. Рисунок с сайта Genomemedicine.
После наступления пубертатного периода производство тимусом наивных Т-клеток резко снижается и на протяжении всей взрослой жизни человека активность этого органа остаётся на самом базальном уровне. Чем это грозит? Созданное за такой короткий период огромное разнообразие TCR действительно обеспечивает эффективный иммунный ответ на большинство потенциальных угроз. Но это разнообразие остаётся константным только некоторое время.
Мы теряем наших бойцов!
Общее разнообразие TCR определяется количеством редких клонов в пуле Т-клеток, поэтому отсутствие возрастных изменений в разнообразии наиболее многочисленных Т-клеточных клонов указывает на то, что клоны наивных Т-клеток теряются с возрастом. Это связано с тем, что клоны наивных Т-клеток обычно малочисленны, поэтому вероятность того, что ни одна клетка данного клона не сможет поделиться или погибнет в результате каких-то случайных событий гораздо выше, чем для клонов с большим числом клеток.
Старики с высоким разнообразием TCR
Исследователи [2] сравнивали Т-клеточные профили периферической крови людей из четырех возрастных групп. Удивительным оказалось то, что люди в возрасте 71–90 лет обладали большим разнообразием TCR и большим процентным содержанием наивных Т-клеток в пуле CD4 + , чем люди возрастной категории 61–66 лет. Возможным объяснением такого отклонения от линейной зависимости стало предположение о восстановлении утраченных функций тимуса вследствие прекращения выработки половых гормонов в пожилом возрасте. Считается, что наиболее заметный спад активности тимуса происходит во время пубертатного периода, когда организм резко начинает вырабатывать большие количества половых гормонов. Вероятно, это связано с перераспределением ресурсов: приоритет в этом возрасте отдаётся развитию половой системы, а процесс созревания наивных Т-клеток в тимусе довольно энергозатратен. Смысл столь ранней инволюции органа может заключаться и в том, что в юном возрасте тимус состоит из молодых тканей, в структуре которых ещё нет дефектов, повышающих вероятность проникновения чужеродных агентов внутрь органа и использование их клетками тимуса для презентации созревающим наивным Т-клеткам как собственных антигенов, экспрессируемых организмом [5].
Другое объяснение явления увеличения разнообразия TCR после 70 лет заключается в том, что люди этой возрастной группы уже перешагнули определённый возрастной порог, пройдя в некотором смысле проверку на прочность — уникальный набор физиологических параметров, включая особенности иммунной системы, сделал их наиболее приспособленными среди всех особей популяции в данных условиях. Из этого можно заключить, что повышенное содержание наивных Т-клеток в субпопуляции CD4 + периферической крови человека коррелирует с долгожительством. Увеличение доли наивных Т-клеток в пуле CD4+, а значит и увеличение разнообразия TCR обеспечивает лучшую иммунорегуляторную функцию, что снижает общее воспаление, усиливающееся по мере старения организма из-за активации аутоиммунных процессов, увеличивает эффективность распознавания раковых клеток и обеспечивает более сбалансированный иммунный ответ [2].
Долгая, но бездетная жизнь

Рисунок 4. Придворные евнухи в Китае. Некоторые евнухи жили более ста лет. Рисунок с сайта Lacasamundo.
Мальчик, которому сделают орхеэктомию (удаление яичек), может быть, и получит дополнительные 10–15 лет жизни, вместе с тем лишившись возможности иметь детей и получив набор других не совсем приятных последствий. Существуют менее радикальные решения, основанные на приёме определённых препаратов, способствующих восстановлению функции тимуса. Одно из таких веществ — грелин, этот гормон вырабатывается слизистой оболочкой желудка и вызывает чувство голода, действуя на центры гипоталамуса. Оказалось, что грелин участвует в Т-клеточном сигналлинге, способен снижать связанное с возрастными изменениями воспаление, способствует восстановлению структуры тимуса и стимуляции его функций. Ряд цитокинов и факторов роста (интерлейкины 7 и 22, фактор роста кератиноцитов) являются потенциальными кандидатами для решения проблемы восстановления функции тимуса у взрослых людей. Интерлейкины обеспечивают дифференцировку и выживание тимоцитов. Фактор роста кератиноцитов необходим для пролиферации и дифференцировки функциональных тканей тимуса, его использование вызывает пролиферацию тимоцитов и увеличивает размеры органа. Возможно также использование веществ, блокирующих выработку стероидных гормонов, таких как аналоги гонадотропин-релизинг гормона, например, люпрона. Люпрон действует на гипофиз, блокируя рецепторы к гонадотропин-релизинг гормону, из-за чего уменьшается выработка лютеинизирующего и фолликуло-стимулирующего гормонов, что ведёт к снижению продукции эстрогена и тестостерона. И всё же, все вышеперечисленные вещества имеют неоднозначное воздействие на организм, и пока ещё нет данных о долгосрочных последствиях их приёма, поэтому их назначают только в случае восстановления после химиотерапии или при ВИЧ-инфекции, когда стимуляция работы тимуса необходима для реконституции иммунной системы [1].
Хранение наивных Т-клеток — полезная инвестиция в будущее
Есть ли иной способ продлить мужскую жизнь? Авторов статьи [2] посетила смелая идея решения этой проблемы. Кроме того, что редко встречающиеся клоны наивных Т-клеток в результате случайных событий теряются с возрастом, они, как и все клетки организма, могут поделиться лишь ограниченное количество раз (примерно 50 — лимит Хейфлика), что обусловлено укорочением теломерных участков хромосом после каждой репликации ядерной ДНК, а делятся наивные Т-клетки раз в 1–2 года. Значит примерно к 70 годам основная часть Т-клеток выйдет из строя. Решение есть — можно запасать наивные Т-клетки! У молодых людей в возрасте до 15–20 лет, когда процессы формирования основного пула наивных Т-клеток уже заканчиваются, нужно брать образцы крови в таком объёме, чтобы количества наивных Т-клеток в них хватило для полного восстановления их пула уже в пожилом возрасте, и заморозить. Очень важно, чтобы забор произошёл именно в этот промежуток времени. Если брать кровь у более взрослых людей, количества циркулирующих наивных Т-клеток просто не хватит для полной реставрации их пула в будущем. Конечно же, такой подход будет эффективен и для женского пола. Эти образцы крови будут не только средством продления жизни, но ещё и подстраховкой в случае аутоиммунных заболеваний или рака, они помогут восстановить иммунную систему после химиотерапии. Создание подобных банков с замороженными образцами крови стало бы ключевым событием в становлении абсолютно новых подходов к лечению заболеваний иммунной системы. Например, СПИД можно было бы вылечить введением в здоровые размороженные Т-клетки заразившегося СПИДом мутации по гену мембранного рецептора CCR5 (CD195), люди с такой мутацией обладают природной резистентностью к ВИЧ [8], и их пересадкой больному, предварительно прошедшему курс химиотерапии.
Итоги
Как бы молодо не выглядел человек, параметры его иммунной системы будут объективно отражать возраст. Такие параметры как количество наивных Т-клеток и разнообразие TCR практически линейно снижаются по мере старения. Если вы являетесь счастливым обладателем повышенного разнообразия TCR, можете надеяться на несколько бонусных лет жизни. В будущем человечество ожидают новые дерзкие подходы к увеличению продолжительности жизни с использованием собственных наивных Т-лимфоцитов, собранных и замороженных много лет назад.
Читайте также:

