Вич в гинекологии реферат
Обновлено: 23.04.2024
Существует несколько классификаций ВИЧ-инфекции, однако в Украине используется классификация ВОЗ, которая отражена в Приказе МОЗ Украины № 120 от 25.05.2000 г. Согласно этой классификации, выделяют 5 стадий в течении ВИЧ-инфекции:
Стадия острого заболевания.
Стадия бессимптомного носительства.
Стадия персистирующей генерализованной лимфаденопатии (ПГЛ).
СПИД-ассоциированный комплекс (СПИД-АК).
Стадия острого заболевания (или острая ВИЧ-инфекция). Инкубационный период от момента инфицирования длится 2-4 недели, иногда — до 9-10 недель. У большинства ВИЧ-инфи-
цированных первыми симптомами острой инфекции являются лихорадка (более чем у 90%), лимфаденопатия (70-80%), фарингит (70%), мононуклеозоподобный синдром (50%), головная боль (30-40%), боли в мышцах и суставах (40-50%) и другие проявления острой респираторной вирусной инфекции. Возможны поражения нервной системы в виде радикуло- и миопатий, менин-гоэнцефалита и даже психоза. Наиболее типично увеличение подчелюстных, подмышечных, затылочных и шейных лимфоузлов.
Острая инфекция ВИЧ сопровождается высоким уровнем вирусной нагрузки. Определение количества вирусных копий в этот период является наиболее достоверным диагностическим методом.
Стадия бессимптомного носительства — латентный период, который длится в течение многих лет. Продолжительность этой стадии зависит от исходного состояния лимфоидной системы и сопутствующих заболеваний. Чем чаще и длительнее болеет человек вирусными, бактериальными и другими воспалительными заболеваниями, тем короче латентный период ВИЧ-инфекции и тем быстрее она переходит в следующую стадию.
Латентный период течения ВИЧ-инфекции нельзя назвать абсолютно бессимптомным, потому что очень часто он проявляется увеличением различных групп лимфоузлов. Если исследовать структуру этих лимфоузлов, то в них можно обнаружить высокую концентрацию вирусов как экстрацеллюлярно, так и интрацеллю-лярно. ВИЧ размножается в лимфоидной ткани, которая до определенного времени является резервуаром для вирусов. С течением времени лимфоидная ткань разрушается, ВИЧ освобождается, и болезнь переходит в следующую стадию.
Стадия персистирующей генерализованной лимфаденопатии (ПГЛ) проявляется увеличением лимфоузлов разных групп, включая паховые, до размеров более 1 см в диаметре. Такое увеличение длится не более 3-х месяцев, а затем происходит их уменьшение. Для этой стадии ВИЧ-инфекции характерна лабильность лимфаденопатии — то увеличение, то уменьшение лимфоузлов.
ПГЛ может наблюдаться и на следующих стадиях ВИЧ-инфекции, однако на этой стадии она является единственным клиническим проявлением.
Количество CD4+ лимфоцитов прогрессивно уменьшается, вирусная нагрузка в крови возрастает, появляются первые признаки следующей стадии болезни — СПИД-АК.
СПИД-ассоциированный комплекс (СПИД-АК) проявляется наличием на фоне ВИЧ-инфекции следующих заболеваний:
кандидозного кольпита или вульвовагинита;
частых обострений хронических воспалительных заболеваний органов малого таза и др.
Клинически СПИД-АК проявляется нарастающей общей слабостью, длительной лихорадкой (более 1 месяца), прогрессирующей потерей массы тела, диареей, анорексией, гепатоспленомегалией, возникновением фурункулеза, паротита и др.
Средняя продолжительность СПИД-АК у больных, не получавших антиретровирусную терапию, составляет 12-18 месяцев, после чего болезнь переходит в свою финальную стадию — СПИД.
— кандидоз пищевода, трахеи, легких, бронхов или других внутренних органов;
цитомегаловирусная инфекция с генерализованным поражением внутренних органов;
генерализованная герпетическая инфекция;
диссеминированный или внелегочный гистоплазмоз;
рак шейки матки;
туберкулез легких и внелегочный;
— другие микобактериозы, диссеминированные или внеле- гочные.
Течение СПИДа характеризуется быстрым развитием синдрома истощения, что обусловлено действием ВИЧ: прогрессирующей потерей массы тела более 10%, нарастающей общей слабостью, хронической усталостью, необъяснимой лихорадкой более 30 дней, хронической диареей. Продолжительность жизни на этой стадии не более 12-18 месяцев. Пациенты, как правило, умирают от осложнений, связанных с оппортунистическими инфекциями.
ВИЧ-инфекция при беременности
В мире: ежегодно родоразрешаются около 2 млн. ВИЧ инфицированных женщин, рождаются свыше 600 000 ВИЧ инфицированных новорожденных.
После 2000 г. количество родов, принятых у ВИЧ-инфицированных увеличилось почти в десять раз: с 668 в 2000 г. до 6365 в 2004 г. (вцелом по стране 0,5%), у девочек – подростков — более чем в двадцать раз.
В последние годы число детей, родившихся от ВИЧ-инфицированных матерей, резко увеличивалось: удваивалось в 2001 и 2002 г.г., и к концу 2004 г. достигло почти 20 000.
Показатель перинатальной смертности среди родившихся у ВИЧ-инфицированных матерей колеблется в пределах 20-25 на 1000 родившихся живыми и мертвыми.
Во время беременности у 31% женщин не проводилась профилактика вертикальной передачи ВИЧ инфекции, во время родов — у 12%.
За последние годы в РФ перинатальное инфицирование ВИЧ уменьшилось с 20% до 10% (в США – в 4 раза: до 1-2%).
Среди беременных доля женщин с наркотической зависимостью составила менее 3%.
Запомните! Все женщины, планирующие беременность, должны пройти скрининг на ВИЧ-инфекцию.
ВИЧ-инфицированная беременная должна знать:
Беременность не несет повышенного риска прогрессирования заболевания.
В отсутствие тяжелых форм заболевания (СПИД) риск неблагоприятных исходов беременности не повышается.
Существует риск передачи заболевания плоду и новорожденному, который можно снизить противовирусным лечением.
Обследование ВИЧ-инфицированных беременных:
Полный анамнез, в том числе предыдущего и настоящего противовирусного лечения, и физикальное исследование.
Уровень вирусной РНК в крови (вирусная нагрузка): повторяется каждый месяц от начала лечения до стабилизации вирусной нагрузки и далее один раз в триместр.
Содержание CD 4+ лимфоцитов (абсолютное и относительное).
Клинический анализ крови и содержание тромбоцитов.
Исследование на ИППП (гонорея, хламидия, сифилис, герпес) при взятии на учет. Рекомендуется повторить в 28 недель беременности.
Исследование на гепатиты В и С.
Исследование на цитомегаловирус и токсоплазмоз (антитела).
Цитологическое исследование шейки матки.
Кожный тест на туберкулез (туберкулиновая проба): папула равная или более 5 мм считается положительной пробой.
Перинатальная передача ВИЧ:
Вертикальная передача составляет 17-25% и осуществляется:
трансплацентарно (25-30%), чаще в последние 2 месяца беременности и менее 2% в первом и втором триместрах;
в родах (70-75%): контакт с инфицированными секретами родовых путей;
через грудное молоко (5-20%). При заражении матери после родов вертикальная передача через грудное молоко возрастает до 29% (16-42%).
Выявление инфицированных новорожденных: практически все новорожденные от инфицированных матерей получают специфические антитела, которые могут определяться в их крови до 18 месяцев жизни. Поиск инфекции у новорожденных методом ПЦР должен начинаться в пределах 48 часов от рождения, с повторными исследованиями через 2 недели, через 1-2 и 3-6 месяцев. Метод позволяет выявить ВИЧ у 25-30% инфицированных новорожденных на момент рождения, у остальных 70-75% через месяц после родов. РНК (или р24 антиген) вируса, выявляемые в первую неделю жизни, свидетельствуют о внутриутробном инфицировании, а в период от 7 до 90 дней жизни – о заражении во время родов (при отсутствии грудного вскармливания).
новорожденный считается ВИЧ инфицированным при двух положительных вирологических тестах из двух отдельных проб;
новорожденный считается не имеющим ВИЧ инфекции при двух или более отрицательных вирологических тестах из двух или более отдельных проб, проведенных через 1 или более месяц после рождения, и подтвержденных хотя бы одним отрицательным тестом в возрасте 4 или более месяцев.
Стадия заболевания (клиническая категория).
Вирусная нагрузка: количество частиц вируса в единице объёма.
Иммунный статус: количество СД 4 (+) лимфоцитов.
Родоразрешение до 34 недель.
Рождение плода первым из двойни (в 2 раза).
Длительность безводного промежутка при преждевременном излитии околоплодных вод: рост вертикальной передачи в 2 раза при промежутке более 4 часов, и далее по 2% на каждый последующий час безводного промежутка в течение суток.
Вмешательства с целью пренатальной диагностики: амниоцентез, биопсия ворсин хориона, забор крови плода: в 2 раза. При наличии интенсивного лечения такой зависимости не отмечено.
Курение и прием наркотических препаратов.
Другие инфекции половых путей, в том числе ИППП и хорионамнионит.
Способ родоразрешения: кесарево сечение, проведенное до начала родовой деятельности, снижает риск инфицирования новорожденного до 6-8%.
Противовирусное лечение снижает риск инфицирования новорожденного до 6-8%.
Кесарево сечение, проведенное на фоне противовирусного лечения, снижает риск инфицирования новорожденного до 1-2%.
При вирусной нагрузке менее 1000 копий/мл кесарево сечение не снижает риск инфицирования новорожденного.
Обстоятельства, не влияющие на вертикальную передачу:
Питание беременных, пищевые добавки, витаминотерапия.
Операции акушерских щипцов, вакуумэкстракции плода, эпизиотомии.
Безводный промежуток на фоне активного противовирусного лечения.
Применение глюкокортикоидов для профилактики СДР новорожденных.
Вакцинация ВИЧ-инфицированной беременной приводит к активации репликации вируса. Возможна вакцинация против гриппа и гепатита Б. Целесообразно все необходимые вакцинации провести до беременности.
Исключаются, проводимые в родах, манипуляции, связанные с травмой кожи головки плода (взятие крови, введение электродов).
Не существует вирусной нагрузки или метода профилактики, исключающих вертикальную передачу.
Беременность не должна быть препятствием для применения оптимальных режимов лечения.
Пациенты, получающие лечение ВИЧ-инфекции до беременности, должны его продолжать и во время беременности.
Если лечение прекращается в I триместре, все препараты отменяются одновременно.
Медикаментозная профилактика вертикальной передачи ВИЧ рекомендуется всем инфицированным беременным вне зависимости от уровня вирусной нагрузки.
Эффективность лечения подтверждается падением вирусной нагрузки на один log и более через 4-8 недель после ее начала. При отсутствии этого падения проводится исследование на лекарственную устойчивость вируса. Если лечение начинается в поздние сроки беременности при высокой вирусной нагрузке, то определение устойчивости вируса к препаратам необходимо проводить перед началом лечения.
Назначение беременным зидовудина, легко переходящего через плаценту и дающего возможность внутривенного введения, рекомендуется в любой комбинации противовирусного лечения, вне зависимости от срока беременности и вирусной нагрузки. Зидовудин, единственный из препаратов своего класса, превращается в плаценте в активный в отношении ВИЧ трифосфат.
Добавление к схеме лечения зидовудином, состоящей из трех этапов, других противовирусных препаратов рекомендуется женщинам, чей клинический, иммунологический, вирологический статус требует назначения лечения, или любой женщине с вирусной нагрузкой более 1000 копий/мл.
Решение о начале терапии ВИЧ-инфекции у беременных основано на тех же принципах, что и у небеременных женщин.
Осложнения наступают с частотой не более 5%, митохондриальная дисфункция – с частотой не более 0,3% без случаев перинатальной смертности.
Длительное лечение новорожденного не может заменить длительного лечения матери.
После лечения матери зидовудином у новорожденных через 6 лет жизни не отмечено нарушений роста, общего развития, повышения частоты злокачественных опухолей.
По данным эксперимента на животных ввиду риска аномалий развития при лечении беременных следует воздержаться от назначения препаратов: эфавиренц, делавирдин, гидроксимочевина.
Возможные варианты лечения беременных
Профилактическое лечение зидовудином (азидотимидин):
В родах: внутривенно 2 мг/кг в течение часа, далее 1 мг/кг/час до родоразрешения.
Следует помнить, что при родах в срок менее 35 недель лечение новорожденного проводится иначе:
при беременности сроком более 30 недель: 1,5 мг/кг в/в или 2,0 мг/кг per os каждые 12 часов, и через 2 недели лечения — через 8 часов.
при беременности сроком менее 30 недель введение зидовудина дважды в сутки проводится в течение 4 недель.
В течение 4 недель перед родами по 200 мг per os дважды в день.
В родах: по 300 мг каждые 3 часа per os.
Профилактическое лечение невирапином:
в начале родов 200 мг per os однократно;
добавление невирапина к уже проводимому лечению не рекомендуется, а повышение частоты его введения в родах не снижает вертикальную передачу.
Высокоинтенсивное (комбинированное) противовирусное лечение: два НИОТ и ингибитор протеаз, показано при более тяжелых формах заболевания.
Клинические варианты применения противовирусного лечения
ВИЧ инфицированные женщины, не получавшие лечения до беремености:
Время начала и выбор лечения должны быть основаны на тех же параметрах, что и при отсутствии беременности;
Трехэтапное лечение зидовудином, начинаемое после первого триместра, рекомендуется всем ВИЧ инфицированным беременным вне зависимости от величины вирусной нагрузки;
Добавление к зидовудину других противовирусных препаратов рекомендуется для беременных, чей клинический, иммунологический или вирологический статус требуют назначения комбинированного лечения;
Комбинированное лечение рекомендуется при вирусной нагрузке более 1000 копий/мл вне зависимости от клинического или иммунологического статуса.
ВИЧ инфицированные женщины, получавшие лечение до беременности:
При диагностике беременности после первого триместра лечение продолжается в том же объеме, при этом обязательным компонентом противовирусной терапии должен быть зидовудин.
При диагностике беременности в течение первого триместра с пациентом обсуждается польза и возможный риск терапии в этот период беременности. При временном прекращении лечения во избежание развития лекарственной устойчивости прием всех препаратов прекращается и возобновляется одновременно.
При любой схеме лечения во время беременности роженице и новорожденному рекомендуется назначение зидовудина.
ВИЧ инфицированным роженицам, не получавшим лечения при беременности, проводится медикаментозная профилактика вертикальной передачи вируса в течение родов:
Внутривенное введение зидовудина с последующим лечением новорожденного в течение 6 недель (вариант А).
Пероральный прием зидовудина и ламивудина в родах с последующим лечением новорожденного в течение 7 дней. Роженице: зидовудина 600 мг в начале родов и далее по 300 мг каждые 3 часа; ламивудина 150 мг в начале родов и далее каждые 12 часов до родоразрешения. Новорожденному: зидовудин 4мг/кг и ламивудин 2 мг/кг каждые 12 часов в течение 7 дней.
Однократный прием невирапина в начале родов и однократный прием невирапина новорожденным в первые 48 часов жизни.
Комбинация введения зидовудина матери (внутривенно) и новорожденному и приема невирапина матерью и новорожденным (клинических испытаний метода не проводилось). Сразу после родов необходима оценка вирусной нагрузки и иммунологического статуса пациента для решения вопроса о необходимости дальнейшего лечения.
Новорожденные от матерей, не получавших лечения ни при беременности, ни в родах:
В первые 12 часов после родов рекомендуется начать прием зидовудина, который продолжается в течение 6 недель.
При известной устойчивости вируса к зидовудину возможна его комбинация с другими противовирусными препаратами.
Сразу после родов необходима оценка вирусной нагрузки и иммунологического статуса родильницы для решения вопроса о необходимости ее дальнейшего лечения.
Новорожденному показано определение РНК вируса в первые 48 часов жизни: при подтверждении его инфицирования лечение должно быть начато как можно скорее.
При половом пути заражения первыми инфицируются дендритические клетки (Лангерганса), расположенные под эпителием. В пределах 2 суток эти клетки сливаются с CD 4+ T-лимфоцитами и перемещаются в дренирующие лимфоузлы, откуда начинается системное распространение вируса, который может быть обнаружен в плазме через 4-11дней после заражения. Риск заражения при половом контакте повышается при травме слизистых оболочек и наличии воспаления тканей (язвенные поражения, уретрит, цервицит). При парентеральном поступлении вируса он инфицирует циркулирующие дендритические клетки и Т-лимфоциты, после чего начинается описанный процесс диссеминации ВИЧ. При перинатальной передаче вируса возможны оба механизма заражения. Риск заражения при всех путях передачи вируса определяется вирусной нагрузкой: количеством вирусных частиц в единице объема крови (в мл).
ВИЧ инфекция характеризуется значительной вариабельностью вируса: генотипической, фенотипической и клинической. В инфицированном организме могут находиться несколько различных геномов вируса. Эта неоднородность является следствием высокого темпа размножения вируса. Цикл репликации вируса составляет примерно 2 дня, и вирус находится в состоянии активного и постоянного размножения. Количество циклов репликаций одной вирусной частицы может составить до 300 в год, и до нескольких тысяч за все время болезни. Подсчитано, что на один цикл размножения приходится одна ошибка в подборе нуклеотида в геноме вируса. Результатом является появление ряда генетических вариантов вируса, некоторые из которых являются благоприятными для его выживания.
Варианты, обладающие тропизмом к Т-лимфоцитам и обладающие способностью формировать синцитиум, связаны с прогрессированием заболевания. При первичной и бессимптомной инфекции преобладают варианты с тропизмом к макрофагам, не формирующие синцитиум.
ВИЧ выявляется и вне клеток: в плазме — у 30% инфицированных, но в низких титрах (10-50 частиц вируса в 1 мл). То же относится к слезам и слюне: 1/10 -1/100 от количества частиц вируса в крови. При вирусном гепатите В в 1 мл крови находится от 100 млн. до 1 млрд. частиц вируса, что делает риск заражения при уколе иглой намного выше, чем при ВИЧ инфекции. В спинномозговой жидкости количество вирусных частиц ВИЧ значительно выше – до 1000 в 1 мл.
Ввиду низкой концентрации частиц ВИЧ в тканях тела, более вероятно передача инфицированных клеток, нежели свободно существующего вируса. Большое количество инфицированных вирусом клеток содержится в сперме и секретах влагалища и шейки матки.
После инфицирования происходит быстрый подъем уровня ВИЧ в плазме крови, широкое распространение вируса в организме с поражением органов, содержащих лимфоидную ткань. На фоне первичной ВИЧ-инфекции, сопровождаемой высоким уровнем виремии, резко падает уровень CD 4 + Т-лимфоцитов. Однако через несколько недель, когда иммунная система замедляет репликацию вируса, система гемопоэза частично замещает погибшие лимфоциты. При этом через 3-4 месяца после начала заболевания вирусная нагрузка существенно снижается, достигая самого низкого для данного больного уровня. Далее она будет только расти, ибо на протяжении всех стадий ВИЧ-инфекции продолжается постоянное размножение вируса и снижение числа CD 4+ Т-лимфоцитов. Следует отметить, что на фоне высокой виремии в острую стадию инфекции существует высокий риск ее вертикальной передачи в родах и при грудном вскармливании.
С окончанием острой фазы инфекции пациент вступает в латентную фазу с отсутствием симптомов заболевания. В эту фазу вирус активно размножается, иногда с высокой скоростью, но инфекция, смерть клеток и их замещение пока находятся в равновесии. Хотя организм инфицированного человека вырабатывает антитела с нейтрализующей активностью к оболочке вируса и специфические Т-клетки с цитотоксической активностью по отношению к протеинам вируса, но более важным в подавлении размножения вируса является секреция цитокинов с антивирусной активностью лимфоцитами с CD 8+ антигенным комплексом (киллеры). Важно отметить, что активность киллеров угнетает размножение вируса, но не убивает инфицированные клетки. Их функция зависит от достаточного количества интерлейкина-2, производимого CD 4+ Т-лимфоцитами, которые и при отсутствии симптомов заболевания начинают свое медленное прогрессивное снижение.
У женщин с ВИЧ инфекцией дисплазия (интраэпителиальная неоплазия) шейки матки встречается в 5 раз чаще, а тяжесть дисплазии соответствует степени иммуносупрессии (количеству CD 4+ клеток). При выявлении поражений шейки у ВИЧ-инфицированных женщин мазок с окраской по Папаниколау является более точным методом диагностики в сравнении с кольпоскопией. У ВИЧ инфицированных чаще наблюдается прогрессирование дисплазии шейки матки и её рецидив после хирургического лечения, что также зависит от степени иммуносупрессии. ВИЧ-инфицированные женщины должны проходить цитологическое обследование дважды в год с кольпоскопическим исследованием при выявлении дисплазии или атипии.
Нарушения иммунной защиты на уровне эндометрия приводят к повышению частоты воспалительных заболеваний органов малого таза у женщин с ВИЧ инфекцией. У заболевших чаще приходится прибегать к хирургическому методу лечения, хотя уровень тубо-овариальных абсцессов у них не повышается. В группе женщин с ВЗОМТ целесообразен скрининг на ВИЧ.
При ВИЧ-инфекции повышена частота бактериального вагиноза, папилломовирусной инфекции. При ВИЧ-инфицировании влагалищный кандидоз встречается в 2 раза чаще, а у женщин с содержанием CD 4+ лимфоцитов менее 200/мкл его частота повышается в 7 раз. У лиц с тяжелой иммуносупрессией он часто является первым симптомом прогрессирования заболевания, его перехода в стадию СПИД.
стероидные гормоны и стерилизация — наиболее эффективные методы контрацепции у ВИЧ инфицированных женщин;
ВМС не рекомендуются ввиду высокой вероятности инфекционных осложнений;
кондом из латекса является надежным методом предупреждения ВИЧ инфицирования, но не беременности;
прерванное половое сношение и метод периодического воздержания также не рекомендуются к применению ввиду своей ненадежности в предупреждении беременности.
Приложение 1. Классификация ВИЧ-инфекции
Категория по содержанию Клиническая категория
СД 4 ( +) Т — лимфоцитов А В C
Более 500 / мкл — более 29% А1 В1 С1
200 — 499 / мкл - 14 — 28% А2 В2 С2
менее 200 / мкл — менее 14% А3 В3 С3
Клиническая категория А: острая (первичная) ВИЧ инфекция, персистирующая генерализованная лимфоаденопатия, и пациенты без симптомов ВИЧ – инфекции.
Клиническая категория В: симптомные состояния, встречающиеся при ВИЧ-инфицировании, но не состояния, входящие в категории А или С.
кандидоз вульвы и влагалища: персистирующий, частый, устойчивый к лечению;
дисплазия шейки матки умеренная или тяжелая;
общие симптомы: лихорадка более 38,5* или понос, длящиеся более 1 мес.;
лейкоплакия волосистых частей тела, рта;
герпес: два и более эпизода и занимающий более 1 дерматома;
идиопатическая тромбоцитопеническая пурпура;
воспалительные заболевания малого таза, особенно, осложненные тубо-овариальным абсцессом;
Клиническая категория С: состояния, указывающие на СПИД:
кандидоз бронхов, трахеи, легких;
инвазивный рак шейки матки;
кокцидиоидомикозы распространенные или внелегочные;
криптоспоридиоз хронический кишечный (более 1 мес);
цитомегаловирусная инфекция, кроме печени, селезенки или лимфоузлов;
цитомегаловирусный ретинит с потерей зрения;
герпес: хронические язвы (более 1 мес), поражения бронхов, легких, пищевода;
гистоплазмозис распространенный или внелегочный;
изоспориазис хронический кишечный (более 1 мес);
лимфома мозга, первичная;
туберкулез любой локализации;
прогрессирующая множественная лейкоэнцефалопатия;
сальмонеллез возвратный, септицемия;
Приложение 2. Клинические симптомы ВИЧ-инфекции
Общие/конституциональные: лихорадка, фарингит (негнойный), лимфоаденопатия, артралгия, миальгия, усталость/недомогание, потеря веса.
Кожные: макулопопулезная сыпь, розеолезная сыпь, везикопустулез, крапивница диффузная, десквамация на стопах/ладонях, язвы кожи и слизистых, алопеция.
Желудочно-кишечный тракт: кандидоз рта, глотки, пищевода, тошнота/рвота, анорексия, боль в животе, понос.
Неврологические: головная боль, боль в глазах, фотофобия, нарушения сознания, периферическая нейропатия, миелопатия, радикулопатия, неврит плечево-го нерва, синдром Джулиана-Барра (острый демиелинезирующий полиневрит).
Приложение 3. Практические рекомендации по лечению ВИЧ-инфекции (университет Джона Хопкинса, США, 1997 г.)
Когда начинать лечение:
острая ВИЧ инфекция: в остром периоде или в течение 6 месячного периода после сероконверсии;
хроническая ВИЧ инфекция: при уровне РНК ВИЧ более 10 тыс. ко-пий/мл или числе СД 4 (+) лимфоцитов менее 500 кл/мм3.
С чего начиннать лечение:
Рекомендуемая схема (доказана наиболее стойкая и выраженная антивирусная активность у большинства больных) - 2 НИОТ: зидовудин и ламивудин; зидовудин и диданозин; зидовудин и залцитабин; ламивудин или диданозин со ставудином, и ингибитор протеаз: ретиновир, индинавир, нелфинавир.
Альтернативная схема (менее эффективна, чем рекомендуемая) - 2 НИОТ в сочетании с невирапином .
Противопоказано: монотерапия любым препаратом, а также зидовудин со ста-вудином, диданозин с залцитабином, залцитабин со ставудином.
Когда изменять схему лечения:
при неэффективности лечения: уровень РНК ВИЧ более 500 копий/мл через 4-6 мес. от начала лечения;
в случае токсичности или непереносимости лекарственных препаратов;
при появлении новых, более эффективных лекарственных препаратов.
Как изменять схему лечения при его неэффективности:Прежняя схема Новая схема
2 НИОТ с ингибитором протеаз 2 новых НИОТ с новым ингибитором протеаз
2 новых НИОТ с невирапином
Новый НИОТ, новый ингибитор протеаз, невирапин
2 новых ингибитора протеаз и НИОТ
2 НИОТ с невирапином 2 новых НИОТ с ингибитором протеаз
2 НИОТ 2 новых НИОТ с ингибитором протеаз или невирапином
Приложение 4. Российские нормативно-законодательные документы по проблеме ВИЧ/СПИД
ВИЧ-инфекция у беременных — это хроническое прогрессирующее инфекционное заболевание, вызванное возбудителем из группы ретровирусов и возникшее до зачатия ребенка или в гестационном периоде. Длительное время протекает латентно. При первичной реакции проявляется гипертермией, кожной сыпью, поражением слизистых, преходящим увеличением лимфоузлов, диареей. В последующем возникает генерализованная лимфаденопатия, постепенно снижается вес, развиваются ВИЧ-ассоциированные расстройства. Диагностируется лабораторными методами (ИФА, ПЦР, исследование клеточного иммунитета). Для лечения и профилактики вертикальной трансмиссии применяется антиретровирусная терапия.
МКБ-10

Общие сведения
ВИЧ-инфекция является строгим антропонозом с парентеральным нетрансмиссивным механизмом заражения от инфицированного человека. За последние 20 лет число впервые выявленных инфицированных беременных увеличилось почти в 600 раз и превысило 120 на 100 тысяч обследованных. Большинство женщин детородного возраста заразились половым путем, доля ВИЧ-позитивных пациенток с наркотической зависимостью не превышает 3%. Благодаря соблюдению правил асептики, достаточной антисептической обработке инструментов для инвазивных процедур и эффективному серологическому контролю удалось существенно сократить частоту инфицирования в результате профессиональных травм, гемотрансфузий, из-за использования загрязненного инструментария и донорских материалов. Более чем в 15% случаев достоверно определить источник возбудителя и механизм инфицирования не удается. Актуальность особого сопровождения ВИЧ-инфицированных беременных женщин обусловлена высоким риском заражения плода при отсутствии адекватного сдерживающего лечения.

Причины
Возбудителем заболевания является ретровирус иммунодефицита человека одного из двух известных типов — ВИЧ-1 (HIV-1) или ВИЧ-2 (HIV-2), представленных множеством подтипов. Обычно инфицирование происходит до начала беременности, реже — в момент или после зачатия ребенка, во время гестации, родов, послеродового периода. Наиболее распространенным путем передачи инфекционного агента у беременных является естественный (половой) через секрет слизистых зараженного партнера. Инфицирование возможно при внутривенном введении наркотических препаратов, нарушении норм асептики и антисептики во время инвазивных манипуляций, выполнении профессиональных обязанностей с возможностью контакта с кровью носителя или больного (медработники, парамедики, косметологи). При беременности роль некоторых искусственных путей парентерального заражения возрастает, а сами они приобретают определенную специфику:
- Гемотрансфузионное инфицирование. При осложненном течении беременности, родов и послеродового периода увеличивается вероятность кровопотери. Схемы лечения наиболее тяжелых кровотечений предполагают введение донорской крови и полученных из нее препаратов (плазмы, эритроцитарной массы). Инфицирование ВИЧ возможно при использовании тестированного на вирус материала от зараженного донора в случае забора крови в период так называемого серонегативного инкубационного окна, длящегося от 1 недели до 3-5 месяцев с момента попадания вируса в организм.
- Инструментальное заражение. Беременным пациенткам чаще, чем небеременным, назначают инвазивные диагностические и лечебные процедуры. Для исключения аномалий развития плода применяют амниоскопию, амниоцентез, биопсию хориона, кордоцентез, плацентоцентез. С диагностической целью выполняют эндоскопические исследования (лапароскопию), с лечебной — наложение швов на шейку матки, фетоскопические и фетальные дренирующие операции. Инфицирование через загрязненные инструменты возможно в родах (при ушивании травм) и при кесаревом сечении.
- Трансплантационный путь передачи вируса. Возможными вариантами решений для пар, планирующих беременность при тяжелых формах мужского бесплодия, являются инсеминация донорской спермой или ее применение для ЭКО. Как и в случаях с гемотрансфузиями, в таких ситуациях возникает риск заражения при использовании инфицированного материала, полученного в серонегативный период. Поэтому с профилактической целью рекомендуется применять сперму доноров, которые благополучно прошли анализ на ВИЧ через полгода после сдачи материала.
Патогенез
Распространение ВИЧ по организму происходит с кровью и макрофагами, в которые изначально внедряется возбудитель. Вирус обладает высокой тропностью к клеткам-мишеням, в мембранах которых содержится специфический протеиновый рецептор CD4, — Т-лимфоцитам, дендритным лимфоцитам, части моноцитов и В-лимфоцитов, резидентным микрофагам, эозинофилам, клеткам костного мозга, нервной системы, кишечника, мышц, сосудистого эндотелия, хорионтрофобласта плаценты, возможно, сперматозоидам. После репликации новая генерация возбудителя покидает инфицированную клетку, разрушая ее.
Наибольший цитотоксический эффект вирусы иммунодефицита оказывают на Т4-лимфоциты I типа, что приводит к истощению клеточной популяции и нарушению иммунного гомеостаза. Прогрессирующее снижение иммунитета ухудшает защитные характеристики кожи и слизистых, уменьшает эффективность воспалительных реакций на проникновение инфекционных агентов. В результате на финальных стадиях заболевания у больной развиваются оппортунистические инфекции, вызванные вирусами, бактериями, грибками, гельминтами, протозойной флорой, возникают типичные для СПИДа опухоли (неходжкинские лимфомы, саркома Капоши), начинаются аутоиммунные процессы, в конечном итоге приводящие к гибели пациентки.
Классификация
Отечественные вирусологи используют в работе систематизацию стадий ВИЧ-инфекции, предложенную В. Покровским. В ее основу положены критерии серопозитивности, степени выраженности симптоматики, наличия осложнений. Предложенная классификация отображает поэтапное развитие инфекции от момента заражения до окончательного клинического исхода:
- Инкубационная стадия. ВИЧ присутствует в организме человека, происходит его активная репликация, однако антитела не определяются, признаки острого инфекционного процесса отсутствуют. Длительность серонегативной инкубации обычно составляет от 3 до 12 недель, пациентка при этом является заразной.
- Ранняя ВИЧ-инфекция. Первичный воспалительный ответ организма на распространение возбудителя длится от 5 до 44 суток (у половины пациенток — 1-2 недели). В 10-50% случаев инфекция сразу принимает форму бессимптомного носительства, что считается более прогностически благоприятным признаком.
- Стадия субклинических проявлений. Репликация вируса и разрушение CD4-клеток приводят к постепенному нарастанию иммунодефицита. Характерным проявлением становится генерализованная лимфаденопатия. Скрытый период при ВИЧ-инфекции продолжается от 2 до 20 лет и более (в среднем — 6-7 лет).
- Стадия вторичной патологии. Истощение защитных сил проявляется вторичными (оппортунистическими) инфекциями, онкопатологией. Наиболее распространенными СПИД-индикаторными заболеваниями в России являются туберкулез, цитомегаловирусная и кандидозная инфекции, пневмоцистная пневмония, токсоплазмоз, саркома Капоши.
- Терминальный этап. На фоне тяжелого иммунодефицита отмечается выраженная кахексия, отсутствует эффект от применяемой терапии, течение вторичных заболеваний становится необратимым. Длительность финальной стадии ВИЧ-инфекции до гибели пациентки обычно составляет не более нескольких месяцев.
Практикующим акушерам-гинекологам чаще приходится оказывать специализированную помощь беременным, находящимся в инкубационном периоде, на раннем этапе ВИЧ-инфекции или ее субклиническом стадии, реже — при появлении вторичных расстройств. Понимание особенностей заболевания на каждом этапе позволяет выбрать оптимальную схему ведения беременности и наиболее подходящий способ родоразрешения.
Симптомы ВИЧ у беременных
Поскольку во время беременности у большинства пациенток определяются I-III стадии заболевания, патологические клинические признаки отсутствуют или выглядят неспецифичными. В течение первых трех месяцев после инфицирования у 50-90% зараженных наблюдается ранняя острая иммунная реакция, которая проявляется слабостью, незначительным повышением температуры, уртикарной, петехиальной, папулезной сыпью, воспалением слизистых оболочек носоглотки, влагалища. У некоторых беременных увеличиваются лимфатические узлы, развивается диарея. При значительном снижении иммунитета возможно возникновение кратковременных, слабо выраженных кандидозов, герпетической инфекции, других интеркуррентных заболеваний.
Если заражение ВИЧ произошло до наступления беременности, и инфекция развилась до стадии латентных субклинических проявлений, единственным признаком инфекционного процесса является персистирующая генерализованная лимфаденопатия. У беременной обнаруживается не меньше двух лимфоузлов диаметром от 1,0 см, расположенных в двух и более группах, не связанных между собой. При ощупывании пораженные лимфатические узлы эластичны, безболезненны, не соединены с окружающими тканями, кожные покровы над ними имеют неизмененный вид. Увеличение узлов сохраняется в течение 3 месяцев и более. Симптомы вторичной патологии, ассоциированной с ВИЧ-инфекцией, у беременных выявляются редко.
Осложнения
Наиболее серьезное последствие беременности ВИЧ-инфицированной женщины — перинатальное (вертикальное) инфицирование плода. Без адекватной сдерживающей терапии вероятность заражения ребенка достигает 30-60%. В 25-30% случаев вирус иммунодефицита попадает от матери к ребенку через плаценту, в 70-75% — во время родов при прохождении через инфицированные родовые пути, в 5-20% — через грудное молоко. ВИЧ-инфекция у 80% перинатально инфицированных детей развивается бурно, а симптомы СПИДа возникают в течение 5 лет. Наиболее характерными признаками заболевания являются гипотрофия, упорная диарея, лимфаденопатия, гепатоспленомегалия, задержка развития.
Внутриутробное инфицирование часто приводит к поражению нервной системы — диффузной энцефалопатии, микроцефалии, атрофии мозжечка, отложению внутричерепных кальцификатов. Вероятность перинатального заражения возрастает при острых проявлениях ВИЧ-инфекции с высокой виремией, значительном дефиците Т-хелперов, экстрагенитальных заболеваниях матери (сахарном диабете, кардиопатологии, болезнях почек), наличии у беременной инфекций, передающихся половым путем, хориоамнионите. По наблюдениям специалистов в сфере акушерства у пациенток, инфицированных ВИЧ, чаще наблюдаются угроза прерывания беременности, самопроизвольные выкидыши, преждевременные роды, возрастает перинатальная смертность.
Диагностика
С учетом потенциальной опасности ВИЧ-статуса пациентки для будущего ребенка и обслуживающего медицинского персонала тест на вирус иммунодефицита включен в перечень рекомендованных рутинных обследований при беременности. Основными задачами диагностического этапа являются выявление возможного инфицирования и определение стадии заболевания, характера его течения, прогноза. Для постановки диагноза наиболее информативны лабораторные методы исследования:
При поступлении на роды ранее необследованной беременной из маргинальных контингентов возможно проведение экспресс-анализа на ВИЧ с помощью высокочувствительных иммунохроматографических тест-систем. Для планового инструментального обследования инфицированной пациентки предпочтительны неинвазивные методы диагностики (трансабдоминальное УЗИ, допплерография маточно-плацентарного кровотока, кардиотокография). Дифференциальная диагностика на этапе ранней реакции проводится с ОРВИ, инфекционным мононуклеозом, дифтерией, краснухой, другими острыми инфекциями. При обнаружении генерализованной лимфаденопатии необходимо исключить гипертиреоз, бруцеллез, вирусные гепатиты, сифилис, туляремию, амилоидоз, красную волчанку, ревматоидный артрит, лимфому, другие системные и онкологические заболевания. По показаниям больную консультируют инфекционист, дерматолог, онколог, эндокринолог, ревматолог, гематолог.
Лечение ВИЧ-инфекции у беременных
Основными задачами ведения беременности при заражении вирусом иммунодефицита человека являются супрессия инфекции, коррекция клинических проявлений, предотвращение инфицирования ребенка. В зависимости от выраженности симптоматики и стадии заболевания назначается массивная политропная терапия антиретровирусными препаратами — нуклеозидными и ненуклеозидными ингибиторами обратной транскриптазы, ингибиторами протеазы, ингибиторами интегразы. Рекомендованные схемы лечения отличаются на разных сроках гестации:
- При планировании беременности. Во избежание эмбриотоксического эффекта женщинам с ВИЧ-позитивным статусом следует прекратить прием специальных препаратов до наступления фертильного овуляторного цикла. В таком случае удается полностью исключить тератогенное воздействие на ранних этапах эмбриогенеза.
- До 13 недели беременности. Антиретровирусные препараты применяют при наличии вторичных заболеваний, вирусной нагрузке, превышающей 100 тысяч копий РНК/мл, снижении концентрации Т-хелперов менее 100/мкл. В остальных случаях фармакотерапию рекомендуется прекратить для исключения негативных влияний на плод.
- С 13 по 28 недели. При диагностике ВИЧ-инфекции во II триместре или обращении инфицированной пациентки на этом сроке в экстренном порядке назначается активная ретровирусная терапия комбинацией из трех лекарственных средств — двух нуклеозидных ингибиторов обратной транскриптазы и одного препарата из других групп.
- С 28 недели до родов. Продолжается противоретровирусное лечение, осуществляется химиопрофилактика передачи вируса от женщины ребенку. Наиболее популярна схема, при которой с начала 28 недели беременная постоянно принимает зидовудин, а перед родами однократно – невирапин. В отдельных случаях используют резервные схемы.
Предпочтительным методом родоразрешения у беременной с диагностированной ВИЧ-инфекцией являются естественные роды. При их проведении необходимо исключить любые манипуляции, нарушающие целостность тканей, — амниотомию, эпизиотомию, наложение акушерских щипцов, использование вакуум-экстрактора. Из-за достоверного увеличения риска инфицирования ребенка запрещено применение препаратов, вызывающих и усиливающих родовую деятельность. Кесарево сечение выполняется после 38 недели гестационного срока при неизвестных показателях вирусной нагрузки, ее уровне больше 1 000 копий/мл, отсутствии дородовой антиретровирусной терапии и невозможности введения ретровира в родах. В послеродовом периоде пациентка продолжает прием рекомендованных противовирусных препаратов. Поскольку грудное вскармливание ребенка запрещено, лактация подавляется медикаментозно.
Прогноз и профилактика
Адекватная профилактика трансмиссии ВИЧ от беременной к плоду позволяет снизить уровень перинатального инфицирования до 8% и меньше. В экономически развитых странах этот показатель не превышает 1-2%. Первичная профилактика инфицирования предполагает использование барьерных контрацептивов, половую жизнь с постоянным проверенным партнером, отказ от употребления инъекционных наркотиков, использование стерильного инструментария при выполнении инвазивных процедур, тщательный контроль донорских материалов. Для предотвращения заражения плода важны своевременная постановка ВИЧ-инфицированной беременной на учет в женской консультации, отказ от инвазивной пренатальной диагностики, выбор оптимальной схемы антиретровирусного лечения и способа родоразрешения, запрет кормления грудью.
1. ВИЧ-инфекция и беременность: Монография / Барановская Е.И., Жаворонок С.В., Теслова О.А., Воронецкий А.Н., Громыко Н.Л. – 2011.
2. ВИЧ-инфекция у беременных: клиническое значение иммунных факторов: Автореферат диссертации/ Громыко Н.Л. – 2012.
3. Анализ клинического случая беременности у женщины с ВИЧ-инфекцией/ Мишина А.В., Незванова Т.В.// Вестник Совета молодых учёных и специалистов Челябинской области. - 2014- №5.
4. Беременность и перинатальные исходы у ВИЧ-инфицированных женщин: Автореферат диссертации/ Терехина Л.А. – 2008.
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисова Э. В., гинеколога со стажем в 35 лет.
Над статьей доктора Борисова Э. В. работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
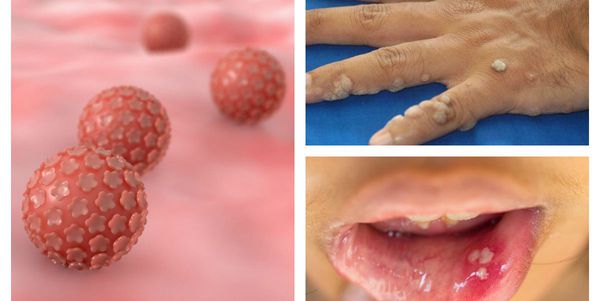
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
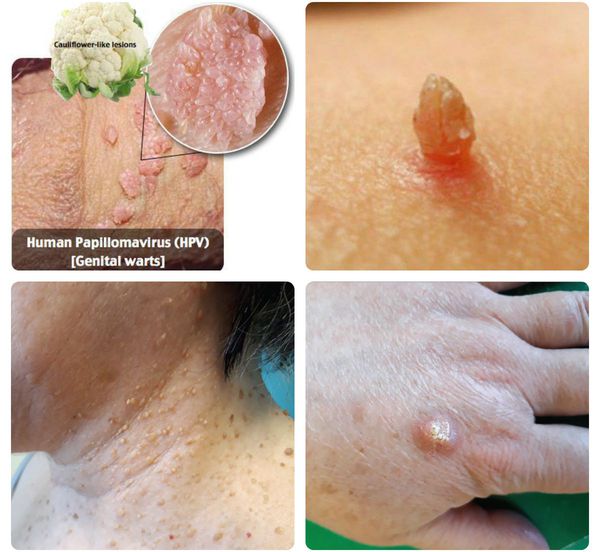
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
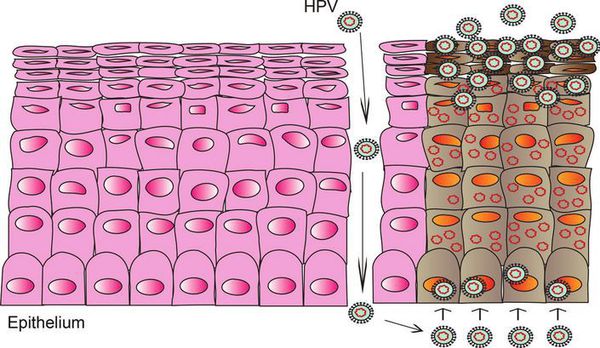
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
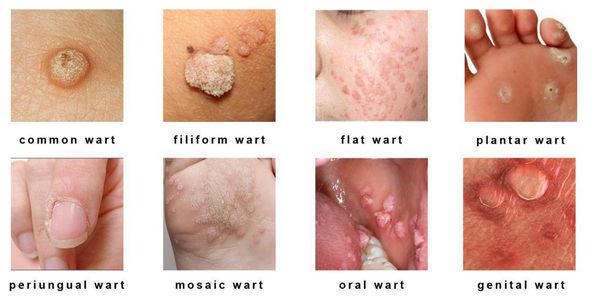
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
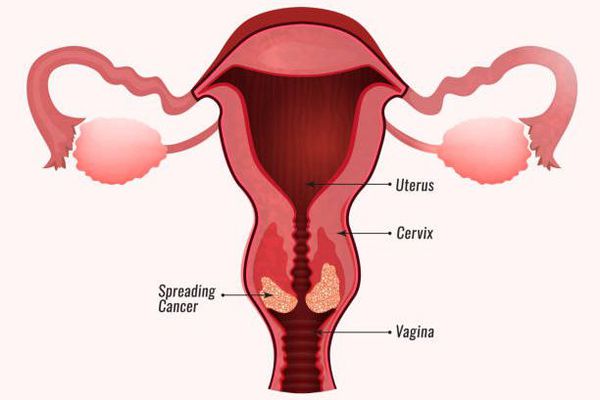
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
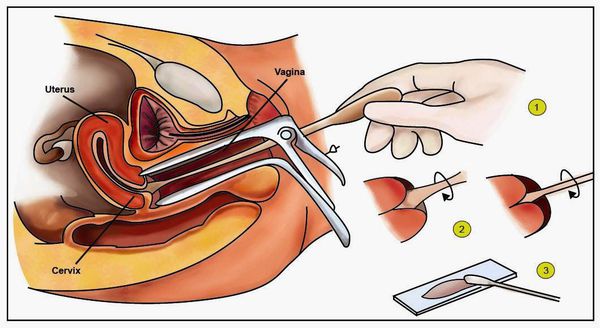
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
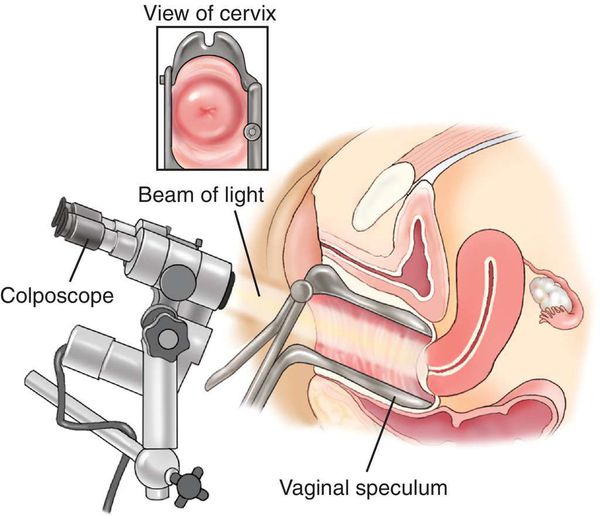
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
Читайте также:

