Власоглав для лечения колита
Обновлено: 23.04.2024
Острый колит характеризуется ярко выраженной симптоматикой. Часто протекает одновременно с воспалением тонкой кишки (энтерит) и желудка (гастрит).
Симптомы, характерные при остром колите, - острая боль, урчание в животе, потеря аппетита, жидкий стул с примесью слизи или крови, повышенная температура тела.
Основными причинами развития острого колита могут быть вирусные инфекции, пищевые отравления, токсические вещества.
Хронический колит, как правило, развивается после острого колита. Протекает с периодическими обострениями. Это заболевание, связанно с воспалительно-дистрофическими изменениями толстой кишки и расстройствами ее функций.
Для хронического колита характерные чередование поноса и запора, боль в различных отделах живота, ощущение недостаточного опорожнения кишечника, ложные позывы на дефекацию, тошнота, отрыжка, ощущение горечи во рту, урчание в животе, недомогание, снижение трудоспособности.
Причинами возникновения хронического колита могут быть нерациональное питание, злоупотребление алкоголем, а также прочие факторы, нарушающие нормальную функцию кишечника. Иногда встречаются случаи развития болезни в результате хронического копростаза (наличие механического препятствия продвижению каловых масс по толстому кишечнику).
- Панколит - поражаются все отделы толстой кишки.
- Тифлит - воспаление слизистой оболочки слепой кишки.
- Трансверзит - воспаление слизистой оболочки поперечной ободочной кишки.
- Сигмоидит - воспаление слизистой оболочки сигмовидной кишки.
- Проктит - воспаление слизистой оболочки прямой кишки.
Иногда поражаются 2 смежных отдела толстой кишки. Например, прямая кишка и сигмовидная, - проктосигмоидит.

Диагностика колита
Диагностика колита начинается с опроса пациента и выяснения причин заболевания. Затем проводится пальпации живота, при которой определяются болезненные участки брюшной стенки, пораженные сегменты толстой кишки и т.д.
При подозрениях на колит необходимо проведение копрологического исследования (анализ кала). При колите в каловых массах в большом количестве содержатся примеси слизи, лейкоциты, клетчатка. При язвенном колите в выделениях содержится примесь крови.
О наличии острого колита также будут свидетельствовать повышенные показатели лейкоцитов, скорости оседания эритроцитов (СОЭ), которые показывает клинический анализ крови.
Инструментальные исследования кишечника проводятся для обнаружения воспалительного процесса в толстой кишке, а также определения его места локализации. Они включают в себя ректороманоскопию, колоноскопию, ирригоскопию. В момент этих исследований берется материал на биопсию.

Манометрия прямой кишки позволяет исследовать тонус аноректальной мышцы и скоординированность сокращений прямой кишки и анальных сфинктеров.
Лечение колита
Если проявляются симптомы колита, следует немедленно обратиться в медицинское учреждение. Как лечить колит может сказать только врач после проведения диагностики. Любые попытки самолечения могут привести к серьезным осложнениям, которые могут угрожать жизни больного.
Лечение колита толстой кишки, прежде всего, подразумевает специальную диету и режим питания. В период обострения требуется соблюдение постельного режима до уменьшения интенсивности болевого синдрома и клинических проявлений заболевания. Лечение язвенного колита может проводиться на дому, однако при тяжелом течении необходима госпитализация больного в стационар.
При колите следует употреблять отварную или печеную пищу в теплом виде. Необходимо дробное питание не менее пяти раз за день, при этом ужинать следует не позднее семи часов вечера. В рационе питания должна преобладать белковая пища. Во избежание развития авитаминоза и анемии диету нужно составлять так, чтобы в организм поступало необходимое количество полезных веществ.
Существует ряд продуктов, употребление которых раздражает слизистую оболочку кишечника, в результате чего усиливается воспалительный процесс, а состояние больного ухудшается. Это цельное молоко, алкоголь, газированная вода, грибы, мясо жирных сортов, пряности, чернослив, курага, соленая и острая пища, овощи в сыром виде, семена подсолнуха, бобовые, кукуруза.
Лечение медикаментами непосредственно зависит от причины и типа заболевания. При инфекционных колитах необходимы антибактериальные препараты, назначенные врачом. Если причиной колита является отравление, необходимо срочно принять адсорбирующие средства, способные связывать токсины. Чтобы снять спазм кишечника, можно принять но-шпу или любой спазмолитик подобного действия.
Антисептическим и адсорбирующим действием одновременно обладают смекта ;и энтеросгель. При сильной диарее или рвоте важно не допустить обезвоживания организма с помощью специальных солевых растворов, например, регидрона.
При тяжелом течении заболевания необходима гормональная терапия, которая заключается в приеме глюкокортикостероидов.
Помимо лекарственной терапии необходим комплекс оздоровительных процедур, таких как физиотерапия, психотерапия (если заболевание вызвано психическими нарушениями), оздоровление в санатории.
Терапевтические манипуляции с микрофлорой: микроскопические круглые черви Trichuris trichiura помогают предотвратить бактериальное повреждение слизистой оболочки кишечника.
Наши представления о микроорганизмах, населяющих кишечник, за последние несколько десятилетий изменились коренным образом. На заре этих исследований считалось, что полезная микрофлора пищеварительной системы представлена несколькими десятками штаммов, которые, сосуществуя с нами, принимают ограниченное участие в пищеварении и обеспечивают нас некоторым количеством определенных витаминов. Реальных масштабов влияния качества и количества облигатной (обязательной для нормального функционирования кишечника) и факультативной (необязательной) микрофлоры на наш организм никто себе даже не представлял.
Но, с учетом впечатляющих размеров и сложности организации нашей микробиоты, можно смело надеяться, что впереди нас ждут еще более удивительные открытия. Недавно в авторитетном журнале PLoS Pathogen были опубликованы результаты исследования, показавшие возможность терапевтического использования микроскопического паразитического червя Trichuris trichiura с целью нормализации разбалансированной кишечной микрофлоры в случае хронических воспалительных заболеваний кишечника.
Многие детали патогенеза хронических заболеваний кишечника (ХВЗК), к коим относят неспецифический язвенный колит и болезнь Крона, достоверно неизвестны, что существенно осложняет поиск методов их лечения. Однако одним из ключевых проявлений этих болезней являются значительные изменения видового состава и количества бактерий кишечника. Известно, что отчасти это может быть связано со сбоями в иммунной системе человека, приводящими к развитию иммунной агрессии в отношении определенных видов бактерий кишечника (в норме отсутствующей).
Введение яиц этого гельминта в кишечник обезьян привело к глобальным перестройкам их микробиома, качественные характеристики которого к окончанию терапии стали напоминать таковые у здоровых обезьян. Более того, отмечалось существенное снижение воспалительных реакций в кишечнике и уменьшение количества бактерий, прикрепленных к пристеночной слизи кишечника. В результате общее состояние обезьян существенно улучшилось, а у большинства из них отмечалось прибавление веса.
Таким образом, авторы показали, что нормализация видового состава микробиома обезьян, страдающих идиопатической хронической диареей, может быть достаточным условием для улучшения состояния их здоровья и предотвращения гибели. В связи с этим, ученые выражают надежду на успех дальнейшего развития данного терапевтического подхода для лечения неспецифического язвенного колита у человека.
К изучению власоглава в качестве терапевтического агента ученые разных лабораторий мира проявляют интерес с 2004 года. Тогда появились первые работы об использовании яиц Trichuris suis (свиного власоглава) для лечения болезни Крона и в меньшей степени неспецифического язвенного колита у свиней. Есть также данные, указывающие на то, что терапия воспалительных заболеваний кишечника с помощью этих гельминтов приводит к снижению заболеваемости астмой, аллергией, и другими болезнями, сопровождающимися воспалительными процессами. Проспективное двойное когортное клиническое исследование, результаты которого были опубликованы в 2007 году (doi:10.1002/ana.21067), свидетельствуют о том, что гельминты даже способны замедлить развитие рассеянного склероза.
Иллюстрации: 1. Власоглав (Trichuris trichiura). 2. Воздействие бактерий на клетки слизистой оболочки кишечника при колите (А) и индукция иммунного ответа Trichuris sp. (В).
Самка, как и у многих других нематод, больше самца. Длина самца 3-4,5 см, самки 3,5-5,5 см. Передний конец тела власоглава тонкий, волосовидный, задний — утолщён. В переднем отделе находится только пищевод, в заднем — все остальные органы. Цвет тела власоглава — от серовато-беловатого до красноватого с поперечной исчерченностью. Локализуется чаще в слепой кишке, иногда в других отделах толстой кишки или в нижней части подвздошной кишки. Власоглав прикрепляется к стенке кишки тонким головным концом тела. Яйца власоглава бочкообразной формы, размер до 23х54 мкм, цвет от светло-коричневого до желтоватого, покрыты скорлупой.
 |
| Власоглав (Trichuris trichiura) |
Яйца власоглава выделяются с фекалиями больных трихоцефалезом. Во время нахождения в почве, под воздействием кислорода и при достаточной влажности воздуха и благоприятных температурных условиях, яйца власоглава созревают. Заражение человека происходит при проглатывании зрелых яиц Trichuris trichiura с загрязненными овощами, фруктами, частицами почвы. В тонкой кишке оболочка яйца разрушается и личинка, благодаря наличию стилета, внедряется в глубокие слои слизистой оболочки, где в течение от трёх до десяти и происходит её дальнейшее развитие после чего личинка выходит в просвет кишки и спускается в слепую кишку, где она за полтора месяца достигает полового созревания. Длительность жизни власоглава в организме человека достигает семи лет.

Жизненный цикл власоглава
Трихоцефалёз (трихуроз)
Для трихоцефалёза характерна боль в животе, чаще в правой подвздошной области, запор или диарея, снижение аппетита, повышенная утомляемость. При количестве паразитов у больного более 1000 возможно изъязвление слизистой толстой кишки, железодефицитная анемия, дизентерия, пролапс (выпадение) прямой кишки, гипоальбуминенмия, раздражительность, головная боль, иногда развиваются судороги или обморочные состояния. B фекалиях больного могут присутствовать прожилки крови и слизи. При тяжелой инвазии симптоматика близка язвенному колиту и болезни Крона.
Диагностируют трихоцефалёз при анализе кала на яйца глистов.
При обнаружении трихоцефалёза проводят лечение больного, а членов семьи обследуют на наличие власоглава. Наблюдение за имеющими близкий контакт с носителем власоглава лицами необходим в течение двух лет. Дважды в год проводится сдача анализов (трехкратно через 15-20 дней) и выборочное исследование санитарно-эпидемиологической службой внешней среды (почвы в микроочаге).
Лечение детей старше двух лет. Альбендазол 400 мг однократно. При интенсивной инвазии (более 1000 паразитов) повторяют в следующие два дня. Или мебендазол по 100 мг два раза в сутки в течение трёх дней.
Яйца гельминтов рода Trichuris, как перспективное средство лечения воспалительных заболеваний кишечника
 |
| Яйца власоглава (Trichuris trichiura) |
Предполагается, что улучшение состояния больных воспалительными заболеваниями кишечника связано с изменением баланса интерлейкинов, синтезируемых Т-клетками слизистой оболочки кишечника. При обострении болезни они выделяют цитокин воспаления ИЛ-17, а ткань, инфицированная нематодами, содержит множество Т-лимфоцитов, синтезирующих ИЛ-22, который участвует в заживлении слизистой оболочки. Организм, пытаясь защититься от гельминта, укрепляет стенку кишечника и его слизистую оболочку, при этом проходят и симптомы болезни.
Следствием приёма яиц Trichuris trichiura является появление в кишечнике больных колоний взрослых гельминтов-паразитов и развитие трихоцефалёза и одновременное существенное уменьшение проявлений воспалительных заболеваний кишечника.
Патент на эту медицинскую технологию был куплен фармацевтической компанией Dr. Falk Pharma GmbH (Германия) и дальнейшие исследования происходили (происходят) при её участии. Однако до настоящего времени метод лечения яйцами Trichuris suis или Trichuris trichiura не получил разрешения на применение в клинической практике.
Trichuris trichiura в систематике эукариот
Разные исследователи придерживаются различных взглядов на систематику червей. По применяемой в США систематике NCBI* вид Trichuris trichiura включён в род Trichuris, который относится к семейству Trichuridae, порядку Trichocephalida, подклассу Dorylaimia, классу Enoplea, типу Нематоды или круглые черви (лат. Nematoda), Линяющие (лат. Ecdysozoa), к Двусторонне-симметричные (лат. Bilateria), подцарству Эуметазои, или настоящие многоклеточные (лат. Eumetazoa), царству Многоклеточные животные (лат. Metazoa), Заднежгутиковые (лат. Opisthokonta), надцарству эукариоты (лат. Eukaryota).
Трихоцефалёз в МКБ-10
Что такое колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Куракина Александра Анатольевича, проктолога со стажем в 11 лет.
Над статьей доктора Куракина Александра Анатольевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Колит (лат. colitis, от греч. kolon (толстый кишечник) и itis (воспаление) — собирательное понятие, включающее большую группу заболеваний с одним общим признаком: воспалением толстого кишечника.
Основные признаки колита: частый жидкий стул с кровью, боль в животе и высокая температура.
Колиты встречаются в практике гастроэнтерологов, инфекционистов, терапевтов, колопроктологов, хирургов и других специалистов.
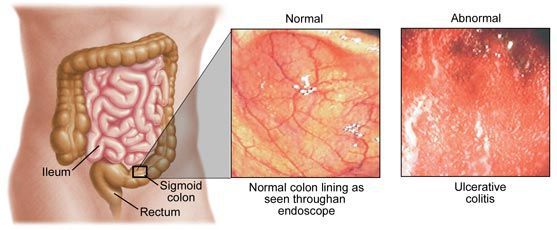
Этиология колита
Основные формы колитов можно описать только по отдельности, в зависимости от этиологического фактора. Размеры статьи не позволяют коснуться всех видов колита. Рассмотрим только основные из них.
Инфекционный колит — это заболевание кишечника, возникающее из-за активизации условно-патогенных микроорганизмов в кишечнике или попадания новых болезнетворных микробов из внешней среды. [1]
Инфекционный колит имеет очень широкое распространение: нет человека, ни разу не переносившего данное заболевание. Количество заболевших увеличивается в жаркий период, когда создаются благоприятные условия для распространения инфекции. Поэтому чаще болеют люди в регионах с жарким климатом (Африка, Юго-Восточная и Средняя Азия). Заболевание чаще встречается в детском возрасте, особенно у детей, посещающих учебные заведения (детские сады, школы и т. д.). Гастроэнтерологи и проктологи могут встречать в практике больных с данной патологией, но она не является профильной. Лечат заболевание обычно инфекционисты.
Причины инфекционного колита:
- бактерии (шигеллы, эшерихии, сальмонеллы, клостридии, иерсинии, брюшнотифозная палочка, кампилобактерии, протей, стафилококки);
- вирусы (аденовирус, энтеровирус, ротавирус);
- простейшие (амебы, лямблии и др.);
- возбудители туберкулеза и сифилиса;
- грибки (кандида, актиномицеты). Возникновение грибкового колита свидетельствует о снижении иммунитета и часто проявляется у лиц, страдающих СПИДом, получающих химиотерапию, стероидные гормоны;
- дисбактериоз.
Формы инфекционного колита:
- катаральная;
- фиброзная;
- катарально-геморрагическая;
- флегмонозная;
- флегмонозно-гангренозная;
- некротическая.
Воспалительные явления могут иметь стадийный характер, а могут сразу иметь картину запущенного воспаления. Его выраженность напрямую зависит от характера инфекции. Некротическое и флегмонозно-гангренозное воспаление встречается при клостридиальной инфекции. Катарально-геморрагическое — при дизентерии. Катаральное воспаление встречается чаще при вирусных заболеваниях. [2]
Ишемический колит — воспаление стенки толстого кишечника, возникающее из-за нарушения процессов кровобращения. Существует хроническое и острое нарушение кровообращения. [3]
Причиной нарушения кровообращения является полное прекращение или критическое снижение притока крови к толстой кишке, вследствие чего возникает воспаление. При тяжёлом течении может приводить к некрозу стенки кишечника. Причиной закупорки сосудов могут быть тромбы, но чаще всего к сужению просвета сосуда приводят атеросклеротические бляшки. Поэтому болезнь чаще проявляется у лиц пожилого возраста. Около 79% больных ишемическим колитом старше 48 лет. [4] Частота встречаемости не имеет связи с половой принадлежностью и регионом. Впервые открыт в 1966 году. Ишемический колит является профильным заболеванием для колопроктологов, но им также занимаются общие хирурги и гастроэнтерологи. [5]
Причины ишемического колита:
-
сосудов;
- закупорка брыжеечных сосудов вследствие эмболии или тромбоэмболии (в результате аллергических реакций, травм, осложнений операций, системного васкулита, ДВС-синдрома);
- снижение давления крови может приводить к нарушению питания стенки кишки.
Закупорка просвета сосуда приводит к ишемии стенки кишки, а как следствие — к некрозу и далее перфорации. [6]
Объём поражения зависит от размера питающей артерии, длительности закупорки. Если закупорка сосуда происходит постепенно (при образовании атеросклеротических бляшек в сосудах), то говорят о хроническом нарушении кровообращения, что в свою очередь приводит к стриктурам.
При критических состояниях и снижении давления крови (например, анафилактический шок, ДВС-синдром и т.д.), происходит централизация кровообращения, при этом резко снижается приток крови к кишечнику, что приводит к ишемии и некрозу.
При атеросклерозе чаще страдает сигмовидная и поперечная ободочная кишка. Воспаление начинается со слизистой оболочки, затем переходит на все слои. [7]
По характеру поражения выделяют:
- транзиторную форму (когда ишемические процессы обратимы);
- стенозирующую (когда формируются стриктуры);
- гангренозную (когда образуются язвы с дальнейшим развитием некроза, поражение носит необратимый характер). [8]
Лучевой колит — образуется в результате ионизирующего воздействия на стенку толстого кишечника.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы колита
Симптомы острого и хронического колита: боль в животе, кровь в кале, диарея, высокая температура, слабость, слизь и кровь в стуле, спазмы.
Симптомы язвенного колита: к перечисленным выше признакам добавляются боли в анусе и анемия.
Боли при колите кишечника:
Инфекционный колит
Клиника инфекционного колита напрямую зависит от возбудителя.
Для любого инфекционного колита независимо от этиологии характерно:
- начало заболевания, как правило, имеет острый характер;
- жидкий частый стул с примесью слизи в кале;
- боли локализуются чаще в левом подреберье, но могут также распространяться по всем отделам живота;
- боль имеет периодический, спазматический характер;
- высокая температура;
- чувство слабости, недомогания;
- сухость кожных покровов и слизистых;
- белый налет на корне языка;
- рвота как первый симптом колита кишечника (если в воспалительный процесс вовлечен желудок).
Для первичной оценки этиологии инфекционного колита оценивают характер дефекации, объём и особенности каловых масс.
Ишемический колит
Симптоматика очень вариабельна, характерно быстрое прогрессирование.
- болезненные ощущения в животе;
- кровь и слизь в стуле;
- неустойчивый, частый стул;
- выраженные боли в околопупочной и левой подвздошной области;
- при ректальном осмотре можно заметить кал с кровью, слизью или гноем;
- при хронической форме боли имеют низкую интенсивность, обычно возникают после еды;
- при длительной хронической ишемии появляются стриктуры в толстой кишке, которые в дальнейшем могут быть следствием непроходимости или малигнизации (раковому перерождению).
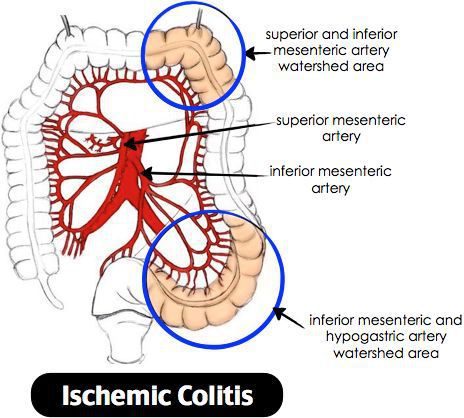
Лучевой колит
Обычно колит формируется у лиц, перенёсших курс лучевой терапии по поводу новообразований, локализующихся в области малого таза или брюшной полости. [12]
- большую чувствительность к излучению имеет тонкий кишечник, формируется лучевой энтерит, который клинически проявляется нарушением абсорбции в тонком кишечнике;
- повреждению кишечника свойствен избирательный характер, обычно воспаление локализуется в прямой и сигмовидной кишке, при этом клиника сопоставима с клиникой язвенного и ишемического колита. При воздействии больших доз радиации клиника развивается не сразу, проявляется обильным, жидким стулом, при этом нарушается всасывание в толстом кишечнике. [13]
Патогенез колита
Толстый кишечник очень восприимчив к ионизирующему излучению. [10] Лучевой колит возникает при воздействии малых доз облучения: происходит атрофия слизистой оболочки (сразу после облучения).
- Усиливаются процессы деления клеток, уменьшается длина ворсинок.
- Активизируются воспалительные процессы с нейтрофильной реакцией. Чаще всего эти процессы локализуются в прямой и сигмовидной кишке.
- При воздействии больших доз (более 40 Гр.) воспалительные процессы могут возникать спустя длительное время после облучения (до нескольких лет), в данной ситуации происходит воспаление мелких сосудов кишечника, что приводит к ишемизации кишечника. Развиваются язвы и стриктуры. Могут поражаться все отделы толстого и тонкого кишечника. [11]
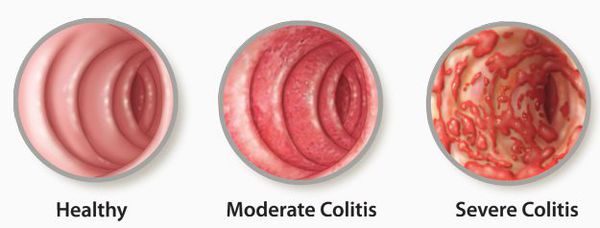
Классификация и стадии развития колита
По течению:
По этиологии:
- язвенный колит кишечника и болезнь Крона (воспалительные заболевания кишечника с неизвестной этиологией);
- инфекционный (этиологический фактор бактериальный, вирусный, грибковый, паразитарный);
- ишемический (развивается вследствие снижения притока крови к толстой кишке);
- спастический (из-за неправильного питания нарушается моторика толстого кишечника и возникают спазмы);
- токсический (при применении нестероидных противовоспалительных препаратов);
- лучевой (при поражении радиацией).
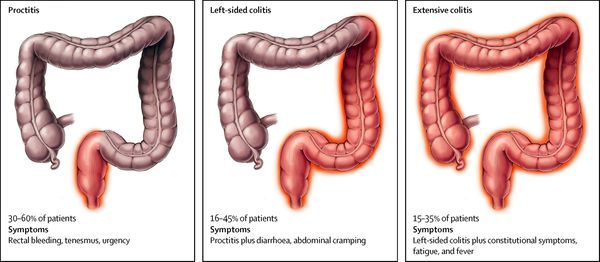
По локализации:
| Вид колита | Локализация |
|---|---|
| проктит | воспаление прямой кишки |
| панколит | тотальное поражение кишечника |
| тифлит | воспаление слепой кишки |
| трансверзит | воспаление поперечной ободочной кишки |
| сигмоидит | воспаление сигмовидной кишки |
| диффузный колит кишечника | охватывает два и более отдела кишечника |
Поражение кишечной стенки подразделяют на три вида:
- катаральный колит кишечника — слабое воспаление, слизистая краснеет, и возникает отёк;
- эрозивный колит кишечника — появляются эрозии;
- атрофический колит кишечника — слизистая атрофируется.
Осложнения колита
- сильное кровотечение;
- перфорация толстой кишки;
- сильное обезвоживание; ;
- воспаление кожи, суставов и глаз;
- повышенный риск рака толстой кишки;
- токсичный мегаколон;
- повышенный риск образования тромбов в венах и артериях [15] .
Диагностика колита
Инфекционный колит:
- Лабораторные методы:
- анализ кала на вирусы, бактерии, паразиты (позволяет точно поставить диагноз);
- серологическое исследование (определяют антитела к вирусам, паразитам);
- анализ крови на стерильность (при подозрении на сепсис);
- общеклинический анализ крови (высокое СОЭ, увеличение количества лимфоцитов при вирусной этиологии).
- Инструментальные методы:
- ректороманоскопия используется как дополнительный метод для дифференциальной диагностики;
- ультразвуковое исследование используется для исключения осложнений.
Ишемический колит:
- Ректороманоскопия дает возможность оценить состояние слизистой оболочки. При осмотре можно отметить наличие точечных кровоизлияний, сглаженность сосудистого рисунка, бледность слизистой. При обнаружении данных признаков показано взятие биопсии.
- Ирригоскопия — самое необходимое исследование. Обнаруживается симптом пальцевых вдавливаний. Признаки дефектов слизистой свидетельствуют о наличии язв, сужения просвета при стриктурах.
- Колоноскопия показана для уточнения распространенности воспаления, также показана биопсия в области измененного участка.
- Ангиография позволяет определить степень сужения сосуда и его локализацию. [9]
- Злокачественные новообразования. Опухоли развиваются достаточно длительное время, в течении многих лет.
- Инфекционный колит. Преобладают симптомы общей интоксикации (слабость, лихорадка и т.д.). Кроме того, имеет место эпидемический анамнез.
- Язвенный колит и болезнь Крона. Для них характерно достаточно медленное прогрессирование. Проявляются обычно в раннем возрасте.
Лучевой колит:
- При сборе анамнеза учитывают наличие факта облучения ионизирующей радиацией.
- Ректороманоскопия и колоноскопия с биопсией позволяют выявить воспаление слизистой оболочки толстого кишечника. При лучевом энтерите воспаление сочетается с атрофией слизистой. Крипты становятся менее глубокими, уменьшается длина ворсинок. При лучевом колите на слизистой обнаруживают язвы, стриктуры. [14]
- Энтерит лучевого генеза следует дифференцировать с болезнями тонкой кишки, при которых страдает функция всасывания (целиакия), при данных заболеваниях происходит атрофия по гиперрегенераторному типу, а при лучевом поражении преобладают гипорегенераторные процессы слизистой.
- Радиационные поражения толстого кишечника дифференцируют с язвенным колитом, болезнью Крона, новообразованиями толстого кишечника. [15]
Лечение колита
Инфекционный колит:
- антибактериальные, противогрибковые средства с учетом чувствительности микроорганизмов. Предпочтение отдают таблетированным формам препаратов;
- восполнение потерянной жидкости и минералов: растворами для приема внутрь (Регидрон и др.), внутривенное введение (раствор Рингера, Трисоль и др.);
- прием сорбентов;
- пробиотики и пребиотики;
- ферменты (креон, фестал);
- симптоматическая терапия (противовоспалительные средства, спазмолитики и др.)
Ишемический колит:
- консервативное лечение колита (щадящая диета, препараты, смягчающие стул, лекарства для улучшения кровотока, дезагреганты, витаминные препараты, дезинтоксикационное лечение, восполнение баланса электролитов и жидкости, гемотрансфузии (при показаниях), антибактериальные препараты);
- оперативное лечение колита.
Показаниями для срочного хирургического лечения служат:
- перфорация, толстокишечная непроходимость. В таком случае удаляется участок кишки, с последующей санацией и дренированием брюшной полости.
- плановое оперативное лечение колита кишечника показано больным в случае сужения (стриктуры) толстого кишечника без явлений острой кишечной непроходимости.
Терапия лучевого колита схожа с терапией язвенного колита и болезни Крона:
- лекарства, содержащие 5-аминосалициловую кислоту (месалазин, салофальк);
- антибактериальная терапия.
Может быть полезно вести дневник питания, чтобы отслеживать, что вы едите, а также свои чувства. Если вы обнаружите, что некоторые продукты вызывают обострение ваших симптомов, вы можете попробовать их устранить.
Диетотерапия
Убедительных доказательств того, что неправильное питание приводит к воспалению кишечника, нет. Но оно может усугубить симптомы болезни, особенно при обострении. Поэтому полезно вести дневник питания и отслеживать свои реакции на определённые продукты.
- есть меньше молочных продуктов — у пациента может быть непереносимость лактозы, т. е. организм не переваривает молочный сахар;
- есть небольшими порциями по 5–6 раз в день;
- пить больше жидкости — предпочтительнее вода; алкоголь и напитки, содержащие кофеин, стимулируют кишечник и могут усилить симптомы болезни [15] .
Прогноз. Профилактика
На сегодняшний день хорошо известны причины возникновения инфекционного колита, разработаны современные методики лечения. Поэтому при неосложненном течении и вовремя начатой терапии удается достигнуть полного выздоровления. Менее благоприятный прогноз у лиц с явлениями иммунодефицита и ослабленной иммунной системой (например, у людей пожилого возраста). Прогноз благоприятный.
Основными методами профилактики являются:
- гигиенические мероприятия (тщательное мытье рук);
- использование только свежих продуктов, чистой воды;
- уделение особого внимания термической обработке пищи.
При транзиторной форме ишемического колита прогноз благоприятный. При гангренозной форме — зависит от вовремя поставленного диагноза и проведенного лечения.
Так как ишемический колит является осложнением других болезней, то для его профилактики необходимо:
- своевременное лечение сопутствующих заболеваний;
- сбалансированное питание.
Лучевой колит приводит к постоянным, необратимым изменениям кишечной стенки, поэтому прогноз неблагоприятный.
При радиационном колите могут появляться язвы и стриктуры на слизистой оболочке толстого кишечника, что может привести к кишечной непроходимости. В таком случае необходимо хирургическое лечение, от своевременности которого зависит прогноз. При правильном и вовремя проведенном лечении прогноз благоприятный. Специальных методов профилактики лучевого колита не существует.
Что такое псевдомембранозный колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Аверина Александра Анатольевича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Аверина Александра Анатольевича работали литературный редактор Вера Васина , научный редактор Роман Васильев и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Псевдомембранозный колит (Pseudomembranous colitis) — это острое воспалительное заболевание толстого кишечника, вызываемое токсигенными штаммами бактерии Clostridium difficile [1] . Микроб вырабатывает токсины А и В, повреждающие кишечную стенку, и белок, угнетающий перистальтику кишечника. В результате возникает диарея, боль в животе, появляется слизь и иногда примесь крови в кале.
Характерным признаком заболевания являются фиброзные наложения на слизистой оболочке толстой кишки [27] [28] .

Псевдомембранозный колит (ПМК) чаще всего развивается после лечения антибиотиками. Его ещё называют Clostridium difficile-ассоциированным псевдомембранозным колитом, антибиотик-ассоциированным псевдомембранозным и клостридиозным колитом.
Эпидемиология
Заболеваемость ПМК лучше всего отслеживается в США и странах западной Европы [2] . В России статистический учёт заражения C. diff не ведётся. Согласно систематическому обзору за 2011 год, каждый 5-й случай из всех антибиотик-ассоциированных диарей (ААД) и каждый 2–3 случай внутрибольничной ААД в странах Европы и Северной Америки вызваны C. diff [3] .
В стационарах США среди внутрибольничных инфекций C. diff занимает первое место (12,1 % от общего количества), опережая K. pneumoniae (9, 7 %) и E. coli (9,3 %) [4] . В 2011 г. было зафиксировано более 450 тыс. случаев C. difficile-ассоциированной болезни и более 29 тыс. смертей от неё [29] .
В европейских странах заболеваемость C. diff составляет около 7 случаев на 10000 койко-дней, т. е. при средней госпитализации 10 дней, 7 случаев из 1000 госпитализаций заканчиваются ПМК. В 20 европейских странах это значение колеблется от 0,7 до 28,7 на 10000 койко-дней [5] .
В России в 2011 году было продано 295 млн упаковок антибиотиков, в 2019 — 379 млн [8] [26] . Антибактериальных препаратов потребляется всё больше, их продажа из аптек не контролируется, поэтому проблемы ААД и ПМК актуальны и в нашей стране.
В клиниках Санкт-Петербурга у пациентов с ААД тест на токсины C. diff был положительным в 47,7 % случаев [6] .
Смертность от ПМК колеблется от 9,3 до 22 % и зависит от возраста пациента, смерть чаще наступает при тяжёлом течении заболевания [7] [26] .
В настоящее время увеличилась внутри- и внебольничная заболеваемость C. difficile-ассоциированной болезнью, расширились группы риска, стали чаще встречаться рецидивы и тяжёлые формы, в том числе вызванные более патогенным штаммом BI/NAP1/027, возросла смертность [27] .
Причины псевдомембранозного колита
Основная причина болезни — это приём антибиотиков. ПМК могут вызывать любые антибактериальные препараты, но наиболее часто к нему приводит применение Клиндамицина, хинолонов, цефалоспоринов 2-го и 3-го поколения, карбапенемов. Реже ПМК развивается после приёма макролидов, пенициллина, Тетрациклина, Тигециклина.
К факторам риска, помимо приёма антибиотиков, относятся:
- возраст старше 65 лет;
- терапия ингибиторами протонной помпы и Н2-гистаминоблокаторами — препаратами, снижающими секрецию соляной кислоты в желудке;
- лечение в стационаре, особенно в отделениях реанимации, — каждые 7 дней госпитализации увеличивают риск ПМК на 8 % [1][9][10] ;
- наличие дополнительной патологии, в том числе воспалительных заболеваний кишечника, ВИЧ, сахарного диабета[31][32][33] ;
- хирургические вмешательства на органах ЖКТ;
- энтеральное питание, в том числе через назогастральный зонд;
- приём иммуносупрессивных препаратов (глюкокортикостероидов, Такролимуса) и противоопухолевых средств [31] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы псевдомембранозного колита
Наиболее частые симптомы лёгкого или умеренного псевдомембранозного колита:
- водянистая диарея (жидкие испражнения, похожие на кашицу) от трёх раз в сутки на протяжении двух и более дней в сочетании с болью в животе;
- лёгкие спазмы в животе, часто сопровождающиеся с позывами на стул, но не всегда приводящие к дефекации;
- примеси слизи, крови или гноя в испражнениях;
- температура тела 38,5 °С и более;
- тошнота или потеря аппетита.
При тяжёлом течении псевдомембранозного колита возникает водянистая диарея с кровью, уровень альбумина снижается менее 30 г/л, что сочетается с одним из следующих симптомов: высоким уровнем лейкоцитов в клиническом анализе крови (> 15×10 9 /л) и/или болезненностью при ощупывании живота. На фоне длительной диареи организм теряет много жидкости, что приводит к обезвоживанию и проявляется тёмно-жёлтой мочой, чувством жажды, усталости, головокружением, спутанностью сознания и заторможенностью [1] [9] .
При рецидиве болезни симптомы появляются повторно менее чем через 8 недель после окончания терапии.
Проявления псевдомембранозного колита схожи с симптомами других инфекций, поражающих толстый кишечник. Но в отличие от них признаки ПМК могут быть слабо выражены и, как правило, наблюдаются долго: от одной недели до нескольких месяцев. Также встречаются случаи, когда человек является носителем возбудителя ПМК — C. diff, но симптомы полностью отсутствуют.
Патогенез псевдомембранозного колита
В основе патогенеза ПМК лежит чрезмерное размножение бактерий C. diff на фоне уменьшения или гибели нормальной микробиоты толстого кишечника. C. diff вырабатывает токсины А и В, которые вызывают воспаление в кишечной стенке. На течение заболевания влияет состояние иммунной системы пациента и патогенные свойства бактерий, такие как вирулентность, наличие токсинов А и В.
Основной путь передачи инфекции — фекально-оральный. Бактерии попадают в организм с загрязнённых поверхностей, например с дверных ручек, смесителей, ручек смыва сливного бачка, мебели или медицинского инвентаря. Также переносить инфекцию может персонал больницы и заражённые пациенты.
Бактерии C.diff образуют споры, которые устойчивы к действию антибиотиков и могут длительно сохраняться в желудочно-кишечном тракте человека, заражая окружающих и вызывая рецидивы заболевания у самого пациента [12] .
Для некоторых людей C.diff — это часть нормальной микрофлоры ЖКТ, но в таком случае численность бактерий контролируется за счёт других микроорганизмов и работы иммунной системы.
Основные поражающие факторы C.diff — это выделяемые ею токсины [1] . Токсин А (энтеротоксин, белковая молекула с массой 308 кДа) влияет на секрецию жидкости, приводит к повреждению слизистой оболочки кишечника (мембран клеток) и вызывает воспалительный ответ со стороны иммунной системы.

Токсин В (цитотоксин, белковая молекула с массой от 250 до 270 кДа) в 1000 раз более цитотоксичен по сравнению с токсином А. Он вызывает распад филаментного актина — белка, поддерживающего целостность клеток. В результате клетки слизистой разрушаются и гибнут. Токсин В опасен для человека, но не приводит к воспалению и повреждению слизистой оболочки кишечника у животных.
Под действием токсинов в кишечной стенке развивается специфическое воспаление с характерными изменениями на поверхности слизистой. Она становится отёчной, разрыхляется, приобретает ярко-красный цвет, на ней исчезает сосудистый рисунок. При контакте эндоскопа со слизистой капельки крови не появляются. Наблюдается множество желтовато-белых бляшек диаметром 3–5 мм, которые плотно фиксированы к слизистой оболочке. При взятии биопсии они отрываются с трудом, торцом эндоскопа не снимаются. Преобладает два типа воспалительных реакций: диффузно-катаральное воспаление слизистой и очаги фибриноидного некроза — бело-жёлтые бляшки, или псевдомембраны, поэтому такой тип колита называется псевдомембранозным.
![Бляшки при ПМК [35]](https://probolezny.ru/media/bolezny/psevdomembranoznyy-kolit/blyashki-pri-pmk-35_s.jpg)
В биоптатах, полученных из воспалительно-изменённых участков слизистой, выявляют скопление иммунных клеток крови и слизистой, расширение капилляров и некроз клеток покровного эпителия [1] .
В биоптатах, взятых из бляшек, присутствует фибрин, обрывки некротизированного покровного эпителия, слизь, лейкоциты, плазматические клетки и колонии бактерий.
Чтобы определить патогенность клостридий, нужно выявить их токсины. Посев биоптатов на питательные среды удовлетворительных результатов не даёт. Метод в данном случае затратен и неинформативен, поэтому токсины C. diff определяют в кале.
Воспалительный процесс, как правило, захватывает несколько отделов толстого кишечника, но чаще поражена его прямая и сигмовидная часть, реже вовлекается вся толстая кишка. Протяжённость её поражения связана с тяжестью течения заболевания: чем больше толстого кишечника вовлечено в воспалительный процесс, тем тяжелее протекает колит и ярче симптомы.
Продолжительное воспаление в кишечной стенке приводит к следующим нарушениям:
- не всасывается жидкость, из-за чего развивается обезвоживание;
- потери крови из образующихся эрозий и язв приводят к анемии;
- кишечная стенка становится проницаемой для токсинов возбудителя и продуктов его жизнедеятельности, находящихся в просвете кишки, из-за чего нарастает общая интоксикация.
При тяжёлом течении прекращается перистальтика толстого кишечника, развивается токсический мегаколон и возникает полиорганная недостаточность, из-за чего пациент может погибнуть.
Классификация и стадии развития псевдомембранозного колита
ПМК входит в группу антибиотик-ассоциированных диарей. В Международной классификации болезней (МКБ-10) псевдомембранозный колит кодируется как АО 4.7 — Энтероколит, вызванный Clostridium difficile.
В зависимости от тяжести течения болезни и клинической картины выделяют следующие формы:
- ПМК лёгкой или умеренной тяжести. Проявляется диареей — неоформленным жидким, кашицеобразным стулом три или более раз в сутки и болью в животе.
- ПМК тяжёлого течения. Сопровождается водянистой диареей с кровью и изменениями в анализах. В биохимическом анализе крови отмечается низкий уровень альбумина (меньше 30 г/л), который сочетается с одним из следующих признаков: высоким уровнем лейкоцитов в клиническом анализе крови (> 15×10 9 /л) в клиническом анализе крови и/или болезненностью при ощупывании живота.
- Осложнённые формы ПМК. Протекают с водянистой диареей с кровью и одним из следующих симптомов: снижение артериального давления, температура тела ≥ 38,5 °C, отсутствие перистальтики тонкого кишечника, помрачение или угнетение сознания. В клиническом анализе крови лейкоциты повышены > 25×10 9 /л или снижены < 2×10 9 /л, возникает органная и почечная недостаточность, требуется искусственная вентиляция лёгких.
- Рецидивирующее течение ПМК. Заболевание развивается повторно менее чем через 8 недель после окончания терапии [1][14] .
Данная классификация используется для выбора схемы лечения.
Осложнения псевдомембранозного колита
Наиболее частые осложнения псевдомембранозного колита:
- Обезвоживание и электролитные нарушения — из-за сильной и длительной диареи нарушается ритм сердца, снижается артериальное давление и мышечный тонус. Чаще эти осложнения развиваются при недостаточном восполнении потерянной жидкости и солей.
- Почечная недостаточность — при стремительном обезвоживании нарушается работа почек, из-за чего снижается частота мочеиспусканий, появляются отёки, по анализам крови видно, что растёт содержание азотистых шлаков.
- Токсический мегаколон — расширение толстой кишки, редкое осложнение с плохим прогнозом. На фоне диареи частота стула резко урежается до одного раза в сутки, в дальнейшем дефекация прекращается полностью. Это происходит из-за замедления и полного прекращения перистальтики толстого кишечника. Из-за распирания толстого кишечника газами и содержимым нарастает вздутие живота, усиливается боль в нём. Интоксикация и электролитные нарушения приводят к резкому ухудшению самочувствия и выраженной слабости. В дальнейшем стенка кишки разрывается, содержимое изливается в брюшную полость (перфорация кишечника) и начинается перитонит. Как правило, это осложнение наблюдается у ослабленных пациентов, находящихся в отделении реанимации и хирургии.
- Перфорация кишечной стенки — образуется сквозное отверстие в кишечной стенке с излитием содержимого кишечника в брюшную полость и развитием перитонита.
- Полиорганная недостаточность — может привести к гибели пациента [1][15] .
Диагностика псевдомембранозного колита
Тесты на C. diff показаны при длительной диарее с болью в животе и/или примесью крови в стуле, возникшей спустя 3–60 суток после выписки из стационара и/или после приёма антибиотиков [1] .
Чтобы выявить токсигенные штаммы C. diff, токсины A и B определяют в кале [16] .
Для этого используют следующие методы:
- Цитотоксиновый копрологический тест. Чувствительность — 95 %, специфичность — 99 %, результат — в течение 2–3 дней.
- ELISA (Enzyme Linked Immuno Sorbent Assay) — фермент-связанный иммуносорбентный тест для определения токсинов. Чувствительность — 70–90 %, специфичность — 99 %, результат — через 4–6 часов.
- ПЦР (полимеразная цепная реакция) на токсин В. Чувствительность — 96 %, специфичность — 100 %, результат — в течение нескольких часов.
Чувствительность теста — это доля положительных результатов среди больных людей, т. е. вероятность правильно определить инфекцию у заболевших, отсутствие ложноотрицательных результатов. Специфичность — доля отрицательных результатов среди здоровых людей, т. е. отсутствие ложноположительных результатов.
Посев кала на C.diff не проводится, так как этим методом не удаётся определить токсигенные штаммы.
С помощью дополнительных методов можно оценить тяжесть состояния пациента и своевременно выявить осложнения.
К дополнительным обследованиям относятся:
- ректороманоскопия или сигмоидоскопия — позволяют обнаружить типичные изменения стенки кишки (множественные желтоватые бляшки 2–10 мм в диаметре, плотно фиксированные на поверхности слизистой оболочки);
- колоноскопия — помимо типичных изменений кишечной стенки, определяется распространённость процесса и поражение толстого кишечника выше сигмовидной кишки [17] ;
- обзорная рентгенография органов брюшной полости — используется, чтобы выявить признаки пареза кишечника и токсического расширения кишки;
- анализ крови — показывает уровень лейкоцитов (при ПМК повышен до 10–50 × 10 9 ), уровень креатинина (выше нормы) и альбумина (ниже нормы).
Гистологическое исследование биоптатов не является необходимым при C. difficile-ассоциированной болезни, но может быть крайне важным для дифференциальной диагностики.
Лечение псевдомембранозного колита
Методы лечения псевдомембранозного колита в российских и зарубежных клинических рекомендациях совпадают [1] [18] . При лёгком и среднетяжёлом течении его проводят в амбулаторных условиях (дома), при тяжёлом и/или осложнённом — в стационаре.
Для лечения ПМК назначаются антибиотики:
Антибиотики подавляют развитие C. diff. Бактерия чувствительна только к трём перечисленным антибактериальным препаратам.
При развитии осложнений ПМК могут применяться следующие методы:
- При токсическом мегаколоне показана колэктомия — удаление толстой кишки.
- Для лечения рецидивирующего ПМК в качестве экспериментального метода рассматривается трансплантация кишечной микробиоты (fecal microbiota transplantation, FMT) [23][24][25] . Кишечную микробиоту берут от здорового донора и при помощи назоинтестинального зонда, клизмы или колоноскопии переносят пациенту в кишечник. В России такое лечение считается экспериментальным. Проводится в научных клинических учреждениях, например в Федеральном научно-клиническом центре ФМБА России.

В качестве вспомогательных и симптоматических препаратов используются:
- Сорбенты (Диоктаэдрический смектит) — эффективно удаляет токсины C. diff, снижая их действие на кишечную стенку, улучшает качество стула.
- Пробиотики (Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium bifidum, Bifidobacterium infantis не менее 1×10 9 КОЕ/г) — подавляют активность C. diff. Данные об их эффективности пока противоречивы [22] .
- Препараты на основе дрожжей Saccharomyces cerevisiae (boulardii) — эффективны как вспомогательные и профилактические средства.
Прогноз. Профилактика
При лёгком или среднетяжёлом течении ПМК и хорошей реакции на стандартную терапию прогноз благоприятный, при тяжёлом и осложнённом — неблагоприятный. При рецидивирующем течении прогноз сомнительный, так как не разработаны эффективные схемы лечения.
Профилактика псевдомембранозного колита
Для профилактики развития ПМК следует:
- чаще мыть руки и соблюдать правила личной гигиены;
- рационально принимать антибиотики — строго по назначению врача с соблюдением всех указаний;
- изолировать пациентов с инфекцией C. diff в отдельные палаты, соблюдать меры санитарного режима;
- тщательно обрабатывать все поверхности хлорсодержащими или другими дезинфицирующими средствами, активными против спор C. diff;
- сокращать сроки госпитализации пациентов старше 65 лет [16] .
Чтобы предотвратить рецидив C. difficile-ассоциированной болезни, после завершения лечения Метронидазолом или Ванкомицином назначаются пробиотики курсом не менее трёх месяцев. Серьёзных побочных эффектов от них не выявлено [34] .
Читайте также:

