Волчанка и отказала одна почка
Обновлено: 25.04.2024
Появление острой боли в области почек практические всегда указывает на наличие определенной проблемы со стороны мочевыделительной системы организма человека. Она может возникнуть внезапно, на фоне абсолютного благополучия. Может сопровождать различные хронические заболевания.
Почки – это парный паренхиматозный орган, имеющий бобовидную форму. Многие считают, что почки отвечают только за выработку мочи. На самом деле, они играют гораздо более важную роль в теле человека:
- Выводят из организма вредные токсины;
- Участвуют в поддержании водно-электролитного баланса в организме;
- Вырабатывают эритропоэтин – гормон, стимулирующий кроветворение;
- Вырабатывают витамин D;
- Участвуют в регуляции артериального давления и т.д.
Каждый год в России от болезней почек страдает около 4%-6% населения, причем большинство нефрологических пациентов являются женщинами. Не стоит забывать, что большая часть патологий почек представляют собой реальную угрозу для здоровья пациента и могут приводить к летальному исходу. Зачастую, болезни почек протекает бессимптомно, поэтому, даже появление незначительной боли в области почки слева или справа, должно стать веской причиной для обращения к специалисту.
Специалисты Юсуповской больницы занимаются диагностикой и лечением пациентов с различными заболеваниями органов мочевыделительной системы. Больница оснащена новейшим оборудованием, позволяющим обследовать каждого больного с помощью инновационных методик. В клинике терапии работают врачи высшей категории, являющиеся признанными специалистами в области нефрологии. В сложных медицинских случаях, пациента всегда проконсультирует консилиум докторов больницы во главе с профессором. Юсуповская больница располагает к себе не только своим высококвалифицированным медицинским персоналом, но и комфортными условиями пребывания.
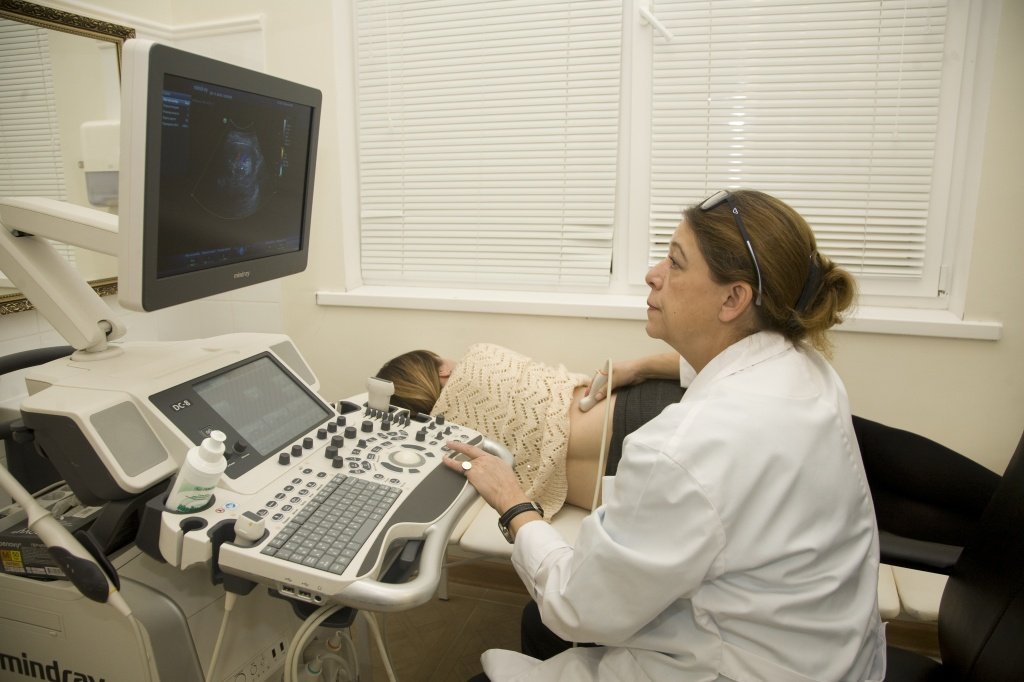
Боль в области почек: причины
Появлению болей в области почек могут предшествовать разнообразные факторы, как инфекционной, так и неинфекционной природы. Среди самых распространенных причин, которые могут вызывать боль в области левой и правой почки следует перечислить следующие:
Острая почечная недостаточность
Острая почечная недостаточность (ОПН) – это состояние, при котором внезапно резко нарушаются все внутрипочечные функции: кровообращение и гидродинамика, клубочковая фильтрация, канальцевая секреция и реабсорбция (обратное всасывание жидкости). В организме пациента происходят следующие изменения:
- Повышение уровня азота в крови;
- Глубокие нарушения водно-электролитного обмена, кислотно-основного состояния;
- Повышение артериального давления;
- Малокровие.
- Причины, по которым развивается острая почечная недостаточность, разделяют на 3 основные группы:
- Преренальная – снижение почечного кровотока;
- Ренальная – непосредственное повреждение паренхимы почек;
- Постренальная – закрытие просвета мочевыводящих путей.
С помощью изменения сопротивляемости приносящих и выносящих клубочковых артериол интенсивность почечного кровотока и скорость клубочковой фильтрации остаются на одном уровне даже во время большого колебания среднего артериального давления. Если артериальное давление ниже 70 мм рт.ст., саморегуляция нарушается, и скорость клубочковой фильтрации уменьшается пропорционально его снижению. Почечная саморегуляция зависит от комбинации расширения приносящих артериол, которую вызывают оксид азота и простагландины, и сужения выносящих артериол под воздействием ангиотензина-2.
Лекарственные препараты, которые взаимодействуют с этими медиаторами (нестероидные противовоспалительные средства или селективные ингибиторы ЦОГ-2, ингибиторы АПФ или АРА), способны в определённых клинических ситуациях вызвать преренальную острую почечную недостаточность. В группу риска входят лица пожилого возраста с атеросклеротическим кардиосклерозом, пациенты, страдающие хроническими заболеваниями почек и со сниженной перфузией почки, которая вызвана обезвоживанием, сужением почечной артерии или гипотензией.
Ранние признаки острой почечной недостаточности часто минимальные и непродолжительные:
- Циркуляторный коллапс, эпизод острой сердечной недостаточности при преренальной ОПН;
- Почечная колика при постренальной острой почечной недостаточности;
- Острый гастроэнтерит при отравлении солями тяжелых металлов;
- Местные и инфекционные проявления при множественной травме.
- Многие симптомы начальной стадии острой почечной недостаточности (отсутствие аппетита, слабость, сонливость, тошнота) неспецифичны. Поэтому врачи Юсуповской больницы для ранней диагностики ОПН применяют лабораторные методы: определение уровня креатинина, калия и мочевины в крови.
- К признакам клинически развёрнутой острой почечной недостаточности относятся симптомы выпадения гомеостатической функции почек:
- Острые нарушения кислотно-основного состояния и водно-электролитного обмена;
- Нарастающая азотемия (повышение уровня азота в крови);
- Поражение лёгких, органов пищеварения, центральной нервной системы (уремическая интоксикация);
- Острые грибковые и бактериальные инфекции.
Олигурия с диурезом менее 500 мл обнаруживается у большинства пациентов с ОПН. У 3-10% больных развивается анурическая острая почечная недостаточность, при которой диурез менее 50 мл в сутки. К олигурии и особенно анурии могут быстро присоединиться симптомы внеклеточной (полостные и периферические отёки), затем внутриклеточной гипергидратации (отёк мозга, лёгких, острая левожелудочковая недостаточность).
Кардинальным признаком ОПН является азотемия – повышение концентрации азота в крови. Её выраженность отражает тяжесть острой почечной недостаточности. При ОПН азотемия нарастает быстро. При некатаболической форме ОПН ежесуточный прирост уровня мочевины крови составляет 10-20 мг%, а креатинин увеличивается на 0,5-1 мг%.
Для лечения постренальной острой почечной недостаточности урологи устраняют обструкцию и восстанавливают нормальный пассаж мочи. После этого постренальная ОПН в большинстве случаев ликвидируется. Если, несмотря на восстановление проходимости мочеточников, сохраняется анурия, применяют диализные методы терапии.
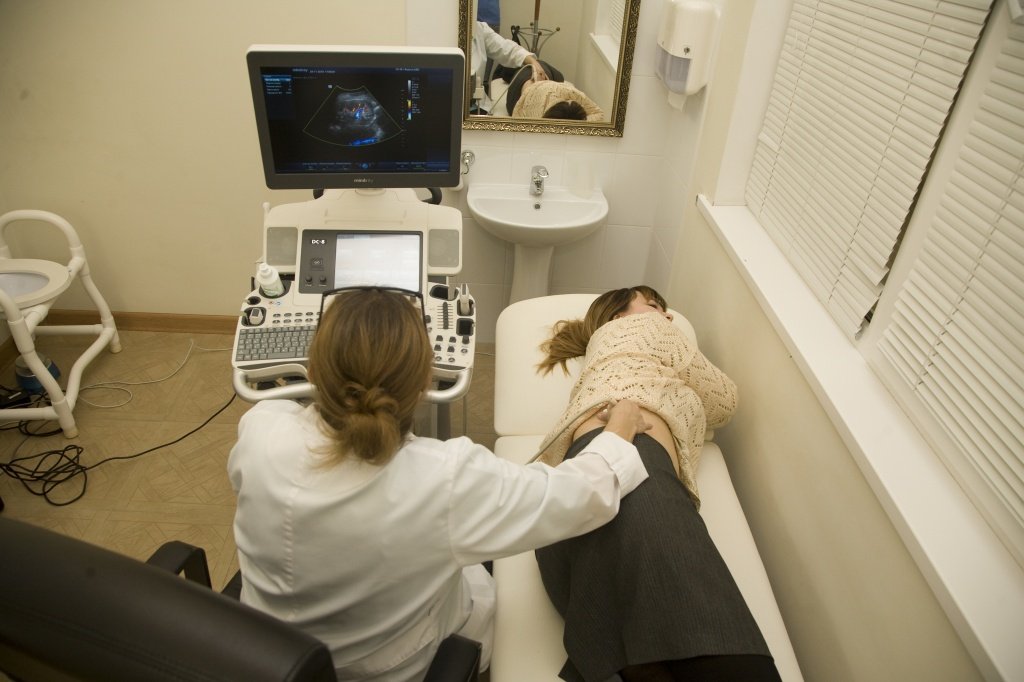
При диагностированной преренальной острой почечной недостаточности врачи направляют усилия на устранение факторов, которые вызвали острую сосудистую недостаточность или гиповолемию, отменяют лекарственные средства, индуцирующие преренальную ОПН. Для выведения из шока и восполнения объема циркулирующей крови внутривенно вводят большие дозы кортикостероидов, крупномолекулярные декстраны (полиглюкин, реополиглюкин), плазму, раствора альбумина. При кровопотере переливают эритроцитную массу.
Если причиной ОПН является гипонатриемия и дегидратация, внутривенно вводят солевые растворы. Все виды трансфузионной терапии врачи отделения реанимации и интенсивной терапии проводят под контролем диуреза и уровня центрального венозного давления. После стабилизации артериального давления и восполнения внутрисосудистого русла переходят на внутривенное, длительное введение фуросемида с допамином.
Нефрологи Юсуповской больницы проводят лечение ренальной ОПН по стадиям. При развитии олигурии у пациентов с уратным кризом, миеломной болезнью, гемолизом (распадом эритроцитов), рабдомиолизом проводят непрерывную длительную инфузионную ощелачивающую терапию. Она включает введение маннитола с изотоническим раствором хлорида натрия, глюкозы с фуросемидом и бикарбоната натрия. Такая терапия предотвращает внутриканальцевое осаждение цилиндров и обеспечивает выведение свободного миоглобина, гемоглобина, мочевой кислоты.
На ранней стадии ренальной ОПН, в течение первых двух-трёх суток развития острой клубочковой недостаточности, при отсутствии полной анурии и гиперкатаболизма проводят лечение фуросемидом, маннитолом, инфузией жидкостей. Свидетельством эффективности консервативной терапии является увеличение диуреза с ежедневным снижением массы тела на 0,25-0,5 кг. Потеря массы тела пациента более 0,8 кг/сутки, сочетающаяся с нарастанием уровня калия в крови является тревожным признаком гипергидратации, которая требует ужесточения водного режима.
Пациентам с некоторыми вариантами ренальной ОПН базисную консервативную терапию дополняют антибиотиками, иммунодепрессантами, плазмаферезом. Если ОПН вызвана сепсисом или токсическими веществами, используют гемосорбцию, которая обеспечивает удаление из крови токсинов. Консервативная терапия при отсутствии эффекта в течение 2-3 суток является бесперспективной и опасной ввиду увеличения риска осложнений от применения больших доз фуросемида (нарушение слуха) и маннитола (гиперосмолярность, острая сердечная недостаточность, гиперкалиемия). В этом случае применяют диализное лечение. Для того чтобы пройти лечение и обследование ОПН, звоните по телефону контакт центра.
Боль в области почек: диагностика и лечение
При проведении дифференциальной диагностики различных заболеваний, вызывающих боли в области почек, начальным этапом является сбор подробного анамнеза пациента и общий осмотр. Во время общего осмотра пациента, особое внимание следует уделить отекам. Проверяют симптом Пастернацкого с обеих сторон, чтобы определить насколько сильной проявляется боль в области почек. Также, измеряется артериальное давление и определяется частота сердечных сокращений.
Для постановки точного диагноза используют – дополнительные метод диагностики. К данным методам относятся:
- Забор крови на ОАК, биохимию;
- ОАМ;
- Анализ мочи по Нечипоренко;
- Проба Зимницкого и Реберга;
- Биопсия почек, позволяющая определить морфологический вид заболевания.
Лечение болей в области почек непосредственно зависит от того, что спровоцировало причину ее возникновения. Если заболевание инфекционной этиологии, то пациенту требуется назначение в терапию антибиотиков и антисептических препаратов. В некоторых ситуациях применяют мочегонные средства. Некоторые тяжелые патологии требуют оперативного вмешательства, например, если речь идет об опухолях почек.

При затяжном приступе почечной колики пациенту выполняют новокаиновую блокаду семенного канатика или маточной связки со стороны поражения.
Врачи Юсуповской больницы индивидуально для каждого пациента подбирают терапию: лекарственные средства, их дозировку, курс лечения. На всех этапах лечения пациента курируют множество специалистов различных узких специальностей. В клинике больному предоставят не только хорошее медицинское обслуживание, но и психологическую поддержку. Запишитесь на прием к врачу-нефрологу по телефону, указанному на сайте.
Диагноз системной красной волчанки (СКВ) в последние десятилетия стал все чаще встречаться в нефрологическом стационаре. Судить о том, насколько актуальна проблема СКВ, можно хотя бы на основании того, что статья
Системная красная волчанка — аутоимунное заболевание, характеризующееся изменениями со стороны клеточного и гуморального иммунного ответа. Фундаментальным нарушением в иммунной системе у больных с СКВ в настоящее время принято считать генетически обусловленный дефект апоптоза (программированной смерти) аутореактивных клонов Т- и В-клеток. В индукции заболевания помимо генетических факторов важную роль играет уровень половых гормонов. Отрицательное влияние эстрогенов подтверждается развитием заболевания преимущественно у женщин детородного возраста, высокой частотой дебюта и/или обострения заболевания после родов и абортов, а также низким уровнем тестостерона и повышенным — эстрадиола у мужчин с СКВ. Среди экзогенных факторов большое значение придается ультрафиолетовому облучению, бактериальным липополисахаридам и различным группам вирусов, активирующих В-клетки, и применению некоторых лекарственных препаратов, в особенности гормональных контрацептивов.
Потеря иммунной толерантности к собственным, в первую очередь ядерным, антигенам приводит к продукции множества комплемент-связывающих аутоантител к компонентам клеточного ядра, цитоплазмы и мембран, в частности к двухцепочечной ДНК и нуклеосомам. Аутоантитела оказывают как прямое повреждающее действие на различные органы и ткани, так и опосредованное — через формирование иммунных комплексов и активацию системы комплемента. Характерно также не только иммунокомплексное, но и тромботическое поражение сосудов, последнее обусловлено наличием антител к кардиолипину, а также развитием антифосфолипидного синдрома (АФС) и вторичного ДВС. Таким образом, системные повреждения имеют смешанный (цитотоксический, иммунокомплексный и тромботический) генез.
Прогрессирующее поражение жизненно важных органов — почек, центральной нервной системы, сердца, легких, системы крови — определяет тяжесть и прогноз заболевания. Поражаются также и другие органы, суставы, серозные оболочки, кожа. Характерной особенностью СКВ является тот факт, что даже через много лет после начала заболевания процесс сохраняет свою активность.
Диагноз устанавливается при наличии четырех и более из следующих клинических и серологических критериев (критерии Американской ревматологической ассоциации, 1982):
Системный характер заболевания и вовлечение почек в патологический процесс именно в период его максимальной активности приводят к тому, что в большинстве случаев в нефрологической клинике приходится сталкиваться с разнообразными экстраренальными проявлениями СКВ (см. таблицу 1). К ним относятся легочные инфильтраты и альвеолярные кровотечения, цереброваскулит и поперечная миелопатия, тромботические поражения сосудов легких, конечностей, кишечника, головного мозга, эндо-, мио- и перикардит, поражения печени, суставов, тромбоцитопения, анемия, лимфоаденопатия, серозиты, разнообразные кожные проявления и другие симптомы. Наибольшее прогностическое значение имеют поражения ЦНС и легких.
Вовлечение центральной и периферической нервной системы при СКВ встречается довольно часто — до 50% случаев. Отмечаются цереброваскулит, двигательные нарушения, моно- и полинейропатия, асептический менингит, острые психозы, цефалгии, дисфория, судороги. Поперечная миелопатия представляет собой хотя и довольно редкое — 1—3%, но прогностически неблагоприятное и плохо поддающееся терапии проявление заболевания.
Поражение легких чаще всего отмечается в виде пульмонита и тромбоэмболии легочной артерии (ТЭЛА). Диффузные альвеолярные кровотечения развиваются менее чем у 2% больных с СКВ, смертность при этой патологии составляет 70—90%.
Большое значение придается в настоящее время антифосфолипидному синдрому. В рамках АФС рассматриваются такие проявления заболевания, как поражения клапанов сердца, тромбозы коронарных артерий, тромботическая легочная гипертензия, пурпура и язвы голеней, синдром Эванса (сочетание гемолитической анемии с тромбоцитопенией), синдром Снеддона (артериальная гипертензия, рецидивирующие тромбозы мозговых артерий и мраморный рисунок кожи).
Среди поражений сердца наиболее часто встречается перикардит (до трети случаев), причем среди пациентов с активной стадией заболевания распространенность перикардита еще выше — он отмечается более чем у половины больных. У некоторых из них перикардит оказывается первым проявлением СКВ. Грозным осложнением является тампонада сердца, встречающаяся, однако, достаточно редко — примерно 1% случаев.
Волчаночный гломерулонефрит (ВГН) представляет собой одно из наиболее серьезных и прогностически значимых проявлений СКВ. Механизм развития люпус-нефрита иммунокомплексный. Связывание антител к ДНК и других аутоантител с базальной мембраной почечных клубочков ведет к активации комплемента и рекрутированию клеток воспаления в гломерулы.
Клинически почечная патология выявляется, по данным разных авторов, у 50—70% больных, а морфологические изменения — еще чаще. Изучение почечных биоптатов больших групп пациентов показало, что вовлечение почек имеет место практически во всех случаях СКВ. Даже при отсутствии мочевого синдрома в биопсийном материале крайне редко не обнаруживаются изменения, особенно при использовании методов иммунофлюоресценции и электронной микроскопии. Помимо собственно ВГН могут развиваться также почечная тромботическая микроангиопатия, тромбозы почечных артерий и вен, обусловленные наличием антифосфолипидных аутоантител, и иммунокомплексные тубулоинтерстициальные повреждения.
Клиническая картина гломерулонефрита (ГН) при СКВ многообразна (см. таблицу 2) и включает в себя практически все выделяемые в настоящее время варианты: минимальный мочевой синдром; выраженный мочевой синдром в комбинации с гипертонией; нефротический синдром (НС), часто сочетающийся с гематурией и гипертонией, и быстро прогрессирующий гломерулонефрит. При этом каких-либо специфических клинических признаков, характерных именно для люпус-нефрита и позволяющих только на основании симптомов поражения почек диагностировать СКВ, нет.
Доминирующим симптомом является протеинурия — до 100% случаев, НС развивается примерно у половины больных. Микрогематурия присутствует почти всегда, но не бывает изолированной; макрогематурия встречается достаточно редко. Преобладают тяжелые формы заболевания, распространенность которых достигает 63%. Артериальная гипертензия зафиксирована в 50% случаев, более чем у половины больных отмечается снижение скорости клубочковой фильтрации, нарушаются также канальцевые функции. Поражение почек часто развивается в начале заболевания, на фоне высокой активности процесса, иногда становится его первым проявлением или возникает в период обострения.
Разнообразны также и морфологические изменения. Имеются характерные для ВГН признаки (фибриноидный некроз капиллярных петель, гиалиновые тромбы, проволочные петли), что в некоторых случаях позволяет поставить диагноз СКВ на основании результатов биопсии почки, но могут обнаруживаться и изменения, свойственные ГН в целом. Согласно отечественной классификации В. В. Серова (1980), выделяют очаговый пролиферативный волчаночный нефрит, диффузный пролиферативный волчаночный нефрит, мембранозный ГН, мезангиопролиферативный ГН, мезангиокапиллярный и фибропластический ГН. Классификация ВОЗ (1995), базирующаяся на данных световой, иммунофлюоресцентной и электронной микроскопии, позволяет выделить шесть классов изменений.
При сопоставлении этих двух классификаций (см. таблицу 3) можно отметить параллели между мезангиопролиферативным гломерулонефритом и II классом и, отчасти, между очаговым пролиферативным волчаночным нефритом и III классом. Класс IV включает в себя диффузный пролиферативный волчаночный нефрит, а также случаи мезангиокапиллярного гломерулонефрита. Класс V соответствует мембранозному нефриту, а VI — фибропластическому.
Частота обнаружения различных морфологических классов варьирует, чаще всего — до 60% случаев — выявляются изменения IV класса, считающегося, по мнению большинства исследователей, прогностически наиболее неблагоприятным. Помимо морфологического типа отрицательное прогностическое значение имеют нарушение функции почек, артериальная гипертензия, выраженная гематурия, а также мужской пол, высокие титры антител к ДНК, низкий уровень комплемента, анемия, тромбоцитопения и наличие полисерозита.
Течение заболевания и прогноз при СКВ вообще и при ВГН в частности в настоящее время не могут рассматриваться вне связи с результатами лечения. За последние 40 лет прогноз заболевания существенно улучшился (см. таблицу 4). Пятилетняя актуариальная выживаемость увеличилась почти в два раза как при СКВ в целом, так и при ВГН. При ВГН с изменениями IV класса динамика еще более яркая. Если 30 и более лет назад выживаемость пациентов с ВГН IV класса редко превышала один-два года, то в последующем пятилетняя актуариальная выживаемость возросла более чем в четыре раза.
Эффективность терапии высокими дозами КС в сочетании с ЦС при ВГН, в том числе с изменениями IV класса, показана во множестве работ и контролированных исследований. Преимущества терапии комбинацией ЦФ с преднизолоном, по сравнению с монотерапией ПЗ у больных с пролиферативным ВГН, наглядно подтверждены показателями почечной выживаемости.
В заключение хочется еще раз подчеркнуть, что проблема диагностики и лечения СКВ весьма актуальна не только для ревматологии и нефрологии, но и для других, на первый взгляд далеких от нее областей медицины. Пациентов с СКВ нередко длительное время обследуют и лечат с различными диагнозами амбулаторно или госпитализируют в инфекционные, неврологические, гинекологические, туберкулезные и другие стационары, из-за чего больные не получают своевременно адекватного лечения. Между тем современная иммуносупрессивная терапия может радикально изменить их судьбу. В связи с этим необходимо еще раз напомнить врачам различных специальностей, что системная красная волчанка — это не так уж редко встречающееся, грозное, опасное для жизни заболевание, требующее своевременной диагностики и лечения.
Е. В. Захарова
ГКБ им. С. П. Боткина, Москва
Волчаночный нефрит — это деструкция гломерулярного аппарата почек вследствие аутоиммунного воспаления при системной красной волчанке. Проявляется отеками, уменьшением диуреза, макрогематурией, повышением АД, нарастающей интоксикацией, которые обычно усугубляют основную симптоматику СКВ, реже являются самостоятельными симптомами волчанки. Диагностируется с помощью общего анализа мочи, определения уровней сывороточного креатинина, аутоантител, волчаночного антикоагулянта, пункционной биопсии почек с гистологическим исследованием биоптата. Для лечения применяют цитостатики, кортикостероиды, ингибиторы рецепторов ангиотензина, проводят ЗПТ, трансплантацию почки.
МКБ-10
Общие сведения
Клинические признаки волчаночного гломерулонефрита определяются почти у половины больных с установленным диагнозом СКВ. Судя по результатам биопсий, распространенность почечной патологии при волчанке может превышать 90%. Заболевание одинаково часто поражает женщин и мужчин, страдающих волчанкой, однако у пациентов мужского пола волчаночный нефрит отличается более ранним началом, тяжелым и агрессивным течением. При возникновении в возрасте старше 40 лет гломерулонефрит имеет меньшую активность и протекает благоприятнее. Актуальность своевременной диагностики нефрологической патологии у больных СКВ обусловлена ухудшением общего прогноза при аутоиммунном поражении почек. Активный люпус-нефрит остается второй по частоте причиной смерти от волчанки и составляет до 23% в структуре летальности при этом заболевании.

Причины
Поражение почек при СКВ обусловлено характерными нарушениями иммунитета. Непосредственной причиной нефрита становится повреждение паренхимы и интерстиция вследствие специфической аутоиммунной деструкции тканей. Специалистами в сфере клинической урологии, нефрологии и ревматологии выявлено два этиологических фактора развития почечной патологии у пациентов, страдающих системной красной волчанкой:
- Иммунные комплексы. При СКВ неконтролируемо усиливается образование антител к собственным клеткам организма. Осаждение циркулирующих иммунных комплексов (ЦИК) в почках потенцирует возникновение специфического воспалительного процесса (гломерулонефрита).
- Волчаночный антикоагулянт. Антифосфолипидные антитела, вытесняя фосфолипид-связывающие протеины, провоцируют усиление коагуляции. Возникающие артериальные и венозные микротромбозы приводят к ишемии и атрофии почечной паренхимы, усугубляя течение нефрита.
Патогенез
Ключевым звеном в развитии волчаночного нефрита является повреждение почечных тканей вследствие аутоиммунной деструкции. В результате поликлональной активации B-лимфоцитов, недостаточной активности T-супрессоров, низкой толерантности к аутоантигенам в организме больного в большом количестве образуются антитела к ДНК, нуклеосомам, кардиолипину, некоторым фракциям комплемента. Первыми в гломерулах обычно осаждаются иммунные комплексы, антигеном в которых являются нуклеосомы, тропные к анионным участкам базальных мембран. В дальнейшем происходит осаждение ЦИК с другими антигенами.
Классификация
В качестве основного критерия систематизации вариантов люпус-нефрита использованы морфологические изменения почечных структур, их распространенность и клинические проявления. Такой подход позволяет максимально точно спрогнозировать течение заболевания и подобрать оптимальную схему лечения. Эксперты ВОЗ различают 6 классов волчаночного нефрита:
- КлассI – мезангиальный нефрит с нормальными клубочками. Морфологические изменения мезангия не выражены, при электронной или иммунофлуоресцентной микроскопии в нем определяются иммунные комплексы. Клиническая симптоматика отсутствует. Наиболее прогностически благоприятный вариант патологии. Пациенты нуждаются в динамическом наблюдении и скрининговых исследованиях для контроля над состоянием почек.
- КлассII – пролиферативный мезангиальный нефрит. Отмечается расширение мезангия, увеличение количества мезангиальных клеток, наличие осажденных ЦИК. В осадке мочи могут выявляться эритроциты, суточная протеинурия не превышает 500 мг. Клинические симптомы поражения почек отсутствуют. Прогноз благоприятный. Базисная терапия предполагает прием блокаторов ангиотензиновых рецепторов, глюкокортикостероидов в низких и средних дозировках.
- КлассIII – пролиферативный очаговый гломерулонефрит. До половины гломерул подверглись эндо- и экстракапиллярной клеточной пролиферации. Участки воспаления сегментарно распределены в паренхиме. Определяется протеинурия и гематурия. Гипертензия, нефротический синдром, повышение концентрации сывороточного креатинина наблюдаются редко. Кроме кортикостероидов назначают цитостатические препараты. Прогноз различный.
- КлассIV – пролиферативный диффузный гломерулонефрит. Иммуновоспалительному некрозу и склерозированию подверглось больше половины гломерул. В клинической картине кроме лабораторных изменений часто выявляется повышение давления, нефротический синдром. Уровень сывороточного креатинина обычно увеличен. Необходима комплексная терапия цитостатиками и стероидами. Прогноз серьезный.
- КлассV – мембранозный гломерулонефрит. Гломерулярная мембрана утолщена. Обнаруживается субэпителиальное и интрамембранозное отложение иммунных комплексов. Преобладает клиника нефротического синдрома, у некоторых больных возможно увеличение АД, появление эритроцитов в моче, изредка повышается уровень креатинина. Рекомендована иммуносупрессорная терапия разными препаратами и ЗПТ. Прогноз сомнительный.
- КлассVI – склерозирующий гломерулонефрит. Склерозировано более 90% клубочковых капилляров. Быстро возникает и нарастает хроническая почечная недостаточность при минимальных изменениях мочевого осадка. Прогноз неблагоприятный. Пациентам требуется раннее назначение заместительной почечной терапии и пересадка почек. Без радикального лечения заболевание переходит в терминальную стадию.
Отечественными специалистами предложена классификация люпус-нефрита с учетом тяжести, особенностей течения и исходов патологического процесса. Быстропрогрессирующую форму аутоиммунного воспаления почек с нефротическим синдромом, злокачественной гипертензией, ранним возникновением ХПН, плохим прогнозом выявляют у 10-12% больных СКВ. Активный нефрит с признаками волчаночного нефротического синдрома обнаруживают у 30-40% пациентов. В 30-33% случаев определяется активный гломерулонефрит, в картине которого преобладает мочевой синдром. У 15-30% больных нефрит протекает латентно и диагностируется только лабораторно.
Симптомы волчаночного нефрита
Заболевание развивается в среднем через год после постановки диагноза СКВ, хотя может быть и единственным висцеральным проявлением волчанки. В 40% люпус-нефрит имеет бессимптомное течение и выявляется лабораторно. В клинике обычно преобладают признаки основной патологии (поражения суставов, характерная эритема, серозиты), к которым присоединяются отеки, локализованные на лице и наиболее выраженные по утрам, уменьшение суточного количества мочи. 2-5% больных отмечают появление видимой примеси крови в моче. При прогрессировании процесса у 60-70% пациентов возникает стойкая артериальная гипертензия с высокими значениями диастолического давления, рефрактерная к традиционным гипотензивным препаратам. Общее состояние зависит от выраженности морфологических изменений, при нефрите легкой степени нарушения отсутствуют, при тяжелом течении нарастают симптомы интоксикации, появляется кожный зуд, сильные головные боли.
Осложнения
Заболевание часто приводит к формированию или обострению сердечно-сосудистой патологии. Наиболее распространенными осложнениями волчаночного нефрита, развивающимися вследствие поражения сосудов при симптоматической артериальной гипертензии с дислипидемией, являются ишемическая болезнь сердца, инсульты. У пациентов могут возникать тяжелые инфекционные процессы (сепсис, некурабельные пневмонии, туберкулез), связанные с резким снижением иммунитета при длительном лечении кортикостероидами и цитостатиками. Нефрит при волчанке повышает риск злокачественной трансформации клеток, в частности – лейкоцитов с развитием В-клеточных лимфом. Почечная недостаточность как исход волчаночного гломерулонефрита обнаруживается у 10-15% больных. У 36% пациентов с быстропрогрессирующим заболеванием наблюдается ДВС-синдром.
Диагностика
Постановка диагноза волчаночного нефрита обычно не представляет сложностей при наличии характерной симптоматики заболевания. Диагностика может быть затруднена, если гломерулонефрит является единственным органным проявлением СКВ. При подозрении на волчаночный генез поражения почек рекомендованы следующие методы исследований:
- Общий анализ мочи. Соответственно клиническому варианту люпус-нефрита в осадке могут определяться эритроциты, лейкоциты, цилиндры. Для всех форм волчаночного гломерулонефрита кроме I класса характерна протеинурия от 200 до 3000-3500 мг белка/сут и более.
- Содержание креатинина в крови. Обычно показатель повышен у пациентов с диффузным пролиферативным люпус-нефритом, реже — при очаговом, мембранозном поражении, склерозирующей форме заболевания. Высокий креатинин служит прогностически неблагоприятным признаком.
- Исследование крови на антитела. Обнаруживается наличие антинуклеарного фактора, антинуклеарных антител, антител к ds-ДНК, нуклеосомам, гистонам. С1q. При проведении анализа применяют иммунофлуоресцентные и иммуногистохимические методы.
- Волчаночный антикоагулянт(LA). Умеренные и высокие показатели теста характерны для сочетания нефрита с антифосфолипидным синдромом. Положительные результаты свидетельствуют о повышенном риске усугубления аутоиммунного воспаления тромботическими процессами.
- Пункционная биопсия почек. Гистологическое исследование биоптата позволяет выявить патогномоничные морфологические изменения тканей. Проводится всем больным с подозрением на люпус-нефрит при измененном общем анализе мочи или повышенном сывороточном креатинине.
В общем анализе крови часто определяется снижение уровня лейкоцитов, эритроцитов, тромбоцитов, ускорение СОЭ. В качестве вспомогательных методов, позволяющих оценить выраженность структурных изменений и функциональную состоятельность почечной паренхимы, могут выполняться УЗИ, КТ, МСКТ, МРТ почек, экскреторная урография, нефросцинтиграфия, комплексное биохимическое исследование крови, нефрологический комплекс, оценка системы гемостаза. Дифференциальная диагностика люпус-нефрита проводится с быстропрогрессирующим и хроническим гломерулонефритом, лекарственной нефропатией, поражениями почек при ревматоидном артрите, других системных заболеваниях соединительной ткани, миеломной болезни, аутоиммунном гепатите, геморрагическом васкулите, первичном и наследственном амилоидозе. По показаниям пациента кроме уролога, нефролога и ревматолога консультирует терапевт, гепатолог, гематолог, онколог, онкогематолог, токсиколог.
Лечение волчаночного нефрита
Основными терапевтическими задачами при ведении пациентов с СКВ, у которых диагностирован специфический гломерулонефрит, являются индукция ремиссии, максимально долгое сохранение функциональной состоятельности паренхимы, профилактика рецидивов и осложнений, улучшение качества жизни и показателей выживаемости. При выборе схемы лечения учитывают активность аутоиммунного процесса, потенциальную обратимость деструктивных изменений, выраженность почечной недостаточности. Больным с неактивным процессом (I класс люпус-нефрита) рекомендован периодический скрининг состояния почек и назначение препаратов для коррекции других клинических проявлений СКВ.
При волчаночном гломерулонефрите II класса терапию начинают с ингибиторов АПФ, оказывающих антигипертензивный и нефропротективный эффекты за счет снижения системного артериального давления без ущерба ренальному кровотоку. Терапевтическая резистентность состояния, нарастание протеинурии, появление признаков гематурии является основанием для дополнительного применения глюкокортикостероидов и имидазольных цитостатиков. Больным с активным люпусным воспалением гломерул III-V класса в качестве базисных назначают иммуносупрессивные лекарственные средства:
- Цитостатические препараты. Являются обязательным элементом индукционного и поддерживающего лечения. При агрессивном течении заболевания предпочтительна пульс-терапия сверхвысокими дозами алкилирующих производных диамидофосфата, которые ингибируют активность B-лимфоцитов. В последующем больных переводят на поддерживающие дозировки имидазольных цитостатиков или селективных производных микофеноловой кислоты.
- Глюкокортикостероиды. В качестве монопрепаратов в настоящее время практически не используются. Эффективно дополняют цитостатическую терапию, обеспечивая более длительное сохранение почечных функций и лучшие показатели выживаемости. Обычно назначаются в низких дозировках и альтернирующих режимах приема. На начальных этапах лечения возможно проведение активной пульс-терапии высокими дозами.
Альтернативными методами ведения больных с терапевтически резистентными вариантами волчаночного гломерулонефрита являются применение ингибиторов кальциневрина, синтетических моноклональных антител к CD20 и CD22-антигенам мембран B-лимфоцитов, антицитокиновых препаратов, молекулярных блокаторов иммунной реакции. Апробируются и внедряются технологии тотального облучения лимфоидной ткани, костного мозга с последующей трансплантацией стволовых клеток.
Симптоматическая терапия люпус-нефрита направлена на коррекцию отдельных клинических проявлений заболевания. При развитии артериальной гипертензии и значительной протеинурии рекомендован прием ингибиторов АПФ или селективных блокаторов рецепторов ангиотензина II. Для устранения возможной дислипидемии используются статины. Пациентам с признаками антифосфолипидного синдрома показаны антикоагулянты и антиагреганты. Нарастание признаков почечной недостаточности, особенно при волчаночных гломерулонефритах V-VI класса, служит основанием для проведения ЗПТ (гемодиализа, перитонеального диализа, гемофильтрации, гемодиафильтрации и др.), а затем трансплантации почки после 3-6-месячного снижения активности аутоиммунного воспаления.
Прогноз и профилактика
Хотя развитие почечной патологии в целом ухудшает прогноз СКВ, при своевременной диагностике и адекватной терапии пятилетняя выживаемость наблюдается у 80-85% больных с тяжелыми формами гломерулонефрита и у 95% с процессами средней тяжести. Первичная профилактика волчаночного нефрита заключается в скрининговых обследованиях пациентов из группы риска по СКВ с целью раннего выявления и назначения комплексного лечения основной патологии, что позволяет снизить вероятность развития поражения почек. Для предупреждения прогрессирования уже имеющегося нефрита необходимо проведение длительной поддерживающей терапии.
1. Лечение волчаночного нефрита с позиций доказательной медицины/ Сущук Е.Л., Торгашина Л.В.// Научно-практическая ревматология. - №6.
2. Патогенез волчаночного нефрита/ Р.М. Стернер, С.П. Хартоно, Д.П. Гранде// Журнал клинической и клеточной иммунологии. – 2004.
3. Волчаночный нефрит: подходы к диагностике и лечению/ Макарова Т. П., Сенек С.А., Фирсова Н.Н., Мрасова В.К., Осипова Н.В., Садыкова Д.И., Ашрафуллина Ч.И.// Практическая медицина. – 2008.
4. Особенности современного течения волчаночного нефрита и факторы риска его прогрессирования: Автореферат диссертации/ Самокишина Н.А. – 2008.
Представлено описание клинического случая пациентки с системной красной волчанкой, трудности в постановке диагноза в связи с атипичным началом и клинической картиной заболевания, даны рекомендации с целью предотвращения поздней диагностики.
Difficulties in diagnostics of systemic lupus erythematosus N. V. Zilberberg, M. M. Kokhan, N. N. Filimonkova, Ya. V. Kascheeva, E. P. Topychkanova, O. G. Rimar, P. S. Gileva
The description of the clinical case of a patient with systemic lupus erythematosus, difficulties in diagnostics due to atypical onset and clinical manifestations were presented, recommendations to prevent late diagnosis are given.
Красная волчанка (КВ) – мультифакториальное аутоиммунное воспалительное заболевание соединительной ткани, характеризующееся гиперпродукцией органонеспецифических аутоантител к различным компонентам клеточного ядра с развитием иммуновоспалительного повреждения тканей и внутренних органов и имеющее широкий спектр клинических проявлений: артрит, серозит, поражение почек и центральной нервной системы (ЦНС), нерубцовая алопеция, язвы слизистых оболочек [1, 2].
В Российской Федерации, как и во всем мире, с середины 1980-х годов наблюдается рост заболеваемости системной красной волчанкой (СКВ) [3, 4]. Распространенность СКВ составляет от 48 до 250 случаев на 100 тыс. населения, а ежегодная первичная заболеваемость — около 50–70 случаев на 1 млн человек в год [5].
Дискоидная красная волчанка (ДКВ) — заболевание кожи из группы коллагенозов, обусловленное повышенной чувствительностью к ультрафиолетовому излучению и характеризующееся последовательным развитием эритематозных высыпаний, фолликулярного гиперкератоза и рубцовой атрофии [3].
Системная и кожная форма КВ имеют ряд общих черт: болеют преимущественно женщины молодого и среднего возраста, отмечается сосудистая эритема, фотосенсибилизация. При кожной форме КВ наблюдается изолированное или преимущественное поражение кожи, для СКВ характерна многосиндромность [7].
В основе терапии больных ДКВ лежит использование системных противомалярийных препаратов и глюкокортикостероидов (ГКС) для наружного применения. Основное место в лечении СКВ занимают ГКC, цитостатики и аминохинолиновые препараты.
Клинический случай
Пациентка Н., 24 лет, поступила в клинику ГБУ СО УрНИИДВиИ в ноябре 2018 г. с жалобами на распространенные высыпания на коже лица, верхних конечностей, ушных раковин, в носовой полости, без субъективных ощущений; ноющие боли в суставах.
Считает себя больной с августа 2018 г., когда впервые появились ноющие боли в плечевых, локтевых суставах, мелких суставах кистей, что связывала с работой официантки. С сентября 2018 г. начала постоянно отмечать усталость, слабость, головную боль, головокружение, субфебрильную температуру тела. Больная расценила данные симптомы как вирусное заболевание и самостоятельно принимала противовирусные препараты, парацетамол, амоксициллин 500 мг 2 раза в день в течение 5 дней, без эффекта.
ОАК от 12.10.2018 г.: СОЭ — 31 мм/ч, лейкопения (2,7 × 10 9 /л). УЗИ органов брюшной полости, почек, щитовидной железы от 12.10.2018 г.: патологии не выявлено. Обследована на ВИЧ, гепатиты В и С (28.10.2018 г.) — результаты отрицательные.
Проведено амбулаторное лечение: дипроспан 1,0 в/м, № 1; глюконат кальция по 2 таблетки (1,0) 3 раза в день, панкреатин 25 тыс. ед. 3 раза в день, Магнерот по 2 таблетки (1,0) 3 раза в день, дезлоратадин 5 мг в сутки. Наружно — Цинковая мазь, мазь Белодерм. Эффекта от лечения не наблюдала.
С ноября 2018 г. отметила появление нового пятна на подушечке большого пальца правой стопы. Постепенно стали нарастать боли в суставах, отметила затруднения при самообслуживании (невозможность носить сумки, открывать бутылки), снижение массы тела на 7 кг при хорошем аппетите в течение последних 6 месяцев.
В связи с отсутствием эффекта от амбулаторного лечения, нарастанием симптоматики, прогрессированием заболевания пациентка направлена в клинику УрНИИДВиИ с целью уточнения диагноза и подбора терапии.
Из анамнеза жизни заслуживает внимания: страдает папилломатозом гортани с 2 лет (лечение хирургическое — 11 операций); дермоидная киста правого уха (оперирована в детстве); курит в течение 3 лет по 4 сигареты в день. Наследственность по кожным заболеваниям отягощена: у двоюродного брата псориаз. В течение 3 лет использовала гормональную контрацепцию: Зоэли (номегэстрол + эстрадиол), последние 2 месяца — пластырь Евра.
Объективно: состояние удовлетворительное, сознание ясное, положение активное, температура тела — 36,8 °С. Периферические лимфоузлы не увеличены. Дыхание везикулярное, хрипов нет, ЧДД — 16 в минуту. Тоны сердца ясные, ритмичные, шумы не выслушиваются. Пульс — 72 удара в минуту, артериальное давление — 110/60 мм рт. ст. Язык обложен белым налетом. Слизистые оболочки губ, щек, дужек миндалин, неба, задней стенки глотки розовые, чистые, гладкие, блестящие. Живот мягкий безболезненный. Симптом поколачивания отрицательный. Почки не пальпируются. Отеков нет. Физиологические отправления в норме.
Status localis. Кожный процесс носит распространенный симметричный полиморфный характер, локализуется на коже лица, верхних и нижних конечностей; представлен пятнами без четких границ застойно красно-розового цвета, 1,0–3,0 см в диаметре; папулами с четкими границами темно-розового цвета, отечными, 2,0–3,5 см в диаметре. На поверхности отдельных элементов визуализируются точечные экскориации в небольшом количестве, покрытые геморрагическими корочками. В области пальцев — пятна застойно-розового цвета, размерами 2,0–3,0 см, местами мишеневидной формы, склонные к слиянию. Дермографизм розовый. Ногтевые пластинки кистей и стоп не изменены (рис. 1, А, Б, В).
.jpg)
Лабораторные данные: ОАК: лейкопения (2,9 × 10 9 /л); незначительный моноцитоз — 9,9%; гемоглобин — 122 г/л; тромбоцитопения (162 × 10 9 /л); повышение СОЭ до 21 мм/ч. Ревмопробы: С-реактивный белок — 3,92 мкг/мл (отрицательный). Иммуноглобулины: повышение IgG до 17,2 г/л. LE-клетки 04.12.2018 г. — не обнаружены. ИФА на ГПИ: обнаружены антитела к описторхам (1:100). Биохимический анализ крови: гиперглобулинемия (40 г/л), понижение креатинина — 58 мкмоль/л, повышение АСТ — 51,1 МЕ/л, повышение СРБ-ультра до 2,26 мг/л, незначительное повышение ЛДГ до 255,2 МЕ/л. Молекулярно-биологическое исследование (ПЦР) на вирус простого герпеса (Herpes simplex virus) — результат отрицательный, ПЦР на вирус Эпштейна–Барр (Epstein–Barr virus) — обнаружено. Микробиологическое исследование материала с кожи лица: Staph. epidermidis умеренный рост. Микробиологическое исследование слизи с миндалин и задней стенки глотки — Candida albicans умеренный рост, чувствительный к флуконазолу.
Пациентке проведена конфокальная лазерная сканирующая микроскопия (КЛСМ) образования на коже лица. В эпидермальном слое (глубина 13,72 мкм) отмечается наличие фолликулярного гиперкератоза (рис. 2, красная звезда), перифолликулярных полей вакуольной дистрофии клеток с единичными воспалительными гиперрефрактильными клетками (рис. 2, голубой круг).
В эпидермально-дермальном соединении (глубина — 74,68 мкм) также визуализируются фолликулярные гиперкератотические пробки (рис. 3, красная звезда), очаги перифолликулярного инфильтрата из воспалительных клеток (рис. 3, красный круг), расположенные перифолликулярно утолщенные коллагеновые волокна (рис. 3, голубой круг).
При поступлении выполнена инцизионная биопсия кожи из очага поражения в области спины. В исследуемом препарате эпидермис тонкий за счет атрофии шиповатого слоя с диффузным и фолликулярным гиперкератозом, умеренным неравномерным акантозом, резкой вакуольной дистрофией клеток, в том числе базального слоя. Пигмент в базальном слое отсутствует. Роговые массы в устьях фолликулов содержат клетки дрожжеподобных грибов.
В сосочковом слое дермы выражен интерстициальный отек с формированием крупной субэпидермальной, унилокулярной полости, содержащей некротизированные эпидермоциты и акантолитические клетки. Эпидермис в области пузыря с серозным пропитыванием и клеточным детритом. Мелкие сосуды расширены, полнокровны. Определяются базофильная дегенерация и фокальный муциноз коллагеновых волокон. Инфильтрат очаговый эпидермо- и фолликулотропный, лимфогистиоцитарный с примесью плазмоцитов и меланофагов (рис. 4, А, Б, В).
_575x.jpg)
Заключение: морфологическая картина соответствует острому интерфейс-дерматиту, возможна при дерматомиозите, СКВ и многоформной экссудативной эритеме.
Консультирована гинекологом: отмена гормональной контрацепции (пластырь Евра), рекомендованы только барьерные методы контрацепции.
На фоне проводимой терапии больная отмечала значительное улучшение общего состояния, уменьшение болезненности и слабости в области суставов, отсутствие головных болей, положительную динамику по кожному процессу (рис. 5, А, Б, В).
.jpg)
Пациентка была направлена на консультацию к ревматологу ГБУЗ СО Свердловская ОКБ № 1. Выполнена рентгенография кистей: костно-суставных изменений не выявлено. Ревматологом выполнены внутрисуставные инъекции препарата дипроспан 1,0 в области проксимальных межфаланговых суставов (ПМФ) с обеих сторон.
Проведенная терапия: преднизолон 20 мг/сут, гидроксихлорохин 200 мг 2 раза/сут, диклофенак 50 мг/сут, омепразол 20 мг/сут. На фоне проводимой терапии достигнута стойкая положительная динамика по кожному процессу — высыпания регрессировали полностью, оставив гиперпигментированные пятна, суставные боли отсутствуют, слабости, температуры, головных болей нет. Выписана с рекомендациями продолжить прием метилпреднизолона по 16 мг/сут в течение 1 месяца, гидроксихлорохина — 200 мг 2 раза в день, далее снижение дозы метилпреднизолона по 1/2 таблетки в 2 недели, далее по 1/4 раз в 2 недели до 6 мг (поддерживающая доза).
На фоне лечения: антитела к двухцепочечной ДНК снизились до 7,6 МЕ/мл (норма до 10). Положительная динамика сохраняется и в настоящее время: суставные боли отсутствуют, слабости, головных болей нет, увеличение массы тела на 2 кг, кожный процесс стабилен — свежих высыпаний нет, сохраняются гиперпигментированные пятна. Пациентка удовлетворена результатами лечения (рис. 6, А, Б, В).
.jpg)
При постановке диагноза ДКВ в первую очередь следует исключить признаки системного заболевания, от чего зависят тактика лечения и прогноз для жизни больного. При СКВ, в отличие от ДКВ, фолликулярный кератоз отсутствует, а атрофия выражена незначительно. Для СКВ клинически характерны артралгия, полисерозиты, эндокардит с поражением митрального клапана, поражения центральной нервной системы, почек, тяжелые васкулиты [8]. LE-клетки при СКВ в острой фазе заболевания обнаруживаются у 90–100%, при ДКВ — в 3–7%, что расценивается как неблагоприятный фактор. Антинуклеарные антитела при СКВ встречаются более чем у 95% больных, при ДКВ — у 30–40% больных. Аутоиммунная гемолитическая анемия, лейкопения и лимфопения с ускоренной СОЭ в крови, белок и цилиндры в моче — косвенные признаки системного заболевания [4].
Поражение кожи при КВ характеризуется значительной гетерогенностью клинических проявлений. В масштабном многоцентровом исследовании, проведенном C. Biazar и соавт. (2013 г.), две и более клинические формы кожной КВ наблюдались у 34,6% больных, острая кожная КВ была ассоциирована с дискоидной КВ у 30,3%, с подострой кожной КВ — у 13,8%, с дискоидной и подострой кожной КВ — у 15,3% пациентов [3].
Острая кожная форма КВ всегда служит проявлением СКВ, которая манифестирует с поражения кожи в 70—85% случаев. Острая форма КВ характеризуется развитием на коже лица в области скул и носа эритемы с цианотичным оттенком в центре и отеком. Реже встречаются распространенные пятнисто-папулезные высыпания [3, 9].
Подострая кожная КВ проявляется развитием папуло-сквамозных или кольцевидных эритематозных высыпаний. При псориазиформной КВ элементы представлены гиперемическими папулами и небольшими бляшками в области плеч, верхней части груди и спины, редко — на коже лица, ушных раковин, волосистой части головы, которые могут сливаться между собой. На поверхности пятен и бляшек имеются плотно сидящие чешуйки и незначительный гиперкератоз, усиливающийся в области устьев волосяных фолликулов. Высыпания при подострой кожной КВ могут разрешаться без рубцов, образуя длительно существующие очаги гипопигментации (гиперпигментации) с телеангиэктазиями на поверхности, или формировать поверхностную рубцовую атрофию. У данной категории больных часто имеются относительно нетяжелые системные проявления КВ: артралгии, артриты без вовлечения почек, ЦНС и серозных оболочек [1].
У большинства пациентов с подострой кожной формой КВ выявляются ANA (60-80%). При проведении дифференциальной диагностики важно учитывать, что для СКВ характерно наличие антител к экстрагируемому ядерному антигену Sm (Smith) — анти-Sm и положительные тесты на анти-dsDNA (антитела к двухцепочечной ДНК) [3].
Следует отметить, что не у всех пациентов будут положительными все иммунологические показатели, характерные при СКВ.
Неврологические симптомы возникают у 25–80% пациентов при СКВ. Нарушения когнитивных функций представлены снижением памяти, внимания, эмоционально-личностными расстройствами. В клинической картине неврологических проявлений встречаются головные боли, чаще мигренозного характера [3].
Заключение
В последние годы участились случаи стертых, молниеносных, атипичных форм диффузных заболеваний соединительной ткани, в частности СКВ. Разнообразие клинической картины, малые кожные проявления в сочетании с яркой, выступающей на первый план патологией внутренних органов приводят к поздней верификации данной нозологической единицы [4, 10].
Дифференциальный диагноз СКВ и кожной формы КВ на сегодняшний день представляется достаточно сложным и трудоемким процессом.
Диагноз СКВ должен устанавливаться на основании клинико-лабораторных данных и в соответствии с классификационными критериями: критерии диагноза Американской коллегии ревматологов (American College of Rheumatology — ACR, 1997 г.) — наличие 4 и более из 11 критериев (чувствительность 90%, специфичность 80%) и критерии диагноза Клиники международного сотрудничества по системной красной волчанке (The Systemic Lupus International Collaborating Clinics — SLISS, 2012 г.) — 4 критерия, один из которых должен быть клинический и один — иммунологический (любой из следующих лабораторных показателей: а-ДНК, АНФ, Sm, aКЛ, C3, C4) (чувствительность 95%, специфичность 74%) [6, 10].
Данное клиническое наблюдение приведено с целью привлечения внимания врачей к проблеме ранней диагностики СКВ и своевременного начала лечения до развития фатальных событий, особенно учитывая, что больными чаще являются женщины репродуктивного возраста. Ошибки диагностики связаны с отсутствием настороженности врачей в отношении СКВ. В связи с этим следует обращать внимание на такие клинические особенности, как начало заболевания в молодом возрасте, суставные боли, наличие высыпаний на коже, язв в ротовой полости, нарушение общего состояния, фотосенсибилизация, гематологические нарушения, предшествующий прием препаратов, способных исказить истинную картину заболевания, и необходимость иммунологических исследований в ранние сроки.
Литература
Н. В. Зильберберг, доктор медицинских наук, профессор
М. М. Кохан, доктор медицинских наук, профессор
Н. Н. Филимонкова, доктор медицинских наук, профессор
Я. В. Кащеева 1 , кандидат медицинских наук
Е. П. Топычканова, кандидат медицинских наук
О. Г. Римар
П. С. Гилёва
ГБУ СО УрНИИДВиИ, Екатеринбург
Сложности в диагностике системной красной волчанки. Клиническое наблюдение/ Н. В. Зильберберг, М. М. Кохан, Н. Н. Филимонкова, Я. В. Кащеева, Е. П. Топычканова, О. Г. Римар, П. С. Гилёва
Для цитирования: Лечащий врач № 5/2020; Номера страниц в выпуске: 36-41
Теги: кожа, иммуновоспалительное повреждение, коллагеноз, высыпания
Читайте также:

