Вяжущие при инфекциях кишечных
Обновлено: 24.04.2024
Для цитирования: Падейская Е.Н. НЕКОТОРЫЕ ВОПРОСЫ АНТИМИКРОБНОЙ ТЕРАПИИ КИШЕЧНЫХ ИНФЕКЦИЙ. РМЖ. 1997;24:5.
В статье представлены возбудители различных кишечных инфекций и рассмотрены вопросы этиотропной терапии этих заболеваний. Используемые для этой цели препараты делятся на две группы: средства, плохо всасывающиеся и оказывающие лишь местное действие,и системные препараты, способные, тем не менее, достигать высоких концентраций в содержимом кишечника.
В статье представлены возбудители различных кишечных инфекций и рассмотрены вопросы этиотропной терапии этих заболеваний. Используемые для этой цели препараты делятся на две группы: средства, плохо всасывающиеся и оказывающие лишь местное действие,и системные препараты, способные, тем не менее, достигать высоких концентраций в содержимом кишечника.
Особое внимание уделено препаратам группы фторхинолонов. Даны рекомендации по использованию антибактериальных средств с учетом этиологии заболеваний.
The paper presens pathogens of various intestinal infections and considers their etiotropic therapy. The agents used for this purpose are divided into two groups: those which are poorly absorbed and produce only local effects and those which have systemic effects and, nevertheless. can achieve high concentrations in the intestinal contents.
Particular attention is given to a group of fluoroquinolones. Recommendations are given on the use of antibiotics according to the etiology of the diseases.
Е.Н. Падейская, профессор, д.м.н., Москва
Prof Ye.N. Padeiskaya, Doctor of Medical Sciences, Moscow
Ш ироко распространенный термин “кишечные инфекции” относится к большой группе инфекционных заболеваний с преимущественным поражением желудочно-кишечного тракта (ЖКТ) и соответствующей симптоматикой (диарея, боли в области живота, в подложечной области, тошнота, иногда рвота, в тяжелых случаях – выраженная интоксикация, обезвоживание). Эти инфекции вызываются главным образом различными патогенными или условно-патогенными бактериями, вирулентные и токсигенные свойства которых определяют особенности патогенеза. Кроме того, поражение ЖКТ может быть вызвано некоторыми протозоа и вирусами (табл. 1) . Общим для этой группы инфекций является орально-фекальный путь заражения (через пищу, воду, контактно-бытовым путем – “болезни грязных рук”), входные ворота инфекции – ЖКТ, основные формы заболевания – гастроэнтерит, энтероколит, колит, гастроэнтероколит или гастрит. При тяжелых формах инфекции (в том числе на фоне иммунодефицитных состояний) могут иметь место токсинемия или бактериемия, реже – септицемия или септикопиемия. Учитывая особенности возбудителей инфекций, патогенез, характер течения и тяжесть процесса, определяющие тактику терапии, каждое заболевание в зависимости от этиологии следует рассматривать отдельно. К кишечным инфекциям, учитывая путь инфицирования и поражение тонкой кишки, обычно относят брюшной тиф и паратифы. При этих заболеваниях на фоне поражения кишечника и инвазии в кровь возбудителя развивается тяжелый генерализованный инфекционный процесс с бактериемией и интоксикацией. Высвобождающийся после гибели сальмонелл эндотоксин оказывает нейротропное действие, вызывает дистрофические изменения в миокарде, повреждает костный мозг. Генерализация процесса с поражением внутренних органов происходит при осложненных формах амебной дизентерии (амебный гепатит, абсцесс печени, поражение центральной нервной системы). Таким образом, понятие “кишечные инфекции” является в значительной степени условным.
Инфекционные диареи различного генеза широко распространены в разных регионах мира, могут протекать в тяжелой форме с выраженной токсинемией, в развивающихся странах остаются одной из основных причин заболеваемости и смертности [1 – 6].
Таблица 1. Возбудители и клинические формы кишечных инфекций
К кишечным инфекциям бактериальной этиологии относятся холера, эшерихиоз, шигеллез, кампилобактериоз, геликобактериоз, иерсиниоз, сальмонеллы, брюшной тиф и паратифы, а также острые диареи, часто недиагностированные по этиологическому фактору. Причиной последних могут быть как возбудители перечисленных выше инфекций, так и некоторые другие условно-патогенные аэробные бактерии. Характер течения заболевания зависит от свойств штаммов, в первую очередь от их токсигенных и инвазивных свойств. Одна из тяжелых свойств эшерихиоза – геморрагический колит с синдромом гемолитической уремии – вызывается токсигенным штаммом кишечной палочки 0156:Н7 [5].
Серьезную проблему для ВИЧ-инфицированных представляют диареи, вызванные Campylobacter spp.: описано до 10 различных представителей Campylobacter, которые могут быть причиной этих диарей [6].
Возбудителем инфекции у человека может быть Cyclospora cayetanensis – энтеропатогенный микроорганизм, вызывающий иногда очень длительную (до 70 дней) диарею [7].
Особое место занимают пищевые токсикоинфекции, патогенез которых определяют бактериальные экзотоксины с энтеротропными свойствами (энтеротоксины, цитотоксины). Они продуцируются различными аэробными и некоторыми анаэробными бактериями, причем и вне организма человека, в частности при размножении бактерий в пищевых продуктах, что и является причиной пищевой интоксикации. Клиника заболевания связана в первую очередь с поражением верхних отделов ЖКТ. Энтеротоксины мoгут продуцировать токсигенные штаммы P. vulgaris, P. mirabilis, Klebsiella spp., Enterobacter spp., Serratia spp., Citrobacter spp., Pseudomonas spp., Aeromonas spp., S. aureus, C. perfringens. Наиболее серьезную опасность представляют термостабильные энтеротоксины, в частности энтеротоксин стафилококка. Чаще энтеротоксины относятся к термолабильным токсинам [2].
К пищевым токсикоинфекциям, с учетом источника заражения и пути инфицирования, можно было бы отнести и заболевание, вызванное токсином Clostridium botulinum. Однако этот токсин характеризуется не энтеротропными, а нейроплегическими свойствами, и заболевание (ботулизм) по патогенезу и клинике принципиально отличается от инфекций с преимущественным поражением ЖКТ.
Таблица 2. Группы антимикробных препаратов, применяющихся для этиотропной терапии бактериальных кишечных инфекций
Лечение кишечных инфекций является комплексным и включает патогенетическую терапию (прежде всего – дезинтоксикацию, при обезвоживании – регидратацию), этиотропное лечение, направленное на инактивацию возбудителя инфекции, диетотерапию (сбалансированную и тщательно подобранную в зависимости от характера ферментативных нарушений при той или иной инфекции), коррекцию нарушений нормальной микрофлоры кишечника с помощью биопрепаратов для предупреждения развития дисбактериоза.
Задачей настоящей работы является рассмотрение разных аспектов этиотропной терапии. Вместе с тем следует подчеркнуть, что патогенетическая и диетотерапия в сочетании с коррекцией микрофлоры должны рассматриваться как важнейшие компоненты лечения кишечных инфекций, а при легких формах заболевания могут быть эффективны и без применения антимикробных препаратов. С другой стороны, этиотропные средства являются важнейшим копонентом терапии при среднетяжелых и тяжелых (особенно генерализованных) формах инфекции, кроме того, они используются для лечения и профилактики бактерионосительства.
Учитывая широкий профиль возбудителей (см. табл. 1) , трудности быстрой микробиологической диагностики острых диарей в большистве случаев на первом этапе проводят эмпирическую терапию. В связи с этим, важно, чтобы антимикробный препарат характеризовался широким антимикробным спектром, включающим, по возможности, всех потенциальных возбудителей этих инфекций. Необходимо также, чтобы препарат:
– достигал высокой концентрации в содержимом кишечного тракта после перорального применения;
– хорошо проникал в клетки фагоцитарной системы (микроорганизмы с внутриклеточной локализацией – одни из важнейших в этиологии рассматриваемых заболеваний);
– оказывал минимальное отрицательное влияние на нормальную микрофлору кишечника;
– не вызывал побочных реакций со стороны ЖКТ.
Кроме того, важно, чтобы у энтеропатогенных бактерий как можно реже развивалась выраженная резистентность к данному препарату.
При пищевых токсикоинфекциях основное значение имеет дезинтоксикационная патогенетическая терапия, и в большинстве случаев нет необходимости прибегать к применению этиотропных средств.
Проблема лекарственной резистентности существенно осложнила этиотропную терапию кишечных инфекций. Особенно демонстративным в этом отношении является пример дизентерии и брюшного тифа. Изучение чувствительности шигелл к антимикробным препаратам в 14 штатах США за период с 1985 – 1986 по 1995 г. показало повышение частоты выделения устойчивых к ампициллину штаммов с 32 до 67%, к ко-тримоксазолу – с 7 до 35% [8]. Значительно возросло число штаммов сальмонелл, в том числе S. typhi, устойчивых к хлорамфениколу, ко-тримоксазолу и ампициллину, причем уровень резистентности может быть очень высоким: минимальная ингибирующая концентрация (МИК) достигает 400 мг/л. Одновременно в ряде регионов отмечается и более тяжелое клиническое течение кишечных инфекций, в частности шигеллеза, что проявляется увеличением продолжительности и тяжести интоксикации и диареи в сочетании с более глубокими деструктивными изменениями в стенке толстой кишки [9].
Для этиотропной терапии кишечных инфекций с учетом лекарственной резистентности в настоящее время успешно используются препараты группы фторхинолонов, эффективность которых при этих заболеваниях очень высокая.
Уже внедренные в практику с 1962 г. нефторированные хинолоны (налидиксовая кислота и аналоги) оказались эффективными при пероральном приеме при дизентерии, вызванной штаммами, устойчивыми к сульфаниламидам и хлорамфениколу. Однако широкое использование этих препаратов способствовало формированию резистентности к ним энтеропатогенов и снижению эффективности. В связи с особенностями фармакокинетики нефторированные хинолоны оказались неэффективными при генерализации процесса, не могли применяться для лечения брюшного тифа и паратифов, несмотря на высокую активность in vitro.
Таблица 4. Эффективность перорального приема офлоксацина при брюшном тифе и сальмонеллезах 1)
За последние 15 лет накоплен большой клинический опыт, свидетельствующий о высокой эффективности фторхинолонов при кишечных инфекциях бактериальной этиологии [1, 4, 10 – 18].
Фторхинолоны высокоэффективны в отношении практически всех возбудителей бактериальных кишечных инфекций, включая штаммы с множественной устойчивостью к бета-лактамам (в частности к ампициллину), хлорамфениколу, препаратам группы ко-тримоксазола. Несмотря на высокую биодоступность, препараты при применении перорально обеспечивают достаточно высокие концентрации в содержимом кишечника, колеблющиеся в пределах 100 – 2500 мг/кг и выше, что на несколько порядков превышает МИК и минимальную бактериостатическую концетрацию фторхинолонов для энтеропатогенов. Препараты создают высокие концентрации в слизистой кишечника и в макрофагах; это особенно существенно, учитывая внутриклеточную локализацию сальмонелл, шигелл, иерсиний, стафилококков. Высокая бактерицидная активность фторхинолонов в сочетании с активностью в отношении полирезистентных штаммов энтеробактерий, высокими концентрациями препаратов в содержимом кишечника и клетках фагоцитарной системы обеспечивают клинический и бактериологический эффект и, как правило, предотвращают формирование бактерионосительства. При генерализованных инфекциях важное значение имеет длительная циркуляция фторхинолонов в организме, хорошее проникновение в органы и ткани и высокие тканевые и внутриклеточные концентрации. Последнее особенно важно при лечении брюшного тифа и паратифов, а также других форм генерализованных сальмонеллезов.
Таблица 5. Эффективность фторхинолонов при лечении больных холерой; курс лечения – 3 дня [12, 17,21, 22, в модификации]
Эти препараты уменьшают чувство боли, препятствуют при местном применении воздействию раздражающих агентов на ткани и находящиеся в них чувствительные нервные окончания. Действие проявляется только при непосредственном соприкосновении со слизистыми оболочками, кожей или раневыми поверхностями. Вызывая образование защитной пленки на поверхности ткани или сорбируя раздражающие агенты, они оказывают местное противовоспалительное и обезболивающее действие, что позволяет широко использовать их при заболеваниях слизистых оболочек. В отличие от местных анестетиков они не обладают избирательностью действия на чувствительные нервные окончания и проводники и не могут применяться для уменьшения боли при болезненных манипуляциях и операциях.
Вяжущие средства при нанесении на слизистые оболочки, кожу. раневые поверхности вызывают уплотнение поверхностного слоя ткани (дубящее действие) с уменьшением ее проницаемости за счет неспецифических физико-химических изменений коллоидов клеток, внеклеточной жидкости, слизи, экссудата. Взаимодействуя с белками, они образуют нерастворимые албуминаты (коагуляция). Формируется плотная эластичная пленка, защищающая ткани от воздействия раздражающих веществ, уменьшающая боль, способствующая сужению капилляров, уменьшению гиперемии, уплотнению стенки сосудов, снижению секреции желез и активности ферментов. Уменьшение проницаемости тканей блокирует экссудацию. Снижая активность ферментов, препараты гасят "пожар обмена" в очаге воспаления. Совокупность указанных эффектов объясняет местное противовоспалительное действие вяжущих средств. Коагулируя белки плазмы, они способствуют остановке капиллярных кровотечений. Коагуляция белков микробной клетки обеспечивает противомикробное действие.
Перечисленные свойства позволяют использовать вяжущие препараты при лечении воспалительных процессов в полости рта.
Вяжущие средства делят на 2 группы:
1. Вяжущие средства неорганической природы (соли тяжелых металлов).
2. Вяжущие средства органической природы (препараты растительного происхождения).
Соли тяжелых металлов, такие как свинца ацетат, висмута субнитрат ( висмута нитрат основной), алюминия ацетат (квасцы), цинка окись, серебра нитрат, оказывают дубящее действие, подсушивают слизистую оболочку. Вяжущие средства органической природы не оказывают выраженного дубящего действия, в меньшей степени подсушивают ткан.
Вяжущие вещества содержатся во многих растениях: шалфея лист, дуба кора, зверобоя трава, ромашки цветки, плоды черники и черемухи, чая листья, арники цветки, лапчатки, змеевика, кровохлебки корневища и т.д. Настои и отвары этих растений применяют для полоскания, "ванночек", примочек при воспалительных заболеваниях ротовой полости, при ангинах, фарингитах, ожогах, трещинах кожи. При заболеваниях желудочно-кишечного тракта их назначают внутрь.
Из растений, содержащих вяжущие вещества, получают оригинальные официнальные препараты с выраженным противовоспалительным, дезодорирующим, противомикробным действием, например, сальвин (из листьев шалфея), ромазулан (из цветков ромашки). Эти препараты можно использовать местно при заболеваниях слизистой оболочки полости рта и пародонта путем орошений, смазывания слизистой, введения турунд, смоченных препаратом, в зубодесневые карманы и т.д.
Танин -галлодубильная кислота, получаемая из дубильных (чернильных) орешков, хорошо растворяется в воде, спирте, глицерине. Обладает выраженным вяжущим действием. Раствор танина применяется для промывания желудка при лечении отравлений, поскольку он осаждает многие алкалоиды и соли тяжелых металлов.
Образующиеся соединения нестойки и должны быть удалены из желудка (неоднократные промывания) и из нижних отделов кишечника (клизмы).
Значительное количество танина содержится в листьях чая, поэтому при отравлениях крепкий настой чая можно использовать для промывания, а также как противовоспалительное средство при катаральных воспалительных процессах слизистых оболочек (полости рта, носа, глаз и т.д.).
При заболеваниях кишечника часто назначают танальбин (белковосвязанный танин), из которого танин освобождается постепенно (по мере переваривания белка), оказывая действие на большом протяжении кишечника. Назначение танина в этих условиях малоэффективно, поскольку он теряет свою активность уже в желудке, соединяясь с белками пищи. При кишечных инфекциях применяют также препарат тансал, в состав которого наряду с танином входит фенилсалицилат, обладающий противомикробным действием.
Обволакивающие средства - индифферентные вещества, способные набухать в воде с образованием коллоидных растворов - слизей. При их применении на поверхности ткани образуется слой слизи, предохраняющий чувствительные нервные окончания от раздражения и оказывающий неспецифическое болеутоляющее и противовоспалительное действие. Кроме того, на крупных коллоидных частицах могут адсорбироваться различные химические вещества, в результате задерживается их всасывание. Наиболее широко используются полисахариды растительного происхождения (слизи из картофельного и рисового крахмала, листьев и цветков мальвы, отвары из корня и листьев алтея, окопника лекарственного, семян льна, овса, раствор яичного белка и т.д.). Коллоидные растворы, обладающие обволакивающими свойствами, могут образовывать и некоторые неорганические вещества, например, магния трисиликат, (алгелдрат (алюминия гидроокись). Обволакивающие средства применяют в форме полосканий и "ванночек" при лечении воспалительных заболеваний, пролежневых язв, кератозов слизистой оболочки полости рта. В качестве противоязвенных и противодиарейных средств их часто назначают внутрь при катаральных и язвенных повреждениях слизистой оболочки желудочно-кишечного тракта (гастриты, энтериты, колиты), так как они защищают слизистую оболочку от раздражений. Это свойство позволяет их использовать совместно с лекарственными препаратами, обладающими раздражающим действием (в микстурах и лекарственных клизмах); следует учитывать, что скорость всасывания лекарств при этом замедляется. При острых отравлениях веществами, вызывающими местное раздражение, обволакивающие средства применяют внутрь и в клизмах (многократно) для уменьшения всасывания и защиты слизистой от раздражения.
Адсорбирующие средства - тончайшие измельченные нерастворимые индифферентные порошки с большой адсорбционной способностью, связывающие на своей поверхности различные вещества, уменьшая всасывание последних, механически защищая слизистую оболочку и находящиеся в ней окончания чувствительных нервов. Это важно при различного рода интоксикациях, в том числе бактериальными токсинами, раздражающими средствами и т.д. В качестве адсорбирующих средств наиболее часто используют, уголь активированный, глину белую. При метеоризме (для поглощения газов), заболеваниях желудочно-кишечного тракта и при острых отравлениях внутрь назначают уголь активированный. При заболеваниях кожи и слизистых оболочек наружно применяют тальк, глину белую, магния окись, цинка окись и т.д.
Проблема острых кишечных инфекций является одной из актуальнейших в отечественном здравоохранении. С одной стороны, уровень заболеваемости остается достаточно высоким, без тенденции к отчетливому снижению, с другой – отмечается появление сероваров, обусловливающих тяжелое течение болезни (S. flexneri 2a, энтерогеморрагическая эшерихия OI57 и др.). Кроме того, получают широкое распространение кишечные инфекции, которые прежде не диагностировались или встречались редко (ротавирусный гастроэнтерит, клебсиеллез и др.).
К сожалению, в лечении острых кишечных инфекций допускается много ошибок, порожденных недостаточной квалификацией специалистов; отжившими догматическими представлениями о сущности патологического процесса; погоней за рекламой суперсовременных лекарственных средств; непониманием сущности регидратационной терапии, прежде всего оральной.
Крайне важно, чтобы практические врачи осознали все опасности, возникающие при развитии кишечного дисбактериоза в случае бесцельного, а порой бесконтрольного применения антибиотиков, особенно при лечении сальмонеллеза и пищевых токсикоинфекций. В лечении острых кишечных инфекций появились новые подходы, основной акцент делается на патогенетическую терапию.
Одной из целей патогенетической терапии острых кишечных инфекций является купирование диарейного синдрома. Предложено множество антидиарейных препаратов, при использовании которых должны учитываться патогенетические особенности указанного синдрома.
Известно, что циклические нуклеотиды способствуют регуляции секреции воды и электролитов в кишечнике. По современным представлениям эндотоксины сальмонелл воздействуют на аденилатциклазу, находящуюся на наружной поверхности мембран энтероцитов. В результате активации аденилатциклазы усиливается образование циклического аденозинмонофосфата (цАМФ). Изменения мембранных белков и биполяризация клеток мембран способствуют повышению проницаемости последних для воды и электролитов, что ведет к диарее. Определенная роль в изменении проницаемости клеточных мембран принадлежит простагландинам, функционально связанным с циклическими нуклеотидами, что приводит к повышенному образованию цАМФ и развитию диареи. Таким образом, избыток гуморального регулятора обмена может стать фактором патогенеза болезни. В связи с этим было предложено использовать индометацин при диарейном синдроме в качестве ингибитора биосинтеза простагландинов.
Рекомендуется так же применение карболонга – порошка из активированных косточковых углей. Он обладает высокими сорбционными свойствами. Его назначают по 5–10 г на прием 3 раза в день.
Одним из эффективных сорбентов является полифепан. Препарат получают при переработке лигнина – продукта гидролиза углеводных компонентов древесины. Выпускается в виде гранул (содержит 40% полифепана) или пасты (50% полифепана). Назначают внутрь взрослым по 1 столовой ложке 3–4 раза в день; перед употреблением препарат тщательно размешивают в течение 2 мин в стакане воды.
Наиболее эффективным сорбентом является диосмектит. Кроме того, диосмектит обладает значительной обволакивающей способностью. Известна способность диосмектита защищать эпителий кишечных ворсинок от разрушения. Препарат выпускается в виде порошка в пакетах, содержащих 3 г лекарственного средства. Содержимое пакета растворяют в 100 мл воды и размешивают. Взрослому рекомендуют принимать 3–4 пакета (9–12 г) в день. Препарат не имеет противопоказаний к применению, его можно назначать беременным и кормящим матерям. При тяжелом течении сахарного диабета применение диосмектита опасно, так как в 1 пакетике содержится 0,75 г глюкозы.
К группе сорбентов относится аттапульгит. Препарат выпускается в таблетках. Начальная доза для взрослого – 2 таблетки, затем назначают по 2 таблетки после каждого акта дефекации. Максимальная суточная доза – 12 таблеток, максимальная продолжительность лечения 2 дня.
Другой группой антидиарейных препаратов являются лекарственные средства, оказывающие опиоидное действие. К ним относят лоперамид и тримебутан. Способность тормозить перистальтику кишечника является характерной особенностью опиатов. Действие лоперамида наступает быстро и продолжается 4–6 ч. Его назначают взрослым при острой диарее, вначале 2 капсулы, а затем по 1 капсуле после каждого акта дефекации, но не более 6 капсул в сутки. Не рекомендуется применение препарата вместе с атропинсодержащими средствами. Лоперамид противопоказан беременным и кормящим грудью женщинам, а также больным неспецифическим язвенным колитом. Группа атропинсодержаших антидиарейных препаратов представлена двумя лекарственными средствами – лиспафеном и реасеком.
Лиспафен уменьшает секрецию желез, понижает тонус гладкой мускулатуры и двигательную активность желудка и кишечника. Взрослым назначают по 2 таблетки 3 раза в день, максимальная суточная доза – 12 таблеток. Реасек назначают по 1 таблетке 2–3 раза в день. К указанной группе препаратов относится тримебутин малеат. В 1 таблетке содержится 100 мг препарата. Тримебутан оказывает положительное действие на регуляцию перистальтики кишечника. При гиперкинетическом состоянии он оказывает спазмолитическое, при гипокинетическом – стимулирующее действие. Воздействует на гладкую мускулатуру всего желудочно–кишечного тракта. Лечебный эффект основан на нормализации моторики кишки, применяется по 1–2 таблетки 3 раза в день. Противопоказан беременным и кормящим грудью женщинам.
В группу лекарственных средств, обладающих обволакивающим и вяжущим свойствами, входит порошок Кассирского и десмол. Антидиарейный порошок (состав: Bismuti subnitrici 0,5; Dermatoli 0,3; Calcii carbonici I 0; Ac. ascorbinici 0,3; Ac. nicotinici 0,01) назначают по 1 порошку 3–4 раза в день.
В отдельных случаях тяжелого течения диареи используются большие дозы висмута – по 2 г 3 раза в сутки. В последние годы для лечения острых диарейных заболеваний успешно применяют висмута субсалицилат, одна таблетка препарата содержит 262 мг активного вещества. Препарат принимают по 2 таблетки 3–4 раза в день. Он оказывает обволакивающее и противовоспалительное действие, повышает выработку слизи и улучшает ее защитные свойства. Наш опыт применения висмута субсалицилата подтверждает эффективность препарата.
Новым средством для лечения диареи, оказывающим патогенетическое воздействие на процессы всасывания и секрецию в кишечнике, является октреотид. Этот гормон увеличивает скорость всасывания воды и электролитов в тонкой кишке, снижает концентрацию вазоактивных пептидов в крови, уменьшает частоту актов дефекации и массу кала. Выпускается в виде свободного пептида – оректида в ампулах, содержащих 0,05, 0,1 и 0,5 мг. Вводится подкожно 1–2 раза в сутки; при необходимости дозу препарата увеличивают.
Проблема дисбактериоза и эубиотики
Острые кишечные инфекции сопровождаются развитием дисбактериоза, либо это состояние развивается после применения антибиотиков. Лечение больных, страдающих кишечным дисбактериозом, требует комплекса терапевтических мер и индивидуально подобранных препаратов с учетом заболевания, на фоне которого возник дисбактериоз. В комплекс терапии дисбактериоза кишечника необходимо включать средства для нормализации кишечной флоры и курс лечения антибактериальными препаратами при появлении патогенной флоры.
Схема лечения дисбактериоза с учетом стадии заболевания:
I стадия – назначение биопрепаратов и лекарств, нормализующих моторную функцию кишечника (спазмолитики, вяжущие, ферменты), а также витаминов и противоаллергических средств;
II стадия –тактика такая же, как в I стадии, но добавляется колибактерин. При отсутствии эффекта через 3–4 недели назначают невиграмон или нитроксалин;
Ill–IV стадии –назначение поливалентного бактериофага, после отмены которого используют ко–тримоксазол (часто в сочетании с метронидазолом); при отсутствии эффекта назначают антибиотики. Одновременно с антибиотиками применяют биопрепараты.
Нормализация кишечной флоры осуществляется эубиотиками. Различают четыре поколения эубиотиков, применяемых для лечения дисбактериоза: I – классические эубиотики (коли–бактерин, бифидумбактерин, лактобактерин); II – самоэлиминирующиеся эубиотики (бактисубтил, биоспорин, споробактерин); III – комбинированные эубиотики (Аципол и др.); IV поколение – иммобилизованные на сорбенте живые бактерии, представители нормальной микрофлоры – бифидумбактерин форте.
Эффективность эубиотиков определяется биологическими свойствами штаммов микроорганизмов: колонизирующей способностью, антимикробной активностью, особенностью воздействия на иммунную систему и другие защитные механизмы [5].
Аципол – эубиотик III поколения, представляющий собой биомассу, состоящую из смеси живых антагонистических активных штаммов ацидофильных лактобацилл и инактивированных прогреванием кефирных грибков. Препарат оказывает многофакторное лечебное действие, отличается высокой активностью в отношении патогенной и условно–патогенной флоры, корригирует нормальную микрофлору кишечника, повышает иммунологическую резистентность организма. Аципол принимают по 1 таблетке 3 раза в сутки вместе с пищей.
Эубиотики обычно назначают в сочетании с ферментами (абомин, ораза, фестал и др.) и антигистаминными препаратами (пипольфен, хлоропирамин, клемастин).
При стафилококковом дисбактериозе лечение обязательно должно включать применение стафилококкового бактериофага. В тяжелых случаях целесообразно назначать антибиотики (оксациллин, цефалоспорины I и II поколений, карбопенемы, ванкомицин, рифампицин) и фторхинолоны.
При протейном дисбактериозе используют поливалентный бактериофаг (протейный, стафилококковый, синегнойный), в тяжелых случаях – антибиотики (ампициллин, карбенициллин, цефалоспорины I и II поколений), в более легких – ко–тримоксазол–480 и полимиксин М.
При синегнойном дисбактериозе используют полимиксин В, тетрациклин, рифампицин, лонгацеф.
В случаях энтеробактериального или бактериоидного дисбактериоза целесообразно применение цефалексина или цефадина, при клостридиозе – метронидазола и ко–тримоксазол–480.
При дисбактериозе эшерихиозной этиологии рекомендуются препараты висмута, а при заболеваниях, обусловленных гемолитическими штаммами – лактобактерин. Антибактериальная терапия осуществляется невиграмоном, нитроксалином, ко–тримоксазолом–480, энтероседивом. Иногда дает эффект коли–бактериофаг.
Для борьбы с дисбактериозом кишечника рекомендуют применение нормазе. Этот препарат представляет собой раствор лактулозы (дисахарид) из молекул галактозы и фруктозы. Способность лактулозы стимулировать рост лактобацилл в толстой кишке, в то же время снижая концентрацию гнилостных бактерий, позволяет восстановить нормальный биоценоз в кишечнике. Продукты метаболизма нормазе стимулируют перистальтику. Суточная доза нормазе для взрослых – 75 мл. Длительность лечения 2–3 недели.
В целях восстановления и профилактики нарушений микроэкологии кишечника в последние годы был предложен пищевой биококтейль (NK). Этот препарат по существу является эубиотиком. При острой диарее его рекомендуют принимать по 2–3 столовые ложки каждые 3–4 ч в течение 1–2 дней, а затем по 1–2 столовые ложки 3 раза в день в течение 1–3 месяцев. При иммунодефицитах, нарушениях обмена и длительной антибиотикотерапии принимают по 1 столовой ложке 2–3 раза в день в течение 1–3 месяцев. Эубиотики обычно назначают в сочетании с ферментами (абомин, ораза, фестал, дигестал, мезим и др.) и антигистаминными препаратами.
В последние годы широкую популярность приобрели ферментные препараты креон и панцитрат–10000. Каждая капсула креона содержит 300 мг панкреатина в микросферах, устойчивых к желудочному соку, что соответствует 8000 ед. липазы, 9000 ед. амилазы и 4500 ед. протеазы. Вначале принимают по 1–2 капсулы во время еды, а затем дневную дозу увеличивают до 3–15 капсул. Активным веществом панцитрата–10000 является панкреатин. Одна капсула препарата содержит 10000 ед. липазы, 9000 ед. амилазы и 500 ед. протеазы. Обычная дозировка препарата – по 2–4 капсулы во время каждого приема пищи.
Этиотропное лечение острых кишечных инфекций
Кишечные антисептики
В настоящее время применяются три препарата этой группы: интестопан, интетрикс и энтероседив.
В последние годы для лечения диарейных заболеваний предложен эрцефурил (нифураксазид), являющийся производным нитрофурана. Этот препарат действует преимущественно в просвете кишечника, показан при лечении диареи бактериального происхождения. По данным исследователей, он активен в отношении кампилобактерий, эшерихий (энтеротоксигенных, энтеропатогенных и энтероинвазивных), сальмонелл, шигелл, холерного вибриона и иерсиний (J. enterocolitica).
Популярным препаратом этой группы является фуразолидон. Препарат эффективен в отношении грамположительных и грамотрицательных бактерий, лямблий и трихомонад. Из числа возбудителей острых кишечных инфекций наиболее чувствительны к нему бактерии дизентерии, брюшного тифа, паратифов А и В. Устойчивость к нему микроорганизмов развивается медленно. Фуразолидон был рекомендован к применению в качестве препарата выбора для лечения острой дизентерии, так как он оказывает минимальное побочное действие на организм, особенно на желудочно–кишечный тракт.
Эффективность лечения острых кишечных инфекций вышеуказанными группами лекарственных средств различна. Терапия кишечными антисептиками всегда носит вспомогательный характер.
Антибиотики и другие антибактериальные препараты
Для лечения острых кишечных инфекций используются различные антибактериальные средства: 1) b–лактамные антибиотики: пенициллины природные, пенициллины полусинтетические, ингибиторы b–лактамаз, цефалоспорины I – IV поколений, карбапенемы, монобактамы; 2) антибиотики других классов: аминогликозиды, тетрациклины, макролиды, рифампицины, линкозамины, хлорамфеникол, полимиксины, гликопептиды; 3) синтетические антибактериальные средства: сульфаниламиды, хинолоны, фторхинолоны, нитрофураны, производные хиноксалина, производные 8–оксихинолина.
Учитывая, что в большинстве случаев острые кишечные инфекции вызываются грамотрицательными микроорганизмами, целесообразно привести перечень антибактериальных средств, действующих на них бактерицидно или бактериостатически: аминопенициллины, цефалоспорины, монобактамы, карбапенемы, аминогликозиды, тетрациклины, хлорамфеникол, полимиксины, хинолоны, фторхинолоны, нитрофураны, комбинированные препараты сульфамидов с триметопримом.
При неосложненном течении острых кишечных инфекций нешигеллезной и нехолерной этиологии лечение должно быть только патогенетическим. В тяжелых случаях особенно при наличии тяжелых фоновых и сопутствующих заболеваний, целесообразно использование кишечных антисептиков. К сожалению, до сегодняшнего дня антибиотики широко применяются для лечения острых кишечных инфекций, что способствует развитию дисбактериоза и более медленной репарации слизистой оболочки кишечника. Нет единства взглядов и на лечение сальмонеллеза. Наша точка зрения, основанная на многолетнем опыте лечения острых кишечных инфекций, заключается в том, что должна проводиться только патогенетическая терапия. Это относится и к гастроинтестинальной форме сальмонеллеза. Единственным исключением является генерализованная форма сальмонеллеза, при которой показана антибиотикотерапия. Мы также резко отрицательно относимся к использованию антибиотиков для лечения носительства при острых кишечных инфекциях.
Таким образом, лечение острых кишечных инфекций направлено на поддержание деятельности ряда функциональных систем, в том числе систем, обеспечивающих уровень АД, массу циркулирующей крови, поддержание оптимальных величин дыхательных показателей, уровня осмотического давления и системы выделения. Используя современные подходы в лечении острых кишечных инфекций, можно избежать развития таких грозных осложнений, как инфекционно–токсический шок, гиповолемический шок, острая почечная недостаточность. Аккуратность и рациональность в применении антибактериальной терапии позволяет избавить наших пациентов от дисбактериоза, адекватно проведенная пероральная регидротация в короткие сроки справляется с основными симптомами острых кишечных инфекций.

Боли, урчание, вздутие живота и ощущение переполненности кишечника могут говорить о колите. Такие симптомы лучше не игнорировать. Ведь невылеченный колит иногда становится причиной тяжелых осложнений, например, язв. К счастью, колит можно вылечить, если вовремя обратиться к врачу и скорректировать питание.
Колит – это воспаление слизистой оболочки или более глубоких слоев толстого кишечника. Заболевание не из приятных, оно вызывает очень сильные боли в животе и бытовой дискомфорт.
Толстый кишечник – продолжение тонкого, здесь происходит завершающая стадия пищеварения. Заканчивается он сфинктером прямой кишки. Благодаря сокращению гладкомышечной мускулатуры, которая составляет срединный слой всех кишок, по толстому кишечнику осуществляется продвижение остатков пищи с соками (химуса) и выведение каловых масс (рис. 1).
Толстый кишечник выполняет важные функции:
- Завершение процесса пищеварения и всасывания полезных веществ (глюкозы, аминокислот, витаминов).
- Формирование каловых масс. Жидкость всасывается в кровь, а клетчатка, остатки непереваренной пищи и слизи - уплотняются. Бактерии могут составлять до 50% массы кала.
- Выделительная. Через толстый кишечник выводятся продукты белкового обмена (креатинин, мочевина, мочевая кислота, остатки непереваренных жиров и клетчатка, множество токсинов).
- Защитная. Обеспечивается полезной микрофлорой, которая препятствует размножению патогенных бактерий. В слизистом слое толстого кишечника содержится около 70% клеток иммунной системы (лимфоцитов), которые при инфекционных угрозах способны синтезировать антитела. Деятельность иммунных клеток во многом зависит от состава микрофлоры.
- Синтез витаминов. Благодаря бифидобактериям в толстом кишечнике образуются витамины группы B, K, E, D, PP, биотин, фолиевая кислота. Они обеспечивают нормальное кроветворение, свертывание крови при кровотечениях, работу нервной системы, здоровое состояние кожи и костно-мышечной системы.
- Особая роль в работе толстого кишечника принадлежит микрофлоре – бифидобактериям, бактероидам, энтерококкам, лактобактериям, кишечной палочке, которые обеспечивают остаточное переваривание пищи, разложение белков, сбраживание углеводов, образование витаминов. Такая флора составляет 96–98% всех микроорганизмов кишечника и весит около 1,5 кг!
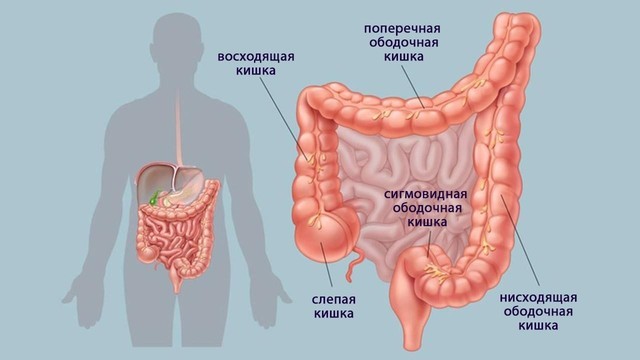
Рисунок 1. Толстый кишечник - это продолжение тонкого кишечника. Именно здесь происходит формирование каловых масс. Он разделяется на ободочную (в нее входят слепая, восходящая, поперечная, нисходящая и сигмовидная кишки) и прямую кишку. Стенка кишки, в свою очередь, состоит из слизистого (внутреннего), мышечного (среднего) и серозного (наружного) слоев. Источник
Оставшиеся 2–4% кишечной микрофлоры составляют условно-патогенные микроорганизмы (УПМ) – протеи, кампилобактер, некоторые стрептококки, цитробактер, дрожжеподобные грибки.
При иммунных сбоях в организме, переедании, заболеваниях органов пищеварения, попадании патогенных микроорганизмов соотношение между нормальной и условно-патогенной флорой изменяется, и количество УПМ превышает допустимые нормы. В этом случае любой негативный фактор, как спусковой крючок, может запустить процесс воспаления. Дисбиоз, таким образом, одна из главных причин возникновения колита.
Причины колита
Важно! Для полноценного излечения важно знать конкретную причину появления колита. Выявить ее может только врач совместно с пациентом. В развитии заболевания большую роль играют пищевые и поведенческие привычки.
Возможными причинами колита могут быть:
- Инфекции. Связаны с попаданием и размножением в кишечнике патогенных микроорганизмов или паразитов: возбудители дизентерии, иерсиниоза, золотистого стафилококка, лямблии, аскариды, амебы и др. Условно-патогенная флора также может стать причиной воспаления толстого кишечника, если начнет преобладать.
- Патология желудочно-кишечного тракта – гастриты, язвенная болезнь, холециститы и панкреатиты, желчнокаменная болезнь, энтериты. Такой колит называют вторичным.
- Наличие любых очагов хронической инфекции, из которых возбудители могут попасть в кишечник (гнойничковые болезни кожи, воспаления дыхательных путей и ЛОР-органов, туберкулез).
- Пренебрежение правилами здорового питания. Это частое переедание, злоупотребление острой и жареной пищей, сладостями и мучными изделиями, недостаточное количество клетчатки в пище, употребление некачественных продуктов.
- Частые стрессовые ситуации и эмоционально-психические факторы.
- Аутоиммунные состояния (когда иммунные клетки “по ошибке” атакуют стенки кишечника) и системные поражения соединительной ткани, предрасположенность к которым часто передается по наследству.
- Лекарственные и токсические нагрузки на организм: прием антибиотиков, противовоспалительных средств, обезболивающих, гормональных препаратов, слабительных, алкоголя. Так, на фоне приема антибиотиков может возникнуть псевдомембранозный колит (антибиотик-ассоциированная диарея), который провоцируется клостридиями – представителями условно-патогенных бактерий кишечника. Под действием антибиотиков и на фоне разрушения полезных микроорганизмов клостридии кишечника размножаются и переходят в токсинообразующую форму, повреждая слизистую толстой кишки.
- Травмы или оперативные вмешательства на органах брюшной полости, когда вследствие спаечного процесса нарушается нормальная анатомия кишки.
Еще одна причина воспаления – врожденные и наследственные патологии кишечника, которые сопровождаются его удлинением или расширением (мегаколон, долихосигма), формированием полипов в просвете кишечника или дивертикулов (выпячивание стенки кишечника в брюшную полость), патологической подвижностью различных отделов кишечника, ферментативной недостаточностью, глютеновой энтеропатией (непереносимостью глиадина – белка злаков).
Виды и формы колита
Существуют различные классификации колитов, основанные на характере течения болезни, причинах ее возникновения, степени тяжести, локализации и так далее.
По течению колит различают на:
По характеру патологических изменений в стенке толстой кишки и глубине поражения различают колиты:
- Катаральный – начальная стадия воспаления, когда в процесс вовлекается только слизистая оболочка. Возникает ее отек, нарушение функции. Чаще протекает в острой форме, сопровождается болями, изменением характера стула и учащением дефекации, возможно повышение температуры.
- Эрозивный – нарушается целостность слизистой кишечника. Воспаление глубже, чем при катаральном колите. На внутренней оболочке кишечника формируются эрозии, которые могут трансформироваться в более глубокие дефекты – язвы.
- Язвенный – тяжелая степень воспаления, при которой поражены все слои кишечника. Образующиеся язвы (рис. 2) могут кровить и создавать угрозу перитонита – тяжелого состояния, связанного с воспалением всей брюшной полости.
- Спастический. Связан со спазмами гладкомышечной мускулатуры и нарушением перистальтики (двигательной функции кишечника). В результате этого возникают запоры, чувство неполного опорожнения кишечника.
- Атрофический – колит, при котором в результате длительных спазмов и застоя кала или системных заболеваний соединительной ткани происходит истончение слизистого и мышечного слоев кишечника. На фоне атрофического колита часто появляются язвы.
- Диффузный. В этом случае воспаляются тонкий и толстый кишечник – развивается энтероколит.
Симптомы
Ведущий признак всех колитов – тупая или схваткообразная боль в животе. Локализация боли зависит от того, какой участок кишечника воспален. Болеть может в области пупка, правой подвздошной области, левом подреберьи и по всему животу. После отхождения газов и похода в туалет обычно наступает временное облегчение, а после еды боль, наоборот, усиливается. Помочь снять болевой симптом могут также спазмолитики и теплый компресс.
Важно! Боль при движениях, ходьбе, беге, тряске и натуживании свидетельствует о тяжелом колите, при котором воспаляется серозная оболочка, покрывающая кишечник снаружи.
Кроме болевого синдрома, колитам свойственны:
Особая форма колита, которая приводит к тяжелым последствиям, инвалидизации и риску летального исхода, – неспецифический язвенный колит (НЯК). Для него характерны:
- диарея частотой 4–8 и более раз в сутки;
- кровь в кале;
- неотложные позывы к дефекации;
- анемия (снижение гемоглобина) в связи с кишечным кровотечением и нарушением всасывания питательных веществ и микроэлементов;
- повышение температуры и учащение пульса при среднетяжелых и тяжелых формах;
- внекишечные проявления в виде артритов, поражения глаз, кожи, щитовидной железы, печени и желчевыводящих путей.
Важно! Колит иногда легко спутать с синдромом раздраженного кишечника, который может вызывать у некоторых людей схожие симптомы. Однако он не связан с воспалением или повреждением тканей кишки. Лечение этих болезней также различается. Другое расстройство с подобными симптомами - целиакия (непереносимость глютена). В этом случае воспаление присутствует, но проходит после отказа от глютеносодержащих продуктов. При возникновении спазмов и болей в животе не пренебрегайте диагностикой, это важный этап лечения, без которого победить болезнь очень трудно.
Диагностика
При подозрении на колит и при его обострении врач рекомендует пациенту следующие исследования:
Лечение
Лечение колита у взрослых проводится комплексно, зависит от выраженности симптомов и причины болезни. При этом назначается определенная диета и медикаментозные средства. Санаторно-курортное лечение может быть эффективным при стихании обострения или в межрецидивный период.
Диета
Избавление от колита немыслимо без соблюдения рекомендаций по питанию. Предпочтение отдается отварным, паровым или запеченным без корочки блюдам. Приветствуется подогретая жидкая и протертая еда с кратностью приема 4–6 раз в сутки малыми порциями. Переедание и голодание крайне неблагоприятно сказывается на течении колитов. При избыточном метеоризме не показаны продукты, которые содержат углеводы и молоко.
Важно! Цель диеты – снизить нагрузку на ЖКТ, ускорить заживление слизистой. Вся употребляемая пища должна быть щадящей и легкоусвояемой, необходимо исключить механические и химические раздражители.
Полезными при колите будут:
- нежирные сорта мяса, рыбы и птицы;
- разваренные каши из гречки, риса, овсяной или манной круп;
- кисели и желе домашнего приготовления;
- подсушенный белый хлеб;
- овощи в отварном и запеченном виде (картофель, кабачки, цветная капуста, тыква, морковь), запеченные яблоки;
- обезжиренный творог и творожные запеканки;
- яйца всмятку или в виде омлета.
Объем потребляемой жидкости должен составлять 1,5–2 л в сутки в виде крепкого чая, отвара шиповника, несладких компотов из яблок, груш, айвы, смородины, некрепкого кофе, какао на воде.
Из десертов не навредит мармелад, пастила, шоколад в малых количествах.
Запрещенные напитки и продукты:
- алкоголь,
- концентрированные соки,
- газированные напитки,
- свежая выпечка и черный хлеб,
- бобовые,
- жирные сорта мяса и рыбы,
- молоко,
- сырые овощи,
- грибы,
- макаронные изделия,
- каши из пшена, пшеницы, ячневой крупы, перловки,
- наваристые бульоны,
- консервы,
- домашние соленья, маринады, пряности,
- копченые и жареные блюда.
Медикаментозное лечение
Для лечения колита используют следующие группы лекарственных средств:
- Антибиотики, нитрофураны и противопаразитарные средства. Назначаются при колитах, которые вызваны патогенной и условно-патогенной флорой, простейшими, глистными инвазиями.
- Средства для восстановления нормальной флоры кишечника:
- пробиотики – препараты, содержащие живые бифидо-, лакто-, колибактерии;
- пребиотики – вещества, которые создают среду для роста полезных бактерий, обладают послабляющим действием, способствуют выведению токсинов;
- синбиотики – содержат и пробиотики, и пребиотики.
- Симптоматические средства. Для устранения болей при колитах назначаются спазмолитики, при повышенном газообразовании – симетикон. Для улучшения переваривания пищи рекомендуются ферментные препараты. При колите с учащением стула эффективными будут вяжущие и обволакивающие препараты, сорбенты. Для нормализации стула при запорах назначают средства на основе лактулозы и натрия пикосульфата.
Если ведущей причиной колита выступает ишемия (недостаточность кровообращения в сосудах кишечника), то применяются средства для лечения атеросклероза, антиагреганты для подавления тромбообразования и специфические сердечно-сосудистые препараты. При колитах, связанных со стрессами и нервно-эмоциональным перенапряжением, в комплекс лечения включаются психотропные препараты.
Особого подхода в лечении требует неспецифический язвенный колит. В основе этого заболевания лежит аутоиммунное воспаление, поэтому для лечения НЯК нужны специфические лекарственные средства. К ним относят:
- аминосалицилаты (в виде капсул для приема внутрь, свечей и для клизм);
- глюкокортикостероидные гормоны;
- цитостатики;
- препараты биологической терапии.
Эффект от лечения НЯК наступает не скоро, длительность терапии в среднем составляет от 12 недель до 2 лет. После устранения симптомов язвенного колита требуется длительное поддерживающее лечение для исключения частых обострений и предотвращения осложнений заболевания.
Могут ли помочь народные средства в лечении колитов?
Для излечения важно поставить диагноз, выявить и устранить причинный фактор. При этом для снятия неприятных симптомов колита могут быть полезны народные средства. Теплый травяной чай или настой из ромашки, фенхеля, мяты, тмина, шалфея, тысячелистника снимают спазмы в кишечнике и ослабляют метеоризм, обладают легким противовоспалительным эффектом.
Для устранения запоров применяют кору крушины, лист сенны, семя льна, душицу, солодку. Вяжущим действием обладают кора дуба, корка граната, черемуха.
Что будет, если колит кишечника не лечить? Осложнения
Длительное хроническое воспаление в толстом кишечнике может привести к неприятным последствиям. Это:
- Астеноневротический синдром с повышенной утомляемостью и слабостью, снижением работоспособности.
- Энтероколит – воспаление толстого и тонкого кишечника. При этом возникают анемия, синдром витаминной недостаточности и нарушения всасывания питательных веществ, что отражается на работе всех систем организма, состоянии кожи, ногтей и волос.
- Непроходимость кишечника. Провоцируется атрофическими и спастическими колитами, аномалиями кишечника и нарушением его подвижности. Непроходимость кишечника сопровождается риском перитонита и требует неотложного хирургического вмешательства.
- Прободение язв кишечника с возникновением состояний, угрожающих жизни. Это кишечное кровотечение, возникновение перитонита и угроза сепсиса – заражения крови.
Важно! Если не лечить колит, есть риск возникновения рака кишечника. Более частая трансформация в рак возникает при язвенном колите.
Профилактика
Колит часто имеет хроническое течение. Для предупреждения обострений или предотвращения этого заболевания важно:
- Соблюдать рекомендации по здоровому питанию: не переедать, не злоупотреблять жирными, жареными, копчеными продуктами, специями, острыми, солеными и консервированными продуктами, сладостями, алкоголем и газированными напитками, фастфудом.
- Не употреблять несвежие продукты, недостаточно термически обработанные мясо и рыбу, немытые овощи, ягоды и фрукты.
- Не заниматься самолечением, особенно антибиотикотерапией.
- Своевременно диагностировать и лечить любую другую патологию ЖКТ, которая провоцирует вторичный колит кишечника.
- Заниматься физкультурой и хорошо высыпаться.
Для поддержания нормальной микрофлоры кишечника следует употреблять кисломолочные продукты, достаточное количество клетчатки (если нет обострения колита). Среди таких продуктов: овощи, фрукты и ягоды, сухофрукты, крупы, бобовые, зерновой хлеб.
Важно! Клетчатка представляет собой сложный углевод, который не ферментируется пищеварительными соками. Она нужна для нормальной работы желудочно-кишечного тракта и поддержания микрофлоры.
Также полезными могут быть препараты на основе пищевых волокон, например, псиллиум (шелуха семян подорожника), который нормализует перистальтику кишечника, частоту и объем стула.
Заключение
Многообразие причин колита, риск осложнений – основание для того, чтобы пациент обратился за квалифицированной помощью, прошел полноценное обследование и лечение. Но даже лучшие препараты и опытные специалисты не смогут побороть болезнь, если пациент пренебрегает правильным питанием и здоровым образом жизни.
Читайте также:

