Язвенно некротический колит диета
Обновлено: 19.04.2024
Что такое колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Куракина Александра Анатольевича, проктолога со стажем в 11 лет.
Над статьей доктора Куракина Александра Анатольевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Колит (лат. colitis, от греч. kolon (толстый кишечник) и itis (воспаление) — собирательное понятие, включающее большую группу заболеваний с одним общим признаком: воспалением толстого кишечника.
Основные признаки колита: частый жидкий стул с кровью, боль в животе и высокая температура.
Колиты встречаются в практике гастроэнтерологов, инфекционистов, терапевтов, колопроктологов, хирургов и других специалистов.
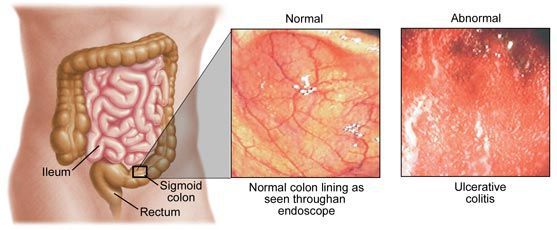
Этиология колита
Основные формы колитов можно описать только по отдельности, в зависимости от этиологического фактора. Размеры статьи не позволяют коснуться всех видов колита. Рассмотрим только основные из них.
Инфекционный колит — это заболевание кишечника, возникающее из-за активизации условно-патогенных микроорганизмов в кишечнике или попадания новых болезнетворных микробов из внешней среды. [1]
Инфекционный колит имеет очень широкое распространение: нет человека, ни разу не переносившего данное заболевание. Количество заболевших увеличивается в жаркий период, когда создаются благоприятные условия для распространения инфекции. Поэтому чаще болеют люди в регионах с жарким климатом (Африка, Юго-Восточная и Средняя Азия). Заболевание чаще встречается в детском возрасте, особенно у детей, посещающих учебные заведения (детские сады, школы и т. д.). Гастроэнтерологи и проктологи могут встречать в практике больных с данной патологией, но она не является профильной. Лечат заболевание обычно инфекционисты.
Причины инфекционного колита:
- бактерии (шигеллы, эшерихии, сальмонеллы, клостридии, иерсинии, брюшнотифозная палочка, кампилобактерии, протей, стафилококки);
- вирусы (аденовирус, энтеровирус, ротавирус);
- простейшие (амебы, лямблии и др.);
- возбудители туберкулеза и сифилиса;
- грибки (кандида, актиномицеты). Возникновение грибкового колита свидетельствует о снижении иммунитета и часто проявляется у лиц, страдающих СПИДом, получающих химиотерапию, стероидные гормоны;
- дисбактериоз.
Формы инфекционного колита:
- катаральная;
- фиброзная;
- катарально-геморрагическая;
- флегмонозная;
- флегмонозно-гангренозная;
- некротическая.
Воспалительные явления могут иметь стадийный характер, а могут сразу иметь картину запущенного воспаления. Его выраженность напрямую зависит от характера инфекции. Некротическое и флегмонозно-гангренозное воспаление встречается при клостридиальной инфекции. Катарально-геморрагическое — при дизентерии. Катаральное воспаление встречается чаще при вирусных заболеваниях. [2]
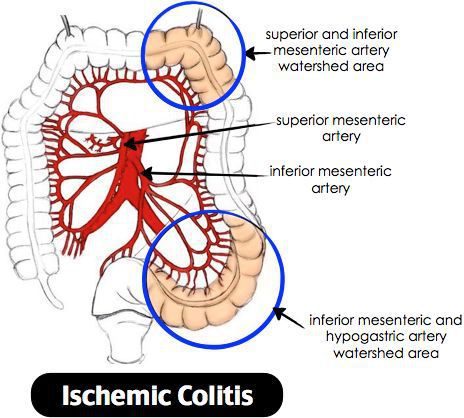
Ишемический колит — воспаление стенки толстого кишечника, возникающее из-за нарушения процессов кровобращения. Существует хроническое и острое нарушение кровообращения. [3]
Причиной нарушения кровообращения является полное прекращение или критическое снижение притока крови к толстой кишке, вследствие чего возникает воспаление. При тяжёлом течении может приводить к некрозу стенки кишечника. Причиной закупорки сосудов могут быть тромбы, но чаще всего к сужению просвета сосуда приводят атеросклеротические бляшки. Поэтому болезнь чаще проявляется у лиц пожилого возраста. Около 79% больных ишемическим колитом старше 48 лет. [4] Частота встречаемости не имеет связи с половой принадлежностью и регионом. Впервые открыт в 1966 году. Ишемический колит является профильным заболеванием для колопроктологов, но им также занимаются общие хирурги и гастроэнтерологи. [5]
Причины ишемического колита:
-
сосудов;
- закупорка брыжеечных сосудов вследствие эмболии или тромбоэмболии (в результате аллергических реакций, травм, осложнений операций, системного васкулита, ДВС-синдрома);
- снижение давления крови может приводить к нарушению питания стенки кишки.
Закупорка просвета сосуда приводит к ишемии стенки кишки, а как следствие — к некрозу и далее перфорации. [6]
Объём поражения зависит от размера питающей артерии, длительности закупорки. Если закупорка сосуда происходит постепенно (при образовании атеросклеротических бляшек в сосудах), то говорят о хроническом нарушении кровообращения, что в свою очередь приводит к стриктурам.
При критических состояниях и снижении давления крови (например, анафилактический шок, ДВС-синдром и т.д.), происходит централизация кровообращения, при этом резко снижается приток крови к кишечнику, что приводит к ишемии и некрозу.
При атеросклерозе чаще страдает сигмовидная и поперечная ободочная кишка. Воспаление начинается со слизистой оболочки, затем переходит на все слои. [7]
По характеру поражения выделяют:
- транзиторную форму (когда ишемические процессы обратимы);
- стенозирующую (когда формируются стриктуры);
- гангренозную (когда образуются язвы с дальнейшим развитием некроза, поражение носит необратимый характер). [8]
Лучевой колит — образуется в результате ионизирующего воздействия на стенку толстого кишечника.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы колита
Симптомы острого и хронического колита: боль в животе, кровь в кале, диарея, высокая температура, слабость, слизь и кровь в стуле, спазмы.
Симптомы язвенного колита: к перечисленным выше признакам добавляются боли в анусе и анемия.
Боли при колите кишечника:
Инфекционный колит
Клиника инфекционного колита напрямую зависит от возбудителя.
Для любого инфекционного колита независимо от этиологии характерно:
- начало заболевания, как правило, имеет острый характер;
- жидкий частый стул с примесью слизи в кале;
- боли локализуются чаще в левом подреберье, но могут также распространяться по всем отделам живота;
- боль имеет периодический, спазматический характер;
- высокая температура;
- чувство слабости, недомогания;
- сухость кожных покровов и слизистых;
- белый налет на корне языка;
- рвота как первый симптом колита кишечника (если в воспалительный процесс вовлечен желудок).
Для первичной оценки этиологии инфекционного колита оценивают характер дефекации, объём и особенности каловых масс.
Ишемический колит
Симптоматика очень вариабельна, характерно быстрое прогрессирование.
- болезненные ощущения в животе;
- кровь и слизь в стуле;
- неустойчивый, частый стул;
- выраженные боли в околопупочной и левой подвздошной области;
- при ректальном осмотре можно заметить кал с кровью, слизью или гноем;
- при хронической форме боли имеют низкую интенсивность, обычно возникают после еды;
- при длительной хронической ишемии появляются стриктуры в толстой кишке, которые в дальнейшем могут быть следствием непроходимости или малигнизации (раковому перерождению).
Лучевой колит
Обычно колит формируется у лиц, перенёсших курс лучевой терапии по поводу новообразований, локализующихся в области малого таза или брюшной полости. [12]
- большую чувствительность к излучению имеет тонкий кишечник, формируется лучевой энтерит, который клинически проявляется нарушением абсорбции в тонком кишечнике;
- повреждению кишечника свойствен избирательный характер, обычно воспаление локализуется в прямой и сигмовидной кишке, при этом клиника сопоставима с клиникой язвенного и ишемического колита. При воздействии больших доз радиации клиника развивается не сразу, проявляется обильным, жидким стулом, при этом нарушается всасывание в толстом кишечнике. [13]
Патогенез колита
Толстый кишечник очень восприимчив к ионизирующему излучению. [10] Лучевой колит возникает при воздействии малых доз облучения: происходит атрофия слизистой оболочки (сразу после облучения).
- Усиливаются процессы деления клеток, уменьшается длина ворсинок.
- Активизируются воспалительные процессы с нейтрофильной реакцией. Чаще всего эти процессы локализуются в прямой и сигмовидной кишке.
- При воздействии больших доз (более 40 Гр.) воспалительные процессы могут возникать спустя длительное время после облучения (до нескольких лет), в данной ситуации происходит воспаление мелких сосудов кишечника, что приводит к ишемизации кишечника. Развиваются язвы и стриктуры. Могут поражаться все отделы толстого и тонкого кишечника. [11]
Классификация и стадии развития колита
По течению:
По этиологии:
- язвенный колит кишечника и болезнь Крона (воспалительные заболевания кишечника с неизвестной этиологией);
- инфекционный (этиологический фактор бактериальный, вирусный, грибковый, паразитарный);
- ишемический (развивается вследствие снижения притока крови к толстой кишке);
- спастический (из-за неправильного питания нарушается моторика толстого кишечника и возникают спазмы);
- токсический (при применении нестероидных противовоспалительных препаратов);
- лучевой (при поражении радиацией).
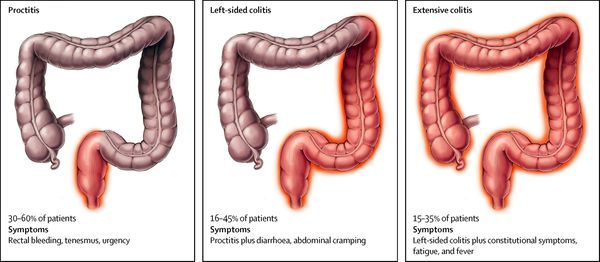
По локализации:
| Вид колита | Локализация |
|---|---|
| проктит | воспаление прямой кишки |
| панколит | тотальное поражение кишечника |
| тифлит | воспаление слепой кишки |
| трансверзит | воспаление поперечной ободочной кишки |
| сигмоидит | воспаление сигмовидной кишки |
| диффузный колит кишечника | охватывает два и более отдела кишечника |
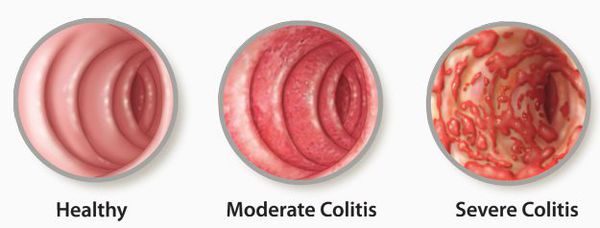
Поражение кишечной стенки подразделяют на три вида:
- катаральный колит кишечника — слабое воспаление, слизистая краснеет, и возникает отёк;
- эрозивный колит кишечника — появляются эрозии;
- атрофический колит кишечника — слизистая атрофируется.
Осложнения колита
- сильное кровотечение;
- перфорация толстой кишки;
- сильное обезвоживание; ;
- воспаление кожи, суставов и глаз;
- повышенный риск рака толстой кишки;
- токсичный мегаколон;
- повышенный риск образования тромбов в венах и артериях [15] .
Диагностика колита
Инфекционный колит:
- Лабораторные методы:
- анализ кала на вирусы, бактерии, паразиты (позволяет точно поставить диагноз);
- серологическое исследование (определяют антитела к вирусам, паразитам);
- анализ крови на стерильность (при подозрении на сепсис);
- общеклинический анализ крови (высокое СОЭ, увеличение количества лимфоцитов при вирусной этиологии).
- Инструментальные методы:
- ректороманоскопия используется как дополнительный метод для дифференциальной диагностики;
- ультразвуковое исследование используется для исключения осложнений.
Ишемический колит:
- Ректороманоскопия дает возможность оценить состояние слизистой оболочки. При осмотре можно отметить наличие точечных кровоизлияний, сглаженность сосудистого рисунка, бледность слизистой. При обнаружении данных признаков показано взятие биопсии.
- Ирригоскопия — самое необходимое исследование. Обнаруживается симптом пальцевых вдавливаний. Признаки дефектов слизистой свидетельствуют о наличии язв, сужения просвета при стриктурах.
- Колоноскопия показана для уточнения распространенности воспаления, также показана биопсия в области измененного участка.
- Ангиография позволяет определить степень сужения сосуда и его локализацию. [9]
- Злокачественные новообразования. Опухоли развиваются достаточно длительное время, в течении многих лет.
- Инфекционный колит. Преобладают симптомы общей интоксикации (слабость, лихорадка и т.д.). Кроме того, имеет место эпидемический анамнез.
- Язвенный колит и болезнь Крона. Для них характерно достаточно медленное прогрессирование. Проявляются обычно в раннем возрасте.
Лучевой колит:
- При сборе анамнеза учитывают наличие факта облучения ионизирующей радиацией.
- Ректороманоскопия и колоноскопия с биопсией позволяют выявить воспаление слизистой оболочки толстого кишечника. При лучевом энтерите воспаление сочетается с атрофией слизистой. Крипты становятся менее глубокими, уменьшается длина ворсинок. При лучевом колите на слизистой обнаруживают язвы, стриктуры. [14]
- Энтерит лучевого генеза следует дифференцировать с болезнями тонкой кишки, при которых страдает функция всасывания (целиакия), при данных заболеваниях происходит атрофия по гиперрегенераторному типу, а при лучевом поражении преобладают гипорегенераторные процессы слизистой.
- Радиационные поражения толстого кишечника дифференцируют с язвенным колитом, болезнью Крона, новообразованиями толстого кишечника. [15]
Лечение колита
Инфекционный колит:
- антибактериальные, противогрибковые средства с учетом чувствительности микроорганизмов. Предпочтение отдают таблетированным формам препаратов;
- восполнение потерянной жидкости и минералов: растворами для приема внутрь (Регидрон и др.), внутривенное введение (раствор Рингера, Трисоль и др.);
- прием сорбентов;
- пробиотики и пребиотики;
- ферменты (креон, фестал);
- симптоматическая терапия (противовоспалительные средства, спазмолитики и др.)
Ишемический колит:
- консервативное лечение колита (щадящая диета, препараты, смягчающие стул, лекарства для улучшения кровотока, дезагреганты, витаминные препараты, дезинтоксикационное лечение, восполнение баланса электролитов и жидкости, гемотрансфузии (при показаниях), антибактериальные препараты);
- оперативное лечение колита.
Показаниями для срочного хирургического лечения служат:
- перфорация, толстокишечная непроходимость. В таком случае удаляется участок кишки, с последующей санацией и дренированием брюшной полости.
- плановое оперативное лечение колита кишечника показано больным в случае сужения (стриктуры) толстого кишечника без явлений острой кишечной непроходимости.
Терапия лучевого колита схожа с терапией язвенного колита и болезни Крона:
- лекарства, содержащие 5-аминосалициловую кислоту (месалазин, салофальк);
- антибактериальная терапия.
Может быть полезно вести дневник питания, чтобы отслеживать, что вы едите, а также свои чувства. Если вы обнаружите, что некоторые продукты вызывают обострение ваших симптомов, вы можете попробовать их устранить.
Диетотерапия
Убедительных доказательств того, что неправильное питание приводит к воспалению кишечника, нет. Но оно может усугубить симптомы болезни, особенно при обострении. Поэтому полезно вести дневник питания и отслеживать свои реакции на определённые продукты.
- есть меньше молочных продуктов — у пациента может быть непереносимость лактозы, т. е. организм не переваривает молочный сахар;
- есть небольшими порциями по 5–6 раз в день;
- пить больше жидкости — предпочтительнее вода; алкоголь и напитки, содержащие кофеин, стимулируют кишечник и могут усилить симптомы болезни [15] .
Прогноз. Профилактика
На сегодняшний день хорошо известны причины возникновения инфекционного колита, разработаны современные методики лечения. Поэтому при неосложненном течении и вовремя начатой терапии удается достигнуть полного выздоровления. Менее благоприятный прогноз у лиц с явлениями иммунодефицита и ослабленной иммунной системой (например, у людей пожилого возраста). Прогноз благоприятный.
Основными методами профилактики являются:
- гигиенические мероприятия (тщательное мытье рук);
- использование только свежих продуктов, чистой воды;
- уделение особого внимания термической обработке пищи.
При транзиторной форме ишемического колита прогноз благоприятный. При гангренозной форме — зависит от вовремя поставленного диагноза и проведенного лечения.
Так как ишемический колит является осложнением других болезней, то для его профилактики необходимо:
- своевременное лечение сопутствующих заболеваний;
- сбалансированное питание.
Лучевой колит приводит к постоянным, необратимым изменениям кишечной стенки, поэтому прогноз неблагоприятный.
При радиационном колите могут появляться язвы и стриктуры на слизистой оболочке толстого кишечника, что может привести к кишечной непроходимости. В таком случае необходимо хирургическое лечение, от своевременности которого зависит прогноз. При правильном и вовремя проведенном лечении прогноз благоприятный. Специальных методов профилактики лучевого колита не существует.
Что такое псевдомембранозный колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Аверина Александра Анатольевича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Аверина Александра Анатольевича работали литературный редактор Вера Васина , научный редактор Роман Васильев и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Псевдомембранозный колит (Pseudomembranous colitis) — это острое воспалительное заболевание толстого кишечника, вызываемое токсигенными штаммами бактерии Clostridium difficile [1] . Микроб вырабатывает токсины А и В, повреждающие кишечную стенку, и белок, угнетающий перистальтику кишечника. В результате возникает диарея, боль в животе, появляется слизь и иногда примесь крови в кале.
Характерным признаком заболевания являются фиброзные наложения на слизистой оболочке толстой кишки [27] [28] .

Псевдомембранозный колит (ПМК) чаще всего развивается после лечения антибиотиками. Его ещё называют Clostridium difficile-ассоциированным псевдомембранозным колитом, антибиотик-ассоциированным псевдомембранозным и клостридиозным колитом.
Эпидемиология
Заболеваемость ПМК лучше всего отслеживается в США и странах западной Европы [2] . В России статистический учёт заражения C. diff не ведётся. Согласно систематическому обзору за 2011 год, каждый 5-й случай из всех антибиотик-ассоциированных диарей (ААД) и каждый 2–3 случай внутрибольничной ААД в странах Европы и Северной Америки вызваны C. diff [3] .
В стационарах США среди внутрибольничных инфекций C. diff занимает первое место (12,1 % от общего количества), опережая K. pneumoniae (9, 7 %) и E. coli (9,3 %) [4] . В 2011 г. было зафиксировано более 450 тыс. случаев C. difficile-ассоциированной болезни и более 29 тыс. смертей от неё [29] .
В европейских странах заболеваемость C. diff составляет около 7 случаев на 10000 койко-дней, т. е. при средней госпитализации 10 дней, 7 случаев из 1000 госпитализаций заканчиваются ПМК. В 20 европейских странах это значение колеблется от 0,7 до 28,7 на 10000 койко-дней [5] .
В России в 2011 году было продано 295 млн упаковок антибиотиков, в 2019 — 379 млн [8] [26] . Антибактериальных препаратов потребляется всё больше, их продажа из аптек не контролируется, поэтому проблемы ААД и ПМК актуальны и в нашей стране.
В клиниках Санкт-Петербурга у пациентов с ААД тест на токсины C. diff был положительным в 47,7 % случаев [6] .
Смертность от ПМК колеблется от 9,3 до 22 % и зависит от возраста пациента, смерть чаще наступает при тяжёлом течении заболевания [7] [26] .
В настоящее время увеличилась внутри- и внебольничная заболеваемость C. difficile-ассоциированной болезнью, расширились группы риска, стали чаще встречаться рецидивы и тяжёлые формы, в том числе вызванные более патогенным штаммом BI/NAP1/027, возросла смертность [27] .
Причины псевдомембранозного колита
Основная причина болезни — это приём антибиотиков. ПМК могут вызывать любые антибактериальные препараты, но наиболее часто к нему приводит применение Клиндамицина, хинолонов, цефалоспоринов 2-го и 3-го поколения, карбапенемов. Реже ПМК развивается после приёма макролидов, пенициллина, Тетрациклина, Тигециклина.
К факторам риска, помимо приёма антибиотиков, относятся:
- возраст старше 65 лет;
- терапия ингибиторами протонной помпы и Н2-гистаминоблокаторами — препаратами, снижающими секрецию соляной кислоты в желудке;
- лечение в стационаре, особенно в отделениях реанимации, — каждые 7 дней госпитализации увеличивают риск ПМК на 8 % [1][9][10] ;
- наличие дополнительной патологии, в том числе воспалительных заболеваний кишечника, ВИЧ, сахарного диабета[31][32][33] ;
- хирургические вмешательства на органах ЖКТ;
- энтеральное питание, в том числе через назогастральный зонд;
- приём иммуносупрессивных препаратов (глюкокортикостероидов, Такролимуса) и противоопухолевых средств [31] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы псевдомембранозного колита
Наиболее частые симптомы лёгкого или умеренного псевдомембранозного колита:
- водянистая диарея (жидкие испражнения, похожие на кашицу) от трёх раз в сутки на протяжении двух и более дней в сочетании с болью в животе;
- лёгкие спазмы в животе, часто сопровождающиеся с позывами на стул, но не всегда приводящие к дефекации;
- примеси слизи, крови или гноя в испражнениях;
- температура тела 38,5 °С и более;
- тошнота или потеря аппетита.
При тяжёлом течении псевдомембранозного колита возникает водянистая диарея с кровью, уровень альбумина снижается менее 30 г/л, что сочетается с одним из следующих симптомов: высоким уровнем лейкоцитов в клиническом анализе крови (> 15×10 9 /л) и/или болезненностью при ощупывании живота. На фоне длительной диареи организм теряет много жидкости, что приводит к обезвоживанию и проявляется тёмно-жёлтой мочой, чувством жажды, усталости, головокружением, спутанностью сознания и заторможенностью [1] [9] .
При рецидиве болезни симптомы появляются повторно менее чем через 8 недель после окончания терапии.
Проявления псевдомембранозного колита схожи с симптомами других инфекций, поражающих толстый кишечник. Но в отличие от них признаки ПМК могут быть слабо выражены и, как правило, наблюдаются долго: от одной недели до нескольких месяцев. Также встречаются случаи, когда человек является носителем возбудителя ПМК — C. diff, но симптомы полностью отсутствуют.
Патогенез псевдомембранозного колита
В основе патогенеза ПМК лежит чрезмерное размножение бактерий C. diff на фоне уменьшения или гибели нормальной микробиоты толстого кишечника. C. diff вырабатывает токсины А и В, которые вызывают воспаление в кишечной стенке. На течение заболевания влияет состояние иммунной системы пациента и патогенные свойства бактерий, такие как вирулентность, наличие токсинов А и В.
Основной путь передачи инфекции — фекально-оральный. Бактерии попадают в организм с загрязнённых поверхностей, например с дверных ручек, смесителей, ручек смыва сливного бачка, мебели или медицинского инвентаря. Также переносить инфекцию может персонал больницы и заражённые пациенты.
Бактерии C.diff образуют споры, которые устойчивы к действию антибиотиков и могут длительно сохраняться в желудочно-кишечном тракте человека, заражая окружающих и вызывая рецидивы заболевания у самого пациента [12] .
Для некоторых людей C.diff — это часть нормальной микрофлоры ЖКТ, но в таком случае численность бактерий контролируется за счёт других микроорганизмов и работы иммунной системы.
Основные поражающие факторы C.diff — это выделяемые ею токсины [1] . Токсин А (энтеротоксин, белковая молекула с массой 308 кДа) влияет на секрецию жидкости, приводит к повреждению слизистой оболочки кишечника (мембран клеток) и вызывает воспалительный ответ со стороны иммунной системы.

Токсин В (цитотоксин, белковая молекула с массой от 250 до 270 кДа) в 1000 раз более цитотоксичен по сравнению с токсином А. Он вызывает распад филаментного актина — белка, поддерживающего целостность клеток. В результате клетки слизистой разрушаются и гибнут. Токсин В опасен для человека, но не приводит к воспалению и повреждению слизистой оболочки кишечника у животных.
Под действием токсинов в кишечной стенке развивается специфическое воспаление с характерными изменениями на поверхности слизистой. Она становится отёчной, разрыхляется, приобретает ярко-красный цвет, на ней исчезает сосудистый рисунок. При контакте эндоскопа со слизистой капельки крови не появляются. Наблюдается множество желтовато-белых бляшек диаметром 3–5 мм, которые плотно фиксированы к слизистой оболочке. При взятии биопсии они отрываются с трудом, торцом эндоскопа не снимаются. Преобладает два типа воспалительных реакций: диффузно-катаральное воспаление слизистой и очаги фибриноидного некроза — бело-жёлтые бляшки, или псевдомембраны, поэтому такой тип колита называется псевдомембранозным.
![Бляшки при ПМК [35]](https://probolezny.ru/media/bolezny/psevdomembranoznyy-kolit/blyashki-pri-pmk-35_s.jpg)
В биоптатах, полученных из воспалительно-изменённых участков слизистой, выявляют скопление иммунных клеток крови и слизистой, расширение капилляров и некроз клеток покровного эпителия [1] .
В биоптатах, взятых из бляшек, присутствует фибрин, обрывки некротизированного покровного эпителия, слизь, лейкоциты, плазматические клетки и колонии бактерий.
Чтобы определить патогенность клостридий, нужно выявить их токсины. Посев биоптатов на питательные среды удовлетворительных результатов не даёт. Метод в данном случае затратен и неинформативен, поэтому токсины C. diff определяют в кале.
Воспалительный процесс, как правило, захватывает несколько отделов толстого кишечника, но чаще поражена его прямая и сигмовидная часть, реже вовлекается вся толстая кишка. Протяжённость её поражения связана с тяжестью течения заболевания: чем больше толстого кишечника вовлечено в воспалительный процесс, тем тяжелее протекает колит и ярче симптомы.
Продолжительное воспаление в кишечной стенке приводит к следующим нарушениям:
- не всасывается жидкость, из-за чего развивается обезвоживание;
- потери крови из образующихся эрозий и язв приводят к анемии;
- кишечная стенка становится проницаемой для токсинов возбудителя и продуктов его жизнедеятельности, находящихся в просвете кишки, из-за чего нарастает общая интоксикация.
При тяжёлом течении прекращается перистальтика толстого кишечника, развивается токсический мегаколон и возникает полиорганная недостаточность, из-за чего пациент может погибнуть.
Классификация и стадии развития псевдомембранозного колита
ПМК входит в группу антибиотик-ассоциированных диарей. В Международной классификации болезней (МКБ-10) псевдомембранозный колит кодируется как АО 4.7 — Энтероколит, вызванный Clostridium difficile.
В зависимости от тяжести течения болезни и клинической картины выделяют следующие формы:
- ПМК лёгкой или умеренной тяжести. Проявляется диареей — неоформленным жидким, кашицеобразным стулом три или более раз в сутки и болью в животе.
- ПМК тяжёлого течения. Сопровождается водянистой диареей с кровью и изменениями в анализах. В биохимическом анализе крови отмечается низкий уровень альбумина (меньше 30 г/л), который сочетается с одним из следующих признаков: высоким уровнем лейкоцитов в клиническом анализе крови (> 15×10 9 /л) в клиническом анализе крови и/или болезненностью при ощупывании живота.
- Осложнённые формы ПМК. Протекают с водянистой диареей с кровью и одним из следующих симптомов: снижение артериального давления, температура тела ≥ 38,5 °C, отсутствие перистальтики тонкого кишечника, помрачение или угнетение сознания. В клиническом анализе крови лейкоциты повышены > 25×10 9 /л или снижены < 2×10 9 /л, возникает органная и почечная недостаточность, требуется искусственная вентиляция лёгких.
- Рецидивирующее течение ПМК. Заболевание развивается повторно менее чем через 8 недель после окончания терапии [1][14] .
Данная классификация используется для выбора схемы лечения.
Осложнения псевдомембранозного колита
Наиболее частые осложнения псевдомембранозного колита:
- Обезвоживание и электролитные нарушения — из-за сильной и длительной диареи нарушается ритм сердца, снижается артериальное давление и мышечный тонус. Чаще эти осложнения развиваются при недостаточном восполнении потерянной жидкости и солей.
- Почечная недостаточность — при стремительном обезвоживании нарушается работа почек, из-за чего снижается частота мочеиспусканий, появляются отёки, по анализам крови видно, что растёт содержание азотистых шлаков.
- Токсический мегаколон — расширение толстой кишки, редкое осложнение с плохим прогнозом. На фоне диареи частота стула резко урежается до одного раза в сутки, в дальнейшем дефекация прекращается полностью. Это происходит из-за замедления и полного прекращения перистальтики толстого кишечника. Из-за распирания толстого кишечника газами и содержимым нарастает вздутие живота, усиливается боль в нём. Интоксикация и электролитные нарушения приводят к резкому ухудшению самочувствия и выраженной слабости. В дальнейшем стенка кишки разрывается, содержимое изливается в брюшную полость (перфорация кишечника) и начинается перитонит. Как правило, это осложнение наблюдается у ослабленных пациентов, находящихся в отделении реанимации и хирургии.
- Перфорация кишечной стенки — образуется сквозное отверстие в кишечной стенке с излитием содержимого кишечника в брюшную полость и развитием перитонита.
- Полиорганная недостаточность — может привести к гибели пациента [1][15] .
Диагностика псевдомембранозного колита
Тесты на C. diff показаны при длительной диарее с болью в животе и/или примесью крови в стуле, возникшей спустя 3–60 суток после выписки из стационара и/или после приёма антибиотиков [1] .
Чтобы выявить токсигенные штаммы C. diff, токсины A и B определяют в кале [16] .
Для этого используют следующие методы:
- Цитотоксиновый копрологический тест. Чувствительность — 95 %, специфичность — 99 %, результат — в течение 2–3 дней.
- ELISA (Enzyme Linked Immuno Sorbent Assay) — фермент-связанный иммуносорбентный тест для определения токсинов. Чувствительность — 70–90 %, специфичность — 99 %, результат — через 4–6 часов.
- ПЦР (полимеразная цепная реакция) на токсин В. Чувствительность — 96 %, специфичность — 100 %, результат — в течение нескольких часов.
Чувствительность теста — это доля положительных результатов среди больных людей, т. е. вероятность правильно определить инфекцию у заболевших, отсутствие ложноотрицательных результатов. Специфичность — доля отрицательных результатов среди здоровых людей, т. е. отсутствие ложноположительных результатов.
Посев кала на C.diff не проводится, так как этим методом не удаётся определить токсигенные штаммы.
С помощью дополнительных методов можно оценить тяжесть состояния пациента и своевременно выявить осложнения.
К дополнительным обследованиям относятся:
- ректороманоскопия или сигмоидоскопия — позволяют обнаружить типичные изменения стенки кишки (множественные желтоватые бляшки 2–10 мм в диаметре, плотно фиксированные на поверхности слизистой оболочки);
- колоноскопия — помимо типичных изменений кишечной стенки, определяется распространённость процесса и поражение толстого кишечника выше сигмовидной кишки [17] ;
- обзорная рентгенография органов брюшной полости — используется, чтобы выявить признаки пареза кишечника и токсического расширения кишки;
- анализ крови — показывает уровень лейкоцитов (при ПМК повышен до 10–50 × 10 9 ), уровень креатинина (выше нормы) и альбумина (ниже нормы).
Гистологическое исследование биоптатов не является необходимым при C. difficile-ассоциированной болезни, но может быть крайне важным для дифференциальной диагностики.
Лечение псевдомембранозного колита
Методы лечения псевдомембранозного колита в российских и зарубежных клинических рекомендациях совпадают [1] [18] . При лёгком и среднетяжёлом течении его проводят в амбулаторных условиях (дома), при тяжёлом и/или осложнённом — в стационаре.
Для лечения ПМК назначаются антибиотики:
Антибиотики подавляют развитие C. diff. Бактерия чувствительна только к трём перечисленным антибактериальным препаратам.
При развитии осложнений ПМК могут применяться следующие методы:
- При токсическом мегаколоне показана колэктомия — удаление толстой кишки.
- Для лечения рецидивирующего ПМК в качестве экспериментального метода рассматривается трансплантация кишечной микробиоты (fecal microbiota transplantation, FMT) [23][24][25] . Кишечную микробиоту берут от здорового донора и при помощи назоинтестинального зонда, клизмы или колоноскопии переносят пациенту в кишечник. В России такое лечение считается экспериментальным. Проводится в научных клинических учреждениях, например в Федеральном научно-клиническом центре ФМБА России.

В качестве вспомогательных и симптоматических препаратов используются:
- Сорбенты (Диоктаэдрический смектит) — эффективно удаляет токсины C. diff, снижая их действие на кишечную стенку, улучшает качество стула.
- Пробиотики (Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium bifidum, Bifidobacterium infantis не менее 1×10 9 КОЕ/г) — подавляют активность C. diff. Данные об их эффективности пока противоречивы [22] .
- Препараты на основе дрожжей Saccharomyces cerevisiae (boulardii) — эффективны как вспомогательные и профилактические средства.
Прогноз. Профилактика
При лёгком или среднетяжёлом течении ПМК и хорошей реакции на стандартную терапию прогноз благоприятный, при тяжёлом и осложнённом — неблагоприятный. При рецидивирующем течении прогноз сомнительный, так как не разработаны эффективные схемы лечения.
Профилактика псевдомембранозного колита
Для профилактики развития ПМК следует:
- чаще мыть руки и соблюдать правила личной гигиены;
- рационально принимать антибиотики — строго по назначению врача с соблюдением всех указаний;
- изолировать пациентов с инфекцией C. diff в отдельные палаты, соблюдать меры санитарного режима;
- тщательно обрабатывать все поверхности хлорсодержащими или другими дезинфицирующими средствами, активными против спор C. diff;
- сокращать сроки госпитализации пациентов старше 65 лет [16] .
Чтобы предотвратить рецидив C. difficile-ассоциированной болезни, после завершения лечения Метронидазолом или Ванкомицином назначаются пробиотики курсом не менее трёх месяцев. Серьёзных побочных эффектов от них не выявлено [34] .

Важный вопрос, часто возникающий как у пациентов, так и у врачей — непереносимость молока и продуктов на его основе у больных ВЗК. Отечественные сайты для пациентов часто рекомендуют исключить молоко из рациона, причем абсолютно всем пациентам. Зарубежные авторы (например, эксперты Европейского общества энтерального и парентерального питания), анализируя результаты клинических исследований, советуют ограничивать или исключать молоко только при наличии лактазной недостаточности.
Что такое лактазная недостаточность?
Лактазной недостаточностью называется дефицит фермента лактазы, который в тонкой кишке расщепляет молочный сахар – лактозу. В результате большое количество нерасщепленного молочного сахара накапливается в просвете кишечника, что вызывает диарею, вздутие живота, тошноту, тяжесть и боли в верхних отделах живота.
Известно, что при переходе на взрослый тип питания у части людей активность фермента лактазы может постепенно снижаться. Этот процесс является генетически опосредованным. В результате у человека, который ранее хорошо переносил молоко и молочные продукты, проявляются неприятные симптомы.
Такое состояние называется лактазной недостаточностью (гиполактазией) взрослых.
Лактазная недостаточность взрослых встречается у 90% азиатских народностей и 80% афроамериканцев, в то время как у представителей белой расы в странах Западной и Северной Европы это состояние отмечается достаточно редко – 10-15% случаев.
Как выявить лактазную недостаточность?
Более точный способ — молекулярно-генетическое исследование с определением мутации гена, отвечающего за продукцию фермента лактазы.
Преимущество метода — его малая инвазивность, для исследования требуется лишь небольшое количество крови пациента. Однако наличие мутации гена не всегда отражает истинную активность фермента в тонкой кишке. Активность лактазы на поверхности клеток тонкой кишки может снижаться при болезни Крона, при этом без генетических мутаций.
Золотой стандарт диагностики лактазной недостаточности — определение активности лактазы на поверхности клеток тонкой кишки.
В качестве материала для исследования используются биоптаты слизистой тонкой кишки, получаемые при гастроскопии. Метод позволяет точно установить дефицит фермента лактазы и выявить степень его дефицита.
Как часто лактазная недостаточность встречается при ВЗК?
Как было сказано выше, исключение молока (реже — кисломолочных продуктов) показано пациентам с ВЗК и доказанной лактазной недостаточностью. Но как часто она вообще встречается у таких пациентов? Данные клинических исследований разнятся, вероятно, из-за этнического разнообразия исследуемых групп. Так, при болезни Крона частота выявления лактазной недостаточности дыхательным тестом и/или генетическим исследованием варьирует от 17 до 70% случаев, при язвенном колите дефицит фермента обнаруживается у 4-44% пациентов.
Выявлена закономерность, согласно которой локализация воспалительного процесса в тонкой кишке при болезни Крона чаще сопровождается дефицитом лактазы (100% случаев при поражении тощей кишки, 68% при терминальном илеите, 55% при илеоколите) по сравнению с изолированным поражением толстой кишки (при колите Крона – 43,5%).
Необоснованно исключение из рациона молока и кисломолочных продуктов для всех пациентов с диагнозом ВЗК. Несомненно, пациент с доказанной лактазной недостаточностью требует резкого ограничения цельного молока в рационе. Но если непереносимость молока была выявлена лишь в период обострения ВЗК, то это совсем не означает, что симптомы непереносимости будут сохраняться в период ремиссии. Многие пациенты, испытывающие неприятные симптомы при употреблении цельного молока, хорошо переносят продукты на его основе. К молочным продуктам, которые обычно хорошо переносятся даже при выраженной лактазной недостаточности, относятся йогурт и сыр. В диетотерапии могут быть использованы также безлактозное молоко и продукты на его основе. Некоторые больные с доказанной лактазной недостаточностью хорошо переносят употребление небольших объемов цельного молока (менее 250 мл в сутки) вместе с другой пищей.
ВЗК и кофе

Хотя в России число людей, употребляющих кофе, уступает численности любителей чая, количество жителей нашей страны, выпивающих хотя бы иногда чашечку кофе составляет по разным оценкам 60-75%.
Положительный эффект от употребления кофе доказан для некоторых хронических заболеваний (неалкогольная жировая болезнь печени, сахарный диабет 2 типа, болезнь Паркинсона, запор и т.д.). Крупное проспективное исследование 2012 года (включавшее более 400 тысяч человек) показало снижение общей смертности, частоты смертей от инсульта и сердечных заболеваний у людей, употребляющих кофе.
В число приверженцев кофе входят и пациенты с ВЗК. Как кофе влияет на кишечник? Насколько вредно (или полезно) пить кофе при болезни Крона и язвенном колите?
Кофе оказывает пребиотическое действие, позитивно влияя на кишечную микробиоту, а также обладает антибактериальной активностью, снижая количество кишечной палочки, бактерий рода Clostridium и увеличивая число лакто- и бифидобактерий. Кроме того, описан стимулирующий эффект кофеина в отношении двигательной активности толстой кишки, и увеличение тонуса сфинктера прямой кишки. Исследование 2014 года показало, что у потребления кофе снижает риск развития первичного склерозирующего холангита, который нередко связан с ВЗК.
Употребление кофе не влияет на риск развития ВЗК, хотя в недавнем мета-анализе показана тенденция к снижению риска развития язвенного колита при употреблении кофе.
Швейцарские исследователи в 2015 году, опросив 442 пациента с ВЗК, выяснили что 3/4 респондентов регулярно употребляют кофе. Среди тех, кто не пил кофе совсем либо пил очень редко, 62% объясняли свой отказ от напитка ухудшением симптомов заболевания. Чаще такой ответ давали пациенты с болезнью Крона — 76,4%. С язвенным колитом — 44,4%. Если же оценивать влияние кофе на симптомы у всех 442 больных, то его негативный эффект отметили 45,2% пациентов с болезнью Крона и 20,2% с язвенным колитом.
Других значимых исследований, с применением лабораторных и эндоскопических методов оценки активности заболевания у больных с ВЗК не проводилось. Таким образом, пациенты с болезнью Крона и язвенным колитом могут употреблять кофе, если он не усиливает симптоматики или появлению новых жалоб.
ВЗК и алкоголь

Что мы знаем об алкоголе при ВЗК? Проводились ли какие-либо исследования на эту тему? Как ни странно, проводились (причем достаточно крупные и убедительные).
В 2017 году опубликованы результаты исследования EPIC, в котором приняли участие 262 451 человек (Bergmann MM. и соавт., 2017). Употребление алкоголя участниками исследования было оценено по количеству (не употребляет, употреблял ранее, низкое, умеренное, высокое потребление алкоголя), с учетом норм для мужчин и женщин. С момента наблюдения (т.е. с 1993 года) язвенный колит был впервые выявлен у 198 участников, болезнь Крона — у 84 человек. Проведенный статистический анализ показал, что употребление алкоголя никаким образом не влияет на вероятность развития язвенного колита и болезнь Крона.
Эти результаты позже были подтверждены (правда, лишь для язвенного колита) мета-анализом клинических исследований, в ходе которого проводилась статистическая оценка результатов 9 работ, посвященных изучению алкоголя как фактора риска ВЗК. Результат прежний — употребление алкоголя не является фактором риска возникновения язвенного колита.
А вот хроническое злоупотребление алкоголем (алкоголизм) повышает риск возникновения ВЗК, о чем убедительно говорит исследование китайских авторов. Они проанализировали данные 10-летнего наблюдения почти 58 тысяч случаев госпитализированных лиц с диагнозом алкогольной интоксикации, сравнив их с контрольной группой, не злоупотребляющей алкоголем. Риск выявления новых случаев ВЗК был выше в 3,17 раза среди страдающих алкоголизмом лиц, из них для болезни Крона в 4,4 раза, для язвенного колита – в 2,33 раза.
Подобные опасения не безосновательное. Известно, что этанол, входящий в состав алкогольных напитков, снижает активность иммунных клеток кишечника и подавляет продукцию некоторых цитокинов, а также (что для ВЗК важнее всего!) увеличивает проницаемость кишечной стенки. Таким образом, в теории навредить кишечнику приемом алкоголя можно, однако степень негативного влияния этанола до сих пор неизвестна.
Исследования не дают однозначного ответа на вопрос, как алкоголь влияет на течение болезни. С одной стороны, количество их ограничено, а число испытуемых редко превышает несколько десятков человек. С другой — большая часть подобных исследований основана на проведении опросов, в том числе ретроспективных.
Тем не менее, некоторые интересные данные доступны для анализа. В 2004 году Jowett и соавторы опубликовали результаты наблюдения за 191 пациентом с язвенным колитом в фазу клинической ремиссии. В течение года пациентам периодически проводили опрос о количестве и характере употребляемых продуктов и напитков, в том числе алкоголя. Через 12 месяцев обострение заболевания наблюдалось у 52% больных.
Установлено, что употребление алкоголя в умеренных дозах не увеличивало риск обострения, тогда как прием высоких доз алкоголя повышал риск обострения язвенного колита в 2,71 раза. Недостатком исследования было отсутствие точных сведений об опасной и безопасной дозах алкоголя.
Еще одна интересная работа была проведена в США. 14 пациентов с язвенным колитом и болезнью Крона в ремиссии, а также 7 здоровых добровольцев приняли участие в исследовании, которое оценивало влияние употребления вина на течение заболевания. На протяжении недели каждый пациент выпивал в день 1-3 бокала красного сухого вина (примерно 0,4 г этанола на 1 кг массы тела). До и после исследования проводилась оценка анализов крови, кала на фекальный кальпротектин, а также кишечная проницаемость. За время исследования не было ни одного случая обострения заболевания. У пациентов отмечено достоверное повышение тонкокишечной (при болезни Крона) и толстокишечной (при язвенном колите) проницаемости. Поскольку кишечная проницаемость играет важную роль в развитии ВЗК и в целом может рассматриваться как ранний маркер воспаления, скорее всего, регулярное употребление вина даже в небольших количествах приведет к обострению заболевания. В то же время у большинства участников перед началом исследования был отмечен повышенный уровень фекального кальпротектина, то есть не исключено, что ремиссия заболевания была лишь клиническая.
Интересно, что через неделю после ежедневного употребления вина уровень кальпротектина у больных ВЗК достоверно снизился.
Наконец, одна из последних работ, также выполненная в США в конце декабря 2017 года, оценивала симптоматику со стороны органов пищеварения у лиц, употребляющих алкоголь. Из 90 пациентов с неактивным ВЗК 62% регулярно употребляли алкоголь в разных количествах, что в целом сопоставимо с данными по стране в целом (61% американцев периодически выпивают). Из общего числа употребляющих алкоголь 75% больных с ВЗК отметили, что в последующем у них отмечается ухудшение симптомов (боли в животе, послабление стула, вздутие живота и т.д.). Данное исследование было вновь построено на опросе пациентов, что ограничивает его ценность.
Не рекомендуется употребление алкоголя одновременно с некоторыми лекарственными препаратами, которые принимают пациенты с ВЗК. Тяжелое лекарственное поражение печени может наблюдаться при одновременном приеме метронидазола и этанола. Прием других медикаментов (меалазины, азатиоприн/меркаптопурин, стероидные гормоны) не исключает возможности эпизодического употребления алкоголя в небольших дозах.
Заключение
Универсальной диеты и диетических рекомендаций для пациентов с язвенным колитом и болезнью Крона не существует. Решение о назначении той или иной диеты принимает лечащий врач.

Питание пациентов с болезнью Крона и язвенным колитом: новые рекомендации
К сожалению, специальной диеты для лиц, страдающих ВЗК, в настоящее время не разработано. Попытки научно доказать эффективность некоторых рационов предпринимались неоднократно, однако на сегодняшний день качество таких исследований оставляет желать лучшего.
В то же время, существует значительно больше данных относительно пользы или вреда для пациентов с язвенным колитом и болезнью Крона некоторых отдельных компонентов пищи. В начале 2020 года были опубликованы Рекомендации по питанию для пациентов (далее, Рекомендации), сформулированные Международной организацией по изучению ВЗК. В этой статье мы разберем некоторые из них.
1. Употребление овощей и фруктов.
А) Пациентам с болезнью Крона рекомендовано употребление умеренного и большого количества овощей и фруктов.
Б) У пациентов, имеющих стриктуру кишки (с клиническими проявлениями), количество нерастворимых волокон в рационе должно быть ограничено.
В) Недостаточно данных, свидетельствующих о пользе/вреде изменения или ограничения в рационе количества овощей и фруктов при язвенном колите.

Пищевые волокна (клетчатка), которая в большом количестве содержится в овощах и фруктах, попадая в толстую кишку, начинает там расщепляться бактериями. Растворимые волокна (пектины, камеди и т.д.) расщепляются быстрее, нерастворимые (целлюлоза и т.ж.) - медленнее. Расщепление пищевых волокон приводит к образованию так называемых короткоцепочечных жирных кислот (КЦЖК), являющихся прекрасным питательным субстратом для эпителиальных клеток слизистой оболочки толстой кишки.
Исследования свидетельствуют о том, что лица с ВЗК (особенно с болезнью Крона) реже употребляли фрукты и овощи до момента возникновения заболевания. Среди пациентов с болезнью Крона в ремиссии обострение в течение 6 месяцев отмечалось на 40% реже в том случае, если рацион содержал большее количество пищевых волокон (24 г против 10 г/сутки). Эти данные идут вразрез с традиционными отечественными рекомендациями по исключению или значимому ограничению овощей и фруктов у пациентов с болезнью Крона даже в ремиссии.
Единственное ограничение в отношении нерастворимых пищевых волокон по мнению авторов Рекомендаций может быть только для пациентов с болезнью Крона, имеющих стриктуру кишки с клиническими симптомами. Им рекомендованы преимущественно растворимые пищевые волокна, которые помимо продуктов содержатся, например в некоторых пищевых добавках, лекарственных средствах и БАДах (например, псиллиум, гидролизованная гуаровая камедь).
Наши комментарии. Несомненно, рекомендация А не может быть применима к очень тяжелым случаям болезни Крона с высокой активностью воспаления в кишечнике. Однако такие лица обычно находятся на стационарном лечении, а обычная пища минимизируется или исключается. Ее заменяют на лечебные смеси и/или питательные растворы.
2. Употребление углеводов, сахарозы и фруктозы
А) Отсутствуют убедительные доказательства о необходимости изменять количество потребляемых углеводов, сахарозы и фруктозы пациентам с болезнью Крона и язвенным колитом.
Б) Лицам с болезнью Крона и язвенным колитом, у которых сохраняются симптомы несмотря на доказанную ремиссию заболевания и отсутствие стриктур(ы), может быть рекомендована диета low FODMAP.

Попытки оценить влияние диеты с ограничением простых углеводов, рафинированных сахаров на активность ВЗК проводились неоднократно. Было показано, что изменение углеводного состава (например, исключение и значимое ограничение сахарозы, фруктозы и т.д.) не снижает риск обострения ВЗК и не влияет на активность болезни. Следовательно, нет никаких оснований для соблюдения низкоуглеводных диет.
В ряде случаев, когда кишечные симптомы (вздутие живота, неустойчивый стул, слабые боли в животе) сохраняются на фоне ремиссии ВЗК, может быть эффективной диета с ограничением ферментируемых углеводов: лактозы, фруктозы, фруктанов, галактанов и многоатомных спиртов. Несмотря на то, что эта диета (известная в англоязычной литературе как диета low FODMAP) не влияет на активность воспаления в кишке, ее соблюдение позволяет части лиц избавиться от описанных выше неприятных симптомов.
Наши комментарии. Отсутствие необходимости менять углеводный состав рациона не должно вводить в заблуждение любителей поесть много сладкого. Следует руководствоваться принципами рационального питания, согласно которым в рационе среднестатистического человека должно быть не более 30-50 г добавленного сахара в сутки. Избыточное употребление простых углеводов (сахаров) может способствовать развитию синдрома избыточного бактериального роста в тонкой кишке, что при водит к появлению жидкого стула, повышенному газообразованию, дискомфорту и болям в животе даже на фоне ремиссии ВЗК.
3. Употребление пшеницы и глютена.
А) Недостаточно доказательств для ограничения пшеницы и глютена в рационе при болезни Крона и язвенном колите.

К счастью, в настоящее время отсутствуют данные о вреде глютена для лиц, не страдающих глютен-ассоциированными заболеваниям (например, целиакией). Известно, что у лиц с ВЗК, исключивших из рациона пшеницу и продукты с высоким содержанием глютена, могут уменьшиться некоторые симптомы: вздутие живота, послабление стула, урчание в животе. Однако этот эффект обусловлен не исключением глютена как такового, а уменьшением в рационе некоторых углеводов. По странному совпадению, те злаки, которые содержат глютен в большом количестве (рожь, пшеница, ячмень), также характеризуются высоким содержанием фруктанов, галактанов и фруктозы.
Таким образом, пациентам с ВЗК не стоит назначать аглютеновую диету с целью повышения эффективности лечения.
Наши комментарии. Следует помнить, что описанные выше углеводы (фруктаны, галактаны и фруктоза) не являются вредными для организма. Симптомы, вызванные их поступлением в кишечник, обычно появляются при употреблении продуктов с этими углеводами в большом количестве. Неоправданное назначение аглютеновой диеты пациентам с болезнью Крона и язвенным колит нередко приводит к снижению массы тела и недостатку некоторых необходимых питательных веществ.
4. Употребление красного мяса, продуктов переработки красного мяса, птицы и яиц.
А) Не существует убедительных доказательств необходимости ограничивать употребление красного мяса, продуктов переработки красного мяса, птицы и яиц в умеренном количестве при болезни Крона.
Б) При язвенном колите следует ограничить красное мясо и продукты его переработки.

В последние годы большой интерес вызывают вопросы безопасности употребления красного мяса и продуктов их переработки. Так, Всемирная организация здравоохранения (ВОЗ) включила красное мясо (говядину, телятину, свинину, ягнятину, баранину, конину и козлятину) в список продуктов, которые могут быть причиной развития рака толстой кишки. Продукты переработки красного мяса (в т.ч. сосиски, сардельки, бекон, ветчина, колбаса, мясные консервы, буженина, солонина, билтонг) ВОЗ рассматривает в качестве канцерогенов. Это означает, что есть веские доказательства того, что они увеличивают риск возникновения рака толстой кишки.
ВОЗ рекомендует ограничить количество красного мяса 700 граммами в неделю (масса мяса до тепловой обработки). Белое мясо, т.е. птица, не повышает риск развития рака толстой кишки.
А что же говорят ученые в отношении мяса и риска развития ВЗК? Одно из крупных исследований, проведенное во Франции в середине 2000-х годов показало, что употребление животного белка (преимущественно мяса и рыбы) в большом количестве увеличивало риск развития ВЗК в 3 раза.
Существуют убедительные доказательства, что риск обострения язвенного колита у пациентов в ремиссии повышается при высоком содержании в рационе красного мяса и продуктов его переработки.
Употребление красного мяса в обычном количестве не связано с повышенным риском обострения заболевания. Употребление яиц, мяса птицы пациентами с болезнью Крона на протяжении 12 месяцев увеличивало вероятность достижения ремиссии.
Наши комментарии. При болезни Крона следует придерживаться рекомендаций ВОЗ: употреблять красное мясо не более 700 г в неделю, а продукты его переработки (любимые многими колбасы, сосиски и т.д.) использовать редко, от случая к случаю. Язвенный колит требует снижения количества красного мяса. Сколько же мяса можно есть? Возможно, тут подойдут нормы, рекомендованные для средиземноморской диеты – не более 120 г красного мяса в неделю.
5. Употребление молока и молочных продуктов.
А) Не сформулировано единое мнение в отношении потребления пастеризованных молока и молочных продуктов при ВЗК.
Б) Непастеризованное молоко и молочные продукты не следует использовать при ВЗК.

Постараемся разобраться. Помимо белков и жиров, молоко содержит один из наиболее известных углеводов – лактозу, которая также называется молочным сахаром. У части здоровых лиц, а также у пациентов с ВЗК может развиться состояние, когда всасывание лактОзы в тонкой кишке снижено. Это состояние называется лактазной недостаточностью, причина которой – снижение активности фермента лактАзы в кишечнике. Проявляется лактазная недостаточность по-разному: кого-то беспокоит диарея, кого-то – вздутие живота.
На сегодняшний момент не доказано негативное влияние молока и молочных продуктов на течение ВЗК. Употребление молочных продуктов не увеличивало риск обострения язвенного колита, при этом исключение этой продуктовой группы из рациона не увеличивало вероятность достижения ремиссии заболевания.
Авторы рекомендаций не смогли прийти к договоренности по поводу молока и молочных продуктов в рационе больных ВЗК. Они объяснили это тем, что состав молока и особенно молочных продуктов в настоящее время неоднороден, продукты нередко содержат добавки (эмульгаторы, загустители и т.д.), что затрудняет оценку.
Непастеризованные молочные продукты не следует использовать при ВЗК ввиду повышенного риска развития инфекций.
Наши комментарии. Молоко и молочные продукты – ценный источник кальция и животного белка, что особенно важно для пациентов с ВЗК, получающих гормональную терапию. Исключение или ограничение потребления этих продуктов показано только при доказанной лактазной недостаточности у лиц, страдающих болезнью Крона и язвенным колитом.
6. Употребление жиров
А) При болезни Крона показано ограничение насыщенных жиров и исключение трансжиров.
Б) При язвенном колите показано исключение трансжиров
В) При язвенном колите показано ограничение потребления продуктов, содержащих миристиновую кислоту
Г) При язвенном колите показано увеличение в рационе продуктов, содержащих омега-3 жирные кислоты

По происхождению все жиры делятся на животные и растительные, и оба вида необходимы организму. Также жиры подразделяются на виды жирных кислот, которые входят в их состав: насыщенные или ненасыщенные. Термины "насыщенный" и "ненасыщенный" говорят о степени "насыщения" молекулы жирной кислоты водородом. В насыщенной жирной кислоте все вакантные места заполнены, а в ненасыщенной - есть двойные связи, которые позволяют присоединить дополнительные атомы водорода. Если двойная связь одна, жирную кислоту называют мононенасыщенной, а если их две или более – полиненасыщенной.
Насыщенные жиры содержатся в мясных, молочных продуктах, кокосовом, пальмовом масле и т.д. Негативный эффект потребления одной из насыщенных жирных кислот – миристиновой – был показан в отношении течения язвенного колита. Увеличение содержания в рационе этой кислоты (а находится она в пальмовом, кокосовом масле и молочных продуктах) являлось независимым фактором риска обострения заболевания в течение года: риск увеличивался в 3 раза.
К мононенасыщенным жирным кислотам относится, например, олеиновая кислота (содержится в оливковом, кунжутном, рапсовом маслах) и пальмитолеиновая кислота (содержится в жире морских рыб и млекопитающих). Одно из исследований показало, что добавление в рацион оливкового масла, богатого олеиновой кислотой, было ассоциировано с большей частотой клинической ремиссии болезни Крона.
Продукты, богатые полиненасыщенными омега-3 и омега-6 жирными кислотами также оценивались в клинических исследованиях. Омега-3 жирные кислоты содержатся в морской рыбе, некоторых орехах и семенах. Небольшое исследование продемонстрировало некоторое снижение воспалительной активности у пациентов с язвенным колитом, которые в течение 8 недель употребляли в пищу рыбу (лосось) в количестве 600 г/неделю. Интересно, что включение в рацион пищевых добавок с омега-3 жирными кислотами не снижало риск обострения язвенного колита. В отношении болезни Крона данные исследований противоречивы – в настоящее время нельзя считать доказанным эффект добавок с омега-3 жирными кислотами в качестве средства профилактики обострения заболевания.
Отдельно обсуждается влияние транс-жиров на течение ВЗК. Транс-жиры или транс-изомеры жирных кислот – это жиры с измененной пространственной структурой. Они встречаются в небольших количествах в естественных продуктах (например, мясо, молоко, сливочное масло), однако большая их часть получается искусственным путем. классическим примером является маргарин – результат переработки жидкого растительного масла в твердый и долго хранящийся продукт.
Одно из исследований показало, что лица с диагнозом язвенный колит значительно чаще и больше употребляли в пищу транс-жиры по сравнению со здоровыми людьми из контрольной группы.
7. Употребление пищевых добавок
А) При болезни Крона и язвенном колите следует ограничить потребление продуктов, содержащих мальтодекстрины и искусственные подсластители
Б) При болезни Крона и язвенном колите следует ограничить потребление продуктов, содержащих каррагенан, карбоксиметилцеллюлозу и полисорбат-80
В) При болезни Крона и язвенном колите следует ограничить потребление переработанных продуктов, содержащих титана диоксид и сульфиты
Рост заболеваемости ВЗК во всем мире в последние годы позволил заподозрить роль пищи в качестве одного из факторов, провоцирующих развитие болезни. Поскольку основные компоненты пищи остались неизменными, высока вероятность того, что всему виной используемые для увеличения срока хранения, внешнего вида и вкуса пищевые добавки.
Установлено, что искусственные подсластители (сукралоза, сахарин и т.д.) вызывают образование воспалительных молекул в кишечнике лабораторных животных. При исследованиях на крысах эти же вещества, а также мальтодекстрины меняли состав кишечной микробиоты.
Некоторые стабилизаторы, загустители и эмульгаторы рассматриваются в качестве возможных факторов, способствующих развитию ВЗК. К ним, в частности, относятся каррагенан (пищевая добавка Е407), карбоксиметилцеллюлоза (Е466) и полисорбат-80 (Е433). В исследованиях на животных показано, что длительное воздействие описанных выше веществ вызывает изменение микробного состава кишечника, повышение кишечной проницаемости, а также развитие процессов воспаления в слизистой оболочке кишечника с его повреждением и образованием эрозий и язв.
Сульфиты используются в пищевой промышленности в качестве консервантов и антиоксидантов для вина, пива, лимонного сока, продуктов переработки красного мяса (например, колбасы), сухофруктов и консервированных фруктов. К ним относятся, например, диоксид серы, сульфиты кальция, калия, натрия (входят в группу пищевых добавок с индексами Е220-228). В экспериментах на мышах было показано, что некоторые бактерии кишечника могут активно размножаться, используя сульфиты как пищу, и вызывают развитие колита. Таким образом, нельзя исключить, что диета, богатая сульфитами не спровоцирует развитие дисбиотических изменений и воспаления в кишечнике человека.
Диоксид титана или двуокись титана (TiO2, добавка Е171) – наночастица, используемая в пищевой промышленности в качестве пищевого красителя. Сам по себе диоксид титана это химически инертный белый порошок, который не подвергается распаду в организме человека и животных. Он широко используется для придания окраски кондитерским изделиям (например, при изготовлении белого шоколада), соусам и т.д. Применение диоксида титана в виде пищевого красителя в настоящее время признано безопасным в определенных дозах. Однако существуют работы (опять же на лабораторных мышах), в которых продемонстрирована активация иммунных клеток кишечника при воздействии на слизистую двуокисью титана. Частицы диоксида титана могут откладываться в эпителии кишечника при поглощении их клетками-макрофагами.
Проведено исследование диеты с исключением двуокиси титана у пациентов с болезнью Крона. В нем приняло участие лишь 20 человек, у части из которых в рационе отсутствовал диокид титана в рационе в течение 4 месяцев. Результат – индекс активности болезни Крона в таких больных снизился в большей степени, чем у лиц на обычной диете. Более крупное исследование сравнивало диету с низким и обычным содержанием диоксида титана в рационе 83 пациентов с болезнью Крона, однако клиническая ремиссия или ответ были достигнуты в обеих группах одинаково часто.
Наши комментарии. Большинство сведений о влиянии пищевых добавок получены из исследований на лабораторных животных. Мы до сих пор не знаем, как долго и в каком объеме нужно съедать ту или иную пищевую добавку, чтобы развился язвенным колит или болезнь Крона. Поэтому можно рекомендовать лишь не делать продукты, богатые перечисленными веществами, основой вашего рациона.
Резюме.
Для пациентов с болезнью Крона рекомендовано:
1) регулярное употребление овощей и фруктов (в отсутствии стриктуры с симптомами);
2) ограничить потребление животных и транс-жиров
3) ограничить потребление продуктов, богатых мальтодекстринами, подсластителями (сукралоза, цикламат, аспартам, адвантам), добавками типа диоксида титана, полисорбата-80 или карбоксиметилцеллюлозы.
Для пациентов с язвенным колитом рекомендовано:
1) регулярное употребление овощей и фруктов (в отсутствии стриктуры с симптомами);
2) ограничить потребление животных и транс-жиров
3) ограничить употребление продуктов, богатых мальтодекстринами, подсластителями (сукралоза, цикламат, аспартам, адвантам), добавками типа диоксида титана, полисорбата-80 или карбоксиметилцеллюлозы.
4) Ограничить употребление в пищу красного мяса и продуктов его переработки (сосиски, колбасы и т.д.)
5) Увеличить употребление натуральных источников омега-3 жирных кислот (например, морская рыба)
Читайте также:

