Заразна ли инфекция почек
Обновлено: 17.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Пиелонефрит: причины появления, симптомы, диагностика и способы лечения.
Определение
Пиелонефрит — неспецифический инфекционно-воспалительный процесс, характеризующийся одновременным или последовательным поражением чашечно-лоханочной системы и паренхимы (основной ткани) почки. Пиелонефрит бывает как односторонним (поражена одна почка) и двусторонним (поражены обе почки).
Причины появления пиелонефрита
Почки имеют два типа тканей: гломерулярную и тубуло-интерстициальную. Первая осуществляет фильтрацию крови и образование мочи, вторая – ее сбор и отток из почек в мочеточники и мочевой пузырь. Пиелонефритом называют воспаление тубуло-интерстициальной ткани, отвечающей за сбор и вывод мочи в мочеточники. Основной причиной возникновения неосложненного заболевания являются бактерии, такие как кишечные палочки, стрептококки, стафилококки, протей и другие. Осложненный пиелонефрит вызывается теми же микроорганизмами, а также синегнойной палочкой и грибами.
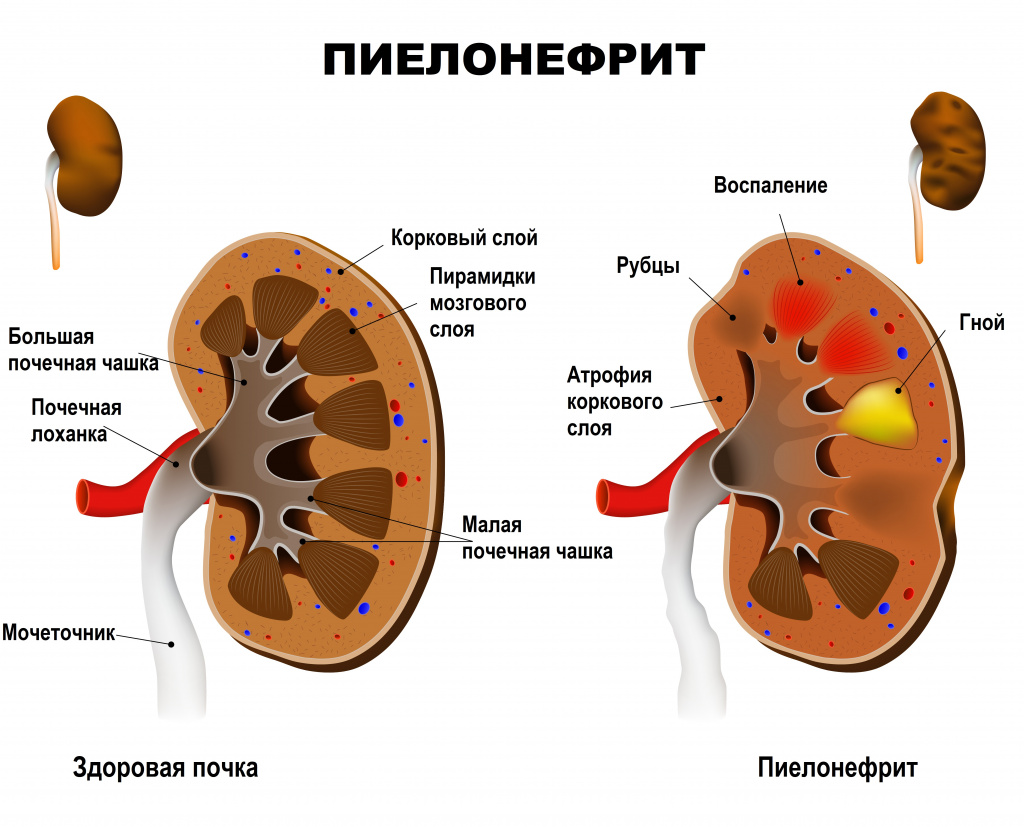
Заболевание может протекать в острой или хронической форме с периодическими обострениями.
Выделяют первичный пиелонефрит, связанный с проникновением и размножением микроорганизмов, и вторичный, вызванный нарушением оттока мочи.
Первичный острый пиелонефрит может манифестировать у практически здоровых людей после переохлаждения или стрессовых ситуаций. Острый обструктивный пиелонефрит обычно обусловлен нарушением оттока мочи, а острый необструктивный – восходящей инфекцией мочевых путей. Хронический пиелонефрит может быть исходом острого пиелонефрита, однако чаще возникает как относительно спокойно протекающий процесс.
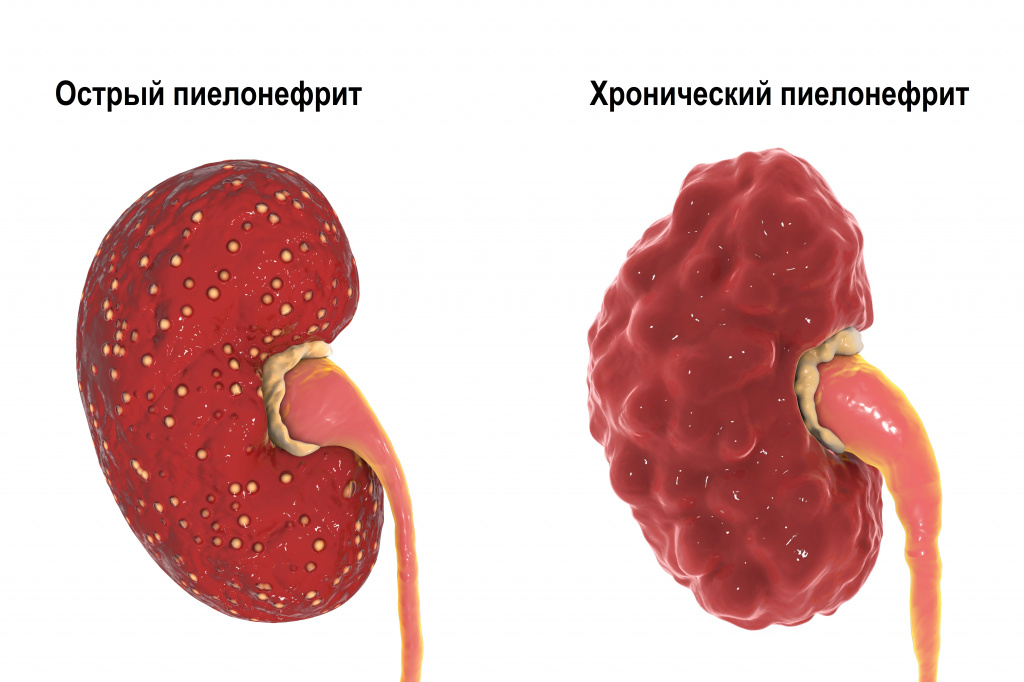
Каждое очередное обострение пиелонефрита сопровождается вовлечением в воспалительный очаговый процесс все новых участков функционирующей почечной паренхимы. В результате вторичного воспаления поверхность почки становится неровной, формируются крупные глубокие сегментарные рубцы, расширяется мочеточник. Чаще процесс локализуется в верхнем сегменте почки.
Болезнь распространена среди всех возрастных групп, встречается как у взрослых, так и у детей. Хронический пиелонефрит является самой распространенной патологией почек, заболеваемость составляет 18 случаев на 1000 человек, острый пиелонефрит — 1 случай на 1000 человек. Чаще заболевание диагностируется у женщин, что обусловлено анатомическим строением уретры – она шире и короче, чем у мужчин.
Женщины, в основном, заболевают до 40 лет, а у мужчин пиелонефрит развивается, как правило, в пожилом возрасте при нарушении уродинамики.
К развитию пиелонефрита предрасполагают следующие факторы:
- некоторые хронические соматические патологии (сахарный диабет, подагра, гиперкортицизм, атеросклероз, воспалительные заболевания органов малого таза и др.);
- бессимптомная бактериурия;
- снижение иммунного статуса организма;
- нарушения работы кишечника;
- аномалии почек и мочевыводящих путей;
- опущение почки (нефроптоз);
- мочекаменная болезнь;
- опухоли предстательной железы, сжимающие уретру;
- гормональный дисбаланс, прием глюкокортикоидов и гормональных контрацептивов;
- беременность, когда увеличенная матка давит на мочеточники, а повышение прогестерона снижает их сократительную способность.
- серозное воспаление;
- гнойное воспаление;
- апостематозный пиелонефрит;
- карбункул почки;
- абсцесс почки.
- активное воспаление;
- латентное воспаление;
- ремиссия или клиническое выздоровление.
В общем анализе мочи возрастает уровень лейкоцитов, что является первым признаком начала острого воспалительного процесса. В анализе крови регистрируются факторы воспаления.
Развернутая клиническая картина острого пиелонефрита:
- повышение температуры тела >38°C (иногда с ознобом);
- болезненность при пальпации в области почки с пораженной стороны (положительный симптом острого пиелонефрита);
- положительный симптом Пастернацкого с пораженной стороны (появление болевых ощущений при легком постукивании в поясничной области).
При хроническом пиелонефрите наблюдается сочетание следующих симптомов, выраженность которых зависит от степени тяжести заболевания:
- Болевой синдром в поясничной области выражен слабо и характерен для фазы активного воспаления. Боль может отдавать в паховую область и на переднюю поверхность бедра. Обычно при первичном пиелонефрите болевой синдром наблюдается с обеих сторон, при вторичном – с одной. Боль не зависит от положения тела. Часто аналогом боли может быть чувство зябкости в поясничной области.
- Интоксикация проявляется анемией, утомляемостью, общей слабостью, снижением работоспособности и познабливанием при сохранении нормальной температуры тела. В вечернее время может быть лихорадка.
- Возникает отечность лица в утренние часы.
- Артериальная гипертензия развивается в среднем у 50-75% больных, чаще отмечается в период обострений.
- Характерны учащенное мочеиспускание и никтурия (выделения большей части суточного объема мочи в ночное время).
- Изменения в общем анализе мочи носят непостоянный характер, выражаются в низком удельном весе мочи при отсутствии обострения, бактериурии и лейкоцитурии в период обострения заболевания.
При обследовании больного хроническим пиелонефритом обращают внимание на болезненность при пальпации в области почки, положительный симптом Пастернацкого с пораженной стороны, наличие полиурии.
Диагностика пиелонефрита
В качестве скринингового теста используют общий анализ мочи и УЗИ органов мочевыделительной системы.
Пиелонефрит - это воспаление почек, вызванное инфекцией. Развитию инфекционного процесса способствуют нарушение оттока мочи, предыдущие заболевания почек, беременность, гормональный дисбаланс, сахарный диабет, анатомические особенности и прием некоторых лекарств.
Причины возникновения и развития пиелонефрита
Воспаление почек возникает, когда инфекция нижних отделов мочевыводящих путей распространяется вверх и, двигаясь через уретру, доходит до мочевого пузыря, а оттуда – по мочеточникам в почки.
Главная причина пиелонефрита – инфекция в сочетании с нарушенным оттоком мочи. Любая проблема, которая нарушает нормальный отток мочи, увеличивает риск острого пиелонефрита. Например, мочевыводящие пути необычного размера или формы с большей вероятностью могут привести к острому пиелонефриту.
Также локальное переохлаждение поясничной области может вызвать развитие пиелонефрита, даже в отсутствие анатомических особенностей и при нормальном оттоке мочи.
Симптомы пиелонефрита
Болезнь может иметь разную клиническую картину, патология может поражать одну или обе почки, носить острый или хронический характер.
Острый пиелонефрит
- высокая температура;
- боль в животе, спине, боку или паху;
- болезненное мочеиспускание;
- мутная моча;
- гной или кровь в моче;
- частое мочеиспускание;
- дрожь, озноб;
- тошнота, рвота.
Хронический пиелонефрит
Пациенты с хронической формой заболевания могут испытывать только легкие симптомы или вовсе не испытывать признаков недуга.
Хронический пиелонефрит чаще встречаются у людей с непроходимостью мочевыводящих путей. Она может быть вызвана инфекциями, пузырно-мочеточниковым рефлюксом или анатомическими аномалиями. Хронический пиелонефрит чаще встречается у детей, чем у взрослых.
Гендерные особенности
Из-за анатомических особенностей женщины чаще страдают пиелонефритом, чем мужчины. Дело в том, что у них уретра короче, а, следовательно, бактериям легче проникать в организм. Это делает женщин более подверженными инфекциям почек и повышает риск острого пиелонефрита.
Кто в группе риска
- пациенты с камнями в почках или другими заболеваниями почек или мочевого пузыря;
- пожилые люди;
- люди с подавленной иммунной системой, (например - диабетом, ВИЧ/СПИДом или онкологическими заболеваниями, приемом гормональных препаратов);
- пациенты с пузырно-мочеточниковым рефлюксом (состояние, при котором небольшое количество мочи возвращается из мочевого пузыря в мочеточники и почки);
- мужчины с заболеваниями простаты;
- люди, которые склонны долго терпеть до похода в туалет в силу психологических особенностей или профессии;
- люди с недержанием мочи – когда по разным причинам ослабевают мышцы, удерживающие содержимое мочевого пузыря внутри, и при кашле, чихании, смехе может непроизвольно выделяться небольшое количество мочи.
- Дети до семи лет – из-за особенностей анатомического развития.
- Молодые женщины. Сразу несколько факторов может спровоцировать патологию: начало половой жизни, беременность, роды.
- Мужчины с аденомой предстательной железы.
Диагностика пиелонефрита
- Первичная консультация врача и общий осмотр. Врач проверит температуру, болезненность в области живота и поясницы, другие общие симптомы.
- Анализы. Первый и самый важный – общий анализ мочи. Обычно необходим общий анализ крови. Также часто целесообразен посев мочи для определения вида возбудителя и его чувствительности к препаратам.
- Врач также может назначить УЗИ для поиска кист, опухолей или других препятствий в мочевыводящих путях, анализ крови на креатинин и мочевину, мочевую кислоту, биохимический анализ мочи.
Лечение пиелонефрита
Антибиотики - это первое средство против острого пиелонефрита. Антибиотик подбирает только врач на основе результатов анализа на вид бактерии и ее чувствительности к препаратам. В острых случаях, если нет возможности дождаться результатов анализов, используется антибиотик широкого спектра действия.
Хотя при правильном лечении симптомы могут пройти уже в течение 2–3 дней, курс антибиотиков необходимо завершить до конца, согласно рекомендации врача (обычно лечение длится от 10 до 14 дней). Если прервать курс терапии досрочно, может выработаться резистентность возбудителя заболевания к антибиотику – это затруднит дальнейшее лечение и увеличит риск хронического пиелонефрита.
Лечение хронического пиелонефрита возможно. Оно проводится по принципам терапии острого пиелонефрита, только требует больше времени и усилий. Лечение предусматривает устранение причины, которая привела к застою мочи, восстановление почечного кровообращения, уничтожение патогенной бактерии при помощи антибиотикотерапии, укрепление общего иммунитета. Даже если удается добиться устойчивой ремиссии, может потребоваться поддерживающая прерывистая антибактериальная терапия. Лечение хронического заболевания – серьезный вызов для медиков и долгий путь для пациента, поэтому так важно своевременно обращаться к врачу при первых симптомах недомогания и не тратить драгоценное время на самолечение.
Без должного лечения острый пиелонефрит переходит в хроническую форму. Если инфекция продолжит распространяться, почки могут быть необратимо повреждены. В редких запущенных случаях инфекция может попасть в кровоток. Последствия этого могут быть крайне серьезные, вплоть до сепсиса и бактериального шока.
Пиелонефрит у беременных
Беременность вызывает множество трансформаций в организме, в том числе и физиологические изменения мочевыводящих путей. Повышенный уровень прогестерона (гормона, поддерживающего нормальное течение беременности) и усиленное давление на мочеточники увеличивают риск пиелонефрита.
Пиелонефрит у беременных может потребовать госпитализации в случае, если это состояние угрожает жизни и матери, и ребенка. Также невылеченные инфекции почек у беременных увеличивают риск преждевременных родов, отслойки плаценты, внутриутробного инфицирования плода и поражения его нервной системы. При правильном и своевременном лечении всех этих последствий можно избежать, роды проходят в срок, прогноз благоприятный и для женщины, и для ребенка.
При беременности крайне важно понимать, первый ли это случай заболевания в анамнезе женщины, или болезнь носила хронический характер, а на фоне беременности произошло обострение. Как показывает статистика, первичное воспаление почек у беременных лечится успешно и без осложнений.
Чтобы предотвратить пиелонефрит у беременных, необходимо сдавать анализ на инфекции при планировании беременности. Также проводят посев мочи в начале второго триместра. Раннее обнаружение ИМП может предотвратить инфекцию почек.
- Умеренная физическая активность, прогулки на свежем воздухе, занятие гимнастикой для беременных. Цель – укрепить мышцы и улучшить тонус внутренних органов, улучшить кровоток.
- Соблюдение питьевого режима. Беременным женщинам необходимо проконсультироваться у своего ведущего врача.
- Опорожнение мочевого пузыря не реже, чем каждые 3-4 часа, дабы не допускать застойных явлений.
- Соблюдение специальной диеты, способствующей оттоку мочи (если воспаления почек были до беременности).
Пиелонефрит у детей
Это распространенное заболевание среди детей, занимающее второе место по частоте случаев после ОРВИ.
Основная группа риска среди детей – дети дошкольного возраста. Девочек, в силу анатомических особенностей, болезнь поражает чаще, чем мальчиков.
Самый распространенный возбудитель детского пиелонефрита – кишечная палочка. Кроме нее, в мазках часто обнаруживают протей (простейших), золотистый стафилококк, энтерококки.
Вовремя замеченный острый пиелонефрит у детей полностью вылечивается в большинстве случаев. После полного восстановления в течение трех лет после болезни требуются регулярное обследование (первые три месяца – раз в 10 дней, дальше – ежемесячно) и наблюдение врача. Спустя три года требуется обследование раз в 3 месяца, чтобы не пропустить важную бессимптомную патологию.
Туберкулез – это инфекционное заболевание, вызываемое палочкой Коха (Mycobacterium tuberculosis). Патоген чаще всего поражает легкие, но существуют и другие формы: туберкулез костей, суставов, почек, кожи и других органов.
Процент смертности от туберкулеза по всему миру высок, он входит в десятку заболеваний, приводящих к летальным исходам [1]. Это не только медицинская, но и социальная проблема, поскольку на заболеваемость, помимо состояния здоровья, также влияют социальные и экономические причины, качество питания и образ жизни. Ключевыми факторами риска считаются вредные привычки, ослабленная иммунная система и хронический стресс.
Как передается туберкулез
Возбудитель передается от человека к человеку воздушно-капельным путем при чихании и кашле и просто при разговоре, а также иногда контактно (через поврежденную кожу или внутриутробно). Бактерии туберкулеза долго сохраняются активными во внешней среде в плохо проветриваемом помещении и попадают в организм здорового человека через предметы быта и продукты питания.
Заражение туберкулезом еще не означает начало заболевания: оно развивается только у 5-15% инфицированных. До развития первых симптомов может пройти несколько недель или месяцев, и основным фактором риска считается ослабление иммунных сил организма [1].
Классификация туберкулеза
- открытая форма (больной активно выделяет микобактерии в воздух и заражает других людей);
- закрытая форма (больной является носителем и не выделяет возбудителя в окружающую среду).
- первичное заражение с локальным воспалением в области проникновения и вовлечением близлежащих лимфоузлов;
- латентный период с образованием очагов воспаления в других органах;
- активная инфекция с ухудшением общего состояния здоровья, образованием каверн (полостей) в легких и множественными поражениями в других органах [2].
Симптомы туберкулеза
Признаки заражения различаются в зависимости от органа, пораженного микобактерией. Общие симптомы включают утомляемость, сниженную трудоспособность, плохой аппетит, повышенную температуру тела, потерю веса, появление румянца на щеках.
- затяжной кашель на протяжении нескольких недель (сухой или мокрый);
- кровохаркание;
- боль в области груди;
- затрудненное дыхание;
- увеличение периферических лимфоузлов (в области головы, шеи и конечностей);
- ночная потливость;
- периодическое повышение температуры.
Диагностика туберкулеза
Это заболевание, особенно закрытая форма, сложно диагностируется. Переход из латентной фазы в активную смазанный, а клинические симптомы не позволяют установить точный диагноз или отсутствуют. В связи с этим решающее значение имеет лабораторная диагностика.
Квантифероновый тест на туберкулез. Этот современный иммунологический метод позволяет выявить латентный туберкулез, а также туберкулезное поражение других органов. Введения туберкулина не требуется, поэтому этот тест подходит уязвимым группам пациентов (беременные и кормящие женщины, пожилые люди, ВИЧ-инфицированные, люди с непереносимостью туберкулина). Для диагностики используется венозная кровь. Наличие в организме активного туберкулеза обуславливает появление в крови особых белков, входящих в состав микобактерий. Т-лимфоциты реагируют на присутствие этих белков и в результате такой сенсибилизации начинают усиленно вырабатывать интерферон-гамма. Квантифероновый тест основан на измерении уровня интерферона-гамма, повышение которого указывает на наличие туберкулезной инфекции в пробе крови.
Метод T-SPOT.TB. Позволяет диагностировать латентную и активную формы легочного и внелегочного туберкулеза. Для исследования используют венозную кровь. В основе метода лежит оценка количества самих сенсибилизированных Т-лимфоцитов. Он также не дает ложноположительных результатов и подходит уязвимым группам пациентов.
Анализ мокроты. Для проведения теста необходимо собрать утреннюю мокроту, которая отделяется при кашле. Во взятом образце определяют наличие самих микобактерий. Анализ подходит только для диагностики туберкулеза легких.
Анализ мочи. Выявляют изменения параметров, характерные для туберкулеза: появление лейкоцитов, эритроцитов, бактерий, белка, гноя, сдвиг реакции мочи в кислую сторону.
Отрицательные лабораторные анализы не гарантируют отсутствие туберкулеза. Пациенты с подозрением на заболевание проходят флюорографию и/или рентгенографию легких. Для выявления внелегочных форм туберкулеза проводят МРТ, КТ и другие инструментальные исследования. Также применяют биопсию (взятие образца тканей) для микроскопических исследований и посевов на питательные среды.
Дифференциальную диагностику проводят с широким рядом заболеваний в тех случаях, когда ни одно исследование не подтвердило наличие микобактерий, присутствуют атипичные симптомы или отсутствует адекватный ответ на противотуберкулезное лечение.
Лечение туберкулеза
- Медикаментозная терапия. Противотуберкулезные препараты разделяют на основные (назначаются пациентам с первичным заражением), резервные (назначаются при неэффективности препаратов основной группы или их непереносимости) и комбинированные (многокомпонентные препараты с фиксированной дозой отдельных компонентов).
- Химиотерапия. Направлена на уничтожение микобактерий или подавление их размножения.
- Симптоматическое лечение конкретных нарушений и симптомов.
- Физиотерапия при туберкулезе легких с целью улучшения питания тканей и стимуляции их восстановления (ингаляции, ароматерапия, электролечение, лазеротерапия, дарсонвализация, магнитотерапия) [3].
Полное выздоровление не гарантирует отсутствие рецидива заболевания в будущем.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
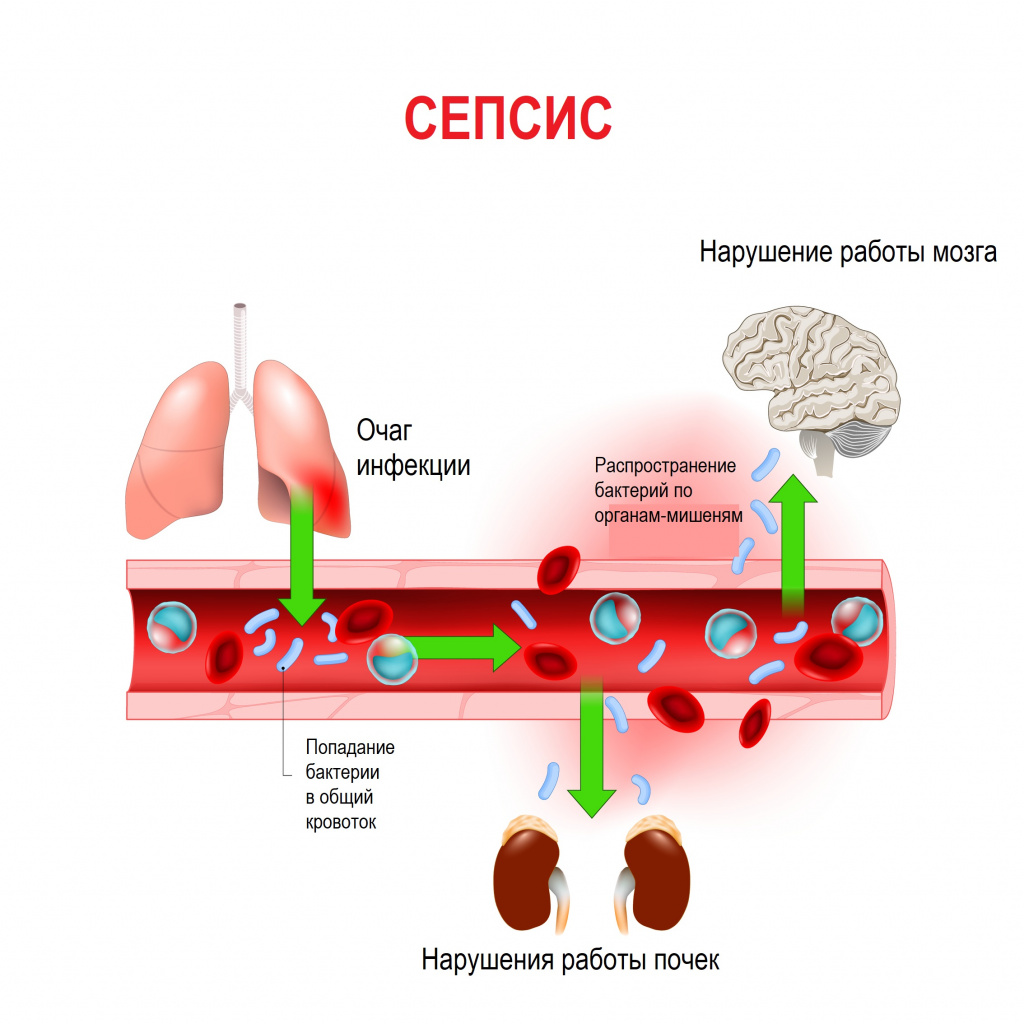
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
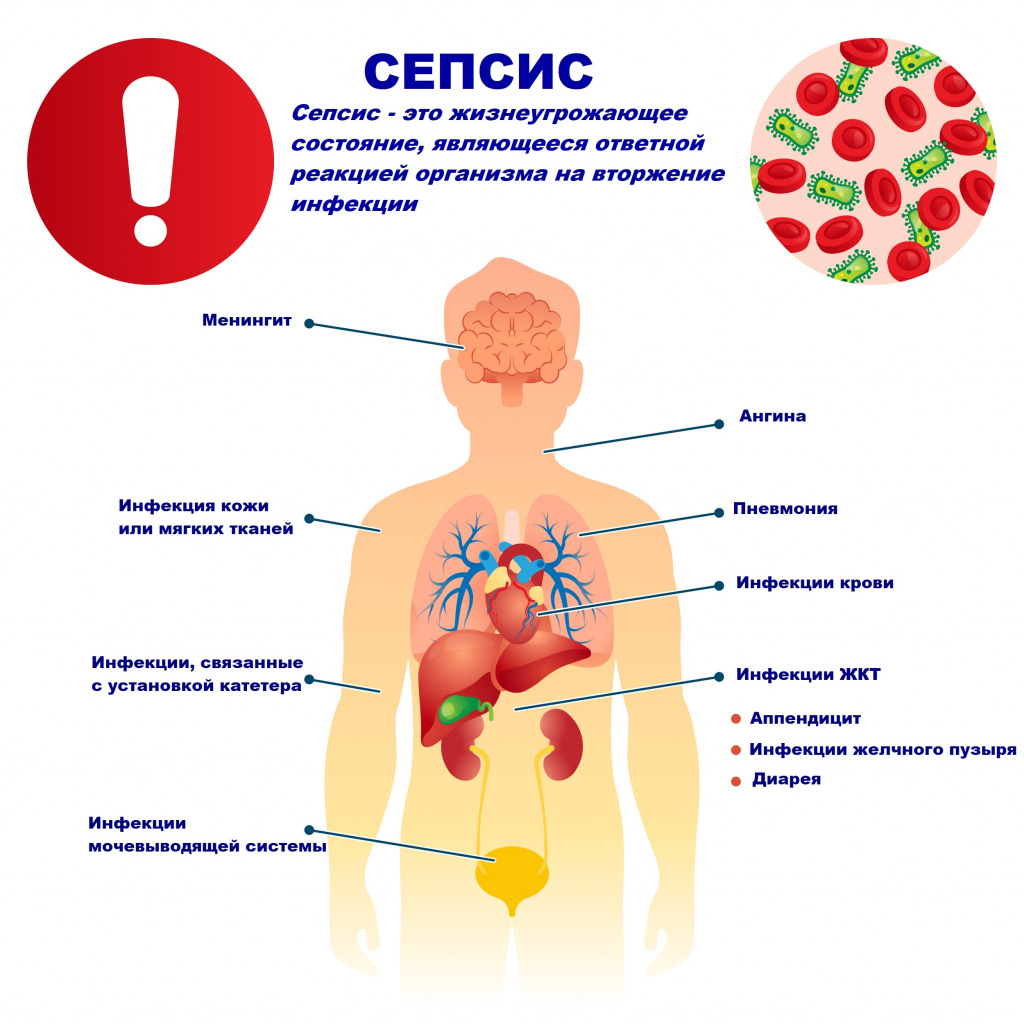
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Читайте также:

