Желчегонные травы при описторхозе
Обновлено: 18.04.2024
Хронический холецистит — воспалительное заболевание желчного пузыря, сочетающееся с функциональными нарушениями и изменениями физико-химических свойств желчи.
Хронический холецистит — воспалительное заболевание желчного пузыря, сочетающееся с функциональными нарушениями (дискинезиями желчного пузыря и сфинктерного аппарата желчевыводящих путей) и изменениями физико-химических свойств желчи (дисхолией).
По данным различных авторов, больные хроническим холециститом составляют 17–19%, в индустриально развитых странах — до 20%.
Классификация
Согласно МКБ-10 выделяют:
Клиника
В клинике преобладает болевой синдром, который возникает в области правого подреберья, реже — в подложечной области. Боль иррадиирует в правую лопатку, ключицу, плечевой сустав, имеет ноющий характер, продолжается в течение многих часов, дней, иногда недель. Нередко на этом фоне возникает острая схваткообразная боль, обусловленная обострением воспаления в желчном пузыре. Возникновение боли и ее усиление чаще связано с нарушением диеты, физическим напряжением, охлаждением, интеркуррентной инфекцией. Обострению болевого приступа обычно сопутствуют повышение температуры тела, тошнота, рвота, отрыжка, понос или чередование поносов и запоров, вздутие живота, чувство горечи во рту.
Рвота — необязательный симптом хронического бескаменного холецистита и наряду с другими диспепсическими расстройствами (тошнота, отрыжка горечью или постоянный горький вкус во рту) может быть связана не только с основным заболеванием, но и с сопутствующей патологией — гастритом, панкреатитом, перидуоденитом, гепатитом. Часто в рвотных массах обнаруживают примесь желчи, при этом они окрашиваются в зеленый или желто-зеленый цвет.
Наблюдаются вялость, раздражительность, нарушение сна. Преходящая желтушная окраска склер и кожных покровов может наблюдаться в связи с затруднением оттока желчи из-за скопления слизи, эпителия или паразитов (в частности, лямблий) в холедохе.
При пальпации живота у больных хроническим холециститом определяются следующие симптомы.
Симптом Кера — в области проекции желчного пузыря, расположенной у места пересечения наружного края правой прямой мышцы живота с краем ложных ребер, появляется болезненность при глубокой пальпации во время вдоха.
Симптом Грекова–Ортнера–Рашбы — болезненность при поколачивании ребром кисти по правой реберной дуге.
Симптом Мерфи — осторожное, мягкое введение руки в зону желчного пузыря, и при глубоком вдохе пальпирующая рука вызывает резкую болезненность.
Симптом Мюсси — болезненность при надавливании на диафрагмальный нерв между ножками грудинно-ключично-сосцевидной мышцы справа.
Инструментальные и клинико-биохимические исследования
При хроническом холецистите в фазе обострения повышается СОЭ, возрастает количество лейкоцитов со сдвигом формулы влево, эозинофилия.
К рентгенологическим методам исследования относят холеграфию, которую проводят после перорального или внутривенного введения контрастного вещества. На снимках выявляются симптомы поражения желчного пузыря: удлинение, извитость, неравномерность заполнения (фрагментированность) пузырного протока, его перегибы.
В последние годы стали использовать комплексную методику, в которую, кроме холеграфии, включают холецистохолангиографию, ультразвуковое и радионуклидное сканирование, компьютерную томографию, лапароскопию. В ряде случаев по особым показаниям проводят лапароскопическую холецистографию. Применение этого метода позволяет просмотреть различные отделы желчного пузыря, отметить степень его наполнения, наличие спаек и сращений, деформаций, состояние стенки.
К неинвазивным методам исследования желчевыводящих путей относят ультразвуковое исследование (УЗИ).
УЗИ не имеет противопоказаний и может применяться в тех случаях, когда рентгенологическое исследование не может быть проведено: в острую фазу заболевания, при повышенной чувствительности к контрастным веществам, беременности, печеночной недостаточности, обструкции магистральных желчных путей или пузырного протока. УЗИ позволяет не только установить отсутствие конкрементов, но и оценить сократительную способность и состояние стенки желчного пузыря (утолщение, склерозирование).
Лечение
Режим
В период выраженного обострения больных нужно госпитализировать. При сильном болевом синдроме, особенно возникшем впервые или осложнившемся механической желтухой, угрозе развития деструктивного холецистита больных следует направлять в хирургическое отделение. При легком течении заболевания лечение проводят амбулаторно.
В период обострения больному рекомендуется постельный режим в течение 7–10 дней. Очень важно состояние психоэмоционального комфорта, особенно при гипертонической дискинезии желчевыводящих путей. При гипокинетической дискинезии постельный режим не рекомендуется.
Питание
В фазе обострения в первые 1–2 дня назначается питье теплой жидкости (некрепкий сладкий чай, соки из фруктов и ягод, разведенные водой, отвар шиповника, минеральная вода без газа) небольшими порциями до 6 стаканов в день, несколько сухариков. По мере улучшения состояния назначается в ограниченном количестве протертая пища: слизистые супы (овсяный, рисовый, манный), каши (манная, овсяная, рисовая), кисели, желе, муссы. Далее включается нежирный творог, нежирная отварная рыба, протертое мясо, белые сухари. Пища принимается 5–6 раз в день.
Многие специалисты рекомендуют в периоде обострения хронического холецистита 1–2 разгрузочных дня. Например:
После купирования обострения назначается диета № 5. Она содержит нормальное количество белков (90–100 г); жиров (80–100 г), около 50% жиров составляют растительные масла; углеводов (400 г), энергетическая ценность 2500–2900 ккал.
Питание дробное (небольшими порциями) и частое (5–6 раз в сутки), что способствует лучшему оттоку желчи.
При хронических холециститах полезны растительные жиры, масла. Они богаты полиненасыщенными жирными кислотами, фосфолипидами, витамином Е. Полиненасыщенные жирные кислоты (ПНЖК) (арахидоновая, линолевая) входят в состав клеточных мембран, способствуют нормализации обмена холестерина, участвуют в синтезе простагландинов, которые разжижают желчь, повышают сократительную способность желчного пузыря. Растительные жиры особенно важны при застое желчи.
Установлено антилитогенное свойство диеты, богатой растительной клетчаткой (яблоки, морковь, арбуз, дыня, помидоры). Целесообразно добавлять к пище пшеничные отруби — до 30 г в сутки. Их обдают кипятком, запаривают; затем жидкость сливают, разбухшие отруби добавляют в блюда по 1–2 столовых ложки 3 раза в день. Курс лечения — 4–6 недель. Овощи, фрукты, отруби способствуют отхождению желчи, уменьшают содержание в ней холестерина, снижают вероятность образования камней.
При гипертонусе желчного пузыря для уменьшения тонуса гладкой мускулатуры назначается диета, богатая магнием (пшеничная и гречневая каши, пшеничные отруби, пшено, хлеб, овощи).
Больным хроническим холециститом не рекомендуются продукты, оказывающие раздражающее действие на печень: мясные бульоны, животные жиры (кроме сливочного масла), яичные желтки, острые приправы (уксус, перец, горчица, хрен), жареные и тушеные блюда, изделия из сдобного теста. Запрещаются алкогольные напитки и пиво.
Купирование болевого синдрома в периоде обострения
При интенсивных болях в правом подреберье, тошноте и повторной рвоте назначают периферические М-холинолитики: 1 мл 0,1% раствора Атропина сульфата или 1 мл 0,2% раствора Платифиллина п/к. Они оказывают и противорвотное действие, уменьшают секрецию поджелудочной железы, кислото- и ферментообразование в желудке.
После купирования интенсивных болей препараты могут быть назначены внутрь: Метацин в дозе 0,004–0,006 г, Платифиллин — по 0,005 г на прием. При наличии противопоказаний можно рекомендовать селективный М-холинолитик Гастроцепин внутрь по 50 мг 2–3 раза в день.
Для купирования боли применяются также миотропные спазмолитики: 2 мл 2% раствора Папаверина гидрохлорида, 2 мл 2% раствора Но-шпы п/к или в/м 2–3 раза в день, 2 мл 0,25% раствора Феникаберана в/м. В начале приступа желчной колики боль может купироваться приемом 0,005 г Нитроглицерина под язык.
При упорных болях используют ненаркотические анальгетики: Анальгин 2 мл 50% раствора в/м или в/в в сочетании с Папаверином гидрохлоридом, Но-шпой и Димедролом; Баралгин 5 мл внутримышечно, Кеторол, Трамал, Триган-Д, Диклофенак. При некупирующихся болях приходится применять наркотические анальгетики: 1 мл 1% раствора Промедола в/м. Не следует применять морфин, т. к. он вызывает спазм сфинктера Одди, препятствует оттоку желчи, провоцирует рвоту. К наркотикам можно добавить 2 мл 0,25% раствора дроперидола в 200–300 мл 5% раствора глюкозы внутривенно капельно, паранефральные новокаиновые блокады.
При наличии у больного гипотонической дискинезии (монотонные тупые, ноющие боли, ощущение тяжести в правом подреберье) холинолитики и спазмолитики не показаны.
В этих случаях можно рекомендовать холекинетики (повышают тонус желчного пузыря, способствуют его опорожнению, уменьшают боль в правом подреберье): растительное масло по 1 столовой ложке 3 раза в день перед едой, ксилит или сорбит по 15–20 г на 1/2 стакана теплой воды 2–3 раза в день, 25% раствор магния сульфата по 1 столовой ложке 2–3 раза в день перед едой.
С этой же целью применяется синтетический гормональный препарат — холецистокинин октапептид (интраназально по 50–100 мкг), он дает и обезболивающий эффект.
При выраженном болевом синдроме у больного с гипотонической дискинезией целесообразно использовать ненаркотические анальгетики, а в дальнейшем — холекинетики.
Регулирующим влиянием на тонус желчевыводящих путей и противорвотным действием обладают метоклопрамид (Церукал) и домперидон (Мотилиум), который можно применять внутрь или в/м по 10 мг 2–3 раза в день.
Антибактериальная терапия (АБТ) в период обострения
АБТ назначается тогда, когда есть основания предполагать бактериальную природу заболевания (лихорадка, лейкоцитоз и др.).
стерилизует желчь и содержимое кишечника (откуда инфекция нередко поступает в желчный пузырь и вызывает воспаление);
Антибактериальные препараты, проникающие в желчь в очень высоких концентрациях
По данным Я. С. Циммермана, наибольшей концентрации в желчи достигают ампициллин и рифампицин. Это антибиотики широкого спектра действия, они оказывают влияние на большинство возбудителей холецистита.
Ампициллин — относится к полусинтетическим пенициллинам, подавляет активность ряда грамотрицательных (кишечная палочка, энтерококки, протей) и грамположительных бактерий (стафилококки и стрептококки). Хорошо проникает в желчные пути даже при холестазе, назначается внутрь по 0,5 г 4 раза в день или в/м по 0,5–1,0 г каждые 6 ч.
Оксациллин — полусинтетический пенициллин, оказывает бактерицидное действие преимущественно на грамположительную флору (стафилококк, стрептококк), но неэффективен в отношении большинства грамотрицательных бактерий. В отличие от пенициллина действует на пенициллиназообразующие стафилококки. Хорошо накапливается в желчи и назначается внутрь по 0,5 г 4–6 раз в день до еды или по 0,5 г 4–6 раз в день внутримышечно.
Оксамп (ампициллин + оксациллин) — препарат бактерицидного действия широкого спектра, подавляет активность пенициллиназообразующих стафилококков. Создает в желчи высокую концентрацию. Назначается по 0,5 г 4 раза в день внутрь или в/м.
Рифампицин — полусинтетический бактерицидный антибиотик широкого спектра действия. Рифампицин не разрушается пенициллиназой, но в отличие от ампициллина не проникает в желчные пути при застойных явлениях в них. Препарат принимается внутрь по 0,15 3 раза в день.
Эритромицин — антибиотик из группы макролидов, активен в отношении грамположительных бактерий, слабо влияет на грамотрицательные микроорганизмы, создает высокие концентрации в желчи. Назначается по 0,25 г 4 раза в день.
Линкомицин — бактериостатический препарат, влияющий на грамположительную флору, в том числе на пенициллиназообразующие стафилококки, и неактивный в отношении грамотрицательных микроорганизмов. Назначается внутрь по 0,5 г 3 раза в день за 1–2 ч до еды или внутримышечно по 2 мл 30% раствора 2–3 раза в день.
Препараты, проникающие в желчь в достаточно высоких концентрациях
Пенициллин (бензилпенициллин-натрий) — бактерицидный препарат, активный в отношении грамположительной флоры и некоторых грамотрицательных кокков, на большинство грамотрицательных микроорганизмов не действует. Не активен в отношении пенициллиназообразующих стафилококков. Назначается в/м по 500 000–1 000 000 ЕД 4 раза в сутки.
Феноксиметилпенициллин — назначается внутрь по 0,25 г 6 раз в сутки до еды.
Тетрациклины — обладают бактериостатическим действием как на грамположительную, так и на грамотрицательную флору. Назначаются внутрь по 0,25 г 4 раза в день.
Высокоэффективны полусинтетические производные тетрациклина. Метациклин принимают в капсулах по 0,3 г 2 раза в день. Доксициклин назначается внутрь в 1-й день по 0,1 г 2 раза в день, затем по 0,1 г 1 раз в день.
Антибиотики группы цефалоспоринов
Применяются цефалоспорины I поколения — цефалоридин (Цепорин), цефалотин (Кефлин), цефазолин (Кефзол); II поколения — цефалексин (Цепорекс), цефуроксим (Кетоцеф), цефамандол (Мандол); III поколения — цефотаксим (Клафоран), цефтриаксон (Лонгацеф), цефтазидим (Фортум).
Препараты I поколения угнетают большинство стафилококков, стрептококков, многие штаммы кишечной палочки, протея.
Цефалоспорины II поколения обладают более широким спектром действия на грамотрицательные бактерии, угнетают резистентные к препаратам I поколения кишечные палочки, различные энтеробактерии.
Еще более широким спектром действия обладают цефалоспорины III поколения, они подавляют, кроме перечисленных бактерий, сальмонеллы, шигеллы.
Кефзол — вводится в/м или в/в по 0,5–1 г каждые 8 ч. Цепорин — вводится в/м по 0,5–1 г каждые 8 ч. Клафоран — вводится в/м или в/в по 2 г 2 раза в день.
Препараты фторхинолонов
Обладают бактерицидными свойствами, препараты широкого спектра действия, достаточно хорошо проникающие в желчь. Назначаются при тяжелой инфекции желчевыводящих путей.
Абактал (пефлоксацин) — назначается внутрь по 0,4 г 2 раза в день во время еды или в/в капельно — 5 мл (0,4 г) в 250 мл 5% раствора глюкозы.
Таривид (офлоксацин) — назначается по 0,2 г 2 раза в день.
Ципролет (ципрофлоксацин) — назначается по 0,5 г 2 раза в день.
Производные нитрофурана
Подавляют как грамположительные, так и грамотрицательные микроорганизмы. Концентрация Фурадонина в желчи в 200 раз превосходит его содержание в сыворотке крови; Фурадонин подавляет также патогенную флору в желудочно-кишечном тракте, действует на лямблии. Фурадонин и Фуразолидон назначают по 0,1–0,15 г 3–4 раза в день после еды.
Хлорофиллипт
Это препарат, содержащий смесь хлорофиллов, находящихся в листьях эвкалипта, подавляет грамположительные и грамотрицательные микроорганизмы, в том числе и пенициллиназообразующие стафилококки. Назначается по 20–25 капель 1% спиртового раствора 3 раза в день.
При обострении хронического холецистита лечение антибактериальными средствами проводится в течение 7–10 дней.
Антибактериальные средства целесообразно сочетать с желчегонными препаратами, оказывающими бактерицидное и противовоспалительное действие (Циквалон по 0,1 г 3–4 раза в день перед едой; Никодин по 0,5 г 3–4 раза в день перед едой).
При обнаружении в желчи паразитов проводится антипаразитарная терапия. При наличии описторхоза, фасциолеза, клонорхоза наряду с эритромицином или Фуразолидоном назначают Хлоксил (по 2 г в виде порошка в 1/2 стакана молока через каждые 10 мин 3–5 раз в течение 2 дней подряд; проводят 2 курса с интервалами 4–6 месяцев).
При обнаружении стронгилоидоза, трихоцефалеза, анкилостомидоза проводится лечение Вермоксом — по 1 таблетке 2–3 раза в день в течение 3 дней, повторный курс назначается через 2–4 недели, применяется также Комбантрин по 0,25 г 1 раз в день в течение 3 дней.
При обнаружении лямблий в желчи проводится антилямблиозная терапия одним из следующих препаратов: Фуразолидон по 0,15 г 3–4 раза в день в течение 5–7 дней; Фазижин по 2 г на прием однократно; Трихопол (метронидазол) по 0,25 г 3 раза в день после еды в течение 5–7 дней; Макмирор по 0,4 г 2 раза в день в течение 7 дней.
Применение желчегонных средств
Классификация желчегонных средств (Н. П. Скакун, А. Я. Губергриц, 1972):
Препараты, стимулирующие желчеобразовательную функцию печени (т. е. стимулирующие образование печенью желчи) — истинные желчегонные (холеретики):
Рассмотрены факторы риска паразитозов у детей, действие паразитов на организм ребенка, подходы к диагностике паразитарной инвазии и принципы комплексного лечения паразитозов с тем чтобы предотвратить дальнейшее развитие функциональных нарушений с формиров
Risk factors of parasitosis in children was considered, as well as the influence of parasites on a child's body, approaches to the diagnostics of parasitic invasions and principles of integrated treatment of parasitic diseases in order to prevent the further development of functional disorders of the formation of organic pathology.
.jpg)
Паразитарное заболевание — развитие болезненных симптомов в результате жизнедеятельности гельминта или простейших в организме человека [1]. Основной фактор выживания и распространения паразитов — их необычайно высокая репродуктивная способность, а также постоянно совершенствующиеся механизмы приспособления к обитанию в теле человека. К сожалению, настороженность медицинских работников в отношении паразитарных заболеваний у населения в настоящее время чрезвычайно низка, а профилактика гельминтозов сведена к лечению выявленных инвазированных пациентов [12, 13]. Вместе с тем многие исследователи отмечают связь широкой распространенности паразитозов у детского населения с развитием функциональной патологии органов пищеварения на фоне нарушений регуляции и высокий риск формирования хронических заболеваний даже при условии естественной санации ребенка с течением времени.
Самые распространенные и изученные заболевания — аскаридоз, энтеробиоз (рис. 1) и лямблиоз — регистрируются повсеместно. В России ежегодно выявляется более 2 млн больных нематодозами. При оценке территориального распределения лямблиоза по России установлено, что самый высокий средний уровень показателей заболеваемости в течение многих лет отмечен в Санкт-Петербурге, причем пораженность детей, посещающих детские учреждения, составляет 35% [2].
Каждый человек в течение жизни неоднократно переносит различные паразитарные заболевания [9]. В детском возрасте паразитозы встречаются чаще. У детей раннего возраста (до 5 лет) этому способствует широкая распространенность репродуктивного материала паразитов (цисты, яйца, личинки (рис. 2)) в окружающей среде и недостаточное развитие гигиенических навыков.
.jpg)
Значимость определенных факторов риска меняется в соответствии с возрастом ребенка. Доказано, что для детей младшего возраста более значимы санитарно-гигиенические условия проживания, а для подростков при сборе анамнеза необходимо уделить внимание социально-экономическим и географическим факторам (пребывание в лагере, туристическая поездка, наличие младшего брата или сестры) (рис. 3).
.jpg)
Транзиторное снижение противоинфекционного иммунитета как фактор риска возникновения паразитоза у детей регистрируется также в период реконвалесценции после вирусных заболеваний, вызываемых вирусами герпетической группы (цитомегаловирус, вирус простого герпеса I и II, вирус Эпштейна–Барр), может возникать в результате ятрогении (применение иммуносупрессивной терапии при аллергических и аутоиммунных заболеваниях). В настоящее время значимая доля детей находится в состоянии дезадаптации, которое также сопровождается снижением иммунной защиты.
Иммунную защиту желудочно-кишечного тракта (ЖКТ) ребенка можно условно разделить на специфическую и неспецифическую. К неспецифической защите относят комплекс условий нормального пищеварения: зрелость ферментативных систем, обеспечение кислотно-щелочного градиента в различных отделах ЖКТ, деятельность нормальной микрофлоры, адекватную моторику.
Отдельно необходимо отметить, что для такого заболевания, как лямблиоз, предрасполагающим фактором инвазии является нерегулярное и недостаточное отделение желчи в кишечник при аномалиях развития желчного пузыря (перетяжки, перегибы). Лямблиоз, выявленный у пациентов педиатрического отделения МОНИКИ, в 100% случаев сопровождался дисфункцией билиарного тракта.
.jpg)
У детей в восстановительном периоде после острых кишечных инфекций, после массивной антибиотикотерапии, а также у пациентов с хронической патологией органов пищеварения сопутствующие нарушения ферментного обеспечения, нормофлоры и моторики кишечника также делают ЖКТ более уязвимым для паразитов (рис. 4).
Специфическая защита слизистой оболочки органов пищеварения зависит от возраста ребенка и его зрелости. Механизм специфической иммунной защиты является одной из наиболее древних систем организма, так как гельминтозы сопровождают человечество в течение многих тысячелетий. Этот механизм представлен прежде всего эозинофилами крови и иммуноглобулином Е.
Классический развернутый антипаразитарный ответ может быть сформирован у ребенка не ранее достижения им 4 лет и тесно связан с качеством и количеством IgE, созревающего к этому возрасту. При контакте организма с паразитом в первую очередь выделяются медиаторы воспаления: интерлейкин, лейкотриен С4, D4, простагландины, тромбоксаны. Увеличивается количество лимфоцитов, продуцирующих IgM и IgG. В клиническом анализе крови отмечается рост уровня эозинофилов и базофилов, связанный с увеличением содержания этих клеток в тканях инвазированного органа. Встречаясь с личинками паразита, тканевые базофилы выделяют гепарин и гистамин, которые в сочетании с лейкотриенами и другими медиаторами воспаления вызывают общие проявления: зуд, реактивный отек, гиперемию, а также могут спровоцировать общие проявления: бронхоспазм, проявления крапивницы или диарею. Аллергическое воспаление при паразитозах развивается по классическому пути и призвано создать условия, приводящие к гибели и/или элиминации паразита [5].
Вместе с тем эозинофилы обладают выраженным цитотоксическим потенциалом, превышающим возможности других клеток крови, что объясняет первостепенное значение эозинофилов в антипаразитарных реакциях и их повреждающую роль при аллергии. Основное действие эозинофилы оказывают в барьерных тканях. В очаге инвазии они дегранулируют, оказывая гельминтотоксическое и цитотоксическое действие. Белки эозинофильных гранул (большой основной протеин, эозинофильная пероксидаза, эозинофильный катионный протеин, эозинофил-производный нейротоксин) токсичны не только для паразита, но и для клеток организма ребенка. Еще одной из важных причин системных и органных поражений, сопутствующих паразитозам, является образование иммунных комплексов [9, 10].
Действие паразитов на организм ребенка осуществляется с вовлечением многих систем. Практически все их виды могут вызывать сдвиг соотношения Th1/Th2 клеток в направлении, благоприятном для их выживания. Описаны случаи, когда продукты выделения паразита оказывали гормоноподобное действие на организм хозяина [5].
Местное влияние паразиты осуществляют, вызывая контактное воспаление слизистой оболочки и стимулируя вегетативные реакции. При этом нарушаются процессы кишечного всасывания, адекватная моторика ЖКТ и его микробиоценоз.
Системное влияние оказывается за счет использования паразитом энергетического и пластического потенциала пищи в ущерб организму ребенка, индукции аллергии и аутоиммунных процессов, целенаправленной иммуносупрессии и эндогенной интоксикации. Проведенными исследованиями показано, что аллергический синдром сопутствует аскаридозу и энтеробиозу в 71,3% случаев. Среди детей с атопическим дерматитом паразитозы выявляются у 69,1%, при этом лямблиоз из числа всех инвазий составляет 78,5% [4].
Особенно узнаваемую клиническую картину формирует токсокароз (рис. 5). Клиническими маркерами этой инвазии являются лейкемоидная реакция эозинофилов (от 20% и выше эозинофилов в формуле крови), сопровождающая ярко и упорно протекающий аллергический синдром в виде атопического дерматита с выраженным зудом и резистентностью к традиционной терапии или тяжелую бронхиальную астму с частыми приступами.
В 75,3% случаев паразитозы сопровождаются разнообразными функциональными нарушениями со стороны ЖКТ. Рядом работ доказано, что паразитарная инвазия способна вызывать нарушения углеводного обмена, а также дисахаридазную недостаточность за счет снижения уровня лактазы [7, 9].
У большинства детей нарушения адаптации являются одним из важных звеньев патогенетического процесса при паразитозе. Следует отметить, что состояние дезадаптации затрагивает в первую очередь лимфоцитарное звено иммуногенеза, что не может не сказываться на созревании и дифференцировке специфического иммунитета.
Диагностика паразитозов
До настоящего времени ведется поиск простого, доступного и надежного метода диагностики паразитозов. Разработанные методики прямого визуального обнаружения требуют минимальной экспозиции диагностического материала, многократных повторных исследований. Известные способы диагностики глистных инвазий и протозоозов, такие как метод толстого мазка фекалий по Като, метод формалин-эфирного осаждения, перианальный соскоб, микроскопия пузырной и печеночной желчи, имеют ряд недостатков, связанных как с особенностями развития паразита, так и с состоянием макроорганизма и его реактивностью.
Непрямые методы исследования (определение специфических антител) обладают недостаточной специфичностью и достоверностью. Известно, например, что, проходя сложный цикл развития от яйца до взрослого состояния, гельминты меняют свой антигенный состав. Антитела в организме хозяина вырабатываются в основном в ответ на поступление экскретов и секретов гельминта, тогда как в иммунодиагностических реакциях используются соматические антитела. Возникающая неспецифическая сенсибилизация организма, общность некоторых антигенов трематод, простейших и человека создают высокий удельный вес ложноположительных серологических реакций в титрах ниже достоверно диагностических. Таким образом, исследование методом иммуноферментного анализа (ИФА) на гельминты является высокочувствительным, но низкоспецифичным методом. Определение паразитов методом полимеразной цепной реакции (ПЦР) является высокоспецифичным и высокочувствительным методом, но из-за дороговизны и сложности не может быть скрининговым, когда, например, нужно обследовать группу детей из детского учреждения.
Не теряет своей актуальности клинический осмотр ребенка и внимательный учет косвенных признаков паразитоза. Важно отметить возможность течения паразитоза при аллергическом и астеническом синдроме, полилимфаденопатии неясного генеза, при нарушениях кишечного всасывания, углеводного обмена, при затяжном и хроническом течении болезней пищеварительного тракта, гепатоспленомегалии неясного генеза. Течение паразитарной инвазии имеет клинические особенности: обычно признаки поражения минимизированы, заболевание носит стертый характер, обострения полиморфны и неярки. Особенностью обострений заболеваний данной группы является их цикличность с периодом в 11–15 дней.
Косвенными лабораторными признаками паразитоза могут быть анемия, базофилия, эозинофилия, увеличение уровня аспартатаминотранферазы (АСТ).
Кроме того, признаки возможной паразитарной инвазии следует учитывать при оценке результатов инструментального исследования. При ультразвуковом исследовании органов брюшной полости у ребенка старше 3 лет косвенными признаками паразитоза являются гепатоспленомегалия, неравномерность паренхимы печени и селезенки за счет мелких гиперэхогенных сигналов, увеличенные лимфатические узлы в воротах селезенки.
Лечение гельминтозов
Лечение гельминтозов должно начинаться с применения специфических антигельминтных препаратов. Современный арсенал лекарственных средств, используемых для лечения кишечных паразитозов, включает значительное количество препаратов различных химических классов [11]. Они применяются как в клинической практике для лечения выявленных больных, так и с целью массовой профилактики.
Определяя препарат для специфической противопаразитарной терапии, следует понимать, что спектр действия этих препаратов не особенно широк. Практически все препараты этой группы применяются многие десятки лет и целесообразно предположить, что паразиты выработали системы приспособления и заболевание может быть резистентным к проводимой терапии. По данным Г. В. Кадочниковой (2004), эффективность такого традиционного препарата, как Декарис, в современных условиях не достигает 57%. Кроме того, эта группа противопаразитарных средств, к сожалению, имеет ряд побочных эффектов: тошноту, рвоту, абдоминальный синдром.
Таким образом, в современных условиях следует отдавать предпочтение более современным препаратам, которые, во-первых, являются универсальными для лечения как нематодозов, так и смешанных глистных инвазий и активны в отношении такого распространенного паразита, как лямблия. Во-вторых, использование одного противопаразитарного препарата, а не их комбинации, ощутимо снижает риск неприятных побочных эффектов. На сегодняшний день единственный представитель этой группы в нашей стране — альбендазол (Немозол).
Для лечения аскаридоза у детей старшего возраста или при рецидивировании заболевания в настоящее время под наблюдением врача может быть применен комбинированный прием антигельминтных средств (например, альбендазол в течение трех дней, затем — Вермокс в течение трех дней). Непременным условием успешной дегельминтизации больных энтеробиозом являются одновременное лечение всех членов семьи (коллектива) и строгое соблюдение гигиенического режима для исключения реинвазии. Следует отметить, что важное значение имеет ежедневная влажная уборка, так как были описаны казуистические случаи распространения репродуктивного материала остриц на частичках пыли на высоту до 1,5 метра.
В педиатрической клинике МОНИКИ разработаны принципы терапии паразитозов, учитывающие особенности патогенеза инвазии и позволяющие качественно и надежно вылечить данную группу заболеваний. Благодаря применению разработанной схемы терапии удается эффективно предотвратить реинвазию и развитие функциональных нарушений органов пищеварения у детей.
Принципы терапии больных паразитозами
1. Прием антипаразитарных препаратов проводится с учетом вида возбудителя инвазии.
Препараты, применяемые в лечениии аскаридоза:
- Вермокс (мебендазол) (для детей с 2 лет) — по 100 мг 2 раза в сутки в течение 3 дней;
- Пирантел — 10 мг/кг однократно;
- Немозол (альбендазол) (для детей с 2 лет) — 400 мг однократно.
Препараты, применяемые в лечении энтеробиоза:
- Вермокс (мебендазол) (для детей с 2 лет) — 100 мг однократно;
- Пирантел — 10 мг/кг однократно;
- Немозол (альбендазол) (для детей с 2 лет) — 400 мг однократно.
Препараты, применяемые в лечении лямблиоза:
- орнидазол 25–30 мг/кг (если масса тела больше 35 кг — 1000 мг) в два приема в течение 5 дней, 1 день — 1/2 дозы, повторный курс через 7 дней;
- Макмирор (нифурател) — по 15 мг/кг 2 раза в сутки в течение 7 дней;
- Немозол (альбендазол) — по 15 мг/кг однократно в течение 5–7 дней.
2. Лечение паразитоза предусматривает измененные в результате жизнедеятельности паразитов свойства пищеварительного тракта ребенка (функциональные нарушения органов пищеварения, ферментопатия, изменение микробиоценоза) и их коррекцию курсами ферментных препаратов и синбиотиков (табл. 1).
3. Обязательное применение энтеросорбентов и комплекса поливитаминов с микроэлементами (табл. 2 и 3).
Таким образом, разработанные в клинике педиатрии МОНИКИ принципы комплексной терапии паразитозов у детей предусматривают поэтапное восстановление функционального состояния ЖКТ, нарушенного в результате местного и системного влияния паразитов. Применение комплексной терапии позволяет предотвратить дальнейшее развитие функциональных нарушений с формированием органической патологии, а также избежать реинвазии.
Литература
Л. И. Васечкина 1 , кандидат медицинских наук
Т. К. Тюрина, кандидат медицинских наук
Л. П. Пелепец, кандидат биологических наук
А. В. Акинфиев, кандидат медицинских наук
Что такое лямблиоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Лямблиоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое кишечными лямблиями, которые колонизируют слизистую оболочку преимущественно тонкого кишечника, нарушают процессы пристеночного пищеварения и способствуют развитию и усугублению поражения желудочно-кишечного тракта и других заболеваний.
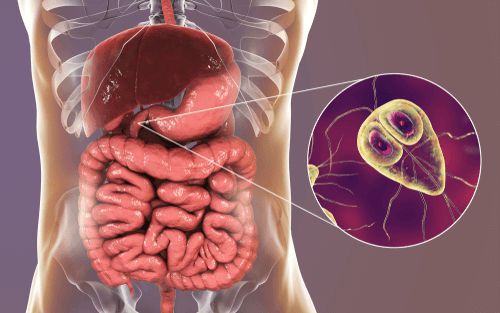
Этиология
Возбудитель — лямблия. Данный род паразитов включает в себя шесть типов, но заболевание человека вызывает только один тип — кишечная лямблия (Giardia duodenalis, Giardia lamblia, Giardia intestinalis). Это жгутиковое микроскопическое простейшее, впервые описанное чешским медиком-анатомом Д.Ф. Лямблем в 1859 году. Оно имеет до восьми генетических подтипов, но для человека патогенны только А и В (также имеют подтипы).
Вид — Giardia lamblia
Возбудитель лямблиоза (кишечная лямблия) существует в виде двух жизненных форм:
- вегетативная (трофозоиты) — стадия активного размножения внутри организма;
- цистная — образуется при неблагоприятных условиях среды.
Трофозоиты — это анаэробные, грушевидные микроорганизмы размерами 9-18 мкм. Они обитают в верхних отделах тонкого кишечника. Подвижны (имеют характерное движение в виде вращения вокруг продольной оси — боковое движение), тело спереди расширено и закруглено, сзади сужено и заострено. Имеют в составе два ядра (между ними пролегают опорные нити — аксостили) и парные органоиды — четыре жгутика и два медиальных тела.
Трофозоиты не имеют цитостома — органа заглатывания пищи и пищеварительной вакуоли, поэтому они всасывают пищу, переваренную хозяином (в основном, углеводы), всей поверхностью тела. Это называется осмотическим питанием.
Как выглядят лямблии:
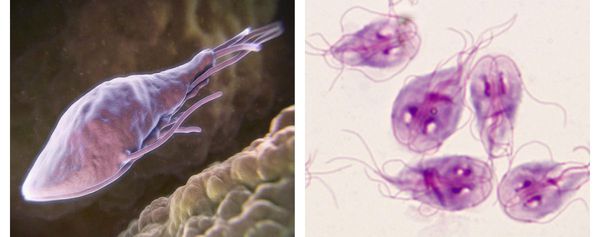
В передней их трети тела расположен присасывательный диск в виде специального углубления. С его помощью лямблии прикрепляются к ворсинкам слизистой оболочки тонкого кишечника. Цитоплазматическая мембрана задней поверхности имеет по краям булавовидные выросты, что также создаёт дополнительную прикрепляющую составляющую.
Размножаются путём продольного деления. Слабо устойчивы в условиях окружающей среды при покидании организма хозяина: при комнатной температуре даже в отсутствии агрессивных факторов быстро погибают.
Цистная форма неподвижна. Паразиты имеют овальную форму, лишены свободных жгутиков (сложно свёрнутые), их размеры достигают 10-14 мкм, окружены толстой, несколько отделённой от тела оболочкой (данная особенность имеет значение при распознавании вида).
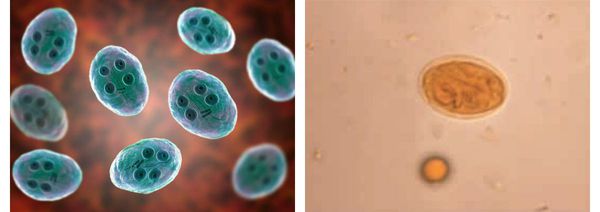
Зрелые цисты внутри имеют четыре ядра, незрелые — два ядра. Образуются в нижних отделах кишечника в процессе выхода из организма с фекалиями. Очень устойчивы во внешней среде: могут сохраняться месяцами в воде при температуре 4-20°C, при хорошей влажности способны сохраняться на контаминированных (обсеменённых) продуктах питания до недели. При кипячении цисты погибают мгновенно, а при высушивании и низкой влажности гибель наступает в течении суток. Устойчивы к бытовому хлорированию воды, действию щелочей и кислот, ультрафиолетовому излучению. Низкие температуры переносит относительно хорошо, но при этом снижая свою жизнеспособность. [1] [3] [6] [9]
Эпидемиология
Распространение заболевания повсеместное, преимущественно в странах с влажным тёплым климатом. Только официально выявляемые случаи в России приближаются к 150 тысячам в год.
Сезонность выражена неярко, некоторый всплеск заболеваемости отмечается в тёплое время года. Возрастной состав больных склоняется в сторону детей.
Источник заражения — люди (больные различными формами лямблиоза и паразитоносители), причём наибольшая заразность наблюдается в подостром периоде заболевания, когда в 1 г фекалий может содержаться до нескольких десятков миллионов цист. Лямблии животных (нечеловеческие типы паразитов) не имеют доказательной базы в плане распространения и заражения человека.
Факторами передачи паразитов выступает загрязнённая цистами термически не обработанная питьевая вода, пища, грязные руки (возможна прямая передача от человека к человеку). Определённую роль в передаче лямблий играют насекомые (тараканы, мухи) и животные (собаки, кошки) — они являются механическими переносчиками (паразиты располагаются на их теле, шерсти, лапках, транзитом в кишечнике).
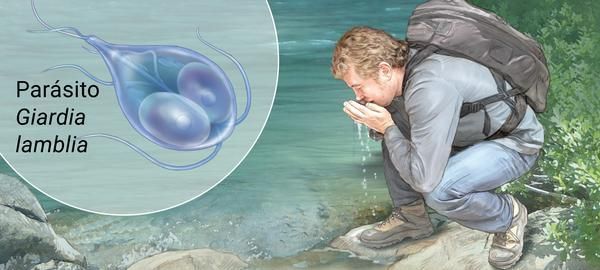
Механизм передачи — фекально-оральный (водный, пищевой и контактно-бытовой пути). Наиболее часто передача осуществляется:
- через водопроводную воду;
- при употреблении плохо промытых зелени и овощей (или промытых под водопроводной водой без последующей термической обработки);
- при нарушении правил санитарной гигиены, особенно в детских коллективах.
Доза заражения — от 10 до 100 цист (в зависимости от индивидуальных свойств иммунной реактивности кишечника). Возможны случаи невосприимчивости к паразитам: цисты лямблий, встречая агрессивно настроенную среду кишечника, проходят транзитом и выделяются в окружающую среду в неизменённом виде.
Иммунитет после лямблиоза нестойкий и ненапряжёный, возможно повторное заражение. Повышенный риск заболевания имеют лица с патологией иммунитета кишечника и дефицитом IgA. [2] [3] [5] [8] [10]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы лямблиоза
Инкубационный период длится от нескольких дней до месяца и более. Чаще всего при заболевании не наблюдается вообще никаких клинических проявлений, особенно у взрослых.
К основным возможным симптомам лямблиоза относятся:
- Симптомы интоксикации и вегетативных изменений — повышенная утомляемость, плаксивость, раздражительность, нарушение ритма сна, головокружения, аритмии, субфебриллитет и другие.
- Симптомы поражения ЖКТ — дискомфорт и боли различной интенсивности и характера в различных отделах живота, тошнота, снижение аппетита, появление чувства горечи во рту, нарушения стула (запоры и поносы), налёт на языке и неприятный запах изо рта, снижение массы тела и другое.
- Симптомы поражения кожи — аллергические высыпания различного характера и локализации, атопический дерматит, бледность и шероховатость кожи, повышенная сухость покровов, хейлит (воспалительные изменения кожи губ и их слизистой), заеды (трещинки в уголках рта), нетипичное/неконтролируемое течение хронических патологий кожи.
- Усиление развития и обострения заболеваний, прямо не связанных с лямблиозом — бронхиальная астма, псевдоаллергические явления, гастриты, язвы желудка и двенадцатиперстной кишки, холецистит, неспецифический язвенный колит, артриты и другое.
- Симптомы мальабсорбции (потери питательных веществ) — авитаминозы, отставание в физическом и умственном развитии, дистрофия (эти проявления более характерны для детей).
Лямблиоз у детей
Как правило, у детей первыми симптомами лямблиоза становится появление субфебрильной или фебрильной температуры (37,1–38,0°C или 38,0–39,0°C), болей в животе, тошноты, иногда рвоты, метеоризма, жидкого стула. Живот при этом болезнен, вздут, урчит по ходу кишечника. Грудные дети становятся беспокойными, кричат, нарушается сон, симптомы лямблиоза усиливаются во время и после кормления, возможно появление аллергодерматозов и опрелостей. В динамике при отсутствии лечения это может приводить к нарушению роста и психоэмоционального развития, частым простудным или аллергическим заболеваниям, развитию хронических проблем органов ЖКТ.
У детей более позднего возраста и взрослых яркие симптомы лямблиоза наблюдаются редко — на первый план выходит постепенное развитие диспепсических явлений со стороны ЖКТ умеренного характера:
- метеоризм;
- дискомфорт и боли в животе преимущественно в околопупочной области и правом подреберье;
- нарушения стула в различных сочетаниях;
- появление налёта на языке;
- иногда горечь во рту и кожные проявления (усиление выраженности угревой сыпи, хронических полиэтиологических заболеваний, например, псориаза и дерматитов);
- возможны вегетативные расстройства, головные боли, головокружения, неустойчивость артериального давления, повышения температуры тела, чувствительность лимфоузлов.
Лямблиоз у беременных
Лямблиоз у беременных не имеет каких-либо специфичных отличий от лямблиоза у остальных людей, но может приводить к повышению риска развития у беременной В-12 дефицитной анемии и снижению веса плода (гипотрофии). [1] [3] [5] [7] [10]
Патогенез лямблиоза
Характерен так называемый "симптом манной крупы" — белёсые полусферические выбухания слизистой оболочки двенадцатиперстной кишки, представляющие собой зоны очагового отёка со скоплением увеличенного количества лейкоцитов.
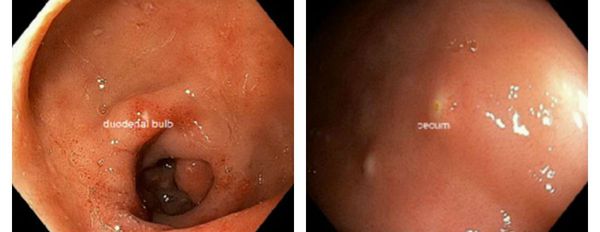
Посредством механического раздражения и выделения паразитами продуктов жизнедеятельности (токсическое влияние) происходит стимуляция образования слизи, повышение регенераторной функции кишечника, нарушение выработки факторов нейрогуморальной регуляции пищеварения (холецистоцикин и других) и двигательной активности гепатогастродуоденальной области. Это ведёт к дезорганизации висцеро-висцеральных связей области двенадцатиперстной кишки, поджелудочной железы и желчевыводящей системы, а также к нарушению функционирования органов ЖКТ, нарушению микробиоценоза кишечника, активизации анаэробной флоры, расстройствам расщепления и всасывания белков, жиров, углеводов, витаминов и микроэлементов.
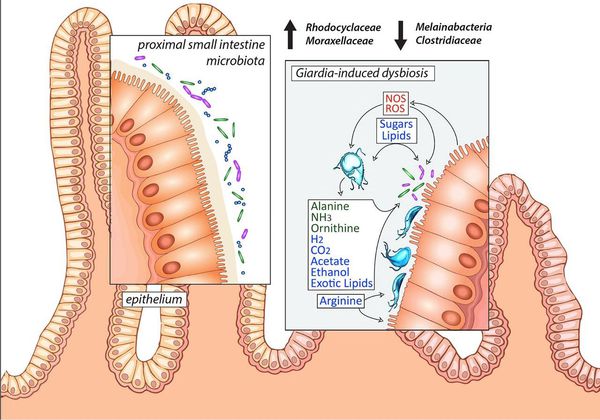
Возникает воспаление слизистой кишечника по типу реакций гиперчувствительности замедленного типа, происходит воздействие на иммунорегуляторные белки (мимикрия), снижение выработки иммуноглобулинов (в частности IgA) из-за нарушения всасывания белков и снижение фагоцитарной активности. Всё это в совокупности со всасываемыми продуктами жизнедеятельности лямблий становится причиной истощения иммунной системы (как кишечника, так и общего иммунитета), развития хронического поражения кишечника, провоцирует длительное обострение имеющихся хронических заболеваний и усугубление ряда аллергозависимых дерматозов. [1] [4] [7] [8]
Классификация и стадии развития лямблиоза
По клинической форме лямблиоз бывает:
- бессимптомным (носительство);
- кишечным — преимущественно симптомы кишечной формы, но можгут быть и гастритические проявления (дискомфорт в животе, неустойчивый стул, тошнота);
- билиарно-панкреатическим (рефлекторный) — дискомфорт в эпигастрии и правом подреберье, привкус горечи во рту, повышенная частота развития плохо контролируемых гастродуоденитов и панкреатитов;
- астено-невротическим — слабость, вялость, повышенная утомляемость, раздражительность, эмоциональная неустойчивость;
- токсико-аллергическим — периодические высыпания на теле, обострение хронических кожных заболеваний и бронхиальной астмы, эозинофилия;
- смешанным.
Течение лямблиоза бывает трёх типов:
- острым — до одного месяца;
- подострым — 1-3 месяца;
- хроническим — более трёх месяцев.
По наличию осложнений лямблиоз бывает:
Выделяют три степени заболевания:
Осложнения лямблиоза
Возможны специфические и неспецифические осложнения лямблиоза.
К специфическим относятся:
-
— зудящие обширные высыпания на теле;
- отёк Квинке — выраженный отёк подкожной клетчатки, иногда сопровождающийся зудоим и чувством удушья;
- офтальмопатия — нарушения восприятия органом зрения;
- артрит — дискомфорт и боли в суставах;
- гипокалиемическая миопатия — слабость определённых групп мышц.
К неспецифическим осложнениям относятся:
- наслоение интеркуррентных заболеваний (вторичная флора);
- белково энергетическая недостаточность (гипо- и авитаминоз, снижение веса, анемия и другие). [1][2][8][10]
Диагностика лямблиоза
Лабораторная диагностика лямблиоза включает в себя:
- Клинический анализ крови — в остром периоде наблюдается эозинофилия, базофилия и повышение СОЭ; в последующие периоды — умеренная эозинофилия или нормальное значение эозинофилов, иногда незначительная базофилия.
- Биохимический анализ крови — иногда отмечается повышение уровня общего билирубина и амилазы.
- Копроовоскопическое исследование кала — "золотой стандарт" диагностики. Оно позволяет выявить цисты (наиболее часто) и вегетативные формы лямблий (в редких случаях). В виду прерывистого цистообразования показано неоднократное исследование с некоторым интервалом (семь дней). Существует широко распространённое заблуждение о том, что кал нужно сдавать "тёплым" (свежим). На самом деле, в этом нет никакой необходимости. Так как данное исследование предполагает обнаружение цист лямблий, которые очень устойчивы во внешней среде, период от дефекации до исследования никоим образом не влияет на информативность результата анализа.
- Иммунохроматографический метод и ПЦР-диагностика кала (выявление антигенов и нуклеиновых кислот паразита) — имеет хорошую информативность и вполне может применяться в комплексе с другими методами исследований.
- ИФА-диагностика — малоинформативное исследование, так как локализация лямблий в просвете кишечника не создаёт условий для полноценного иммунного ответа, который наблюдается в основном у детей при остром заболевании, что создаёт значительное число ошибочных результатов как гипо-, так и гирпедиагностики.
- Дуоденальное зондирование (выявление вегетативных форм лямблий в двенадцатиперстной кишке) — может применяться в сложных диагностических случаях и при подозрении на коинвазирование (например, описторхами при описторхозе).
- УЗИ органов брюшной полости и ФГДС — позволяют выявить признаки нарушения моторики гепатобилиарной области. [2][3][5][6][9]
Дифференциальная диагностика предполагает исключение следующих заболеваний:
- паразитарные заболевания другой этиологии (как кишечной, так и внекишечной локализации);
- хронический гастродуоденит (симптомосходная симптоматика);
- кишечные инфекции (сальмонеллёз, дизентерия, ротавирус и другие);
- дисбиоз кишечника (сборное понятие, характеризующееся неустойчивостью стула, дискомфортом в животе различного характера, снижением веса и другими симптомами). [1][5][9]
Лечение лямблиоза
Лечение острой формы лямблиоза, которая возникает в основном у детей, должно осуществляться в стационаре и включать в первую очередь дезинтоксикационную и дегидратационную терапию, а также щадящее питание.
Медикаментозная терапия
При подтверждении диагноза проводится этиотропное лечение одним из противолямблиозных препаратов (нитрогруппа) в сочетании с желчегонными средствами, и лекарствами, улучшающими микрофлору кишечника.
При длительном хроническом течении в виду персистирующей колонизации лямблиями слизистой оболочки тонкого кишечника и местным иммунодефицитом курс лечения должен быть комплексным, включающим:
- диета (потреблять меньше углеводов);
- средства этиотропного воздействия (химиопрепарат);
- приём желчегонных препаратов;
- иммунотерапию (усиление фагоцитоза и восполнение дефицита IgA);
- устранение дисбиоза кишечника (пробиотики).
К сожалению, в последнее время всё чаще встречаются штаммы лямблий, устойчивых к различным видам противопаразитарной терапии, поэтому средняя вероятность успешной эрадикационного лечения не превышает 85%.
Гигиена при лечении лямблиоза
Лямблиоз редко передаётся между членами семьи, если соблюдать простейшие гигиенические правила: мыть руки после посещения уборной, перед едой и после контакта с животными.
Лечение народными средствами
Эффективность и безопасность методов народной медицины научно не доказана. Без адекватного лечения лямблиоз может привести к различным осложнениям: крапивнице, отёку Квинке, нарушениям зрения, артриту и слабости мышц.
Лечение лямблиоза у детей
Новорождённых от лямблиоза, как правило, не лечат, так как нет подходящих препаратов. В основном рекомендуется улучшать микрофлору и работу кишечника.
Детей старшего возраста лечат так же, как и взрослых, но подбирают необходимую дозировку и форму препарата.
Лечение лямблиоза у беременных
Беременным лечение, как правило, противопоказано (потенциальный вред препаратов превышает пользу от лечения), в основном предпочтение отдаётся улучшению флоры и работы кишечника.
Контроль излеченности
После курса лечения проводится паразитологический контроль методом копроовоскопии или ПЦР не ранее двух недель после завершения курса лечения длительностью в три месяца со сдачей анализа раз в месяц. [1] [3] [4] [5]
Прогноз. Профилактика
При назначении адекватного лечения прогноз благоприятен, осложнения редки.
Специфической профилактики не разработано. Основной упор следует делать на меры соблюдения санитарных норм:
Что такое синдром Жильбера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Синдром Жильбера — это генетический пигментный гепатоз с аутосомно-доминантным типом наследования, протекающий с повышением уровня неконъюгированного (свободного) билирубина, чаще проявляющееся в период полового созревания и характеризующийся доброкачественным течением [1] .
Краткое содержание статьи — в видео:
Синонимы названия болезни: простая семейная холемия, конституциональная или идиопатическая неконъюгированная гипербилирубинемия, негемолитическая семейная желтуха.
По распространённости данное заболевание встречается не менее, чем у 5 % населения, в соотношении мужчин и женщин — 4:1. Впервые заболевание описал французский терапевт Августин Жильбер в 1901 году.
Чаще синдром Жильбера проявляется в период полового созревания и характеризуется доброкачественным течением. Основным проявлением этого синдрома является желтуха.
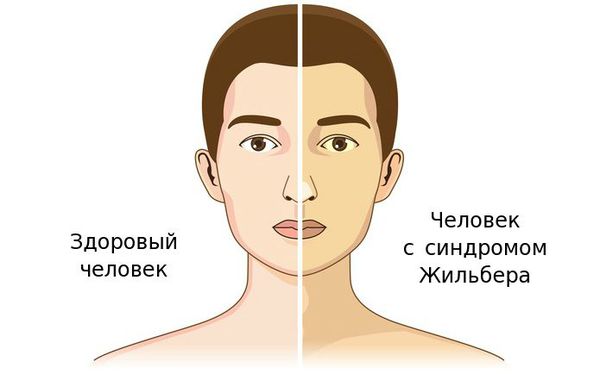
К провоцирующим факторам проявления синдрома можно отнести:
- голодание или переедание;
- жирную пищу;
- некоторые лекарственные средства;
- алкоголь;
- инфекции (грипп, ОРЗ, вирусный гепатит);
- физические и психические перегрузки;
- травмы и оперативные вмешательства.
Причина заболевания — генетический дефект фермента УДФГТ1*1, который возникает в результате его мутации. В связи с этим дефектом функциональная активность данного фермента снижается, а внутриклеточный транспорт билирубина в клетках печени к месту соединения свободного (несвязанного) билирубина с глюкуроновой кислотой нарушается. Это и приводит к увеличению свободного билирубина.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Жильбера
Некоторые специалисты трактуют синдром Жильбера не как болезнь, а как физиологическую особенность организма.
До периода полового созревания данный синдром может протекать бессимптомно. Позже (после 11 лет) возникает характерная триада признаков:
- желтуха различной степени выраженности;
- ксантелазмы век (жёлтые папулы);
- периодичность появления симптомов [1] .
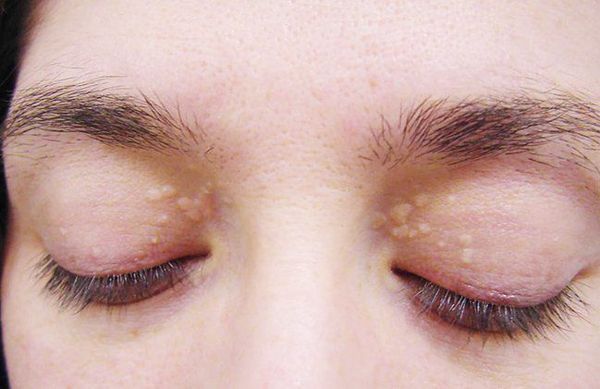
Желтуха чаще всего проявляется иктеричностью (желтушностью) склер, матовой желтушностью кожных покровов (особенно лица), иногда частичным поражением стоп, ладоней, подмышечных впадин и носогубного треугольника.
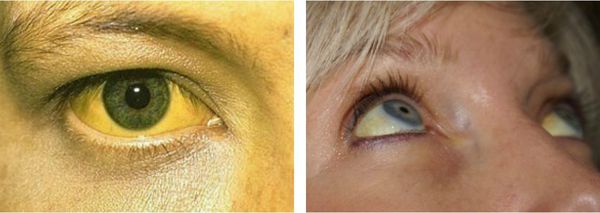
Заболевание нередко сочетается с генерализованной дисплазией (неправильным развитием) соединительной ткани.
Усиление желтухи может наблюдаться после перенесения инфекций, эмоциональной и физической нагрузки, приёма ряда лекарственных препаратов (в частности, антибиотиков), голодания и рвоты.
Клиническими проявлениями заболевания общего характера могут быть:
- слабость;
- недомогание;
- подавленность;
- плохой сон;
- снижение концентрации внимания.
В отношении ЖКТ синдром Жильбера проявляется снижением аппетита, изменением привкуса во рту (горечь, металлический привкус), реже возникает отрыжка, тяжесть в области правого подреберья, иногда наблюдается боль ноющего характера и плохая переносимость лекарственных препаратов.
При ухудшении течения синдрома Жильбера и существенном повышении токсичной (свободной) фракции билирубина может появляться скрытый гемолиз, усиливая при этом гипербилирубинемию и добавляя в клиническую картину системный зуд.
Патогенез синдрома Жильбера
В норме свободный билирубин появляется в крови преимущественно (в 80-85 % случаев) при разрушении эритроцитов, в частности комплекса ГЕМ, входящего в структуру гемоглобина. Это происходит в клетках макрофагической системы, особенно активно в селезёнке и купферовских клетках печени. Остальная часть билирубина образуется из разрушения других гемсодержащих белков (к примеру, цитохрома P-450).
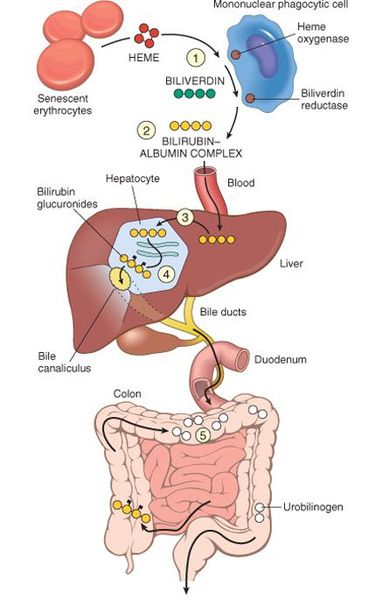
У взрослого человека в сутки образуется приблизительно от 200 мг до 350 мг свободного билирубина. Такой билирубин слаборастворим в воде, но при этом хорошо растворяется в жирах, поэтому он может взаимодействовать с фосфолипидами ("жирами") клеточных мембран, особенно головного мозга, чем можно объяснить его высокую токсичность, в частности токсичное влияние на нервную систему.
Первично после разрушения комплекса ГЕМ в плазме билирубин появляется в неконъюгированной (свободной или несвязанной) форме и транспортируется с кровью при помощи белков альбуминов. Свободный билирубин не может проникнуть через почечный барьер за счёт сцепления с белком альбумином, поэтому сохраняется в крови.
В печени несвязанный билирубин переходит на поверхность гепатоцитов. С целью снижения токсичности и выведения в клетках печени свободного билирубина при помощи фермента УДФГТ1*1 он связывается с глюкуроновой кислотой и превращается в конъюгированный (прямой или связанный) билирубин. Конъюгированный билирубин хорошо растворим в воде, он является менее токсичным для организма и в дальнейшем легко выводится через кишечник с желчью.
При синдроме Жильбера связывание свободного билирубина с глюкуроновой кислотой снижается до 30% от нормы, тогда как концентрация прямого билирубина в желчи увеличивается.
В основе синдрома Жильбера лежит генетический дефект — наличие на промонторном участке A(TA)6TAA гена, кодирующего фермент УДФГТ1*1, дополнительного динуклеотида ТА. Это становится причиной образования дефектного участка А(ТА)7ТАА. Удлинение промонторной последовательности нарушает связывание фактора транскрипции IID, в связи с чем уменьшается количество и качество синтезируемого фермента УДФГТ1, который участвует в процессе связывания свободного билирубина с глюкуроновой кислотой, преобразуя токсичный свободный билирубин в нетоксичный связанный.
Вторым механизмом развития синдрома Жильбера является нарушение захвата билирубина микросомами сосудистого полюса клетки печени и его транспорта глутатион-S-трансферазой, которая доставляет свободный билирубин к микросомам клеток печени.
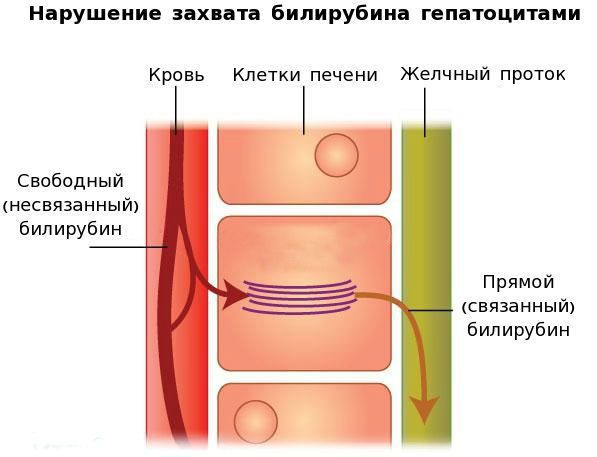
В конечном итоге вышеперечисленные патологические процессы приводят к увеличению содержания свободного (несвязанного) билирубина в плазме, что обуславливает клинические проявления заболевания [6] .
Классификация и стадии развития синдрома Жильбера
Общепринятой классификации синдрома Жильбера не существует, однако условно можно разделить генотипы синдрома по полиморфизму.
Читайте также:

