Золотистый стафилококка и алкоголь
Обновлено: 18.04.2024
Бактериофаг представляет собой прозрачную жидкость желтого цвета различной интенсивности, возможен зеленоватый оттенок.
Биологические свойства
Пиобактериофаг поливалентный обладает способностью специфически лизировать бактерии стафилококков, стрептококков (в том числе энтерококков), протея, клебсиелл пневмонии, синегнойной и кишечной палочек.
Состав
В 1 мл препарата содержится:
Действующее вещество.
Стерильные очищенные фильтраты фаголизатов бактерий Staphylococcus spp., Streptococcus spp., Proteus (P. vulgaris, P. mirabilis), Pseudomonas aeruginosa, Klebsiella pneumoniae, энтеропатогенных Escherichia coli (с активностью по Аппельману - не менее 10 -5 ) - до 1,0 мл.
Вспомогательное вещество.
Фармакотерапевтическая группа
Прочие терапевтические средства.
Классификация по ICTV: Caudovirales.
Код АТХ: V03А.
Фармакологические свойства
Специфическая активность. Препарат должен лизировать бактерии Staphylococcus, Streptococcus, Proteus vulgaris, Proteus mirabilis, Kl. pneumoniae, Ps. aeruginosa, E. coli в разведении не менее 10 -5 по методу Аппельмана.
Фармакодинамика. Активность бактериофага при наличии фагочувствительности бактериального штамма проявляется в виде проникновения, внутриклеточного размножения, разрушения бактериальной клетки и выхода фаговых частиц, готовых к заражению новых бактериальных клеток.
После перорального однократного приема бактериофага, фаговые частицы обнаруживаются через 1 час в образцах крови, через 1-1,5 часа на поверхности ожоговых ран и в бронхиальном содержимом, через 2 часа в ликворе и моче. В каловых массах выявлялось фаговых частиц в 3 раза больше, чем в моче.
По данным литературы, клиническая эффективность фаготерапии сопоставима с результатами лечения у пациентов, получающих антибиотикотерапию.
Фармакокинетика. Исследования по фармакокинетике, проведенные на лабораторных животных доказали, что бактериофаг, введенный любым способом, поступает в общий ток крови, но обычно в крови не задерживается, а адсорбируется различными тканями, оседая в первую очередь в лимфатических узлах, в печени и селезенке. Выведение из организма происходит через кишечник и почки.
По литературным данным длительность пребывания бактериофагов и уровень выхода фагов зависят от присутствия гомологичного фагочувствительного штамма-возбудителя инфекции в организме. При отсутствии гомологичного возбудителя через 2 часа после однократного приема наблюдается массивное выделение фагов с мочой, снижающееся до единичных к концу первых суток. Однако низкий уровень выхода фагов может поддерживаться до 6 суток. Высокое содержание фаговых частиц в образцах и длительное его выделение свидетельствует о происходящем в организме процессе размножения бактериофагов в очаге инфекции.
Гематоэнцефалический барьер у здорового животного является барьером для проникновения фагов в центральную нервную систему. Нарушение центрального барьера даже в слабой степени влечет за собой поступление бактериофага из кровяного русла в ликвор.
Показания к применению
Лечение и профилактика гнойно-воспалительных и энтеральных заболеваний, вызванных стафилококками, стрептококками, протеями, клебсиеллами, синегнойной и кишечной палочками:
- заболевания уха, горла, носа, дыхательных путей и легких - воспаления пазух носа, среднего уха, ангина, фарингит, ларингит, трахеит, бронхит, пневмония, плеврит;
- хирургические инфекции - нагноение ран, ожоги, абсцесс, флегмона, фурункулы, карбункулы, гидроаденит, панариции, парапроктит, мастит, бурсит, остеомиелит;
- урогенитальные инфекции - уретрит, цистит, пиелонефрит, кольпит, эндометрит, сальпингоофорит;
- посттравматические конъюктивиты, кератоконъюктивиты, гнойные язвы роговицы и иридоциклиты;
- энтеральные инфекции - гастроэнтероколит, холецистит, дисбактериоз;
- генерализованные септические заболевания;
- гнойно-воспалительные заболевания новорожденных - омфалит, пиодермия, конъюктивит, гастроэнтероколит, сепсис и др.;
- другие заболевания, вызванные бактериями стафилококков, стрептококков (в том числе энтерококков), протея, клебсиелл пневмонии, синегнойной и кишечной палочек.
При тяжелых проявлениях инфекций, вызванных стафилококками, стрептококками, протеем, клебсиеллой пневмонии, синегнойной и кишечной палочками, препарат назначается в составе комплексной терапии.
С профилактической целью препарат используют для обработки операционных и свежеинфицированных ран, а также для профилактики внутрибольничных инфекций по эпидемическим показаниям.
Важным условием эффективной фаготерапии является предварительное определение фагочувствительности возбудителя.
Способ применения и дозировка
Перед использованием флакон с бактериофагом необходимо взболтать и просмотреть. Препарат должен быть прозрачным и не содержать осадка.
Лечение гнойно-воспалительных заболеваний с локализованными поражениями должно проводиться одновременно как местно, так и приемом препарата внутрь в течение 7-20 дней (по клиническим показаниям).
В зависимости от характера очага инфекции бактериофаг применяют:
1. Местно в виде орошения, примочек и тампонирования жидким фагом в количестве до 200 мл в зависимости от размеров пораженного участка. При абсцессах бактериофаг вводят в полость очага после удаления гноя с помощью пункции. Количество вводимого препарата должно быть несколько меньше объема удаленного гноя. При остеомиелите после соответствующей хирургической обработки в рану вливают бактериофаг по 10-20 мл.
2. Введение в полости - плевральную, суставную и другие ограниченные полости до 100 мл бактериофага, после чего оставляют капиллярный дренаж, через который в течение нескольких дней повторно вводят бактериофаг.
3. При циститах, пиелонефритах, уретритах препарат принимают внутрь. В случае, если полость мочевого пузыря или почечной лоханки дренированы, бактериофаг вводят через цистостому или нефростому 1-2 раза в день по 20-50 мл в мочевой пузырь и по 5-7 мл в почечную лоханку.
4. При гнойно-воспалительных гинекологических заболеваниях препарат вводят в полость вагины, матки в дозе 5-10 мл ежедневно однократно.
5. При гнойно-воспалительных заболеваниях уха, горла, носа препарат вводят в дозе 2-10 мл 1-3 раза в день. Бактериофаг используют для полоскания, промывания, закапывания, введения смоченных турунд (оставляя их на 1 час).
6. При конъюктивитах и кератоконъюктивитах препарат закапывают по 2-3 капли 4-5 раз в день, при гнойной язве роговицы - по 4-5 капель, при гнойных иридоциклитах препарат применяют по 6-8 капель каждые 3 часа в сочетании с приемом внутрь.
7. При лечении стоматитов и хронических генерализованных пародонтитов препарат используют в виде полосканий полости рта 3-4 раза в день в дозе 10-20 мл, а также введением в пародонтальные карманы турунд, пропитанных пиобактериофагом, на 5-10 минут.
8. При кишечных формах заболевания, заболеваниях внутренних органов, дисбактериозе бактериофаг применяют через рот и в виде клизм в течение 7-20 дней. Через рот бактериофаг дают 3 раза в сутки натощак за 1 час до еды. В виде клизм назначают 1 раз в день вместо одного приема через рот.
Рекомендуемые дозировки препарата
| Возраст пациента | Доза на 1 прием (мл) | |
| Внутрь | В клизме | |
| 0-6 мес. | 5 | 10 |
| 6-12 мес. | 10 | 20 |
| От 1 года до 3 лет | 15 | 20-30 |
| От 3- до 8 лет | 20 | 30-40 |
| От 8 лет и старше | 20-30 | 40-50 |
В случае, если до применения бактериофага для лечения ран применялись химические антисептики, рана должна быть тщательно промыта стерильным 0,9% раствором натрия хлорида.
Применение бактериофага у детей (до 6 месяцев). При сепсисе, энтероколите новорожденных, включая недоношенных детей, бактериофаг применяют в виде высоких клизм (через газоотводную трубку или катетер) 2-3 раза в сутки (см. табл.). При отсутствии рвоты и срыгивания возможно применение препарата через рот. В этом случае он смешивается с грудным молоком. Возможно сочетание ректального (в клизмах) и перорального (через рот) применения препарата. Курс лечения 5-15 дней. При рецидивирующем течении заболевания возможно проведение повторных курсов лечения. С целью профилактики сепсиса и энтероколита при внутриутробном инфицировании или опасности возникновения внутрибольничной инфекции у новорожденных детей бактериофаг применяют в виде клизм 2 раза в день в течение 5-7 дней.
При лечении омфалитов, пиодермий, инфицированных ран препарат применяют в виде аппликаций ежедневно двукратно (марлевую салфетку смачивают бактериофагом и накладывают на пупочную ранку или на пораженный участок кожи).

Новость
Структурная формула нового пептидного антибиотика.
Автор
Редакторы
- Антибиотики
- Биомолекулы
- Биотехнологии
- Здравоохранение
- Микробиология
- Фармакология
Немецкие ученые обнаружили новое оружие для борьбы с больничным монстром — мультирезистентным золотистым стафилококком. Долгие годы оно скрывалось не в вечной мерзлоте или Марианской впадине, а прямо под нашим носом. Вернее — в нём.
В последние годы во всем мире увеличилось количество инфекционных заболеваний, вызванных устойчивыми к антибиотикам бактериями. Организмы с множественной лекарственной резистентностью (multidrug-resistant organisms, MDRO), такие как метициллин-резистентный золотистый стафилококк, нечувствительные к ванкомицину энтерококки или резистентные к цефалоспоринам третьего поколения грамотрицательные бактерии, в ближайшие десятилетия могут стать более частыми причинами смерти, чем рак [1].
Несколько лет назад удалось обнаружить, что представители человеческой микробиоты способны производить бактериоцины, поражающие близкородственных бактерий [2]. Например, в 2014 году из человеческого комменсала Lactobacillus gasseri выделили и описали новый синтезируемый рибосомами тиопептидный антибиотик — лактоциллин [3].
Семейные разборки
Немецкий исследователь Александр Ципперер со своими сотрудниками в июле 2016 года сообщил о том, что обнаружил в человеческом носу бактерию Staphylococcus lugdunensis IVK28, которая подавляет рост метициллин-резистентного золотистого стафилококка (methicillin-resistant Staphylococcus aureus, MRSA) [1].
Золотистый стафилококк
Стафилококки относятся к типичным бактериям-комменсалам, колонизирующим кожу и поверхности слизистых оболочек. Staphylococcus aureus — шаровидные грамположительные бактерии, вырабатывающие каротиноидный пигмент, который придает их клеткам золотистый цвет (рис. 1). Эти микроорганизмы чрезвычайно устойчивы к внешним воздействиям и выживают в воздухе, пыли, почве, продуктах питания, на оборудовании пищевых производств и предметах быта [6], [7].

Рисунок 1. Staphylococcus aureus и лейкоциты.

Рисунок 2. Метициллин-резистентные золотистые стафилококки.
Staphylococcus aureus — бактерия условно-патогенная, проявляющая свои патологические свойства только в благоприятных условиях, а создает их, как правило, ослабление иммунитета носителя. Активная жизнедеятельность стафилококка может привести к разнообразным заболеваниям [5], [7], [8]:
- кожи (прыщи, фурункулы, синдром ошпаренной кожи);
- органов дыхания (плеврит, пневмония);
- костной и соединительной тканей (артрит, остеомиелит);
- нервной системы и органов чувств (отит, менингит);
- сердечно-сосудистой системы (эндокардит, флебит, стафилококковая бактериемия).
Факторы патогенности S. aureus — это микрокапсула, компоненты клеточной стенки, ферменты агрессии и токсины. Микрокапсулы защищают клетки бактерий от фагоцитоза, способствуют их адгезии и распространению по организму хозяина. Составляющие клеточной стенки (например пептидогликан, тейхоевые кислоты и белок А) вызывают развитие воспаления, обездвиживают фагоциты и нейтрализуют иммуноглобулины. Коагулаза, главный фермент агрессии, вызывает свертывание плазмы крови [7], [9].
Наиболее опасны метициллин-резистентные стафилококки (methicillin-resistant S. aureus, MRSA) (рис. 2). Метициллин — это модифицированный пенициллин, с помощью которого еще недавно успешно боролись со стафилококковой инфекцией. MRSA устойчивы не только к метициллину, но и к другим антибиотикам пенициллиновой группы (диклоксациллину, оксациллину, нафциллину и др.), а также к цефалоспоринам. В последнее время выявлены штаммы и с более широким спектром устойчивости: ванкомицин-резистентные (VRSA) и гликопептид-резистентные (GISA) [6], [9], [10].
Штамм S. lugdunensis IVK28 эффективно боролся со своим вредоносным родственником лишь в условиях недостатка железа и только на твердых агаризованных средах (рис. 3, слева). Механизм противостояния был неясен, а потому Ципперер провел транспозонный мутагенез клеток выделенного штамма — чтобы выявить ген, ответственный за синтез смертельного для S. aureus вещества.

В итоге удалось получить мутанта IVK28, который не мог подавлять рост MRSA. Анализ места встройки транспозона показал, что тот нарушил структуру гена предполагаемой нерибосомной пептидсинтетазы (НРПС). Оказалось, что этот ген вместе с другими последовательностями, связанными с биосинтезом антибиотиков, входит в состав оперона размером 30 т.п.н. Это указывало на то, что предполагаемая молекула ингибитора может быть комплексом нерибосомных пептидов.
Оперон методом ПЦР обнаружили во всех культурах S. lugdunensis, а значит, он характерен для всего вида, а не только для штамма IVK28. Однако GC-состав оперона (26,9%) отличался от GC-состава остального генома S. lugdunensis (33,8%), что свидетельствовало о возможном заимствовании этого полезного генетического кластера у других видов бактерий — путем горизонтального переноса .
Оперон состоит из генов lugA, B, C и D, кодирующих пептидсинтетазные белки (см. врезку ниже), а также из других генов, чьи продукты необходимы для синтеза и транспорта нерибосомного пептида.
Чтобы окончательно вменить оперону участие в антибактериальной деятельности S. lugdunensis, наименьший ген (lugD) удалили. Мутант ΔlugD, как и ожидалось, не мог подавлять рост золотистого стафилококка, но когда в него ввели плазмиду с работающим геном lugD, агрессивный фенотип восстановился (рис. 3, в центре и справа).
Секретное оружие
Выделенный Ципперером продукт lug-оперона оказался нерибосомным циклическим пептидом, состоящим из пяти аминокислот (двух D-валинов, L-валина, D-лейцина и L-триптофана) и тиазолидинового гетероцикла (рис. 4). Назвали антибиотик лугдунином.

Химическим синтезом удалось получить продукт с идентичными природному лугдунину химическими свойствами и антибактериальным эффектом. Ученые предположили, что этот антибиотик ингибирует синтез бактериальных биополимеров — белков, ДНК и пептидогликанов [5].
Нерибосомные пептиды
Этот класс пептидов синтезируется в клетках низших грибов и бактерий без участия рибосом. Нерибосомные пептиды (НРП) также встречаются и у высших организмов, которые имеют бактерий-комменсалов [12].
НРП подразделяются на несколько функциональных групп [13]:
- антибиотики (ванкомицин);
- предшественники антибиотиков (ACV-трипептид — предшественник пенициллина и цефалоспорина);
- иммуносупрессоры (циклоспорин);
- противоопухолевые пептиды (блеомицин);
- сидерофоры (пиовердин);
- токсины (HC-токсин);
- сурфактанты (сурфактин).
Строение
Синтез
Каждый модуль состоит как минимум из трех доменов:
- конденсирующего (принимающего пептидную цепь из предыдущего модуля);
- аденилирующего (выбирающего нужную аминокислоту);
- пептидильного (образующего пептидную связь).
Нередко модули включают и другие домены, в том числе эпимеризующий, который преобразует L-аминокислоты в D-формы [14].
По аналогии с триплетным рибосомным кодом для синтеза белка существует и нерибосомный, код НРПС, определяемый 10 остатками аминокислот в субстрат-связывающем кармане аденилирующего домена. От комбинации этих остатков зависит то, какая аминокислота будет встроена в пептид конкретным модулем НРПС. Зная этот код, можно предсказывать субстратную специфичность аденилирующих доменов и даже произвольно изменять ее посредством замены аминокислот в домене [14].
В экспериментах немецких ученых лугдунин действовал не только на метициллин-резистентных стафилококков, но и на гликопротеин-резистентных, и даже на других грамположительных бактерий типа листерии и ванкомицин-резистентного энтерококка (табл. 1). Минимальная ингибирующая концентрация (МИК) нового бактериоцина — 1,5–12 мкг × мл −1 , что говорит о высокой активности вещества. При этом такие концентрации никак не влияли на человеческую сыворотку, не вызывали лизис нейтрофилов или эритроцитов и не ингибировали метаболическую активность моноцитов. Бактериальные же клетки под действием лугдунина в концентрации даже ниже МИК прекращали синтезировать ДНК, РНК, белки и компоненты клеточной стенки. В этом отношении лугдунин напоминает даптомицин, дающий такой же эффект, но способ действия которого пока не изучен. Не было отмечено возникновения резистентности клеток S. aureus к лугдунину даже после их месячного выращивания на малых концентрациях.
| Виды и штаммы | Резистентность | МИК лугдунина (мкг × мл −1 ) |
|---|---|---|
| Staphylococcus aureus USA300 (LAC) | MRSA | 1,5 |
| + 50% человеческой сыворотки крови | 1,5 | |
| Staphylococcus aureus USA300 (NRS384) | MRSA | 1,5 |
| Staphylococcus aureus Mu50 | GISA | 3 |
| Staphylococcus aureus SA113 | 3 | |
| Staphylococcus aureus RN4220 | 3 | |
| Enterococcus faecium BK463 | VRE | 3 |
| Enterococcus faecalis VRE366 | VRE | 12 |
| Listeria monocytogenes ATCC19118 | 6 | |
| Streptococcus pneumoniae ATCC49619 | 1,5 | |
| Bacillus subtilis 168 (trpC2) | 4 | |
| Pseudomonas aeruginosa PAO1 | >50 | |
| Escherichia coli DH5α | >50 | |
| Условные обозначения: MRSA — метициллин-резистентные S. aureus; GISA — устойчивые к гликопротеинам S. aureus; VRE — ванкомицин-резистентные Enterococcus. Таблица из [1]. | ||
Испытания в боевых условиях
Как и полагается, способность лугдунина лечить стафилококковые инфекции продемонстрировали in vivo на мышиной модели (рис. 5). У шести мышей сбрили шерсть на спине и, повредив кожу многократным приклеиванием/отклеиванием пластыря, нанесли на это место золотистого стафилококка. Затем кожу обработали мазью, содержащей 1,5 мкг лугдунина, и спустя шесть часов оценили результат. Обработка новым антибиотиком сильно сокращала или даже полностью уничтожала популяцию S. aureus. Причем не только на поверхности кожи, но и в более глубоких ее слоях.

Рисунок 5. Общая схема подхода к идентификации природного антибиотика. Из бактериальных популяций человеческого тела отбирают представителей, которые не могут сосуществовать с интересующими патогенными бактериями. Этих возможных конкурентов тестируют по отдельности на средах с инфекционным агентом. Из культуры, успешно подавляющей рост патогенов, выделяют антибиотик, действие которого проверяют на животных моделях.
[5], рисунок модифицирован и адаптирован
Чтобы понять, может ли S. lugdunensis помешать колонизации носовой полости позвоночных животных золотистым стафилококком в естественных условиях, ученые провели следующий эксперимент. В носы хлопковых хомяков ввели два вида смешанных культур (S. aureus + S. lugdunensis IVK28 и S. aureus + S. lugdunensis IVK28ΔlugD) и каждую по отдельности. В контрольных случаях, когда вводили по одному штамму, все три культуры стабильно колонизировали носовую полость. Однако при введении смеси S. aureus + S. lugdunensis IVK28 количество золотистого стафилококка через 5 дней значительно уменьшилось по сравнению со смесью S. aureus + S. lugdunensis IVK28ΔlugD. Этот эксперимент показал, что продукция лугдунина позволяет штамму IVK28 эффективно конкурировать с золотистым стафилококком in vivo.
Оставалось разобраться, предотвращает ли присутствие S. lugdunensis в носу человека колонизацию бактериями S. aureus. Ципперер и его коллеги исследовали мазки из носовых ходов 187 госпитализированных больных. Из них у 60 человек (32,1%) обнаружили золотистого стафилококка и у 17 человек (9,1%) — S. lugdunensis. И только у одного пациента с S. lugdunensis в носу обитал S. aureus. У всех выделенных штаммов S. lugdunensis ПЦР-анализ продемонстрировал наличие lug-оперона, а все обнаруженные штаммы S. aureus оказались восприимчивы к лугдунину.
Перспективы
Лугдунин оказался первым обнаруженным бактериоцином нового класса — макроциклических тиазолидиновых пептидных антибиотиков. Все проверенные штаммы S. aureus (как природные, так и лабораторные) не смогли выработать резистентности к нему. Это дает надежду на то, что лугдунин в будущем станет коммерческим препаратом для борьбы с золотистым стафилококком.
И наконец, сам факт обнаружения нового антибиотика у представителя человеческой микробиоты должен послужить стимулом для активизации поиска других продуцентов бактериоцинов в составе именно таких сообществ. В дальнейшем это поможет медикам успешнее сдерживать наступление мультирезистентных патогенов.

Обзор
Автор
Редакторы

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Немного о VR
В видео есть часть, где представлена VR-работа. Чтобы лучше понять, что где находится — прочитайте, пожалуйста, описание ниже:
- Для удобства рассмотрения внутренних процессов, происходящих в бактериальной клетке, клеточная стенка и цитоплазматическая мембрана сделаны прозрачными.
- В цикле репродукции вируса рассматривается один вид бактериофага. Это стафилококковый бактериофаг 80α (альфа).
- Процессы репликации, трансляции и транскрипции упрощены, и для лучшего ви́дения этих процессов они немного разнесены в пространстве.
Золотистый стафилококк
Стафилококки — грамположительные и не спорообразующие кокки, которые образуют пары, короткие цепочки или гроздья. Род Staphylococcus содержит много видов, которые отделяются друг от друга на основе продукции фермента коагулазы [1].
Золотистый стафилококк (Staphylococcus aureus) — коагулазоположительный вид, является одним из самых вирулентных видов.
Золотистый стафилококк — часто безвредный обитатель эпителия кожи и слизистых оболочек человека, но также связан с серьезными системными и местными инфекциями [2] и является одной из наиболее распространенных причин пищевых инфекций во всем мире. S. aureus производит 15 энтеротоксинов.
Энтеротоксины бактериальные токсины, которые вызывают секрецию жидкости из клеток кишечника.
Борьба с золотистым стафилококком
Борьба с бактериями велась издавна. Люди пробовали лечить раны растениями. И методом проб и ошибок подбирали нужные противомикробные лекарства [3].
Уже в 1940 году появились первые сведения об устойчивости бактерий к пенициллину.
Бактериофаг
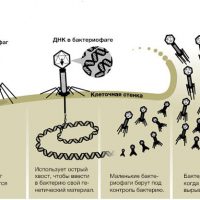
В 1919 году, еще до обнаружения пенициллина, Феликс Д’Эрелль открыл совершенно другой метод борьбы с бактериями. Но потом он так и не смог конкурировать с антибиотиками. Речь идет о бактериофаговой терапии.
Бактериофаги (фаги) — это вирусы, которые используют для размножения только прокариотические клетки. Эти вирусы встречаются в природе повсеместно [6]. S. aureus был одним из первых организмов, использованных для демонстрации существования бактериофага [2].
В 1920–1940-е годы проводили множество исследований по клиническому применению бактериофагов, но стабильных результатов получено не было. На Западе от бактериофаговой терапии начали отказываться [7].
Борьба золотистого стафилококка и бактериофага
Сейчас фаговые препараты представляют собой смеси нескольких бактериофагов. Мы остановимся на одном из стафилококковых фагов.
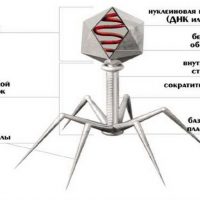
Фаг 80α — умеренный бактериофаг лямбда семейства Siphoviridae с геномом в виде двухцепочечной ДНК. 80α способен к генерализованной трансдукции, а также может выступать в качестве помощника для мобилизации островков патогенности SaPI [2], которые, как было показано, кодируют такие факторы вирулентности, как токсины синдрома токсического шока и коагулаза [1].
Как и у других бактериофагов, капсид 80α собирается в виде пустого предшественника — прокапсида. Горсти фаговой ДНК упаковываются в прокапсиды через портальную вершину в АТФ-зависимом процессе, который требует малых и больших субъединиц фермента терминазы. Упаковка ДНК сопровождается расширением капсида и структурной перестройкой оболочки.
Для бактериофаговой терапии рекомендуется использовать те бактериофаги, которые идут по литическому пути развития (с разрывом клетки).
Бактериофаговые препараты
Сейчас с развитием современных методов генной инженерии и молекулярной биологии бактериофаговая терапия оживает в новых исследованиях. И на данный момент бактериофаговая терапия применяется очень осторожно и строго контролируемо, во избежание повторения истории с антибиотиками.
Однако не везде соблюдаются такие строгие стандарты. В Западной Европе после открытия антибиотиков от использования бактериофагов довольно быстро отказались. В Восточной Европе, несмотря на отсутствие крупных и контролируемых клинических испытаний, они оставались относительно популярным лечением в XX веке [8].
Приглашение от авторов проекта
Мы хотим, чтобы у всех была возможность окунуться в микромир. Поэтому приглашаем жителей Санкт-Петербурга лично посетить виртуальную реальность. Чтобы сделать это, напишите Надежде в Instagram (irreal.art) или Ярославе в VK.
Так мир познакомился с микроорганизмами, питающимися бактериями, которые много тысяч лет делали свое дело слаженно, не давая бактериям уничтожить все живое на земле. В 1921 г. Д. Мэйсон и Р. Брайон впервые описали успешное лечение стафилококковой инфекции кожи с помощью стафилококкового бактериофага. Во время Второй мировой войны бактериофаги использовались при гнойно-септических инфекциях, дизентерии, тифе и др.
Бактериофаги еще в прошлом столетии доказали свою эффективность и безопасность. Почему же бактериофаги до сих пор не стали основными средствами борьбы с инфекцией? Это объясняется несколькими причинами. Главная — открытие новой группы препаратов – антибиотиков, надолго оттеснившее интерес к бактериофагам. Плюс:
- недостаточная информированность врачей и пациентов,
- отсутствие фагов ко многим патогенным бактериям,
- неэффективность лечения в связи с неправильным подбором бактериофагов для лечения конкретного больного,
- недостаточно изученное иммунологическое взаимодействие бактериофагов и организма человека,
- отсутствие нормативно-правовых аспектов применения бактериофагов в лечении инфекций человека.
Что такое бактериофаги![Механизм]()
В 1939 году А. Флемингом был открыт антибиотик, и началась эра антибиотиков в лечении бактериальных инфекций. Появилось большое количество антибиотиков 1, 2, 3, 4 поколений, причем антибиотики последнего поколения, которыми пользуются и сейчас, появились еще в 70-е годы прошлого столетия. На Западе и Америке отказались от бактериофагов и активно начали применять антибиотики.
Но А. Флеминг предупреждал о некоторых обязательных моментах применения антибиотиков:
- строгих показаниях к назначению,
- соблюдении продолжительности и запрете прерывания курса лечения,
- адекватных дозах препарата,
- способах введения,
- назначения их обязательно врачом,
- отпуске антибиотиков исключительно по рецепту.
Несоблюдение хотя бы части этих требований могло привести и, как оказалось, приводит к кризису антибиотиковой эры. Бактерии перестают реагировать на препараты. Пока ещё действуют антибиотики последнего поколения, решая труднейшие клинические проблемы, но рассчитывать на появление новых антибиотиков не приходится.
Россия на сегодняшний день оказалась самой развитой страной в области микробиологии изучения бактериофагов. Бактериофаги – это естественные антагонисты бактерий.
Каков механизм действия бактериофагов
Сегодня многие заболевания вызываются стафилококками, стрептококками, клебсиеллами и другими бактериями, и успешно могут лечиться бактериофагами. Это естественная альтернатива антибиотикам, возврат к природе.
Какие преимущества имеют бактериофаги в лечении бактериальных инфекций
Бактериофаги много тысяч лет делали свое дело, не давая бактериям уничтожить все живое на земле.
Бактериофаги могут применяться и у беременных, и у детей, во всех возрастных группах людей. Противопоказаний к их применению нет.
Фаги совместимы с различными лекарствами, в том числе с антибиотиками, причем они уменьшают непереносимость (резистентность) бактерий к антибиотикам.
Курс лечения бактериофагами более короткий (7-14 дней). Фаги практически не дают побочных явлений. Они определяются бактериальной зараженностью и распадом бактерий с выделением эндотоксина, но они значительно меньше, чем при приеме антибиотиков, эти явления легко снимаются приёмом энтеросорбентов. Бактериофаги можно применять при аллергических реакциях на антибиотики.
Бактериофаги, благодаря своей специфичности воздействия на бактерии, не убивают хорошие бактерии и не изменяют нормальную микрофлору кишечника. Они, в отличие от антибиотиков, не нарушают микробиом человека.
Какие виды бактериофагов известны
Известно, что бактериофаги действуют на один штамм бактерий, поэтому производятся препараты бактериофагов, действующих против разных штаммов одного возбудителя:
- стафилококковый бактериофаг,
- сальмонеллезный бактериофаг,
- стрептококковый бактериофаг,
- клебсиеллёзный бактериофаг (Клебсиелла пневмония),
- бактериофаг псевдомонас (против синегнойной палочки).
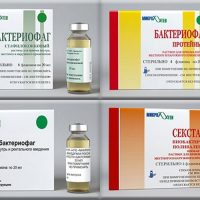
Производятся препараты против двух и более возбудителей, поливалентные бактериофаги:
- бактериофаг дизентерийный, действующий на разные штаммы дизентерийной палочки,
- клебсиеллезный бактериофаг против трёх видов клебсиелл,
- бактериофаг бактериальный поливалентный очищенный (действует на стрептококк, стафилококк, протей, клебсиеллу пневмонию, кишечную палочку, синегнойную палочку),
- пиобактериальный комплексный бактериофаг (против стафилококка, стрептококка, двух видов протея, двух видов клебсиеллы, энтерококков, энтеропатогенной кишечной палочки, синегнойной палочки),
- бактериофаг интестин-бактериальный против дизентерийной палочки, сальмонеллы, кишечной палочки, протея, энтерококков, стафилококков, синегнойной палочки,
- пиобактериофаг поливалентный или секстафаг (против стафилококка, стрептококка, протея, синегнойной палочки, клебсиеллы пневмонии, энтеропатогенной кишечной палочки).
Особенность бактериофагов – узкая специфичность, в следствие чего они могут применяться против определенных штаммов бактерий, поэтому необходимо иметь большую коллекцию бактериофагов, из которой можно выбрать подходящий препарат или фаговый коктейль для конкретного пациента. Коллекция бактериофагов составляет более 200 препаратов.
Производителем бактериофагов в России является научно-производственное объединение Микроген — мировой лидер изучения бактериофагов.
При каких заболеваниях применяются бактериофаги
Бактериофаги применяются при:
- трофических язвах,
- раневых инфекциях,
- инфекциях органов дыхания,
- мочеполовой системы,
- желудочно-кишечных тракта,
- болезнях лор-органов и др. заболеваниях.
Инфекции желудочно-кишечного тракта, вызванные сальмонеллой, золотистым стафилококком, протеем, и др. и сопровождающиеся диареей (поносами), успешно лечатся бактериофагами.
Применяться бактериофаги при острых кишечных инфекциях могут:
- в виде монотерапии при легких формах,
- в сочетании с антибиотиками при
- средне-тяжелых формах болезни,
- бактерионосительстве – выделении энтеропатогенных бактерий,
- комплексной терапии условно-патогенной флоры и нарушении микробиома (микрофлоры) кишечника.
Используются бактериофаги в дерматологии, в детской практике, хирургии. С профилактической целью — в детских садах и школах для предотвращения эпидемий, например, дизентерии. Бактериофаги уже более 100 лет на службе человека. Может быть, как раз сейчас начинается эпоха бактериофагов. В новосибирском научном центре разрабатываются технологии персонализированного лечения. Медицинские центры Франции, Бельгии, Швейцарии проводят клинические исследования коктейлей бактериофагов.
![]()
Важным условием успешного лечения бактериофагами является знание микрофлоры тех органов, где предполагается бактериальная инфекция. Ниже приведены необходимые исследования микрофлоры для различных очагов заражения:
Участок заражения Обследование желудочно-кишечный тракт анализ на микробиом толстой кишки (на дисбактериоз) носоглотка мазок на микрофлору урологические заболевания посев мочи,
посев секрета простатыгинекологические заболевания мазки раневые поверхности и язвы,
в том числе при диабетической стопепосев В настоящее время при выявлении бактериального возбудителя болезни есть возможность определить его чувствительность к бактериофагу. Перед началом лечения необходимо пройти это обследование.
Как принимаются бактериофаги
Бактериофаги хранятся в холодильнике при температуре 2-8 градусов.
Бактериофаги — это крупные частицы. Они трудно проникают в ткани органов, поэтому лучше вводить их при лечении прямо к месту локализации инфекции. Это могут быть ингаляции при легочной патологии, промывания при лор-заболеваниях, аппликации при трофических язвах, ожогах, ранах. При инфекциях мочевыводящих путей для достижения успеха препараты бактериофагов вводятся в полость мочевого пузыря (хронический цистит).
Для внутреннего употребления есть бактериофаги во флаконах по 20 мл, 4 флакона в упаковке. Перед употреблением флакон следует подержать в руке, согреть, перелить в чистую посуду и принять внутрь. Принимать 2 раза в день натощак и после ужина, курс лечения 6 дней.
![Забор бактериофага из 100-мл флакона]()
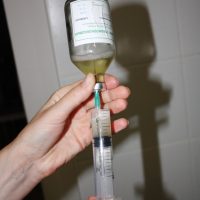
Есть упаковки по 50 мл и 100 мл. Поскольку следует максимально сохранять стерильность препарата (при помутнении запрещён его приём), необходимый для однократного приёма объём следует набирать в шприц.
В настоящее время проводят лечение бактериофагами диабетической стопы. Из больных тканей берут мазок для выявления конкретных патогенных бактерий. Затем из коллекции бактериофагов подбирают те, которые способны ликвидировать именно эти бактерии. Бактериофаг наносят на стерильную салфетку, прикладывают к ране. Лечение около недели.
Бактериофаги применяются в медицине местно или внутрь. Еще в 30-ые годы прошлого столетия бактериофаги доказали свою безопасность и высокую эффективность в клинических условиях. Но покупать бактериофаги и лечиться самостоятельно не стоит.
Заключение
Не всегда бактериофаги могут заменить антибиотики. Так, если имеет место острая ситуация, когда заподозрена бактериальная инфекция, но нет времени определить бактериальный фон болезни, чтобы подобрать препарат бактериофаг, то применяется лечение антибиотиками. При хронических инфекционных болезнях, когда установлена нечувствительность бактерий к антибиотикам и бактериальный фон заболевания, предпочтение следует отдать бактериофагам.
Хотя бактериофаги, возможно, не смогут полностью заменить антибиотики, но вместе они могут бороться со многими серьезными болезнями в клинической практике.
Стафилококки — бактерии, относящиеся к грамположительным неподвижным коккам. Они всегда присутствуют на теле человека и являются условно-патогенной микрофлорой, которая в нормальных условиях не вызывает нарушений в работе организма и активизируется при предрасполагающих факторах (обычно это снижение иммунитета). Также существуют патогенные типы стафилококка, которые, проникая в организм, вызывают заболевания.
![]()
Общая характеристика возбудителя
Staphylococcus aureus — неподвижные бактерии, не образующие спор. Это распространенные микроорганизмы, которые в большинстве случаев являются частью нормальной микрофлоры кожи и не вызывают никаких проблем. Обычно стафилококк распространяется в носу, паховой и подмышечной областях.
Если количество бактерий превышает допустимые нормы, то они начинают проникать в глубокие слои кожи через микротрещины, вызывая различные кожные инфекции и абсцессы.
Стафилококк имеет 27 штаммов, но наиболее распространенными являются:
- золотистый,
- эпидермальный,
- сапрофитный,
- гемолитический.
Опасность этих микроорганизмов заключается в том, что они вырабатывают токсичные вещества и ферменты, которые нарушают нормальное функционирование и жизнедеятельность клеток внутренних тканей и слоев кожи.
- Гемолитический стафилококк чаще всего поражает верхние дыхательные пути и вызывает гнойную ангину, тонзиллит, бронхит и другие воспалительные заболевания. Бактерии этого типа очень сложно поддаются лечению.
- Золотистый стафилококк устойчив ко всем антибиотикам пенициллинового ряда, а также к антисептикам. Он долго сохраняется во внешней среде даже под действием высокой температуры и прямых солнечных лучей. Бактерия поражает кожные покровы, вызывая экзему, фурункулы, поражения слизистых оболочек. Золотистый стафилококк может стать причиной токсического шока.
- Эпидермальный стафилококк обитает на поверхности кожных покровов и слизистых оболочек любого здорового человека, не нанося вреда его здоровью. Если же бактерия проникает в кровь человека с ослабленным иммунитетом, это вызывает заражение крови и последующее воспаление внутренней оболочки сердечной мышцы.
- Сапрофитный стафилококк — наименее опасная разновидность бактерии данного типа. При попадании в организм он вызывает общую интоксикацию организма, которая проявляется в повышении температуры тела, головной боли, мышечной слабости.
![]()
Источники заражения
Источниками инфицирования становятся не только те лица, которые страдают любой формой стафилококковой инфекции, но и здоровый (бессимптомный) носитель. Бессимптомное носительство обнаруживается у 20–30% здоровых людей. Среди них — работники медицинской сферы, у которых часто выявляют штаммы стафилококка, устойчивые к антибиотикам.
Есть риск заражения при употреблении некоторых продуктов (молочнокислые продукты, кондитерские изделия, особенно с кремом).
Стафилококки проникают в организм через слизистые оболочки и повреждения на коже (царапины, порезы, раны).
Если у человека снижен иммунитет (например, после длительной болезни или операции), то этот микроорганизм вызовет заболевания тканей, кожи и внутренних органов.![]()
Заболевания, которые провоцирует стафилококк
Эта бактерия вызывает нарушения в работе таких систем, как:
- дыхательная (плеврит, пневмония, ангина);
- центральная нервная (менингит);
- пищеварительная (энтерит, парапроктит, энтероколит);
- костно-мышечная (остеомиелит, артрит);
- мочеполовая (уретрит, орхит, цистит);
- сердечно-сосудистая (перикардит, эндокардит).
Также стафилококк вызывает патологии кожи и подкожной клетчатки (фурункулы, панариции, пиодермия, пузырчатка новорожденных), а также органов чувств (конъюнктивит, отит).
Симптомы
Каждое из заболеваний, которое вызывает стафилококк, имеет свои симптомы. К общим проявлениям, характерных для поражения этим микроорганизмом, относят:
- местное повышение температуры тела на участке, через который стафилококк проник в организм;
- отечность тканей из-за повышения проницаемости сосудов;
- нагноение ран и порезов;
- зуд и покраснение слизистой оболочки глаз;
- нарушение обоняния и носового дыхания;
- сильные головные боли;
- боль в суставах;
- выраженная одышка.
В большинстве случаев человек является носителем стафилококка, не подозревая об этом, так как в здоровом организме он никак не проявляет себя.
Диагностика и лечение
Методы диагностики подбираются в зависимости от специфики заболевания, вызванного стафилококком. Для выявления этой бактерии назначают такие исследования:
- бактериологический мазок для забора и дальнейшего исследования материала;
- посев крови и мочи;
- серологические анализы.
Лечение стафилококковой инфекции осуществляется с применением антибактериальных препаратов. Они подбираются и назначаются исключительно лечащим врачом, с учетом чувствительности конкретного типа стафилококка к таким средствам.
Детям раннего возраста при необходимости вводят гипериммунный антистафилококковый иммуноглобулин.
При затяжном течении сепсиса или кожных инфекций, спровоцированных стафилококком, вводится стафилококковый анатоксин.При тяжелых формах стафилококкового поражения пациенты госпитализируются, вне зависимости от возраста. Новорожденных детей, особенно недоношенных, направляют на стационарное лечение даже при слабой выраженности симптомов стафилококковой инфекции.
Если микроорганизм спровоцировал образование гнойных очагов, выполняется их вскрытие и дренирование; при отмирании тканей их иссекают.
![]()
Профилактика
Стафилококк с каждым годом становится все более устойчивым к различным видам антибактериальных препаратов. Это осложняет лечение. В таких условиях лучше предотвратить заражение микроорганизмом.
Читайте также: