 Пищевая сода (гидрокарбонат натрия) — кислая соль, состоящая из натрия и угольной кислоты. Выглядит как белый порошок, состоящий из мелких кристаллов. В качестве пищевой добавки встречается в кулинарии и пищевой промышленности. В виде растворов используется и в медицине.
Пищевая сода (гидрокарбонат натрия) — кислая соль, состоящая из натрия и угольной кислоты. Выглядит как белый порошок, состоящий из мелких кристаллов. В качестве пищевой добавки встречается в кулинарии и пищевой промышленности. В виде растворов используется и в медицине.
Содержание
Химическая формула пищевой соды
Гидрокарбонат натрия имеет формулу NaHCO3, где Na — натрий, H — водород, CO — углерод.
Значение атомной массы — 84,00 а.е.
Молярная масса вещества составляет 84,007 г/моль.
Плотность натрий двууглекислого составляет 2,16 г/см3.
Формула реакции пищевой соды и уксуса
NaHCO3 + CH3COOH → CH3COONa + CO2↑ + H2O
Формула реакции пищевой соды и лимонной кислоты
Н3С6Н5О7 + 3NaHCO3 → Na3C6H5O7 + 3CO2 + 3H2O
Об истории открытия
Впервые упоминания о соде появляются в воспоминаниях Диоскорида Педания — врача из Рима, который описал метод получения порошка с помощью упаривания вещества из озёрной воды.
Первая «искусственная» сода появилась только в XVIII веке. Для искусственного получения вещества в 1736 году химику Анри Дюамелю де Монсо понадобилось использовать метод кристаллизации. Впервые промышленным способом содовый порошок был получен в России. В основу промышленного получения легло открытие химика Эрика Лаксмана, установившего, что сода получается путем спекания древесного угля и природного сульфата натрия. Э. Лаксману удалось опробовать этот метод на заводе по производству стекла в Тальцинске. Но, метод не получил широкого распространения.
Впервые промышленным способом содовый порошок был получен в России. В основу промышленного получения легло открытие химика Эрика Лаксмана, установившего, что сода получается путем спекания древесного угля и природного сульфата натрия. Э. Лаксману удалось опробовать этот метод на заводе по производству стекла в Тальцинске. Но, метод не получил широкого распространения.
Более удачная попытка состоялась в 1791 году, когда французский химик Н. Лебман начал получать соду путем сплавления мела, смеси сульфата натрия и древесного угля. Было создано предприятие, дававшее 120 кг. содового порошка ежедневно.
Технология Лебмана с успехом применялась в Европе, а в 1864 году в России открылся первый завод такого типа. Это было барнаульское предприятие, созданное промышленником М. Прагом. Позже в России открылся крупный завод, дававший 20 000 тонн содового порошка ежегодно.
На новом предприятии производство велось по аммиачной технологии, которая была предложена и запатентована еще 1838—1840 годах. Аммиачный метод был более экономным и позволял получать соду более высокого качества, поэтому к 1916-1920 годам были закрыты все предприятия, работающие по технологии Лебмана.
Химический состав пищевой соды по ГОСТ
Сода, использующаяся в пищевой промышленности. Обозначается как добавка Е500. Согласно ГОСТ, 100 гр. пищевой соды состоит из:
- Золы — 36,9 гр.
- Воды — 0,2 гр.
- Натрия — 24,7 гр.
- Селена — 0,2 мкг.
Смотрите также: что такое гидроксид натрия.
Калорийность пищевой соды
Натрий двууглекислый не содержит пищевых волокон, белков, жиров и углеводов. Калорийность на 100 гр. — 0 калорий.
Растворимость соды в воде
Бикарбонат натрия хорошо растворяется в воде, образуя другие химические соединения. В горячей воде он растворяется лучше, с холодной взаимодействует слабо. Готовый водный раствор обладает слабой щелочной реакцией. Водный содовый раствор является электролитом с хорошей токопроводимостью.
Готовый водный раствор обладает слабой щелочной реакцией. Водный содовый раствор является электролитом с хорошей токопроводимостью.
Пищевая сода — это щелочь или кислота?
Кислотность или щелочность любого раствора химического вещества вычисляется по значению показателя водорода (ph). К растворам с кислотной средой относятся растворы, имеющие pH 6 и ниже. Растворы с pH 8 и более высокими показателями относятся к растворам со щелочной средой.
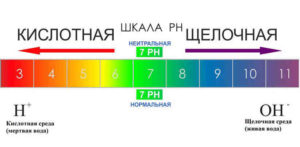 У водного раствора гидрокарбоната натрия рН равен 9, поэтому он относится к слабой щелочи, способной к нейтрализации действия сильных кислот.
У водного раствора гидрокарбоната натрия рН равен 9, поэтому он относится к слабой щелочи, способной к нейтрализации действия сильных кислот.
Чем отличается кальцинированная сода от пищевой смотрите в этой статье.
Как добывают пищевую соду?
Естественным способом пищевая сода добывается на берегах высохших содовых водоемов. В природе содовые образования содержатся в целой группе минералов. Самым распространенным считается трона — минерал, из которого содовый порошок получают после тщательной очистки, дробления и нагрева. Природное сырьё для получения соды состоит из обширной группы минеральных образований, содержащих углекислый натрий. Все сырье делится на две группы:
Природное сырьё для получения соды состоит из обширной группы минеральных образований, содержащих углекислый натрий. Все сырье делится на две группы:
- Горные породы, содержащие необходимые минералы и подземные воды, обладающие высоким содержанием карбоната натрия.
- Содовые месторождения, содержащие залежи трона, натрона и галита. Рапные и высохшие озёра, на берегах которых образуются «содовые сугробы».
 В России использование минералов для выщелачивания гидрокарбоната натрия прекратилось в 1971 году. Ранее соду добывали в шахтах, выщелачивая вещество раствором, который затем откачивался на поверхность.
В России использование минералов для выщелачивания гидрокарбоната натрия прекратилось в 1971 году. Ранее соду добывали в шахтах, выщелачивая вещество раствором, который затем откачивался на поверхность.
На видео репортаж о том, как производят соду в современных условиях в Башкирской компании.
Сейчас содовый порошок получается с помощью аммиачно-хлоридного способа: через концентрат хлорида натрия, предварительно насыщенный аммиаком, пускают углекислый газ. Из полученного вещества химическим путем выделяют соду, а аммиак, остающийся от процесса выделения, возвращают обратно в производственный процесс.
Как хранить пищевую соду?
Большая часть «бытовых» упаковок с содой выпускается в картонных коробках, в которых содержится пакет с содовым порошком. Коробка должна находиться в сухом, прохладном месте и не подвергаться воздействию влаги и солнечных лучей.
Если упаковка открыта, хранить пищевую соду лучше в герметичной емкости — так вы убережете порошок от попадания влаги. Срок хранения открытой упаковки — 6 месяцев, в запечатанной упаковке с соблюдением условий хранения содовый порошок хранится 18 месяцев.
Смотрите далее: пищевая сода — применение в быту.



 (3 оценок, среднее: 3,67 из 5)
(3 оценок, среднее: 3,67 из 5)