100 вирусных частиц это
Обновлено: 24.04.2024
После того, как ВИЧ (вирус иммунодефицита человека) попал в организм, он начинает размножаться в клетках, которые имеют определенные рецепторы. Преимущественно это клетки иммунной системы – Т-лимфоциты, макрофаги, клетки Лангерганса, клетки микроглии. Больше всего от воздействия ВИЧ страдают именно Т-лимфоциты, так называемые СD4-клетки, или Т-хелперы. В результате размножения вируса внутри этих клеток они разрушаются, постепенно их число уменьшается. Таким образом, для того чтобы выяснить, как далеко зашла инфекция, и насколько активен вирус в организме человека, используются два основных показателя – количество CD4-клеток в периферической крови и вирусная нагрузка (количество вирусных частиц, которое исследуется также в периферической крови).
Анализ на вирусную нагрузку необходимо сдавать всем пациентам в следующих случаях:
- при выявлении ВИЧ-инфекции
- перед началом АРТ (антиретровирусной терапии), если оно по каким-либо причинам было отложено на месяц и более после выявления заболевания
- через 4 недели после начала или смены схемы АРТ (по любым причинам)
- с определенной периодичностью (1 раз в 3-6 месяцев) на фоне лечения
Кровь на вирусную нагрузку при ВИЧ-инфекции необходимо сдавать не ранее, чем через 3 часа после последнего приема пищи, при этом можно пить воду без газа.
Как правило, у пациентов, у которых впервые выявлена ВИЧ-инфекция, и которые еще не получали АРТ, выявляется высокая вирусная нагрузка – это несколько десятков, сотен тысяч, а иногда и миллионов копий вируса в 1 мл крови. Прием антиретровирусных препаратов подавляет размножение вируса, и постепенно показатели вирусной нагрузки падают. Число CD4-лимфоцитов при этом увеличивается (если изначально этот показатель был снижен). Однако анализ на вирусную нагрузку является более чувствительным маркером эффективности проводимой терапии, чем количество CD4-лимфоцитов. Снижение количества вируса в организме происходит постепенно. В течение первого месяца лечения ожидаемое снижение вирусной нагрузки составляет около 1lg, (то есть она должна упасть в 10 раз по сравнению с уровнем до лечения). К 12-16 неделе терапии обычно показатели вирусной нагрузки составляют менее 400 копий/мл или становятся неопределяемым . Затем, если терапия подобрана правильно, пациент не прерывает и не пропускает прием препаратов, вирусная нагрузка остается нулевой. Нулевая вирусная нагрузка не означает, что вируса совсем нет в организме.

Это значит, что его количество так мало, что оно не улавливается существующими тест-системами. Чувствительность имеющихся в распоряжении лабораторий тест-систем может быть различной – наиболее часто используются анализаторы, которые могут выявить более 20, 40 и 150 копий ВИЧ в 1 мл крови. Считается нормой, если пациент достигает нулевой вирусной нагрузки в течение 6 месяцев непрерывного лечения (нередко это происходит быстрее).
В дальнейшем на фоне АРТ показатели вирусной нагрузки в норме сохраняются на неопределяемом уровне, однако допускаются единичные подъемы не более 200 коп/мл. Если же в нескольких подряд анализах крови выявляется повышение количества вируса, у пациента, дисциплинированно принимающего препараты, в первую очередь необходимо исключить устойчивость вируса к одному или нескольким применяемым лекарствам. Для этого также существует специальный тест. При подтверждении резистентности ВИЧ показана смена схемы терапии с учетом того, к каким препаратам вирус по-прежнему чувствителен, а к каким – приобрел устойчивость, и их применение нецелесообразно.

Медицинский редактор: руководитель Университетской клиники, к.м.н., врач-инфекционист Коннов Данила Сергеевич
Вирусная нагрузка – важный показатель состояния организма ВИЧ-положительного пациента. Она рассчитывается путем подсчета количества копий РНК ВИЧ (вирусных частиц) в 1 миллилитре плазмы крови. Полученные показатели указывают на степень тяжести вирусной инфекции. Благодаря им можно оценить эффективность проводимой ВААРТ, и прогнозировать дальнейшее развитие заболевания. Для создания более полной картины болезни, анализ на вирусную нагрузку проводится вместе с тестом на уровень CD4-лимфоцитов – антигены иммунной системы, отображающие ее состояние.
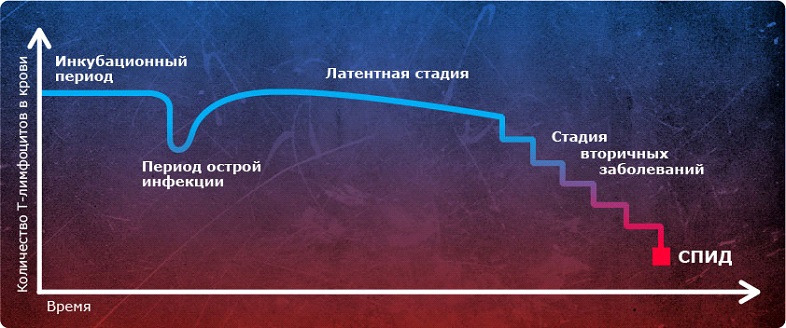
Без приёма терапии со временем снижается уровень СД4 клеток.
Как можно узнать уровень вирусной нагрузки на организм?
По сути, вирусная нагрузка отображает количество ВИЧ в крови. В то время как количество CD4 клеток демонстрирует состояние иммунной системы. Регулярный мониторинг этих двух показателей позволяет своевременно принимать решения – назначать ВААРТ и корректировать лечение, тем самым сдерживая прогрессирование ВИЧ-инфекции.
Анализ на вирусную нагрузку необходимо делать в следующих случаях.
- При подозрении на ВИЧ-инфекцию.
- При постановке диагноза ВИЧ.
- До начала антиретровирусной терапии – каждые 3-6-12 месяцев.
- Через 1 и 3 месяца после начала ВААРТ и далее каждые 3-4 месяца в ходе ее проведения.
Именно оценивая динамику вирусной нагрузки, лечащий инфекционист может сделать заключение об эффективности лечения и при необходимости корректировать ВААРТ.
Для определения вирусной нагрузки проводятся лабораторные исследования, с применением одного из нижеследующих методов.
- ПЦР (полимеразная цепная реакция) – обнаруживает вирус, начиная с 20 - 40 копий в 1 мл крови.
- Метод разветвленной ДНК – менее чувствительный и обнаруживает большое количество копий.
- NASBA (метод транскрипционной амплификации) – очень чувствительная методика, способная увеличивать белки вируса, для того чтобы определить его количество. Однако в России NASBA пока не получил широкое распространение.
Принципиальное различие методов и степень их чувствительности могут стать причиной недостоверного результата. Поэтому специалисты рекомендуют для определения вирусной нагрузки выбрать какой-нибудь один метод и использовать его на постоянной основе.
Расшифровка результатов исследований на ВИЧ
Полученные в ходе исследования вирусной нагрузки результаты расшифровываются следующим образом.
- До 10 000 копий вируса – низкая вирусная нагрузка.
- Свыше 100 000 копий – высокая вирусная нагрузка.
- 0 копий – вируса в организме нет, что считается нормой для здорового человека и указывает на необходимость повторного исследования для ВИЧ-инфицированных пациентов.
Неопределяемая вирусная нагрузка – минимальное количество копий, наличие которых невозможно зафиксировать с помощью выбранного метода исследования.
Таким образом, неопределяемая вирусная нагрузка – это показатель, к которому стремятся все ВИЧ-инфицированные пациенты. Такой результат указывает на то, что вирус в организме есть, но его количество ничтожно мало и на данный момент человеку ничего не угрожает. Одна при этом обязательно необходимо оценить общее состояние иммунной системы. Для этого нужно определить количество CD4+антигенов Т-лимфоцитов. Норма клеток и возможные отклонения приведены в нижеследующей таблице.
| Количество CD4 | Возможные действия пациента |
|---|---|
| 1500 – 500 кл/мл | норма |
| 500 - 350 кл/мл | необходимо начать ВААРТ |
| 200 кл/мл и ниже | проводят ВААРТ |
| Менее 100 кл/мл | проводят ВААРТ и симптоматическую терапию |
Оценивая показатели вирусной нагрузки и CD4 можно сделать достоверное заключение о состоянии здоровья пациента. Если зафиксирована низкая вирусная нагрузка, например, 4000 копий и показатели CD4 в норме, то ВААРТ эффективна. И наоборот – высокая вирусная нагрузка при снижении показателей CD4 свидетельствуют о низкой эффективности лечения.
Как уменьшить вирусную нагрузку?
Тест на вирусную нагрузку отражает степень тяжести ВИЧ-инфекции и состояние организма. Естественно, что столкнувшись с высокими показателями нагрузки, пациенты стремятся ее снизить. Нередко для этой цели они прибегают к альтернативным методам лечения. Но проблема в том, что единственный способ снизить вирусную нагрузку – это эффективная ВААРТ. Иммуностимуляторы, иммуномодуляторы, витаминные комплексы, отвары трав и прочие средства, не оказывают никакого влияния на развитие ВИЧ-инфекции. Снизить нагрузку можно только с помощью антиретровирусной терапии.
Преимущества неопределяемой низкой нагрузки
Низкая или неопределяемая вирусная нагрузка желательна по нескольким причинам.
- Минимальный риск прогрессирования инфекции.
- Минимальный риск развития резистентности к препаратам ВААРТ.
- Минимальный риск передачи инфекции во время незащищенного полового контакта.
- Максимальный шанс родить здорового ребенка (для женщин).
После того, как ВИЧ (вирус иммунодефицита человека) попал в организм, он начинает размножаться в клетках, которые имеют определенные рецепторы. Преимущественно это клетки иммунной системы – Т-лимфоциты, макрофаги, клетки Лангерганса, клетки микроглии. Больше всего от воздействия ВИЧ страдают именно Т-лимфоциты, так называемые СD4-клетки, или Т-хелперы. В результате размножения вируса внутри этих клеток они разрушаются, постепенно их число уменьшается. Таким образом, для того чтобы выяснить, как далеко зашла инфекция, и насколько активен вирус в организме человека, используются два основных показателя – количество CD4-клеток в периферической крови и вирусная нагрузка (количество вирусных частиц, которое исследуется также в периферической крови).
Анализ на вирусную нагрузку необходимо сдавать всем пациентам в следующих случаях:
- при выявлении ВИЧ-инфекции
- перед началом АРТ (антиретровирусной терапии), если оно по каким-либо причинам было отложено на месяц и более после выявления заболевания
- через 4 недели после начала или смены схемы АРТ (по любым причинам)
- с определенной периодичностью (1 раз в 3-6 месяцев) на фоне лечения
Кровь на вирусную нагрузку при ВИЧ-инфекции необходимо сдавать не ранее, чем через 3 часа после последнего приема пищи, при этом можно пить воду без газа.
Как правило, у пациентов, у которых впервые выявлена ВИЧ-инфекция, и которые еще не получали АРТ, выявляется высокая вирусная нагрузка – это несколько десятков, сотен тысяч, а иногда и миллионов копий вируса в 1 мл крови. Прием антиретровирусных препаратов подавляет размножение вируса, и постепенно показатели вирусной нагрузки падают. Число CD4-лимфоцитов при этом увеличивается (если изначально этот показатель был снижен). Однако анализ на вирусную нагрузку является более чувствительным маркером эффективности проводимой терапии, чем количество CD4-лимфоцитов. Снижение количества вируса в организме происходит постепенно. В течение первого месяца лечения ожидаемое снижение вирусной нагрузки составляет около 1lg, (то есть она должна упасть в 10 раз по сравнению с уровнем до лечения). К 12-16 неделе терапии обычно показатели вирусной нагрузки составляют менее 400 копий/мл или становятся неопределяемым . Затем, если терапия подобрана правильно, пациент не прерывает и не пропускает прием препаратов, вирусная нагрузка остается нулевой. Нулевая вирусная нагрузка не означает, что вируса совсем нет в организме.

Это значит, что его количество так мало, что оно не улавливается существующими тест-системами. Чувствительность имеющихся в распоряжении лабораторий тест-систем может быть различной – наиболее часто используются анализаторы, которые могут выявить более 20, 40 и 150 копий ВИЧ в 1 мл крови. Считается нормой, если пациент достигает нулевой вирусной нагрузки в течение 6 месяцев непрерывного лечения (нередко это происходит быстрее).
В дальнейшем на фоне АРТ показатели вирусной нагрузки в норме сохраняются на неопределяемом уровне, однако допускаются единичные подъемы не более 200 коп/мл. Если же в нескольких подряд анализах крови выявляется повышение количества вируса, у пациента, дисциплинированно принимающего препараты, в первую очередь необходимо исключить устойчивость вируса к одному или нескольким применяемым лекарствам. Для этого также существует специальный тест. При подтверждении резистентности ВИЧ показана смена схемы терапии с учетом того, к каким препаратам вирус по-прежнему чувствителен, а к каким – приобрел устойчивость, и их применение нецелесообразно.

Медицинский редактор: руководитель Университетской клиники, к.м.н., врач-инфекционист Коннов Данила Сергеевич

В настоящее время описаны 2 серотипа вируса: ВИЧ-1 и ВИЧ-2, различающиеся по структурным и антигенным характеристикам. Наибольшее эпидемиологическое значение имеет ВИЧ-1, который доминирует в современной пандемии и имеет наибольшее распространение на территории Российской Федерации. По данным электронной микроскопии, вирионы ВИЧ имеют округлую форму диаметром 100-120 нм. Наружная мембрана вируса построена из белков клетки хозяина и пронизана собственными белками вируса, которые обозначены как оболочечные белки.
Вирусная частица представляет собой ядро (cor), окруженное оболочкой. Ядро содержит двойную вирусную РНК, обратную транскриптазу (ревертазу), интегразу, протеазу. Различают два основных белка оболочки - трансмембранный гликопротеин с молекулярной массой 41 кД (gр41) и внешний гликопротеин - 120 кД (gр120) (табл. 1).
Таблица 1. Группы белков ВИЧ-1 и ВИЧ-2
| Группа белков | ВИЧ -1 | ВИЧ -2 |
| Белки оболочки вируса | gр160, 120, 41 кД | gp140, 105, 36 кД |
| Белки сердцевины | p55, 24, 17 кД | p56, 26, 18 кД |
| Ферменты вируса | p66, 51, 31 кД | p68 кД |
Примечание. Молекулярная масса белков выражена в килодальтонах - кД; gp - гликопротеины; р - протеины.
Нуклеоид вируса имеет округлую форму, но принимает продолговатую после отпочковывания вирусной частицы от клетки. Оболочка нуклеотида содержит протеин с молекулярной массой 24кд (р24). Между наружной оболочкой вириона и нуклеоидом существует каркас, состоящий из матриксного белка 17кд (р17).
В естественных условиях ВИЧ может сохраняться в высушенном биосубстрате в течение нескольких часов в жидкостях, содержащих большое количество вирусных частиц, таких как кровь и эякулят - в течение нескольких дней, а в замороженной сыворотке крови активность вируса сохраняется до нескольких лет.
Нагревание до температуры 56°С в течение 30 мин приводит к снижению инфекционного титра вируса в 100 раз, при 70°- 80°С вирус гибнет через 10 мин; через 1 мин инактивируется 70% этиловым спиртом, 0,5% раствором гипохлорита натрия, 1% глутаральдегидом, 6% перекисью водорода. ВИЧ относительно мало чувствителен к УФ-облучению, ионизирующей радиации.
| env | gp120 | Самый наружный белок обеспечивает связывание с клетками-мишенями. Лиганды - молекула CD4 + ; галактозилцерамиды; рецепторы для цитокинов |
| gp41 | Обеспечивает интернализацию вириона в клетку | |
| gag | р24 | Составляет оболочку ядра вируса (нуклеокапсида) |
| р17 | Составляет матриксное вещество вируса | |
| р9 | Связан с геномной РНК | |
| р7 | То же | |
| pol | р66 | Обратная транскриптаза (синтез ДНК на матрице РНК) |
| р31 | Интеграза (встраивает ДНК вируса в клеточный геном) | |
| р10 | Протеаза (расщепляет большие белковые трансляты на дифинитивные белки вируса) | |
| tat | p14 | Существенен для экспрессии белков оболочки (Env) |
| nef | p27 | Может усиливать и ингибировать репликацию ВИЧ |
| vif | p23 | Необходим для выхода новорожденных вирусов из клетки-мишени (вероятно, участвует в фолдинге белков Env) |
| vpu | p16 | Необязателен для жизненного цикла вируса; усиливает отпочковывание вируса из клетки-мишени |
Гликопротеин gр120 обусловливает присоединение ВИЧ к рецепторам СD4 клеток человека. При попадании ВИЧ в клетку под действием обратной транскриптазы синтезируется ДНК ВИЧ, встраиваемая в ДНК клетки-хозяина, которая в дальнейшем начинает продуцировать вирусные частицы.
Основа естественного иммунитета - это действие неспецифических механизмов, в большинстве своем реагирующих на повреждение тканей воспалительными реакциями. Некоторые клетки (макрофаги - МФ) и гуморальные факторы (комплемент, лизоцим) направлены на уничтожение бактерий. Другие клетки могут секретировать интерферон, действие которого в основном направлено против вирусов.
Адаптивный иммунитет основан на свойствах Т- и В-лимфоцитов избирательно отвечать на чужеродные вещества (антигены) с образованием специфической памяти и продукцией антител.
Попадая в организм человека, ВИЧ поражает различные органы и ткани, но, в первую очередь, клетки, несущие маркер СD4 + . В таблице 3 приведены основные типы клеток, поражаемых ВИЧ. В цитоплазме пораженных клеток освобождается вирусная РНК, и с помощью фермента обратной транскриптазы на основе вирусной РНК синтезируется ДНК - копия, которая встраивается в ДНК клетки хозяина (провирус). При каждом новом делении клетки все ее потомство содержит ретровирусную ДНК. В пораженной клетке начинают создаваться структурные элементы ВИЧ, из которых при помощи другого фермента - протеазы, собираются новые полноценные вирусы, в свою очередь поражающие новые клетки-мишени. С течением времени большинство зараженных клеток погибает.
Таблица 3. Типы клеток, поражаемых ВИЧ
| Тип клеток | Ткани и органы |
| Т-лимфоциты, макрофаги | Кровь |
| Клетки Лангерганса | Кожа |
| Фолликулярные дендритные клетки | Лимфоузлы |
| Альвеолярные макрофаги | Легкие |
| пителиальные клетки | Толстая кишка, почки |
| Клетки шейки матки | Шейка матки |
| Клетки олигодендроглии, астроциты | Мозг |
Уменьшение клеток, несущих рецептор СD4 + , приводит к ослаблению цитотоксической активности CD8+ Т-лимфоцитов, уничтожающих инфицированные вирусом клетки. В результате теряется контроль за проникающими в организм возбудителями бактериальных, вирусных, грибковых, протозойных и других инфекций (оппортунистических), а также за клетками злокачественных опухолей. Одновременно происходит нарушение функции В-лимфоцитов, поликлональная активация которых приводит, с одной стороны, к гипергаммаглобулинемии, а с другой - к ослаблению их способности продуцировать вируснейтрализующие антитела. Повышается количество циркулирующих иммунных комплексов, появляются антитела к лимфоцитам, что еще больше снижает число CD4 + Т-лимфоцитов. Возникают аутоиммунные процессы.
Оппортунистические инфекции, как правило, имеют эндогенное происхождение и возникают за счет активации собственной микрофлоры человека вследствие снижения напряженности иммунитета (например, эндогенная активация микобактерий туберкулеза из очагов Гона).
Цитопатическое действие ВИЧ приводит к поражению клеток крови, нервной, сердечно-сосудистой, костно-мышечной, эндокринной и других систем, что определяет развитие полиорганной недостаточности, характеризующейся разнообразием клинических проявлений и неуклонным прогрессированием ВИЧ-инфекции.

Вирус иммунодефицита человека (ВИЧ)
Процесс присоединения вирусной частицы к поверхности клетки-мишени и последующее слияние вирусной и клеточной мембран происходит при помощи гликопротеидного комплекса gp120/gp41. Оба белка, входящие в состав этого комплекса, кодируются вирусным геном env и синтезируются сначала в виде белка-предшественника gp160, который по остаткам аспарагина гликозилируется богатыми маннозой олигосахаридами, а затем процессируется с образованием двух субъединиц [1].
Гликопротеидные поверхностные комплексы gp120/gp41 формируют тримеры. На поверхности среднего вириона насчитывается около 20 таких тримеров [2, 3]. В зрелом комплексе субъединицы gp120 и gp41 связаны нековалентно. Белок gp41 является трансмембранным, а gp120 связывается на стадии инфекции с рецептором CD4, расположенном на мембране T-лимфоцитов [4].
В результате взаимодействия gp120 с рецептором CD4 конформация вирусного белка меняется, что дает ему возможность впоследствии связаться с одним из двух корецепторов на поверхности Т-лимфоцита : CCR5 или CXCR4. Это событие влечет за собой конформационные изменения уже в субъединице gp41, которые и провоцируют последующее слияние вирусной и клеточной мембраны [5].
Вместе с клеточной мембраной вирусная частица захватывает и некоторые поверхностные белки заражаемых клеток [6]. В данной модели представлены три белка, захваченные вирионом из клетки-хозяина : ICAM-1 , HLA-DR1 и DAF.
HLA-DR1 (Human Leukocyte Antigen) — это одна из молекул главного комплекса гистосовместимости класса II. Молекулы этого класса участвуют в презентации антигенов CD4+ Т-лимфоцитам и могут связываться с рецепторами CD4 на их поверхности. Наличие молекул HLA в мембране вириона ВИЧ повышает его вирулентность [9].
ICAM-1 (Intercellular Adhesion Molecule 1) , также известный как CD54) в организме человека участвует в межклеточных взаимодействиях и формировании иммунологических синапсов [7]. Молекула ICAM — это гомодимер, структурно сходный с иммуноглобулинами. Наличие ICAM в оболочке ВИЧ также увеличивает его вирулентность [8].
CD55 (также известный как DAF, Decay-accelerating factor) в человеческих клетках участвует в негативной регуляции клеточной системы комплемента, блокируя сборку мембраноатакующего комплекса. Считается, что этот белок в мембране ВИЧ может предохранять вирион от уничтожения иммунной системой [10].
Мембраны вирусных частиц ВИЧ формируются из мембран зараженных вирусом клеток. При этом вирусная и клеточная мембраны отличаются по соотношению входящих в их состав липидов. Благодаря этому вирусная мембрана оказывается менее пластичной и отличается от клеточной по ряду других свойств [11].
В сравнении с мембраной Т-лимфоцитов, в липидной оболочке ВИЧ содержится существенно больше сфингомиелинов (на), фосфатидилсерина и холестерина, тогда как уровень типичных для клеток млекопитающих фосфатидилхолина и фосфатидилэтаноламина в вирусной мембране ниже в 2–3 раза [12]. Состав вирусной мембраны имеет принципиальное значение для жизнедеятельности ВИЧ. Так, например, ингибирование биосинтеза сфинголипидов может снижать инфекционную способность вируса [13].
Вирусные частицы ВИЧ отпочковываются от сравнительно плотных участков клеточной мембраны со специфическим липидным составом — липидных рафтов. Считается, что эти участки выполняют функции доставочных или концентрационных платформ в таких процессах как передача клеточных сигналов, сортировка мембранных белков или формирование клеточной полярности [14].
Матрикс, образованный структурным белком MA (matrix protein, также обозначаемый как p17)расположен непосредственно под липидной оболочкой вириона, который, как и три других белка ВИЧ (CA, NC и p6), формирующих капсид, нуклеокапсид и участвующих в сборке и nbsp;созревании вириона, кодируется вирусным геном Gag [15].
В зрелом вирионе матрикс состоит из тримеров MA [16]. Каждая из субъединиц тримера связана с молекулой миристиновой кислоты, за счет которой они заякориваются в вирусной мембране [17].
Внутри зрелой вирусной частицы ВИЧ находится капсид, содержащий генетический материал вируса, а также белки, часть из которых имеет вирусное происхождение, а часть захватывается вирионом из хозяйской клетки [6].
Белок p6 , один из продуктов гена Gag, оказывается в зрелом вирионе между матриксом и капсидом. Это совсем небольшой белок, который необходим для эффективного почкования формирующихся вирусных частиц [21].Также этот белок способствует попаданию в вирион белков Vpr [22].
Белок Vpr тоже кодируется вирусным геномом и осуществляет ряд важных функций, среди которых индукция ареста клеточного цикла в фазе G2, индукция апоптоза и транспорт вирусного преинтеграционного комплекса в ядро инфицированной клетки [23]. При этом другие регуляторные и вспомогательные белки ВИЧ обычно не присутствуют в зрелом вирионе.
Из клеточных цитоплазматических белков, захваченных вирионом при почковании, в пространстве между матриксом и капсидом оказывается существенное количество актина.
Актин — это структурный белок . Наряду с другими элементами цитоскелета он важен для формирования вирусных частиц, однако после этого подобные белки не играют роли в жизнедеятельности ВИЧ [24].
Капсид ВИЧ имеет форму усеченного конуса. Он формируется из порядка 250 гексамеров и 12 пентамеров белка СА (capsid protein, также обозначаемый p24).
Белок СА является продуктом вирусного гена Gag [18]. Наряду с СА, Gag кодирует еще три структурных белка. Продукты этой рамки считывания синтезируются сначала в виде белка-предшественника p55. Начало сборки вирусной частицы происходит, когда p55 связывается с клеточной мембраной. После почкования нового вириона p55 разрезается вирусной протеазой на 4 структурных белка: MA, CA, NC и p6 [19].
Соотношение продуктов рамки считывания Gag таково, что не все белки СА участвуют в формировании капсида. Некоторые остаются в виде димеров в пространстве между капсидом и матриксом [20].
В непосредственной близости от капсида внутри вириона встречаются некоторые белки хозяйской клетки. В данную модель включен белок циклофилин, который связывается с гексамерами CA.
Циклофилин (CypA) — это пептидил-пролиновая изомераза, которая в клетках участвует в процессах фолдинга различных белков. В жизненном цикле ВИЧ циклофилин задействован на стадии распаковки попавшего в цитоплазму клетки капсида [25].
Внутри капсида вирусной частицы ВИЧ упакован геном вируса и такие вирусные ферменты как обратная транскриптаза и интеграза. Также в капсиде оказываются захваченные из клетки-хозяина лизиновая тРНК и лизил-тРНК синтетаза [6].
Геном вируса иммунодефицита состоит из двух идентичных, не связанных ковалентно одноцепочечных молекул РНК, каждая из которых имеет длину порядка 10000 нуклеотидов [26]. Упаковка РНК внутри капсида осуществляется с помощью структурного белка NC (nucleocapsid protein, также обозначаемый p7), который является продуктом гена Gag.
Белок p7 связывает РНК, покрывая участки одноцепочечной молекулы длиной 5 нуклеотидов [27].
Вирусная РНК кэпирована с 5’-конца и полиаденилирована с 3’-конца. Помимо этого РНК ВИЧ имеет сайт связывания лизиновой транспортной РНК, которая служит праймером для осуществления обратной транскрипции вирусного генома [28].
Интеграза, также как и обратная транскриптаза, является продуктом ретровирусного гена Pol. Она состоит из четырех одинаковых субъединиц и необходима для встраивания вирусной ДНК в геном клетки [32, 33].
Молекула лизиновой тРНК присутствует в зрелом капсиде ВИЧ. Она взаимодействует не только с сайтом отжига тРНК-праймера, но и с другими участками геномной РНК вируса [29]. Ее захват из цитоплазмы клетки-хозяина осуществляется совместно с молекулой лизил-тРНК синтетазы.
Молекула лизил-тРНК синтетазы при формировании вирусной частицы взаимодействует с вирусным белком p55 [30].
Обратная транскриптаза (ревертаза), которая находится в капсиде ВИЧ и после попадания в клетку синтезирует ДНК-копию вирусного генома, является гетеродимером, одна из субъединиц которого обладает РНКазной активностью [31].


















Первые разновидности вируса иммунодефицита человека появились в начале XX века в Африке (34). Ближайшими эволюционными предками ВИЧ были аналогичные вирусы обезьян, а первыми заразившимися людьми могли быть охотники, разделовавшие убитых животных. В настоящее время, согласно данным Всемирной организации здравоохранения, ВИЧ заражены почти 37 миллионов человек по всему миру, а в 2015 году от иммунодефицита, вызванного этим вирусом, погибло более миллиона человек (35).
Строение и биология ВИЧ
Вирус иммунодефицита человека (ВИЧ, HIV — Human Immunodeficiency Virus, англ.) относится к роду лентивирусов (Lentivirus) семейства ретровирусов (Retroviridae).ВИЧ заражает преимущественно клетки иммунной системы человека (CD4+ Т-лимфоциты, макрофаги и дендритные клетки).
Уменьшение количества CD4+ Т-лимфоцитов приводит к развитию синдрома приобретенного иммунодефицита (СПИД) (36).
Существует несколько разновидностей ВИЧ, наиболее распространенной из которых является HIV-1. Размеры вирусной частицы ВИЧ варьируют в пределах от 100 до 180 нм. Она окружена мембраной, в которой заякорены поверхностные белковые комплексы. Часть этих комплексов кодируется геномом самого вируса (как продукты гена Env — белки gp120/gp41), а часть (например белки ICAM-1, HLA-DR1, CD55 и ряд других), как и сама мембрана, захватывается из хозяйской клетки. Мембранные белки ВИЧ позволяют вирусной частице взаимодействовать с рецепторами на поверхности клеток-мишеней. После этого мембраны частицы и клетки сливаются, а содержимое вириона попадает внутрь цитоплазмы (4, 6).
Вирион содержит белковый капсид конической формы, в котором находится РНК-геном вируса и ферменты, обеспечивающие его размножение в клетке (15). Внутри частицы ВИЧ, как и на поверхности его мембраны, помимо белков, кодируемых геномом самого вируса, находятся белки, захваченные из клетки-хозяина.
После проникновения внутрь клетки обратная транскриптаза ВИЧ синтезирует ДНК-копию его генома, которая встраивается в клеточный геном, образуя провирус. Впоследствии клеточные ферменты синтезируют на матрице провируса новые молекулы вирусной РНК, а также регуляторные и структурные белки вируса. Образовавшиеся вирусные белки осуществляют сборку и почкование новых вирусных частиц (37).
Геном вируса иммунодефицита человека представлен двумя идентичными молекулами РНК, каждая из которых имеет длину чуть меньше 10000 нуклеотидов. Всего геном включает 9 генов. Они кодируют 15 различных белков (38).
За синтез основных белковых продуктов ВИЧ ответственны гены (открытые рамки считывания) Gag, Pol и Env. Рамка Gag кодирует структурные белки. Ее продукты связываются с вирусной мембраной, формируют капсид и упаковывают геномную РНК. Рамка Pol кодирует ферменты, необходимые для размножения вируса и интеграции его генетического материала в геном клетки. Рамка Env отвечает за синтез поверхностных рецепторов, которые позволяют ВИЧ связываться с клетками-мишенями и заражать их. Продукты остальных генов ВИЧ (такие как Tat, Rev, Vif, Vpr, Vpu и Nef) осуществляют некоторые изменения в метаболизме клетки-хозяина, регулируют процессы размножения и сборки вируса, а также подавляют активность клеточных противовирусных систем (38).
Модель вируса
Данная модель вируса иммунодефицита человека объединяет результаты более 100 научных публикаций ведущих специалистов в области вирусологии, рентгеноструктурного анализа и ЯМР-спектроскопии. В ней воссозданы установленные к настоящему времени точные пространственные структуры 17 белков вирусного и клеточного происхождения в различныхконформациях (с учетом межбелковых взаимодействий), а также структуры трансмембранных участков ряда белков и их гликозилированных форм.
Для моделирования мембраны вирусной частицы потребовалось более 160 тысяч молекул липидов 8 видов в соотношениях, характерных для реальной частицы ВИЧ.
Задача построения научно достоверных моделей вирусов, решаемая в рамках некоммерческого проекта Viral Park компании Visual Science, осложняется тем, что ни один из имеющихся на сегодняшний день научных подходов, будучи применён отдельно от других, не позволяет получить изображение целой вирусной частицы в атомном или даже молекулярном разрешении. Тем не менее, сотни работ разных авторов со всего мира проливают свет на многие вопросы структуры и морфологии компонентов вирионов, а также их взаимодействия. При тщательном анализе всех научных работ, с учетом мнений признанных экспертов из мировых научных центров и помощи специалистов Отдела молекулярного моделирования компании Visual Science, методами структурной биоинформатики заполняющих пробелы в имеющихся исследованиях по молекулярной биологии, вирусологии и кристаллографии, появляется возможность создать максимально точные и достоверные модели вирусов, которые и представлены в проекте Viral Park.
Читайте также:

