Анализ на вирус рака шейки матки
Обновлено: 25.04.2024
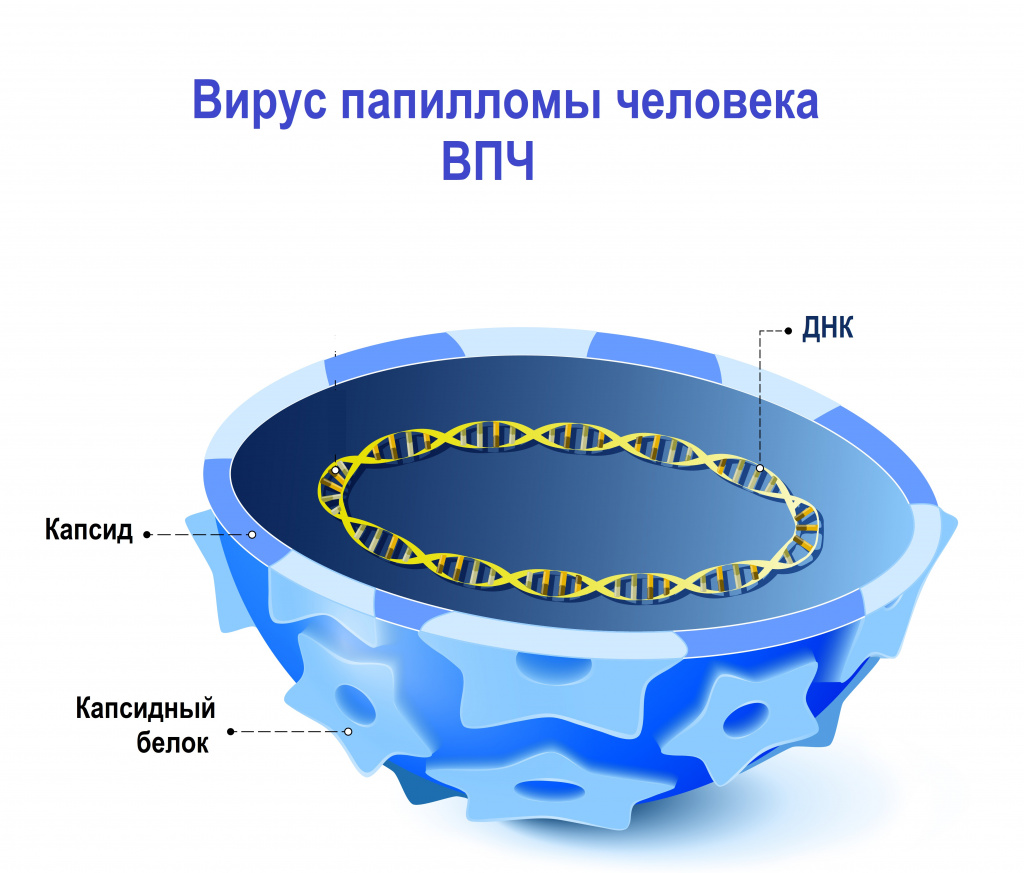
Вирус папилломы человека (ВПЧ) - ДНК-содержащий вирус семейства Papillomaviridae. В это семейство входят распространенные и генетически разнообразные вирусы, инфицирующие и поражающие клетки эпителия (кожа, слизистые аногенитальной области, ротовой полости).
Известно более 130 генотипов ВПЧ. По клинической классификации их делят на кожные и аногенитальные типы папилломавирусов. Именно аногенитальные типы ВПЧ вызывают поражения слизистых оболочек влагалища и шейки матки. Самые безобидные из этих заболеваний - доброкачественные остроконечные кондиломы половых органов, самое опасное - рак шейки матки.
Передаются вирусы папилломы человека при половых контактах. С началом половой жизни этим вирусом заражается подавляющее большинство женщин. Следует учитывать, что риск заражения ВПЧ зависит и от количества половых партнёров и от сексуального поведения единственного партнёра (распространенность ВПЧ у мужчин примерно равна распространенности среди женщин).
Сама по себе папилломавирусная инфекция - не заболевание. Через 6-18 месяцев у ~80% инфицированных женщин вирус уходит из организма самостоятельно, без какого-либо лечения, не вызывая болезней (спонтанная элиминация). И только у небольшого процента женщин с хронической (персистентной) инфекцией, обусловленной высокоонкогенными генотипами ВПЧ, через 10-20 лет может развиться рак шейки матки. Кажется, времени для успешной диагностики и лечения вполне достаточно, но расслабляться не стоит.
Папилломавирусная инфекция очень коварна, и связанные с нею предраковые изменения, как правило, не только не вызывают никакого беспокойства и дискомфорта, но часто и не обнаруживаются при обычном гинекологическом осмотре.
Поэтому для выявления папилломавирусной инфекции применяется ВПЧ-тест методом полимеразной цепной реакции (ПЦР). ВПЧ-тест - надежный помощник врача: обнаружение папилломавируса и определение его генотипа позволяет определить дальнейшую тактику ведения и лечения женщины.
При этом нужно учитывать, что выявление ВПЧ группы высокого канцерогенного риска у женщин не является основанием для постановки диагноза злокачественной опухоли, но служит поводом к дальнейшему обследованию, более интенсивному наблюдению и, при необходимости, лечению предраковых изменений слизистой шейки матки.
К группе низкого канцерогенного риска относятся 6, 11 генотипы ВПЧ: они могут быть причиной остроконечных кондилом и дисплазий легкой степени. Анализ на ВПЧ 6 и 11 генотипов применяется для дифференциальной диагностики с заболеваниями не папилломавирусной этиологии и при обследовании беременных для оценки риска развития папилломатоза гортани у новорожденных.
Сдать анализ на ВПЧ у женщин методом ПЦР (ВПЧ-тест) можно самостоятельно, без направления врача. Если ВПЧ-инфекция не выявлена (отрицательный результат ВПЧ-теста), то риск развития рака шейки матки низок. Но следует помнить - при продолжении активной половой жизни риск инфицирования ВПЧ сохраняется.
Все дополнительные анализы на вирус папилломы человека и другие исследования должны проводиться по назначению и под контролем врача.
Если поражение слизистой шейки матки выявлено на ранней стадии, предшествующей раку, то лечение более эффективно и практически не имеет побочных эффектов. Если не обнаружено никаких патологических изменений слизистой шейки матки, то и необходимости в лечении нет: вероятнее всего, организм справится с вирусом самостоятельно.
Однако через 1 год необходимо пройти повторное ВПЧ-тестирование и, если вирус все еще присутствует, снова обследоваться у врача-гинеколога.
Анализ на вирус папилломы человека (ВПЧ) методом ПЦР и цитологические исследования.
Основой современных скрининговых программ раннего выявления онкологической патологии шейки матки является цитологическое исследование по Папаниколау (ПАП-тест, окраска по Папаниколау). К сожалению, далеко не во всех российских медицинских учреждениях используется эта методика, очень часто применяются другие, менее совершенные способы приготовления (окраски) цитологического мазка.
Именно поэтому для традиционного цитологического скрининга характерно большое количество ложноотрицательных и неопределенных результатов, требующих повторных исследований.
Согласно последним международным и отечественным рекомендациям совместное применение анализа на ВПЧ (ВПЧ-теста методом ПЦР) и цитологического исследования (ПАП-теста) является предпочтительным методом для раннего выявления онкологической патологии шейки матки у женщин старше 29 лет. Такой скрининг необходимо проходить регулярно - один раз в 3 года.
Выявление ДНК ВПЧ 14 типов в урогенитальном соскобе используется для подтверждения инфицированности, для профилактического скрининга рака шейки матки (вместе с цитологическим исследованием).
Жидкостная цитология с применением технологии ThinPrep® – стандарт проведения цитологического исследования биоматериала шейки матки. Тест применяют при скрининговых и диспансерных обследованиях женщин с целью ранней диагностики и профилактики рака шейки матки. Исследование показано женщинам в возрасте 21-65 лет (при отсутствии установленной патологии) один раз в 3-5 лет.
Международный стандартизованный метод своевременного распознавания вероятной онкологической патологии шейки матки. Проводится одновременное выявление ДНК ВПЧ в соскобе эпителиальных клеток слизистой шейки матки и цервикального канала методом ПЦР и цитологическое исследование клеток с окрашиванием по Папаниколау и формулировкой результата в соответствии с классификацией Bethesda.
Рак шейки матки (РШМ) является вторым по распространенности типом рака среди женского населения, от которого ежегодно умирает более 250 000 женщин во всем мире. Процесс развития РШМ длительный. Период от интраэпителиального поражения клеток низкой степени (LSIL – low grade squamous intraepithelial lesion), интраэпителиального поражения клеток высокой степени (HSIL – high grade squamous intraepithelial lesion) до инвазивного рака шейки может составить 10-15 лет. Это означает, что у женщин достаточно времени для проведения соответствующих профилактических мероприятий, препятствующих развитию инвазивного РШМ.
Согласно рекомендациям Всемирной организации здравоохранения (ВОЗ), профилактикой РШМ являются скрининговые исследования – тестирование всех женщин старше 30 лет, у большинства из которых симптомы не проявляются. При скрининге проводят визуальный осмотр шейки матки с применением раствора уксусной кислоты или тестирование на ВПЧ.
Существует более ста генотипов вируса папилломы человека. Инфицирование этим вирусом – достаточно распространенное явление. Передается инфекция обычно половым путем, в редких случаях возможна вертикальная передача вируса от матери ребенку во время родов.
Клинические проявления папилломавирусной инфекции могут отсутствовать. Часто наблюдается естественная элиминация вируса, особенно в молодом возрасте. Но персистенция вируса в эпителии шейки матки в течение длительного времени может вызывать его патологические изменения, а также приводить к развитию рака шейки матки.
В настоящее время в ряде стран, в том числе и в России, при проведении скрининговых программ для выявления рака шейки матки, предраковых и фоновых состояний применяется только цитологическое исследование соскоба слизистой шейки матки с окрашиванием по Папаниколау. С целью цитологической диагностики интраэпителиальных неоплазий со слизистой цервикального канала и влагалищной части шейки применяется метод жидкостной цитологии – стандартизированная технология приготовления цитологического препарата (тест № 518 ).
По данным исследования POBASCAM (Нидерланды), клинически значимые состояния CIN2+ (дисплазия шейки матки средней степени тяжести) и выше могут быть выявлены раньше, если параллельно использовать цитологическое исследование и определение ВПЧ методом ПЦР в сравнении с использованием только цитологического исследования.
Для удобства взятия биоматериала и возможности сочетать выполнение двух исследований у пациентки за один визит к врачу применяется технология выполнения ВПЧ-тестирования методом ПЦР из пробы, взятой для выполнения жидкостной цитологии. Технология ко-тестирования обеспечивает стандартизованное взятие биоматериала с помощью щетки Cervex-Brush combi и положительно влияет на чувствительность метода жидкостной цитологии. Врач-цитолог дополнительно получает информацию о ВПЧ-статусе пациента.
Необходимым условием получения достоверного результата исследования ПЦР является соблюдение техники взятия соскоба эпителиальных клеток. В состав тестов по диагностике и мониторингу ВПЧ введен специальный параметр – контроль взятия материала (КВМ). КВМ представляет собой тест по определению количества геномной ДНК человека в биоматериале, источником которой являются эпителиальные клетки, попадающие в пробу при правильной технике взятия биоматериала.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер
Определение ДНК вируса папилломы человека: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показание к назначению исследования
Вирусы папилломы человека (ВПЧ) - это группа генетически разнообразных ДНК-содержащих вирусов, относящихся к семейству Papillomaviridae и поражающих эпителий кожных покровов и слизистых оболочек ротовой полости и аногенитальной зоны.
Инфицирование вирусом папилломы человека клинически может проявляться остроконечными кондиломами, папилломами или злокачественной трансформацией клеток. По данным, которые приводит Всемирная организация здравоохранения, 50-80% населения инфицировано ВПЧ, а 5-10% из них имеют клинические проявления заболевания.
Наследственный материал (геном) вируса папилломы человека заключен в белковую оболочку, состоящую из больших (L1) и малых (L2) структурных белков. В зависимости от строения генома L1 были выявлены и описаны различные типы вируса папилломы человека. К настоящему времени выявлено и описано более 200 генотипов вируса папилломы человека, около 45 из них могут инфицировать эпителиальный слой урогенитального тракта.
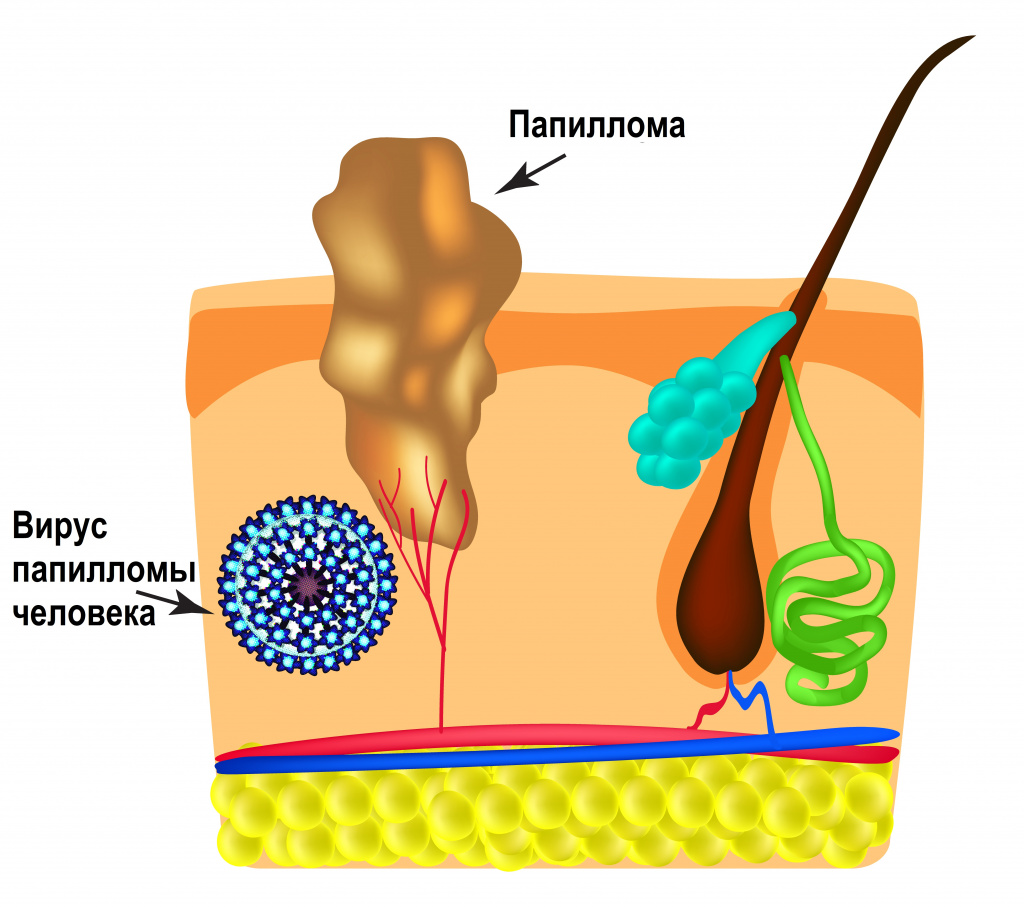
ВПЧ обладает тропностью (свойством поражать определенные органы и/или ткани) к коже и слизистым оболочкам. Источником возбудителя инфекции является больной человек или вирусоноситель.
Основной путь передачи возбудителя - половой (генитально-генитальный, мануально-генитальный, орально-генитальный), однако возможна передача и при соприкосновении (при кожном контакте). Кроме того, ВПЧ может передаваться от матери плоду во время родов.
Риск передачи при однократном половом контакте равен 80% - особенно у девушек, не достигших половой зрелости, из-за особенностей строения эпителия шейки матки в юном возрасте.
Факторы, способствующие инфицированию вирусом папилломы человека и развитию заболевания:
- раннее начало половой жизни;
- частая смена половых партнеров;
- сопутствующая урогенитальная инфекция и нарушение биоценоза влагалища;
- частые роды и аборты;
- иммунодефицитные состояния;
- генетическая предрасположенность и гормональные факторы.
Интервал между инфицированием ВПЧ и инвазивным (проникающим) раком составляет около 10 лет или более.
Инвазивному раку предшествуют предраковые поражения шейки матки, вульвы, влагалища, анального канала, полового члена различной степени тяжести.
Вирус папилломы человека не проникает в кровь, поэтому инфекционный процесс протекает без развития воспалительной реакции.
Выделяют вирусы высокого онкогенного (или канцерогенного) риска (типы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) и низкого онкогенного риска (типы 6, 11, 42, 43, 44).
Типы ВПЧ низкого канцерогенного риска связаны с развитием остроконечных кондилом, папиллом и дисплазиями легкой степени. Типы ВПЧ высокого канцерогенного риска, наряду с остроконечными кондиломами и дисплазиями, также могут вызывать злокачественную трансформацию эпителия, приводя к развитию рака.
Например, высокоонкогенные типы ВПЧ 16 и 18 вызывают в 70% случаев рак шейки матки, в 80% рак вульвы и влагалища, в 92% анальный рак, в 95% рак ротовой полости, в 89% рак ротоглотки, в 63% рак полового члена. Генотипы ВПЧ 6 и 11 обуславливают практически все виды аногенитальных бородавок и большинство случаев рецидивирующего респираторного папилломатоза.
Таким образом, дифференцированное определение ДНК вируса папилломы человека назначают в следующих случаях:
- для подтверждения ВПЧ при наличии папилломатозных разрастаний и изменений на слизистых оболочках половых органов;
- для скрининга (обследования лиц, не считающих себя больными) с целью выявления скрыто протекающего заболевания;
- для контроля эффективности проводимой терапии.
- с 21 года до 29 лет - не реже 1 раза в 3 года;
- с 30 до 69 лет - не реже 1 раза в 5 лет.
Высокая сексуальная активность предполагает проведение скрининга с18 лет.
Подготовка к процедуре
Обследование женщин целесообразно проводить в первую половину менструального цикла, но не ранее 5-го дня. Допустимо обследование во второй половине цикла, но не позднее, чем за 5 дней до предполагаемого начала менструации.
Накануне и в день обследования пациентке не рекомендуется спринцевать влагалище. Забор биоматериала не следует осуществлять ранее 24-48 часов после полового контакта, интравагинального УЗИ и кольпоскопии.
Соскоб из уретры проводят до или через 2-3 часа после мочеиспускания.
Мужчинам необходимо исключить половые контакты за 1–2 суток до взятия мазка (соскоба). Нельзя мочиться в течение 1,5-2 часов до процедуры.
Срок исполнения
До 2 рабочих дней, указанный срок не включает день взятия биоматериала.
Что может повлиять на результат
В случае несоблюдения правил подготовки полученный результат может быть некорректным.
Дифференцированное определение ДНК ВПЧ (вируса папилломы человека, Humanpapillomavirus, HPV) 21 типа (6, 11, 16, 18, 26, 31, 33, 35, 39, 44, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82) + КВМ
Синонимы: Анализ урогенитального соскоба на ВПЧ. HPV DNA, 21 Types, Scrape of Urogenital Epithelial Cells. Краткое описание исследования «Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) 21 типа (6, 11, 16, 18, 26, 31, 33, 35, 39.
Исследуемый материал: соскоб эпителиальных клеток урогенитального тракта.
Форма представления результатов: количественный результат по каждому выявляемому показателю.
Единицы измерения: логарифм копий ДНК ВПЧ на 105 эпителиальных клеток (lg копий ДНК/105 эпит. клеток).
До проведения тестов по выявлению ДНК ВПЧ выполняется контроль взятия материала (КВМ). Если в пробе значение КВМ неудовлетворительное (менее 4 lg (10000) копий ДНК человека в пробе), исследование ДНК ВПЧ не проводится и рекомендуется повторное взятие биологического материала.
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т. д.
Расшифровка показателей
Количественный формат теста позволяет выявить вирус, оценить степень риска и возможное наличие предраковых изменений при высокой вирусной нагрузке.
Интерпретация положительного результата
В анализируемом образце биологического материала обнаруженная ДНК, специфичная для вируса папилломы человека исследуемых типов в выявленной концентрации, свидетельствует о наличии возбудителя.
Если абсолютное содержание ВПЧ превышает клинически значимое, напротив обнаруженного штамма вируса указывается его концентрация. Чем выше значение, тем выше риск развития болезней, вызываемых вирусом папилломы человека.
Рост вирусной нагрузки через 3, 6 и 9 мес. после проведенного лечения свидетельствует о возможности рецидива.
- генотипы низкого онкогенного риска: 6, 11, 44;
- генотипы высокого онкогенного риска: 16, 18, 26, 31, 33, 35, 39, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82.
Выявление нескольких генотипов вируса предполагает менее благоприятный прогноз течения заболевания и более высокий риск персистенции.
При обнаружении 16 и 18 генотипов рекомендуется проводить кольпоскопическое обследование, не откладывая.
При выявлении других типов высокого риска назначают цитологическое обследование, а при его положительном результате - кольпоскопию.
Дополнительное обследование при отклонении от нормы
Врач интерпретирует результат анализа с учетом данных о пациенте и болезни, заключений осмотра, цитологического и гистологического исследований.
Гинеколог, уролог или проктолог может назначить дополнительные исследования:
-
цитологическое исследование биоматериала соскобов вульвы и влагалища, кроме шейки матки (окрашивание по Папаниколау, Рар-тест);
В цитологическом методе диагностики для окрашивания биологического материала используют несколько способов окраски. Применение определённого метода окрашивания позволяет решить специфические задачи. Каждый метод окрашивания имеет свои особенности, специфику, например, характер окрашивания ядра, ц.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Рак шейки матки: причины появления, симптомы, диагностика и способы лечения.
Определение
Рак шейки матки (РШМ) — это заболевание женской репродуктивной системы, характеризующееся развитием на шейке матки злокачественной опухоли, прорастающей из слизистой оболочки шейки матки (цервикального канала или эктоцервикса).
Шейка матки – это мышечно-соединительнотканный орган, покрытый эпителиальной тканью, который соединяет влагалище с телом матки, и представляющий собой полый цилиндр размером 2-6 см. Его нормальное функционирование влияет на сексуальную жизнь, способность к зачатию, протекание беременности и нормальные роды. Шейка матки состоит из плотной мышечной ткани, которая расслабляется к моменту овуляции, чтобы сперматозоиды свободно проникли к яйцеклетке, и плотно смыкается во время беременности, чтобы ребенок не родился раньше времени.
На сегодняшний день РШМ входит в пятерку самых распространенных онкологических заболеваний и занимает 5-е место среди поражений женской половой сферы.
В России ежегодно выявляется около 18 000 новых случаев, причем до 40% патологический процесс определяется на поздних (III–IV) стадиях заболевания. В последние годы в нашей стране отчетливо выражена тенденция роста заболеваемости РШМ у женщин моложе 35 лет.
Причины появления рака шейки матки
Развитие рака шейки матки не связано с наличием известных наследственных синдромов. Врачи считают основной причиной заболевания вирус папилломы человека (ВПЧ) онкогенных генотипов.
ВПЧ привносит свои гены в строение клеток ДНК, они перестают созревать и могут активно делиться. В результате на месте мутировавшей клетки появляется злокачественная опухоль. Со временем она увеличивается и метастазирует.
В качестве факторов риска развития данной патологии рассматриваются:
- раннее начало половой жизни;
- беспорядочная смена сексуальных партнеров;
- отказ от барьерных контрацептивов;
- длительное применение гормональной контрацепции;
- иммуносупрессивная терапия при аутоиммунных заболеваниях и лечении онкологических заболеваний других локализаций;
- инфекции, передающиеся половым путем: генитальный герпес, ВИЧ, хламидиоз;
- длительная зависимость от курения.
Классификация заболевания
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем МКБ-10: C53 – Злокачественное новообразование шейки матки.
Клиническая стадия РШМ устанавливается до начала специальной терапии, что необходимо для выбора метода и планирования лечения.
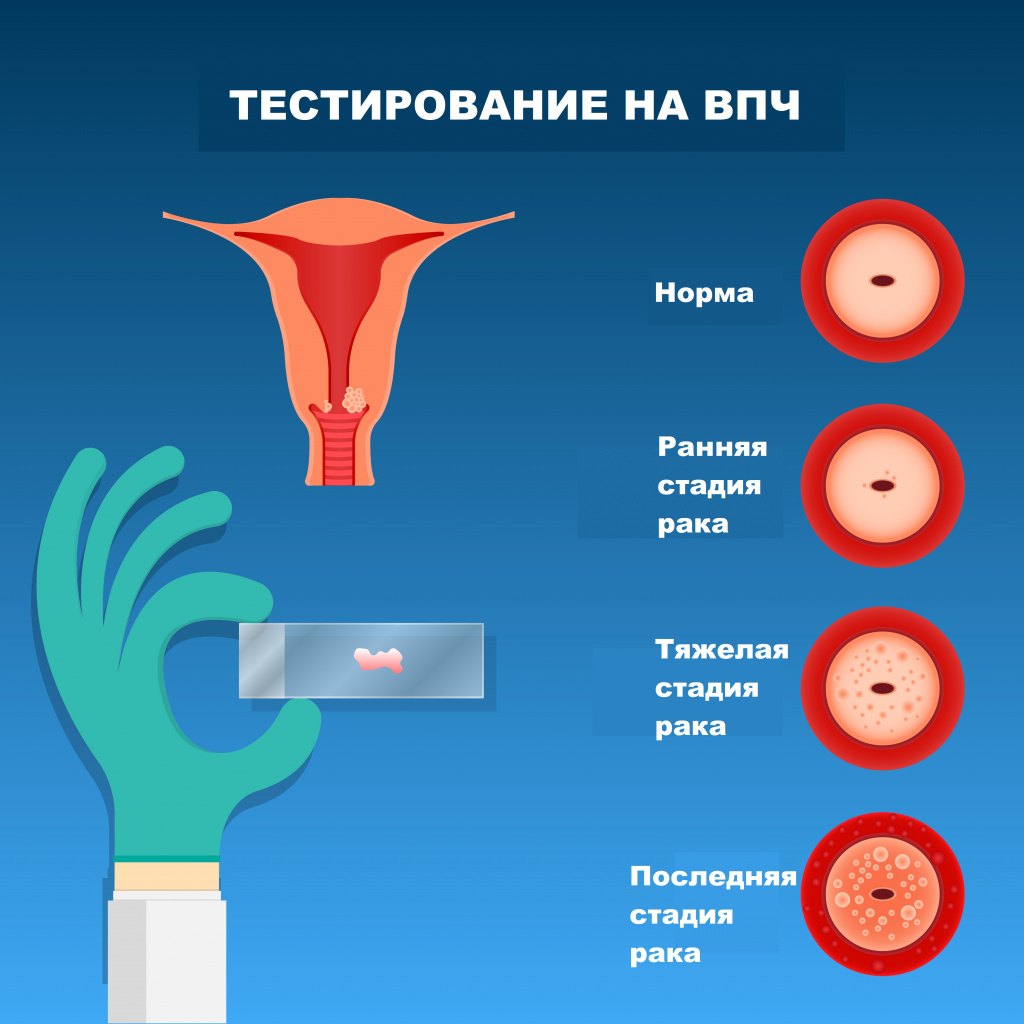
Стадия 0. Раковые клетки находятся только на поверхности канала шейки матки. На этом этапе они еще не образуют опухоль и не проникают вглубь тканей.
Стадия I. Опухоль локализована в шейке, может прорастать в матку и близлежащие лимфоузлы. Новообразование не выходит за пределы органа и не распространяется на другие внутренние органы.
Стадия II. Новообразование проникает в тело матки или выходит за ее пределы, распространяется на верхние отделы влагалища. В опухолевый процесс не вовлечены стенка таза и нижняя треть влагалища, не затронуты окружающие органы и лимфоузлы.
Стадия III. Опухоль поражает нижнюю треть влагалища и стенки таза, может блокировать мочеточники, достигать крупных размеров и поражать ближайшие лимфоузлы.
Стадия IV. Опухоль широко распространена вокруг шейки матки, поражены лимфоузлы, мочевой пузырь, прямая кишка, другие отдаленные органы.
У каждой стадии есть несколько подстадий – А1, А2, В1 и т. д. Их используют врачи при постановке точного диагноза.
Гистологически различают 2 основные группы РШМ: плоскоклеточный рак (70-80%), железистый, или аденокарцинома (10-20%). Приблизительно в 10% случаев выявляют низкодифференцированный рак. Другие гистологические типы злокачественных опухолей этой локализации составляют не более 1%. Наиболее злокачественный и крайне редкий тип РШМ – саркома.
Симптомы рака шейки матки
На начальных стадиях онкологический процесс протекает бессимптомно и обнаруживается только при расширенном гинекологическом осмотре. К признакам того, что опухоль проросла через верхний слой слизистой в подлежащие ткани, можно отнести:
- кровянистые выделения или влагалищные кровотечения – контактные (после полового акта) и спонтанные;
- водянистые обильные бели (лейкорея);
- продолжительные, обильные и болезненные менструации;
- вагинальные кровотечения в менопаузе;
- боль при половом акте;
- болезненные мочеиспускания;
- продолжительные спазмические боли внизу живота и области матки, отдающие в поясницу.
При распространенной злокачественной опухоли пациентки жалуются на дизурию (нарушение мочеиспускательного процесса) и трудности в процессе дефекации.
Мутные выделения, имеющие неприятный запах, характерны для присоединения бактериальной инфекции. Также наблюдаются метастатическое изменение подключичных и паховых лимфоузлов.
Диагностика рака шейки матки
При постановке диагноза врач принимает во внимание данные анамнеза, физикального обследования, которое включает ректовагинальное исследование, пальпацию органов брюшной полости и всех групп периферических лимфатических узлов, аускультацию и перкуссию легких, пальпацию молочных желез, а также результаты лабораторных и инструментальных исследований.
-
общий (клинический) анализ крови развернутый;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Состав профиля: №345УРО Лактобактерии, определение ДНК (Lactobаcillus spp., DNA) в соскобе эпителиальных клеток урогенитального тракта + КВМ (контроль взятия материала) №305УРО Гарднерелла, определение ДНК (Gardnerella vaginalis, DNA) в соскобе эпителиальных клеток урогенитального тракта №3023 ИН.
Влагалищная часть шейки матки — эктоцервикс выстлана многослойным плоским неороговевающим эпителием. У женщин репродуктивного возраста он постоянно перестраивается путем пролиферации-созревания-десквамации и полностью замещается новой популяцией клеток каждые 4 - 5 дней. В норме плоский эп.
Синонимы: Анализ урогенитального соскоба на ВПЧ. HPV DNA, 21 Types, Scrape of Urogenital Epithelial Cells. Краткое описание исследования «Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) 21 типа (6, 11, 16, 18, 26, 31, 33, 35, 39.
Синонимы: Анализ урогенитального соскоба на ВПЧ. HPV DNA, 16, 18 Types, Scrape of Urogenital Epithelial Cells. Краткое описание исследования «Дифференцированное определение ДНК ВПЧ высокого онкогенного риска 2-х типов (16, 18) в соскобе эпителиальных клеток урогенитального тракт.
Синонимы: Анализ урогенитального соскоба на ВПЧ. HPV DNA, 14 Types, Scrape of Urogenital Epithelial Cells. Краткое описание исследования «Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) высокого онкогенного риска 14 типов (16, 18, 31.
Комплексное исследование биоптатов шейки матки, включающее морфологическое описание и гистохимическую оценку экспрессии p16INK4a для уточнения биологического потенциала диспластических изменений в эпителии шейки матки. Рак шейки матки является превалирующим среди онкологически.
Комплексное исследование биоптатов шейки матки, включающее морфологическое описание и гистохимическую оценку экспрессии p16INK4a для уточнения биологического потенциала диспластических изменений в эпителии шейки матки. Рак шейки матки является превалирующим среди онкологи.
Синонимы: Анализ на антиген плоскоклеточной карциномы; Антиген плоскоклеточного рака; Опухоль ассоциированный маркер SCCА; Маркер опухоли из плоского эпителия; Маркер плоскоклеточного рака. Tumor-associatedantigen-4; ТА-4. Краткое описание исследования «Антиген плоскоклеточной карциномы&ra.
Кольпоскопия проводится с целью уточнения характера патологических изменений шейки матки, обнаруженных при осмотре её с помощью влагалищных зеркал. Кольпоскопия (греч. kolpos влагалище + skopeo наблюдать, исследовать) — метод исследования слизистой оболочки влагалищной части шейки ма.
Всем пациенткам с РШМ в целях определения распространенности опухолевого процесса рекомендуются:
-
ультразвуковое исследование органов малого таза, брюшной полости, пахово-бедренных, забрюшинных и надключичных лимфоузлов;
Ультразвуковое сканирование органов женской репродуктивной системы для оценки формы и размеров, а также исключения патологии.
Сканирование внутренних органов брюшной полости для оценки его функционального состояния и наличия патологии.
Ультразвуковое сканирование группы лимфатических узлов для оценки их размеров и структуры с целью выявления воспалительных или онкологических заболеваний.
Исследование, позволяющее получить данные о состоянии органов малого таза, выявить патологические изменения и опухоли.
Исследование, позволяющее получить данные о состоянии органов брюшной полости (печень, желчный пузырь, селезенка, почки, поджелудочная железа), сосуды брюшной полости и абдоминальные лимфатические узлы), органы малого таза.
Рентгенологическое исследование структуры легких с целью диагностики различных патологий.
Исследование, позволяющее получить данные о состоянии органов грудной клетки и средостения.
Безопасное и информативное сканирование структур головного мозга для диагностики его патологий.
Сканирование головного мозга, черепа и окружающих их тканей, позволяющее диагностировать различные патологии.
При обнаружении признаков заболевания следует обратиться к врачу-гинекологу . Для подбора методов лечения могут потребоваться консультации гинеколога-онколога (врача, который специализируется на лечении рака женских половых органов, в том числе операциях по его удалению), радиационного онколога (врача, который использует радиацию для лечения различных видов онкологии), медицинского онколога – специалиста по применению химиотерапии, других медицинских методов лечения.
Лечение рака шейки матки
Выбор метода лечения определяется индивидуально и зависит от распространенности процесса и тяжести сопутствующей соматической патологии. При лечении рака шейки матки используют хирургические методы, лучевую и химиотерапию, таргетную (целевую) терапию, а также их комбинации.
На нулевой стадии онкологии обычно применяют хирургический метод в качестве единственного и самостоятельного терапевтического подхода. Предраковые клетки удаляются под местной анестезией. На первой стадии без признаков сосудистой инвазии рекомендована конизация шейки матки – иссечение клиновидного лоскута с опухолью и окружающими здоровыми тканями.
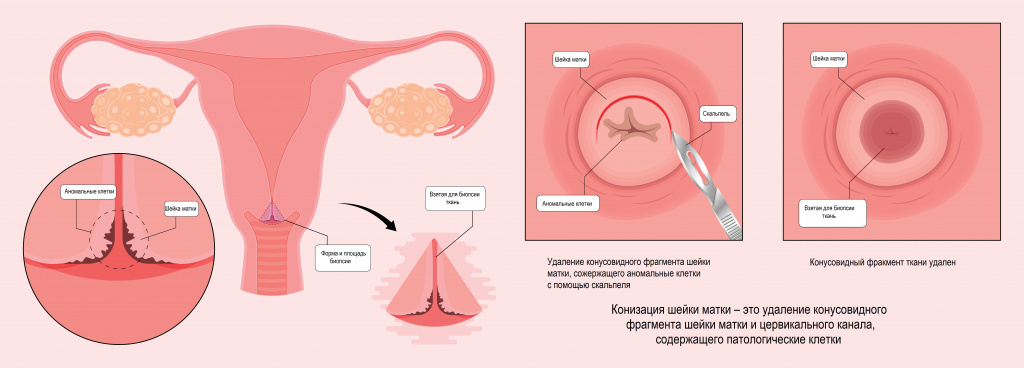
При сосудистой инвазии меньше 1 см, размере опухоли меньше 2 см и спокойных лимфоузлах показано удаление шейки матки с сохранением, по желанию пациентки, детородной функции (остаются матка с придатками). Операция может быть выполнена абдоминальным, влагалищным, смешанным доступом, включая лапароскопическую технику.
При инвазивном РШМ показана радикальная гистерэктомия с тазовой лимфодиссекцией – хирургическое иссечение матки с шейкой, придатками и регионарными лимфоузлами.
В зависимости от стадии рака используют лучевую дистанционную терапию или внутреннее облучение с влагалищным аппликатором.
- Для некоторых стадий лучевая терапия назначается как самостоятельный метод или как дополнение к хирургическому лечению. В большинстве случаев лучевую и химиотерапию проводятся совместно, поскольку химиопрепараты усиливают действие облучения.
- Для лечения рака шейки матки на поздних стадиях (с метастазами) или при рецидиве опухоли.
В настоящее время активно изучается вопрос сохранения иммунитета при лучевой и химиотерапии с целью обеспечения организму возможности задействовать собственные противоопухолевые механизмы. Считается, что относительно эффективным является введение интерферонов.
При распространении рака за пределы матки хирургическое лечение противопоказано. Стандартная терапевтическая схема для таких больных включает лучевую, химио- или паллиативную терапию. Разовые и суммарные дозы, периодичность сеансов определяют на основании клинической картины.
При оперативном лечении рака шейки матки описаны случаи инфицирования ракового очага. В литературе отмечается, что осложнения чаще всего встречаются при неоперабельных стадиях рака.
Болевой синдром появляется на поздних стадиях заболевания, когда опухоль прорастает в тазовые нервные сплетения, тазовую брюшину и сдавливает соседние органы. Как правило, боли характеризуются как постоянные, ноющие и зачастую плохо поддающиеся терапии.
Синдром сдавления органов малого таза заключается в нарушении работы мочевыводящей системы и прямой кишки. Опухоль может приводить к ухудшению проходимости мочеточников, что приводит к гидронефрозу и нарушению функций почек. Нарушение функции прямой кишки проявляется болью при дефекации, изменениями формы стула и запорами.
Кровянистые выделения из половых путей могут появиться и на ранних стадиях, но на поздних они становятся обильными, сложно купируются и часто становятся причиной смерти больных раком шейки матки.
На поздних стадиях возможно формирование свищей между влагалищем и мочевым пузырем или влагалищем и прямой кишкой, которые проявляются в виде выделения мочи или каловых масс из половых путей.
Непосредственной причиной смерти в запущенных случаях, как правило, становятся:
- тяжелая местная инфекция, переходящая в сепсис и перитонит;
- инфекция мочевых путей (пиелонефрит, уремия);
- тромбоз сосудов (легких, брыжейки);
- острая анемия в результате обильных кровотечений; метастатическая пневмония.
Развитие РШМ рассматривается как последовательный многоступенчатый процесс: от неизмененного эпителия шейки матки через предраковые заболевания (дисплазию) и преинвазивный рак до инвазивного рака. Длительность перерождения, как правило, занимает около 10 лет, поэтому раннее выявление и лечение предраковых поражений шейки матки является наиболее важным аспектом профилактики, позволяющим предотвратить развитие заболевания.
Основным методом скрининга и ранней диагностики считается доступный, простой и весьма информативный метод — исследование мазка с наружной части шейки матки и цервикального канала для выявления патологических клеток.
В Российской Федерации цитологическое исследование обязательно для всех женщин, самостоятельно обратившихся в смотровой кабинет.
С целью предотвращения заболевания ВПЧ, являющегося основной причиной развития рака шейки матки, проводится вакцинация.
Кроме того, в целях профилактики необходимо:
- минимум раз в полгода проходить осмотр у гинеколога;
- один раз в год выполнять кольпоскопию, чтобы оценить состояние шейки матки и исключить патологии;
- отказаться от курения (оно нарушает кровообращение в органах малого таза).
- Клинические рекомендации. Рак шейки матки. Ассоциация онкологов России, Российское общество клинической онкологии, Российское общество специалистов по профилактике и лечению опухолей репродуктивной системы. 2020. – 66 с.
- Минкина Г.Н. Цитологический скрининг рака шейки матки: от традиционного ПАП-теста к компьютерным технологиям // Акушерство, гинекология и репродукция. 2017; 11 (1): 56-63. DOI: 10.17749/2313-7347.2017.11.1.056-063.
- Клиническая онкогинекология : руководство / под ред. В. П. Козаченко. - 2-е изд., перераб. и доп. – Москва: БИНОМ, 2016. – 424 с.
- Рак шейки матки / под ред. И. В. Берлева, А. Ф. Урманчеевой. – Санкт-Петербург: ЭкоВектор, 2018. – 437 с.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Во всем мире рак шейки матки является четвертым по распространенности видом рака среди женщин; по оценкам, в 2020 г. произошло 604 000 новых случаев заболевания. Примерно 90% от произошедших в 2020 г. 342 000 случаев смерти от рака шейки матки имело место в странах с низким и средним уровнем дохода. Вероятность заболевания раком шейки матки у женщин с ВИЧ-инфекцией в шесть раз выше, чем у женщин, не инфицированных ВИЧ, и, согласно оценкам, c ВИЧ связано 5% всех случаев заболевания раком шейки матки (2). Кроме того, во всех регионах мира роль ВИЧ в развитии рака шейки матки выше среди женщин более молодого возраста.
В странах с высоким уровнем дохода имеются программы, в рамках которых осуществляются вакцинация против ВПЧ среди девочек и регулярный скрининг и назначение необходимого лечения среди женщин. Скрининг позволяет выявлять предраковые поражения на стадиях, когда их можно легко лечить.
В странах с низким и средним уровнем дохода такие профилактические меры менее доступны, и рак шейки матки часто выявляется лишь на поздних стадиях, когда развиваются симптомы. Ограниченно доступными могут быть также услуги по лечению раковых поражений (например, хирургическая операция, лучевая терапия и химиотерапия), что приводит к более высокой смертности от рака шейки матки в этих странах.
Высокую глобальную смертность от рака шейки матки (стандартизированный по возрасту показатель: 13,3/100 000 в 2020 г.) можно снизить путем принятия ряда эффективных мер в различных возрастных группах.
ВПЧ и рак шейки матки
Подавляющее большинство (более 95%) случаев рака шейки матки вызваны вирусом папилломы человека (ВПЧ).
ВПЧ является наиболее распространенной вирусной инфекцией половых путей. Им в какой-то момент жизни заражается большинство сексуально активных женщин и мужчин, иногда неоднократно. У более 90% зараженных инфекция впоследствии исчезает.
Рак шейки матки – наиболее распространенное из обусловленных ВПЧ заболеваний. Почти все случаи развития рака шейки матки объясняются заражением ВПЧ.
Хотя в большинстве случаев заражение ВПЧ проходит само собой, а предраковые поражения самопроизвольно излечиваются, все женщины подвержены риску перехода инфекции в хроническую форму и прогрессирования предраковых поражений в инвазивный рак шейки матки.
У женщин с нормальным иммунитетом рак шейки матки может развиваться в течение 15–20 лет. Однако при нарушениях иммунной системы, например у женщин с нелеченой ВИЧ-инфекцией, этот процесс может занять всего
5–10 лет.
Комплексный подход к борьбе с раком шейки матки
В Глобальной стратегии по ускорению элиминации рака шейки матки как проблемы общественного здравоохранения, принятой Всемирной ассамблеей здравоохранения в 2020 г., рекомендуется применять комплексный подход к профилактике рака шейки матки и борьбе с ним. Рекомендуемый комплекс мер включает мероприятия, охватывающие весь жизненный цикл.
Подход к борьбе с раком шейки матки, охватывающий весь жизненный цикл

- Вакцинация против ВПЧ
- Санитарное просвещение и предупреждения в отношении употребления табака
- Половое воспитание с учетом возраста и культуры
- Мужское обрезание
- Скрининг с помощью высокоэффективного теста, эквивалентного или превосходящего тест на ВПЧ
- Немедленное или как можно более быстрое назначение лечения предраковых поражений после получения положительного результата молекулярного теста на ВПЧ
- Хирургическая операция
- Лучевая терапия
- Химиотерапия
- Паллиативная помощь
Профилактика рака шейки матки должна вестись на основе междисциплинарного полхода и включать такие компоненты, как информирование населения, социальная мобилизация, вакцинация, скрининг, лечение и паллиативная помощь.
Вакцинация против ВПЧ
В настоящее время имеются четыре преквалифицированные ВОЗ вакцины, все из которых защищают от ВПЧ типов 16 и 18, которые, как известно, вызывают как минимум 70% раковых заболеваний шейки матки. Девятивалентная вакцина защищает еще от пяти канцерогенных типов ВПЧ, вызывающих еще 20% раковых заболеваний шейки матки. Две из этих вакцин защищают также от ВПЧ типов 6 и 11, приводящих к развитию аногенитальных кондилом.
Результаты клинических испытаний и пост-маркетингового наблюдения свидетельствуют о том, что вакцины против ВПЧ позволяют безопасно и эффективно предупреждать ВПЧ-инфекции, серьезные предраковые поражения и инвазивный рак (3).
Вакцины против ВПЧ наиболее эффективны, если вводятся до заражения ВПЧ. Поэтому в целях профилактики рака шейки матки ВОЗ рекомендует проводить вакцинацию девочек в возрасте от 9 до 14 лет, когда большинство из них еще не начали половую жизнь. В некоторых странах начата вакцинация мальчиков, поскольку она предупреждает развитие связанных с ВПЧ видов рака у мужчин.
Вакцинация против ВПЧ не заменяет скрининг на рак шейки матки. В странах, где предусмотрена вакцинация против ВПЧ, для сокращения заболеваемости и смертности в связи с раком шейки матки необходимо проводить программы общепопуляционного скрининга, позволяющие выявлять и лечить предраковые состояния и рак шейки матки.
Скрининг и лечение предраковых поражений шейки матки
Скрининг
Скрининг на рак шейки матки включает тестирование на ВПЧ-инфекцию для выявления предраковых состояний с последующим назначением соответствующего лечения. Тестирование проводится среди женщин, не имеющих симптомов и чувствующих себя совершенно здоровыми. Если скрининг выявляет ВПЧ-инфекцию или предраковые поражения, их можно легко лечить и тем самым предотвратить развитие рака. Скрининг может также выявить рак на ранней стадии, когда существует высокая вероятность излечения.
В настоящее время в обновленном руководстве ВОЗ странам рекомендуется использовать для цервикального скрининга тесты на ВПЧ, в частности:
- тесты на ДНК ВПЧ, позволяющие выявлять высокоопасные штаммы ВПЧ, вызывающие почти все виды рака шейки матки;
- тесты на мРНК ВПЧ, позволяющие выявлять ВПЧ-инфекции, приводящие к появлению атипичных клеток.
Тесты на ВПЧ, в отличие от визуального обследования, позволяют получить объективный результат. Они зарекомендовали себя простотой использования, возможностью выявления большего числа предраковых и раковых состояний и спасения большего числа жизней. Их применение также более экономически оправдано по сравнению с визуальными методами обследования или цитологией (мазок Папаниколау).
В общей популяции женщин скрининг должен проводиться с использованием валидированного теста на ВПЧ начиная с 30-летнего возраста с интервалом каждые 5–10 лет; среди женщин с ВИЧ-инфекцией его следует проводить начиная с 25-летнего возраста. Кроме того, скрининг среди ВИЧ‑инфицированных женщин должен проводиться чаще, каждые 3–5 лет.
Для проведения цитологии и теста на ВПЧ медицинским персоналом применяются аналогичные процедуры взятия цервикального образца. ВОЗ допускает возможность самостоятельного взятия образцов пациенткой при проведении теста на ДНК (но не мРНК) ВПЧ. Для уверенного выполнения данной процедуры женщинам должна оказываться надлежащая поддержка.
Скрининг должен быть увязан с лечением и ведением пациентов с положительными результатами скрининга. ВИЧ-положительным женщинам в условиях нехватки ресурсов лечение может назначаться без подтверждающей диагностики. При этом лечение ВИЧ-положительных женщин можно начинать только после получения положительного на ВПЧ результата теста (например, визуального обследования с использованием уксусной кислоты).
Лечение предраковых положений
В случае необходимости лечения предраковых поражений и соответствия пациентки критериям лечения рекомендуется проводить удаление пораженных тканей методом криотерапии или термоабляции. Оба метода лечения эффективны и безопасны и могут выполняться в амбулаторных условиях.
Лечение инвазивного рака шейки матки
Женщин с симптомами, позволяющими предполагать рак шейки матки, необходимо направлять в соответствующие медицинские учреждения для дальнейшего обследования, диагностики и лечения.
Симптомы ранней стадии рака шейки матки могут включать:
- нерегулярные кровянистые выделения или небольшие кровотечения в период между менструациями у женщин репродуктивного возраста;
- кровянистые выделения или кровотечения в постклимактерический период;
- кровотечения после полового акта; и
- обильные влагалищные выделения, иногда с неприятным запахом.
По мере развития рака шейки матки могут появляться более серьезные симптомы, включая:
- постоянные боли в области спины, ноги и/или таза;
- потеря веса, усталость, потеря аппетита;
- выделения с неприятным запахом и неприятные ощущения во влагалище; и
- отек ноги или обеих нижних конечностей.
На более поздних стадиях могут возникать другие тяжелые симптомы в зависимости от того, на какие органы распространился рак.
Диагноз рака шейки матки должен ставиться на основе результатов гистопатологического исследования. Определение стадии проводится на основе размера опухоли и распространения болезни в пределах таза и на удаленные органы. План лечения зависит от стадии болезни и включает хирургическую операцию, лучевую терапию и химиотерапию. Паллиативная помощь также является важным элементом ведения онкологических пациентов, позволяющим облегчать чрезмерную боль и страдания.
Деятельность ВОЗ
- 90% девочек к 15 годам должны быть в полной мере вакцинированы против ВПЧ;
- 70% женщин должны пройти скрининг на основе высокоэффективного теста в возрасте 35 лет и затем в возрасте 45 лет; и
- 90% женщин с выявленной болезнью шейки матки должны получать лечение (обеспечить лечение для 90% женщин с предраком; обеспечить ведение 90% женщин с инвазивным раком).
ВОЗ разработала руководство и инструментарий по профилактике рака шейки матки и борьбе с ним путем вакцинации, скрининга и лечения, а также терапии инвазивного рака. ВОЗ сотрудничает со странами и партнерами в разработке и осуществлении всеобъемлющих программ в соответствии с глобальной стратегией.
Библиография
(1) Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021:71:209–49. doi:10.3322/caac.21660.
(3) Lei et al. (2020) HPV Vaccination and the Risk of Invasive Cervical Cancer.
N Engl J Med 2020;383:1340-8. DOI: 10.1056/NEJMoa1917338
Читайте также:

