Антиген к коровому антигену гепатита с
Обновлено: 26.04.2024
всем мире. В настоящее время абсолютно очевидны серьезные проблемы, связанные с данной инфекцией: высокая частота формирования хронических форм, бессимптомное течение, манифестация заболевания на поздних стадиях (цирроз печени), четкая ассоциация с развитием гепатоцеллюлярной карциномы. Ассамблея ВОЗ в 2016 г. определила глобальную стратегию по борьбе с вирусными гепатитами, предполагающую элиминацию этих инфекций к 2030 г. Важнейшими целями этой программы, принятой 194 странами мира, являются сокращение числа новых случаев заражения вирусными гепатитами на 90% и числа случаев смерти от него на 65% по сравнению с уровнем 2016 г.
Актуальность проблемы объяснима еще и фактом выявления значительной частоты коинфекции ВГС и вирусом гепатита В (ВГВ). Маркеры вируса гепатита В (ВГВ) обнаруживаются у пациентов с ХГС в 22% случаев, что определяет важность вакцинации больных ХГС без коинфекции ВГВ против вирусного гепатита В. Установлена низкая частота перинатальной передачи ВГС от матерей с ХГС детям (3,5%), в то время как у женщин с сочетанием ХГС и ВИЧ-инфекции перинатальная передача ВГС составляет 14–16%.
Группы риска по заражению ВГС: медицинские работники; лица, использующие инъекционные наркотики; пациенты с ВИЧ; лица, которым были сделаны татуировки с помощью нестерильных инструментов; пациенты, получающие переливание крови или ее компонентов до 1992 г., пациенты отделений гемодиализа, дети, рождённые от матерей с ВГС.
Большинство пациентов с ОГС не демонстрируют каких-либо симптомов заболевания, у некоторых из них наступает спонтанная элиминация вируса, с которой ассоциируются следующие факторы: женский пол, молодой возраст, течение заболевания с клинической симптоматикой, клиренс РНК ВГС в течение 4 недель от начала клинической манифестации заболевания, генотип интерлейкина 28В (ИЛ 28В) СС. Однако ни один из этих параметров не может лечь в основу предсказания характера течения заболевания у каждого конкретного пациента.
Хронический гепатит С - хроническое заболевание печени, продолжающееся более 6 месяцев, в основе которого лежат инфицирование и поражение печени ВГС и манифестирующее морфологически некротическими, воспалительными и фибротическими изменениями печеночной ткани различной степени тяжести.
Диапазон исходов инфекции, вызванной ВГС, широк и колеблется от минимального до тяжелого поражения печени, включая развитие ЦП и ГЦК. Через 20– 30 лет после инфицирования ВГС вероятность развития ЦП колеблется от 4 до 45%. Прогрессирование фиброза печени имеет нелинейный характер и длится, как правило, в течение 20–40 лет от момента инфицирования. У части больных этот процесс происходит чрезвычайно медленно.
Выделен ряд факторов, которые могут оказывать отрицательное влияние на естественное течение гепатита С: возраст старше 40 лет к моменту инфицирования, мужской пол, раса (неевропейская), злоупотребление алкоголем, ожирение, нарушение обмена железа, метаболический синдром и др.
Верификация диагноза гепатита С основывается на обнаружении специфических маркеров гепатита С – определение суммарных антител к гепатиту С и маркерного спектра, состоящего из антител к структурным и неструктурным белкам вируса класса М и G.
Антитела класса М к core-антигену начинают выявляться в крови, начиная с 2 недели от начала заболевания, могут циркулировать как при остром, так и хроническом течении заболевания. Обнаружение антител класса М у новорожденного ребенка от матери, инфицированной гепатитом С, означает внутриутробное инфицирование плода. Антитела класса G начинают синтезироваться через 3-4 недели от начала заболевания, их циркуляция достаточно длительная.
При положительном результате на суммарные антитела в вирусу гепатита С (анти-HCV) обязательно необходимо проводить подтверждающее исследование, используя тест на выявление маркеров гепатита и определение РНК вируса с помощью полимеразной цепной реакции в реальном времени.
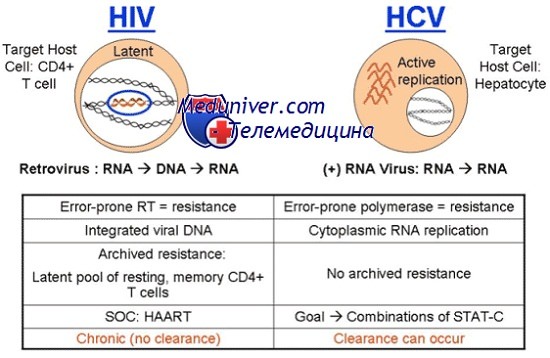
Белки и антигены вируса гепатита С. Диагностика ВГС
Сегодня известно минимум 10 структурных и неструктурных белков, кодируемых геномом HCV. К структурным белкам относят core, envelop 1 и envelop 2. Белок core является белком нуклеокапсида, тогда как envelop 1 и envelop 2 — гликопротеины внешней оболочки вируса. В структурной зоне кодируется также белок р7, функция которого не ясна, однако аналогия с другими представителями семейства Flaviviridae позволяет предположить, что его функция связана с высвобождением вириона из инфицированной клетки.
Этот белок отщепляется клеточной пептидазой от envelop 2, но не во всех случаях, что обусловливает существование envelop 2 в виде двух форм более и менее протяженной.
Неструктурная область генома HCV кодирует 6 белков — NS2, NS3, NS4A, NS4B, NS5A и NS5B. Белок NS2 является вирусной металлозависимой протеиназой. Белок NS4A действует как эффектор или кофактор для NSЗ-протеолитической активности в NS4A/NS4B, NS4B/NS5A, NS5A/NS5B сайтах нарезания полипротеина вируса.
В настоящее время фрагменты структурных и неструктурных белков, полученных генноинженерным путем (рекомбинантные белки) или с помощью химического синтеза, используют в качестве антигенов при конструировании иммуноферментных тест-систем. Первое поколение иммуноферментных тест-систем появилось на рынке в 1989 году и было основано на прямом ИФА. В качестве иммуносорбента были использованы фрагменты двух белков, NS3 и NS4, обозначаемых как 5-1-1 и С100-3.
Одновременно были разработаны и подтверждающие тесты на основе иммуноблота с рекомбинантными белками (RIBA). Чувствительность этих тест-систем первого поколения составляла только 64% для ИФА и 55% для иммуноблота. Тест-системы второго поколения появились на рынке в 1991 году. В качестве антигенов, сорбированных на твердой фазе, в этих тест-системах использовали капсидные белки (фрагмент с22-3) и антигены неструктурных регионов NS3 (фрагменты с200 и сЗЗс) и NS4, что позволило повысить чувствительность и специфичность исследований. Поскольку гуморальный иммунный ответ на капсидные антигены (структурные белки) нагинается быстрее, гем на неструктурные белки, период от инфицирования до выявляемой сероконверсии удалось уменьшить до двух месяцев.
Подтверждающие тест-системы на основе иммуноблота позволяли идентифицировать участвующие в реакции антигены. Результаты, полученные при помощи этих тест-систем, интерпретировали как положительные лишь при реакции антител, находящихся в исследуемом субстрате, по крайней мере, с двумя антигенами, тогда как при наличии реакции лишь с одним из антигенов результат считали неопределенным. Было установлено, что специфичность второго поколения тест-систем зависела от источника антигенов. В 1993 году на рынке появилось третье поколение тест-систем. В дополнение к вышеупомянутым антигенам в этих тест-системах используются также антигены, аминокислотная последовательность которых соответствует иммунодоминантным участкам NS5 белков.
В тест-системах первого, второго и третьего поколений в качестве антигенов использовались или рекомбинантные, или синтетические пептиды. В настоящее время можно выделить также тест-системы четвертого поколения, в которых в качестве иммуносорбента используют сочетания рекомбинантных и синтетических пептидов.
Опыт применения тест-систем различных поколений в мире очень большой. Было установлено, что если с помощью тест-систем первого или второго поколения у больных с острым вирусным гепатитом С антитела выявляли на 10-16, а в ряде случаев и 25-30 неделе от начала заболевания, то диагностикумы третьего поколения позволяли сократить этот срок до 2-3 недель. Согласно обобщенным данным чувствительность тест-систем первого, второго и третьего поколений составляет соответственно 70-80%, 92-95% и 97%.
В то же время, по данным С. Colin, 2001, чувствительность тест-систем третьего поколения составила 98,9% у пациентов с хроническими заболеваниями печени и 97,2% на специальных контрольных панелях сывороток. Достижение высокой чувствительности иммуноферментных тест-систем 3 и 4 поколения сопряжено с некоторыми проблемами в обеспечении специфичности исследований, что в ряде случаев может приводить к появлению ложноположительных результатов. В литературе имеются данные о возможных погрешностях в специфичности ELISA 3 тест-систем. Они являются общими для всех ELISA тест-систем, включая тест-системы для диагностики СПИДа.
Ложнопозитивные результаты могут быть следствием повышенного содержания в образцах гамма-глобулинов (сыворотки пациентов африканской расы, миеломная болезнь, ревматоидные факторы), заболеваний печени (цирроз, рак), аутоиммунных заболеваний (коллагенозы, аутоиммунные гепатиты), других вирусных инфекций (ВИЧ, гепатит В) и длительного хранения сывороток в меняющихся температурных условиях. Проведение какой-либо иммунизации также может сопровождаться повышением частоты ложнопозитивных реакций. Рекомендуемые в настоящее время меры по устранению этой проблемы следующие: а) повторная постановка образца в этой же ИФТС; б) повторная детекция anti-HCV в другой ИФТС; в) использование подтверждающих тестов на основе ИФА и иммуноблота.
Однако использование предлагаемых способов подтверждения результатов зачастую приводят к расхождениям в их итоговой трактовке, что показано исследованиями российских и зарубежных исследователей.
В настоящее время производители ИФТС для детекции anti-HCV достигают высокой чувствительности или за счет более полного выявления антител к NS3 или антител к антигенам core. Сравнительные исследования, выполненные на различных группах риска и специальных контрольных панелях показали, что тест-системы, лучше выявлявшие антитела к NS3, оказались несколько более чувствительными, чем тест-системы, лучше выявлявшие антитела к антигенам core. Их чувствительность составляла, соответственно 99,9% и 98,6%.
Основные Аг частиц Дейна — поверхностный HBsAg и сердцевинный HBcAg. AT против HBsAg и HBcAg появляются в течении заболевания.
Наличие AT против HBsAg прямо связано с невосприимчивостью к инфекции (постинфекционный или поствакцинальный иммунитет).
HBsAg. Первый идентифицированный Аг вируса гепатита В; впервые его выделил Б. Блюмберг (1965) из крови австралийского аборигена, поэтому этот Аг также называют австралийским.
HBsAg часто образует дефектные морфологические частицы 1-го типа, лишённые инфекционных свойств (побочные метаболиты репликативного цикла). В цитоплазме заражённых клеток возникает излишек HBsAg, связанного с клеточной мембраной и эндоплазматическим ретикулумом.
HBsAg появляется в крови через 1,5 мес после инфицирования; постоянно циркулирует в сыворотке инфицированных лиц, а его очищенные агрегаты входят в состав вакцины против вируса гепатита В.
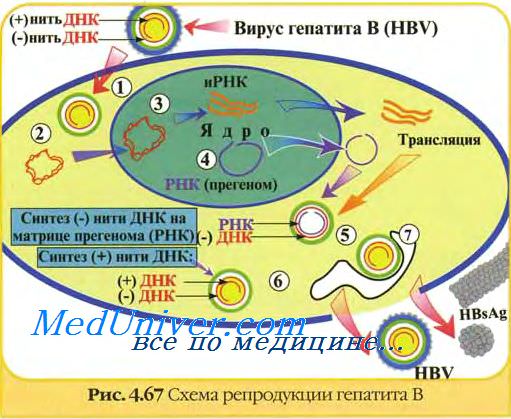
HBsAg включает два полипептидных фрагмента: preS( обладает выраженными иммуно-генными свойствами (рекомбинантный продукт можно использовать для приготовления вакцинных препаратов); preS2 — полиглобулиновый рецептор, приводящий к адсорбции вируса на гепатоцитах.
HBcAg. Сердцевинный HBcAg представлен единственным антигенным типом; его обнаруживают только в сердцевине частиц Дейна. Аг маркирует репликацию вируса в гепатоцитах. Может быть обнаружен только при морфологическом исследовании биоптатов или аутопсийного материала печени. В крови в свободном виде его не определяют.
Точечные мутации в участке, кодирующем синтез предшественника HBсAg, приводят к подавлению репликации HBсAg-продуцирующих мутантов вируса гепатита В, первоначально выделенных при молниеносных формах гепатита. Переход от HBeAg в HBcAg'-формы наблюдают у пациентов с хроническими, сравнительно умеренными поражениями.
HBeAg. He входит в состав частиц Дейна, но связан с ними, так как появляется в сыворотке в инкубационном периоде, сразу мосле появления HBsAg.
Образование HBеAg транслируется РНК, содержащей участки сердцевинного Аг и его предшественника. После завершения трансляции образующаяся молекула HBeAg выводится из клетки.
Функции HBeAg неизвестны; тем не менее HBeAg можно расценивать как наиболее чувствительный диагностический показатель активной инфекции.
Обнаружение HBeAg у пациентов с хроническим гепатитом указывает на активацию процесса, что представляет высокую эпидемическую опасность. Аг может отсутствовать при инфекции, вызванной мутантным штаммом вируса.
HBxAg — наименее изученный Аг. Предположительно опосредует злокачественную трансформацию клеток печени.
ДНК появляется в сыворотке одновременно с другими Аг вируса. Исчезает из кровотока в начале второй недели острого заболевания. Длительное персистирование — свидетельство хронической инфекции. В диагностике острого гепатита В определение ДНК используют редко.
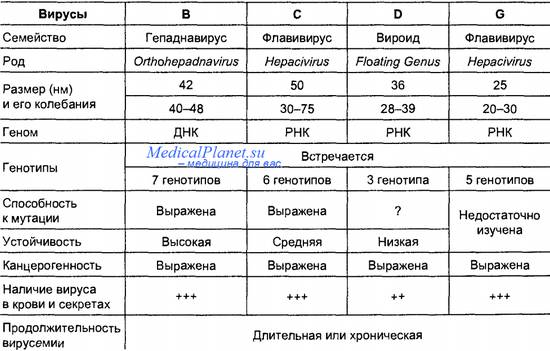
Диагностика гепатитов В и С у гематологических больных - анализы, особенности
Современная этиологическая диагностика вирусных гепатитов основана на обнаружении специфических маркеров соответствующих вирусов. Один из методов их выявления — тестирование различных антигенов вируса и антител к ним в ИФА. Наиболее прогрессивна и информативна так называемая генная диагностика: обнаружение вирусной РНК или ДНК с помощью ПЦР.
Для диагностики гепатита В в ИФА исследуют:
1) HBsAg-поверхностный антиген гепатита В, ранее называвшийся австралийским. Он указывает на факт инфицированности гепатитом В;
2) HbeAg — антиген инфекционности, свидетельствующий об активной вирусной репликации;
3) анти-НВс —антитела к ядерному антигену вируса гепатита В: класса IgM—ранние антитела острого периода, класса IgG—поздние антитела к ядерному антигену;
4) анти-НВе — антитела к HBeAg, чаще всего характеризующие прекращение активной репликации вируса (так называемая сероконверсия);
5) анти-HBs—антитела к HBsAg, обеспечивающие протективный иммунитет.
С помощью ПЦР для диагностики гепатита В тестируют ДНК вируса гепатита В — основного маркера репликации вируса.
Для диагностики гепатита С исследуют:
1) с помощью ИФА наличие анти-HCV-антител к вирусу гепатита С (для их выявления желательно использовать тест-системы второго — третьего поколения, отличающиеся большей специфичностью). Они указывают только на инфицированность вирусом гепатита С;
2) с помощью ПЦР наличие РНК вируса гепатита С — основного маркера репликации вируса.
Говоря о специфической диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями (ОГЗ), следует рассмотреть вопрос о применимости стандартных подходов к выявлению различных маркеров этих вирусов у данного контингента в связи с возможным нарушением процесса антителообразования на фоне глубокой иммуносу-прессии, развивающейся в ходе полихимиотерапии (ПХТ).
Исследования, в которых сделана попытка подтвердить или опровергнуть роль антительных маркеров у пациентов с онкологическими гематологическими заболеваниями, пока единичны.
Так, в отдельных работах сообщается, что при гепатите В иммуносупрессия нарушает обычную последовательность обнаружения в сыворотке крови антигенов и антител: у больных, которые до начала ПХТ были анти-НВs-позитивными, в процессе лечения могут вновь определяться HBsAg и HBeAg, свидетельствуя о несостоятельности анти-HBs в качестве протективных антител. Угнетение механизмов, ограничивающих вирусную репликацию, ведет к тому, что виремия нередко достигает высокого уровня.
Если антитела к столбняку, дифтерии и полиомиелиту сохраняются во время и после ПХТ, то титры антител к вирусам (ветряной оспы, кори и гепатита В) резко снижаются. Это в большей мере относится к детям с лейкозами, чем с солидными опухолями. Снижение или отсутствие выработки анти-HBs отметили также R. Repp и соавт. и R. Rokicka-Milewska и соавт.. Если при гепатите В эта особенность может отразиться только на ретроспективной диагностике, то для распознавания гепатита С, основанного чаще всего на обнаружении анти-HCV с помощью ИФА, такое положение может иметь принципиальное значение, препятствуя полному и своевременному выявлению всех инфицированных.
Антитела к вирусу гепатита С (анти-HCV) вообще образуются медленно, в течение 8—15 нед от момента инфицирования, но у иммунокомпетентных лиц персистируют в организме длительно и в большинстве случаев пригодны для выявления гепатита С, являясь в настоящее время рутинным и скрининговым маркером.
Некоторые авторы, проводившие немногочисленные и небольшие по объему исследования у иммунокомпрометированных пациентов, указывают на возможность отсроченного образования антител к вирусу гепатита С и считают недостаточным использование только ИФА для диагностики данного заболевания у этого контингента пациентов. В частности, С. Cornu и соавт. обнаружили, что у 5 из 6 обследованных ими иммунокомпрометированных пациентов анти-HCV начали обнаруживаться лишь спустя 14 мес и более от момента инфицирования, установленного с помощью ПЦР.
По данным М. Arico и соавт., антительная диагностика позволяет выявить около 70 % детей с ОЛЛ, инфицированных вирусом гепатита С. Значение ПЦР в выявлении пациентов, инфицированных вирусами гепатитов В и С, продемонстрировано при обследовании турецких детей: у 13,9 % больных с онкологическими гематологическими заболеваниями диагноз гепатита В установлен только при обнаружении ДНК вируса гепатита В, а 5,8 % анти-HCV-негативных детей оказались инфицированными вирусом гепатита С при тестировании РНК.
В то же время синтез анти-НВс IgM, сопутствующий в иммунокомпетентном организме вирусной репликации и являющийся одним из ее маркеров, у пациентов с онкологическими гематологическими заболеваниями почти отсутствует, а у пациентов без онкологических гематологических заболеваний происходит их активная наработка (7,7 % против 78,6 %).
С общебиологической точки зрения, выявленные феномены ждут объяснения, а в прикладном плане они демонстрируют особенности специфической диагностики инфицированности вирусом гепатита В у больных с онкологическими гематологическими заболеваниями и необходимость поиска других подходов к распознаванию болезни. Этой цели служит использование ПЦР, которая позволяет существенно повысить выявляемость пациентов с онкологическими гематологическими заболеваниями, инфицированных вирусом гепатита В: в 16 % случаев обнаружение ДНК этого вируса было единственным маркером инфицирования.
Более того, у 50 % детей, находившихся на полихимиотерапии и позитивных по каким-либо маркерам вируса гепатита В, вирусная ДНК выявлялась в отсутствие HBeAg, т. е. была единственным показателем репликации вируса, в то время как среди детей без онкологических гематологических заболеваний подобная ситуация встречалась лишь в 14,5 % случаев, т. е. в 3,5 раза реже.
При гепатите С также не обнаружено параллелизма между выявлением анти-HCV и РНК вируса гепатита С. Весьма демонстративным было преимущество тестирования РНК перед антительной диагностикой: у 44,4 % детей с онкологическими гематологическими заболеваниями РНК вируса гепатита С оказалась единственным маркером инфицирования.
Как и при гепатите В, диагностическая значимость генных и антительных маркеров зависит от фазы ПХТ. Период интенсивного и поддерживающего лечения онкологического гематологического заболевания при гепатите С — это время абсолютной репликативной активности и резкого снижения антителообразования, способность к которому частично восстанавливается по завершении полихимиотерапии. В наших наблюдениях у 74,9 % детей это сопровождалось продолжением вирусной репликации.
Практические выводы о специфической диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями сводятся к следующему:
1) рутинные подходы недостаточны для распознавания инфицированности пациентов с онкологическими гематологическими заболеваниями вирусами гепатитов В и С;
2) необходимо комплексное исследование всего известного спектра маркеров;
3) ведущую, определяющую роль в диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями играет тестирование ДНК вируса гепатита В и РНК вируса гепатита С в ПЦР;
4) только путем внедрения ПЦР-диагностики в учреждениях для больных с онкологическими гематологическими заболеваниями можно обеспечить полную и своевременную диагностику гепатитов В и С;
5) обязательность обследования всех пациентов с помощью современных маркеров:
— при поступлении;
— при повышении активности АЛТ на этапах ПХТ;
— каждые 3—6 мес в ходе и в течение года после ПХТ.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
всем мире. В настоящее время абсолютно очевидны серьезные проблемы, связанные с данной инфекцией: высокая частота формирования хронических форм, бессимптомное течение, манифестация заболевания на поздних стадиях (цирроз печени), четкая ассоциация с развитием гепатоцеллюлярной карциномы. Ассамблея ВОЗ в 2016 г определила глобальную стратегию по борьбе с вирусными гепатитами, предполагающую элиминацию этих инфекций к 2030 г. Важнейшими целями этой программы, принятой 194 странами мира, являются сокращение числа новых случаев заражения вирусными гепатитами на 90% и числа случаев смерти от него на 65% по сравнению с уровнем 2016 г.
Актуальность проблемы объяснима еще и фактом выявления значительной частоты коинфекции ВГС и вирусом гепатита В (ВГВ). Маркеры вируса гепатита В (ВГВ) обнаруживаются у пациентов с ХГС в 22% случаев, что определяет важность вакцинации больных ХГС без коинфекции ВГВ против вирусного гепатита В. Установлена низкая частота перинатальной передачи ВГС от матерей с ХГС детям (3,5%), в то время как у женщин с сочетанием ХГС и ВИЧ-инфекции перинатальная передача ВГС составяет 14–16%.
Группы риска по заражению ВГС: медицинские работники; лица, использующие инъекционные наркотики; пациенты с ВИЧ; лица, которым были сделаны татуировки с помощью нестерильных инструментов; пациенты, получающие переливание крови или ее компонентов до 1992 г., пациенты отделений гемодиализа, дети, рождённые от матерей с ВГС.
Большинство пациентов с ОГС не демонстрируют каких-либо симптомов заболевания, у некоторых из них наступает спонтанная элиминация вируса, с которой ассоциируются следующие факторы: женский пол, молодой возраст, течение заболевания с клинической симптоматикой, клиренс РНК ВГС в течение 4 недель от начала клинической манифестации заболевания, генотип интерлейкина 28В (ИЛ 28В) СС. Однако ни один из этих параметров не может лечь в основу предсказания характера течения заболевания у каждого конкретного пациента.
Хронический гепатит С - хроническое заболевание печени, продолжающееся более 6 месяцев, в основе которого лежат инфицирование и поражение печени ВГС и манифестирующее морфологически некротическими, воспалительными и фибротическими изменениями печеночной ткани различной степени тяжести.
Диапазон исходов инфекции, вызванной ВГС, широк и колеблется от минимального до тяжелого поражения печени, включая развитие ЦП и ГЦК. Через 20– 30 лет после инфицирования ВГС вероятность развития ЦП колеблется от 4 до 45%. Прогрессирование фиброза печени имеет нелинейный характер и длится, как правило, в течение 20–40 лет от момента инфицирования. У части больных этот процесс происходит чрезвычайно медленно.
Выделен ряд факторов, которые могут оказывать отрицательное влияние на естественное течение гепатита С: возраст старше 40 лет к моменту инфицирования, мужской пол, раса (неевропейская), злоупотребление алкоголем, ожирение, нарушение обмена железа, метаболический синдром и др.
Верификация диагноза гепатита С основывается на обнаружении специфических маркеров гепатита С – определение суммарных антител к гепатиту С и маркерного спектра, состоящего из антител к структурным и неструктурным белкам вируса класса М и G.
Структурные белки (core- белок - ядерный, белки оболочки -Е1 и Е2, необходимы для формирования вирусного капсида. Основным структурным белком вируса гепатита С является core-протеин, который обладает РНК-связывающей активностью и образует нуклеокаспид вируса. Именно с этим структурным белком связывают прямое цитопатическое действие вируса С на печеночную клетку. Одновременно с этим показано, что данный белок обладает онкогенным эффектом. В эксперименте было установлено, что core-протеин вируса гепатита С подавляет процесс апоптоза и тем самым способствует развитию опухолевого процесса. Однако до настоящего времени все еще не выяснено, коррелирует ли наличие core-протеина с уровнем РНК и различных генотипов вируса.
Антитела класса М к core-антигену начинают выявляться в крови, начиная с 2 недели от начала заболевания, могут циркулировать как при остром, так и хроническом течении заболевания. Обнаружение антител класса М у новорожденного ребенка от матери, инфицированной гепатитом С, означает внутриутробное инфицирование плода. Антитела класса G начинают синтезироваться через 3-4 недели от начала заболевания, их циркуляция достаточно длительная.
Неструктурные белки (p7, NS2, NS3, NS4A, NS4B, NS5A и NS5B) выполняют различные регуляторные функции. Неструктурный белок NS2 является цинк-зависимой протеиназой, а NS3 - серин-протеиназой, участвующей в сборке вириона. Функция NS4 недостаточно известна, хотя предполагается, что этот белок участвует в качестве Ко-фактора для NS3 серин-протеазы [3]. Достаточно хорошо выяснена функция белка NS5. Изучено, что данный белок является РНК- зависимой РНК-полимеразой - ферментом, который крайне необходим для синтеза вирусной РНК, т.е. репликации вируса С. Установлено, что NS5A подавляет активность интерферона. G. Reyes (2002) показал, что NS5A ингибирует процесс апоптоза и тем самым становится фактором канцерогенеза.
При положительном результате на суммарные антитела в вирусу гепатита С (анти-HCV) обязательно необходимо проводить подтверждающее исследование, используя тест на выявление маркеров гепатита и определение РНК вируса с помощью полимеразной цепной реакции в реальном времени.
- диагностика гепатита С;
- подтверждение положительных и сомнительных результатов скрининговых исследований.
Положительный результат: инфицированность вирусом гепатита С (необходимо дополнительно выявлять HCV РНК и подтверждать наличие антител определение подтверждающего теста с определением антител к структурным и неструктурным антигенам).
Если в подтверждающем тесте выявлены антитела только к одному из неструктурных антигенов вируса, результат считается неопределенным. Такие пациенты должны быть обследованы на наличие РНК вируса гепатита С, а через 2-3 недели от момента первого забора крови повторно исследовать кровь на наличие антител к гепатиту С.
Несмотря на высокую точность ИФА, на результаты диагностики могут повлиять: тяжелые иммунодефицитные состояния; беременность; рассеянный склероз; обострения респираторных заболеваний; вакцинация; аутоиммунные системные заболевания соединительной ткани; гематологические недоброкачественные опухоли; систематическое проведение гемодиализа.
Читайте также:

