Аттенуированных штаммов вируса что это
Обновлено: 23.04.2024
варианты патогенных микроорганизмов, полностью лишенные вирулентности или сохранившие остаточную вирулентность для одного из хозяев. Некоторые из стабильных А.ш. используют для изготовления живых вакцин, напр., туляремийной, сибиреязвенной, чумной, сыпнотифозной и др. А.ш. изолируют из природных популяций или получают в результате искусственного воздействия мутагенами.
Смотреть что такое "Аттенуированные штаммы" в других словарях:
Штаммы ОПВ (оральной полиовирусной вакцины) — аттенуированные штаммы полиовируса, аттестованные национальным контрольным учреждением для использования в оральных вакцинах. Источник: Постановление Главного государственного санитарного врача РФ от 22.05.2003 N 99 О введении в действие… … Официальная терминология
Вакци́ны — (лат. vaccinus коровий) препараты, получаемые из микроорганизмов или продуктов их жизнедеятельности; применяются для активной иммунизации людей и животных с профилактической и лечебной целями. Вакцины состоят из действующего начала специфического … Медицинская энциклопедия
Вакцины инактивированные — Инактивированные вакцины корпускулярные (цельновирионные) вакцины, представляют собой бактерии или вирусы, инактивированные химическими или физическими факторами или обоими факторами вместе. Для их приготовления могут быть использованы… … Официальная терминология
Иммунизация — I Иммунизация (лат. immunis свободный, избавленный от чего либо; синоним: иммунопрофилактика, прививки предохранительные, прививки профилактические) специфическая профилактика заразных болезней людей и животных. Иммунопрофилактика ряда… … Медицинская энциклопедия
ВАКЦИНАЦИЯ — мед. Вакцинация (активная иммунопрофилактика) комплекс мероприятий, направленных на формирование противоинфекци онного иммунитета с помощью введения в организм человека Аг возбудителей инфекционных болезней. Вакцинация признана ВОЗ идеальной… … Справочник по болезням
Прививка (медицина) — Вакцинация введение антигенного материала с целью вызвать иммунитет к болезни, который предотвратит заражение, или ослабит его последствия. Антигенным материалом могут служить: живые, но ослабленные штаммы микробов; убитые (инактивированные)… … Википедия
Вакцины. Виды антигенов вакцин. Классификация вакцин. Виды вакцин. Живые вакцины. Ослабленные ( аттенуированные ) вакцины. Дивергентные вакцины.
Вакцины — иммунобиологические препараты, предназначенные для активной иммунопрофилактики, то есть для создания активной специфической невосприимчивости организма к конкретному возбудителю. Вакцинация признана ВОЗ идеальным методом профилактики инфекционных заболеваний человека. Высокая эффективность, простота, возможность широкого охвата вакцинируемых лиц с целью массового предупреждения заболевания вывели активную иммунопрофилактику в большинстве стран мира в разряд государственных приоритетов. Комплекс мероприятий по вакцинации включает отбор лиц, подлежащих вакцинации, выбор вакцинного препарата и определение схемы его использования, а также (при необходимости) контроль эффективности, купирование возможных патологических реакций и осложнений. В качестве Аг в вакцинных препаратах выступают:
• цельные микробные тела (живые или убитые);
• отдельные Аг микроорганизмов (наиболее часто протективные Аг);
• токсины микроорганизмов;
• искусственно созданные Аг микроорганизмов;
• Аг, полученные методами генной инженерии.
Большинство вакцин разделяют на живые, инактивированные (убитые, неживые), молекулярные (анатоксины) генно инженерные и химические; по наличию полного или неполного набора Аг — на корпускулярные и компонентные, а по способности вырабатывать невосприимчивость к одному или нескольким возбудителям — на моно- и ассоциированные.
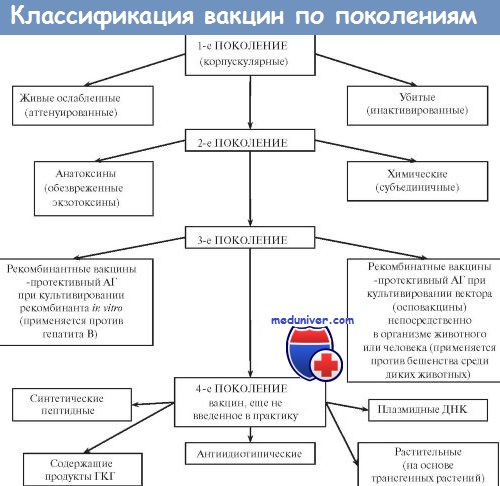
Живые вакцины
Живые вакцины — препараты из аттенуированных (ослабленных) либо генетически изменённых патогенных микроорганизмов, а также близкородственных микробов, способных индуцировать невосприимчивость к патогенному виду (в последнем случае речь идёт о так называемых дивергентных вакцинах). Поскольку все живые вакцины содержат микробные тела, то их относят к группе корпускулярных вакцинных препаратов.
Иммунизация живой вакциной приводит к развитию вакцинального процесса, протекающего у большинства привитых без видимых клинических проявлений. Основное достоинство живых вакцин— полностью сохранённый набор Аг возбудителя, что обеспечивает развитие длительной невосприимчивости даже после однократной иммунизации. Живые вакцины обладают и рядом недостатков. Наиболее характерный — риск развития манифестной инфекции в результате снижения аттенуации вакцинного штамма. Подобные явления более типичны для противовирусных вакцин (например, живая полиомиелитная вакцина в редких случаях может вызвать полиомиелит вплоть до развития поражения спинного мозга и паралича).
Ослабленные ( аттенуированные ) вакцины
Ослабленные (аттенуированные) вакцины изготавливают из микроорганизмов с пониженной патогенностью, но выраженной иммуногенностью. Введение вакцинного штамма в организм имитирует инфекционный процесс: микроорганизм размножается, вызывая развитие иммунных реакций. Наиболее известны вакцины для профилактики сибирской язвы, бруцеллёза, Ку-лихорадки, брюшного тифа. Однако большая часть живых вакцин — противовирусные. Наиболее известны вакцина против возбудителя жёлтой лихорадки, противополи-омиелитная вакцина Сэйбина, вакцины против гриппа, кори, краснухи, паротита и аденовирусных инфекций.
Дивергентные вакцины
В качестве вакцинных штаммов используют микроорганизмы, находящиеся в близком родстве с возбудителями инфекционных болезней. Аг таких микроорганизмов индуцируют иммунный ответ, перекрёстно направленный на Аг возбудителя. Наиболее известны и длительно применяются вакцина против натуральной оспы (из вируса коровьей оспы) и БЦЖ для профилактики туберкулёза (из микобактерий бычьего туберкулёза).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
ДИЧ-мутации вирусов. Аттенуация вируса серийными пассажами.
ДИЧ образуются при серийном пассировании в культурах клеток или эмбрионах птиц. При высокой множественности заражения их концентрация возрастает. Это обусловлено несколькими механизмами: 1) их укороченный геном размножается быстрее; 2) они менее часто уклоняются от функционирования в качестве матриц транскрипции мРНК и 3) они обладают повышенным афинитетом для вирусной репликазы, дающим им преимущество перед их полно-геномными аналогами. Этим также объясняется то, почему ДИЧ интерферируют с репликацией инфекционных вирионов с полноразмерным РНК геномом, прогрессивно повышая эффективность в серийных пассажах.
Морфологически ДИЧ подобны родительским вирионам и содержат все структурные белки в той же пропорции, что и стандартный вирус. Однако у вируса верикулярного стоматита ДИЧ короче (пулевидные частицы), образуются путем множественных делеций генома и содержат от 60 до 25% вирусного генома. Они интерферируют только с гомотипичными штаммами вируса. Образование дефектных частиц может зависеть от вакцинного штамма вируса.
Заражение культуры клеток вакцинным штаммом Эдмонстон-Шварц и Эдмонстон-Эндерс вируса кори при небольшой множественности заражения не индуцировали образования субгеномной РНК.
Генерация некоторых дефектных ДНК вирусных геномов может сопровождаться значительными модификациями ДНК. Например, ДИЧ парвовируса обычно содержат копии оригинальной геномной ДНК, хотя иногда с примесью ДНК клеточного происхождения.
ДИЧ могут снижать вирулентность стандартного вируса. Разведенный вирус может оказаться вирулентным, а концентрированный - не вирулентным. Роль ДИЧ при различных инфекциях все еще выясняется.
В последние годы секвенирование генома вирусов привело к пониманию механизма аттенуации и позволило повысить эффективность и безопасность живых вакцин. У большинства вирусов за вирулентность и тропизм ответственны несколько генов, которые действуют различными путями. Например, в отличие от системной инфекции, вызванной вирулентным полевым вирусом, некоторые вакцинные вирусы, обладающие тропизмом к респираторному тракту, размножаются только в верхних дыхательных путях; в других случаях, вакцинный вирус, введенный орально, размножается только в специфических эпителиальных клетках кишечника.
Аттенуированный штамм 17-D вируса желтой лихорадки обладает пониженным тропизмом к печени обезьян и это является признаком, с помощью которого мутант может быть признан аттенуированным для человека. Это подтверждалось при дальнейших исследованиях в клинических условиях.
Подобным образом штаммы полиовируса, аттенуированные естественным путем или пассированием в культуре клеток, утратили нейровирулентность.
Аттенуация вируса серийными пассажами в неестественном хозяине
Большинство живых вирусных вакцин, применяемых сегодня, получены эмпирически серийными пассажами в гетерологичном организме или культуре клеток естественного или гетерологичного хозяина. Адаптация вируса к более интенсивному размножению в необычных условиях сопровождается прогрессирующим снижением и потерей вирулентности для естественного хозяина.
Серийные пассажи в гетерологичном хозяине были классическим способом эмпирической аттенуации вируса. Например, вирусы чумы крупного рогатого скота и классической чумы свиней были аттенуированы и использованы в качестве соответствующих живых вакцин после длительного серийного пассирования в организме кролика. Значительно раньше таким способом получен аттенуированный вирус бешенства. Аттенуированные штаммы многих вирусов получены серийным пассированием в эмбрионах птиц.
В процессе многочисленных пассажей в неестественном хозяине или культуре клеток исходный вирулентный штамм вируса может накопить множество точечных мутаций в геноме, которые лежат в основе аттенуации. Однако, несмотря на многие весьма ценные практические результаты, аттенуация вирусов путем пассирования в системе неестественного хозяина — в целом процесс неуправляемый, а результаты его непредсказуемы.
Живые вакцины против чумы КРС (ЧКРС) являются одними из наиболее безопасных и эффективных вирусных вакцин. Вирус ЧКРС аттенуирован разными способами и практически с одинаковым результатом. Три типа аттенуированных вакцин использовали десятилетиями для ликвидации ЧКРС: лапинизированную, капринизированную и культуральную. Капринизированная вакцина была первой живой вакциной против ЧКРС и использовалась до недавнего времени в Индии. Лапинизированный штамм (Накамура-Ш) адаптировали к культуре клеток почки телят или куриным эмбрионам. Лапинизирован-но-авинизированную (LA) вакцину в основном применяли в Азии.
Аттенуация вирусов посредством длительного пассирования в клеточных культурах в настоящее время является основным методом получения живых вирусных вакцин. Этот метод основан на селекции пассажных мутантов, отличающихся биологическими свойствами от исходных вирулентных штаммов. Полученные таким образом аттенуированные иммуногенные штаммы аккумулируют в себе множество спонтанных мутаций, что гарантирует им генетическую и фенотипическую стабильность, хотя генетическая основа аттенуации используемых живых вирусных вакцин в большинстве случаев остается невыясненной.
Идентификация вирусных генов, определяющих вирулентность, представляет огромный интерес для получения авирулентных вакцинных штаммов, а также их использования в качестве носителей чужеродных генов. Поэтому изучению молекулярных основ аттенуации вирусов уделяется большое внимание. Наиболее часто с этой целью сопоставляют первичную структуру геномов вирулентных и аттенуированных штаммов и реже прибегают к изучению влияния инактивации или делетирования различных генов на вирулентные свойства вирусов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Аттенуация вирусов. Генетические мутации вирусов.
Все вирусные популяции характеризуются генетическим полиморфизмом, в основе которого лежат спонтанные мутации как результат ошибок при считывании вирусного генома в процессе репликации.
Спонтанные мутации ответственны за фенотипические изменения различных свойств вируса, в том числе вирулентности. В природе вирусы в процессе передачи от хозяина к хозяину совершают множество циклов репродукции. В этот период постоянно генерируются спонтанные мутации, которые могут вызывать изменения свойств вируса. В организме природного хозяина селекционируются преимущественно вирулентные вирусные частицы, которые способны передаваться серийно восприимчивым организмам.
Адаптация вирусов к неестественным условиям репродукции сопровождается прогрессирующей селекцией спонтанных мутантов адекватно новым условиям размножения.
Вирулентность вируса может быть снижена разными путями, в том числе пассированием в культурах клеток особенно неестественного хозяина. При этом преимущественно накапливаются мутанты, которые размножаются быстрее, чем полевой вирус. Затем такие мутанты селекционируют и определяют пригодность для использования в качестве живой вакцины. Аттенуированные мутанты часто являются пригодными в качестве живых вакцин потому, что они не долго размножаются в организме естественного хозяина и в то же время часто вызывают выраженный иммунный ответ.
У РНК-вирусов защитный механизм считывания генетической информации менее эффективен, чем у ДНК-вирусов. Они обладают значительно более высокой скоростью мутации, не менее чем в 100 раз, чем ДНК-вирусы ДНК-вирусы генетически более стабильны и труднее адаптируются. Частота ошибок у РНК-зависимых полимераз значительно выше, чем у ДНК-зависимых полимераз. На 10 000 оснований РНК-вирусов приходиться примерно одна мутация. РНК-полимераза коронавирусов может привести примерно к трем редким мутациям вируса на каждые 30 кb генома в процессе репродукции. Нелетальные мутанты РНК-вирусов накапливаются достаточно быстро. Гены, кодирующие разные белки, изменяются с разной скоростью.
Классическая аттенуация вирусов связана с селекцией спонтанных мутантов с пониженной вирулентностью. Идеально, аттенуация вирусных штаммов не должна сопровождаться потерей способности удовлетворительно размножаться в организме естественного хозяина, изменением антигенности и потерей протективных свойств.
Генетические мутации наиболее часто сопровождаются заменой единичных нуклеотидов (точечные, миссенс мутации). Реже мутации связаны с делецией или инсерцией единичных нуклеотидов или блоков нуклеотидов. Фенотипическая экспрессия мутаций может проявляться изменением различных свойств вируса.
Точечные мутации, сопровождающиеся специфическими аминокислотными заменами, в кодируемых вирусом белках могут снижать их функцию in vivo и тем самым вызывать аттенуацию вируса для хозяина. По уровню аттенуации и их потенциальной полезности для живых вирусных вакцин различают три класса точечных мутаций: чувствительные к температуре (ts мутанты); зависящие от протеолитического расщепления (Ра мутанты) и с измененным тканевым (клеточным) тропизмом.
Ts мутанты обычно являются условно летальными вирусами, которые эффективно размножаются при 32—34°С. Аттенуирующие ts мутации идентифицированы в большинстве, если не во всех генах вирусов; ts мутацию можно вызвать почти в любом гене. Ts мутанты особенно пригодны для иммунизации людей против респираторных вирусных болезней. Они хорошо размножаются в верхнем отделе респираторного тракта человека (32—34°С) и плохо — в нижнем (37°С).
Обнаружение ts мутантов (неспособных удовлетворительно размножаться при температуре несколько выше, чем нормальная температура тела) обычно отражает снижение вирулентности и указывает на возможность их использования в качестве живой вакцины. Однако, даже вакцины, содержащие более чем одну мутацию, доставляют беспокойство, связанное с возможностью восстановления вирулентности в процессе размножения в привитом организме.
Вакцинные штаммы полиовируса являются температурочувствительными со значительно сниженной способностью к размножению и нейровирулентностью для обезьян при введении в спиной мозг. Однако такие штаммы хорошо размножаются в кишечнике вакцинированных животных и могут вызывать виремию, и создают иммунитет. Хотя вакцинный вирус выделяется с фекалиями, контактная передача чувствительным организмом происходит очень редко.
Аттенуация путем адаптации вируса к размножению при пониженной температуре приводит к получению холодоадаптированных (Са) мутантов. К Са мутантам относятся безопасные вакцинные штаммы для интраназального применения, т.к. они хорошо размножаются при пониженной температуре носовой полости (около 33°С у большинства видов млекопитающих), но не при температуре низлежащих респираторных путей и легких. Холодоадаптированные вакцинные штаммы против гриппа, содержащие мутации почти в каждом гене, не давали реверсии. В 1997 году вакцину против гриппа людей, основанную на таких мутациях, использовали в США. Са мутанты успешно использовали при создании живых вакцин против ряда вирусных болезней животных.
Ра мутанты играют важную роль в аттенуации вирусов, инфекционность которых зависит от протеолиза структурного белка.
Известно, что протеолитическое расщепление парамиксовирусов необходимо для активации инфекционности и играет важную роль в проявлении тканевого тропизма и патогенности. Трипсин-подобные ферменты, присутствующие в клетках хозяина, требуются для расщепления предшественника белка сплавления FO на две субъединицы F1 и F2. Ра мутанты устойчивые к активации трипсином, оказывались аттенуированными.
Протеолитическое расщепление ГА вируса гриппа клеточными протеазами является важным для инфекционности вирусного потомства. В культуре клеток куринного эмбриона не происходит расщепления гемагглютинина.
Точечные мутации могут сочетаться с делеционными мутациями.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
АТТЕНУАЦИЯ (латинский attenuatio уменьшение, ослабление) — стойкое необратимое ослабление вирулентности патогенных микроорганизмов. Впервые аттенуированные штаммы микроорганизмов были получены Л. Пастером (1880), применившим их в качестве вакцинных для борьбы с куриной холерой, сибирской язвой и бешенством. Аттенуированные штаммы микроорганизмов нашли широкое применение при изготовлении живых вакцин против чумы, туляремии, бруцеллеза, сибирской язвы, туберкулеза, бешенства, гриппа, желтой лихорадки, кори, полиомиелита, Ку-лихорадки и пр. (см. Вакцины).
При получении аттенуированных штатов обычно используют длительные пассажи на животных, в частности, резистентных к возбудителю, в культуре ткани и в питательных средах при измененной температуре или при добавлении в среду сапонина, желчи, антибиотиков и других веществ. Значительно быстрее можно получать аттенуированные штаммы путем обработки микроорганизмов мутагенами с последующей селекцией клонов, обладающих сниженной вирулентностью. Аттенуированные штаммы встречаются также среди микроорганизмов, циркулирующих в природе.
Механизм аттенуации связан с селекцией в процессе пассажей мутантов, обладающих сниженной вирулентностью, однако образующаяся популяция обычно генетически гетерогенна и содержит как аттенуированные микроорганизмы, так и сохранившие вирулентность. Поэтому важным заключительным этапом получения аттенуированных штаммов является клонирование, то есть выделение из образующейся популяции микроорганизмов клонов, обладающих наиболее сниженной вирулентностью, с последующим приготовлением из таких клонов генетически однородной популяции. Примерами получения аттенуированных штаммов может служить получение штаммов: вируса бешенства (путем пассажей через организм кролика), туберкулезных бактерий БЦЖ (путем их пассирования в течение 13 лет на среде из глицеринового картофеля с добавлением желчи) и вируса желтой лихорадки (при пассажах вируса в куриных эмбрионах и культуре ткани).
Применение живых вакцин из аттенуированных штаммов микроорганизмов требует постоянного контроля стабильности наследственных свойств и генетической однородности популяции.
Читайте также:

