Биопарокс противовирусное или нет
Обновлено: 17.04.2024
RESEARCH OF MICROFLORA STRUCTURE AND LOCAL IMMUNITY IN PATIENTS WITH ACUTE RHINOSINUSITIS IN TREATMENTS BY NEW FORM OF BIOPAROX
K. G. Dobretsov 1 , O. A. Kolenchukova 2 , A. V. Sipkin 1
The paper presents the study of effectiveness of Bioparox new form (Servier, France) in the treatment of acute rhinosinusitis. 52 patients with severe and middle acute rhinosinusitis were treated: 25 patients - local use of aerosol Bioparox (new dose: 2 inhalations in each nasal passage, for times daily, during 7 days). Results: endoscopic inflammation criteria were less expressed in Bioparox treatment (2,4±0,5 points) in comparison with traditional method (3,6±0,4 points); bacterial number on 7 day: Staphylococcus - 10 3 /ml versus 10 5 /ml in control, Streptococcus - 5,5х10 3 /ml versus 10 8 /ml in control and absence of Enterococcus versus 5,5х10 2 /ml in control. The use of Bioparox improved local immunological criteria (IL-1β on 7 day - 2,6 pg/mg versus 3650 pg/mg - control; TNFa - 1,0 pg/pg versus 10,0 pg/mg - comparison group). Thus, results confirmed effectiveness of new form of Bioparox in the treatment of acute rhinosinusitis.
Key words: acute rhinosinusitis, Bioparox, microflora, immunity, local therapy.
Bibliography: 11 articles
Быстрый эффект Биопарокса при остром риносинусите основан на сочетании антибактериального и противовоспалительного действия [6]. Элиминация возбудителя из очага воспаления снижает антигенную бактериальную нагрузку и восстанавливает местный иммунитет [3]. Таким образом, анализ микробной флоры и местного иммунитета позволяет судить об эффективности той или иной терапии при остром риносинусите.
Цель работы: исследовать эффективность новой формы Биопарокса при лечении острого риносинусита на основе изучения состава микробной флоры и местного иммунитета.
Характеристика больных и методы исследования
На базе ЛОР отделения Дорожной клинической больницы на станции Красноярск нами было пролечено 52 человека с острым риносинуситом средней и тяжелой степени тяжести: 31 мужчина (59,6%) и 21 женщина (40,4%).
По возрасту преобладали больные от 20 до 29 лет (28 человек; 53,8%). Наиболее типичным оказалось двухстороннее гнойное поражение верхнечелюстных пазух и клеток решетчатого лабиринта (33 человека; 63,5%), одностороннее воспаление верхнечелюстной пазухи наблюдалось у 13 пациентов (25,0%), одностороннее поражение лобной пазухи - у 5 человек (9,6%) и двухстороннее - у 1 пациента (1,9%). У 3 больных (5,8%) был диагностирован пансинусит. Установлено, что до начала лечебных мероприятий патологический процесс имел риногенный, бактериальный, неосложненный характер.
Социально-бытовые условия у всех больных были расценены ими как относительно удовлетворительные, т. е. они имели постоянную работу и место жительства, материальное состояние семьи позволяло поддерживать достаточный уровень питания.
В исследование не включались пациенты с гиперпластическими процессами в пазухах, с риногенными внутриглазничными и внутричерепными осложнениями, пациенты с сахарным диабетом, получавшие курсы антибиотикотерапии в течение последнего месяца или курсы лучевой, системной кортикостероидной и химиотерапии в течение последнего года, имеющие в анамнезе аллергические реакции на антибиотики группы цефалоспоринов и пенициллинов, лабораторно подтвержденными иммунодефицитными состояниями, а также беременные и кормящие женщины.
Всем 52 больным с риносинуситами проводилась системная антибактериальная терапия (внутримышечные инъекции цефалоспоринов II-III поколения в течение 7 дней), назальные деконгестанты (нафтизин 0,05% по 2 капли 2 раза в день - 7 дней), а также промывание полости носа по Проетцу (1 раз в день - 7-10 дней).
В зависимости от методов местного лечения все больные были распределены на 2 примерно равные группы:
Группа I - состояла из 25 человек с острым риносинуситом, которым применялось местное лечение новой формой Биопарокса (по 2 ингаляции в каждый носовой ход 4 раза в день, 7 дней).
Группа сравнения - состояла из 27 больных с острым риносинуситом, которые не получали Биопарокс.
В качестве оценки результатов лечения нами применялись учет жалоб с помощью анкетирования, эндоскопия полости носа, бактериологическое исследование и определение иммунного статуса.
Кроме этого, критериями эффективности проводимой терапии являлось проведение и количество пункций и/или трепанопункций, которые выполнялись больным через 7 дней лечения. Показаниями для проведения манипуляций после недельного курса консервативной терапии было наличие не менее двух критериев:
1. боли в области щеки и/или лба 5 баллов и выше;
2. гнойное отделяемое из носа;
3. сохранение температуры тела 37,5 град, и выше.
Интенсивность болей оценивалась больным при помощи 10-балльной визуально-ана логовой шкалы (ВАШ). При этом ответы пациентов характеризовались следующим образом: от 0 баллов - отсутствие боли, до 10 баллов - мучительная (нестерпимая) боль.
При бактериологическом исследовании выделение микроорганизмов проводили на трех питательных дифференциально-диагностических средах. Для выделения микрофлоры использовали желточно-солевой агар, кровяной агар и агар Эндо. При микроскопии нативного материала использовали окраску по Граму. Выросшие колонии изолировали в чистую куль туру для дальнейшей идентификации. О чистоте культуры судили с помощью визуального и микроскопического контроля [5]. Бактериологическое исследование проводилось путем забора носового секрета на 1-е и 7-е сутки лечения.
Оценка иммунологического статуса включала определение уровня иммуноглобулинов, сывороточных и секреторных провоспалительных цитокинов.
Определение иммуноглобулинов проводили методом радиальной иммунодиффузии в геле по Манчини [7].
Готовили три двухкратных разведения стандартной сыворотки в физиологическом растворе (0,9% раствор хлорида натрия) 1:2, 1:4, 1:8 (по 0,05 мл каждого разведения). Инкубацию проводили при комнатной температуре во влажной камере. При определении IgG срок инкубации составлял 24 часа, при определении IgA 24/18 часов, при определении IgM -48 часов. Затем измеряли диаметры колец преципитации. По результатам измерения диаметров колец стандартной сыворотки строили калибровочную кривую в полулогарифмических координатах.
Иммунологическое исследование проводилось в 1-е и 7-е сутки лечения.
Результаты и обсуждение. Все больные исследуемой группы I при поступлении, как и в группе сравнения, предъявляли жалобы на выделения из носа, заложенность носа, боль/давление в области лица, ухудшение или потерю обоняния, слабость. На 5 сутки лечения жалобы на выделения из носа и заложенность носа у больных группы сравнения регистрировались у 18 (66,7%) и 16 (59,2%) больных соответственно. Аналогичные жалобы больные I группы в этот период предъявляли реже - 9 (36,0%) и 7 (28,0%) пациентов (р<0,05). На 10 сутки традиционного лечения жалобы сохранялись у 1/3 больных (8 человек; 29,6%). В группе I на 10 день жалобы на выделения из носа и заложенность носа предъявляли лишь 3 пациента (12,0%) (р<0,01).
Учитывая сохранение болей в области щеки и/или лба (6,1±0,8 балла) и наличие гнойного отделяемого из носа, 4 пациентам (14,8%) группы сравнения после 7-ми дневного курса терапии проводись пункции верхнечелюстных пазух. Повторные пункции верхнечелюстных пазух понадобились 2 пациентам (7,4%). У больных группы I однократная пункция верхнечелюстной пазухи проводилась только одному больному (4,0%) (р<0,01). Манипуляция проводилась в связи с наличием боли в области щеки (7,0 баллов) и гнойного отделяемого из носа после недельного курса терапии. Показаний для проведении трепанопункций лобных пазух больным обеих групп исследования отмечено не было.
При эндоскопическом исследовании полости носа в первые сутки болезни у всех больных с риносинуситом отмечались гиперемия, отек, влажность слизистой оболочки, обильные слизисто-гнойные выделения из носа. Интенсивность этих критериев оценивалась в баллах. Таким образом, в 1-е сутки терапии сумма баллов у больных обеих групп была максимальной: 4,2±0,5балла - в группе сравнения, 4,6±0,2 балла - в группе I. На 5 сутки лечения выраженность эндоскопической картины у больных I группы значительно уменьшилась и составила 2,4±0,5 балла, а в группе сравнения - 3,6±0,4 балла (р<0,05). К 10 суткам явления воспаления в полости носа купировались практически у всех больных группы I, интенсивность эндоскопических критериев равнялась 0,5±0,4 балла. У пациентов группы сравнения явления воспаления сохранялись и на 10 сутки (1,2±0,4 балла, р<0,05).
При микробиологическом исследовании у больных обеих групп исследования в первые сутки доминирующим родом были грамм положительные бактерий. Использование Биопарокса в новой дозировке сохранило выраженный антибактериальный эффект, что привело к обеднению микробного пейзажа на седьмые сутки лечения у больных I группы исследования. Так, в группе I бактерии рода Staphylococcus определялись в титре 1000 КОЕ/мл, против 100000 КОЕ/мл в группе сравнения (р<0,01); Streptococcus - 55000 КОЕ/мл, против 100000000 КОЕ/мл в группе сравнения (р<0,001); Enterococcus - не определялись, против 5500 КОЕ/мл в контроле (р<0,001) (табл. 1).
Таблица 1
Бактериологический анализ отделяемого из носа у больных с острым риносинуситом (N=52, median С25-С75)
Кроме антибактериального эффекта Биопарокс обладает еще и выраженным противовоспалительным действием. Это проявляется в уменьшении медиаторов воспаления и восстановлении иммунологических показателей.
При изучении уровня иммуноглобулинов на 7-е сутки достоверных отличий в группах лечения получено не было. Так, в группе I уровень IgM составит 10,15±1,3г/л; а в группе сравнения -13,90±3,5г/л; IgM в группе I - 0,78±0,3 г/л; в контроле - 1,48±0,5 г/л; IgA в группе I - 3,85±1,1г/л; в группе сравнения 1,19±0,6 г/л. Концентрация slgA в обеих группах была одинаковой (30,0 г/л). Отсутствие изменений специфических показателей гуморального иммунитета у пациентов с острым риносинуситом на 7-сутки свидетельствует об эффективности, в первую очередь, системной антибактериальной терапии. Однако, при дальнейшем изучении провоспалительных иммунологических показателей определено, что для полного купирования воспалительной реакции этого недостаточно. С этой точки зрения новая форма Биопарокса позволяет восстановить уровни цитокинов и повысить иммунный ответ на воспаление, как местно, так и всего организма в целом.
Рис. 1. Динамика уровня провоспалительного секреторного цитокина ИЛ- 1β у больных с острым риносинуситом (N=52, М±m).
Рис. 2. Динамика уровня провоспалительного секреторного цитокина ФНО-α у больных с острым риносинуситом (N=52, М±m).
Нормализация иммунного барьера в носовом секрете у больных группы I объясняется снижением острой воспалительной реакции в слизистой оболочке. Это происходило за счет как антибактериального, так и противовоспалительного действия Биопарокса, чего при традиционной терапии не отмечалось.
Выводы:
Результаты клинического исследования подтвердили эффективность применения новой формы Биопарокса при лечении острого риносинусита. Использование Биопарокса привело к значительному снижению микробной флоры и восстановлению местного иммунитета у больных с воспалением носа и околоносовых пазух.
Таким образом, необходимость применения новой формы Биопарокса при лечении острого риносинусита не вызывает сомнений, а уменьшение частоты введения препарата увеличивает его комплаентность.
ЛИТЕРАТУРА
1. Бондарь В. С., Поздняков И. О., Пузырь А. П. Применение наноалмазов для разделения и очистки белков. Физика твердого тела 2004; 4: 737-739.
2. Васильев А. Е. Наноносители лекарственных веществ // Новая аптека 2003; 1: 64-67.
3. Воробьев А. А. Основы микробиологии, вирусологии и иммунологии. М.: Мастерство 2002; 224.
4. Завгородняя Е. Г. Цитокины и их место в диагностике и лечении ряда заболеваний ЛОРорганов. //Вестн. оторинолар. 2008; 3: 74-76.
5. Зубков М. Н. Сбор биологического материала для бактериологического исследования //Клинич. микробиология и антимикробная химиотерапия 2004; 2: 144-148.
6. Козлов В. С., Шиленкова В. В., Державина Л. Л. Влияние препарата биопарокс на слизистую оболочку полости носа при остром катаральном риносинусите // Вестн. оторинолар. 2007; 4: 45-74.
7. Лебедев К. А. Иммунология в клинической практике. М.: Медицинская электронная библиотека 1996; 387.
8. Овчинников А. Ю., Дженжера Г. Е., Лопатин А. С. Острый бактериальный риносинусит: в поисках оптимального антибиотика. Рос. ринология 2009; 1: 4-7.
9. German-Fattal М., Mosges R. How to improve current therapeutic standards in upper respiratory infections: value of fusafungine // Curr. Med. Res. Opin. 2004; 20(11): 1769-1776.
10. Lu A. H., Salabas E. L., Schuth F. Magnetic nanoparticles: synthesis, protection, functionalization, and application //Angew. Chem. Int. Ed. Engl. 2007; 46 (8): 1222-1244.
11. Yao L., Xu S. Long-range, high-resolution magnetic imaging of nanoparticles //. Angew. Chem. Int. Ed. Engl. 2009; 48 (31): 5679-5682.
Аэрозольный алюминиевый баллон, оснащенный клапаном дозирующего действия.
Содержимое баллона: раствор желтого цвета со специфическим запахом.
Фармакологическое действие
Фармакодинамика
Фузафунгин является антибиотиком местного действия с противовоспалительными свойствами.
В условиях in vitro препарат оказывает антимикробное действие на следующие микроорганизмы, что позволяет предполагать аналогичный эффект in vivo: стрептококк группы А (group A Streptococci), пневмококк (Pneumococci), стафилококк (Staphylococci), некоторые штаммы нейссерий (Neisseria), некоторые анаэробы, грибы рода кандида (Candida albicans) и микоплазма пневмониа (Mycoplasma pneumoniae).
Фузафунгин оказывает выраженное противовоспалительное действие за счет снижения концентрации фактора некроза опухоли (TNF-α) и подавления синтеза свободных радикалов макрофагами при сохранении фагоцитоза.
Фармакокинетика
Фузафунгин в основном распределяется в ротоглотке и полости носа. В плазме крови фузафунгин может обнаруживаться в очень низкой концентрации (не более 1 нг/мл), что не влияет на безопасность применения препарата.
Показания
Лечение инфекционно-воспалительных заболеваний верхних дыхательных путей у взрослых и подростков с 12 лет:
состояние после тонзиллэктомии;
Противопоказания
повышенная чувствительность к активному веществу или к вспомогательным веществам, входящим в состав препарата;
Применение при беременности и кормлении грудью
Клинические данные о применении в период беременности отсутствуют. В связи с этим назначать препарат беременным женщинам следует с осторожностью.
В длительных исследованиях на лабораторных животных не выявлено эмбрио-, генотоксических эффектов и тератогенного действия на плод.
В связи с отсутствием данных об экскреции с грудным молоком применение препарата Биопарокс ® кормящим женщинам не рекомендуется.
Побочные действия
Со стороны иммунной системы: очень редко — анафилактический шок.
Со стороны нервной системы: очень часто — дисгевзия (нарушение вкусовых ощущений).
Со стороны органов зрения: очень часто — гиперемия конъюнктивы.
Со стороны дыхательной системы, органов грудной клетки и средостения: очень часто — чиханье; часто — сухость в носу, сухость в горле, раздражение горла, кашель; очень редко — приступы бронхиальной астмы, бронхоспазм, одышка, ларингоспазм, ангионевротический отек, в т.ч. отек гортани.
Со стороны ЖКТ: часто — тошнота; неустановленной частоты — рвота.
Со стороны кожи и подкожных тканей: очень редко — сыпь, зуд, крапивница, отек Квинке.
Если любые из указанных в описании побочных эффектов усугубляются, или пациент заметил любые другие побочные эффекты, не указанные в описании, следует сообщить об этом врачу.
Взаимодействие
Специальных исследований по изучению взаимодействия с другими лекарственными препаратами не проводилось.
Способ применения и дозы
Местно (для высвобождения в полости рта и/или в носовой ход).
Взрослым и детям старше 12 лет: по 4 высвобождения в полость рта и/или по 2 высвобождения в каждый носовой ход 4 раза в день.
Для максимального использования активности препарата Биопарокс ® важно соблюдать предписанную дозу и выполнять правила использования приложенных насадок. Для стойкого терапевтического эффекта необходимо соблюдать длительность предписанного лечения: не рекомендуется прекращать лечение при появлении первых признаков улучшения, т.к. преждевременное прекращение терапии может привести к рецидиву.
Препарат следует всегда иметь при себе, поместив его в приложенный футляр для портативной переноски.
Длительность обычного курса лечения не должна превышать 7 дней.
По окончании курса терапии необходимо обратиться к врачу для оценки эффективности лечения.
При сохранении симптомов заболевания и/или повышенной температуры на фоне терапии препаратом Биопарокс ® необходимо сообщить об этом лечащему врачу.
В случае наличия выраженных клинических проявлений бактериальной инфекции возможно проведение лечения препаратом Биопарокс ® в комбинации с системными антибиотиками.
Способ применения препарата Биопарокс ®
1. Перед первым использованием для активации баллона следует нажать на его основание 4 раза.
2. Надеть на баллон соответствующую насадку: (белую, для ингаляции препарата через рот (2) или желтую, для его введения через нос) (рис. 1).
Использование препарата через нос (при рините, ринофарингите, синусите):
Баллон с препаратом необходимо держать вертикально насадкой вверх, зажав его между большим и указательным пальцами.
1. Прочистить нос перед использованием препарата.
2. Закрепить желтую насадку на баллоне и ввести ее в носовой ход (зажав при этом противоположный носовой ход и закрыв рот). При использовании не следует делать вдох.
3. Энергично и до упора нажать на основание баллона два раза, удерживая баллон в вертикальном положении (рис. 2).
Использование препарата через рот (при фарингите, тонзиллите, состоянии после удаления миндалин, ларингите)
Надеть на баллон белую насадку (рис.3) и ввести ее в рот, плотно зажав губами. Держать баллон, как указано на рис.4. При использовании не следует делать вдох.
Держать баллон вертикально и энергично до упора нажать 4 раза на основание баллона, как указано на рис. 4.
Насадки для рта и носа необходимо дезинфицировать через день с помощью ватного тампона, смоченного в 90% этиловом спирте.
Передозировка
Имеется ограниченная информация о передозировке фузафунгина.
Симптомы: нарушение кровообращения, онемение во рту, головокружение, усиление боли в горле, жжение в горле.
Лечение: в случае передозировки лечение должно быть симптоматическим, с последующим наблюдением.
Особые указания
Чрезмерно длительное использование препарата может привести к развитию суперинфекции. Не рекомендовано превышение длительности стандартного 7-дневного курса терапии в соответствии с общими правилами применения антибиотиков. По окончании 7-дневного курса терапии необходимо обратиться к врачу для оценки эффективности лечения. Если симптомы и клинические признаки заболевания не уменьшаются на протяжении 7 дней терапии, следует рассмотреть возможность альтернативного лечения. Пропиленгликоль может вызывать раздражение кожи.
В случае развития аллергических реакций прием препарата должен быть прекращен, не следует возобновлять прием препарата.
В связи с риском развития анафилактического шока в случае появления респираторных, ларингиальных симптомов или кожных (зуд, генерализованная эритема) симптомов может потребоваться незамедлительное в/м введение эпинефрина (адреналина). Рекомендуемая доза составляет 0,01 мг/кг в/м. При необходимости в/м инъекцию можно повторить через 15–20 мин.
В состав препарата входит незначительное количество этанола, менее 100 мг/доза. Не распылять препарат в глаза. Не допускать хранения препарата вблизи сильных источников тепла. Не подвергать воздействию температуры выше 50 °C.
Не допускать нарушения герметичности корпуса баллона и его сжигания даже после полного использования препарата.
Влияние на способность управлять транспортными средствами, механизмами. Биопарокс ® не влияет на способность к управлению автомобиля и скорость психических и физических реакций.
Форма выпуска
Аэрозоль для местного применения дозированный, 0,125 мг/ высвобождение. По 10 мл раствора в аэрозольный алюминиевый баллон. По 400 высвобождений (100 доз) в алюминиевый баллон. Баллон имеет клапан дозирующего действия, снабженный двумя насадками-распылителями: для носа (желтая) и рта (белая), колпачком-активатором. Один баллон с насадками-распылителями и колпачком-активатором в контурной ячейковой упаковке с футляром для портативной переноски и инструкцией по медицинскому применению в картонной пачке.
Производитель
Произведено: Закрытое Акционерное Общество Фармацевтический Завод ЭГИС, Венгрия.
Закрытое Акционерное Общество Фармацевтический Завод ЭГИС, Венгрия: 9900, Кёрменд, ул. Матяш Кирай 65, Венгрия.

1 доза содержит фузафунгина 125 мкг (1 флакон - 50 мг);
400 доз в баллончике алюминиевом объемом 10 мл в комплекте с насадками-распылителями и колпачком-активатором, в картонной пачке.
Фармакологическое действие
Биопарокс - антибиотик для местного применения, системного действия не оказывает. Обладает антибактериальной и противовоспалительной активностью.
Биопарокс - аэрозоль в виде микрочастиц, которые проникают в наиболее удаленные и труднодоступные отделы дыхательных путей (синусы, бронхиолы).
Препарат активен в отношении: Streptococcus spp. группы A, Streptococcus pneumoniae (старое название - Pneumococcus), Staphylococcus spp., некоторых штаммов Neisseria spp., некоторых анаэробов, а также Mycoplasma spp., грибов рода Candida.
Показания к применению
Местное лечение воспалительных и инфекционных заболеваний носоглотки и дыхательных путей (синусит, ринит, ринофарингит, фарингит, тонзиллит, состояния после тонзиллэктомии, ларингит, трахеит, бронхит).
Противопоказания
- повышенная чувствительность к препарату;
- детский возраст до 2.5 лет.
Беременность и период лактации
Способ применения и дозы
Взрослым назначают по 1 сеансу каждые 4 ч. Обычно 4 раза в сутки.
Каждый сеанс включает в себя 4 ингаляции через рот и/или 4 ингаляции через каждую ноздрю.
Детям назначают по 1 сеансу каждые 6 ч.
Длительность обычного курса лечения не должна превышать 7 дней.
При синуситах, ринитах, ринофарингитах следует проводить ингаляции через нос с использованием носового наконечника. Перед проведением ингаляции следует высморкаться, затем частично ввести носовой наконечник в ноздрю. Необходимо основательно и длительно нажимать на дно флакона, делая глубокий вдох для полного орошения носовых ходов и синусов. Вдыхание каждой дозы аэрозоля должно проводиться с закрытым ртом.
При фарингитах, тонзиллитах, состояниях после тонзиллэктомии, ларингитах следует проводить ингаляции через рот, используя наконечник для рта. Следует снять носовой наконечник, слегка поворачивая его; адаптировать наконечник для рта на флакон, поместить наконечник в рот, обхватив его губами; затем основательно и длительно нажимая на дно флакона, сделать глубокий вдох для полного орошения миндалин и глотки.
При трахеитах, бронхитах перед проведением ингаляции необходимо откашляться, затем глубоко вдохнуть аэрозольную смесь и задержать дыхание на несколько секунд для полного орошения бронхов.
Побочное действие
Взаимодействие с другими лекарственными средствами
Особенности применения
Биопарокс не следует применять в течение длительного времени, поскольку это может привести к нарушению нормальной микробной флоры с риском распространения инфекции. Обычно длительность лечения ограничивается 10 днями, в противном случае лечебную тактику необходимо пересмотреть.
Для максимального использования активности Биопарокса необходимо соблюдать число предписанных сеансов и выполнять правила употребления двух приложенных наконечников.
Для получения стойкого терапевтического эффекта необходимо соблюдать длительность предписанного лечения: не рекомендуется прекращать сеансы при появлении первых признаков улучшения - это может привести к рецидиву.
Необходимо применение препарата в комбинации с антибиотиками для системного применения в случаях генерализации инфекции.
Биопарокс может быть использован для лечения пациентов пожилого возраста.
Для проведения регулярных сеансов необходимо всегда иметь флакон при себе, поместив его в футляр.
Рекомендуется ежедневно дезинфицировать два наконечника с помощью ватного тампона, смоченного в этаноле (90°).
Использование в педиатрии
действующее вещество: интерферон альфа-2b рекомбинантный человеческий 100000 МЕ/мл;
вспомогательные вещества: трометамол, трометамола гидрохлорид, гипромелоза, динатрия эдетат, лизина гидрохлорид, калия хлорид, метилпарагидроксибензоат (E 218), вода для инъекций.
1 мл препарата содержит 23 капли.
Код классификации
Иммунобиологические и биологические свойства
В состав препарата НАЗОФЕРОН входит рекомбинантный человеческий интерферон альфа 2b. Интерферон альфа-2b оказывает противовирусное, иммуномодулирующее, антипролиферативное и антибактериальное средство. Биологическое действие интерферона характеризуется следующими эффектами: противовирусный − угнетает репликацию вирусов (аденовирусов, вирусов гриппа и др.) за счет ингибирующего действия на процессы транскрипции и трансляции; антипролиферативный − угнетает размножение клеток (большинства ДНК- и РНК- содержащих вирусов). Интерферон инициирует синтез специфического фермента − протеинкиназы, которая препятствует трансляции благодаря фосфорилированию одного из инициирующих факторов этого процесса; активизирует специфическую рибонуклеазу, которая повреждает матричную РНК вируса. К эффектам интерферона относятся также: стимуляция продукции других цитокинов, индукция специфических ферментов, угнетение пролиферации клеток, иммуномодуляция (усиление фагоцитарной активности макрофагов и специфической цитотоксичности лимфоцитов по отношению к клеткам-мишеням).
Фармакокинетика
Исследования фармакокинетики не проводились ввиду низкой биодоступности препаратов рекомбинантных белков при интраназальном применении, вследствие чего концентрация активного вещества, достигаемая в крови при использовании препарата в рекомендуемых дозах, значительно ниже предела обнаружения и не имеет клинической значимости.
Показания к применению
Способ применения и дозировка

При первых признаках заболевания ОРВИ (на протяжении 5 дней)
Детям от 1 месяца до 1 года − по 1 капле в каждый носовой ход 5 раз в день (разовая доза − 8000 МЕ, суточная доза − 40000 МЕ);
Детям от 1 до 3 лет − по 2 капли 3-4 раза в день (разовая доза − 16000 МЕ, суточная доза – 48000-64000 МЕ);
Детям от 3 до 14 лет − по 2 капли 4-5 раз в день (разовая доза − 16000 МЕ, суточная доза – 64000-80000 ME);
Взрослым – по 3 капли 5-6 раз в день (разовая доза – 24000 МЕ, суточная доза – 120000-144000 МЕ).
Для профилактики респираторных вирусных инфекций
При контакте с больным и при переохлаждении − в соответствии с возрастной дозировкой 2 раза в день в течение 5-7 дней. В случае необходимости профилактические курсы повторяют. При однократном контакте достаточно одного закапывания.
При сезонном повышении заболеваемости − в соответствии с возрастной дозировкой однократно утром с интервалом через 1-2 дня.
Схема использования капель назальных во флаконе, закупоренном капельницей:
1. Снять защитный колпачок с флакона.
2. Повернуть флакон насадкой вниз и перед первым применение капель сделать несколько пробных нажатий на насос-дозатор.
3. Поместить конец насадки поочередно в каждый носовой ход и нажать на насос-дозатор необходимое количество раз в соответствии с дозировкой.
4. После применения закрыть флакон колпачком.
Не следует применять препарат в случае нарушения целостности и маркировки упаковки, при изменении физических свойств (цвета или прозрачности жидкости) и после окончания срока годности.
Чтобы избежать распространения инфекции, рекомендовано индивидуальное использование.
Побочное действие
В единичных случаях − сыпь на коже.
В случае появления нежелательных реакций следует проконсультироваться с врачом.
Противопоказания
Повышенная чувствительность к интерферону альфа-2b и другим компонентам, входящим в состав препарата, тяжелые формы аллергических заболеваний в анамнезе.
Период беременности или кормления грудью.
В статье представлены данные и обсуждены основные причины заболеваемости детей острыми респираторными вирусными инфекциями в Санкт-Петербурге; приведены результаты применения топического аэрозольного антибиотика фузафунгина (Биопарокс) у 28 детей в возрасте от 3 до 17 лет, страдавших острыми респираторными заболеваниями. Обладающий выраженным противовоспалительным действием и не имеющий побочных эффектов, Биопарокс может быть альтернативой применению системных антибиотиков у часто болеющих детей как при острых респираторных заболеваниях, так и в профилактике активации бактериальной инфекции дыхательных путей.
Ключевые слова: респираторная инфекция, дети, местная антибактериальная терапия, фузафунгин
LOCAL ANTIBACTERIAL THERAPY OF FREQUENTLY ILL CHILDREN: AN EXPERIENCE OF USING BIOPAROX
N.D.Soroka 1 , S.P.Gomozova 2 , E.V.Korshunova 1 , E.K.Volochugina 1 , T.G.Vlasova 3 , L.V.Ostrovskaya 1
1 St.Petersburg Medical Academy of Post-Graduate Education;
2 Municipal Pediatric Hospital No 19, St.Petersburg;
3 Municipal Pediatric Hospital No 37, St.Petersburg
The article presents data and discusses main causes of the incidence of acute respiratory viral infections among the pediatric population in St.Petersburg; it describes the results of using the topic antibiotic fusafungin (Bioparox spray) in 28 children aged from 3 to 17 years, who suffered from acute respiratory diseases. Having a strong anti-inflammatory effect and no side effects, Bioparox might be an alternative to using systemic antibiotics in frequently ill children to treat acute respiratory diseases and prevent activation of bacterial infection of the respiratory tract.
Key words: respiratory infection, children, local antibacterial therapy, fusafungin
Острые респираторные заболевания (группа этиологически неоднородных болезней, объединенных общими эпидемиологическими и клиническими характеристиками) ежегодно регистрируются более, чем у 20 млн. детей (по данным Министерства здравоохранения и социального развития Российской Федерации) [1, 2]. Подавляющее большинство респираторных заболеваний имеет вирусную природу. Именно острые респираторные вирусные инфекции (ОРВИ) занимают лидирующее положение в структуре детской заболеваемости, составляя 90% всех болезней респираторного тракта инфекционной природы [1, 2]. Несмотря на широкое внедрение в лечебную практику большого числа профилактических средств и противовирусных препаратов (воздействующих на ключевые звенья патогенеза воспалительного процесса), ОРВИ остаются малоуправляемыми инфекциями. По данным Всемирной организации здравоохранения, каждый ребенок в течение года переносит несколько эпизодов респираторных инфекций, большинство из которых протекают легко и статистикой не фиксируются [1, 3].
Анализ учтенной заболеваемости детей ОРВИ и гриппом в Санкт-Петербурге за последние 10 лет представлен на рис. 1. Как видно из диаграммы, в течение только 2003 г. в Санкт-Петербурге ОРВИ переболели 605 378 детей, или 75% всего детского населения города. К причинам столь стабильно высокой заболеваемости ОРВИ у детей можно отнести: чрезвычайно большое количество (более 200 видов) возбудителей; высокую изменчивость антигенной специфичности вирусов (особенно вирусов гриппа) и тропность вирусов к слизистой оболочке дыхательных путей; отсутствие эндемичности вирусной инфекции; нестойкость противовирусного иммунитета; анатомо-физиологические особенности строения дыхательных путей и адаптивно-защитных механизмов детского организма; высокий уровень промышленных и транспортных загрязнений внешней среды (особенно в крупных городах).
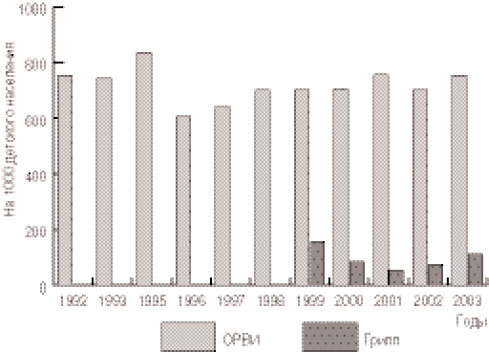
Рис. 1. Заболеваемость детей ОРВИ и гриппом в Санкт-Петербурге (1992-2003 гг.).
ОРВИ в педиатрии тесно связаны с большим количеством проблем. ОРВИ являются причиной значительного экономического ущерба: если прямые расходы (непосредственно на лечение) составляют 25%, то косвенные (связанные с временной нетрудоспособностью или снижением продуктивности труда родителей) превышают 70%. Расчеты, проведенные И.Л.Шахининой в 1998 г., показали, что экономические потери от ОРВИ за 1998 г. в Москве составили 1,5 млрд. руб., а в 1997 г. по Российской Федерации (ОРВИ-Грипп) -16,6 млрд. руб. [4].
Неоспорима синергическая и кондуктивная роль ОРВИ в формировании воспалительных процессов, вызванных бактериальной флорой (бронхитов, пневмоний и др.) как в амбулаторных условиях, так и в стационаре (внутрибольничные ОРВИ значительно повышают опасность заражения госпитальными штаммами резистентных к антибиотикам микроорганизмов) [3, 5].
Основные патогенетические механизмы ОРВИ можно представить следующей схемой (рис. 2). В ней выделены три узловых звена, которые необходимо учитывать при построении программы лечения ОРВИ (сочетание этиотропного, патогенетического и симптоматического лечения).
Рис. 2. Патогенетические механизмы острой респираторной вирусной инфекции.
Этиотропное лечение (противовирусное или антибактериальное - при наличии признаков активности бактериальной инфекции) широкого распространения у детей не получило [6, 7]. Это связано с малым количеством разрешенных в педиатрической практике препаратов, обладающих специфической противовирусной активностью; значительное их число, кроме возрастных ограничений, имеет и серьезные побочные эффекты. Необходимо также учитывать, что основным условием эффективности противовирусных средств является раннее их назначение (с первых симптомов заболевания), что не всегда возможно. Определенную роль играет и высокая стоимость большинства противовирусных средств. Многочисленными исследованиями доказана неэффективность антибиотикотерапии при ОРВИ, протекающих с симптомами поражения как верхних (ринит, фарингит, ларингит, синусит), так и нижних дыхательных путей (трахеит, бронхит). Необоснованное назначение антибактериальной терапии, особенно у детей раннего возраста, способствует формированию бактериальной резистентности, рецидивирующему течению респираторных инфекций; удлинению сроков выздоровления и формированию лекарственной аллергии у предрасположенных детей. Таким образом, педиатр должен взвешивать необходимость и целесообразность назначения системных антибиотиков при острых неосложненных инфекциях верхних дыхательных путей.
В случае такого выбора в ряде случаев альтернативой может служить местная антибактериальная терапия, позволяющая подавить активность бактериальной инфекции и препятствовать ее распространению на дистальные отделы бронхолегочной системы, что особенно важно при лечении инфекции носоглотки у часто и длительно болеющих детей [1, 3, 7, 8].
Попытки ингаляции системных антибиотиков не увенчались успехом из-за низкой эффективности и большого числа побочных эффектов (нарушения в составе микрофлоры носоглотки, в том числе активизация грибковой флоры, высокий риск формирования лекарственной аллергии, местное раздражающее действие и др.) [5].
В этой связи нам представляется, что наиболее рациональным препаратом для проведения местной антибиотикотерапии в настоящее время можно считать Биопарокс (Фузафунгин) - топический аэрозольный антибиотик, обладающий бактериостатическим и противовоспалительным эффектами. Его действующим началом является фузафунгин, полученный из гриба-микомицета Fusarium lateritium WR 437. Подавляя процесс размножения и препятствуя адгезии микробов к слизистой оболочке дыхательных путей, Биопарокс одномоментно оказывает и антимикотическое действие (особенно в отношении Candida albicans), что уменьшает риск развития вторичного кандидоза (см. таблицу). Биопарокс действует на микробную флору в течение 12 ч; оптимальный эффект наблюдается в течение 4 ч после введения препарата [7, 9].
Таблица. Антимикробный спектр действия Биопарокса
| Грамположительные бактерии | Грамотрицательные бактерии | Прочие |
| Staphylococcus aureus Streptococcus A,C,G Streptococcus mutants Streptococcus pneumoniae | Грамотрицательные кокки: Moraxella catarrhalis Грамотрицательные бациллы: Listeria monocytogenes Actinomyces pyogenes Nocardia asteroides Nocardia brasiliensis Pasteurella multocida Haemophilus influenzae | Mycoplasma pneumoniae Анаэробы: Clostridium perfringens Clostridium butyricum Propionibacterium acnes Грибы: Candida albicans |
Противовоспалительные свойства Биопарокса обусловлены подавлением выработки провоспалительных цитокинов (интерлейкинов-1, -6, ФНО, супероксидов), стимуляцией образования интерлейкина-2 и естественных клеток-киллеров, повышением концентрации иммуноглобулинов A и лизоцима в секрете носоглотки; активацией макрофагов и фагоцитарной активности нейтрофилов; повышением неспецифической резистентности слизистой оболочки верхних дыхательных путей и пр. 7.
Препарат выпускается в форме дозированного аэрозоля, содержащего 20 мл (400 доз по 0,125 мг) активного раствора и снабжен двумя насадками (назальной и оральной). Ингаляции детям проводятся (начиная с 2,5-летнего возраста) 4 раза/сут, по 4 дозы через рот и/или по 4 дозы в каждый носовой ход. При необходимости Биопарокс может комбинироваться с системными антибиотиками и другими противовоспалительными средствами. Средняя продолжительность курса лечения составляет 7-10 дней.
Цель настоящего открытого исследования: оценка воздействия Биопарокса на отдельные симптомы ОРВИ и определение возможностей препарата в профилактике вторичных бактериальных осложнений.
Пациенты и методы. Под наблюдением находилось 28 детей в возрасте от 3 до 17 лет с клиническими проявлениями острой респираторной инфекции: в амбулаторных условиях (20 детей) и в условиях специализированного пульмонологического отделения (8 пациентов). 22 ребенка посещали школу и относились к группе часто и длительно болеющих; 8 человек имели неблагоприятный преморбидный фон (атопические заболевания нижних дыхательных путей и хронические заболевания ЛОР-органов). Все пациенты получали комплексное лечение острого респираторного заболевания по единому протоколу; в исследование не были включены дети, которым было показано назначение системных антибиотиков или до начала исследования уже проводилась антибиотикотерапия (местная или системная).
Основные симптомы заболевания у наблюдавшихся больных представлены на рис. 3.
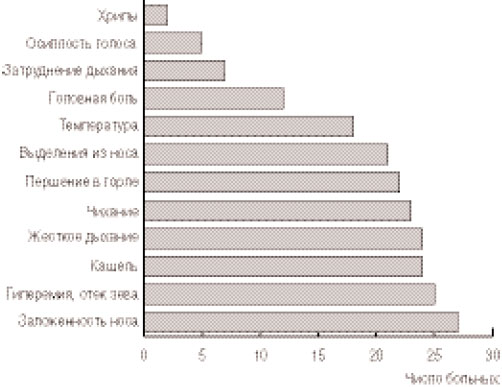
Рис. 3. Основные клинические симптомы ОРЗ.
Острый ларингит или ларинготрахеит был диагностирован у 4 пациентов, острый ринит и ринофаренгит - у 18 детей, острый трахеобронхит и бронхит - у 6 больных. Проявления интоксикации (нарушения самочувствия, недомогание, головная боль, умеренная лихорадка) отмечены у 11 детей.
У 19 детей до начала лечения отмечались умеренно выраженный лейкоцитоз и повышенная СОЭ.
Биопарокс был включен в комплексную терапию ОРЗ в 1-2-й или на 5-10-й дни заболевания в связи с отсутствием эффекта от традиционного лечения. Основным показанием к применению Биопарокса была необходимость профилактики бактериальной инфекции (хроническая носоглоточная инфекция) или признаки ее активности (интоксикация, гнойная мокрота или слизисто-гнойные выделения из носа) а также неэффективность предшествующей симптоматической терапии. Препарат применялся 4 раза в день по 4 ингаляции через рот и в каждый носовой ход; курс лечения в среднем составил 7 дней. Дети, лечившиеся амбулаторно, осматривались педиатром до начала лечения, на 7-й и 10-14-й дни от начала приема Биопарокса; а при необходимости - и в более отдаленные сроки (до полного выздоровления). Результаты лечения оценивались на основании: дневников ежедневного самоконтроля, где учитывались признаки обратного развития симптомов заболевания (улучшения самочувствия, исчезновение интоксикации и др.); данных физикального обследования (исчезновение хрипов, жесткого дыхания); динамики лабораторных показателей.
Симптомы ринита у подавляющего большинства детей значительно уменьшились к 5-му дню лечения и полностью исчезли у 22 детей через 8 дней приема препарата (рис. 4): чихание и зуд в носу исчезли через 6 дней, а выделения из носа - через 7-8 дней применения Биопарокса. У 5 пациентов (со склонностью к атопии и хроническим аденоидитом) длительно (свыше 10 дней) сохранялись заложенность носа и необильные слизистые выделения; однако и у них на фоне лечения препаратом отмечалась существенная положительная динамика (исчезновение гиперемии и уменьшение отека слизистой оболочки при риноскопии).
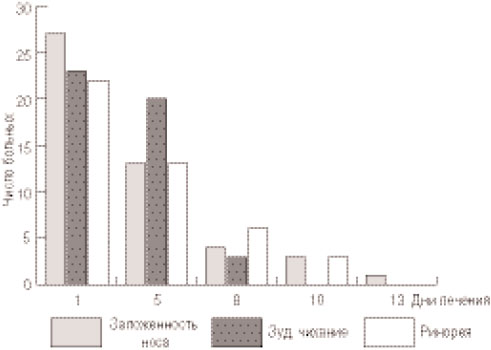
Рис. 4. Динамика обратного развития клинических проявлений ринита у детей на фоне лечения Биопароксом.
Симптомы острого ларингита и ларинготрахеита у большинства наблюдаемых детей полностью исчезали к 9-му дню лечения; охриплость голоса, боль и першение в горле исчезали в основном к 6-му дню лечения (рис. 5). Дольше всего сохранялась гиперемия зева у детей с хроническим тонзиллитом или гипертрофией небных миндалин; в этой группе дети получали Биопарокс до 10 дней.
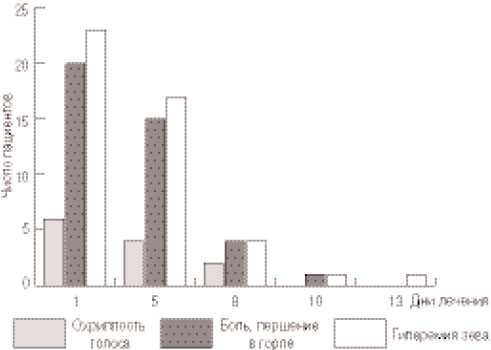
Рис. 5. Динамика обратного развития клинических проявлений ларингита/ларинготрахеита у детей на фоне лечения Биопароксом.
При остром бронхите или трахеобронхите (рис. 6), затруднение дыхания, неприятные ощущения в грудной клетке к 6-му дню наблюдения определялись лишь у 1 пациента; кашель, жесткое дыхание и хрипы на 5-й день лечения не определялся у 4 детей, а на 10-й день - у 21 ребенка. Длительный (более 13 дней), непродуктивный кашель на фоне жесткого дыхания был зафиксирован у 6 детей с отягощенным преморбидным фоном, что потребовало дополнительного назначения противокашлевых препаратов.
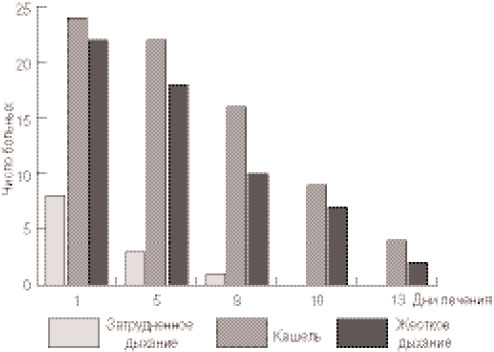
Рис. 6. Динамика обратного развития клинических проявлений бронхита/трахеобронхита у детей на фоне лечения Биопароксом.
Симптомы интоксикации у всех больных через 5 дней лечения полностью были купированы.
Полное клиническое выздоровление к 13-му дню от начала лечения Биопароксом достигнуто у 24 детей; у 4 пациентов (с неблагоприятным преморбидным фоном) сохранялись нечастый сухой кашель, заложенность носа и жесткий характер дыхания, потребовавшие дополнительной симптоматической терапии. Ни у одного ребенка, получавшего Биопарокс, не возникло показаний к проведению антибактериальной терапии. В ходе наблюдений не были зафиксированы ни побочные явления, ни обострения аллергических заболеваний, ни бактериальные осложнения.
Эффективность и переносимость препарата, как врачами, так и пациентами была оценена как отличная (18 человек) или хорошая (5 пациентов).
Нежелательные явления (умеренно выраженная сухость слизистых полости рта после ингаляций и неприятные ощущения во рту в первые дни приема) были отмечены у 2 пациентов, но не потребовали отмены препарата.
Таким образом, топический аэрозольный антибиотик Биопарокс является эффективным препаратом с выраженным противовоспалительным действием и может быть рекомендован в качестве стартового антибактериального препарата в лечении ОРВИ с признаками активизации бактериального процесса. Для получения оптимального терапевтического эффекта рационально назначение препарата в первые дни ОРЗ.
ЛИТЕРАТУРА
1. Коровина Н.А., Овсянникова Е.М. Вопр. современной педиатрии. 2002; 1(1): 1-4.
2. Крослак М. ОРВИ или грипп? Легкое дыхание. Науч.-практ. изд. для врачей. 2005; 16: 2-3.
3. Зайцева О.В., Щербакова М.Ю. Острые респираторные заболевания у детей: современные аспекты лечения и профилактики. М., 2004, с.4.
4. Шахинина И.Л. Грипп и острые респираторные заболевания - приоритетная социально-экономическая проблема здравоохранения. Информ. сб. М., 1998; 10-17.
5. Овчинников Ю.М., Свистушкин В.М., Никифорова Г.Н. Рациональное местное лечение при воспалительных заболеваниях верхних дыхательных путей. Инфекции и антимикробная терапия, 2000; 6 (2): 190-102.
6. Белоусов Ю.М. Антимикробная терапия. РМЖ; 1998; 12(7): 10-13.
7. Балясинская Г.Л. Биопарокс в лечении заболеваний ЛОР-органов у детей. Практ. рекомендации по материалам VIII Конгресса педиатров России. М., 1998: 20.
8. Barth V. et al. Местная антибактериальная терапия заболеваний верхних дыхательных путей. М., 2000: 12-14.
9. .Pandraud L. Therapeutic Efficacy and Clinical Ecceptability of Fusafungine in Follicular Pharyngitis; Cur. Med. Res. and Opinion. 2002; 7(18): 381-388.
Читайте также:

