Болезнь альцгеймера и гепатит
Обновлено: 19.04.2024
Болезнь Альцгеймера — это прогрессирующая форма нейродегенеративного расстройства, приводящего к нарушению нейронных связей и отмиранию клеток головного мозга. Указанные изменения вызывают слабоумие и потерю дееспособности. Заболевание чаще всего встречается у лиц преклонного возраста, но зафиксированы случаи и среди молодых людей.
Признаки болезни Альцгеймера: рассеянность, постоянные провалы в памяти (пациент забывает, куда положил свои вещи, что покупал, где живет), повторение одних и тех же рассказов, нарушение концентрации внимания, раздражительность, сонливость или бессонница, проблемы с устной и письменной речью.
Диагностировать патологию помогает сбор анамнеза. Специалист назначает проведение аппаратных исследований: ПЭТ, ЭЭГ, КТ или МРТ. Дополнительно проводят лабораторные исследования: анализ крови, генно-молекулярный анализ.
Альцгеймер относится к неизлечимым видам болезней. Терапия состоит из приема медикаментов в сочетании с психосоциальной методикой поддержания и стабилизации пациента.
Причины возникновения
Факторы, вызывающие деменции, остаются загадкой, и до сегодняшнего дня ученые не определили точную причину, дающую толчок развитию заболевания. Доподлинно известно только то, что у человека нарушаются обменные процессы в коре головного мозга. Из-за этого происходит накопление вредных веществ — бета-амилоидов (сенильных бляшек) и тау-белка.
Вышеперечисленные предположения стали основой трех теорий, которые объясняют этиологию развития патологии.
- Холинергическая гипотеза утверждает, что деменции начинают образовываться из-за снижения синтеза ацетилхолина, именно он несет ответственность за передачу соответствующих импульсов из коры головного мозга в мышечные структуры. Гипотеза подвергается критике из-за того, что восстановление уровня содержания основного вещества в организме человека не препятствует развитию патологии.
- Амилоидная гипотеза настаивает на том, что причина возникновения дегенерации тканей начинается с отложения бета-амилоидных пептидов. Они выполняют защитную функцию. При нарушении процесса обмена полезные вещества превращаются в компоненты, которые наносят вред.
- Теория Тау рассматривает последовательность в цепочке нарушений, связанных с отклонениями в структуре тау-белка, который начинает проявлять несвойственную ему функциональность и уничтожает нейроны.
Не стоит исключать и генетическую предрасположенность: если у кого-то из близких родственников имелся в анамнезе такой диагноз, то велика вероятность его появления и у наследника.
Мнение эксперта

Автор: Георгий Романович Попов
Врач-невролог, кандидат медицинских наук
Болезнью Альцгеймера страдают по большей части люди пожилого возраста от 65 лет. Чем старше человек, тем выше шанс развития данного заболевания. В возрастной группе от 80 до 85 лет насчитывается до 40% пострадавших. Такой вид деменции носит дегенеративный характер и не поддается лечению. Процесс разрушения клеток мозга в скором времени проявится в виде слабоумия, а самолечение без профессионального осмотра может усугубить положение.
Диагностировать болезнь самостоятельно на раннем этапе не предоставляется возможным. А откладывание похода к врачу может отрицательно сказаться на состоянии больного из-за высокой скорости развития этого вида деменции. Для точного определения диагноза необходимо применение специальной аппаратуры и консультации врачей-неврологов. Специально подготовленные тесты помогут установить причины заболевания и сформировать оптимальный курс лечения. Такие условия предлагает Юсуповская больница. Качественная помощь от ведущих врачей позволит сдерживать патологические процессы, что даст больному возможность вести нормальный образ жизни.
Симптомы и признаки болезни Альцгеймера
Признаки Альцгеймера прогрессируют медленно. Первые симптоматические проявления деменции появляются задолго до подтверждения диагноза. Выделяют четыре стадии недуга.
- Предеменция. Обнаруживается сложно, так как ее можно ошибочно принять за стресс. Человек испытывает чувство усталости, снижается память (больной не может запомнить список из нескольких наименований, плохо усваивает информацию), исчезает интерес к жизни, появляется замкнутость и апатия.
- Ранняя деменция. Симптоматика осложняется дефектами речи: забываются названия предметов быта, снижается скорость речи, сокращается словарный запас, происходит путаница похожих слов, ухудшается почерк. Именно в это время больной обращается в клинику.
- Умеренная деменция. Характеризуется затруднениями в построении логических связей. Человек одевается не по погоде, теряется в пространстве, не помнит, как дойти домой, не знает свой адрес, забывает родных и себя самого. Появляется плаксивость, агрессия, нарушается долговременная память.
- Тяжелая деменция. Человек полностью деградирует, он не способен управлять физиологическими процессами в организме, не в состоянии самостоятельно принимать пищу.
С таким диагнозом при правильном уходе человек может дожить до глубокой старости. В России и в зарубежных странах для таких пациентов существуют специальные клиники и пансионаты, где больным помогают адаптироваться, вспомнить элементарные навыки самообслуживания.
Признаки болезни Альцгеймера на ранней стадии
Ранние симптомы болезни Альцгеймера не всегда заметны, чаще на них не обращают внимания. К ним относят:
- речевые изменения — фразы плохо связываются между собой, язык становится бедным, а разговор пустым;
- длительный сон — значительно усугубляет проблемы с памятью, очень важно при таком заболевании, чтобы ночной сон длился не более 6-7 часов;
- поведенческие изменения — у человека меняется характер, привычки, возникают трудности с принятием решения и планированием дня;
- нечувствительность к боли — сильную болезненность пациент описывает как легкий дискомфорт;
Признаки болезни Альцгеймера в пожилом возрасте
Люди преклонного возраста часто скрывают наличие проблем со здоровьем, поэтому стоит обратить внимание на:
- кратковременную память: как часто пожилые люди забывают информацию, теряют вещи или не помнят, где они лежат;
- бессонницу ночью и сонливость днем;
- нетвердую походку;
- утрату интереса к привычным и любимым занятиям: рыбной ловле, вязанию, вышиванию;
- проблемы с разговорной и письменной речью: значимые слова замещаются местоимениями, мозг теряет способность четко мыслить — отмечаются пространные размышления;
- изменения в характере: излишняя подозрительность, нервозность, навязчивые поучения;
- гипертрофированное чувство доверчивости и наивность толкают больных Альцгеймером на необдуманные поступки (могут отдавать деньги мошенникам);
- неаккуратный внешний вид.
На первых этапах развития недуга пожилые люди не требуют постоянного контроля и внимания. Когда симптоматика прогрессирует, а признаки деменции усугубляются, пациентам необходим специальный уход.
Симптомы болезни Альцгеймера у молодых
Склонность к развитию заболевания можно определить после прохождения молекулярно-генетического анализа. Научно доказано существование пяти основных участков в геноме человека, провоцирующих проблемы с обменом веществ и несущих смерть нейронам. Они располагаются на 1, 12, 14, 19 и 21 хромосомах. Мутационные изменения на этих участках способствуют накоплению отрицательного амилоида и тау-белка.
У ребенка с генными аномалиями такого плана часть мозга, отвечающая за память, меньше на 6%, чем у здорового малыша. Со временем эта часть уменьшается до критической отметки.
Наличие синдрома Дауна у ребенка значительно увеличивает риск развития Альцгеймера, симптоматика обнаруживается не сразу в связи со спецификой первичного заболевания. Такие дети изначально отстают в развитии, у них плохая память, внимание, низкая адаптация.
У детей с синдромом Дауна быстрей происходит старение организма, соответственно, изменения в области головного мозга выступают подстегивающим фактором. Практически у всех таких детей по достижению 40 лет диагностируется Альцгеймер.
Признаки Альцгеймера у женщин
По статистическим данным женская часть населения больше подвержена сенильному слабоумию, чем мужчины, большинство из которых просто не доживают до 70-80 лет. У женщин после менопаузы снижается выработка эстрогена, который способствует регулировке метаболизма в мозге. Поэтому их организм больше склонен к накапливанию отрицательных веществ, несущих смерть нейронам.
Признаки Альцгеймера у мужчин
Ранние признаки болезни Альцгеймера у представителей полов отличаются:
- женщины испытывают проблемы с памятью, вниманием, реакцией, логическими связями между предметами;
- мужчины первоначально сталкиваются с речевыми отклонениями и затруднениями в движениях и моторике.
Эти данные предоставила исследовательская группа на Международной конференции в Торонто. Было обследовано более 1000 человек, посмертная экспертиза которых указала на некоторые расхождения в симптоматике.
Прогноз болезни Альцгеймера
Значительная часть пациентов живет от 5 до 14 лет. Поэтому очень важно выявить патологию на раннем этапе развития, что поможет увеличить срок жизни до максимально возможной отметки.
С помощью специальных методик и лекарственных препаратов можно сдерживать аномальные изменения в тканях головного мозга и улучшить качество жизни.
Диагностика
Стоит выделить основные методы обследования пациентов с подозрением на сенильное слабоумие.
- Нейропсихологические тесты. Они заключаются в выполнении определенных действий, направленных на способность запоминания, пересказ прочитанного, несложные вычисления. Проверяется степень ориентирования во времени и пространстве.
- Магнитно-резонансная томография (МРТ) предоставляет более точные данные, определяет зоны и площадь поражения участков в головном мозге, а именно присутствие бляшек, структурные нарушения. Для установления динамики дегенеративных нарушений МРТ проводят до трех раз с перерывами в месяц.
- Компьютерная томография (КТ) — назначается редко и только тогда, когда площадь поражения отчетливо заметна.
- Позитронно-эмиссионная томография (ПЭТ) — современный способ диагностики, с его помощью можно выявить заболевание на стадии предеменции.
- Электроэнцефалография (ЭЭГ) — назначается по необходимости.
- Лабораторные процедуры — сдается анализ крови (общий, биохимический), а также выявляется наличие генных мутаций.
Специалисты отмечают, что при наличии сопутствующих недугов — сахарного диабета, высокого уровня холестерина в крови, артериальной гипертензии — течение Альцгеймера прогрессирует более стремительно.
Лечение
Доступные методы терапии не могут излечить Альцгеймер, они способны лишь улучшить качество жизни больного, снизить симптоматические проявления.
Чаще всего назначают мемантин и антихолинэстеразные средства. С их помощью можно поддержать защиту нейронов от гибели. Есть несколько побочных эффектов: сильные приступы головной боли, головокружение, галлюцинации.
Ингибиторы холинэстеразы никак не показали себя, кроме того, что на фоне их приема происходит снижение веса, появление гастрита и мышечных спазмов. Они не замедляют течение недуга и не укрепляют здоровье.
Если поведение пациента агрессивное и антисоциальное, то ему назначают антипсихотики, но их стоит принимать только в крайних случаях. По данным медицинских исследований, их прием может привести к двигательным расстройствам, снижению когнитивной функции, также они в разы повышают смертность.
К психосоциальным методам лечения стоит отнести арт-лечение, которое направлено на полное расслабление. Такая терапия помогает пациенту успокоиться, снижает агрессию, улучшает концентрацию и настрой.
Профилактика и прогноз
Болезнь Альцгеймера в преклонном возрасте прогрессирует медленно — от 5 до 14 лет, если обнаруживается раньше (в 40 лет), развивается стремительно. В этом случае третий-четвертый этап наступает на второй год после подтверждения диагноза. Однако правильно подобранное лечение может продлить жизнь такого больного до 10 лет.
Замедлить развитие симптоматических проявлений помогу следующие мероприятия:
- здоровый образ жизни;
- качественное и сбалансированное питание;
- занятия спортом (лечебная гимнастика, йога, бег, пешие прогулки, плавание);
- интеллектуальный труд.
Ученые доказали: чем выше показатели IQ, тем больше количество устойчивых нейронов. Человеку с генетической предрасположенностью следует тренировать память, мышление, логику. В этом хорошо помогают ребусы, головоломки, кроссворды, живое общение, наличие интересов. Стоит начать играть в шахматы.
Следует полностью пересмотреть свою жизнь, отказаться от вредных привычек, отдавать предпочтение здоровой пище (с высоким содержанием Омега-3), следить за весом и уровнем холестерина в крови.

Болезнь Альцгеймера является нейродегенеративным заболеванием, различные патогенетические е аспекты которого все еще исследуются. Это расстройство характеризуется прогрессирующим снижением когнитивных функций и потерей определенных типов нейронов и синапсов. Наиболее узнаваемыми патологическими находками при болезни Альцгеймера являются амилоидные бляшки и нейрофибриллярные клубки. Амилоидные бляшки представляют собой внеклеточные скопления аномально свернутых амилоидных бета-белков (Aβ) с 40 или 42 аминокислотами (Aβ40 и Aβ42), двумя побочными продуктами метаболизма белка-предшественника амилоида (APP). Нейрофибриллярные клубки в основном состоят из парных спиральных нитей, состоящих из гиперфосфорилированных тау, белковых стабилизирующих микротрубочек. Этиология болезни Альцгеймера многофакторная. Существуют спорадические формы и семейные формы, связанные с мутациями в трех генах: APP, пресенилин 1 (PSEN1) и пресенилин 2 (PSEN2). Семейные формы встречаются реже (<0,5%) по сравнению со спорадическими формами. В настоящее время считается, что генетические факторы и факторы окружающей среды взаимодействуют между собой , вызывая начало болезни Альцгеймера .
Недавно было высказано предположение, что болезнь Альцгеймера может быть связано с дисбиозом микробов в кишечнике. Действиетльно , фактически кишечная флора способна влиять на деятельность мозга и вызывать его дисфункции. Антибиотики обычно используются для удаления или предотвращения бактериальной колонизации в организме человека, без воздействия на конкретные типы бактерий. В результате своего действия антибиотики широкого спектра действия могут значительно повлиять на состав кишечной микробиоты, уменьшить ее биоразнообразие и задержать колонизацию на длительный период после своего введения. Таким образом, действие антибиотиков при болезни Альцгеймера может быть широким и даже противоположным по своему эффекту. Изменение микробиоты кишечника может вызывать изменения в деятельности мозга, что повышает вероятность терапевтических манипуляций с микробиомом при болезни Альцгеймера и других неврологических расстройствах.
Способ, которым микробиота кишечника регулирует , MGBA может быть различного рода. Эти микроорганизмы способны синтезировать и высвобождать нейротрансмиттеры и нейромодуляторы, такие как жирные кислоты с короткой цепью (SCFA), биогенные амины (например, серотонин, гистамин и дофамин) и другие метаболиты аминокислот, такие как серотонин илигамма - аминомаслянную кислоту ( ГАМК) и триптофан. Все эти молекулы действуют как нейротрансмиттеры или как предшественники нейротрансмиттеров в мозге и регулируют активность нейронов. Тем не менее, все еще существует необходимость в более надежных экспериментальных доказательствах, чтобы доказать, что изменения кишечной микробиоты ответственны за изменения в поведении. Многие исследования действительно подтверждают эту корреляцию, но не доказывают прямую причинно-следственную связь.
Другая возможность уже негативного влияния заключается в том, что кишечная микробиота продуцирует токсичные вещества для мозга. Микробиота кишечника может выделять нейротоксичные вещества, такие как d- молочная кислота и аммиак. Кроме того, в процессе воспаления кишечная микробиота выделяет другие белки, потенциально вредные для мозга, такие как провоспалительные цитокины и другие врожденные активаторы иммунной системы у хозяина. Результат этих процессов может привести к ухудшению памяти, усилению тревоги и других когнитивных дисфункций. Согласно последним исследованиям, изменения в микробиоте кишечника связаны с различными неврологическими заболеваниями, которые включают не только расстройства тревожного и депрессивного спектра, но также нейродегенеративные заболевания или резистентную к терапии эпилепсию. Среди нейродегенеративных заболеваний имеются данные исследований о возможном участии дисбиоза кишечника в патогенезе болезни Альцгеймера, болезнях Паркинсона и Хантингтона и рассеянном склерозе.
Согласно гипотезе амилоидного каскада, эти отложения приводят к синаптической дисфункции и лежат в основе клинических симптомов деменции, наблюдаемой при болезни Альцгеймера. Тем не менее, эта гипотеза была оспорена из-за неоднократных неудач в клинических испытаниях с препаратами, нацеленными на Aβ . Стало очевидным, что Aβ-дисгомеостаз предшествует изменениям в других белках и различных типах клеток, которые вносят свой вклад в когнитивный фенотип болезни Альцгеймера. Роль активации микроглии в ответ на отложение Aβ стала важным фактором в патогенезе болезни Альцгеймера. Некоторые гены, кодирующие белки врожденного иммунного ответа, были определены как ключевой элемент патогенеза этого психического расстройства. Среди них рецептор комплемента 1 , CD33, и TREM2, по-видимому, прямо или косвенно участвуют в ответе микроглии на отложение Aβ. Как показано на моделях трансгенных животных, изменения этих генов приводят к дисфункциональному ответу микроглии, которая не может сгруппироваться вокруг бляшек Aβ.
Последние данные указывают на то, что сам Aβ, хотя он раннее считался провоспалительным пептидом, по-видимому, обладает "врожденной" противомикробной активностью. Эти данные позхволяют предположить , что нейровоспалительные процессы могут быть причиной, а не следствием нейродегенеративных процессов при болезни Альцгеймера. Тем не менее, пока не ясно, является ли воспаление первичным явлением при болезни Альцгеймера , поскольку многие исследования показали, что отложение Аβ может предшествовать микроглиозу. Последние гипотезы предполагают, что в мозге пациентов с болезнью Альцгеймера существует порочный круг между накоплением Aβ и активацией микроглии и , что вызванное микроглией нейровоспаление может быть мишенью для разработки лекарств против болезни Альцгеймера. В связи с этим возникает идея, что изменение микробиоты кишечника, состояние, называемое дисбиозом, может быть одним из факторов, способствующих нейровоспалительным процессам, наблюдаемым при болезни Альцгеймера.
Были предложены некоторые теории патогенеза нейропсихиатрических расстройств , основанные на роли кишечной микробиоты, включая прямое действие этих микробов (микробная инфекция ) , косвенные действия (гипотеза антимикробной защиты, гигиеническая гипотеза), и гипотеза , касающаяся процессов, связанных со старением иммунной системы. В связи с этим важное значение имеют исследования с использованием патогенов грызунов, так называемых "свободных от микробов". У этих животных наблюдалось значительное снижение патологии Aβ, которая снова появляется, когда мыши подвергаются воздействию микробиоты кишечника контрольных мышей. Было показано, что хроническая инфекция Helicobacter ( H. ) pylori у пациентов с болезнью Альцгеймера вызывает высвобождение медиаторов воспаления и связана со снижением показателя MMSE по сравнению с неинфицированными пациентами. Более того, сывороточные уровни Aβ40 и Aβ42 выше у пациентов с болезнью Альцгеймера , инфицированных H. pylori и другими бактериями, такими как Borrelia burgdorferi и Chlamydia pneumoniae. . В клетках нейробластомы было также продемонстрировано, что воздействие H. pylori фильтрата индуцирует гиперфосфорилирование тау, сходное с тем, которое наблюдается при патологии тау при болезни Альцгеймера.
Все эти бактерии могут действовать синергично, вызывая инфекции в головном мозге пациентов с болезнью Альцгеймера. В лизатах гиппокампа и височной доли головного мозга пацеинтов с болезнью Альцгеймера наблюдались высокие уровни бактериального липополисахарида. Анализ крови у пациентов с амилоидозом головного мозга и когнитивными нарушениями также выявил повышение уровня провоспалительных цитокинов, а также повышение уровня провоспалительных ( Escherichia / Shighella ) и снижение противовоспалительных ( Escherichia rectale ) кишечных микробов . Вирусная инфекция также была предположена для описания процессов патогенеза болезни Альцгеймера. В частности, многие исследования показали, что вирус простого герпеса типа 1 (HSV1) представляет собой важный фактор риска для развития заболевания, особенно для носителей ApoE-ε4. Другие вирусы, такие как цитомегаловирус (ЦМВ) и вирус ветряной оспы, также были связаны с болезнью Альцгеймера, хотя роль этих вирусов как отдельных факторов риска данного психического расстройства неясна.

Гипертония, диабет 2 типа и ожирение - все это хорошо известные факторы риска деменции .
Колебания артериального давления
Даже небольшое повышение артериального давления в среднем возрасте связано с повышением риска деменции на 30% два десятилетия спустя. Но прием лекарств от артериального давления может помочь людям избежать этого риска, согласно исследованию, опубликованному 19 мая 2020 года в JAMA .
Как краткосрочная, так и долгосрочная изменчивость артериального давления вызывает или отражает патологические состояния, связанные с когнитивным снижением и деменцией. Поскольку известно, что вариабельность артериального давления связана со смертностью, ишемической болезнью сердца, инсультом и терминальной стадией почечной недостаточности. Вероятно, гемодинамическая нестабильность приводит к воспалению, эндотелиальной дисфункции и окислительному стрессу с последующим повреждением структуры и функции мозга. Следовательно, колебания артериального давления могут быть пагубными для нервных клеток, приводя к гибели клеток и атрофии гиппокампа из-за гипоперфузии головного мозга и болезни мелких сосудов. Также предполагается, что центральная вегетативная дисфункция может сопровождать деменцию, что может способствовать ухудшению вариабельности артериального давления и уровня глюкозы
Колебания и высокие уровни глюкозы и гликированного гемоглобина
Вариабельность уровня глюкозы и HbA1c, отражающая краткосрочные и долгосрочные колебания гликемии, связана с различными осложнениями у пациентов с диабетом как 1-го, так и 2-го типа. Было показано, что колебания уровня глюкозы в большей степени, чем постоянная гипергликемия, влияют на функцию эндотелия, адгезию моноцитов и окислительный стресс у людей, а также исследования in vitro. Это может быть связано с гиперактивацией киназы-3β гликогенсинтазы и гиперфосфорилированием тау-белка, ассоциированного с микротрубочками, что приводит к нарушению функции нейронов
Из клинической практики известно, что более высокие уровни глюкозы в крови ли массы тела связана с умеренными когнитивными нарушениями, болезнью Альцгеймера и деменцией, что указывает на новый путь лечения этого нейродегенеративного расстройства и профилакти в плане изменение риска. Полагают, что деменция тесно связана с дисгликемией и инсулинорезистентностью в центральной нервной системе и деменция даже упоминается в литературе , как диабет 3 типа.
Увеличение веса
Изменчивость массы тела и связанная с ней дисфункциональная продукция определенных гормонов может отрицательно сказаться на здоровье мозга. Например, более высокие уровни лептина связаны с более низким риском деменции
Биохимические показатели и прогрессирование болезни Альцгеймера
Полагаю, что читателю моего Блога, особенно, неврологам и психиатрам будут интересны некоторые параллели между выраженностью когнитивных нарушений при болезни Альцгеймера и некоторыми изменениями биохимических показателей . Ниже представлены сравнительные аспекты исследований , проведенных в нашей клиники ( ООО "Психическое здоровье" ) с данными , ряда зарубежных исследований.
Высокие уровни липопротеидов высокой плотности (ЛПВП), витамина D и фолиевой кислоты коррелируют с оценками когнитивных функций, в то время как высокие уровни общего холестерина, HbA1c, ЛПНП отрицательно влияют на оценки когнитивных функций. Показатели MMSE обратно коррелируют с возрастом, уровнями tHcy ( гомоцистеина ) в плазме и холестерина и липопротеинов низкой плотности (ЛПНП.) Однако после корректировки на возраст, пол и статус лечения статинами сохранялась только обратная связь между оценками MMSE и уровнями холестерина , ЛПНП. Уровни tHcy в плазме значительно увеличиваются с возрастом и обратно пропорциональны уровням витамина B (12) и фолиевой кислоты, что изменяет взаимосвязь между оценками MMSE и уровнями tHcy в плазме.
Отметим, что более высокая вариабельность холестерина связана с более низким мозговым кровотоком и большей гиперинтенсивной нагрузкой на белое вещество. Это может быть опосредовано эндотелиальной дисфункцией или нестабильностью бляшки в результате повторяющихся колебаний в составе атеросклеротических бляшек, которые могут вызывать цереброваскулярное повреждение.

Уровни биохимических маркеров периферической крови, включая альбумин, щелочную фосфатазу, аланинаминотрансферазу (АЛТ), аспартатаминотрансферазу (АСТ) и общий билирубин, используются для оценки функции печени. Возможно, что аминотрансферазы являются суррогатными биомаркерами метаболического функционирования печени. Печень является основным метаболическим центром; следовательно, изучение связи функции печени с биомаркерами когнитивных функций, результататми нейровизуализации и исследований спинномозговой жидкости (CSF) улучшило бы понимание роли метаболической дисфункции при болезни Альцгеймера
Данные многочисленных исследований свидетельствует о важной роли функции печени в патогенезе болезни Альцгеймера (AD). Измененные ферменты печени приводят к нарушениям в связанных с печенью метаболитах, включая аминокислоты с разветвленной цепью, эфирные фосфатидилхолины и липиды.
Увеличение значений отношения AST к ALT и более низкие уровни ALT показали постоянную значительную связь со сниженным метаболизмом глюкозы в мозге, особенно в орбитофронтальной коре и височных долях - участках мозга, вовлеченных в процессы памяти и нарушения исполнительного функционирования. Гипометаболизм глюкозы в мозге является ранним признаком болезни Альцгеймера и когнитивных нарушений на продромальной стадии этого нейродегенеративного расстройства. Кроме того, ALT и AST являются ключевыми ферментами в глюконеогенезе в печени и производстве нейротрансмиттеров, необходимых для поддержания синапсов. Аланинаминотрансфераза катализирует обратимую реакцию трансаминирования между аланином и α-кетоглутаратом с образованием пирувата и глутамата, в то время как AST катализирует обратимую реакцию между аспартатом и α-кетоглутаратом с образованием оксалоацетата и глутамата. Снижение уровня АLT приводит к снижению уровня пирувата, который необходим для производства глюкозы через глюконеогенез в печени, а глюкоза распределяется в различных тканях организма в качестве источника энергии. Таким образом нарушается энергетический гомеостаз. Кроме того , измененные уровни ALT и AST могут влиять на уровни глутамата - возбуждающего нейротрансмиттера центральной нервной системы, участвующего в синаптической передаче, который также играет важную роль в процессах памяти. В случае низкого метаболизма глюкозы в мозге через цикл трикарбоновых кислот доступно меньшее количество α-кетоглутарата, что способствует катаболизму глутамата по сравнению с синтезом глутамата в обратимой реакции (катализируемой AST и ALT). Глутамат действует как нейромедиатор примерно в двух третях синапсов в неокортикальных и гиппокампальных пирамидных нейронах и, таким образом, участвует в процессах памяти и других когнитивных функциях через длительное потенцирование. В выборке здоровых взрослых уровни ALT и AST в плазме достоверно коррелировали с уровнями глутамата в плазме, что указывает на то, что более низкие уровни ALT будут снижать уровни глутамата в плазме.
Отметим, что у пожилых людей более низкие уровни АLT в сыворотке связаны со смертностью и считаются биомаркером для повышения хрупкости, саркопении и / или снижения уровня пиридоксина (витамин B6). Пиридоксинфосфат является коферментом для синтеза аминокислот, нейротрансмиттеров (например, серотонина и норэпинефрина) и сфинголипидов. Аланин аминотрансфераза уменьшается с 63 лет и может быть признаком старения печени. Уровень глутамата также снижается с возрастом.
Повышенные отношения AST к ALT наблюдаются у людей с неалкогольной жировой болезнью печени, которая является печеночным проявлением метаболического синдрома. В исследовании Framingham Heart Study безалкогольное жировое заболевание печени было связано с меньшим общим объемом мозга, даже после корректировки на несколько сердечно-сосудистых факторов риска. Дисфункция печени также связана с развитием заболеваний, включая сердечно-сосудистые заболевания и резистентность к инсулину, из-за нарушений метаболизма глюкозы и липидов, основных физиологических функций печени. Таким образом, используя отношение AST к ALT в качестве маркера общего метаболического нарушения, наше исследование предоставляет доказательства связи между измененным метаболическим статусом и AD, когнитивными и AD эндофенотипами. В дополнение к уровням ALT и отношению AST к ALT, повышенные уровни щелочной фосфатазы были в значительной степени связаны с плохой когнитивной функцией. Щелочная фосфатаза - это фермент, который в основном экспрессируется в печени и почках, а также в эндотелиальных клетках головного мозга. Нейронная форма щелочной фосфатазы играет роль в развитии пластичности и кортикальных функций, зависящих от активности, внося свой вклад в метаболизм γ-аминомасляной кислоты. Изменения уровня щелочной фосфатазы в плазме могут возникнуть в результате повреждения центральной нервной системы. Это согласуется с результатами Оксфордского проекта по изучению памяти и старения, в котором сообщалось о повышении уровня щелочной фосфатазы у людей с болезнью Альцгеймера и обратной связи с состоянием когнитивной сферы .
Результаты исследований показывают, что сниженные уровни ALT и повышенное отношение AST к ALT, которые наблюдались у пациентов с AD, связаны с плохим когнитивным функционированием. Исследователи также обнаружили, что повышенное отношение AST к ALT было связано с более низкими уровнями амилоида-β 1-42 в CSF, большим отложением амилоида-β и более высокими уровнями p-tau и t-tau CSF. Кроме того, авторы исследований наблюдали, что сниженные уровни ALT были связаны с более сильным отложением амилоида-β и структурной атрофией.
Что такое болезнь Альцгеймера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Полякова Т. А., невролога со стажем в 13 лет.
Над статьей доктора Полякова Т. А. работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Болезнь Альцгеймера — это хроническое нейродегенеративное заболевание, с медленным началом и значительным ухудшением с течением времени. В 70 % случаев болезнь Альцгеймера приводит к деменции.
Этиология. Факторы риска
Заболевание на данный момент изучено плохо. Предполагается, что в 70% случаев болезнь Альцгеймера объясняется генетическими причинами, среди других факторов риска — черепно-мозговые травмы, депрессия, эндокринные заболевания в анамнезе (гипотиреоз), эстрогенная недостаточность у женщин.
Сопутствующие заболевания
Исследования последних лет показывают, что усиливают предрасположенность к болезни Альцгеймера гипертония, гиперлипидемия, гипергомоцистеинемия, сахарный диабет, метаболический синдром, инсулинорезистентность, заболевания сердца, а также наличие в истории болезни инсульта [1] .
Статистические данные
Болезнь Альцгеймера — наиболее распространённая форма деменции, она встречается в 60–70 % случаев. В мире деменцией страдают около 50 миллионов человек, каждый год выявляется 10 миллионов новых случаев [12] .
В развитых странах болезнь Альцгеймера является одним из наиболее дорогостоящих заболеваний. В России затраты на содержание больных деменцией составляют 74,8 млрд рублей в год [2] .
Распространённость и факторы риска
Заболевание более распространено среди женщин. Предположительно, это связано со следующими факторами:
- продолжительность жизни женщин больше, чем мужчин, а возраст — самый значимый фактор риска развития болезни Альцгеймера;
- риск развития болезни увеличивается на 70 % для людей с депрессией, у женщин она встречается чаще;
- более низкий уровень образования связан с повышенным риском деменции, в некоторых странах у женщин уровень образования ниже, чем у мужчин;
- при беременности часто возникают гипертонические расстройства, они связаны с повышенным риском ухудшения когнитивных функций даже спустя десятилетия после беременности [13] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы болезни Альцгеймера
Признаки болезни Альцгеймера на ранней стадии часто ошибочно принимаются за нормальные признаки старения.
Кратковременная потеря памяти — наиболее распространенный ранний симптом болезни Альцгеймера, который выражается в том, что больному трудно запоминать последние события. В трети случаев заболевание можно распознать по изменениям поведения.
По мере усугубления болезни возникают следующие симптомы:
- проблемы с речью;
- дезориентация;
- перепады настроения;
- потеря мотивации;
- снижение критики;
- больные не в состоянии вспомнить нужное слово, и им приходится заменять его другим (парафазии), однако они хорошо повторяют сказанное.
- со временем возникают затруднения при назывании предметов (аномии).
- уже на ранней стадии возникают трудности с пониманием сложных грамматических структур (семантическая афазия), к которому затем присоединяется отчуждение смысла слова. [3]
Важный признак болезни Альцгеймера — нарушение способности справляться с повседневностью. При заболевании возникают проблемы с самообслуживанием и поведенческие расстройства.
Признаки болезни Альцгеймера у мужчин и женщин
Признаки болезни Альцгеймера у женщин и мужчин схожи, однако у женщин она чаще сопровождается депрессией.
Патогенез болезни Альцгеймера
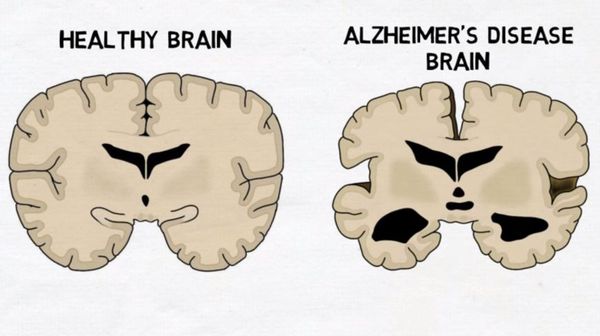
Существуют отличительные патоморфологические признаки болезни Альцгеймера: амилоидные (сенильные) бляшки — это внеклеточные отложения в виде скопления фрагмента белка, называемые бета-амилоидом; нейрофибриллярные клубочки — скрученные микроскопические нити тау-белка внутриклеточной локализации. Происходит потеря связи между клетками мозга, ответственными за память, обучение и общение. Эти соединения, или синапсы, передают информацию из клетки в клетку. Важная роль в патогенезе принадлежит воспалительному процессу, связанному с активацией микроглии, которая инициируется накоплением амилоида. [1]
Патофизиология болезни Альцгеймера:
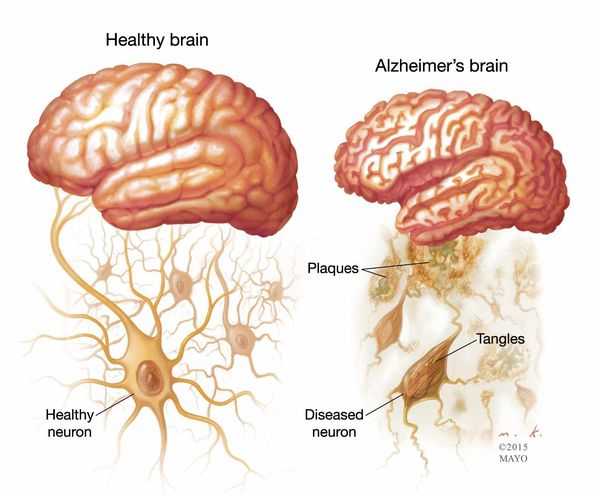
Макроскопически выявляется диффузная атрофия головного мозга с уменьшением объёма извилин и расширением боковых борозд, наиболее выраженная в височно-теменной области.
У значительной части больных цереброваскулярная патология может инициировать или усиливать дегенеративный процесс, связанный с отложением амилоида или другими характерными для заболевания изменениями.
Классификация и стадии развития болезни Альцгеймера
Типичный фенотип болезни Альцгеймера — сочетание выраженных мнестических нарушений гиппокампального типа с акустико-мнестической афазией, зрительно-пространственными нарушениями и апраксией. [3]
Три атипичных фенотипа болезни Альцгеймера (неамнестических):
- с ведущим афатическим дефектом (логопенический вариант первичной прогрессирующей афазии);
- с доминирующими зрительно-пространственными нарушениями (задняя корковая афазия);
- преимущественно с дизрегуляторными нарушениями (лобный вариант болезни Альцгеймера).
Заболевание также подразделяется на формы с ранним началом, зачастую с положительным семейным анамнезом (до 65 лет) и поздним началом (старше 65 лет). Они отличаются патогенезом, генетическими факторами и разной скоростью прогрессирования.
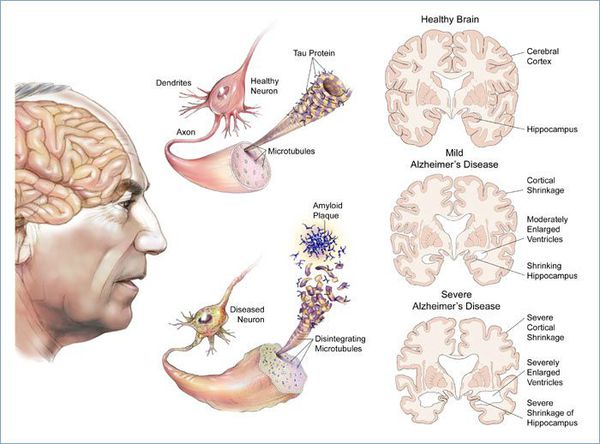
Три стадии болезни Альцгеймера:
Первая (предеменция, ранняя деменция): больные обслуживают себя сами, но им нужна помощь для решения финансовых вопросов, приготовления пищи и т. д.
Вторая (умеренная деменция): зависимость от посторонней помощи растет — больные не способны самостоятельно одеться, осуществить гигиенические процедуры, долго оставаться дома без присмотра.
Третья (тяжёлая деменция): больные не могут выполнить ни одно из привычных повседневных действий без помощи других людей.
Переход от одной стадии к другой коррелирует со снижением оценки по MMSE (Краткая шкала психического статуса), которая является надежным инструментом для отслеживания динамики заболевания.
Осложнения болезни Альцгеймера
Продолжительность жизни людей с болезнью Альцгеймера после установления диагноза обычно колеблется от трех до десяти лет. Более четырнадцати лет после установления диагноза живут менее 3% больных. Уменьшение выживаемости связано с тяжелыми когнитивными нарушениями, снижением уровня физической активности, частыми падениями и нарушениями в неврологическом статусе. Сопутствующие соматические заболевания также влияют на продолжительность и качество жизни при болезни Альцгеймера. Пневмония и обезвоживание — наиболее частые непосредственные причины смерти, вызванной болезнью Альцгеймера. Кроме того, чем старше возраст, тем выше общий возраст выживаемости. У мужчин прогноз менее благоприятен по сравнению с женщинами.
Диагностика болезни Альцгеймера
Трудности ранней диагностики болезни Альцгеймера во многом объясняются "маскированным" характером заболевания в этот период, когда отсутствуют явные внешние признаки деменции. Для постановки диагноза, определения тактики ведения пациента необходимо выявить характер и выраженность когнитивных нарушений.
Нейропсихологический тест
Основной метод оценки когнитивных функций — нейропсихологическое обследование, которое проводит врач, обученный данным методам исследования. В некоторых странах практикуется обследование больных их родственниками с помощью шкал для оценки когнитивных функций: монреальской когнитивной шкалы, Адденбрукской, шкала краткого исследования психических функций MMSE.
Биомаркеры болезни Альцгеймера
Молекулярная диагностика на ранней стадии заболевания также создаёт перспективы для раннего назначения лечения болезни Альцгеймера. Определение биомаркеров в плазме является менее инвазивной альтернативой для диагностики болезни Альцгеймера. Биомаркеры классифицируются на биомаркеры накопления амилоида и биомаркеры нейродегенерации. Основные биомаркеры отражают патологию амилоида (внеклеточное накопление Aβ1-40/1-42) или внутриклеточные включения нейрофибриллярных клубочков (гиперфосфорилированного тау). [4] [5]
Согласно рекомендациям 4-го Канадского консенсуса по диагностике и лечению деменции и рациональному использованию биомаркеров для диагностики болезни Альцгеймера и других деменций (CCCDTD4, 2011): [6]
1. Определение биомаркеров цереброспинальной жидкости не рекомендуются для диагностики болезни Альцгеймера с типичной клинической картиной (2А уровень).
2. Исследование биомаркеров не рекомендуется для скрининга здоровых людей с целью оценки риска развития болезни Альцгеймера в будущем (уровень 1В).
3.Биомаркеры цереброспинальной жидкости можно рассматривать в особых случаях, когда есть атипичные признаки или диагностические трудности при дифференциальной диагностике лобного варианта болезни Альцгеймера от лобно-височной деменции, а также случаи первично прогрессирующей афазии как следствие болезни Альцгеймера или лобно-височной дегенерации (уровень 2В).
МРТ и КТ головного мозга
Современные методы нейровизуализации — магнито-резонансная томография и компьютерная томография головного мозга — позволяют расширить диагностические возможности прижизненной диагностики болезни Альцгеймера.
МРТ и КТ проводят для выявления поддающихся лечению причин деменции и нарушений, которые могут усугубить симптомы. Структурные изменения по данным магнитно-резонансной томографии являются более прогностически значимыми для дальнейших изменений в когнитивной сфере, чем биомаркеры цереброспинальной жидкости. По данным магнитно-резонансной томографии, признаки цереброваскулярного заболевания, такие как лейкоареоз и множественные подкорковые лакунарные инфаркты, чаще наблюдаются у пациентов с болезнью Альцгеймера, чем в контрольной группе. [7] Асимметричная атрофия медиальных отделов височной доли также не исключает сосудистую деменцию.
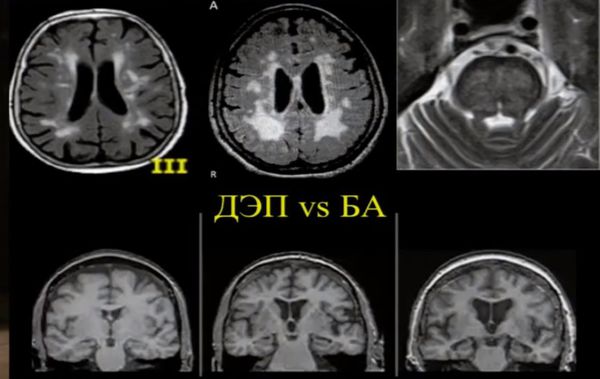
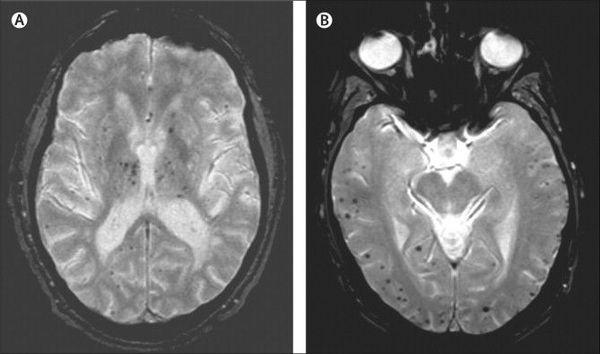
Описана смешанная модель патогенеза болезни Альцгеймера, которая предполагает взаимодействие церебральной амилоидной ангиопатии с сосудистыми факторами на ранних стадиях патологического процесса. Предполагается, что синергия между накоплением амилоида и цереброваскулярной патологией может инициировать дальнейшую дисфункцию нейронов и нейродегенерацию. [8] В этом отношении церебральные микрокровоизлияния, выявляемые в режиме Т2 градиентного эхо на магнитно-резонансной томографии, являются дополнительным и доступным диагностическим маркером, повышающим диагностическую значимость лейкоареоза и свидетельствующим в пользу церебральной амилоидной ангиопатии или гипертонической микроангиопатиии, особенно в случаях смешанной патологии и тяжелого когнитивного дефицита.
Локализация церебральных микрокровоизлияний является дифференциально-диагностическим признаком ведущего патологического процесса. В случае болезни Альцгеймера наблюдается корковая локализация микрокровоизлияний, в случае дисциркуляторной энцефалопатии или сосудистой деменции будут визуализироваться микрокровоизлияния в глубинных отделах мозга. [9] [10]
Одним из наиболее перспективных методов диагностики болезни Альцгеймера является позитронно-эмиссионная томография с лигандом, который связывается с амилоидом (PiB), однако накопление амилоида и захват соответствующего лиганда нарастают на стадии умеренных когнитивных нарушений, но после конверсии в деменцию дальнейшего накопления не происходит. [11]
Лечение болезни Альцгеймера
Болезнь Альцгеймера пока не поддается лечению. Но благодаря группе новых препаратов и симптоматическому лечению Альцгеймера можно сделать так, что снижение интеллекта больных будет более постепенным.
Лекарства
К таким средствам относятся:
- ингибиторы холинэстеразы (донепезил, ривастигмин, галантамин)
- блокаторы NMDA-глутаматных рецепторов (акатинол-мемантин).
Облегчение расстройств психики и поведения, сопровождающих болезнь Альцгеймера
С целью лечения сопутствующих расстройств психики и поведения используются также антидепрессанты и нейролептики.
Поддерживающие методы
Существуют и нелекарственные методы воздействия — тренировки интеллектуальных функций. Нейропсихологическая реабилитация позволяет стимулировать к развитию новых нейронный сетей, обучая рабочие нервные клетки.
Специальная диета при болезни Альцгеймера не требуется: питание не влияет на развитие заболевания.
Прекращение лечения
Причиной для прекращения приёма антидементных препаратов может стать выраженная брадикардия, но это осложнение возникает крайне редко.
Рекомендации для ухаживающих за близкими с болезнью Альцгеймера
При уходе за больным человеком важно организовать для него безопасное и удобное пространство.
Также важно внимательно выбирать обувь и одежду.
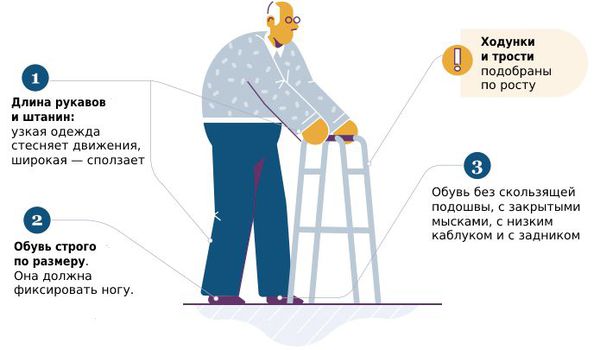
Такими занятиями могут быть:
- прогулки;
- общение с домашними животными;
- уход за растениями;
- наблюдения за рыбками в аквариуме;
- прослушивание радиопередач и музыки;
- творчество, например лепка и живопись;
- чтение книг, при невозможности это могут делать близкие люди вслух.
Ухаживая за больным, не следует игнорировать своё здоровье. Пациенту нужно обеспечить нормальное питание, режим, активный образ жизни — это в полной мере относится и к близким больного человека.
Где обеспечивают уход при болезни Альцгеймера
Государственных специализированных пансионатов по уходу за людьми с болезнью Альцгеймера в нашей стране пока нет.
Прогноз. Профилактика
С увеличением осведомлённости общества о деменции будет расти и потребность в помощи по уходу, понадобятся значительные затраты для её организации. Пока же преобладает в основном неформальная помощь в семьях. Усилия по улучшению качества и доступности помощи потребуют вложений в меры первичной профилактики, и возможно, это позволит контролировать "эпидемии" деменций в разных регионах мира. В качестве основных мишеней первичной профилактики рассматриваются улучшение образования и устранение сосудистых факторов риска.
Профилактика
На сегодняшний день одной из основных целей профилактики является создание различных новых форм внебольничной помощи пациентам пожилого и старческого возраста с целью улучшения диагностики когнитивных нарушений разной степени тяжести, более раннее выявление заболеваний. С такой целью в развитых странах созданы клиники памяти, Альцгеймеровские центры. [2]
Продолжительность жизни
В среднем люди с болезнью Альцгеймера живут 3 – 11 лет после выявления заболевания, но некоторые — 20 лет и более. Продолжительность жизни зависит от степени нарушений при постановке диагноза [14] .
Юридические вопросы
Требования для признания гражданина недееспособным раскрываются в статье 29 Гражданского кодекса РФ. Потеря дееспособности компенсируется больному человеку установлением опёки. Опекун "восполняет" утраченные возможности гражданина, признанного недееспособным, и действует в его интересах.
Процедура признания гражданина недееспособным описана в 31 главе Гражданского процессуального кодекса РФ, в статьях 281–285.
Читайте также:

