Бурневич э з противовирусная терапия
Обновлено: 17.04.2024
Прогноз HCV-инфекции у детей в целом более благоприятный, чем у взрослых, однако у 4-6% детей с хронической HCV-инфекцией имеются признаки выраженного фиброза или цирроза при биопсии печени. Эффективное раннее лечение гепатита С у детей может предупредить последствия хронической инфекции. В настоящее время в лечении детей с ХГС применяется комбинация препаратов — пегилированного интерферона-α (Пег-ИФН-α) с рибавирином. Одним из факторов, влияющих на эффективность лечения, являются нежелательные явления. Наблюдаемые нежелательные явления у детей идентичны таковым у взрослых, в большинстве случаев они носили умеренный и преходящий характер и не потребовали коррекции дозы/отмены лечения.
Of antiviral therapy and their correction in children with chronic hepatitis C
Forecast HCV-infected children are generally more favorable than in adults, but at 4-6% of children with a chronic HCV infection has signs advanced fibrosis or cirrhosis at a liver biopsy. Effective early treatment of hepatitis C at children can warn consequences of a chronic infection. Now in treatment of children of HGC the combination of medications – pegylated interferon-α (Peg-Inf-α) with ribavirin is applied. One of the factors that influence the effectiveness of treatment, adverse events are. The observable adverse events at children are identical to that at adults, in most cases they had moderate and passing character and correction of dose/cancellation of treatment didn’t demand.
Инфекции, вызванные вирусами гепатитов В (HBV) и С (HCV), являются наиболее частой причиной формирования хронических заболеваний печени, в том числе у детей. По сравнению со взрослыми, у детей чаще наблюдается спонтанный клиренс виремии и ниже вероятность развития фульминантного гепатита и прогрессирования инфекции с развитием выраженного фиброза и цирроза печени [1, 2]. Хотя прогноз в целом более благоприятный, чем у взрослых, тем не менее, у 4-6% детей с хронической HCV-инфекцией имеются признаки выраженного фиброза или цирроза при биопсии печени [5]. Эффективное раннее лечение гепатита С у детей может предупредить последствия хронической инфекции, улучшить прогноз и качество жизни и, кроме того, снизить затраты системы здравоохранения на противовирусную терапию (ПВТ) в будущем, во взрослой практике, а также на лечение осложнений – цирроза печени, гепатоцеллюлярной карциномы.
Наиболее значимыми предикторами эффективности ПВТ – достижения стойкого вирусологического ответа у детей, также как и у взрослых, являются: генотип, уровень вирусной нагрузки, наличие быстрого и раннего вирусологического ответа. Не менее важным фактором, влияющим на эффективность лечения, являются нежелательные явления (НЯ). Появление и выраженность одних НЯ, таких как гриппоподобный синдром, депрессия, снижают приверженность пациента к лечению. Развитие других НЯ, чаще всего гематологических – лейкопении, нейтропении, анемии, требуют модификации доз противовирусных препаратов или досрочного завершения терапии [2, 3, 4, 8].
Цель: изучение переносимости ПВТ детей больных ХГС препаратами Пег-ИФН-α и рибавирина.
В исследование включены ранее не получавшие ПВТ 29 детей и подростков в возрасте от 6 до 17 лет. Всем пациентам проводились следующие исследования:
— ПЦР на РНК ВГС, генотипирование;
— биохимические и гематологические исследования;
— определение тиреоидного статуса (гормональный профиль – ТТГ, АТПО, Т3, Т4 и УЗИ);
Лечение больных проводилось препаратами Пег-ИФН-α 2b и рибавирина в течение 24 или 48 недель в зависимости от генотипа и наличия вирусологического ответа на 4, 12 неделях терапии. При проведении ПВТ мы руководствовались следующими правилами:
— подбор доз противовирусных препаратов исходя из МТ/поверхности тела – 40 мкг/кг/нед./60 мкг/м 2 /нед;
Расчет дозы ПегИнтрона на основании площади поверхности тела для детей с 3 лет проводится по следующей формуле:

140 смх 30 кг/3600 = 1,166666
Корень квадратный из 1,166666 = 1,08 м 2
1,08 м 2 х 60 мкг = 65 мкг/нед
— поддержание доз противовирусных препаратов в ходе всего курса лечения, особенно в течение первых 12 недель;
-ранняя диагностика и коррекция нежелательных явлений (при регулярном наблюдении с проведением контрольных лабораторных исследований).
С целью профилактики НЯ осуществлялось тщательное обследование пациента на предмет выявления противопоказаний к ПВТ, сопутствующей патологии, особое внимание обращая на заболевания с аутоиммунным компонентом.
Результаты и их обсуждение
В проведенном нами исследовании во время ПВТ детей ХГС выявлены разнообразные нежелательные явления. Наиболее часто наблюдались гриппоподобный синдром, головная боль, анорексия, гематологические НЯ, ИФН-индуцированная депрессия/субдепрессия. Нами отмечено, что характер и выраженность НЯ среди детей зависят от сроков проведения ПВТ.
На 1-2-й неделях лечения наблюдались:
— Гриппоподобный синдром у 89,6% больных проявлялся в виде повышения температуры до фебрильных цифр (в основном в первые сутки-двое после инъекции Пег-ИФН-α). Для коррекции этого синдрома использовали парацетамол, НПВС. В последующем температурнаяреакция снижалась, но начинали нарастать астенический и диспепсический синдромы. В рамках гриппоподобного синдрома следует выделить головную боль, как правило, беспокоившую 20,6% детей после первых инъекций Пег-ИФН-α.
— Миалгия, артралгия у 13,8% детей. Коррекция проводилась приемом НПВС (1-2 кратно в суточной дозе, при отсутствии противопоказаний).
На 4-12 недели ПВТ регистрировались:
— Кожный зуд и сыпь, гиперемия в местах инъекций — в 6,8% случаев. Для уменьшения, купирования этих симптомов использовали антигистаминные препараты, кортикостероидные мази. В качестве профилактики появления эритемы в местах инъекций Пег-ИФН-α рекомендовали чередование участков введения препарата.
— Анорексия — на снижение аппетита жаловались 13,8% родителей, дети которых получали ПВТ. В данных случаях основными рекомендациями были кормление детей по аппетиту, приготовление любимых блюд.
— Общая слабость, как проявление астенического синдрома, было у 13,8% детей. Увеличение физической активности, либо объёма принимаемой жидкости помогали уменьшить астенические явления.
— Интерферон-индуцированная депрессия у 20,6% детей проявлялась в виде раздражительности, плаксивости, беспокойства, бессонницы. Бессонница, кроме того, может быть обусловлена и неправильным — поздним приемом вечерней дозы рибавирина. Коррекция депрессии осуществлялась при активном участии психотерапевта, в редких случаях – назначением антидепрессантов.
На 12-24-й неделе лечения отмечались:
— Усиление выпадения волос – у 6,8% детей. Следует отметить, что данное состояние сопровождалось психологическим дискомфортом. Позитивное воздействие оказывала разъяснительная беседа с детьми и родителями о транзиторности данного явления. В качестве лечебных мероприятий рекомендовали использование цинк- или миноксидил содержащих средств для укрепления волос.
— Снижение веса – у 3,4% детей, как правило, старшей возрастной группы. Исходя из других исследований и собственного опыта, у всех детей наблюдается задержка роста, которая после завершения терапии прекращается. Отдаленные результаты показывают, что эти дети не отстают в развитии от сверстников, не получавших ПВТ.
— Гематологические нежелательные явления. Среди всех НЯ по своей важности они стоят на первом месте. В зависимости от степени их выраженности проводится уменьшение доз препаратов или прекращение терапии (табл. 1).
Рекомендации по коррекции дозы ПВТ при гематологических НЯ
Бурневич Э.З., Никулкина Е.Н.
Кафедра терапии и профболезней МПФ ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития России, Москва
Рассмотрены показания к противовирусной терапии (ПВТ) цирроза печения при HCV-инфекции (комбинация пегилированного интерферона ? и рибавирина). Обсуждаются особенности ПВТ и трудности ее проведения у этой категории больных, в т. ч. готовящимся к трансплантации печени. Подчеркивается, что единственная категория из указанной группы больных, подлежащая ПВТ согласно всем современным правилам ее проведения, – пациенты с компенсированным циррозом печени (5 баллов по шкале Child-Turcotte-Pugh), в т. ч. с начальными признаками портальной гипертензии, когда в качестве цели ПВТ преследуется достижение стойкого вирусологического ответа.
Хроническая HCV-инфекция является одной из наиболее частых причин развития цирроза печени (ЦП) [1], причем в течение ближайших нескольких десятилетий ожидается рост частоты ЦП в исходе хронического гепатита С (ХГС) [2]. Как известно, больные ЦП в исходе ХГС характеризуются неблагоприятным ближайшим прогнозом в связи с высокой частотой развития декомпенсации цирроза, формирования гепатоцеллюлярной карциномы (ГЦК) и, следовательно, летального исхода.
Как известно, формирование ЦП при хронической HCV-инфекции является критической стадией течения инфекционного процесса в печени – развитие внутрипеченочного сосудистого шунтирования с последующим образованием регенераторных узлов знаменует собой качественно новый этап заболевания, характеризующийся высоким риском развития декомпенсации ЦП и ГЦК. Рост портального давления в печеночных венах выше 12 мм рт. ст. является следующим шагом в сторону декомпенсации ЦП. Фармакологическое снижение портального давления, эндоскопические и хирургические процедуры, снижающие риск кровотечения из варикозно расширенных вен пищевода (ВРВП), не влияя на HCV как этиологический фактор ЦП, не предотвращают истощения функционального резерва гепатоцитов, тем более не снижают риск развития ГЦК. Неуклонное прогрессирование вирусного ЦП приближает момент, когда единственным жизнеспасающим методом лечения становится ортотопическая трансплантация печени (ОТП), однако рецидив HCV-инфекции в трансплантате (частота – 100 %) приводит к высокой частоте развития цирроза в трансплантированной печени (15–30 % в течение 5 лет) с крайне высоким риском его последующей декомпенсации (40 % в течение года) [3, 4]. Кроме того, частота потери трансплантата после ОТП в связи с ЦП в исходе ХГС достигает 25–30 %, что объясняет более низкую выживаемость больных HCV-инфекцией по сравнению с пациентами с другими нозологическими формами поражения печени, по поводу которых выполнялась ОТП [5]. Хотя в настоящее время противовирусная терапия (ПВТ) активно внедряется в практику ведения больных в посттрансплантационном периоде, многие аспекты ее проведения еще не разработаны, частота стойкого вирусологического ответа (СВО) относительно невелика, а лечение сопровождается большим числом нежелательных явлений (НЯ), в т. ч. реакцией отторжения донорского органа.
Таким образом, до момента проведения ОТП наряду с симптоматическим и патогенетическим лечением целесообразной является этиотропная терапия ЦП в исходе ХГС, т. е. ПВТ. В 2003 г. был предложен алгоритм выбора лечебной тактики при ЦП в исходе ХГС [4], подробно изложенный ранее [6]. На необходимость лечения больных ЦП в исходе ХГС указывается и в последних рекомендациях Американской ассоциации по изучению заболеваний печени (2009) [7]. Однако накопленный за последние годы опыт ПВТ данной категории больных, к сожалению, свидетельствует, что надежды, возлагавшиеся на ПВТ больных декомпенсированным ЦП, во многом не оправдались и казавшаяся возможность избежать или отдалить момент выполнения ОТП не подтвердилась в клинических исследованиях, что заставило существенно пересмотреть многие аспекты предложенных ранее терапевтических подходов [8–10].
ПВТ “истинного” компенсированного ЦП
Под “истинным” компенсированным ЦП понимается клиническая ситуация, когда по данным традиционных методов лабораторного и инструментального обследования отсутствуют признаки ЦП (5 баллов по шкале Child–Turcotte–Pugh – СТР), а цирротическая траснформация печеночной паренхимы выявляется при биопсии печени (и/или с помощью методов неинвазивной диагностики фиброза – сывороточных тестов, эластографии печени). Данные больные в обязательном порядке подлежат ПВТ, причем ее эффективность, особенно при использовании современного стандарта лечения – комбинации пегилированного интерферона α (Пег-ИФН-α) и рибавирина, только в небольшой степени уступает результатам лечения больных ХГС без продвинутого фиброза печени (табл. 1), что подтверждается в данных группах больных в регистрационных исследованиях M.W. Fried и соавт. и M.P. Manns и соавт.: частота СВО – 43 и 44 соответственно [11, 12].
Таблица 1.Противовирусная терапия компенсированного цирроза в исходе хронического гепатита С.
Важно понимать, что ПВТ больных компенсированным ЦП преследует те же цели, что и лечение больных ХГС без продвинутого фиброза: достижение СВО, который в подавляющем большинстве случаев свидетельствует об эрадикации HCV-инфекции, что реализуется резким снижением риска декомпенсации ЦП, развития ГЦК и наступления “печеночной смерти” [13–15]. Кроме того, благодаря лечению больных компенсированным ЦП была опровергнута долгое время существовавшая догма о необратимости ЦП [14, 16, 17]. Регресс фиброза в цирротической печени, равно как уменьшение или исчезновение некровоспалительных изменений в результате эрадикации HCV-инфекции, представляет собой важные механизмы ремоделирования печени, что отражается в улучшении прогноза больных [18]. Однако необходимо учитывать, что, несмотря на достижение СВО у больных компенсированным ЦП, возможно дальнейшее прогрессирование печеночного процесса. Так, 10-летнее наблюдение за больными ЦП в исходе ХГС свидетельствует, что риск печеночных осложнений составляет 40 % в отсутствие эффекта ПВТ и только 10 % у больных с СВО, а риск развития декомпенсации ЦП, ГЦК и “печеночной” смерти на 100 человеко-лет равен соответственно 1,9; 2,1 и 1,4 против 0; 0,66 и 0,19 [19, 20]. Эти данные диктуют необходимость длительного наблюдения за больными ЦП в исходе ХГС даже при достижении СВО, поскольку части из них в конечном итоге может потребоваться выполнение ОТП в связи с декомпенсацией ЦП и/или развитием ГЦК.
Необходимо помнить, что ПВТ больных компенсированным ЦП характеризуется более частым развитием НЯ, в т. ч. приводящих к преждевременному прекращению лечения (табл. 1) [18, 21–28]. В связи с этим необходимо более тщательное обеспечение высокой приверженности лечению путем тщательного и частого лабораторного контроля с целью раннего выявления НЯ, прежде всего гематологических – анемии, нейтропении, тромбоцитопении.
В настоящее время для коррекции анемии рекомендуются эритропоэтин альфа и дарбпоэтин, позволяющие поддерживать достаточный уровень гемоглобина, что в свою очередь обеспечивает возможность сохранения терапевтических доз противовирусных препаратов и улучшает качество жизни больных, однако применение препаратов рекомбинантного эритропоэтина альфа сопряжено с риском развития серьезных НЯ, среди которых наиболее опасны тромботические осложнения и парциальная красноклеточная аплазия костного мозга [29].
Несмотря на тот факт, что у больных ХГС без продвинутого фиброза и в случае компенсированного ЦП при ПВТ комбинацией Пег-ИФН-α и рибавирином не показана корреляция между числом нейтрофилов и инфекционными осложнения [30, 31], для коррекции нейтропении, тем не менее, рекомендуется использование гранулоцитрного колониестимулирующего фактора [32].
Тромбоцитопения нередко впервые появляется у больных “истинным” компенсированным ЦП во время ПВТ, но в большинстве случаев не достигает критических степеней. В ближайшие годы достойное место в коррекции тромбоцитопении займет эльтромбопаг – пероральный фактор роста тромбоцитов [33].
Однако, с другой стороны, место факторов роста в коррекции НЯ при ПВТ не совсем понятно – помимо их высокой стоимости в ряде исследований не было продемонстрировано повышение частоты СВО в результате их применения, несмотря на сохранение исходных доз противовирусных препаратов. Многие вопросы ПВТ больных компенсированным ЦП в исходе ХГС также остаются без ответа. Главным из них является продолжительность лечения: 48 недель вне зависимости от генотипа HCV или дифференцированный подход – 48 недель при инфицировании HCV 1-го генотипа и 24 недели при HCV 2-го и 3-го генотипов. К сожалению, в настоящее время нет проспективных контролируемых исследований, которые могли бы ответить на этот вопрос.
В ряде исследований показано положительное прогностическое значение полного раннего вирусологического ответа (РВО; авиремия через 12 недель ПВТ) при лечении данной категории больных, однако, совершенно не изучены вопросы пролонгации ПВТ при формировании медленного вирусологического ответа (достижение авиремии только через 24 недели лечения), равно как и не определено значение быстрого вирусологического ответа (авиремия через 4 недели лечения) в аспекте сокращения курса лечения. Для ответа на эти вопросы требуется проведение соответствующих клинических исследований.
ПВТ компенсированного ЦП с признаками портальной гипертензии
Нередко у больных компенсированным ЦП в исходе ХГС выявляются начальные признаки портальной гипертензии – небольшая спленомегалия с “мягкой” тромбоцитопенией (80–100 × 109/л), ВРВП I ст., тем не менее по шкале CTP сумма баллов составляет 5. Несмотря на то что в приведенные в табл. 1 исследования также включались больные с признаками портальной гипертензии, только одна работа посвящена оценке эффективности ПВТ именно у этой категории пациентов [34]. В исследовании, включившем 51 больного ЦП в исходе ХГС (81 % – HCV 1-го генотипа) с ВРВП I ст., тромбоцитопенией (≤ 100 × 109/л) и спленомегалией (длинник по селезенке ≥ 13 см), частота СВО в результате ПВТ Пег-ИФН-α2b по 1,0 мкг/кг/нед и рибавирином в дозе 800 мг/сут в течение 52 недель составила только 21,6 % (13,3% при генотипах 1 и 4, 83,3% – при генотипах 2 и 3), при этом преждевременно прекратили лечение из-за развития НЯ у 37 % больных. Это свидетельствует о том, что результаты лечения пациентов с компенсированным ЦП и признаками портальной гипертензии хуже, чем у больных “истинным” компенсированным ЦП. В то же время в результате ПВТ наряду с регрессированием фиброза печени отмечается уменьшение выраженности, а часто и исчезновение признаков портальной гипертензии [13].
Длительная низкодозовая поддерживающая терапия больных компенсированным ЦП
Во многих исследованиях было показано, что в случае недостижения полного РВО шанс на формирование СВО при продолжении ПВТ до 48 недель крайне низок. До недавнего времени предполагалось, что ввиду серьезного ближайшего прогноза у данных больных будет рациональна длительная низкодозовая поддерживающая монотерапия Пег-ИФН-α. К настоящему времени закончились три крупных клинических исследования (HALT-C, COPILOT, EPIC3), которые были призваны оценить целесообразность такого терапевтического подхода.
В исследовании HALT-C 1050 больных компенсированным ЦП, получавших без эффекта стандартную ПВТ, были рандомизированы в две группы: первая (n = 517) получала Пег-ИФН-α2а по 90 мкг/нед, вторая (n = 533) – плацебо (в течение 3,5 лет). Оказалось, что частота достижения конечных точек (летальный исход, декомпенсация ЦП, развитие ГЦК, прогрессирование фиброза по K. Ishak и соавт. ≥ 2 баллов) была сопоставимой – 34,1 и 33,8 % соответственно [35]. Аналогичные результаты были продемонстрированы в исследованиях COPILOT и EPIC [36, 37].
Таким образом, в настоящее время низкодозовая поддерживающая терапия больных компенсированным ЦП в исходе ХГС признана необоснованной.
ПВТ декомпенсированного ЦП
При наличии асцита, ВРВП высоких степеней, печеночной энцефалопатии, желтухи и лабораторных признаков печеночно-клеточной недостаточности (снижение уровня альбумина, гипокоагуляция) имеются прямые показания к выполнению ОТП, однако 100 %-ная частота реинфицирования донорской печени заставила десятилетие назадначать изучение возможности проведения ПВТ при признаках декомпенсации ЦП (табл. 2) [38–46], хотя портальная гипертензия, печеночно-клеточная недостаточность, кахексия, нередкие сопутствующие заболевания у таких больных (сахарный диабет, ишемическая болезнь сердца, хронические обструктивные заболевания легких), а также исходная панцитопения в значительной степени затрудняют противовирусное лечение.
Таблица 2.ПВТ декомпенсированного ЦП в исходе ХГС.
В последующие годы происходила оценка эффективности ПВТ с использованием Пег-ИФН-α и рибавирина. Первое исследование провели А. Iacobellis и соавт. (2007), однако авторы сразу указали на тот факт, что ни у одного больного ЦП класса С по шкале CTP не удалось достигнуть СВО, при этом отмечалась высокая частота инфекционных осложнений [42]. В других исследованиях использовались низкие дозы Пег-ИФН-α с различной продолжительностью применения в зависимости от генотипа HCV [44] или традиционные дозы Пег-ИФН-α при низких дозах рибавирина [43, 45, 46]. Интерпретация полученных данных во многом затруднена неоднородностью групп больных (в частности, часто в общий анализ включались пациенты с компенсированным ЦП), однако четко прослеживается низкая частота СВО, особенно при инфицировании НСV 1-го генотипа (табл. 2).
В отличие от цели ПВТ больных компенсированным ЦП в исходе ХГС (формирование СВО) лечение больных декомпенсированным ЦП с учетом крайне низкой частоты СВО (особенно при инфицировании HCV 1-го генотипа) предусматривает в качестве задачи достижение авиремии перед ОТПдля профилактики HCV-реинфекции в посттрансплантационном периоде. Безусловно достижение СВО у больных декомпенсированным ЦП ассоциируется с улучшением функционального резерва печени (табл. 3) [42, 44, 45], однако обращает на себя внимание, что после курса ПВТ средний балл по шкале CTP составляет 6–7, а значит, по-прежнему ближайший прогноз этих больных не благоприятен и им требуется выполнение ОТП. Правда, в этой ситуации срок ожидания ОТП в значительной степени удлиняется и позволяет выполнять оперативное пособие в плановом порядке.
Таблица 3. Динамика баллов по шкале Child–Turcotte–Pugh у больных декомпенсированным ЦП, достигших СВО в результате ПВТ.
Не стоит забывать о том, что во время ПВТ у больных декомпенсированным ЦП еще выше частота серьезных НЯ, являющихся причиной остановки лечения. Среди НЯ доминирующими по частоте и прогностически значимыми являются инфекционные осложнения. Если у больных ХГС без продвинутого фиброза и компенсированным ЦП нет взаимосвязи между числом нейтрофилов и инфекционными осложнениями во время ПВТ, о чем было сказано выше, то эта взаимосвязь совершенно очевидна у пациентов с декомпенсированным ЦП. Так, по данным Х. Forns и соавт., в группе больных декомпенсированным ЦП (расчетное время выполнения ОТП < 4 месяцев), получавших ПВТ Пег-ИФН-α2а и рибавирином, а также филграстимом при развитии нейтропении < 750 × 106/л, частота инфекционных осложнений составила 25 %, в то время как в контрольной группе без лечения – 6 %, при этом наиболее часто развивались спонтанный бактериальный перитонит, инфекция мочевыводящих путей, панникулит, пневмония, сепсис [47]. Также важно, что у больных декомпенсированным ЦП во время ПВТ крайне высока частота анемии и тромбоцитопении.
Трудоемкость ПВТ больных декомпенсированным ЦП объясняется необходимостью комплексной терапии, включающей коррекцию отечно-асцитического синдрома (мочегонные), профилактику кровотечения из ВРВП (неселективные β-адреноблокаторы, лигирование ВРВП, наложение трансъю-гулярного внутрипеченочного стент-шунта) и инфекционных осложнений (антибиотики), коррекцию печеночной энцефалопатии (L-орнитин-L-аспартат, лактулоза, рифаксимин) и печеночно-клеточной недостаточности (инфузии альбумина и свежезамороженной плазмы). Многочисленные исследования показали, что ПВТ больных декомпенсированным ЦП часто несет бoльший риск осложнений, чем потенциальную пользу, особенно при ≥ 10 баллов по шкале CTP, поэтому попытка назначения ПВТ для достижения авиремии перед ОТП считается оправданной только у больных с 6–9 баллами по шкале CTP [8, 9].
Таблица 4. Противовирусная терапия при циррозе печени в исходе хронического гепатита Ссогласно балльной оценке по системе Child–Turcotte–Pugh.
Заключение
Лечение больных ЦП в исходе ХГС – трудная задача (табл. 4). Частота СВО прогрессивно снижается параллельно увеличению числа серьезных НЯ по мере нарастания степени тяжести ЦП по шкале CTP, и, таким образом, ПВТ больных ЦП (особенно декомпенсированным) в исходе ХГС следует признать малоэффективной и небезопасной. Стратегически важно всех больных с явлениями декомпенсации ЦП (≥ 6 баллов по шкале СТР) направлять в центры трансплантации печени для постановки в лист ожидания ОТП. Больным с 6–9 баллами по шкале СТР перед ОТП может быть предпринята попытка ПВТ (предпочтительнее в LADR-режиме) с целью достижения авиремии к моменту выполнения операции для предотвращения реинфицирования донорской печени. При бoльших степенях декомпенсации (10–11 баллов по шкале СТР) вопрос о назначении противовирусных препаратов решается в индивидуальном порядке, а для больных с терминальным ЦП в исходе ХГС (12–15 баллов по шкале СТР) жизнеспасающим методом лечения является ОТП. Единственная категория пациентов, подлежащая ПВТ согласно всем современным правилам ее проведения, – больные компенсированным ЦП (5 баллов по шкале СТР), в т. ч. с начальными признаками портальной гипертензии, когда в качестве цели ПВТ преследуется достижение СВО. Длительная низкодозовая поддерживающая терапия в лечении больных ЦП в исходе ХГС, не отвечающих на ПВТ (отсутствие полного РВО), на сегодняшний день не обоснованна. Перспективы изменения лечебной тактики в отношении больных декомпенсированным ЦП связывают с разработкой нейтрализующих антител к HCV, назначаемых в беспеченочную фазу ОТП, однако результаты клинических исследований во многом противоречивы и пока далеки от реальной клинической практики [48, 49]. Реальной альтернативой, вероятно, является специфическая целевая ПВТ (STAT-C) с применением ингибиторов вирусной протеазы и/или полимеразы [50].
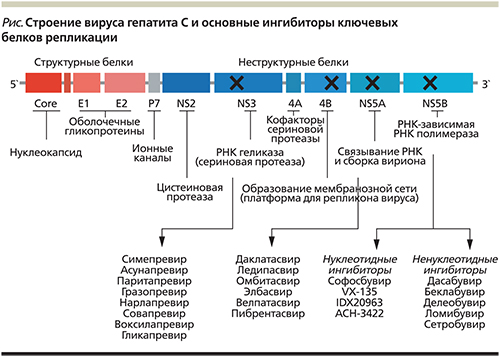
В июле и сентябре 2016 г. опубликованы последние рекомендации EASL и AASLD по лечению ЦП при ХГС, что легло в основу информации по выбору оптимального лечения вирусного цирроза печени в мире и в нашей стране (табл. 1–4).
Все рекомендуемые схемы лечения ПВП для 1-го генотипа вируса имеют высокую степень доказательности эффективности. Основной терапевтической схемой у первичных нелеченых пациентов с компенсированным ЦП при 1-м генотипе вируса является комбинация софосбувира (Соф) 400 мг и ледипасвира (Лед) 90 мг в одной таблетке 1 раз в день утром во время еды в течение 12 недель. При 1а-генотипе вируса лечение комбинацией Соф+Лед первичных пациентов в течение 12 недель комбинируют с РБВ, рассчитанным по весу пациента: 75 кг–1200 мг/сут (степень доказательности А1). При плохой переносимости РБВ или противопоказаниях к нему рекомендована терапия Соф+Лед при 1а-генотипе в течение 24 недель (степень доказательности В1). Комбинация Соф+Лед+РБВ на протяжении 12 недель показана также больным компенсированным ЦП с классом А по Чайлду–Пью, 1а-генотипом и наличием исходных мутаций резистентности (МР) NS5A (если они исследованы) к Лед в позициях M28A/G/T, Q30E/G/H/K/R, L31M/V, P32L/S, H58D и/или Y93C/H/N/S. Пациенты с 1а-генотипом без данных мутаций могут получать лечение Соф+Лед без РБВ с планируемым достижением устойчивого вирусологического ответа (УВО) на 12-й неделе (в 97% случаях) [6].
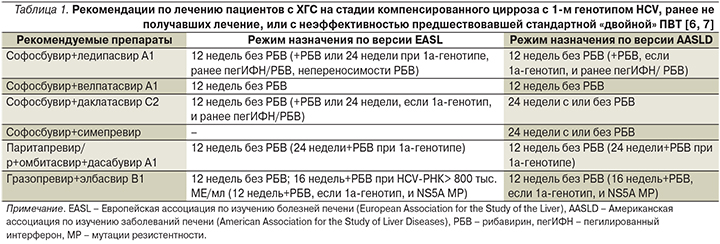
Наиболее оптимальным режимом лечения компенсированного ЦП при 1-м, 2-, 3-м генотипах HCV в настоящее время считается комбинация двух пангенотипных препаратов: Соф 400 мг и велпатасвира (Вел) 100 мг в одной таблетке 1 раз в день во время еды 12 недель без РБВ: УВО на 12-й неделе достигается в 99% случаев [6]. Лечение компенсированного ЦП с 1-м генотипом вируса Соф 400 мг+даклатасвиром (Дак) 60 мг в режиме 1 раз в день во время еды проводится в течение 24 недель в комбинации с РБВ, рассчитанным по весу 75 кг 1000/1200 мг, или без РБВ на усмотрение врача, оценивающего факторы прогноза ответа на ПВТ. УВО на 12-й неделе у пациентов с 1а-генотипом HCV достигается в 76% случаев, получающих комбинированную терапию Соф+Дак+РБВ в течение 24 недель, и у 100% пациентов с 1в-генотипом вируса, однако долгосрочный прогноз не оценен. В любом случае риск появления резистентности к ингибитору неструктурного белка 5А (NS5A) может обусловить неудачу терапии, в связи с чем всем пациентам с 1а-генотипом и ЦП рекомендован 24-недельный курс ПВТ в комбинации с РБВ [7].
3D-терапия (Викейра Пак) фиксированными дозами паритапревира (Пар) 75 мг, усиленного ритонавиром (Р) 50 мг, в комбинации с омбитасвиром 12,5 мг в одной таблетке (2 таблетки утром) в комбинации с дасабувиром (Дас) 250 мг дважды в день во время еды (суточная доза – 150/100/50 мг и 500 мг соответственно) и РБВ по весу 75 кг 1000/1200 мг 24 недели у пациентов с компенсированным ЦП и 1а-генотипом HCV позволяет достигать УВО на 12-й неделе 94% пациентов, 12-недельный курс лечения характеризовался УВО на 12-й неделе у 89% пациентов [8]. Рекомендации по лечению больных с 1-м генотипом вируса Викейрой Пак зависят от степени компенсации ЦП: при компенсированном ЦП, класс A по Чайлду–Пью 3D-терапия рекомендована; при декомпенсированном ЦП, класс В и С по Чайлду–Пью противопоказана. При 1-м генотипе HCV 3D-терапия в течение 12 недель без РБВ характеризуется достижением УВО на 12-й неделе у 89–96,7% пациентов [8, 9]. Пациенты с компенсированным ЦП должны быть информированы о редком нежелательном явлении (НЯ) – декомпенсации ЦП с быстрым нарастанием уровня билирубина и трансаминаз сыворотки и подлежат тщательному динамическому мониторингу ПВТ.
Гразопревир (Граз) 100 мг и элбасвир (Элб) 50 мг в одной таблетке 1 раз в день 12 недель без РБВ рекомендованы для пациентов с 1в-генотипом вируса. Если нет данных о мутациях резистентности к NS5A региону вируса, то при 1а-генотипе ориентируются на вирусную нагрузку (ВН): при ВН >800 тыс. МЕ/мл лечение проводят в течение 16 недель с РБВ по весу 75 кг 1000/1200 мг, при виремии ≤800 тыс. МЕ/мл длительность терапии 12 недель без РБВ. При наличии исходных мутаций резистентности к Элб в зоне NS5A (М28А/G/T, Q30D/E/G/H/K/L/R, L31F/M/V, H58D и/или Y93C/H/N/S) пациенты ЦП с 1а-генотипом вируса и высокой ВН >800 тыс. МЕ/мл получают лечение 16 недель с РБВ по весу. Без мутаций резистентности и при низкой вирусной нагрузке

В Рекомендациях Американской ассоциации по изучению заболеваний печени (American Association for the Study of Liver Diseases, AASLD) для пациентов с компенсированным ЦП с 1-м генотипом вируса рекомендована также терапия симепревиром (Сим) 150 мг/сут и Соф 400 мг/сут с или без РБВ, рассчитанным по весу 75 кг 1000/1200 мг, в течение 24 недель в отсутствие клинически значимой мутации резистентности Q80K. Эффективность ПВТ достигает 95–97% [7]. Не рекомендуется исследование мутаций резистентности до начала терапии ПВП. Встречаемость исходных мутаций NS5A составляет 10–15% при 1-м генотипе и обусловливает снижение активности NS5A ингибиторов более чем в 5 раз при 1а-генотипе вируса и наличии клинически значимых мутаций резистентности в позициях М28,Q30, L31и Y93, выявляемых у 5–10% пациентов [7]. Тестирование вариантов резистентности перед выбором схемы лечения обсуждается в отдельных группах: при наличии длительно существующих HCV-инфекции и ЦП, отсутствии эффекта от предшествовавшей ПВТ, в т.ч. с использованием ПВП 1-го поколения. Преодоление резистентности возможно комбинацией различных ПВП, в т.ч. с РБВ, и увеличением длительности терапии до 24 недель.
У пациентов с компенсированным ЦП С и генотипом-2 наиболее эффективной схемой ПВТ является комбинация Соф+Вел 12 недель без РБВ с достижением УВО на 12-й неделе в 99–100% случаев. Данная схема лечения не зависит от мутаций резистентности ключевых белков вируса NS5A и NS5B [6, 7]. Альтернативной схемой ПВТ при компенсированном ЦП является комбинация Соф+Дак без РБВ в течение 16 или 24 недель в зависимости от коморбидности.
ПВТ компенсированного ЦП с 3-м генотипом HCV у первичных (нелеченых) больных проводится комбинацией Соф+Вел +PБВ 12 недель, учитывая возможный риск Y93-мутаций резистентности в этой группе пациентов. УВО на 12-й неделе в клинических исследованиях достигается в 93% случаев. При непереносимости или наличии противопоказаний к назначению РБВ лечение Соф+Вел проводится в течение 24 недель [7]. Альтернативное лечение компенсированного ЦП с 3-м генотипом HCV Соф+Дак+РБВ по весу в течение 24 недель.
Доступных комбинаций ПВТ для лечения пациентов с ЦП и 3-м генотипом вируса С в настоящий момент в РФ нет в связи с отсутствием Соф в аптечной сети.
Лечение пациентов с декомпенсированным ЦП с наличием показаний к ортотопической трансплантации печени (ОТП) или без них без ГЦР представлено в табл. 4. Безынтерфероновый режим – единственно возможное лечение в этой группе больных печеночно-клеточной недостаточностью (менее 18–20 баллов по шкале MELD) и у пациентов после трансплантации печени. ПВТ проводится незамедлительно, доза РБВ первоначально может быть 600 мг с подбором переносимой дозы в последующем. При декомпенсированном ЦП не используются ингибиторы протеазы NS3/4A.
Пациентам с компенсированным ЦП и ГПЦ, находящимся в листе ожидания ОТП, показана незамедлительная ПВТ до проведения ОТП по общим рекомендациям для пациентов с компенсированным ЦП без ГЦР. Пациентам с рецидивом HCV-инфекции после ОТП и компенсированным или декомпенсированным ЦП (классы А, В, С по Чайлду–Пью) при 1-м и 2-м генотипах HCV рекомендована комбинация Соф+Вел+РБВ в течение 12 недель. При 3-м генотипе комбинация Соф+Вел+РБВ рекомендована к применению в течение 24 недель. Необходимость в РБВ для лечения рецидива HCV-инфекции после ОТП при компенсированном ЦП (класс А по Чайлду–Пью) не продемонстрирована и нуждается в дальнейшем изучении [6]. Стартовая доза РБВ при декомпенсированном ЦП может быть 600 мг в зависимости от уровня гемоглобина и степени тяжести ЦП с постепенным подбором переносимой дозы. При непереносимости РБВ или наличии противопоказаний к его применению в отношении пациентов с декомпенсированным ЦП рекомендованы Соф+Вел и Соф+Дак в течение 24 недель без РБВ.
Пациенты с декомпенсированным ЦП (классы В и С по Чайлду–Пью) в отсутствие показаний к ОТП должны наблюдаться в специализированных центрах. При ЦП с 1-м генотипом вируса рекомендованы Соф+Лед+РБВ, Соф+Вел+РБВ, Соф+Дак+РБВ в течение 12 недель. При 2-м генотипе HCV применяют Соф+Вел+РБВ или Соф+Дак+РБВ в течение 12 недель. При 3-м генотипе HC-терапию Соф+Вел+РБВ или Соф+Дак+РБВ продлевают до 24 недель как и при наличии противопоказаний к РБВ или при его непереносимости. Доза РБВ рассчитывается по весу 75 кг 1000/1200 мг, но в связи с тяжестью состояния пациента и декомпенсацией ЦП может быть уменьшена до 600 мг с последующим подбором переносимой дозы.
Таким образом, лечение компенсированного и декомпенсированного ЦП в исходе ХГС широко практикуется в мире, но в Российской Федерации представляет значительные трудности, имеет ограниченные возможности и требует обсуждения необходимости незамедлительной регистрации генериков для лечения сложной и довольно многочисленной когорты больных ХГС.
Литература
1. Кожевникова Г.М., Канестри В.Г., Абдурахманов Д.Т., Моисеева С.В. Лечение хронического гепатита С у пациентов с ВИЧ-инфекцией. Клин. Гепатология. 2011;3:32–8.
2. Hoofnagle J.H. Hepatitis C: the clinical spectrum of disease. Hepatology. 1997;26(3 Suppl.1):S15–S20.
3. Халилулин Т.Р., Гармаш И.В., Малая И.П., Виллевальде С.В. Клинико-эпиде-миологическая характеристика и распространенность HCV-инфекции у больных общесоматического стационара. Клин. гепатология. 2012;2:9–13.
4. Знойко О.О., Бурневич Э.З. Даклатасвир и асунапревир – новый режим терапии хронического гепатита С при инфицировании ВГС генотипа 1b. Инфекционные болезни. 2016;1;1–12.
5. Абдурахманов Д.Т. Хронический гепатит С: новые парадигмы лечения. Клин. гепатология. 2013;2:3–6.
6. European Association for the Study of the Liver. EASL Recommendations on Treatment of Hepatitis C 2016. SUMMARY. J. Hepatology. 2016, September 16.
8. Бурневич Э.З., Никулкина Е.Н. Омбитасвир+паритапревир/ритонавир и дасабувир+/-рибавирин – оптимальная противовирусная терапия хронического гепатита С препаратами прямого противовирусного действия с различными точками блокады жизненного цикла HCV 1-го генотипа. Клин. фармакология и терапия. 2015;2:2–15.
9. Poordad F., Hezode C., Trinh R., Kowdley K.V., Zeuzem S., Agarwal K. et al. ABT-450/r-ombitasvir and dasabuvir with ribavirin for hepatitis C with cirrhosis. N. Engl. J. Med. 2014;370(21):1973–82.
10. Инструкция по применению лекарственного препарата для медицинского приема Викейра Пак МЗ РФ от 13.12.2016. ЛП- 002965.
11. McPhee F.,Suzuki Y., Toyota Y., Karino Y., Chayama K., Kavakami Y., Bhore R., Zhou N., Hemander D., Mendez P., Kumada H. Elderly and cirrhotic patients without baseline NS5A polymorphisms in HCV genotype 1b have very high sustained virologic responses to daclatasvir plus asunaprevir. The 24th Annual Meeting of the Asian Pacific Association for the Study of the Liver. Istambul, Tyrkey, March 12–15, 2015.
12. Бурневич Э.З., Никулкина Е.Н. Комбинация даклатасвира и асунапревира в лечении хронического гепатита С при инфицировании HCV 1-го генотипа. Клин. фармакология и терапия. 2015;24(4):1–12.
14. Инструкция по медицинскому применению препарата Асунапревир (РФ).
Об авторах / Для корреспонденции
Климова Е.А. 1 , Знойко О.О. 1 , Чуланов В.П. 2 ,3 , Гусев Д.А. 4 , Исаков В.А. 5 , Жданов К.В. 6 , Бацких С.Н. 7,8 , Кижло С.Н. 4 , Мамонова Н.А 7 , Козлов К.В. 6 , Сукачев В.С. 6 , Тархова Е.П. 9 , Красавина Э.Н. 9 , Самсонов М.Ю. 9 , Ющук Н.Д. 1
Narlaprevir, ritonavir, and sofosbuvir in non-cirrhotic chronic hepatitis C genotype 1 infected patients
Klimova E.A. 1 , Znoyko O.O. 1 , Chulanov V.P. 2,3 , Gusev D.A. 4 , Isakov V.A. 5 , Zhdanov K.V. 6 , Batskikh S.N. 7,8 , Kizhlo S.N. 4 , Mamonova N.A. 7 , Kozlov K.V. 6 , Sukachev V.S. 6 , Tarkhova E.P. 9 , Krasavina E.N. 9 , Samsonov M.Yu. 9 , Yushchuk N.D. 1
1 A.I. Evdokimov Moscow State University of Medicine and Dentistry of the Ministry of Healthcare of the Russian Federation, 127473, Moscow, Russian Federation
2 I.M. Sechenov First Moscow State Medical University of the Ministry of Healthcare of the Russian Federation (Sechenov University), 119991, Moscow, Russian Federation
3 National Medical Research Center of Phthisiopulmonology and Infectious Diseases, Ministry of Healthcare of the Russian Federation, 127473, Moscow, Russian Federation
4 Centre for the Prevention and Control of AIDS and Infectious Diseases, 190103, Saint Petersburg, Russian Federation
5 Federal Research Center of Nutrition, Biotechnology and Food Safety, 109240, Moscow, Russian Federation
6 Kirov Medical Military Academy of the Ministry of Defense of Russian Federation, 194044, Saint Petersburg, Russian Federation
7 Central Research Institute of Epidemiology, 111123, Moscow, Russian Federation
8 Moscow Clinical Research Center named after A.S. Loginov оf the Moscow Department of Health, 111123, Moscow, Russian Federation
9 JSC R-Pharm, 119421, Moscow, Russian Federation
Aim of investigation - to estimate efficacy and safety of combination of direct-acting antivirus agents narlaprevir/ritonavir and sofosbuvir in patients with chronic hepatitis C.
Material and methods. Treatment naive, non-cirrhotic patients with chronic HCV infection (GT1) were enrolled at the study. Patients received therapy with the combination of narlaprevir 200 mg QD, ritonavir 100 mg QD and sofosbuvir 400 mg QD. Treatment duration was 12 weeks in group A and 8 weeks in group B. Preliminary results with rate of sustained virological response 12 weeks after treatment (SVR12) and main data of safety and tolerability of the investigating combination for all group A patients are presented.
Results and discussion. All 60 patients from group A reached SVR12 (100%; 95% CI 94-100%). Adverse events (AEs) during treatment period were registered in 28 (46.7%) patients. No serious AEs occurred. In total, treatment of narlaprevir/ritonavir and sofosbuvir combination during 12 weeks demonstrated high efficacy with good safety profile.
Keywords: chronic hepatitis C, hepatitis C virus, narlaprevir, ritonavir, sofosbuvir
Funding. The study is sponsored by the company R-Pharm JSC; the creation of basic documents, conducting research, processing the obtained data, statistical analysis, writing a report is carried out by the Contract Research Organization ALMEDIS.
Conflict of interests. The authors declare no conflict of interests.
For citation: Klimova E.A., Znoyko O.O., Chulanov V.P., Gusev D.A., Isakov V.A., Zhdanov K.V., Batskikh S.N., Kizhlo S.N., Mamonova N.A., Kozlov K.V., Sukachev V.S., Tarkhova E.P., Krasavina E.N., Samsonov M.Yu., Yushchuk N.D. Narlaprevir, ritonavir, and sofosbuvir in non-cirrhotic chronic hepatitis C genotype 1 infected patients. Infektsionnye bolezni: novosti, mneniya, obuchenie [Infectious Diseases: News, Opinions, Training]. 2020; 9 (1): 50-6.
Противовирусная терапия препаратами прямого противовирусного действия (ПППД) привела к качественным изменениям в лечении хронической инфекции, вызванной вирусом гепатита С (ВГС). Высокие показатели излечения с использованием современных схем терапии ПППД с высоким профилем безопасности позволяют искоренить проблему на глобальном уровне, в связи с этим Всемирная организация здравоохранения (ВОЗ) выступила с призывом к ликвидации вирусного гепатита как угрозы для общественного здравоохранения к 2030 г. [1, 2].
Цель работы - изучить эффективность и безопасность терапии ХГС, вызванного генотипом 1 ВГС, с применением комбинации ПППД, включающей нарлапревир, ритонавир и нуклеотидный NS5В-ингибитор полимеразы ВГС софосбувир.
Материал и методы
Эффективность и безопасность комбинации нарлапревира/ритонавира и софосбувира, применяемой в течение 12 или 8 нед (группа А и В соответственно), у пациентов с хронической инфекцией, вызванной ВГС генотипа 1, изучали в многоцентровом открытом клиническом исследовании II фазы.
Проведение данного исследования было разрешено Минздравом России, одобрено Советом по этике Минздрава России, а также независимыми этическими комитетами всех клинических центров, принимавших участие в исследовании. Данное исследование проводили согласно действующему российскому законодательству в соответствии с принципами надлежащей клинической практики (ClinicalTrials. gov ID: NCT04246723).
В исследование включали пациентов обоего пола от 18 до 70 лет с хронической инфекцией, вызванной ВГС генотипа 1, ранее не получавших противовирусной терапии, с показателями РНК ВГС в плазме крови ≥10 000 МЕ/мл на момент скрининга и без цирроза печени. Отсутствие цирроза подтверждали данными биопсии печени, выполненной в течение 2 лет до скрининга, либо данными эластометрии с помощью аппарата Fibroscan® (показатели ≤12,5 кПа в течение 6 мес до исходной оценки/дня 1), либо результатами исследования с использованием шкал FibroTest® ≤0,48 и APRI ≤1 на этапе скрининга. В исследование включены пациенты с соответствующими протоколу клинико-лабораторными показателями, без клинически значимых отклонений электрокардиограммы, с клиренсом креатинина по формуле Кокрофта-Голта ≥60 мл/мин.
К основным критериям исключения из исследования отнесены признаки декомпенсированного поражения печени, сопутствующие инфекции вирусом гепатита В и ВИЧ.
Данное исследование включало 3 периода: скрининга, терапии и наблюдения. Длительность периода скрининга составляла около 2 нед, в течение которых проводили обследование больных в соответствии с протоколом и подтверждали их соответствие критериям включения в исследование.
Прошедшие скрининг пациенты получали терапию комбинацией препаратов: нарлапревир 200 мг 1 раз в сутки, ритонавир 100 мг 1 раз в сутки и софосбувир 400 мг 1 раз в сутки.
В соответствии с дизайном исследования длительность терапии в группе А составила 12 нед, в группе В - 8 нед; в группу А требовалось включить 60 пациентов, в группу В -25 пациентов.
По протоколу набор пациентов в группу В осуществляли после завершения набора в группу А, при этом критерием включения пациентов в группу В была исходная вирусная нагрузка РНК ВГС
Рис. 1. Дизайн исследования
НВР - нарлапревир; РТВ - ритонавир; СОФ - софосбувир; УВО12 - устойчивый вирусологический ответ через 12 нед после лечения; УВО24 - устойчивый вирусологический ответ через 24 нед после лечения.
Длительность периода наблюдения в обеих группах исследования после окончания терапии составит 24 нед, включая первичную точку эффективности: количество пациентов, достигших устойчивого вирусологического ответа через 12 нед после лечения (УВО12), и дополнительный период наблюдения, также длительностью 12 нед, соответствующий показателю устойчивого вирусологического ответа через 24 нед после лечения (УВО24).
В настоящее время оба показателя (УВО12 и УВО24) приняты в качестве показателей достижения эффекта терапии регуляторными органами Европы и США с учетом того, что их соответствие между собой >99% [3, 11].
Помимо первичной точки эффективности (УВО12), в исследовании также определяется количество пациентов, достигших неопределяемого уровня РНК ВГС в разные сроки противовирусной терапии, на момент ее окончания, а также спустя 4, 12 и 24 нед. Кроме того, регистрируют случаи неэффективности терапии: вирусологический прорыв и рецидив заболевания.
Вирусологический прорыв определяют как повышение уровня РНК ВГС по крайней мере на 1 log10 выше минимального значения либо выявляемый уровень РНК ВГС после снижения его менее порога обнаружения (15 МЕ/мл).
В ходе исследования проведена оценка профиля безопасности и переносимости исследуемой комбинации. Общепринятые критерии оценки нежелательных явлений по шкале токсичности Common Terminology Criteria for Adverse Events (CTCAE) использованы для оценки выраженности выявленных на фоне проводимой терапии отклонений лабораторных показателей.
Статистический анализ демографических и исходных характеристик пациентов, показателей эффективности терапии проводили в анализируемой когорте, включавшей всех пациентов, получивших по крайней мере 1 дозу препаратов исследуемой схемы терапии. Описательная статистика для непрерывных переменных представлена с указанием среднего значения, медианы, стандартного отклонения, минимального и максимального значения, количества имеющихся наблюдений.
Категориальные данные анализировали с использованием абсолютных и относительных частот для каждой категории. Анализ эффективности основан на измерениях уровня РНК ВГС (по отношению к пределу обнаружения).
В ходе статистического анализа будет оценено, превосходит ли частота УВО12 в группе А (12-недельная терапия ранее не получавших лечения пациентов) соответствующий показатель в контрольной группе. Заданное контрольное значение основано на 95% доверительном интервале (ДИ) для обобщенного показателя УВО12, рассчитанного с помощью метаанализа устойчивого вирусологического ответа у ранее не получавших противовирусной терапии пациентов с ХГС и генотипом 1 вируса при применении схемы терапии с пегилированным интерфероном и рибавирином: 53% (95% ДИ 46-59) для пегилированного интерферона альфа-2а и 45% (95% ДИ 39-53) для пегилированного интерферона альфа-2Ь [12].
В статье приведены материалы промежуточного анализа для группы пациентов, завершивших 12 нед терапии (группа А) и прошедших 12-недельный период наблюдения, соответствующий первичной конечной точке эффективности.
Результаты и обсуждение
Предварительные результаты исследования включают первичную конечную точку эффективности (УВО12) для всех пациентов группы А, а также основные данные по безопасности и переносимости исследуемой комбинации.
Пациентов в исследование набирали в 5 клинических центрах Москвы и Санкт-Петербурга. Этап скрининга прошел 71 пациент, подписавший информированное согласие; из них 60 пациентов, соответствующих критериям включения/ исключения, получили лечение препаратами (нарлапревир/ ритонавир и софосбувир) и закончили период наблюдения, соответствующий точке УВО12. Медиана времени до постановки диагноза ХГС у данных пациентов составила 7,86 года.
В табл. 1 представлена исходная демографическая характеристика пациентов группы А. В данной группе преобладали женщины (66,7%), возраст пациентов варьировал от 22 до 69 лет (медиана возраста - 40 лет). Большинство женщин из группы терапии А (n=24) были способны к деторождению и использовали надлежащие методы контрацепции для предупреждения беременности в ходе исследования.
Таблица 1.
Исходные характеристики пациентов группы А
Основные характеристики (n=60)*
Исходные показатели стадии фиброза печени по шкале METAVIR, n (%)
Примечание. * - 59 пациентов относились к европеоидной расе, у 1 пациента этническая принадлежность не определена; ** - возраст рассчитывали как число полных лет со дня рождения до даты подписания информированного согласия.
До начала исследования у большей части пациентов из данной группы определили слабовыраженный фиброз печени F0-F1 (75,0%) по шкале METAVIR, у 9 (15,0%) пациентов выявлена стадия фиброза F3. Исходная вирусная нагрузка в данной группе изменялась в диапазоне от 5150 до 9 050 000 МЕ/мл. Случаев досрочного прекращения терапии и выбывания пациентов из исследования по каким-либо причинам у пациентов группы А не было. Все 60 пациентов группы А достигли УВО12 (100%; 95% ДИ 94-100).
Через 2 нед терапии неопределяемый уровень РНК ВГС установлен у 45 (75,0±5,6%) пациентов (95% ДИ 62,1-85,3); на 4-й неделе - у 58 (96,7%) пациентов (95% ДИ 88,5-99,6). В последующие недели терапии, на момент окончания лечения и в период наблюдения у всех пациентов данной группы достигнут неопределяемый уровень РНК ВГС. Доля пациентов, достигших неопределяемого уровня РНК ВГС на различных сроках терапии и наблюдения, представлена на рис. 2.
Рис. 2. Доля пациентов, достигших неопределяемого уровня РНК вируса гепатита С в различные сроки наблюдения
УВО4 - устойчивый вирусологический ответ через 4 нед после лечения; УВО12 - устойчивый вирусологический ответ через 12 нед после лечения.
Таблица 2.
Характер и частота развития нежелательных явлений у пациентов группы А
По меньшей мере одно
Результаты лабораторных исследований, проведенных в рамках данного протокола, были систематизированы в соответствии с классификацией CTCAE (версия 4.03). Подавляющее большинство НЯ были легкой или умеренной степени тяжести и соответствовали степени I или II по шкале токсичности CTCAE. Отдельно взятые нежелательные явления встречались с частотой менее 10%. С наибольшей частотой регистрировали диарею (8,3%), головную боль (8,3%) и сонливость (6,7%).
Направления в области разработки отечественных схем противовирусной терапии гепатита С приближаются к международным: применяются ПППД с укорочением длительности курса терапии, эффективность которых близка к 100% [3, 13]. Схема терапии ХГС с применением отечественного ингибитора протеазы ВГС нарлапревира в комбинации с ритонавиром и софосбувиром продемонстрировала высокую эффективность при хорошем профиле безопасности.
ЛИТЕРАТУРА
REFERENCES
Читайте также:

