Чего нет в клетке возбудителя чумы ядра мембраны рибосом
Обновлено: 19.04.2024
К 120-летию открытия А. Йерсеном и Ш. Китазато микроба чумы Yersinia pestis
Об авторе
Виктор Васильевич Сунцов — доктор биологических наук, ведущий научный сотрудник Института проблем экологии и эволюции им. А. Н. Северцова РАН. Занимается изучением происхождения и эволюции возбудителей природноочаговых инфекций, в частности чумы.
Диаграмма публикаций по проблеме чумы, фиксирующая скачок их числа с 2003 г.
Немного истории
Карта распространения чумы в Европе. Пандемия, начавшаяся в центральных районах Азии, достигла берегов Черного моря в 1347 г.
Когда появился микроб чумы?
Доказанное в 1980 г. молекулярными методами непосредственное родство псевдотуберкулезного (Y. pseudotuberculosis) и чумного (Y. pestis) микробов привело к выводу об их недавней дивергенции, правда, без указания времени и места, когда именно и где это случилось [5]. Высокое сходство их геномов позволяло некоторым авторам даже объединить их в один вид в качестве отдельных подвидов, хотя вызывают они совершенно разные болезни. И псевдотуберкулезного, и чумного микробов относят к семейству Enterobacteriaceae — возбудителям кишечных инфекций, но последний, будучи паразитом крови, не имеет к ним никакого отношения. У него иная адаптивная среда, и в принципе его нужно отнести к другому семейству [3].
Микрофотография чумной палочки. Увел. ×200. Фото с сайта cdc.gov
Идея недавнего отделения чумного микроба от псевдотуберкулезного была неожиданной, но отнюдь не новой. В 1950–1970-х годах такие мысли высказывали В. Н. Беклемишев, В. А. Бибикова, А. И. Дятлов, Л. Н. Классовский, В. С. Петров, Н. М. Хрусцелевская. Но тогда подобные интуитивные ощущения эволюционной молодости возбудителя чумы выглядели теоретически чуждыми, паранаучными и деструктивными, поэтому они не нашли поддержки у ортодоксов.
Головокружение от успехов
В современных исторических реконструкциях в биологии доминирует новая филогенетика (молекулярная филогенетика, генофилетика). Отчасти это лидерство оправдано широкими возможностями, которые предоставляют молекулярные структуры и компьютерные технологии филогенетических построений, позволяющие сравнивать и обрабатывать миллионы признаков, — таких, как последовательности нуклеотидов. Все составляющие новой филогенетики полезны, они необходимы для создания естественных филогенетических схем, но недостаточны, особенно в отношении прокариот. Молекулярная генетика — молодая наука, и закономерности молекулярной эволюции пока не вполне ясны. Филогении можно выстраивать только по гомологичным признакам, а их выявление, в том числе и на молекулярном уровне, представляет немалую проблему. Выводы на основе применения разных молекулярно-генетических методов далеко не однозначны, порой не согласуются между собой и с данными других наук: экологии, биогеографии, микробиологии и др. Такая обескураживающая разноголосица свойственна и заключениям в отношении микроба чумы.
Происхождение Yersinia pestis: взгляд натуралиста
Знание экологии монгольского сурка и его блох позволяет понять селективные (адаптационные) процессы, проходившие в микробных популяциях в природе, и причинно-следственные связи в эволюционных филумах. Появление возбудителя чумы в Центральной Азии предопределили два природных фактора: аридность горно-степных ландшафтов, постепенно увеличивающаяся с олигоцена-миоцена, и максимальное похолодание в сартанское время последнего оледенения. Проще говоря, индуктором видообразования микроба чумы был сухой и холодный климат Центральной Азии в конце ледниковой эпохи. Кроме того, в возникновении чумного микроба важную роль играет физиология, точнее поведение монгольского сурка, связанное с устройством зимовочной пробки, а также особенности сурочьей блохи O. silantiewi.
В Центральной Азии, в горно-степных поселениях сурка тарбагана влажность почвы очень низкая, всего 2–7% [3], а грунт в зимовочной норе зверька сухой и щебнистый. Изготовить из него земляную пробку внутри норы, в вертикальном лазе диаметром 15–20 см, все равно, что замазать сухим песком отверстие в потолке размером с футбольный мяч. Из-за дефицита почвенной влаги у монгольского сурка выработалось специфичное поведение. При залегании в спячку он устраивает зимовочную пробку из специально подготавливаемой смеси мелкозема, щебня и влажных каловых масс, которые летом собираются в отнорках (уборных). Для перетаскивания камней, обвалянных в фекалиях, сурки используют зубы, при этом частицы фекалий, а с ними и возбудитель псевдотуберкулеза, попадают в ротовую полость. Итак, во рту спящих тарбаганов — экскременты, а в них — кишечный паразит, микроб псевдотуберкулеза!
Монгольский сурок тарбаган и его зимовочная (постоянная) нора. Вверху: зимовочная пробка, состоящая из смеси мелкозема, щебня и цементирующих их экскрементов (1); гнездовая камера (2); отнорки-уборные, в которых в летние месяцы сурки накапливают строительную смесь (3). Внизу: слой мелкозема и щебня (а); и коренные породы (б), приведены температуры грунта и спящих сурков во время раскопки (февраль 1979 г.)
Сурки — типичные семейно-колониальные животные. Группировки из 2–22 разновозрастных и разнополых зверьков совместно зимуют в одной постоянной, или зимовочной, норе. У каждого зверька в течение зимней спячки более длительные периоды глубокого сна (торпора) чередуются с короткими периодами бодрствования (эутермии). В торпорной фазе температура тела снижается до 2–5°C, в эутермной может достигать нормальной, у активных сурков — около 37°С. За осенне-зимне-весеннее время сурки не вполне синхронно просыпаются до 15 раз, примерно дважды в месяц. Таким образом, каждый зверек в течение периода подземной жизни имеет два гомеостатических состояния, между которыми лежит промежуток физиологической гетеротермии. Отсюда следствие: блохи в холодное время года питаются на сурках, температура тела которых лежит в диапазоне 5–37°C. Обратим внимание на непрерывность температур!
В 1970-х годах в тувинском очаге чумы, расположенном в Центральной Азии, мы изучали зимнюю спячку тарбагана. В феврале-марте, во время максимального зимнего промерзания грунта (до глубины более 2 м), раскопали три зимовочных норы. Из них изъяли восемь глубоко спящих и девять проснувшихся активных зверьков, среди которых были молодые, полувзрослые и взрослые особи. Из их шерсти собрали 230 личинок O. silantiewi, 60 живых и 452 пустых коконов, а из ротовой полости торпидных зверьков — дополнительно 20 личинок. Пустые коконы (от 4 до 87) обнаружили также на 22 зверьках, отловленных в первые две недели после весеннего пробуждения.
Тувинский природный очаг чумы, Монгун-Тайгинский мезоочаг. Снеговое покрытие в зимне-весенние месяцы не превышает 30–40%, грунт промерзает на глубину более 2 м к началу января, а оттаивает в июле
Отметим распределение коконов на шерсти: большая часть прикреплена на голове, у основания хвоста и на наружной стороне задних ног. Все личинки, извлеченные из ротовой полости, оказались с кровью и увеличенными в размерах за счет развития жирового тела, что свидетельствовало о полноценности пищи и об их готовности к окукливанию. У спящих зверьков поврежденная личинками слизистая ротовой полости и язык обильно кровоточили, изо рта заметно выступала кровяная пена, а рот, зубы, лапы были обильно испачканы экскрементами (следами устройства зимовочной пробки осенью). Незарубцевавшиеся раны в ротовой полости мы наблюдали у всех сурков, отловленных после выхода из нор в конце марта и начале апреля, что говорит о массовости описываемого явления, его общепопуляционном характере.
Отсюда понятна причина концентрации пустых коконов на голове, хвосте и наружной стороне задних ног у спящих и недавно пробудившихся сурков тарбаганов. Зимой грунт промерзает глубже гнездовых камер, и личинки переходят из гнездовой выстилки на более теплые тела спящих зверьков. При этом некоторые личинки, произвольно перемещаясь в шерсти, попадают в ротовую полость сурка, где, питаясь на слизистой, травмируют ее. Перед окукливанием личинки покидают ротовую полость и прикрепляются к шерсти близ рта. Зная позу свернувшегося в шар спящего сурка, у которого нос уткнулся в анус, а задние ноги прижаты к щекам, легко предсказать места прикрепления коконов.
На основе новых эколого-географических, палеоклиматических и генетических данных можно сформулировать основные постулаты теории происхождения и мировой экспансии микроба чумы.
Происхождение, естественное распространение в Евразии и антропогенная мировая экспансия микроба Y. pestis во время первой (I), второй (II) и третьей (III) пандемий. 1 — южная граница зоны многолетнемерзлых грунтов; 2 — граница доминантного распространения в природе микроба Y. pseudotuberculosis O:1b; 3 — ареал сурка-тарбагана, район происхождения микроба чумы; 4 — первичные природные очаги; 5 — вторичные природные очаги; gly + (gly − ) — способность (неспособность) штаммов ферментировать глицерин
Предковая форма возбудителя чумы — микроб псевдотуберкулеза 1-го серотипа (Y. pseudotuberculosis O:1b), который доминирует в северо-центрально-азиатских и дальневосточных районах с суровым климатом.
Метаморфоза микроба псевдотуберкулеза в чумную бактерию произошла в конце позднего плейстоцена. За весь четвертичный период глубокое промерзание грунта (2 м и более) в Центральной Азии отмечено только в сартанское время позднего плейстоцена и в голоцене, т. е. не ранее 22 тыс. лет назад [10].
В ультраконтинентальном районе зимнего антициклона в Центральной Азии личинки блох, паразитирующие на монгольском сурке тарбагане, зимой переходят к факультативной гематофагии, что приводит к устойчивому контакту крови сурков с псевдотуберкулезным микробом [3].
Теперь уже можно легко представить, как сапрозоонозный кишечный псевдотуберкулезный микроб постепенно эволюционировал в облигатный паразит крови незимоспящих грызунов: экскременты тарбагана → спящий сурок → активный сурок → незимоспящий грызун.
Знание молекулярно-генетических, популяционных и биоценотических факторов, а также их многообразных связей позволяет выделить в эволюционной истории возбудителя чумы основные вехи.
IV. Во время третьей пандемии с корабельными крысами микроб уже другого подвида (orientalis) из Азии вновь проник в Африку и впервые на быстроходных морских судах добрался до Нового Света, где закрепился в виде вторичных природных очагов в популяциях земляных белок, луговых собачек, полевок, морских свинок.
В поисках согласия
Экологический сценарий происхождения, эволюции и мировой экспансии возбудителя чумы весьма заметно расходится с гипотезами, построенными на основе генетических данных. Где же истина? Какой из них достоин большего одобрения?
В пользу экологического сценария говорит следующее:
Такие аргументы делают этот экологический сценарий наиболее правдоподобным в сравнении с другими, позволяют принять его за исходную гипотезу и наполнять его генетическими признаками. Биологическое содержание сценария, понятное широкому кругу исследователей, дает существенные гносеологические преимущества перед слишком редуцированными историческими реконструкциями. К примеру, некоторые авторы из-за сходства отдельных генетических признаков у кавказского подвида Y. pestis caucasica и псевдотуберкулезного микроба считают Кавказ родиной чумы и выстраивают соответствующую филограмму [11, 12]. Но на Кавказе, в относительно теплом климатическом регионе, нет псевдотуберкулезного микроба 1-го серотипа или он встречается крайне редко! Истоки чумы следует искать в холодных, суровых краях — как в предложенном сценарии.
Несмотря на разительное несходство экологической и генетической филогений, между ними нет непреодолимой пропасти, более того, есть безусловные точки соприкосновения. Экологический сценарий для молекулярных и генетических признаков очерчивает диапазон генетической изменчивости микробной популяции, вступившей на путь видообразования, выделяет рамки экологической достоверности генетических фактов, привлекаемых для филогенетических выводов [3, 13].

Обзор
Автор
Редактор

Один монах, странствуя по белому свету, встретил Чуму, которая направлялась в его город.
— Ты куда это направляешься, Чума? — спросил он ее.
— Иду в твой родной город, — ответила она. — Мне нужно забрать там тысячу жизней.
Через некоторое время монах снова встретил Чуму на своем пути.
— Почему ты меня обманула тогда? — спросил он ее с укором. — Ты говорила, что должна забрать тысячу жизней, а забрала пять тысяч.
— Я тогда сказала тебе правду, — ответила Чума. — Я действительно забрала тысячу жизней. Остальные умерли от страха.
Жертвы чумы исчислялись сотнями тысяч и даже миллионами человек, вымирали города, становились безлюдными целые области, и ужас пандемий чумы затмевал ужасы всех войн, какие знала история человечества. Целые тысячелетия люди не понимали, что является источником заболевания [2].
Библия — одно из древнейших дошедших до нас свидетельств эпидемий чумы (1 книга Царств, глава 5; 4 книга Царств, глава 19, стихи 35–36). В мировой истории отмечают три пандемии этой болезни:
Бубонная форма чумы является наиболее распространенной формой заболевания и при отсутствии лечения приводит к гибели 40–60% заболевших. Легочная форма возникает либо как осложнение бубонной или септической форм, либо при вдыхании воздуха, зараженного возбудителем чумы. Если лечение не начинают в первые 24 часа после появления симптомов, смерть наступает через 48 часов [8].
В природе чумной микроб встречается практически на всех континентах, исключая Австралию, Антарктиду, а также Арктику, что обусловливает ежегодно регистрируемые случаи этой болезни. Стремительная эволюция микроорганизмов приводит к появлению популяций бактерий (штаммов), устойчивых к антибиотикам [9], что в случае с возбудителем чумы особенно опасно. Кроме того, этих бактерий могут использовать в качестве агента биотерроризма. Все вышесказанное объясняет необходимость изучения чумного микроба.
Возбудитель чумы Yersinia pestis — самая опасная бактерия в мире [10]. Что делает ее столь смертоносной?
Факторы вирулентности, или вооружен и очень опасен
Со времен открытия возбудителя чумы в 1894 году французом Александром Йерсеном и японцем Китасато Сибасабуро ученые пытались выяснить, что определяет патогенность Y. рestis. В результате многолетней тяжелой и рискованной работы, которая продолжается и по сей день, выделили следующие факторы патогенности возбудителя:
- белки внешней мембраны (Yersinia outer proteins — называемые Yop-белками, эффекторными белками, или комплексом Yop-вирулона) [11];
- комплекс области пигментации [12];
- активатор плазминогена [13];
- капсульный антиген [14];
- пили адгезии или pH6-антиген [15].
Белки внешней мембраны, или зачем возбудителю чумы шприц?

Рисунок 1. Схема действия системы секреции III типа.
Комплекс области пигментации, или может ли стать потребность в чем-либо фактором патогенности?
Активатор плазминогена, или двуликий Янус
При вдыхании чумных микробов (и развитии легочной чумы) этот белок обеспечивает быстрое размножение бактерий в тканях легких и приводит к развитию молниеносной пневмонии и отеку легких, тогда как в отсутствии Pla инфекция не развивается в смертельную пневмонию. Установлено, что активатор плазминогена нарушает постоянство внутренней среды организма хозяина и блокирует иммунные реакции, направленные на уничтожение патогена [27].
Капсульный антиген, или скользкий тип этот возбудитель чумы
Бактерии окружены капсулой из слизистого вещества (фракция I, Fra1), которая препятствует поглощению и обезвреживанию Y. pestis иммунными клетками организма-хозяина в процессе фагоцитоза. На выявлении этого вещества-антигена основаны многие современные методы лабораторной диагностики чумы, оно входит в состав многих экспериментальных химических вакцин против чумы. Однако позднее обнаружили популяции бактерий, лишенные капсулы [28]. Кроме того, слизистая капсула есть у многих других микроорганизмов, например, возбудителя сибирской язвы, туляремии. Капсульное вещество иерсинии образуют при температуре 37 °С.
Антигены, схожие с рН6, были обнаружены у ряда возбудителей, вызывающих менее опасные болезни — кишечные инфекции (Y. pseudotuberculosis [31], Y. enterocolitica [32], Escherichia coli [8]).
Температурный фактор, или то, что действительно имеет значение
Необходимо заострить внимание на особой роли температуры в физиологии чумного микроба. Именно при температуре 37 °С у него повышаются питательные потребности [33] и синтезируются практически все известные детерминанты вирулентности (рис. 2) [34]. У других бактерий подобная зависимость выражена в меньшей степени, что позволяет говорить о ведущей роли температурного фактора в вирулентности возбудителя чумы [8].
Геном или все важное внутри
Помимо хромосомы у чумного микроба есть плазмиды — внехромосомные участки ДНК [38]. Большинство белковых факторов вирулентности закодированы на плазмидах: эффекторные белки на плазмиде pCad; капсула — pFra; активатор плазминогена — рPla (pPst, pPCP). Плазмиды pFra и рPla обнаружены только у Y. pestis (видоспецифические), pCad является общей с возбудителем псевдотуберкулеза (родоспецифическая) [20].
Заключение
В настоящее время продолжается работа по выявлению новых, еще не изученных маркеров вирулентности [39]. С использованием 2D-электрофореза, масс-спектрометрии, полногеномного секвенирования проводят сравнительный анализ отличающихся по вирулентности популяций чумного микроба для выявления различий в их белковых спектрах и геномных последовательностях. Ранее не известные белки и участки генома становятся объектом пристального внимания и изучения как потенциальные детерминанты вирулентности.
Таким образом, патогенность возбудителя чумы — это множественный (полидетерминантный) признак. Соединение многих факторов в единое целое создает страшную угрозу чумных эпидемий, с противостоянием которым, однако, прогрессивное человечество успешно справляется.
Общее строение клетки: ядро, цитоплазматическая мембрана, цитоплазма
Клетка — основная функциональная единица организма. Ядро клетки служит хранилищем огромного объёма генетической информации и одновременно центром её активной экспрессии. Существует большое количество различных типов клеток (клетки эпителия, печени, нервных волокон и др.), особенности метаболизма которых обусловлены находящимися в их цитоплазме органеллами, а также множеством растворимых ферментов, характерных для каждого вида клеток.
Цитоплазматическая мембрана, или плазмолемма, — барьер для растворимых в воде молекул, который отделяет внутреннее содержимое клетки от внешней среды. Она состоит из двух параллельных рядов фосфолипидов, которые образуют гидрофобную липидную прослойку между двумя гидрофильными слоями из фосфатных групп.
Плазмолемма пронизана различными белками, гидрофобные части которых находятся внутри билипидного слоя, а гидрофильные — на внешней и внутренней поверхности мембра ны. Микроворсинки — удлинения на верхней (апикальной) части плазмолеммы, которые увеличивают поверхность мембраны и облегчают обмен молекулами.
Ядро клетки. Генетическая информация заключена в хромосомах, которые находятся в ядерном матриксе. Матрикс — сетчатый внутриядерный каркас, состоящий из белкового материала и тесно примыкающий к ядерной оболочке.
Ядрышком называют морфологически выраженную структуру внутри ядра, в которой происходит синтез рибосомальной РНК (рРНК). В ядре клеток человека обычно присутствует одно ядрышко, в котором во время интерфазы возникают ядрышковые организаторы акроцентрических хромосом.
Ядро окружено двойной мембраной, называемой ядерной оболочкой, которая пронизана ядерными порами.
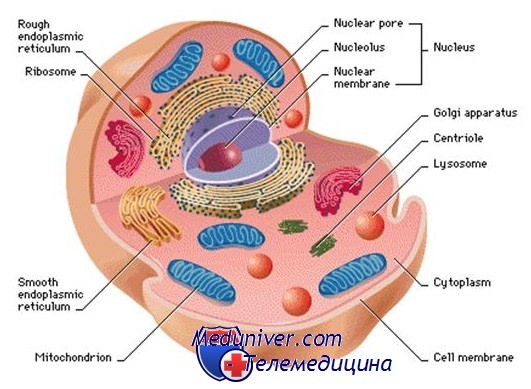
Цитоплазма клетки. Цитоплазма состоит из гелеобразного цитозоля, содержащего запасы гликогена, липидные вкрапления и свободные рибосомы, который пронизан рядами взаимосоединённых волокон и трубочек, образующих цитоскелет. Основные структурные компоненты цитоскелета — микротрубочки, микрофиламенты и промежуточные филаменты.
Микротрубочки — прямые полые цилиндры, стенки которых состоят из чередующихся молекул а- и b-тубулина. Они исходят из клеточного центра (центросомы), который имеет пару центриолей— цилиндрических структур, образованных девятью триплетами микротрубочек. Подобное строение свойственно также базальным тельцам реснитчатого эпителия.
Сеть микротрубочек играет важную роль в поддержании структуры и размера клетки, а также при расхождении хромосом во время деления и движения ресничек и сперматозоидов.
Микрофиламенты представляют собой двуспиральные полимеры белка актина и находятся в основном по периметру клетки. Они участвуют в движении клетки и изменении её формы.
Промежуточные филаменты имеют трубчатую структуру и соединяют десмосомы. В зависимости от вида клетки в их состав входит один или несколько из пяти определённых белков.
Митохондрии — самые крупные и наиболее распространённые в цитоплазме органеллы, основной функцией которых служит обеспечение организма энергией посредством синтеза АТФ. Митохондрии — самовоспроизводящиеся полуавтономные органеллы, содержащие рибосомы и до десяти и более копий кольцевых нитей митохондриальной ДНК.
Данная ДНК кодирует митохондриальные гены. В митохондриях присутствуют ферменты, необходимые для функционирования цикла трикарбоновых кислот, а также большое количество ферментов, участвующих в окислении жирных кислот.
Пероксисомы частично отвечают за детоксикацию различных веществ (в том числе этанола), однако их основная задача — окисление жирных кислот.
Эндоплазматическая сеть (ЭПС) — основной центр синтеза белков и липидов, который также служит начальным этапом секреторного пути белков. ЭПС представляет собой обширный лабиринт из связанных с мембраной каналов, который соединяется непосредственно с ядерной оболочкой.
Вблизи ядра на поверхности ЭПС есть рибосомы (гранулярная ЭПС), в то время как на участках, расположенных дальше, рибосомы отсутствуют (агранулярная или гладкая ЭПС). ЭПС играет важную роль в нейтрализации токсинов. Белки, синтезируемые в ней, затем попадают в комплекс Гольджи — ряд расположенных друг над другом сплюснутых везикул. После этого белки депонируются или попадают в секреторные везикулы для осуществления экзоцитоза, т.е. выведения из клетки в ответ на внешнее воздействие.
Эндоцитоз. Эндоцитозом называют процесс поглощения и переработки клеткой компонентов окружающей среды. При опосредованном рецепторами пиноцитозе происходит захват мелких частиц путём образования везикулы с жидкостью на поверхности цитоплазматической мембраны и её последующего поглощения клеткой. При этом образуются окаймлённые впячивания. Более крупные частицы связываются с мембраной и поглощаются в составе фагоцитарных вакуолей (фаголизосом); растворы поглощаются при помощи жидкостного пиноцитоза.
Содержимое пиноцитарных и фагоцитарных везикул, которые часто называют эндосомами, обычно обрабатывают лизосомы, содержащие разрушающие ферменты — лизоцимы.
Межклеточные соединения. В случае плотного соединения образуется непроницаемая перемычка между внешней (апикальной) и базолатеральной поверхностями эпителиальных клеток. При липких соединениях клетки связаны с помощью опоясывающих (длинные волокна) и точечных (расположены непосредственно в месте скрепления) десмосом. Гемидесмосомы (полудесмо-сомы) соединяют эпителиальные клетки через базальные мембраны (производные экстрацеллюлярного матрикса).
Причина болезни Шарко—Мари—Тута, сцепленной с Х-хромосомой, — дефект белка, участвующего в щелевом соединении клеток.
Большинство лекарственных препаратов вступают во взаимодействие с рецепторами цитоплазматической мембраны. Различные противоопухолевые препараты, такие, как винкристин или винбластин, повреждают систему микротрубочек, в то время как колхицин, применяемый для исследования хромосом, угнетает клетки во время метафа-зы митоза. Клофибрат снижает продукцию дополнительных пероксисом, его используют для снижения уровня липопротеинов в сыворотке крови.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Ядро клетки и ядерная оболочка
Основные положения:
• Ядро является самой крупной клеточной органеллой и ограничено оболочкой, состоящей из двух мембран
• Часть ядра занимает генетический материал
• Ядерные поры служат средством транспорта больших молекул через ядерную оболочку, обеспечивая вход их в ядро и выход из него
Как показано на рисунке, ядро обычно представляет собой самый крупный видимый компартмент эукариотической клетки, содержит почти весь ее генетический материал (фактически весь, за исключением небольшого числа генов, присутствующих в митохондриях и хлоропластах).
Размеры ядра зависят от количества содержащейся в нем ДНК. Поэтому занимаемый им объем широко варьирует; обычно для клеток дрожжей он составляет 1-2% от всего объема клетки, а для большинства соматических клеток животных около 10% (В зависимости от типа организма и клеток ядро выглядит по-разному). Генетический материал образует массу, называемую хроматин, который занимает часть ядра.
Ядро окружено оболочкой, которая состоит из двух концентрически расположенных мембран, наружной и внутренней (Ядро окружено ядерной оболочкой). Между двумя мембранами находится люмен. Внешняя мембрана оболочки ядра переходит в мембраны ЭПР, а люмен оболочки сливается с люменом ЭПР. Внутренняя ядерная мембрана обычно поддерживается сетью филаментов, которая называется ядерная ламина. Эта сеть находится внутри ядра и заякорена во внутреннюю мембрану.
Поскольку небольшие молекулы свободно перемещаются между цитозолем и ядром, то водная среда в компартментах имеет одинаковый состав. Однако вещества с молекулярной массой, превышающей примерно 40 000 Д (что соответствует небольшим белкам), могут поступать в ядро и выходить из него только при участии системы транспорта через комплексы ядерных пор, которые закреплены в оболочке ядра.
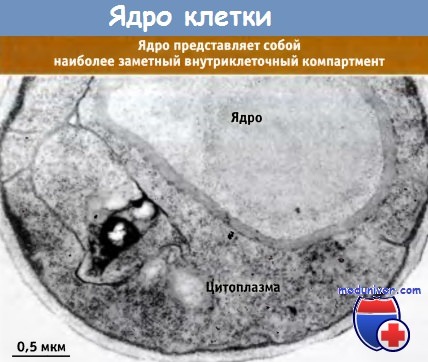
Хотя часть клетки, которую занимает ядро, для разных клеток различна,
в эукариотической клетке обычно оно представляет собой наиболее заметный внутриклеточный компартмент.
Поры ядерной оболочки наиболее заметны при исследовании ядра в электронном микроскопе (Ядерные поровые комплексы представляют собой симметричные каналы). Каждый комплекс имеет центральный канал, через который осуществляется импорт и экспорт молекул, по размерам превышающим предел, при котором возможна их свободная диффузия. Эти каналы обеспечивают различное содержание белков и других больших молекул в ядре и цитоплазме клетки.
В ядре находятся более мелкие компартменты, которые обладают специальными функциями, хотя они и не ограничены мембранами (Ядро содержит субкомпартменты, которые не окружены мембраной). Основным субкомпартментом в ядре является ядрышко, видимое в световом микроскопе. В ядрышке происходит синтез рибосомальных РНК и сборка субъединиц рибосом.
Зачем клеткам эукариот нужно ядро? Ядро защищает ДНК и обеспечивает клетке возможность сконцентрировать регуляторные белки и ферменты репарации в одном месте. Геном человека в 750 раз превышает геном Е. coli, и, таким образом, каждая определенная последовательность ДНК занимает, соответственно, меньшую часть генома. Различные регуляторные белки должны присутствовать в больших концентрациях для того, чтобы они могли найти свои мишени.
Это облегчается тем, что структура-мишень (например, геном) и регуляторные белки сосредоточены в небольшой части клетки (например, в ядре). Ядро также обеспечивает большую степень защиты генома от случайных повреждающих воздействий.
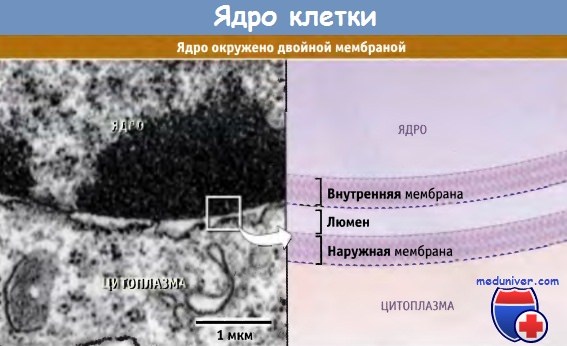
Ядро окружено оболочкой, состоящей из наружной и внутренней мембран.
Мембраны разделены люменом, переходящим в люмен эндоплазматического ретикулкума.
Наличие в клетке ядра имеет важные последствия. На рисунке ниже показано, что транспорт макромолекул между ядром и цитоплазмой носит двухсторонний характер. Все необходимые ядру белки (включая белки репликации и транскрипции) должны поступать из цитоплазмы. В то же время иРНК транскрибируются в ядре, но должны выходить в цитоплазму, где происходит синтез белка. Эта картина полностью отлична от характерной для клеток прокариот, у которых процессы транскрипции и трансляции сопряжены друг с другом, т. е. происходят в одно время и в одном месте.
Регуляция транспорта молекул в ядро и их выхода из него представляет собой один из важнейших регуляторных механизмов.
Обычно клетка эукариот содержит одно ядро. Однако в некоторых исключительных случаях образуются клетки, содержащие много ядер. Это особенно характерно на ранних этапах развития насекомых, например дрозофилы. В этом случае происходит большое количество делений ядра, не сопровождающихся клеточным делением, и образуется синцитий, содержащий сотни ядер, находящихся в общей цитоплазме. Другой пример образования синцития -слияние мышечных клеток млекопитающих.
В качестве иллюстрации другого крайнего случая назовем некоторые дифференцированные клетки, например зрелые эритроциты млекопитающих, у которых отсутствует ядро. (В подтверждение того, что они все-таки являются клетками, заметим, что эритроциты представляют собой продукты терминальной дифференцировки, которые произошли из клеток.)
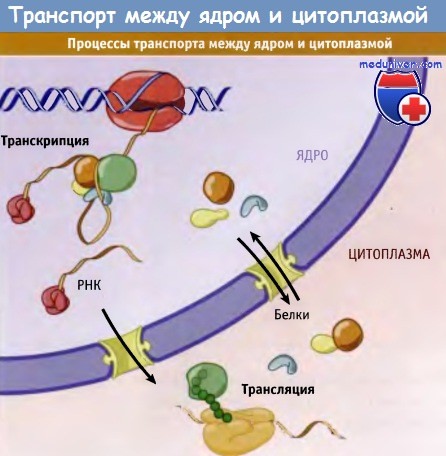
РНК транспортируется из ядра в цитоплазму,
а белки транспортируются в ядро (иногда они снова выходят из ядра).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

