Чем опасен наркоз при гепатите с
Обновлено: 23.04.2024
ПВТ — противовирусная терапия
СН — сердечная недостаточность
ХГС — хронический гепатит С
HCV — вирус гепатита С
NT-pro-BNP — N-концевой предшественник мозгового натрийуретического пептида
Хронический гепатит С (ХГС) — актуальная междисциплинарная проблема. Хорошо изучены различные внепеченочные проявления ХГС, такие как смешанная криоглобулинемия, гломерулонефрит, поздняя кожная порфирия, красный плоский лишай, синдром Шегрена и др. Однако существует целый ряд системных проявлений, которые нуждаются в более тщательном изучении, в частности поражение сердца. При ХГС описаны миокардит, гипертрофическая (ГКМП) и дилатационная (ДКМП) кардиомиопатии, коронарит вследствие криоглобулинемического васкулита мелких сосудов сердца, аритмогенная дисплазия правого желудочка, аневризма левого желудочка, раннее развитие атеросклероза и ишемической болезни сердца [1—6]. Возможно развитие цирротической кардиомиопатии (КМП), которая наблюдается при циррозах печени различной этиологии, в том числе вирусной. Развивается диастолическая дисфункция миокарда и синдром удлиненного интервала Q—T, выраженность которого увеличивается по мере нарастания декомпенсации функции печени [7—11]. Наконец, широко используемая противовирусная терапия (ПВТ) ХГС может сопровождаться кардиотоксичностью интерферона (ИФН), имеющей клинические особенности и нередко проявляющейся развитием декомпенсации деятельности сердца.
Миокардит является одним из мало изученных внепеченочных проявлений ХГС [3, 4]. В клинике им. Е.М. Тареева описана серия наблюдений из 22 больных хроническим гепатитом вирусной этиологии с миокардитом, у 13 из которых диагностирован цирроз печени. Поражение сердца у 4 больных стало причиной летального исхода. В 3 наблюдениях на аутопсии выявлена картина хронического активного миокардита: обширные очаги лизиса кардиомиоцитов (КМЦ) с очаговой лимфогистиоцитарной инфильтрацией; многочисленные продуктивные и продуктивно-деструктивные эндофлебиты; диффузный фиброз стромы; лимфогистиоцитарная инфильтрация стромы. В одном случае диагностированы диффузный кардиосклероз, миокардиофиброз, диффузный склероз эндокарда. Особенностью двух других наблюдений явились выраженные изменения в проводящей системе сердца: волокна проводящей системы замурованы в грубоволокнистую фиброзную ткань, отмечены резко выраженная дистрофия и некробиоз КМЦ. У этих больных наблюдались различные нарушения проводимости [4].
Первичные КМП представляют собой гетерогенную группу заболеваний миокарда различной этиологии. Наибольший интерес к проблеме миокардитов и КМП, ассоциированных с HCV-инфекцией, отмечен у исследователей из Японии. Выявлена высокая распространенность HCV-инфекции у больных ГКМП, ДКМП и миокардитом [17—20]. При многоцентровом исследовании по программе Комитета по изучению идиопатических КМП в Японии, антитела HCV в сыворотке выявлены у 74 (10,6%) из 697 больных ГКМП и у 42 (6,3%) из 633 больных ДКМП, значительно превышая частоту обнаружения антител HCV у сопоставимых по возрасту доноров крови (2,4%) [20].
По данным A. Matsumori [1], у 113 больных ГКМП, HCV-инфекция диагностирована у 16 (14,1%), причем ни у одного из них не было семейного анамнеза по ГКМП. В 4 наблюдениях имелись указания на гемотрансфузии в анамнезе, у 10 больных определялся повышенный уровень трансаминаз в сыворотке, у 7 выявлен гепатоцеллюлярный рак. При морфологическом исследовании отмечены умеренная или выраженная гипертрофия правого и левого желудочков, фиброз различной степени и умеренная клеточная инфильтрация миокарда. РНК HCV генотипа 1b выявлена в сыворотке у 7 больных, РНК HCV в ткани миокарда — у 6, минус-цепи РНК HCV обнаружены в биоптатах сердца у 2 больных. Другая группа исследователей выявила антитела HCV у 18 (22,5%) из 80 больных ГКМП [21].
Многоцентровое исследование, проводимое научным комитетом по изучению КМП Всемирной федерации заболеваний сердца, ставило задачу выявления вирусных геномов энтеровирусов, аденовируса, цитомегаловируса и HCV в формалиновых срезах ткани сердца. Геном HCV выявлен в 2 (18%) из 11 биоптатов больных ДКМП и миокардитом в Италии и у 4 (36%) из 11 больных в США, у 2 из них выявлен миокардит и у 2 — аритмогенная дисплазия правого желудочка. Несмотря на то что метод выявления генома HCV в парафиновых (фиксированных в формалине) срезах менее чувствительный, чем в замороженных образцах, предполагается, что HCV-инфекция может быть более частой причиной ряда заболеваний миокарда, в первую очередь миокардита [22]. Показано также, что частота развития КМП, обусловленных HCV, варьирует в различных регионах мира и различных популяциях. Среди больных КМП в Канаде (Ванкувер) РНК HCV не обнаружена ни в одном из 24 образцов ткани сердца. Ряд европейских исследователей также высказываются против связи HCV-инфекции и заболеваний сердца [23].
В последние годы также изучается вопрос о взаимосвязи ХГС и уровня натрийуретических пептидов. Так, в крупном ретроспективном исследовании антитела к HCV выявлены у 59 (4,4%) из 1355 больных с СН неясной этиологии, что значительно превышало частоту НCV-инфекции в общей популяции (1,8%). Уровень N-концевого предшественника мозгового натрийуретического пептида (NT-pro-BNP) в сыворотке у больных с СН и ХГС достоверно выше, чем у больных с СН без маркеров HCV (р<0,0001) [24]. Интересным представляется исследование А. Antonelli и соавт. [25], которые выявили повышенный уровень NT-pro-BNP у 34% больных ХГС, в то время как в группе неинфицированных, сопоставимых по полу и возрасту, повышение данного лабораторного показателя отмечалось лишь в 6% наблюдений. Это может свидетельствовать в пользу субклинического поражения сердца у некоторых больных ХГС.
Генетические факторы и патогенетические звенья поражения сердца при HCV. Несмотря на то что в последнее время в литературе описываются клинические наблюдения ДКМП и ГКМП, ассоциированных c HCV [1, 6, 18, 21]; механизм, посредством которого HCV приводит к их развитию, полностью не изучен. У ряда пациентов с ассоциированной с HCV КМП идентифицированы HLA- и не-HLA-гаплотипы, которые дают основание полагать, что фактором развития данного вида поражения сердца является генетическая предрасположенность. Так, в развитии ДКМП участвует α-фактор некроза опухоли (α-ФНО) — один из ключевых цитокинов, усиление синтеза которого наблюдается при HCV-инфекции [26].
Причиной миокардита, приводящего к ДКМП и СН, могут быть некоторые вирусы, обладающие тропизмом к миокарду [27, 28]. Считается, что в основе развития вирусного миокардита и прогрессирования его в КМП лежат механизмы смерти клетки в результате апоптоза, а также индуцированные вирусами иммунные реакции [29]. Предполагаемым иммунным механизмом является постоянное обновление иммунокомпетентных клеток и продуцируемых ими цитокинов [30, 31]. Среди всех цитокинов, участвующих в развитии и прогрессировании миокардита, наиболее важную роль играет α-ФНО [32—34]. Отдельные исследования показали, что имеется связь как между сниженной функцией миокарда и повышенной экспрессией α-ФНО, так и между концентрацией α-ФНО в плазме и миокарде у больных миокардитом [35] и ДКМП [36]. С помощью иммуногистохимического анализа установлено, что α-ФНО продуцируется КМЦ при вирусных миокардитах, ассоциированных с аденовирусом, цитомегаловирусом, вирусом Эпштейна—Барр, вирусами гриппа, А и B, а также HCV [35, 37]. Отрицательный инотропный эффект α-ФНО обусловлен связыванием α-ФНО со специфическими рецепторами TNFR1 и TNFR2, которые экспрессируются на мембране КМЦ [38]. Также вероятно, что α-ФНО ингибирует кальциевые каналы L-типа, что приводит к снижению систолической функции миокарда [39]. Другим механизмом, посредством которого α-ФНО влияет на миокард, является стимулирование продукции оксида азота (NO), который оказывает отрицательное инотропное действие на миокард, действуя как эндогенный ингибитор и фактически уменьшая положительный инотропный ответ на β-адренергическую стимуляцию [40].
Некоторые гены, например гены системы HLA, причастны к клиренсу и персистенции HCV-инфекции [41]. В нескольких исследованиях сообщалось, что ДКМП и ГКМП ассоциируются с некоторыми аллелями системы HLA. Так, у инфицированных HCV пациентов, у которых развивается ДКМП, более часто выявляются гаплотипы HLA-DPB1*0901 и HLA-DRB1*1201, а у инфицированных HCV пациентов с ГКМП — гаплотипы HLA DRB1*0901 и DQB1*0303 [1, 42]. По данным других авторов, развитие ДКМП, ассоциированной с HCV, наиболее отчетливо коррелирует с аллелями не-HLA-генов, чем с генами системы HLA [43]. Таким образом, пилотные исследования демонстрируют, что имеется генетическая предрасположенность к развитию поражения миокарда у пациентов с ХГС (рис. 1).

Рис. 1. Генетическая предрасположенность к поражению миокарда при HCV-инфекции.
По данным N. O’Garra и соавт. [44], в печени развивается выраженный CD4+ Th1 клеточный ответ, наиболее вероятно индуцируемый интерлейкином (ИЛ) 12, ИФН-α и ИФН-β, которые продуцируются моноцитами, нейтрофилами и макрофагами после стимуляции Toll-like-рецепторов HCV производными продуктами. Если определенные гаплотипы кодируют молекулы главного комплекса гистосовместимости (ГКГ) II класса с более высоким сродством к производным пептидам HCV, то их функция как молекул, презентирующих антигены клеткам Th1 CD4+, повышается. После активации клетки Th1 CD4+ продуцируют ИФН-γ, который активирует макрофаги к продукции провоспалительных цитокинов [44]. Главными цитокинами, продуцируемыми макрофагами, являются ИЛ-1 и α-ФНО [45], которые могут приводить к обновлению иммунных клеток и высокой концентрации α-ФНО в миокарде.
Другим механизмом, посредством которого гаплотипы HLA могут влиять на развитие ДКМП, ассоциированной с HCV, в контексте α-ФНО является так называемая неклассическая функция клеток ГКГ II класса, т. е. их роль в качестве сигнальных трансдукционных молекул, активируемых суперантигенами в клетках некоторых типов [46, 47]. Суперантигены являются протеинами бактериального или вирусного происхождения, которые активируют до 20% Т-клеточной популяции путем одновременного связывания Т-клеточных рецепторов и молекул ГКГ II класса, что приводит к массивному высвобождению цитокинов, которые секретируются как Т-клетками, так и антигенпрезентирующими клетками [48—50]. В контексте полиморфизма HLA предполагалось, что они принимают непосредственное участие в исходе, к которому приводит продукция цитокинов, стимулируемая суперантигенами [51, 52]. Можно предположить, что определенные гаплотипы HLA кодируют эпитопы молекул ГКГ II класса с высоким сродством к производным HCV суперантигенам или антителам, а это ведет к чрезмерной продукции цитокинов, в частности α-ФНО. Более активное обновление иммунных клеток может привести у генетически предрасположенных инфицированных HCV пациентов к развитию миокардита и впоследствии к ДКМП. Следует отметить, что часто при ассоциированном с HCV хроническом активном миокардите у пациентов отмечался нормальный уровень активности печеночных трансаминаз в сыворотке крови вплоть до формирования терминальной стадии СН [53].
Развитие и прогрессирование вирусного миокардита, в том числе у больных ХГС, осуществляется через различные патогенетические звенья (рис. 2): 1) прямое действие вируса на миокард; 2) непрямое (иммунологическое) действие; 3) смерть клеток в результате апоптоза.

Рис. 2. Механизмы поражения миокарда при HCV-инфекции. АФК — активные формы кислорода.
Воздействие HCV на миокард. Ряд исследователей указывают на возможность прямого воздействия HCV на миокард. Показано, что HCV реплицируется в миокарде, о чем свидетельствует выявление там негативных цепей РНК [53—55]. Механизм, посредством которого протеин HCVcorе вызывает повреждение миокарда, остается неясным; однако он может быть сходным с механизмом поражения печени. Показано, что изменения в структуре рецепторов TNFR1, вызываемых протеином HCVcorе, повышают чувствительность клеток к цитолизу, опосредованному α-ФНО [56]. Кроме того, протеин HCVcorе вызывает дисфункцию митохондрий, что приводит к развитию окислительного стресса клеток печени [57, 58]. Фактически, протеин HCVcore ограничивает свое действие в митохондриях, в частности он взаимодействует с наружной мембраной митохондрий, повышает поглощение кальция митохондриями и вызывает окисление глутатиона, что приводит к дальнейшему повышению продукции АФК [59, 60]. Повышение образования АФК инициирует продукцию α-ФНО [61], который, как отмечено ранее, оказывает отрицательное инотропное действие на миокард. В некоторых ранее проводимых исследованиях продемонстрировано, что у пациентов с острой и хронической СН, развившихся в исходе КМП, в миокарде определяется повышение выработки АФК [62, 63].
К тому же ряд исследований на животных подтверждают роль протеина HCVcore в развитии КМП. В частности, развитие КМП наблюдалось у трансгенных мышей, носителей гена HCVcore, в возрасте 12 мес. Гистологический анализ миокарда этих мышей выявил гипертрофию КМЦ, кардиальный фиброз, дезорганизацию, дефицит и лизис миофибрилл, вакуолизацию и деформацию ядер, повышенное количество митохондрий неправильной формы [55], что убедительно подтверждает определяющие действие протеина HCVcore на развитие КМП, ассоциированной с HCV.
Непрямой иммунологический механизм поражения миокарда включает вовлечение в патологический процесс В-клеток, Т-клеток и макрофагов. Участие В-клеток в КМП, ассоциированной с HCV, предположено в результате обследования 3 пациентов с ассоциированным с HCV миокардитом, ответивших на иммуносупрессивную терапию. В сыворотке крови этих больных выявлены антитела к миокарду, что дало основание предполагать иммунологический механизм повреждения клеток. В дальнейшем подтверждение иммуноопосредованного механизма КМП, ассоциированной с HCV, было основано на эффективности иммуносупрессивных препаратов (преднизолон и азатиоприн), терапия которыми привела к нормализации размеров камер сердца и регрессу признаков СН, несмотря на продолжающуюся персистенцию HCV [54].
Прямой и непрямой механизмы развития ДКМП, ассоциированной с HCV, связаны со смертью клеток через апоптоз. Благодаря способности повышать продукцию АФК, протеин HCVcore может инициировать митохондриальный путь апоптоза. АФК могут вызывать диссоциацию цитохрома С на внутренней мембране митохондрий, что приводит к активации каспаз, результатом чего является фрагментация геномной ДНК и смерть клетки [64]. В результате связывания лигандов с внеклеточными рецепторами суперсемейства рецепторов α-ФНО происходит активация рецепторзависимого сигнального пути апоптоза [65]. Наиболее важными лигандами этих рецепторов являются α-ФНО и Fas-лиганд (FasL). Высокий уровень α-ФНО в миокарде у пациентов с ассоциированным с HCV миокардитом может активировать данный механизм смерти клеток путем взаимодействия с рецепторами ФНО [66].
Заключение
Имеются убедительные доказательства того, что поражение сердца служит одним из внепеченочных проявлений HCV-инфекции. Механизм, посредством которого HCV может приводить к поражению миокарда у генетически предрасположенных пациентов, является многофакторным и включает прямое повреждающее действие вируса, аутоиммунный механизм и апоптоз.
Поражение миокарда при ХГС может прогрессировать в хронический персистирующий миокардит через прямой (вирусный) и непрямой (иммунный) механизмы повреждения, которые приводят к активации зависимой от рецепторов смерти КМЦ, результатом чего является развитие фиброза миокарда с возможной трансформацией в ДКМП. Кроме того, описаны случаи взаимосвязи HCV и ГКМП.
До настоящего момента HCV-инфицированным больным с вовлечением сердца ПВТ, как правило, не проводилась из-за побочных эффектов ИФН. Однако за последние несколько лет в ПВТ вирусного гепатита С произошли кардинальные изменения. Длительное изучение механизмов репликации HCV привело к созданию ингибиторов протеаз HCV (NS¾A, NS5A, NS5B), которые позволяют достичь элиминации вируса у 90—99% пациентов за существенно более короткий срок (как правило, 12 нед) без применения препаратов ИФН (так называемая безинтерфероновая терапия). Это делает данную терапию гораздо более безопасной и хорошо переносимой, в том числе в отношении миокарда [67—69].
Нуждается в отдельном изучении вопрос эффективности и безопасности ПВТ у пациентов с ХГС и ассоциированного с ним поражения сердца, включая сравнение только ПВТ и сочетания ПВТ с сердечно-сосудистыми препаратами и/или иммуносупрессорами. Выявление антител к миокарду и определение уровня α-ФНО в сыворотке крови во время терапии может быть использовано для оценки влияния терапии на данные маркеры.
Советы хирургам по защите от инфекций передающихся через кровь
1. Какие заболевания, передающиеся с кровью, имеют наибольшее значение для хирурга?
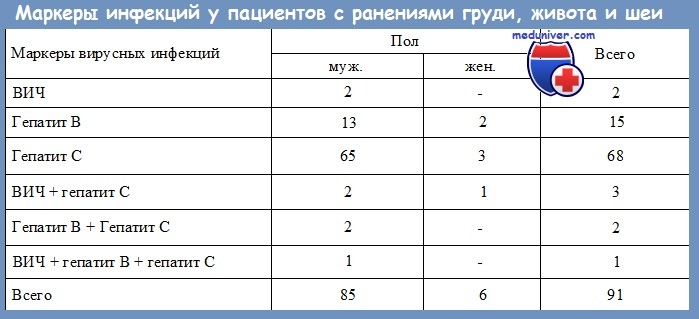
Обычно среди возбудителей, передающихся при контакте с зараженной кровыо, основное внимание уделялось вирусу иммунодефицита человека (ВИЧ), однако рост заболеваемости гепатитом С в Северной Америке привел к тому, что именно гепатит сейчас является наиболее частым среди заболеваний, передающихся таким путем.
В настоящее время инфицирование вирусом гепатита В, который уже почти 50 лет считается профессиональной патологией хирургов, реже приводит к развитию заболевания, что связано с распространением прививок и разработкой сравнительно эффективной схемы лечения в случае контакта с вирусом.
2. Каков сравнительный риск заражения ВИЧ, HBV и HCV?
а) ВИЧ. На данный момент приблизительно 1 миллион жителей США инфицированы ВИЧ. Последние наблюдения показывают, что передача ВИЧ в больничных условиях происходит редко. Медработники составляют только 5% от всех больных СПИДом, и у большинства из них есть другие факторы, помимо профессиональных, вероятно, и вызвавшие заболевание. Наибольший профессиональный риск отмечен у медицинских сестер и работников лабораторий.
С 1 января 1998 года не отмечено ни одного документированного случая передачи ВИЧ от больного к врачу в результате профессионального контакта.
б) HBV. Нет сомнений, что все хирурги за время нормальной трудовой карьеры контактируют с HBV. Считается, что 1,25 миллиона жителей США болеют хроническим гепатитом В. Чрескожная инъекция инфицированной иглой приблизительно в 30% случаев приводит к развитию острого заболевания. В 75% гепатит В протекает клинически скрыто, а 10% инфицированных на всю жизнь остаются носителями вируса.
У многих носителей, потенциально заразных для окружающих, заболевание протекает бессимптомно, с минимальным прогрессированием или без прогрессирования. Примерно в 40% болезнь постоянно прогрессирует, приводя к циррозу, печеночной недостаточности или даже к генатоцеллюлярному раку.
в) HCV. Гепатит С стал для хирургов самой главной проблемой. Считается, что хроническим гепатитом С страдают приблизительно 4 миллиона жителей США. Риск сероконверсии при чрескожной инъекции инфицированной иглой составляет около 10%, однако в 50% острое заболевание приводит к хроническому носительству инфекции. О течении гепатита С до сих пор существуют различные мнения, однако почти у 40% больных хроническая HCV-инфекция приводит к развитию цирроза.
В последнем случае высок риск развития рака печени, вероятность которого достигает 50% в течение 15 лет.
3. Обеспечивает ли вакцинация против гепатита В полную защиту от заболевания?
В настоящее время для всех хирургов и лиц, работающих в операционной, доступна эффективная вакцинация против гепатита В. Вакцину против гепатита В получают с помощью рекомбинантной технологии; она не является разрушенными частицами вируса, полученными от инфицированных людей. Вводят три дозы вакцины, после чего следует определить титр поверхностных антител, чтобы убедиться в успешности вакцинации.
Приблизительно у 5% вакцинированных людей выработки антител не происходит и требуется повторная вакцинация. Некоторые люди остаются рефрактерными к вакцинации, для них сохраняется риск острого гепатита В. Вакцинация не гарантирует иммунизацию.
Согласно некоторым исследованиям, 50% практикующих хирургов не обладают достаточным иммунитетом к HBV из-за различных причин: отсутствия вакинации у старых хирургов, более чем 5-летнего срока после вакцинации, недостаточного количества рекомбинантной вакцины или неправильной вакцинации и, наконец, неспособности выработать соответствующий иммунный ответ.
4. Существует ли риск заражения больных от хирургов, инфицированных HBV?
Передача вируса гепатита В от хирурга к больному документирована. Анализ крови хирургов, которые могут заразить больных, как правило, положителен на е-антиген вируса гепатита В. Е-антиген является продуктом распада вирусного нуклеокапсида и говорит об активной репликации вируса в печени. Обнаружение е-антигена свидетельствует о высоких титрах вируса и сравнительно высокой заразности больного.
Большое количество документированных случаев передачи гепатита В больным от лиц, занятых в хирургии, может вызвать особенные проблемы и ограничение клинической деятельности для клиницистов, передавших эту инфекцию. В одном из последних отчетов из Англии сообщается о передаче вируса гепатита В больному даже от хирурга с отрицательным анализом па е-антиген HBV.
В последнее время одна национальная организация призывает ограничить деятельность е-антиген-положительных хирургов. Вопрос, можно ли хирургу с хроническим гепатитом В продолжать практику, будет обсуждаться в будущем.
5. Какова правильная тактика при чрескожном контакте с кровью больного, у которого есть гепатит В?
Тактика зависит от вакцинированности медработника. Если он вакцинирован и имеет положительный титр антител, то ничего предпринимать не надо. Если медработник не вакцинирован и не имеет антител к HBV, то ему или ей следует ввести дозу анти-HBV иммуноглобулина и начать серию вакцинации против гепатита В.
Медработникам, которые ранее были успешно вакцинированы от гепатита В, однако не имеют или имеют незначительный титр антител, следует ввести дозу анти-HBV иммуноглобулина и повторную дозу вакцины против гепатита В. Поскольку в большинстве случаев таких контактов с больным неизвестно, инфицирован он или нет, то, в общем, хирургам необходимо знать, есть ли у них антитела, и периодически повторять иммунизацию против гепатита В через каждые 7 лет.
6. Чем HCV отличается от HBV? Кто из них опаснее?
а) Заболеваемость в США:
- HBV: примерно 1,25 миллиона больных.
- HCV: примерно 4 миллиона больных.
б) Путь и последствия заражения:
- HBV: ДНК-вирус, передающийся с кровью; острая форма переходит в хроническую в 10% случаев.
- HCV: РНК-вирус, передающийся с кровью; острая форма переходит в хроническую в 50% случаев.
в) Профилактика:
- HBV: эффективная рекомбинантная вакцина.
- HCV: в настоящее время вакцины не существует.
г) Защита после контакта:
- HBV: людям, которые не были вакцинированы и не имеют антител к HBV, целесообразно введение анти-HBV иммуноглобулина.
- HCV: клиническая эффективность анти-HCV иммуноглобулина не доказана. Среди больных, с которыми имеют дело хирурги в США, больше лиц с хроническим гепатитом С, чем с хроническим гепатитом В, а вакцины против HCV-инфекции нет. Риск сероконверсии для гепатита С составляет 10% против 30% для гепатита В, однако HCV-инфекция гораздо чаще переходит в хроническую форму (50% против 10%). Поэтому HCV-инфекция представляет для хирургов гораздо большую угрозу.
7. Насколько высок риск для медработника заразиться ВИЧ?
Передача инфекции подтверждалось, если был зафиксирован контакт медработника с кровью или биологическими жидкостями инфицированного больного, после чего была отмечена сероконверсия ВИЧ. Профессиональный риск безусловно выше у медицинских сестер и работников лабораторий. Общее число заражений несравнимо с большим количеством контактов с вирусом, которые, по всей видимости, имели место с начала эпидемии (начало 1980-х годов).
8. Меньше ли риск заражения ВИЧ при выполнении операций лапароскопическим способом?
В последнее время лапароскопическую хирургию у ВИЧ-инфицированных больных считают хорошей заменой открытым вмешательствам. Данный метод уменьшает вероятность контакта с кровью и острыми инструментами, однако за счет некоторых его особенностей возможно заражение хирургов иными путями, чем при обычной операции. При десуфляции пневмонеритонеума во время лапароскопических вмешательств происходит разбрызгивание капелек ВИЧ-инфицированной крови в операционной. Риск заражения можно уменьшить, направляя воздух в закрытую систему и принимая соответствующие меры предосторожности при смене инструментов.
9. Является ли эффективным методом защиты использование двойных перчаток?
Вследствие возможности контакта поврежденной кожи с кровыо риск заражения людей, работающих в операционной, вирусом гепатита или ВИЧ повышен. Хотя двойные перчатки могут не предотвратить повреждения кожи, показано, что они явно уменьшают вероятность контакта с кровыо. Исследования, посвященные контакту с кровыо в операционной, показали, что в 90% такой контакт происходит па коже рук хирурга дистальнее локтя, включая область, защищенную перчатками. Согласно одному исследованию, если хирург надевает две пары перчаток, то вероятность контакта его кожи с кровыо уменьшается па 70%. Прокол наружной пары перчаток наблюдали в 25% случаев, в то время как прокол внутренней пары — только в 10% (в 8,7% у хирургов и в 3,7% у ассистентов). Прокол внутренней пары перчаток отмечался при операциях, длившихся более 3 часов; он всегда сопровождался проколом наружной пары. Наибольшее повреждение происходило па указательном пальце неведущей руки.
10. Представляет ли большую угрозу для хирургов попадание капелек в глаза?
Исследование эпидемиологических центров показало, что приблизительно в 13% случаев документированной передачи ВИЧ имел место контакт со слизистой и кожей. Попадание капелек в глаза часто недооценивают, хотя этот вид контакта легче всего предотвратить. В недавно проведенном исследовании изучали 160 пар защитных экранов для глаз, используемых хирургами и ассистентами. Все операции длились 30 минут и более. На экранах подсчитывали количество капелек, вначале макроскопических, потом микроскопических. Кровь была обнаружена на 44% из исследуемых экранов. Хирурги замечали брызги всего в 8% случаев. Лишь 16% капелек были видны макроскопически. Риск попадания капелек в глаза был выше для хирурга, чем для ассистента, и увеличивался с увеличением времени операции. Доказано, что важным является также тип вмешательства: риск выше при сосудистых и ортопедических операциях. Защита глаз должна быть обязательной для всех работающих в операционной, особенно для непосредственно оперирующих лиц.
11. Как часто кровь хирурга контактирует с кровью и биологическими жидкостями больного?
Контакт с кровью возможен при повреждениях кожи (уколы, порезы) и соприкосновении с кожей и слизистыми (прокол перчатки, царапины на коже, попадание капелек в глаза). Контакт вследствие повреждения кожи наблюдают в 1,2-5,6% хирургических процедур, а контакт вследствие соприкосновения с кожей и слизистыми — в 6,4-50,4%. Разница в приводимых цифрах обусловлена различиями в сборе данных, выполняемых процедурах, хирургической технике и мерах предосторожности. Например, хирурги в San Francisco General Hospital принимают крайние меры предосторожности, надевая водонепроницаемую форму и две пары перчаток. Случаев передачи инфекции какому-нибудь медработнику при контакте его неповрежденной кожи с инфицированными кровью и биологическими жидкостями не отмечено. Однако сообщалось о заражении ВИЧ медработников, не имеющие других факторов риска, вследствие контакта с их слизистыми и кожей ВИЧ-инфицированной крови. Вероятность передачи инфекции при таком контакте остается неизвестной, поскольку в проспективных исследованиях у медработников после контакта их слизистой и кожи с ВИЧ-инфицированной кровью сероконверсии отмечено не было.
Риск заражения существует для всех работающих в операционной, однако он намного выше для хирургов и первых ассистентов, поскольку 80% случаев загрязнения кожи и 65% случаев повреждений приходится именно на них.
12. Только ли хирургической техникой объясняется загрязнение кожи?
Кожа с царапинами может контактировать с кровью или биологическими жидкостями даже при соблюдении всех мер предосторожности. К сожалению, далеко не вся защитная одежда защищает в равной степени. В одном исследовании отмечены дефекты у 2% стерильных хирургических перчаток сразу после их распаковки.
13. Какова вероятность сероконверсии после контакта крови медработника с кровью больного для ВИЧ и HBV?
Вероятность сероконверсии после укола иглой составляет 0,3% для ВИЧ и 30% для HBV.
14. Какова вероятность для хирурга заразиться ВИЧ на рабочем месте за все время его карьеры?
Риск передачи ВИЧ хирургу можно вычислить, зная частоту обнаружения ВИЧ у хирургических больных (0,32-50%), вероятность повреждения кожи (1,2-6%) и вероятность сероконверсии (0,29-0,50%). Таким образом, риск заразиться ВИЧ от конкретного больного находится в интервале от 0,11 на миллион до 66 на миллион. Если хирург выполняет 350 операций в год в течение 30 лет, то риск заражения на протяжении всей карьеры для него составляет от 0,12% до 50,0%, в зависимости от переменных величии. В этом подсчете допущено несколько предположений:
а) Мы допустили, что заболеваемость ВИЧ является величиной постоянной, однако считается, что в Соединенных Штатах за год она увеличивается на 4,0-8,6%.
б) Учитывается только контакт с зараженной кровью при повреждении кожи; возможность контакта со слизистыми и кожей (без ее повреждения) не принимается во внимание.
в) Риск считается одинаковым для всех операций, однако известно, что он зависит от длительности и срочности операции, а также от объема кровопотери.
Очевидно, что эти предположения не способствуют точности вычислений, поэтому подсчитанная вероятность — всего лишь грубая оценка на основании имеющихся данных.
15. Знают ли хирурги о своем профессиональном риске?
16. Есть ли эффективные методы уменьшить риск заражения хирургов инфекциями, передающимися с кровью?
Профилактике заражения HBV, помимо общих мер предосторожности, способствует высокоэффективная вакцина, которая, однако, не используется так часто, как следовало бы. Большинство хирургов в возрасте 45 лет и старше не вакцинированы. Также отработан протокол лечения после контакта. Наиболее прагматичный подход для профилактики передачи HCV и ВИЧ — уменьшить вероятность повреждения кожи и контакта с кожей и слизистыми за счет применения оптимальных методик и мер предосторожнсти.
Наконец, при попадании крови необходимо быстро ее удалить. При загрязнении кистей или рук следует их немедленно обработать. Если это невыполнимо, то область контакта надо смочить раствором повидон-йода, а когда это будет возможно — обработать.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Риск хирургической операции при болезнях печени (шкала Чайлд-Пью)
Заболевания печени могут служить причиной развития основных колоректальных симптомов и оказывать влияние на течение сопутствующих колоректальных заболеваний. Компенсированная функция печени является не только обязательным условием поддержания гомеостаза, но и ключевым моментом в ситуациях, требующих сверхзатрат организма в интра- и послеоперационном периодах. Дисфункция печени развивается как вследствие первичных заболеваний печени (например, цирроза, гепатита), так и вторично, в результате заболеваний внепеченочной локализации (например, при замещении паренхимы печени метастазами, шоковая печень и т.д.). Соответствующая оценка течения колоректальных заболеваний, а также заболеваний печени важна для внесения поправок в программу ведения больных.
Анамнез и дополнительная информация (например, сведения о гепатите, злоупотреблении алкоголем, признаках дисфункции печени в прошлом, метастатическом поражении и т.д.), печеночные знаки при объективном осмотре и изменения биохимических параметров являются руководством к действию.
а) Проблемы:
• Рутинное исследование функции печени у больных без факторов риска: не рекомендовано, показатели функции печени обычно не отражают хронического характера течения заболевания.
• Если назначаемые препараты метаболизируются в печени, они обладают свойством накапливаться.
• Пониженный уровень мочевины и синтеза креатинина => ложное снижение серологических показателей и переоценка почечной функции => в случае необходимости лучше определять клубочковую фильтрацию (GFR).
• Портальная гипертензия:
- Несет значительный риск интраоперационного кровотечения, в частности, в сочетании со спаечным процессом после предыдущих операций.
- Может приводить к варикозу ректальных вен (внимание: геморрой не связан с заболеваниями печени!).
• Риск послеоперационной декомпенсации печени зависит от типа анестезии (например, галотановая), стабильности состояния во время операции, особенностей (например, плановая или ургентная) и типа вмешательства (например, абдоминальные и кардиоторакальные вмешательства значительно увеличивают риск).
• Кровотечение из ЖКТ (пред/послеоперационное) может вызвать декомпенсацию и энцефалопатию.
б) Параметры оценки риска операции при болезнях печени:
• Срочность и объем хирургической операции: плановая или экстренная, абдоминальная или аноректальная операция.
• Сопутствующие осложнения: сердечно-легочные, почечные.
• Тяжесть и прогноз колоректального заболевания.

• Тяжесть и прогноз болезни печени:
- Классификация Чайлд-Пью:
1) Естественное течение болезни и ожидаемая продолжительность жизни.
2) Летальность при абдоминальном хирургическом вмешательстве: Чайлд-Пью А - 5-10%; Чайлд-Пью В - 20-40%; Чайлд-Пью С - 70-80%.
- Подсчет MELD - модели для конечной стадии заболеваний печени:
1) Предиктор 3-х месячной летальности.
2) Предиктор хирургической летальности: < 10 =>благоприятно для операции; 10-15 => всесторонне взвешенное решение об операции; > 15 => операция противопоказана.
- Другие шкалы оценки: Классификация Американской Ассоциации Анестезиологов (ASA), APACHE II (пациенты ПИТ)
- Тесты синтетической функции печени: белок, факторы I (фибриноген), II (тромбопластин), V, VIII, IX, X, XII и XIII.
- Вторичные патологические изменения: тромбоцитопения (гиперспленизм), гепаторенальный синдром, энцефалопатия, портальная гипертензия (например, брюшной и ректальный варикоз).

в) Противопоказания к плановой операции при болезнях печени:
• Острый, особенно фульминантный гепатит.
• Манифестирующая печеночная недостаточность.
• Некорригируемая коагулопатия, тяжелая тромбоцитопения.
• Цирроз печени класса С по Чайлду-Пью, MELD > 15.
• Тяжелое внепеченочное осложнение: сердечно-легочная декомпенсация, заболевание почек.
г) Периоперационное ведение больного с заболеваниями печени
I. Предоперационый период:
• Профилактический трансюгулярный внутрипеченочный портальный шунт (TIPS): показан при портальной гипертензии, 25% риске энцефалопатии.
• Бета-блокаторы.
• Консервативное лечение асцита: диуретики (например, спиронолактон), ограничение жидкости.
• Коррекция коагулопатии: витамин К, свежезамороженная плазма, фактор VIIA.
• Оценка целесообразности нутритивной поддержки.
• Профилактика энцефалопатии: кишечные антибиотики, лактулоза.
II. Интраоперационный период:
• Мониторинг и коррекция коагулопатии: свежезамороженная плазма, фактор VIIA, переливание тромбоцитарной массы.
• Установка перитонеального дренажа (пассивное дренирование), даже если без операции необходимости в дренаже не было.
• Коррекция баланса жидкости: медикаментозное лечение асцита (диуретики, ограничение жидкости).
• Тщательный мониторинг функции печени: протромбиновое время, общий билирубин, электролиты, почечная функция.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Проведение хирургических операций – привычное и даже повседневное явление. Вмешательство со стороны врачей может потребоваться в любой, даже неожиданный момент, начиная от запланированной процедуры и заканчивая внеплановым проведением. Но, существует перечень пациентов и ситуацией, когда по причине противопоказаний врачи не могут оказать помощь пациенту.
Проведение операции при гепатите C
В большинстве случаев ситуация будет зависеть от того, плановая или внеплановая операция. При проведении запланированной процедуры следует ряд серьезной подготовки, врачи рассматривают доступную альтернативу и, при полном отсутствии вариантов, предлагают пациенту лечь на операционный стол.
Плановые операции в этом плане легче. Врач может предпринять соответствующие меры, если имеется возможность предложить больному альтернативу или провести дополнить исследования на предмет активности вируса.
Противопоказания к проведению
Специалист не имеет права отказать в экстренной помощи человеку, находящемуся в критическом положении. Врачебный отказ повлечет ряд последствий, как для человека, так и специалиста.
При гепатите C существенную проблему при проведении хирургического вмешательства составляет нестабильность печени. Неизвестно, как отреагирует желчегонный орган на вводимый наркоз и сможет ли самостоятельно вывести остатки веществ из организма.
Если необходимость вмешательства высокая и приближена к угрозе жизни, специалист может перенести время проведения операции и за дополнительное время подготовиться соответствующим образом.
В некоторых случаях, вмешательство со стороны хирурга является безотлагательным:
- обострение алкогольного гепатита;
- цирроз печени невирусного типа;
- обострение печеночной недостаточности.
В вышеперечисленных случаях под вопросом встает дальнейшая дееспособность органа, поэтому врач, невзирая на имеющийся риск, проводит прямое вмешательство.
К ряду запрещенных случаев, когда больным гепатитом людям отказывают в проведении операции, относятся перекрестные инфекционные вирусологические патологии, оказывающие серьезное воздействие на организм.
Тело человека, под влиянием HCV, испытывает громадную нагрузку. Наличие второго заболевания не оставляет даже шанса для проведения операции без колоссального риска для жизни человека. В подобных ситуациях рассматривается альтернативное лечение или экстренная терапия перекрестной болезни.

К врачу-инфекционисту обратилась 45-летняя женщина с положительным результатом анализа на антитела к гепатиту С.
Жалобы
Никаких симптомов болезни и других проблем со здоровьем пациентка не испытывала. Боли в желудочно-кишечном тракте не было.
Анамнез
При подготовке к операции пациентка прошла необходимые обследования, среди которых был обязательный анализ на вирусные гепатиты. Анализ на гепатит оказался С положительным.
За последние полгода женщина не посещала стоматологов и других операций не делала. Длительное время ходила к мастеру маникюра в один и тот же салон красоты.
Обследование
- общее состояние удовлетворительное;
- печень в пределах нормы (гладкая и эластичная, выступает на 1 см из-под края рёберной дуги);
- кожа и слизистые оболочки чистые, нормального цвета;
- язык влажный с небольшим беловатым налётом на корне;
- дыхание в лёгких в норме, без хрипов;
- живот мягкий, безболезненный, не вздут;
- стул и мочеиспускание в норме.
Так как ранее у пациентки выявили антитела к гепатиту С, а ВИЧ и гепатит В не подтвердились, женщину направили на дообследование:
- биохимический анализ крови — все показатели в норме;
- общий анализ крови — уровень тромбоцитов снижен до 150х10⁹/л;
- развёрнутый анализ крови на гепатит В — антитела не выявлены;
- анализ на антитела к гепатиту С — положительный;
- анализ крови методом ПЦР (полимеразной цепной реакции) — обнаружена РНК гепатита С, генотип 3а;
- УЗИ органов брюшной полости — печень увеличена, структура неоднородная (диффузная), найдены признаки хронического холецистита;
- фибросканирование — обнаружен фиброз (рубцевание) печени 1-й степени по шкале METAVIR.
Диагноз
Хронический вирусный гепатит С минимальной биохимической активности, генотип 3а и фиброз печени 1-й степени.
Лечение
Чтобы наблюдать за течением болезни, пациентку поставили на диспансерный учёт. Ей рекомендовали регулярно посещать инфекциониста и пройти противовирусную терапию.
Женщина исправно принимала противовирусные препараты и вовремя сдавала контрольные анализы. Уже через две недели анализ ПЦР на РНК дал отрицательный результат.
По прошествии полного курса лечения все показатели биохимического и общего клинического анализа крови также были в пределах нормы.
Пациентка оставалась под наблюдением врача в течение трёх месяцев после лечения. По истечению этого срока она сдала контрольные анализы ещё раз — все показатели были в норме.
С учётом проведённой терапии, низкого уровня фиброза печени и устойчивого положительного вирусологического ответа на лечение женщину сняли с учёта.
Заключение
Поэтому пациенты должны быть аккуратны при выборе стоматологической клиники, салона красоты или других заведений, связанных с инвазивными процедурами, например нанесением татуировок, проколами для пирсинга и др.
У нас в стране нет обязательного обследования на вирусные гепатиты, но его желательно периодически проходить всем жителям, особенно тем, кто входит в группу риска.
Читайте также:

