Что такое супрессивная терапия герпеса
Обновлено: 24.04.2024
В статье представлены современные подходы к назначению терапии при острых проявлениях герпесвирусной инфекции, а также к выбору препаратов в целях профилактики ее обострений.
- КЛЮЧЕВЫЕ СЛОВА: герпесвирусная инфекция, этиотропная терапия, супрессивная терапия
В статье представлены современные подходы к назначению терапии при острых проявлениях герпесвирусной инфекции, а также к выбору препаратов в целях профилактики ее обострений.
Герпесвирусные инфекции (ГВИ) широко распространены в мире. В частности, в Европе частота встречаемости достигает 50–80%, в странах Азии – до 90–100% [1]. Свыше 90% населения планеты инфицированы вирусом простого герпеса (ВПГ). До так называемой сексуальной революции прослеживалась четкая зависимость между типом ВПГ и локализацией высыпаний: ВПГ 1-го типа чаще связывали с локализацией в области лица, ВПГ 2-го типа – с генитальной локализацией. В последние годы подобная зависимость утратила актуальность из-за возросшей популярности орогенитальных контактов.
Среди врачей разных специальностей бытует мнение, что только тяжелые формы рецидивирующих ГВИ кожи или слизистых оболочек, инфекционный мононуклеоз, ветряная оспа и опоясывающий герпес требуют применения специфических этиотропных препаратов. Кроме того, часто необоснованно назначают различные иммуномодулирующие препараты в виде монотерапии. Отсутствие этиотропного лечения и наличие сопутствующих заболеваний и состояний, которые расцениваются как провоцирующие факторы, угнетающие иммунный ответ (аутоиммунные заболевания, заболевания желудочно-кишечного тракта и эндокринной системы, острые и хронические воспалительные заболевания органов малого таза, психотравма и хронический стресс, воздействие ультрафиолетового излучения, употребление алкоголя, гормональные циклы, медицинские инвазивные вмешательства, злокачественные новообразования и иммуносупрессивная терапия при их лечении), снижают эффективность терапии, приводят к частым рецидивам заболевания и распространению ГВИ в популяции.
Клинические формы
Клинические формы проявления ГВИ крайне разнообразны. Только при поражении кожи и слизистых оболочек выделяют [2]:
- первичную инфекцию;
- герпетический стоматит (первичный герпес лица и полости рта);
- первичный герпес половых органов;
- первичный герпес другой локализации;
- герпес новорожденных;
- герпетическую экзему Капоши;
- первичный герпес на фоне иммунодефицита;
- рецидивы;
- герпес лица и полости рта;
- герпес половых органов;
- рецидивирующий герпес иной локализации;
- рецидивирующий герпес на фоне иммунодефицита;
- хронический язвенный герпес;
- диссеминированную инфекцию;
- диссеминированное поражение кожи;
- генерализованный герпес (диссеминированное поражение внутренних органов и кожи).
Герпесвирусные инфекции классифицируют по степени тяжести [3]:
- легкое течение (частота рецидивов один-два раза в год, ремиссия не менее шести месяцев);
- среднее (частота рецидивов от трех до пяти раз в год, ремиссия не менее трех месяцев);
- тяжелое (частота рецидивов более шести раз в год, ремиссия от нескольких дней до шести недель);
- бессимптомное.
Диагностика
Диагностика ВПГ представляет большую медико-социальную проблему, поскольку клинические проявления разнообразны и зависят от множества причин: типа вируса, генетической устойчивости человека к ВПГ, тяжести и длительности заболевания, состояния иммунного статуса, механизма инфицирования, вирусной нагрузки, возраста пациента, давности заболевания, наличия сопутствующей патологии.
Алгоритм диагностики ГВИ включает:
- общеклиническое обследование;
- сбор иммунологического, аллергологического, дерматологического и инфекционного анамнеза;
- осмотр дерматолога, аллерголога-иммунолога, офтальмолога, гинеколога, невролога и других профильных специалистов;
- диагностику методом полимеразной цепной реакции (ПЦР) в режиме реального времени (определение ДНК вируса простого герпеса (1-го или 2-го типа) в крови, слюне, моче, содержимом везикул, соскобе со дна эрозии, слизистой уретры, стенок влагалища и цервикального канала, конъюнктивы глаз). Учитывая высокую диагностическую значимость данного метода и зависимость смертности новорожденных от виремии, вызванной ВПГ 1-го и ВПГ 2-го типов, некоторые исследователи рекомендуют использовать ПЦР для лабораторного скрининга на генерализованную герпетическую инфекцию среди детей высокого риска и женщин репродуктивного возраста;
- серологическую диагностику: анализ крови на IgM и IgG к ВПГ методом иммуноферментного анализа (ИФА). Наличие антител свидетельствует об инфицировании, но не всегда позволяет связать клинические проявления инфекции с вирусом герпеса: у части бессимптомных носителей выявляются высокие титры антител, тогда как у ряда пациентов с выраженной симптоматикой титры антител остаются низкими. Использование ИФА целесообразно при исследовании парных сывороток, полученных с интервалом 7–10 дней. Показателем первичной инфекции считается четырехкратное увеличение антител класса IgG к ВПГ;
- цитоморфологические методы (проведение световой микроскопии биоматериала после его окрашивания на предметном стекле);
- иммунофлуоресцентный анализ (используется в основном в научных исследованиях).
В клинической практике для постановки диагноза ВПГ обычно ограничиваются данными анамнеза и клинических проявлений болезни, а также выявлением ДНК ВПГ методом ПЦР в отделяемом из высыпаний, когда диагноз из-за локализации поражений или анамнестических данных вызывает сомнения.
В ряде случаев генитальная локализация ГВИ трудно диагностируется. Только в 20% случаев диагноз верен. 20% пациентов – вирусоносители, которые никогда не имели клинических симптомов или признаков заболевания. Нередко при рецидивах ВПГ генитальной локализации, протекающего в атипичной форме (без выраженных клинических признаков), диагноз кандидоза ошибочен. И наоборот: при заболеваниях, протекающих с язвенными поражениями (сифилисе, болезни Бехчета и др.), ставят диагноз герпеса.
Положительные результаты исследования методом ПЦР подтверждают наличие у пациента генитального герпеса, требующего лечения. Отрицательный результат теста не исключает диагноз, поскольку недостаточное количество материала, его потери при транспортировке в лабораторию и быстрое заживление очага инфекции способны привести к ложноотрицательному результату. В таких ситуациях исследование проводится два-три раза с интервалом две – четыре недели [4].
Полностью элиминировать вирус герпеса из организма не представляется возможным. Поэтому терапия герпетической инфекции направлена на блокаду репродукции вируса.
Противовирусная терапия наиболее эффективна в фазе репликации вируса. При обострении хронической инфекции, вызванной ВПГ, показана противовирусная терапия в комбинации с иммунопрепаратами на фоне патогенетической и симптоматической терапии.
Этиотропная терапия ГВИ считается общепризнанным подходом к лечению острых проявлений инфекции и профилактике ее обострений. Современные этиотропные противогерпетические препараты (ацикловир, валацикловир, фамцикловир) по уровню доказательности относятся к группе A [5]. Молекула валацикловира по сравнению с таковой ацикловира характеризуется более высокой биодоступностью (54%) и длительностью полувыведения (10–20 часов). Это позволяет снизить кратность приема препарата до двух раз в сутки и увеличить приверженность пациентов терапии.
Механизм действия противогерпетических препаратов заключается в угнетении синтеза вирусной ДНК и репликации вирусов за счет конкурентного ингибирования вирусной ДНК-полимеразы.
Последнее время на российском фармацевтическом рынке появляется большое количество препаратов валацикловира. Форма выпуска – таблетки, покрытые пленочной оболочкой, в стандартной дозе 500 мг (валацикловира гидрохлорида гидрат 611,70 мг), а также в дозе 1000 мг (валацикловира гидрохлорида гидрат 1223,40 мг). Клиническую эффективность валацикловира у пациентов с хронической рецидивирующей ГВИ изучали в исследовании [6].
Выделяют два основных способа применения противовирусных химиопрепаратов: эпизодическое назначение (при необходимости, обострениях ГВИ) и пролонгированная терапия. В первом случае препарат назначают коротким курсом 5–10 дней, во втором пациенты принимают препарат ежедневно в течение нескольких месяцев или лет не только для купирования данного рецидива, но и для профилактики последующих обострений [7–9].
Показаниями для назначения супрессивной терапии являются:
- тяжелое течение с частыми обострениями;
- отсутствие продромального периода;
- особые обстоятельства (отпуск, свадьба и т.д.);
- использование иммуносупрессивной терапии;
- наличие психосексуальных расстройств;
- предотвращение риска передачи инфекции.
У пациентов с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные, общеукрепляющие средства). Как правило, таким пациентам показаны длительные курсы противовирусных препаратов (в частности, ацикловир, валацикловир, фамцикловир) [10].
При использовании супрессивной схемы лечения дозы препаратов зависят от клинического течения рецидивов генитального герпеса. Если количество рецидивов не более десяти в год, суточная доза валацикловира составляет 500 мг. При количестве рецидивов свыше десяти в год валацикловир используют в дозе 1000 мг.
В лечении ГВИ легкого и среднетяжелого течения широко используются иммуномодулирующие препараты, интерфероны (ИФН), индукторы интерферона, а также витаминотерапия. При тяжелых формах ГВИ целесообразно внутривенное введение иммуноглобулина.
При тяжелом и длительном течении ВПГ-инфекции в случае курсового использования названных препаратов в качестве монотерапии отмечается недостаточный клинический эффект. При длительном приеме развиваются побочные и нежелательные эффекты. ИФН представляет собой только часть противовирусной защиты иммунной системы и не может заменить другие ее звенья при их несостоятельности. Использование иммунокорректоров без оценки иммунного статуса, индивидуального подбора и контроля их действия бывает малоэффективно или способно приводить к усилению иммунной дисфункции либо гипореактивности ряда звеньев иммунитета вследствие неадекватной стимуляции. Назначение препаратов для местного применения (мази, содержащие ацикловир, Эпиген интим спрей (глицирризиновая кислота) и др.) носит вспомогательный характер, поскольку пузырьковые высыпания на коже лишь одно из проявлений тяжелой ВПГ-инфекции.
Как показывают данные литературы и накопленный нами опыт, вирус герпеса способен реплицировать в других клетках и органах (в орофарингеальной области, лимфоузлах, слизистой прямой кишки и т.д.).
Клинический случай
К врачу аллергологу-иммунологу обратилась пациентка М. 32 лет с жалобами на пузырьковые высыпания на слизистой оболочке красной каймы губ, болезненность в области высыпаний, головную боль, нарушение сна, утомляемость, раздражительность.
Анамнез заболевания. Аналогичные симптомы беспокоят в течение пяти лет. Высыпания локализуются в области носогубного треугольника. Частота рецидивов – от шести до восьми раз в год. В течение полугода обострения ежемесячные. В 2013 и 2015 гг. – два эпизода герпетического кератита (заключение офтальмолога на руках). Неоднократно обращалась к дерматологу по месту жительства – курсы ацикловира 200 мг пять раз в сутки в течение трех – пяти дней с кратковременным эффектом. Кроме того, использовалась местная противовирусная терапия в виде мазей. Настоящее обострение в течение трех дней связывает со стрессом на работе (полгода работает на новом месте, рабочий график ненормированный). Самостоятельно применяла местную терапию без значимого эффекта.
Объективно. Состояние удовлетворительное. Температура тела 36,7 ºС.
На слизистой оболочке красной каймы верхней губы слева сгруппированные пузырьковые высыпания с серозным содержимым, желтоватые корочки, мокнутие.
Лабораторная диагностика. Выявлена ДНК ВПГ 1-го типа методом ПЦР из содержимого везикулы.
Консультация невролога. Астеноневротический синдром. Назначен Атаракс 25 мг по 1/2 таблетки на ночь в течение трех недель. Соблюдение режима труда и отдыха. Во время повторной консультации принято решение об отмене препарата.
Консультация оториноларинголога. Хронический тонзиллит, простая форма, стадия ремиссии. Рекомендован курс промывания лакун миндалин № 10.
Пациентке рекомендована супрессивная терапия препаратом валацикловир 1000 мг один раз в сутки шесть месяцев. Соблюдение указаний невролога, оториноларинголога. Повторная консультация через два с половиной – три месяца.
Пациентка повторно явилась на прием через три месяца. Жалоб не предъявляла. На фоне проводимого лечения рецидивов ГВИ не отмечалось. Со слов больной, стрессовый фон на работе уменьшился, сон нормализовался (отменила Атаракс месяц назад).
Через два месяца после завершения курса супрессивной терапии жалобы отсутствовали. Рецидивов ГВИ не наблюдалось.
При наличии герпетической инфекции следует проводить адекватную терапию с учетом характера поражения (локальная, генерализованная форма), первичного или рецидивирующего течения заболевания.
- купирование клинических симптомов, ускорение разрешения клинических проявлений, уменьшение площади поражения, снижение общей интоксикации;
- предупреждение развития острого процесса или рецидива,
- уменьшение частоты рецидивов, укорочение их длительности, увеличение временного периода между рецидивами заболевания, а также облегчение их течения;
- улучшение качества жизни пациентов;
- предупреждение развития осложнений;
- предупреждение дальнейшего распространения возбудителя, снижение риска инфицирования полового партнера или новорожденного.
Половые партнеры пациентов с герпетической инфекцией (ГИ) урогенитального тракта подлежат активному выявлению. Лечение необходимо прово дить у них при клинических проявлениях герпеса. Следует рекомендовать воздерживаться от половой жизни или использовать презервативы во время обострений. Лечение должно проводиться с учетом образа жизни и потребности в подавлении, связанной с влиянием физических и психосоциальных факторов.
Важно при этом учитывать, что достижение положительного результата при лечении генитального герпеса (ГГ) сопряжено с рядом сложностей. Полная элиминация возбудителя – вируса простого герпеса (ВПГ) – невозможна. Несмотря на достигнутые успехи в лечении ГГ, существующие методы не обеспечивают полной элиминации вирусов из организма.
Методы лечения герпетической инфекции
- применяют эффективные противовирусные химиопрепараты
- применяют средства, повышающие специфическую и неспецифическую резистентность организма (интерферон и его индукторы, иммуномодуляторы, вакцины);
- проводят серотерапию и серопрофилактику (лечение и профилактику иммунными сыворотками) с использованием специфических иммуноглобулинов человека или иммунизированных животных;
- применяют местные и антисептические средства для купирования кожно-слизистых поражений.
Противовирусная терапия генитального герпеса
- лечение первичного эпизода ГГ;
- эпизодическая противовирусная терапия (для купирования каждого отдельного эпизода обострения ГИ);
- профилактическая (превентивная или супрессивная) терапия (непрерывное лечение на протяжении определенного времени для предупреждения рецидивов и предотвращения передачи инфекции другим лицам).
Существует ряд противовирусных препаратов, способные быстро и эффективно купировать острые проявления генитального герпеса. В адекватной дозировке большинство этих препаратов одинаково эффективно уменьшают тяжесть и продолжительность обострений генитального герпеса. Однако клинический опыт их применения показал, что, облегчая выраженность симптомов болезни, они не предотвращают наступление рецидивов и, в большинстве случаев, не снижают их частоту.
Профилактическая (супрессивная) противовирусная терапия
В многочисленных исследованиях показано, что продолжительная профилактическая терапия противовирусными препаратами значительно уменьшает бессимптомное и субклиническое (в продромальный период) выделение вируса.
Изученные в настоящее время иммунопатогенетические особенности рецидивирующей герпетической инфекции убедительно указывают на нарушения клеточного иммунного ответа у данной категории больных. При герпесе развиваются иммунодефицитные состояния, обусловленные недостаточностью различных звеньев иммунной системы. Чтобы добиться нормализации иммунологических показателей у больных с данной патологией, необходимо продолжать лечение и в межрецидивный период для коррекции остаточных иммунологических нарушений.
Важным благоприятным эффектом профилактической терапии является снижение психологического давления на пациентов.
Вакцина от герпеса
Вакцино-профилактика ГГ находится в стадии научных и экспериментальных разработок. До настоящего времени не получено ни одной эффективной профилактической вакцины против ВПГ. Природа ВПГ-инфекции, заключающаяся в локальном поражении с последующим латентным периодом без системной вирусемии, приводит к тому, что даже успешная выработка специфических антител не предохраняет от последующего рецидива.
Разработанные вакцины (живые, убитые и рекомбинантные) не нашли широкого применения из-за отсутствия надежных методов оценки эффективности курсов вакцинации, критериев продолжительности вакцинации и дальнейшей реабилитации больных.
Генитальный герпес можно и нужно лечить
Лечение генитального герпеса - это многоплановая задача, сложный и длительный процесс. Правильное лечение и назначение лекарственных средств может проводиться только квалифицированным специалистом с учетом проведенной диагностики и истории болезни. Для каждого пациента терапия должна подбираться индивидуально. При тяжелом течении заболевания показано лечение в стационаре.
Результат лечения в значительной мере зависит от опыта врача, а также от терпения и тщательного выполнения пациентом рекомендаций врача. Существующий сегодня арсенал противовирусных и иммунных препаратов позволяет решить очень многие проблемы, возникающие у лиц, страдающих рецидивирующими формами ГГ с поражением гениталий, ягодиц и другими более редкими локализациями. Раннее начало лечения имеет большое значение для получения значительного противовирусного эффекта.

Основным местом локализации первичной генитальной инфекции ВПГ у женщин является шейка матки. Чаще всего, герпетические поражения у женщин локализуются на больших и малых половых губах (68,6%), в области вульвы (41,8%), клитора (35,7%), влагалища и шейки матки (84,4%).
ВПГ был изолирован из шейки матки во время первичного заражения у 88—90 % женщин с первичной инфекцией ВПГ-2, которые имели везикулезную сыпь на наружных гениталиях, у 65 % — с повторным эпизодом инфекции ВПГ-2, и у 80 % женщин с ВПГ-1. Большинство (89 %) женщин, выделяющих вирус при первичном эпизоде заболевания, имели изменения на шейке матки.
Особенностью генитального герпеса (Herpes genitalis) женских половых органов является многоочаговость. В патологический процесс нередко вовлекаются нижний отдел мочеиспускательного канала, слизистая оболочка ануса и прямой кишки. Вовлечение в инфекционный процесс этих органов может происходить вторично, вслед за возникновением герпеса наружных гениталий, но может протекать и как изолированное поражение.
Рецидивирующая герпетическая инфекция (РГИ) может проявляться клиникой вульвовагинита и цервицита, вызывать поражения слизистой матки, труб и придатков. В 83,6 % случаев при стойких, не поддающихся терапии кольпитах, лейкоплакиях шейки матки выделяют вирус простого герпеса (ВПГ) как один из ведущих этиологических факторов заболевания.
По некоторым данным, в 66 % случаев у женщин герпетическая инфекция (ГИ) протекает атипично. Об имеющейся длительно текущей хронической ГИ можно говорить на основании особенностей клинического течения, наличия герпетического антигена в эпителиальных клетках вульвы, влагалища и периферической крови.
д) хронических часто рецидивирующих сальпингоофоритах (воспаление маточных труб и яичников) и эндометритах, не поддающихся стандартной антибактериальной терапии;
У 1–2% женщин, поступающих в гинекологическую клинику, независимо от основного заболевания, обнаруживают цитологические доказательства ВПГ-инфекции.
Герпес наружных половых органов у женщин
При рецидивирующем герпесе (РГ) наружных половых органов у женщин, очаг поражения находится в области наружных гениталий и перианальной области. Герпетические высыпания у женщин возникают на больших и малых половых губах, области лобка и промежности.
Типичная форма РГ наружных гениталий характеризуется ярко выраженными симптомами болезни, классическим развитием очага поражения (эритема, образование везикул, развитие эрозивно-язвенных элементов, эпителизация) и субъективными ощущениями (зуд, чувство жжения, болезненность, недомогание). проявляется повторяющимися пузырьковыми высыпаниями. Выраженная симптоматика позволяет врачам визуально поставить диагноз РГГ, своевременно назначить лечение и информировать больного об инфекционном характере заболевания и опасности заражения полового партнера.
Герпес нижнего отдела урогенитального тракта, анальной области и ампулы прямой кишки
Поражение слизистых оболочек входа во влагалище, влагалища, влагалищной части шейки матки, цервикального канала, уретры, мочевого пузыря, анальной области и ампулы прямой кишки проявляется в двух клинических формах:
- очаговой, характеризующейся появлением типичных для простого герпеса слизистых оболочек везикулезно-эрозивных элементов,
- диффузной, при которой патологический процесс протекает по типу неспецифического воспаления.
Герпес верхнего отдела полового тракта (поражение матки, маточных труб).
Типичная клиническая картина герпетических поражений органов верхнего отдела мочеполового тракта проявляется симптомами неспецифического воспаления. Неспецифические герпетические поражения внутренних половых органов проявляются эндоцервицитом, эрозией шейки матки, вагинитом. Ряд авторов цервициты без наружных язв также относят к атипичным проявлениям ГГ.
Клинические проявления герпетических поражений внутренних половых органов не имеют специфических особенностей по сравнению с воспалительными процессами невирусной этиологии. Обычно больные предъявляют жалобы на выделения из влагалища, периодически появляющиеся боли в малом тазу, области проекции матки, яичников.
Герпетические поражения шейки матки
Герпетические поражения шейки матки могут носить типичный и нетипичный характер. В типичном варианте генитального герпеса – это всегда хорошо заметные множественные, довольно мелкие, с четкими границами округлые эрозии; высыпные элементы быстро минуют везикулярную стадию, в которой, кстати, эти элементы плохо различимы без применения кольпоскопии. Проблема причастности ВПГ к развитию нетипичных герпетических изменений слизистой шейки матки в настоящее время находится в стадии исследований.
При кольпоскопии в острый период герпетической инфекции шейки матки определяют изъязвление с неровными краями с сукровицей в области дна. Эволюция этого поражения идет от изъязвления с красным дном к простой эрозии до полного исчезновения в течение 3-х недель. К предшествующим изменениям относят маленькие буллезные образования, затем округлые микроэрозии с последующим формированием простых красных пятен, которые похожи на местный пятнистый кольпит.
Исследования показали, что выделение ДНК ВПГ с поверхности эрозии шейки матки в 60 % случаев сопровождается репликативной фазой ГИ (репликация и сборка вирусных частиц в инфицированных клетках). При эрозии и дисплазии шейки матки ВПГ-2 выявляется в 27,2% случаев непосредственно в соскобах со слизистой цервикального канала и сопровождается повышением титра специфических иммуноглобулинов в крови до диагностических уровней.
Особое значение влияние герпетической инфекции на состояние эпителия шейки матки имеет у женщин, длительно принимающих оральные гормональные контрацептивы. Известно, что длительный прием комбинированных стероидов в той или иной мере усиливает процессы плоскоклеточной метаплазии, а также может вызывать эффект эндоцервикальной гиперплазии, причем этот эффект в случае его развития наблюдается как в эпителии цервикального канала, так и в участках псевдоэрозии на фоне эктропиона, в полипах слизистой цервикального канала. В связи с этим прием оральных комбинированных контрацептивов может являться кофактором в развитии рака шейки матки, особенно в сочетании с герпетической инфекцией.
Герпетический цервицит
Герпетический цервицит – это воспалительный процесс, вызванный ВПГ. Для клинических проявлений герпетического цервицита характерно разнообразие проявлений — от легкой гиперемии с небольшим количеством эрозий до тяжелого некротического поражения (под эрозией шейки матки понимают дефект эпителия в результате воспаления). Цервицит диагностируется у 70-90% женщин с герпетическим поражением половых органов. Шейка матки при герпетическом эндоцервиците отечна, часто имеет эрозии, легко кровоточит при манипуляциях.
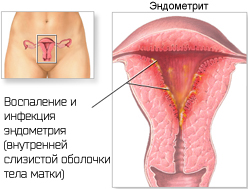
Герпетический эндометрит
Эндометрит — это воспаление внутренней (слизистой) оболочки матки (эндометрия) с поражением как функционального, так и базального слоя. Эндометрит, вызванный вирусом простого герпеса, является следствием длительной персистенции (существования) вируса в эндометрии. Герпетический эндометрит, как правило, возникает при атипичном или бессимптомном течении ГГ, типичная форма отмечается редко (~20% случаев). Клинические симптомы при вирусном поражении эндометрия чаще всего отсутствуют или проявляются нетипично, что приводит к ошибкам в диагностике и позднему началу лечения.
При герпетическомпоражении ткани нарушаются факторы местного и общего иммунитета, целостность поверхности эпителия, что приводит к созданию благоприятных условий для развития других инфекционных процессов .
Клинически герпетический эндометрит чаще проявляется во второй фазе менструального цикла или во время беременности, что, возможно, обусловлено повышением уровня простагландинов в этот период или супрессией Т-клеточного звена иммунитета, способствующих реактивации ВПГ, персистирующего в эндометрии. Субклиническая латентная внутриматочная герпетическая инфекция является важным фактором невынашивания беременности. Эндометриты ВПГ-этиологии встречаются нечасто, но эти заболевания очень опасны и могут вызвать гибель женщины и плода.
Герпес уретры и мочевого пузыря (герпетический уретрит)
Герпетический уретрит у женщин субъективно проявляется болями и резями в начале мочеиспускания, частыми позывами к мочеиспусканию. У 4,8% женщин имеет место очень болезненное мочеиспускание, или задержка мочеиспускания в результате инфекции уретры и слизистой оболочки мочевого пузыря. Нормализация функции мочевого пузыря у больных с задержкой мочеиспускания обычно происходит в течение 6–10 дней.
При осмотре наблюдаются гиперемия наружного отверстия уретры, наличие скудных слизистых выделений; при уретроскопии в передней части уретры иногда удается обнаружить мелкие поверхностные эрозии, катаральное воспаление.
Герпетический цистит
Ведущими симптомами герпетического цистита являются цисталгия, появление болей в конце мочеиспускания, дизурические явления. При герпетическом цистите появляются гематурия (кровь в моче), появление болей в конце мочеиспускания, боли в области мочевого пузыря. У женщины это может быть первым и единственным признаком ВПГ-инфицирования мочеполовой сферы. Он нередко возникает в первые 1-3 месяца после начала половой жизни или после смены полового партнера.
Герпес анальной области и прямой кишки
Очаг поражения в анальной области обычно представляет собой рецидивирующую трещину, что нередко является поводом для диагностических ошибок. Такие больные с ошибочным диагнозом "трещина заднего прохода" попадают к хирургам. Зудящая форма герпеса ануса и герпетическое поражение геморроидальных узлов, также трудны для диагностики.
Поражение анальной области может возникнуть первично как самостоятельное заболевание или вторично – в результате затекания отделяемого влагалища и мацерации слизистой оболочки ануса при наличии у пациентки герпетического кольпита, сопровождающегося обильной экссудацией.
При поражении сфинктера и слизистой оболочки ампулы прямой кишки (герпетический проктит) больных беспокоят зуд, чувство жжения и болезненность в очаге поражения, возникают мелкие эрозии в виде поверхностных трещин с фиксированной локализацией, кровоточащие при дефекации. При ректоскопии определяется катаральное воспаление, иногда эрозии.
Герпес внутренних гениталий - субклиническая и бессимптомная формы.
Для субклинической формы герпеса внутренних гениталий (влагалища, матки, яичников и т.д.) типично отсутствие у пациентки жалоб, иногда имеются указания на периодически появляющиеся необильные слизистые выделения из влагалища. При гинекологическом осмотре симптомы воспаления не выявляются. При динамическом лабораторном исследовании мазков отделяемого канала шейки матки, влагалища и уретры периодически выявляется повышенное количество лейкоцитов (до 200–250 и выше в поле зрения), свидетельствующее о наличии воспалительного процесса. При вирусологическом исследовании мазков методом иммунофлюоресценции в лейкоцитах определяется антиген ВПГ.
Бессимптомная форма герпеса внутренних гениталий характеризуется отсутствием у больных каких-либо жалоб на половую сферу, объективных клинических данных, подтверждающих воспаление. При лабораторном исследовании отделяемого урогенитального тракта выделяется ВПГ, в то время как в мазках признаков воспаления (лейкоцитоза) нет. Бессимптомная форма герпеса внутренних гениталий выявляется у 20–40% женщин, страдающих РГГ ягодицы и бедра. Это важное обстоятельство необходимо учитывать при планировании беременности у женщин с этой формой РГГ в связи с существующей вероятностью развития во время беременности осложнений ВПГ-инфекции.
Согласно данным литературы, у 83,6% женщин, страдающих не поддающимися терапии кольпитами и лейкоплакией шейки матки, ВПГ является одним из факторов заболевания. Доказано, что ВПГ может быть причиной развития эндометрита и сальпингоофорита.
Герпетический вульвовагинит
У женщин часто встречаются герпетический вульвовагинит, особенностью течения которого является нередкое присоединение отека пораженной области. Вирус герпеса могут изолированно поражать вульву и влагалище. Заражение происходит от больных. Герпетический вульвовагинит проявляется мелкими пузырьками на гиперемированной вульве. Пузырьки содержат прозрачную, а при присоединении вторичной инфекции — гнойную жидкость. Через 5—7 дней пузырьки вскрываются с образованием эрозий и язвочек, которые покрываются струпом. В начале заболевания выражены жжение, боли и зуд в области вульвы. Общие симптомы включают головную боль, озноб, повышение температуры тела.
Генитальный герпес во время беременности
Заболевание ВПГ женщин во время беременности может явиться причиной гибели плода, мертворождения, преждевременных родов. Герпесвирусы вызывают до 30% спонтанных абортов на ранних сроках беременности и свыше 50% поздних выкидышей, занимают второе место после вируса краснухи по тератогенности (развитие уродств плода).
Тяжелейшие формы неонатального герпеса развиваются при инфицировании новорожденного вирусом простого герпеса в родах. При первичном ГГ у матери инфицируется от 30% до 80% детей, при рецидивирующем герпесе – 3–5%. Инфицирование плода во время родоразрешения, если у матери в конце беременности имели место герпетические высыпания, происходит у 50% женщин, больных РГГ; при этом у 60–80% инфицированных детей развивается энцефалит.
Герпес менструальный
Менструальный герпес — это генитальный герпес (ГГ) с монотонным типом рецидивирования и тяжелым течением, характеризующийся ежемесячными обострениями инфекционного процесса до, во время или после менструации. Такое течение заболевания может стать для женщины сильнейшим психотравмирующим фактором, ограничивающим ее социальную активность и снижающим качество жизни.
Этот вариант ГИ является сложным для лечения. Поэтому разработка адекватных и эффективных способов лечения и профилактики рецидивов у больных с данными формами ГГ остается актуальной. Европейские стандарты лечения пациенток предусматривают длительную (годами) супрессивную терапию противовирусными препаратами , что не исключает повторного рецидирования ГГ и бессимптомного вирусовыделения, появления побочных эффектов и резистентности вирусов герпеса к лекарственной терапии.
Генитальный герпес сохраняется на протяжении всей жизни человека, и его влияние выходит за рамки физических симптомов, включая и психосексуальное воздействие.
Признание психосексуального аспекта заболевания, связанного с вызываемой вирусом простого герпеса (ВПГ) инфекцией, подтверждает важность просвещения и консультирования больных.
Супрессивная терапия при генитальном герпесе оказывает положительное психосоциальное действие, а также уменьшает степень риска его передачи.
Дискретное самолечение генитального герпеса требует назначения удобной схемы нечастого приема препарата. Соблюдение больным режима и схемы лечения и, следовательно, эффективность, вероятнее всего, связаны с простой схемой приема препарата.
Эффективное предупреждение возникновения рецидивов генитального герпеса можно осуществить с помощью валацикловира, назначаемого 1 раз в сутки.
 |
Там, где для реализации эффективных методов борьбы с ИППП имелись средства, наибольшие усилия, были направлены прежде всего на борьбу с такими бактериальными ульцерозными болезнями, как сифилис, шанкроид, после чего на борьбу с гонореей, а затем и хламидиозом. Однако традиционные методы борьбы, вероятно, оказали незначительное влияние на распространение инфекции, вызываемой ВПГ или вирусом папилломы человека (ВПЧ). Несмотря на особое значение, придаваемое безопасным половым контактам, в обследовании, проведенном в США, было выявлено увеличение положительных результатов серологических реакций в период между 1976–1980 гг. и 1988–1994 гг. на 30% [1]. В группы с самыми высокими показателями такого увеличения входили подростки (4−кратное повышение частоты возникновения случаев) и взрослые люди от 20 до 30 лет (2−кратное повышение). Для определения темпов роста этих показателей в других регионах необходимо проведение популяционных серологических исследований.
Первичное заражение герпетической инфекцией половых путей переходит в хроническую болезнь, характеризующуюся повторяющимися вспышками. Инфекция сохраняется на протяжение всей жизни человека, хотя характер проявления клинических признаков и симптомов меняется в зависимости от различных связанных с образом жизни ситуаций [2]. У инфицированных людей реактивация инфекции, вызываемой половых органов, наблюдается в среднем 4–5 раз в год [3]. Между приступами у больных отмечаются бессимптомные периоды, но тем не менее они, возможно, выделяют вирус (бессимптомное выделение), что делает вероятным передачу ими в любое время данного вируса половому партнеру. Поскольку физические симптомы, связанные во многих случаях с повторными приступами, относительно незначительны, данная инфекция вызывает последствия, выходящие за рамки этих физических симптомов. Тревожность и изменение эмоционального состояния часто сопутствуют генитальному герпесу. Для больного характерны чувство депрессии, желание уединения и страх, что его оттолкнет партнер [4]. У многих больных психосексуальное влияние распространяется за пределы первичного приступа, особенно если эти вопросы не учитываются при первоначальном ведении больных. При оптимальном ведении болезни, вызываемой ВПГ половых органов, необходимо применение мультифакторного подхода. В острой фазе болезни первой задачей лечения является ослабление проявления ее симптомов, а также необходимость просвещения больного по вопросам данного состояния.
В течение длительного периода времени просвещение больного позволяет ему проводить лечение самому и справляться с необходимостью брать на себя личную ответственность за снижение степени риска передачи данной инфекции. Больные, как правило, стремятся к знаниям, и они получают их из разнообразных источников (например, групповые занятия, и горячие линии). Поскольку полученные данные могут быть противоречивыми, то врачам важно направлять больных к достоверным и точным источникам информации.
· супрессивная (профилактическая) терапия, посредством которой подавляется реактивация ВПГ и предупреждается проявление продромальных повторных вспышек болезни;
· краткосрочное (эпизодическое) лечение отдельных вспышек герпеса по мере их возникновения, посредством которого прекращается размножение вируса, причем заживляются эрозии и прекращаются боли.
Целью лечения при приступах является приостановление интенсивного размножения ВПГ, которое предшествует и сохраняется при вспышках герпеса. Данное лечение не оказывает никакого влияния на обострение бессимптомного выделения вируса, которое периодически возникает между клинически выраженными приступами, а также на последующую частоту рецидивов.
Применение антивирусных препаратов значительно способствует лечению генитального герпеса, но стратегия беспрерывной супрессивной терапии для предотвращения повторных вспышек вызываемой ВПГ инфекции до сих пор широко не используется. К возможным препятствиям к применению супрессивной терапии при генитальном герпесе относятся ограниченные знания о ряде положительных психологических факторов, связанных с предупреждением приступов, игнорированием предпочтений больного, беспокойство относительно возможности развития лекарственной резистентности и других вопросов, связанных с безопасностью применения препарата, а также ограниченные денежные средства.
Было показано, что супрессивная терапия при генитальном герпесе обеспечивает психологическое преимущество над лечением, проводимом при приступах.
Было показано, что супрессивная терапия при генитальном герпесе обеспечивает психологическое преимущество над лечением, проводимом при приступах [5, 6]. В результате этого улучшение качества жизни играет решающую роль в таком вопросе, как оказание помощи больным преодолевать последствия хронической ИППП, и в конце концов они начинают принимать участие в своем лечении.
Поскольку можно считать, что супрессивная терапия приносит наибольшую пользу тем больным, которые не справляются со своими симптомами, и больным, имеющим резко выраженные симптомы или очень часто повторяющие вспышки герпеса (см. таблицу), следует обсудить положительное влияние такой схемы при выборе вида лечения у всех больных с рецидивами болезни.
Подробный анализ имеет существенное значение для определения соответствующей стратегии. При выборе супрессивной терапии важно обеспечить правильность назначения схемы лечения антивирусными препаратами, которая может отличаться в зависимости от анамнеза и тяжести болезни.
Однако цель ликвидации латентной инфекции, вызываемой ВПГ, недостижима и, вероятно, недостижима и с помощью имеющихся методов лечения. Следующим наилучшим подходом является поддержание латентного состояния данной инфекции так, чтобы вспышки болезни не повторялись. Этого можно достичь проведением непрерывной супрессивной терапии. Идеальный вид супрессивной терапии при генитальном герпесе должен обеспечивать:
· очевидность воздействия на выделение (симптомное и бессимптомное) ВПГ для предотвращения его передачи половым путем;
Точка зрения больных в отношении идеальных свойств антивирусного препарата сводится к следующим требованиям:
Ни один из современных методов лечения не обладает всеми перечисленными характеристиками, хотя были достигнуты значительные успехи в применении супрессивной терапии в результаты улучшения биологической доступности пролекарств валацикловира и фамцикловира. С помощью однократного в сутки приема валацикловира можно добиться эффективного предотвращения рецидивов генитального герпеса [8].
 |
| Вирус генитального герпеса |
До 70% случаев передачи генитального ВПГ происходит при бессимптомном характере болезни при наличии у больного данного вируса
Большую озабоченность вызывает тот факт, что в клинических условиях передача вируса часто происходит от партнера (партнерши), который (которая) не знает о наличии у себя инфекции. Можно предположить, что уменьшение уровня выделения вируса позволит понизить степень риска передачи ВПГ половым путем у дискордантных пар. Для купирования рецидивов генитального герпеса одобрено применение валацикловира, фамцикловира и ацикловира, а длительная терапия одним из этих препаратов уменьшает уровень выделения вируса, но не устраняет его [11–13]. Не определено и количество препарата, требуемое для снижения уровня бессимптомного выделения вируса, что в свою очередь также влияет на передачу болезни. В проводимом в настоящее время исследовании по оценке валацикловира изучается гипотеза, согласно которой антивирусная терапия снижает степень риска передачи ВПГ половым путем. Также проводятся экспериментальные исследования по изучению выделения вируса материнским организмом и степени риска вертикальной передачи возбудителя (от матери к новорожденному ребенку).
Передача вируса часто осуществляется от партнера, который не знает о наличии у него (нее) инфекции
Бессимптомное выделение вируса наиболее часто наблюдается в ранние годы после первичного инфицирования [10]. Следовательно, значимость супрессивной терапии повышается при ее назначении сразу же после первоначальной вспышки болезни, когда психологическое влияние на диагностику инфекции наиболее выражено, степень риска передачи возбудителя наивысшая и больные особенно нуждаются в консультациях и поддержке. Степень необходимости в супрессивной терапии будет меняться в зависимости от различных этапов жизни больного и тяжести болезни. Время от времени следует повторно оценивать стратегию ведения больных. Больные могут выбрать супрессивную терапию в периоды особых трудностей или проблем, например во время экзаменов в колледже, при разрыве отношений с супругом (супругой) и другом (подругой), при развитии отношений с новыми лицами.
Предупреждение передачи вируса включает в себя глубокое понимание больным данного состояния и сотрудничества. Просвещение больного является таким образом важной частью борьбы с распространением инфекции, вызываемой ВПГ, а также неотъемлемой частью лечения психологического аспекта этой болезни. В недавно проведенном исследовании отношения больных к своей болезни выявлено, что самолечение и личная борьба с ВПГ половых органов имеют первостепенное значение [7]. Это не только вызывает у больных чувство ответственности за свое заражение этой болезнью, но также может купировать признаки болезни, характерные для ИППП.
Клиническая эффективность и безопасность ацикловира при длительном лечении инфекции, обусловленной ВПГ половых органов, были продемонстрированы во многих исследованиях, проведенных в течение последних 10–15 лет [14–17]. Было также показано положительное влияние супрессивной терапии генитального герпеса ацикловиром на психологию больных. Критический обзор применения ацикловира в течение 10 лет (1982–1992 гг.) подтверждает его клиническую эффективность при ряде показаний, обусловленных инфекцией, вызываемой вирусом герпеса [18].
Имеющиеся антивирусные препараты для лечения и борьбы с генитальным ВПГ (ацикловир, валацикловир и фамцикловир) обладают одинаковым в количественном отношении механизмом действия, т.е. избирательного фосфорилирования в инфицированных ВПГ клетках и конкурентного субстратного ингибирования полимеразы дезоксирибонуклеиновой кислоты (ДНК), ведущей к окончанию считывания цепи ДНК вируса. Однако они отличаются своей специфичностью и сродством к своим ферментам [19].
Ацикловир является первым избирательным аналогом нуклеозида с профилем приемлемой безопасности для широкого применения. Этот препарат, вызывающий минимальные побочные реакции [20], применяли у больных для купирования генитального герпеса до 10 лет. Новейшие препараты расширили врачам возможность выбора метода лечения [21].
Читайте также:

