Что такое торс вирус
Обновлено: 25.04.2024
В обзоре представлены литературные данные о ближневосточном респираторном синдроме, опасном инфекционном заболевании человека, вызываемым новым коронавирусом MERS-CoV, характеризующимся развитием пневмонии, нередко — острого респираторного дистресс-синдро
Middle East respiratory syndrome is a dangerous human disease caused by a new coronavirus. It is known that the most common clinical manifestation of the infection is pneumonia; a significant number of patients registered in the development of acute respiratory distress syndrome (ARDS).
Ближневосточный респираторный синдром, Middle East respiratory syndrome (MERS), является респираторным заболеванием с высокой летальностью, вызываемым новым РНК-содержащим бетакоронавирусом (MERS-CoV), впервые изолированным в 2012 г. у пациента в Саудовской Аравии. В последующем MERS-CoV-инфекция получила распространение и к 2015 г., кроме стран Ближнего Востока, затронула в общей сложности 25 стран мира. Особое внимание к данной инфекции было привлечено начавшейся 20 мая 2015 г. вспышкой заболевания MERS в Корее, самой крупной за пределами Ближнего Востока. На 22 сентября 2015 г. Всемирная организация здравоохранения (ВОЗ) сообщила о более чем 1569 лабораторно подтвержденных случаях ближневосточного респираторного синдрома (рис.), летальность при котором составила 35,3% (554 человека). Известно, что MERS-CoV-инфекция может протекать в различных формах — от бессимптомных, легких и среднетяжелых до развития острого респираторного дистресс-синдрома и полиорганной недостаточности, которые приводят к летальному исходу, особенно у пациентов с сопутствующими заболеваниями. Это определяет интерес к ранней диагностике, разработке методов терапии и мер профилактики инфекции, в том числе предотвращения распространения ее в лечебных учреждениях.
История открытия и место MERS-CoV среди коронавирусов
Международный комитет по таксономии вирусов различает четыре рода подсемейства Coronavirinae: Alphacoronavirus, Betacoronavirus, Gammacoronavirus и Deltacoronavirus. К роду Alphacoronavirus принадлежат вирусы HCoV-229E и HCoV-NL63, относящиеся к числу эндемических человеческих коронавирусов. Внутри рода Betacoronavirus различают четыре монофилетические линии (A, B, C, D). Линия А включает HCoV-OC43 и HCoV-HKU1, эндемические человеческие коронавирусы, линия В — SARS-CoV, вызвавший вспышки тяжелого острого респираторного синдрома (SARS, ТОРС) в 2003 г. Линии C и D включают вирусы, которые до 2012 г. обнаруживались только у летучих мышей. В июне 2012 г. в результате молекулярно-биологического изучения биопроб пациента, умершего от тяжелой пневмонии и почечной недостаточности в г. Джидда (Саудовская Аравия), был выделен новый коронавирус, который принадлежит к линии С и, таким образом, является первым вирусом рода Betacoronavirus линии С, который выделен от человека. 15 мая 2013 г. специалисты Международного комитета по таксономии вирусов приняли решение присвоить новому вирусу название Middle East respiratory syndrome coronavirus (MERS-CoV), коронавирус ближневосточного респираторного синдрома.
Распространение инфекции в мире
Чаще всего MERS-CoV-инфекция регистрируется у взрослых (98%), средний возраст заболевших — 50 лет.
Эпидемиология
В ходе изучения вируса возник вопрос, появился ли MERS-CoV в человеческой популяции недавно или персистировал много лет. Ретроспективный анализ сывороток крови, полученных в 2012 г. от доноров крови и рабочих скотобоен в Саудовской Аравии, не выявил антител к MERS-CoV [9].
Ранее сообщалось, что резервуаром MERS-CoV в природе являются летучие мыши [4–6]. Однако MERS-CoV никогда не изолировались от летучих мышей [7]. В поисках источника инфекции на Аравийском полуострове были проведены серологические исследования других видов животных. Единственным подтвержденным зоонозным источником инфекции сегодня являются верблюды. Антитела к MERS-CoV обнаружены при исследовании сывороток одногорбых верблюдов Camelus dromedarius в Омане в 100% случаев и на Канарских островах (Испания) в 14% [8]. Антитела к вирусу также были выявлены и в архивных образцах сывороток крови верблюдов Camelus dromedarius, полученных в Саудовской Аравии в 1993 г. и Объединенных Арабских Эмиратах в 2003 г. [7, 10]. В Западной и Северной Африке образцы сыворотки были серопозитивны уже с 1992 г. [7], что отражает широкое распространение MERS-CoV в популяции верблюдов на протяжении многих лет. Большинство верблюдов инфицируются новым коронавирусом при рождении и в первые месяцы жизни. Около трети молодых верблюдов впоследствии становятся бессимптомными носителями данной инфекции.
Заражение человека от верблюда при прямом контакте подтверждено лишь в небольшом проценте случаев, однако заражение возможно при употреблении инфицированного непастеризованного верблюжьего молока, которое весьма распространено в Саудовской Аравии [10]. Эпидемиологическую опасность представляют также моча, кровь и недостаточно термически обработанное мясо верблюдов [7, 11].
Передача от человека к человеку MERS-CoV подтверждена эпидемиологическими и генетическими исследованиями вспышек в медицинских учреждениях и домашних вспышек [12, 13]. Так, в апреле-мае 2013 г. в Аль-Хасе, в Саудовской Аравии, заболело 23 пациента отделения гемодиализа и интенсивной терапии, смертность составила 65% [13]. Считают, что заболевание от человека к человеку передается воздушно-капельным и контактным путем [7]. Передача от человека к человеку MERS-CoV в лечебных учреждениях была также установлена в 2014 г. во время вспышки инфекции Jeddah, Саудовская Аравия [14]. Все случаи заболевания в Южной Корее в 2015 г. MERS-CoV-инфекцией, за исключением первого завозного случая, связаны с одной цепочкой передачи и ассоциируются с медицинскими учреждениями. Таким образом, коронавирусная инфекция в Корее преимущественно возникала как внутрибольничная.
Drosten et al. [15] показали, что индекс контагиозности при контакте 26 пациентов с 280 домашними лицами составил 4%.
Установлено, что заболеваемость MERS носит сезонный характер с пиком в марте–апреле, что связано с заражением от молодых верблюдов, небольшие пики были также отмечены в сентябре и ноябре 2013 г. и 2014 гг.
Патогенез и клиническая картина
Установлено, что MERS-CoV активно проникает и размножается в клетках бронхиального эпителия и альвеолярных пневмоцитах ΙΙ типа человека [1]. Также показано, что клеточным рецептором для MERS-CoV является CD26 (DPP4), который в организме человека экспрессируется преимущественно в клетках бронхиального эпителия, почек и Т-лимфоцитах [2]. Регистрируются деструктивные изменения эпителиальных клеток дыхательных путей, дискинезия ресничек, нарушение мукоцилиарного клиренса. Как и при SARS-CoV-инфекции, при MERS-CoV обнаруживаются диффузные альвеолярные повреждения, сквамозная метаплазия альвеолоцитов, геморрагии и апоптоз, бронхиолит, образование эозинофильных гиалиновых мембран, нарушение функции сурфактанта. Однако MERS-CoV гораздо активнее внедряется в альвеолоциты, вызывает дисрегуляцию 207 генов в клетках легких. Часто развивается пневмония и респираторный дистресс-синдром взрослого типа. Помимо острого альвеолярного повреждения, MERS-CoV способен поражать самые различные органы — печень, почки, кишечник.
Почечная дисфункция или недостаточность возникает нередко и является следствием или гипоксического повреждения, или прямого повреждения вирусом ткани почек. Изучение патогенеза заболевания затрудняется сложностями получения образцов тканей человека по культурным и религиозным соображениям и проводится преимущественно на экспериментально инфицированных животных. У инфицированных макак развиваются легкие формы болезни с очевидной клеточной инфильтрацией в легких при рентгенологическом исследовании. У инфицированных мармазеток, напротив, развивается тяжелая интерстициальная пневмония и в ткани легких выявлены нейтрофильная и макрофагальная инфильтрация и альвеолярный отек [16, 17].
В настоящее время мало известно о протективном иммунном ответе у выздоровевших пациентов с MERS. Показано, что MERS-CoV вызывает ослабленные реакции врожденного иммунитета с задержкой индукции провоспалительных цитокинов в клеточной культуре in vivo, что может способствовать дисрегуляции иммунного ответа [18–22]. Подобные данные были получены и у пациентов с SARS. Неэффективные В- и Т-клеточные ответы с пролонгированной экспрессией цитокинов были выявлены у пациентов с тяжелым заболеванием SARS, тогда как быстрое переключение врожденного иммунного ответа и мощный противовирусный антительный ответ были установлены у выздоровевших пациентов [23].
Предполагают, что вирус может ускользать от действия факторов врожденного иммунного ответа и способен блокировать систему интерферона.
Клиническая картина MERS-CoV-инфекции
По данным литературы, у пациентов без сопутствующих заболеваний в большинстве случаев MERS-CoV-инфекция протекает практически бессимптомно или в легкой форме. Серьезная клиническая картина MERS развивается наиболее часто у лиц с сопутствующей патологией, такой как сахарный диабет, почечная недостаточность, ожирение, предшествующая иммуносупрессия, болезни сердца и легких (6–10), а также у лиц старше 65 лет [15, 24, 27, 28].
Инкубационный период, в случае передачи инфекции от человека к человеку, варьирует от 2 до 14 дней (составляя в среднем 5 дней).
MERS в типичных случаях начинается с лихорадки, озноба, кашля, болей в горле, миалгий, артралгий, с последующей одышкой и быстрым развитием пневмонии в течение первой недели болезни, часто требующей респираторной и другой органной поддержки [24, 28–32]. У большинства пациентов с манифестной формой MERS имеет место респираторное заболевание, у иммуноскомпроментированных лиц заболевание может проявиться лихорадкой, ознобом, диареей и лишь затем развитием пневмонии [33]. По аналогии с SARS, у трети пациентов с MERS имеют место гастроинтестинальные симптомы, такие как рвота и диарея [30, 31].
По данным анализа вспышек MERS-CoV в Саудовской Аравии, болезнь характеризовалась острым началом с повышением температуры до 38–39? С (98% случаев), ознобом (87%), головной болью (11%), головокружением и слабостью (38%), миалгиями (32%), болями в глазных яблоках. Ринорея и першение в горле отмечались редко — в 8% и 14% случаев соответственно. Частым симптомом был кашель (у 83% больных). В начальные сроки кашель чаще был сухой (у 56%), порою изнуряющий, имел тенденцию к усилению вечером и ночью. В некоторых случаях наблюдались симптомы поражения желудочно-кишечного тракта — тошнота, диарея, необильная рвота (21–30%). В разгаре заболевания лихорадка сохранялась, появлялся продуктивный кашель (в 44% случаев), стеснение в области грудной клетки, одышка (в 72% случаев), кровохарканье (17%). Среднее время от начала заболевания до госпитализации составляло 0–4 дня, от начала болезни до поступления в палату интенсивной терапии 1–5 дней, от начала болезни до летального исхода — 5–11 дней [7].
Пневмония развивалась у абсолютного большинства пациентов с тяжелым течением MERS-CoV на первой неделе заболевания. В легких с обеих сторон выслушивались влажные крепитирующие, мелкопузырчатые хрипы. При перкуссии определялось притупление легочного звука [34].
Одним из тяжелейших проявлений MERS-CoV, как и SARS-CoV, является острый респираторный дистресс-синдром (ОРДС). Для него характерны признаки поражения нижних дыхательных путей — одышка, чувство нехватки воздуха, усиление кашля, значительные физикальные изменения в легких с появлением большого количества хрипов, нарастающая гипоксия и гипоксемия, снижение SaO2 < 90%.
Характерна стойкая тахикардия, повышение центрального венозного давления. Систолическое давление в легочной артерии (по данным эхокардиографии) выше 30 мм рт. ст. Появляются первые признаки полиорганной недостаточности — нарушение функции почек. Появляются периоды олигурии, но плотность мочи не снижена (1015–1020) и осмолярность нормальна (400–500 мосм/л).
В периферической крови у части больных MERS выявляется лейкопения, лимфопения менее 1,5 × 10 9 /л, тромбоцитопения менее 140 × 10 9 /л. При биохимическом анализе крови у половины больных регистрируется повышение активности лактатдегидрогеназы (в 48%), реже — аланинаминотрансферазы (в 11%), аспартатаминотрансферазы (в 14%). У части пациентов выявляется коагулопатия потребления и повышение креатинина крови [7, 11, 35, 38, 34].
У детей MERS возникает редко. Так, из 11 лабораторно подтвержденных случаев инфицирования детей в Саудовской Аравии, у 9 человек инфекция протекала бессимптомно, а у 2 заболевание протекало в манифестной форме на фоне врожденной генетической патологии: синдрома Дауна и муковисцидоза [39].
Критерии диагностики
Критерии диагностики MERS разработаны ВОЗ, Центром по контролю и предотвращению болезней США и Министерством здравоохранения Саудовской Аравии. В дополнение к лихорадке, пневмонии и острому респираторному дистресс-синдрому, в диагностике важную роль играет эпиданамнез, в частности, факт пребывания в эндемичных районах Ближнего Востока и других стран, в которых были зафиксированы случаи MERS, контакт с больными, посещавшими страны Аравийского полуострова, или с теми, у кого подозревали MERS [7]. Для верификации случаев MERS-CoV-инфекции используются лабораторные методы диагностики.
ВОЗ рекомендует использовать два метода лабораторной диагностики этого заболевания — двухэтапную обратно-транскриптазную полимеразную цепную реакцию в реальном времени (ОТ-ПЦР-РВ) и иммуноферментный анализ [40]. Материал для исследования берется как из верхних, так и из нижних дыхательных путей: мазок из носа, носоглотки и/или горла; мокрота, аспират из трахеи, бронхоальвеолярный лаваж. Наибольшая концентрация вируса MERS-CoV содержится в секрете нижних дыхательных путей, поэтому контагиозность инфекции не столь высока, как при гриппе. Установлено, что в бронхоальвеолярном лаваже даже через месяц от начала заболевания в некоторых случаях можно выделить MERS-CoV [7]. Последний может содержаться в крови, моче и кале пациентов, но в более низкой концентрации, чем в дыхательных путях [7, 11]. Для улучшения этиологической диагностики исследования клинического материала из разных отделов дыхательных путей проводят в динамике через каждые 2–3 дня. Материалы отправляют в лабораторию как можно раньше. В случае задержки требуется замораживание с применением сухого льда.
Метод иммуноферментного анализа (ИФА) применяется ретроспективно с целью определения наличия вирусоспецифических антител в сыворотках крови реконвалесцентов. ИФА-анализ проводится двухкратно: на первой неделе заболевания и через 14–21 день. При однократном проведении анализа сыворотка крови берется не ранее 14-го дня от начала заболевания [7, 15, 41]. Результаты ИФА должны тщательно интерпретироваться, так как возможны перекрестные реакции с другими коронавирусами [42].
Тактика ведения больных
Госпитализации подлежат [11]:
- Лица с лихорадкой и пневмонией или ОРДС (установленных на основании клинических или рентгенологических данных), посещавшие страны Аравийского полуострова за 14 дней до появления первых симптомов заболевания или имевшие тесный контакт с больным, который посещал Аравийский полуостров.
- Лица с наличием лихорадки и симптомов респираторного заболевания при условии, если они находились в медицинском учреждении (в качестве пациента, работника или посетителя), где были выявлены случаи заболевания MERS-CoV.
Этиотропные лекарственные средства должны быть назначены как можно раньше (в первые часы/дни заболевания). В качестве противовирусного препарата широкого спектра действия рекомендован Рибавирин. Дозировка препарата зависит от клиренса креатинина:
- при клиренсе креатинина > 60 мл/ мин — по 400 мг в/в каждые 8 часов в течение 3 дней, затем перорально по 1200 мг 2 раза в день в течение еще 7 дней;
- при клиренсе креатинина 30–60 мл/ мин — по 300 мг в/в каждые 12 часов в течение 3 дней, затем перорально по 600 мг два раза в день в течение еще 7 дней;
- при клиренсе креатинина < 30 мл/ мин — по 300 мг в/в каждые 24 часа в течение 3 дней, затем перорально по 600 мг 1 раз в день 7 дней.
В экспериментальных исследованиях на модели макак-резусов, инфицированных MERS-CoV, была показана эффективность применения комбинации Рибавирина и Интерферона-α2b (ИФН-α2b) [43], что позволило сделать вывод о перспективности такого метода лечения MERS-CoV. Данная комбинация применялась у тяжелобольных пациентов (Рибавирин 400–600 мг каждые 8 часов в сочетании с ИФН-α2b в дозе 100 мкг 2 раза в день подкожно), установлено повышение их выживаемости [44]. Несколько препаратов ингибируют MERS-CoV в клеточной культуре, включая интерфероны 1-го типа (ИФН-α и особенно ИФН-β), циклоспорин, хлорохин, хлорпромазин, лоперамид, лопинавир [7, 44–47], но эффективны ли эти препараты in vivo, пока неизвестно.
В лечении больных MERS с успехом использовались моноклональные антитела anti-MERS-CoV и сыворотка крови выздоровевших больных [48–51].
Системные кортикостероиды назначались эмпирически в некоторых случаях, для подавления иммунопатологических реакций, но не влияли на выживаемость пациентов [29, 52]. Кроме того, у больных SARS во время эпидемии 2002–2003 гг. они даже ухудшали состояние [7, 53], поэтому должны использоваться с осторожностью.
Профилактика
При госпитализации больного с подозрением на MERS предусмотрена профилактика внутрибольничной инфекции:
- пациент должен быть изолирован в бокс инфекционного стационара (при перемещении пациентов необходимо применять маски-респираторы);
- медперсонал должен применять средства индивидуальной защиты (перчатки, халат, очки для защиты глаз, средства защиты органов дыхания), должна соблюдаться гигиена рук (мыть с мылом под проточной водой или с помощью антисептических средств на спиртовой основе);
- за состоянием здоровья медицинских работников должен осуществляться контроль в течение 14 дней после последнего контакта с больным.
Посещения больного родственниками и знакомыми должны быть ограничены, а также должно быть сокращено количество персонала, имеющего прямой контакт с пациентом.
Заключение
Появление и распространение MERS-CoV-инфекции является достаточно серьезным явлением в мире. Расшифрован генетический код возбудителя, оказалось, что MERS-CoV, подобно вирусу SARS, является разновидностью коронавируса, резервуаром которого являются животные. Данный зооноз преодолел межвидовой барьер и стал передаваться от человека человеку. Изучены основные пути распространения болезни, механизмы повреждающего действия возбудителя, типичные клинические проявления заболевания, разработана тактика лечения, ведется интенсивный поиск препаратов прямого противовирусного действия. Высокие патогенные свойства вируса, охват заболеваемостью многих стран, вовлечение в сферу распространения новых регионов таят угрозу прогрессирования эпидемии этого потенциально особо опасного заболевания. Возможность завоза MERS-CoV-инфекции в разные регионы мира и высокий риск внутрибольничного инфицирования требуют особой бдительности эпиднадзора, диагностических и лечебных служб, знаний врачей основных профилактических мероприятий. Масштаб распространения данной инфекции нам еще предстоит узнать.
Литература
Е. И. Краснова 1 , доктор медицинских наук, профессор
В. В. Проворова, кандидат медицинских наук
Н. И. Хохлова, кандидат медицинских наук
И. В. Куимова, доктор медицинских наук
ТОРС – это воспалительная патология легочной ткани вирусной этиологии. Характеризуется нарастающей тяжелой дыхательной недостаточностью вследствие респираторного дистресс-синдрома. Клиническая картина также включает в себя лихорадку, сухой кашель, выраженную одышку. Диагностика осуществляется с помощью молекулярно-генетических методов (выявление возбудителя) и серологических исследований (поиск антител). Лечение заболевания преимущественно патогенетическое и симптоматическое, этиотропного препарата с доказанной вирулицидной эффективностью в настоящее время не разработано.
МКБ-10
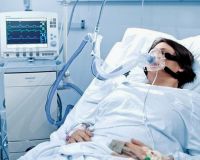
Общие сведения

Причины ТОРС
Характеристика воздудителя
Возбудитель инфекции – РНК-содержащий коронавирус SARS–CoV. Представляет собой сферический микроорганизм с шиповидными выростами, тропизмом к клеткам альвеол, печени, кишечника, также почек, сердца, глаза. Резервуар инфекции в дикой природе – летучие мыши, источник – больной или бессимптомный носитель. Основной путь передачи – воздушно-капельный, также передача вируса может осуществляться контактным и гораздо реже ‒ фекально-оральным путем.
Факторы риска
Основные факторы риска: возраст старше 65 лет, иммунные дефициты, связанные с ВИЧ-инфекцией, онкологическими болезнями, приемом системных кортикостероидов. К уязвимой группе относят лиц с заболеваниями легких, сердечно-сосудистой системы, сахарным диабетом, ожирением. Высока вероятность заболевания у медицинских работников, лиц, осуществляющих уход за больными дома.
Патогенез
При попадании на слизистую рото- и носоглотки коронавирусы колонизируют эпителий. Они имеют различные механизмы связи с рецепторами. Так, с эпителиальными клетками взаимодействие происходит посредством аминопептидазы. Ведущая роль в механизме связывания с рецепторами клеток человека принадлежит гликопротеину шиповидных отростков. Вышедшие вирионы способны вновь сорбироваться на поверхности клеток, вызывая их слияние и стимулируя иммунный ответ хозяина.
Основными клетками-мишенями являются клетки альвеолярного эпителия, макрофаги. Коронавирусы, обладая способностью к индукции апоптоза, вызывают некроз пораженных тканей. Индуцирование слияния клеток оказывает сильное воздействие на их проницаемость, приводит к нарушению водно-солевого баланса и транспорта белков. В этих условиях развивается недостаточность сурфактанта, возникают симптомы легочного дистресс-синдрома.
Симптомы ТОРС
Первые симптомы тяжелого острого респираторного синдрома возникают после инкубационного периода, который составляет 5 дней (от 2 до 10 суток). Обычно пациенты предъявляют жалобы на гриппоподобный синдром: лихорадку более 38,5°C, ознобы, головную боль. Отмечается выраженная слабость, боли в мышцах, снижение работоспособности. К концу первой недели болезни или к началу второй появляется сухой мучительный кашель, который при коронавирусной инфекции обычно беспокоит больных по ночам.
Наиболее грозным проявлением ТОРС является одышка. Пациенты отмечают нарастающее чувство нехватки воздуха, особенно в ночные часы, при разговоре или натуживании, затруднение, как вдоха, так и выдоха. Позднее больные вынуждены принимать позу с опорой на руки, дыхание становится хриплым, шумным, кожа приобретает багрово-синюшный оттенок. Параллельно могут возникать першение, сухость в горле, симптомы диареи.
Осложнения
Диагностика
Диагностика коронавирусной инфекции, её лечение осуществляется совместно врачами-инфекционистами, пульмонологами, реаниматологами. Другие медицинские специалисты привлекаются по показаниям. Важен сбор эпидемиологического анамнеза, включая данные о путешествиях в эндемичные районы, семейных, рабочих контактах больного. Основные клинические, инструментальные и лабораторные методы диагностики ТОРС:
Дифференциальная диагностика
Схожие клинические симптомы наблюдаются при гриппе, респираторно-синцитиальной вирусной патологии, MERS, что требует их лабораторной верификации. Необходимо дифференцировать ТОРС с пневмониями, вызванными Haemophilus influenzae, Mycoplasma pneumoniae, Chlamydia species, реже Legionella species, Сoxiella burnetii, пневмококком. Дифференциальный диагноз проводится с ХОБЛ, бронхоэктатической болезнью, анафилаксией.
Лечение ТОРС
Симптомы SARS, выявляемые у пациента, являются показанием к госпитализации, за исключением легких случаев, когда допускается амбулаторное лечение с соблюдением правил самоизоляции, обязательным медицинским контролем состояния. Стационары должны быть оборудованы палатами интенсивной терапии, реанимационными отделениями. Специфической диеты нет, питьевой режим вне противопоказаний не ограничивается.
Консервативная терапия
Стандартизированное лечение ТОРС отсутствует. Предпочтительна симптоматическая терапия: жаропонижающие, препараты сурфактанта, дезинтоксикационные и иные средства. Использование системных кортикостероидов увеличивает риск внутрибольничных инфекций ‒ диссеминированных грибковых заболеваний, нарушений обмена веществ, остеонекроза. Данные препараты, назначаемые на ранних стадиях ТОРС, могут пролонгировать виремию.
Вирус ТОРС склонен к нозокомиальному распространению, поэтому использование небулайзеров, спейсеров и кислородотерапии через назальные катетеры либо маску должно быть запрещено или строго ограничено. При нарастании дыхательной недостаточности, респираторных симптомов дистресс-синдрома пациент переводится на ИВЛ. По показаниям применяется ЭКМО.
Экспериментальное лечение
Лечение с использованием рибавирина не доказало своей эффективности при ретроспективном исследовании. Применение высоких доз препарата приводило к задокументированному снижению гемоглобина у 59% пациентов, среди 36% больных регистрировался гемолиз, были отмечены гепатотоксичные, кардиотоксичные эффекты. Сочетание с лопинавиром/ритонавиром снижало частоту интубаций, а также общую смертность до 2,3%.
Лопинавир, бустированный ритонавиром, является препаратом для терапии ВИЧ-инфекции. Лечение с введением данного средства при ТОРС показало снижение вирусной нагрузки коронавируса, позволяло уменьшить дозу метилпреднизолона. Ингибирующим эффектом на возбудителя также обладал интерферон альфакон-1, однако исследование проводилось всего на 9 пациентах, сопровождалось приемом кортикостероидов и не было контролируемым.
Лечение при помощи пассивной иммунизации с помощью плазмы выздоровевших больных использовалось на небольшом числе пациентов, однако имело эффект в виде значительного снижения смертности по сравнению с плацебо либо отсутствием терапии. Наилучшие результаты получены в группе инфицированных ТОРС, которым вводили плазму не позднее 14-го дня болезни. Также предлагалась концепция человеческих моноклональных антител.
Прогноз и профилактика
Прогноз при своевременном выявлении, отсутствии соматической декомпенсированной патологии благоприятный. Летальность ТОРС составляет около 4%, варьирует от 0 до 40% в зависимости от исходного состояния заболевшего. Специфическая профилактика (вакцина) находится в стадии разработки. Неспецифические меры: использование масок заболевшими, частое мытье рук с мылом, кашлевой этикет, в медицинских учреждениях – строгое соблюдение санитарных норм.
2. SARS (Severe Acute Respiratory Syndrome), или ТОРС (тяжелый острый респираторный синдром)/ Н. В. Астафьева, Е. Г. Белова// Лечащий врач. – 2003- № 9.
4. Immune responses in COVID-19 and potential vaccines: Lessons learned from SARS and MERS epidemic/ E. Prompetchara, Ch. Ketloy, T. Palaga// Asian Pacific Journal of Allergy and Immunology. - 2020.
Ближневосточный респираторный синдром – это острое, высоколетальное инфекционное заболевание, вызываемое РНК-содержащим бета-коронавирусом. Патогномоничными симптомами инфекции служат преимущественное поражение дыхательного тракта с высокой вероятностью развития респираторного дистресс-синдрома взрослых. Клинически заболевание проявляется лихорадкой, одышкой, кашлем, кровохарканьем. Диагностика патологии подразумевает обнаружение вируса и Ат к нему в биоматериале заболевшего. Этиотропная терапия состояния включает противовирусные препараты; в лечении также используются симптоматические средства (жаропонижающие, муколитики и другие).
МКБ-10
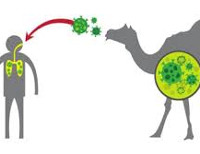
Общие сведения
Ближневосточный респираторный синдром (БВРС, MERS) представляет собой острое вирусное поражение респираторного тракта. Впервые о данном заболевании стало известно в 2012 году, когда в Саудовской Аравии был выявлен пациент с симптомами данной болезни. К 2015 г. эпидемия MERS охватила 25 стран Ближнего Востока, Африки, Азии, Европы. Наиболее массовая вспышка инфекции, вызванная бета-коронавирусом, случилась в Южной Корее, где погибло более 30 человек, в карантине находились почти 3000 контактных лиц. Заболеваемость повышается в зимне-весенний сезон (особенно в марте и апреле), что связывают с инфицированием человека от молодых верблюдов. Чаще поражаются взрослые (более 90%) в возрасте 50 лет и старше.

Причины БВРС
Возбудитель заболевания – коронавирус ближневосточного респираторного синдрома, принадлежащий к роду бета-коронавирусов линии С. Впервые у человека данный вирус был выделен в 2012 году, ранее обнаруживался только среди одногорбых верблюдов. Изучение вопроса показало, что животные инфицировались при рождении либо в первые месяцы жизни, в дальнейшем примерно треть из них становились бессимптомными носителями коронавируса. Следовательно, источниками инфекции могут быть как больные животные, люди, так и носители вируса.
Заражение людей с помощью аэрогенного механизма передачи от верблюдов доказано в небольшом числе случаев болезни, чаще всего причиной инфицирования служило употребление в пищу некипяченого верблюжьего молока, недостаточно термически обработанного мяса, соприкосновение с мочой, кровью и фекалиями больного животного при уходе за ним. Заражение здоровых лиц от больного человека происходит преимущественно воздушно-капельным путём, может реализоваться при контакте с инфицированными биологическими жидкостями и в быту через контаминированные коронавирусом предметы обихода.
Описаны внутрибольничные заражения: южнокорейская эпидемия является следствием внутригоспитального инфицирования от нулевого пациента с завозным случаем болезни. Возбудитель малоустойчив в окружающей среде: чувствителен к воздействию стандартных доз дезинфектантов, ультрафиолетовому облучению и нагреванию.
Группами риска по заболеванию являются лица старше 65 лет, с сопутствующими заболеваниями (сахарный диабет, ожирение, патологии почек, сердца, болезни лёгких, ВИЧ-инфекция, злокачественные новообразования), жители коммунальных квартир, бараков, общежитий, военнослужащие, ветеринары, скотоводы, сотрудники зоопарков, цирков, медработники и сотрудники сферы обслуживания. У детей болезнь встречается редко, описанные случаи наблюдались среди больных с врожденными патологиями (синдром Дауна, муковисцидоз и другие).
Патогенез
Патогенез заболевания изучен недостаточно, патоморфологические исследования ввиду религиозных убеждений не могли быть проведены в ряде стран. Определено, что бета-коронавирус обладает тропностью к клеткам бронхиального эпителия и альвеолярным пневмоцитам 2 типа, клеткам почек и Т-лимфоцитам. При попадании в респираторный тракт возбудитель активно размножается в эпителии трахеи, вызывая дискинезию ресничек, клетках бронхов, подвергая их массовой деструкции и нарушая мукоцилиарный клиренс. Внутри альвеолоцитов вирус способен вызывать дисрегуляторные изменения в генах.
Почечная недостаточность при данной патологии обусловлена прямым повреждающим действием вируса, и, в неменьшей степени, гипоксическим поражением тканей. Патогистологически при MERS обнаруживаются геморрагические проявления, апоптоз, диффузные поражения альвеол, сквамозная метаплазия альвеолоцитов, явления бронхиолита, а также формирование эозинофильных гиалиновых мембран, нарушение активности сурфактанта. Были описаны явления портально-долькового гепатита и миозита с атрофическими изменениями мышц; серое и белое вещество головного мозга, кардиомиоциты при данной болезни не имели специфических повреждений.
Иммунитет после перенесенного заболевания, его длительность, напряженность изучаются; есть данные о возможности повторного заражения. Считается, что вирус способен вызывать функциональный паралич системы продукции интерферона, может задерживать физиологическое образование провоспалительных цитокинов.
Симптомы БВРС
Через 2-4 дня развивается клиника тяжелой вирусной пневмонии. Беспокоит появление кашля с необильной мокротой, чувство сжатия, стеснения в груди, одышка с тенденцией к усугублению, иногда появляется кровохарканье. Нарастание дыхательной недостаточности вынуждает больных принимать специальную позу, облегчающую их состояние (сидя, опершись на руки). Отмечается западание межреберных промежутков, надключичных ямок, синюшный оттенок кожи конечностей, изменения сознания (от возбуждения до апатии). Могут появиться признаки поражения мочевыделительной системы в виде тенденции к олигоурии.
Осложнения
Опасность БВРС заключается в развитии острого респираторного дистресс-синдрома, сопровождающегося резкой гипоксией и гипоксемией. Самостоятельное дыхание становится затруднительным, больные нуждаются в вентиляционном пособии. Кроме ДН, к числу наиболее частых осложнений ближневосточного респираторного синдрома следует отнести острую сердечную, почечную, полиорганнную недостаточность. В связи с выполнением инвазивных медицинских манипуляций и лечебных процедур (внутривенные, внутримышечные инъекции, искусственная вентиляция лёгких, постановка сосудистых, мочевых катетеров и др.) возможно появление вторичной бактериальной инфекции.
Диагностика
При подозрении на бета-коронавирусную инфекцию обязательна консультация инфекциониста, пульмонолога и реаниматолога, при выраженном гастроэнтерите - гастроэнтеролога. Этиологическая верификация возбудителя и вспомогательная диагностика проводится физикальными, лабораторными и инструментальными методами, включающими:
Дифференциальную диагностику проводят с атипичной пневмонией (ТОРС) и COVID-19. Необходимо исключить другие респираторные заболевания: грипп, легионеллёз, орнитоз, аспергиллёз, микоплазмоз, пневмоцистоз, туберкулезный казеозный распад лёгких. Требуется разграничение с брюшным тифом, сепсисом, бактериальными пневмониями, бронхитами. Симптомы гастроэнтерита следует дифференцировать с вирусными диареями, энтеровирусной инфекцией, пищевыми отравлениями, сальмонеллёзом и шигеллёзом.
Лечение БВРС
Госпитализации в инфекционный стационар подлежат все больные с подозрением на инфекцию. Контактные лица подвергаются разобщению с коллективом на максимальный срок инкубационного периода MERS (14 суток). Больным рекомендуется обильное питьё, частый приём легких и питательных блюд небольшими порциями.
Специфического лечения ближневосточного респираторного синдрома не разработано. Существующие этиотропные препараты широкого спектра действия должны быть введены в первые дни, в идеале – в первые часы заболевания. Во время вспышек на Ближнем Востоке и Корее наилучшие результаты лечения достигались при применении рибавирина, часто в сочетании с интерфероном α2β. Успешным оказалось использование моноклональных антител к бета-коронавирусу, препаратов сыворотки крови реконвалесцентов. Использование системных глюкокортикостероидов не влияло на уменьшение смертности больных MERS, в ряде случаев их применение было оправдано уменьшением выраженности иммунопатологических реакций.
Симптоматическая терапия предусматривает использование муколитиков, вазопротекторов, антибиотиков (в случае доказанного вторичного бактериального поражения), дезинтоксикационных средств (реополиглюкин, глюкозо-солевые растворы) и других. Нарастание дыхательной недостаточности является показанием для начала оксигенотерапии и перевода больных на искусственную вентиляцию лёгких.
Прогноз и профилактика
Прогноз заболевания зависит от возраста, наличия сопутствующей патологии, своевременности обращения за медицинской помощью, но всегда серьёзный. Среднее число дней до поступления в стационар составляет 0-4 суток от дебюта клинических проявлений; до наступления состояния, требующего неотложных реанимационных мероприятий, ‒ 1-5 суток от начала болезни. Смерть чаще всего наступает через 5-11 дней; летальность при заболевании составляет около 35 %.
Средств специфической профилактики (вакцин) на данном этапе развития медицины не существует, но ведутся активные разработки в этой области. К неспецифическим мерам профилактики относится избегание посещений стран с высокой заболеваемостью MERS (ОАЭ, Саудовская Аравия, Южная Корея, Бахрейн, Катар и ряд других), употребления в пищу верблюжьего мяса и некипяченого молока, отказ от массовых мероприятий, контактов с больными людьми и животными. При вынужденном пребывании рядом с потенциальным источником заражения рекомендуется использование одноразовых масок или респираторов, защитных очков или щитков на глаза, перчаток, халатов (эти правила распространяются и на медицинских работников), частое гигиеническое мытье рук с мылом или антисептическим средством на спиртовой основе.
1. Ближневосточный респираторный синдром/ Краснова Е.И., Проворова В.В., Хохлова Н.И., Куимова И.В.// Лечащий врач. – 2015.
2. Коронавирус ближневосточного респираторного синдрома (БВРС-КоВ) – информация и обзор последних публикаций (по состоянию на 20 января 2014 г.)/ ВОЗ.
4. Эпидемическая вспышка ближневосточного респираторного синдрома в Республике Корея (май-июль 2015 г.): причины, динамика, выводы/ Щелканов М.Ю., Ананьев В.Ю., Кузнецов В.В., Шуматов В.Б.// Тихоокеанский медицинский журнал – 2015 - №3.
Что такое острые респираторные заболевания (ОРЗ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Острые респираторные заболевания (ОРЗ) — группа острых инфекционных заболеваний, при которых возбудители проникают в организм человека через дыхательные пути и вызывают синдром поражения респираторного тракта и общей инфекционной интоксикации. Употребление термина ОРВИ (острое респираторное вирусное заболевание) при отсутствии лабораторно подтверждённой этиологической расшифровки является некорректным.
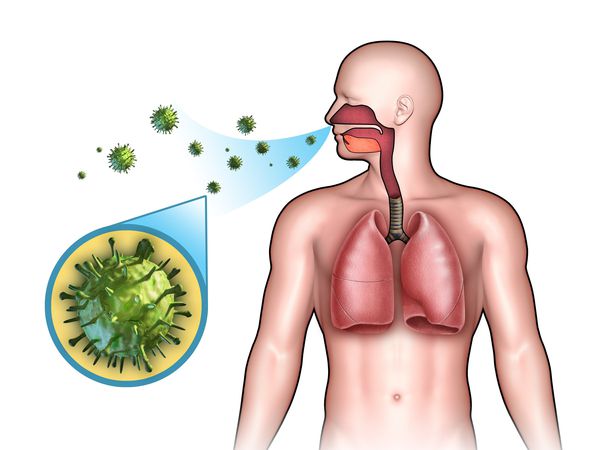
Этиология
ОРЗ — полиэтиологический комплекс заболеваний, т. е. они могут быть вызваны различными видами возбудителей:
- бактерии (стафилококки, стрептококки, пневмококки, гемофильная палочка, моракселла катаралис и др.);
- вирусы (риновирусы, аденовирусы, респираторно-синцитиальный вирус, реовирусы, коронавирусы, энтеровирусы, герпесвирусы, вирусы парагриппа и гриппа);
- хламидии (х ламидия пневмония , хламидия пситаки, хламидия трахоматис );
- микоплазмы (м икоплазма пневмония ).
Чаще всего возбудителем ОРЗ являются вирусы, поэтому термин ОРВИ используют небезосновательно. В последнее время иногда встречается употребление термина ОРИ (острая респираторная инфекция) [2] [4] .
Эпидемиология
ОРЗ — это преимущественно антропонозы, т. е. болезни, способные поражать только человека . Являются самой многочисленной и частой группой заболеваний у человека (до 80 % всех болезней у детей). Поэтому они представляют серьёзную проблему для здравоохранения различных стран вследствие наносимого ими экономического ущерба.
Источник инфекции — больной человек с выраженными или стёртыми формами заболевания. Восприимчивость всеобщая, иммунитет к некоторым возбудителям (аденовирусы, риновирусы) стойкий, но строго типоспецифичный. Это значит, что заболеть ОРЗ, вызванным одним видом возбудителя, но разными серотипами (их могут быть сотни), можно многократно. Заболеваемость повышается в осенне-зимний период, может принимать вид эпидемических вспышек, довлеет к странам с прохладным климатом. Чаще болеют дети и лица из организованных коллективов (особенно в период адаптации).
Основной механизм передачи — воздушно-капельный (аэрозольный, в меньшей степени воздушно-пылевой путь), но может также играть роль контактно-бытовой механизм (контактный — при поцелуях, бытовой — через загрязнённые руки, предметы или воду) [2] [7] .
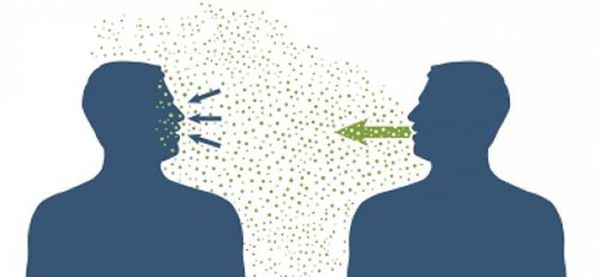
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острых респираторных заболеваний (ОРЗ)
Инкубационный период различен и зависит от вида возбудителя, может варьироваться от нескольких часов до 14 дней (аденовирус).
Для каждого возбудителя ОРЗ имеются свои специфические особенности протекания заболевания, однако все их объединяет наличие синдромов общей инфекционной интоксикации (СОИИ) и поражения дыхательных путей в той или иной степени. СОИИ проявляется общей слабостью, адинамией, быстрой утомляемостью, повышенной температурой тела, потливостью и др.
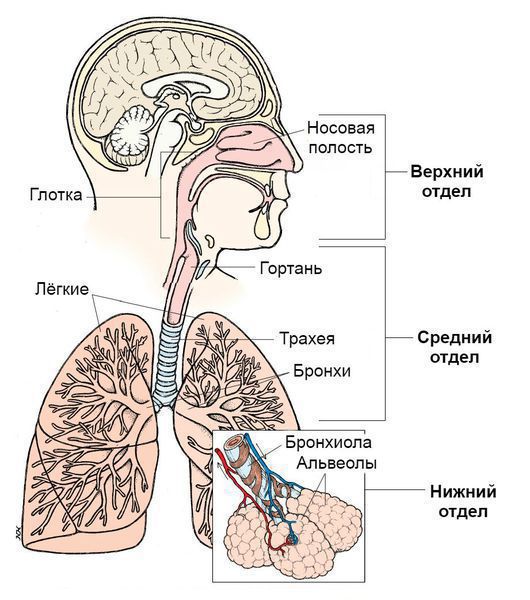
Синдром поражения респираторного тракта (СПРТ) — основной синдром для данных заболеваний, он включает:
- Ринит — воспаление слизистой оболочки носа. Характеризуется заложенностью носа, снижением обоняния, чиханием, выделениями из носа — сначала прозрачными слизистыми, затем слизисто-гнойными (более плотные выделения жёлто-зелёного цвета появляются в результате присоединения вторичной бактериальной флоры). — воспаление слизистой оболочки глотки. Основные симптомы: першение и боли в горле различной интенсивности, сухой кашель — "горловой".
- Ларингит — воспаление слизистых оболочек гортани. Проявляется осиплостью голоса, иногда афонией (отсутствием голоса), кашлем и болью в горле.
- Трахеит — воспаление трахеи. Сопровождается мучительным, преимущественно сухим кашлем, саднением и болями за грудиной.
- Бронхит — воспаление слизистой оболочки бронхов. При этом возникает кашель с наличием мокроты и без, сухие хрипы, редко крупнопузырчатые хрипы при аускультации (выслушивании).
- Бронхиолит — воспаление бронхиол (мелких бронхов). Характеризуется наличием кашля различной интенсивности и хрипов разных калибров.
Дополнительными синдромами могут быть:
- синдром экзантемы (высыпания на кожных покровах);
- тонзиллита (воспаления миндалин);
- лимфаденопатии (ЛАП) — увеличения лимфатических узлов ; ( воспаления слизистой оболочки глаза) ;
- гепатолиенальный синдром (увеличение печени и селезёнки);
- геморрагический синдром ( повышенная кровоточивость) ;
- синдром энтерита (воспаления слизистой оболочки тонкого кишечника) .
Алгоритм по распознаванию ОРЗ различной этиологии:
Наиболее распространенным заболеванием, имеющим тяжёлое течение и высокий риск развития осложнений является грипп. Инкубационный период гриппа длится от нескольких часов до 2-3 дней. В отличие от других острых респираторных заболеваний, при гриппе сначала появляется синдром общей инфекционной интоксикации (высокая температура, озноб, сильная головная боль, слезотечение, боль при движении глазных яблок, ломота в мышцах и суставах). На 2-3-день присоединяются симптомы поражения респираторного тракта: першение в горле, насморк, сухой надсадный кашель.
Типичное ОРЗ начинается с чувства дискомфорта, першения в носу и горле, чихания. В течение непродолжительного периода симптоматика нарастает, першение усиливается, появляется чувство интоксикации, повышается температура тела (обычно не выше 38,5 ℃), появляется насморк, неярко-выраженный сухой кашель. В зависимости от вида возбудителя и свойств микроорганизма могут последовательно появляться все перечисленные синдромы ОРЗ в различных сочетаниях и степени выраженности. Возможно появление осложнений и неотложных состояний [6] [7] .
Патогенез острых респираторных заболеваний (ОРЗ)
- у аденовирусов — гликопротеином (фибриллы);
- у парамиксо- или ортомиксовирусов шипами гемагглютинина;
- у коронавирусов — S-белком соединения и гликолипидами.
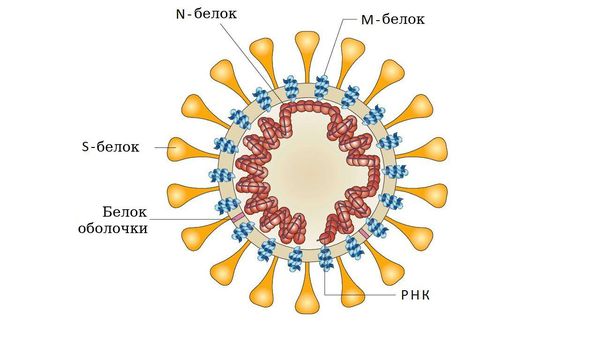
Взаимодействие болезнетворного агента с клеточными рецепторами необходимо не только для прикрепления его к клетке, но и для запуска клеточных процессов, подготавливающих клетку к дальнейшей инвазии. Т. е. наличие соответствующих рецепторов на поверхности клеток — это один из важнейших факторов, определяющих возможность или невозможность возникновения инфекционного процесса. Внедрение возбудителя в клетку хозяина вызывает поток сигналов, активирующих целый ряд процессов, с помощью которых организм пытается от него освободиться, например, ранний защитный воспалительный ответ, а также клеточный и гуморальный иммунный ответ. Повышение метаболизма клеток представляет собой защитный процесс, но с другой стороны в результате накопления свободных радикалов и факторов воспаления запускается патологический процесс:
- нарушается липидный слой клеточных мембран эпителия верхних отделов респираторного тракта и лёгких;
- нарушаются матричные и барьерные свойства внутриклеточных мембран, увеличивается их проницаемость;
- развивается дезорганизация жизнедеятельности клетки вплоть до её гибели.
Второй этап инфицирования характеризуется вирусемией — попаданием вируса в кровь и распространением по всему организму. В совокупности с повышением деятельности защитных механизмов и появлением в крови продуктов распада клеток этот процесс вызывает интоксикационный синдром.
Третий этап характеризуется усилением выраженности реакций иммунной защиты, элиминацию (выведение) микроорганизма и восстановление строения и функции поражённой ткани хозяина [5] [7] .
Классификация и стадии развития острых респираторных заболеваний (ОРЗ)
По вовлечению отдельных частей дыхательной системы:
- Инфекции верхних дыхательных путей. Верхние дыхательные пути начинаются с носа и включают голосовые связки в гортани, придаточные пазухи носа и среднее ухо.
- Инфекции нижних дыхательных путей. Нижние дыхательные пути начинаются с трахеи и бронхов и заканчиваются бронхиолами и альвеолами.
По клинической форме:
- Типичная.
- Атипичная:
- акатаральная (отсутствие признаков поражения дыхательных путей при наличии симптомов общей инфекционной интоксикации);
- стёртая (маловыраженная клиника);
- бессимптомная (полное отсутствие клинической симптоматики).
По течению:
По степени тяжести:
По длительности течения:
- острое (5-10 дней);
- подострое (11-30 дней);
- затяжное (более 30 дней) [8] .
Осложнения острых респираторных заболеваний (ОРЗ)
Если острое респираторное заболевание не пролечить вовремя, могут появиться различные более серьёзные заболевания:
- Связанные с ЛОР-органами: отит, синуситы, бактериальный ринит, ложный круп.
- Связанные с лёгочной тканью: вирусные пневмонии, вирусно-бактериальные и бактериальные пневмонии, абсцесс лёгкого ( ограниченный очаг гнойного воспаления в лёгочной ткани) , эмпиема плевры ( скопление гноя в плевральной полости) . Пневмония проявляется значимым ухудшением общего состояния, выраженным кашлем, усиливающимся на вдохе, при аускультации звуком крепитации ( потрескиванием или похрустыванием) , влажными мелкопузырчатыми хрипами, иногда одышкой и болями в грудной клетке.

- Связанные с поражением нервной системы: судорожный синдром, неврит ( воспаление нерва) , менингит ( воспаление оболочек головного и спинного мозга) , менингоэнцефалит (воспаление оболочек и вещества головного мозга), синдром Гийена—Барре и др. [10]
- Связанные с поражением сердца: миокардит (воспаление сердечной мышцы).
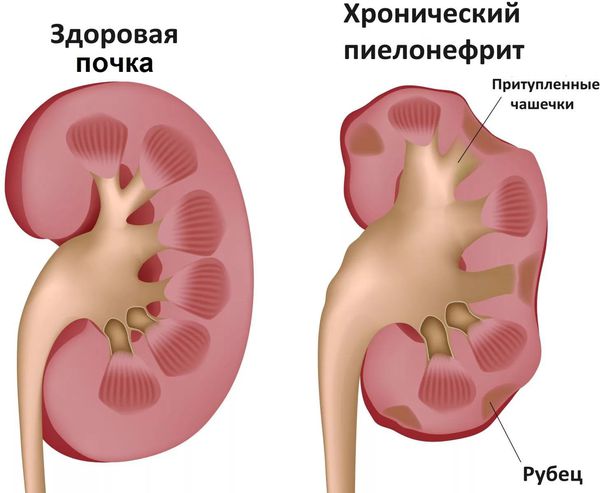
- Связанные с обострением хронических заболеваний: обострение ревматизма, тонзиллита, туберкулёза, пиелонефрита (воспаление почки) и др. [7]
Диагностика острых респираторных заболеваний (ОРЗ)
В широкой рутинной практике лабораторная диагностика ОРЗ (особенно при типичном неосложнённом течении) обычно не проводится. В отдельных случаях могут использоваться:
- Развёрнутый клинический анализ крови. При этом может обнаружиться лейкопения ( снижение количества лейкоцитов) и нормоцитоз ( нормальный размер эритроцитов) , лимфо- и моноцитоз ( увеличение числа лимфоцитов и моноцитов) , при наслоении бактериальных осложнений — нейрофильный лейкоцитоз со сдвигом влево (увеличение количество нейтрофилов и появление их незрелых форм );
- Общеклинический анализ мочи (изменения малоинформативны, указывают на степень интоксикации).
- Биохимические анализы крови. Может выявляться С-реактивный белок (указывает на наличие инфекции). При некоторых системных возбудителях, например аденовирусной инфекции, характерно повышение АЛТ.
- Серологические реакции. Возможна ретроспективная диагностика методами РСК, РА, ИФА, однако она редко используется в практической деятельности. В настоящее время широко применяется ПЦР-диагностика мазков-отпечатков, но её применение ограничено в основном стационарами и научно-исследовательскими группами.
При подозрении на развитие осложнений проводят соответствующие лабораторные и инструментальные исследования (рентген придаточных пазух носа, органов грудной клетки, КТ и др.) [3] [5] .
Лечение острых респираторных заболеваний (ОРЗ)
ОРЗ встречается очень часто и в большинстве случаев протекает в лёгкой и средней степени тяжести, поэтому обычно больные проходят лечение дома. При тяжёлых формах (с риском развития или развившимися осложнениями) пациенты должны проходить терапию в условиях инфекционного стационара до нормализации процесса и появления тенденций к выздоровлению. В домашних условиях лечением ОРЗ занимается терапевт или педиатр (в некоторых случаях инфекционист).
Пища должна быть разнообразной, механически и химически щадящей, богатой витаминами, рекомендуются мясные нежирные бульоны (идеально подходит негустой куриный бульон и т. п.), обильное питьё до — 3 л/сут. (тёплая кипячёная вода, чай, морсы). Хороший эффект оказывает тёплое молоко с мёдом, чай с малиной, отвар брусничных листьев.
Медикаментозная терапия ОРЗ включает в себя этиотропную (т. е. воздействующую на возбудителя заболевания), патогенетическую (дезинтоксикация) и симптоматическую (уменьшение беспокоящих симптомов) терапию.
Этиотропная терапия имеет смысл лишь при назначении в раннем периоде и лишь при ограниченном спектре возбудителей (в основном при гриппе). Использование средств отечественной фарминдустрии ("Арбидол", "Кагоцел", "Изопринозин", "Амиксин", "Полиоксидоний" и т. п.) не обладают никакой доказанной эффективностью и могут иметь эффекта, лишь в качестве плацебо.
В качестве симптоматической терапии могут быть использованы препараты следующих групп:
- жаропонижающие при температуре у взрослых свыше 39,5, у детей — свыше 38,5 ℃ (парацетамол, ибупрофен);
- противовирусные и антибактериальные глазные капли при конъюнктивите;
- сосудосуживающие капли в нос при заложенности носа и насморке (не более 5 дней);
- солесодержащие капли в нос при рините для разжижения слизи;
- противоаллергические препараты при аллергическом компоненте ОРЗ;
- средства противовоспалительного и противомикробного действия местного действия (таблетки, пастилки и др.);
- средства для улучшения образования, разжижения и выделения мокроты (муколитики);
- антибиотики широкого спектра действия (при отсутствии улучшения в течении 4-5 дней, присоединении вторичной бактериальной флоры и развитии осложнений) [2][6] .
Прогноз. Профилактика
Прогноз при ОРЗ — положительный. Больные обычно выздоравливают в течение 5-10 дней без неблагоприятных последствий. Осложнения респираторных заболеваний могут возникнуть при гриппе, другие возбудители менее агрессивны. Также неблагоприятные последствия возможны у пациентов с ослабленным иммунитетом. После выздоровления организмом вырабатывается иммунитет к той инфекции, которой человек переболел .
Ведущую роль в профилактике распространения ОРЗ (исключая грипп) является:
Читайте также:

