Что убивает вирус иммунодефицита
Обновлено: 23.04.2024
Все мы хорошо знаем, что АРВТ достигла больших успехов, она весьма эффективна. Благодаря чему? Благодаря тому, что в клетке, в которой размножается вирус, есть специальные мишени для АРВТ-препаратов. Что это за мишени? Это ферменты вируса, отвечающие за проникновение в клетку, обратную транскрипцию, интеграцию и, наконец, созревание вирусных частиц.
Цель АРВТ — это стабильное снижение вирусной нагрузки. Каждый, кто лечит ВИЧ-инфекцию, хорошо знает, что сначала вирусная нагрузка снижается очень быстро. Практически за несколько недель она теоретически может упасть до неопределяемого уровня. Почему он достигается так быстро? Потому что на первом этапе применения АРВТ основной мишенью для лекарств являются СД4 лимфоциты, которые находятся, как мы понимаем, в кровотоке и легко доступны для препаратов.
Сейчас мы можем констатировать, что кроме уже названного этапа есть еще и второй этап снижения нагрузки. Этот этап связан с вирусом, попавшим в клетки-макрофаги. Лекарства сюда проникают намного хуже, намного медленнее. Тем не менее продолжение терапии позволяет несколько снизить вирусную нагрузку и в них.
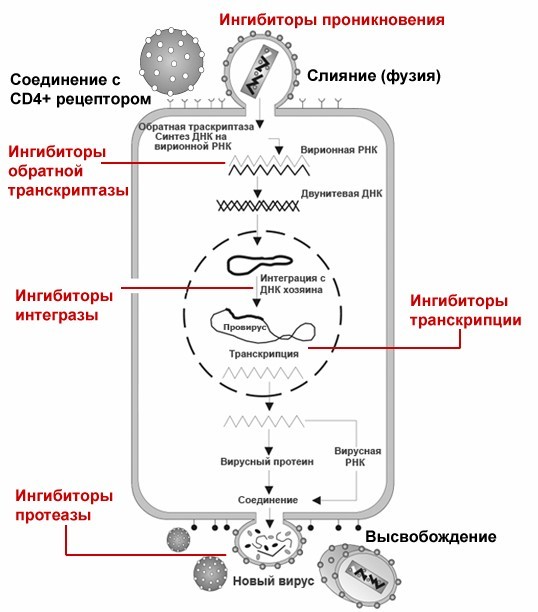
Схема работы антиретровирусной терапии.
Но что происходит с вирусной нагрузкой после того, как она стала неопределяемой? Чтобы ответить на этот вопрос, существуют так называемые ультрачувствительные методы. После того как вирусная нагрузка наконец выходит на плато, мы видим лишь единичные копии РНК вируса, но снизить ее еще больше уже не представляется возможным.
На заре такого рода исследований первой мыслью, которая пришла в голову ученым, было увеличить интенсивность терапии, чтобы достичь полного уничтожения вирусных частиц в организме. Для этого были испробованы несколько вариантов, которые были связаны с повышением дозировок, с увеличением количества препаратов в схеме, с применением новых препаратов. Но ни один из перечисленных инструментов не привел к желаемым результатам. Это, очевидно, указывало на то, что размножение вируса не является главным источником остаточной виремии. Так, к настоящему времени сформировалось представление о так называемых резервуарах ВИЧ.
Спящие хелперы
по теме
Лечение
Как устроены ВИЧ и АРВТ? Объясняем на пальцах
Резервуары бывают двух видов: анатомические и клеточные. Анатомические резервуары — это такие зоны организма, куда не проникает либо плохо проникает лекарство. Таких зон в организме немало. Прежде всего, это центральная нервная система, лимфоузлы, это ЖКТ и костный мозг.
Главный клеточный резервуар — так называемые латентно-инфицированные клетки. Дело в том, что почти все клетки-мишени вируса, в первую очередь хелперные клетки, в определенный момент своей жизни, чтобы выполнить свою функцию, приходят в состояние активации, а после того, как они ее выполнили, дают себе команду апоптоза и погибают.
Клетки памяти сохраняют способность к делению. И делятся простым митозом. Часть из них погибает, но другие могут реактивироваться. Состояние их реактивации достигается разными способами. Иногда это химическое воздействие, иногда физическое, иногда какая-то дополнительная инфекция, которая оказывается в организме.
Т-хелпер
Как только латентно инфицированная клетка оказывается реактивирована, она начинает производить новые вирусные частицы. Что и дает ту самую остаточную виремию, о которой мы говорили выше.
Что делать с этим? Существуют две стратегии излечения. Одна из них называется стерилизующей терапией, или радикацией. Другая — функциональное излечение. Радикация — это полное уничтожение всех резервуаров в организме таким образом, чтобы в нем не осталось ни одной молекулы РНК и ни одной молекулы ДНК вируса.
Функциональное излечение предполагает, что вирус в организме остается в очень небольшом количестве, но при этом излечивающее воздействие приводит к тому, что последующая терапия такому пациенту больше не требуется.
Два пути
Первый случай радикации, о котором мы все уже слышали, — это, конечно, так называемый Берлинский пациент.
Для того, чтобы вирусу присоединиться к клетке, ему нужны два рецептора: один СД4, а другой CCR5. Полноценный CCR5 рецептор кодирует ген CCR5 дикого типа. Но бывает, что в составе этого гена встречается делеция, то есть потеря части хромосомы. Она называется дельта32. В этом случае у человека формируется неполноценный рецептор, а вирус не может присоединиться к клетке-мишени.
Люди с такой мутацией встречаются, и если эта мутация у них в гомозиготе, то они полностью защищены от инфицирования ВИЧ — за редкими исключениями.
Берлинскому пациенту, который был гетерозиготен по дельта32, в результате острого миелогенного лейкоза пришлось сделать полное облучение организма и химиотерапию. АРВТ временно пришлось отменить. После переливания стволовых клеток дельта32 двенадцать лет назад в его организме не удалось встретить ни РНК, ни ДНК вируса.
Так человечество столкнулась с первым случаем полного излечения от ВИЧ-инфекции.
Макрофаг
Уже в этом году, летом, мы услышали еще о двух таких пациентах. У них ситуация была попроще. Лимфома Ходжкина. Лечение было менее тяжелым, им не делали полного облучения, да и химиотерапия была не такая тяжелая. Однократно каждому из них перелили стволовые клетки. В итоге: Лондонский пациент находится в ремиссии уже более двух лет, а Дюссельдорфский — приближается к году.
Считается, что это тоже случаи полного излечения. Но для всех пациентов такая терапия не подойдет. Несмотря на то, что инициатива продолжается и существует целая программа, которая собирает коллекцию стволовых клеток дельта32. На данный момент собрана коллекция потенциальных доноров: около 40 тысяч человек. Безусловно, не всем удастся подобрать донора.
Модификация этого подхода — генная терапия, которая предполагает, что можно взять клетки у человека, уже инфицированного ВИЧ, и вырезать ген CCR5, получив клетки, аналогичные стволовым клеткам дельта32.
В целом, теоретически, это вполне возможно сделать. Такие технологии недавно были использованы на мышах. Более того, в этом году подобную геннотерапевтическую манипуляцию, хоть эксперимент и был воспринят научным сообществом неоднозначно, провели на человеческих эмбрионах. Это знаменитые китайские близнецы.
Впрочем, тут же, появилось несколько публикаций о том, что отсутствие гена CCR5 не совсем безразлично для организма, и люди, у которых такой рецептор отсутствует, подвержены многим другим рискам.
по теме

Лечение
Здесь речь идет о реактивации латентных клеток, чтобы сделать их доступными для АРВТ. На первый взгляд, идея очень хорошая, но на пути этой стратегии уже встретилось немало трудностей. Хотя в некоторых экспериментах объем резервуаров все-таки удавалось снизить, вирусная нагрузка остаточной виремии у пациентов сохранилась. То есть уничтожить вирус в организме врачам так и не удалось.
Основная проблема связана с тем, что резервуары неоднородны. Все клетки в организме, которые имеют на своей поверхности соответствующие рецепторы, могут быть инфицированы. Но они все разные. И разработать препарат, который одинаково работал бы со всеми ними, ученым еще не удалось.
Лабиринт из тупиков
Как этого добиться? На эту тему сейчас проходят исследования. Некоторые из них касаются ограничения процесса инициации транскрипций, в котором принимает участие белок, носящий название Tat. Это самый главный вирусный трансактиватор транскрипций. А также клеточные белки, которые связаны с этим же этапом.
Некоторые связаны с идеей блокирования окружения провирусной ДНК и изменением структуры хроматина. Новые препараты, работающие по этой технологии, так называемые ингибиторы фактора LEDGF/p75, скоро будут апробированы в клинике.
Итак, проблема полного излечения ВИЧ волнует сейчас очень многих ученых, но мы находимся в начале этого сложного лабиринта, который рано или поздно приведет нас к искомой цели.
В каком состоянии находится проблема на данный момент в целом? В этом лабиринте, как вы понимаете, много тупиков. И некоторые из этих тупиков уже пройдены, а это тоже очень важно. Важно понимать, куда ходить не стоит, потому что по мере того, как ошибочные решения будут исключаться, мы, наверное, найдем правильный ответ и придем к искомой цели.
Лично мне кажется, что сейчас настает очень интересный момент. Накопление новых данных идет с огромной скоростью. Во всем мире еженедельно публикуется множество исследований и многие выглядят очень и очень перспективно. А стало быть, в ближайшие несколько лет нам можно ожидать прорыва.
В середине 1980-х ученые идентифицировали вирус иммунодефицита человека и сразу же стали искать лекарство. История антиретровирусной терапии началась в 1987 году, когда для лечения ВИЧ-инфекции стали использовать препарат зидовудин. Но его эффективность была невысокой, а побочные эффекты слишком сильными. Первая высокоэффективная терапия появилась только через десять лет — в 1996 году. Эта комбинация из нескольких лекарств блокирует размножение попавшего в организм вируса сразу на нескольких этапах его цикла. С тех пор ВИЧ-инфекция — не смертельное, а хроническое заболевание, которое можно контролировать при должном лечении.
Антиретровирусные препараты (АРВ) подавляют размножение ВИЧ, но неспособны полностью удалить вирус из организма, именно поэтому их нужно принимать постоянно в течение всей жизни. Как только концентрация препарата в крови падает ниже порогового значения, вирус снова начинает размножаться. Это особенно опасно, ведь если вирус размножается в присутствии небольшого количества лекарства, то он вырабатывает устойчивость к этому препарату.
Пить таблетки на протяжении всей жизни с точностью до минут — не самая простая задача. Этому мешают и банальная забывчивость, и разные случайные обстоятельства. А чем чаще человек нарушает время приема терапии, тем выше риск развития у вируса устойчивости. Именно поэтому врачи стараются назначать схемы с приемом лекарств один раз в день и с минимальным числом таблеток — чем реже и меньше нужно принимать лекарств, тем проще соблюдать режим. Правильное соблюдение режима приема терапии называют высокой приверженностью лечению.
Сейчас лучшими схемами считаются те, при которых пациенту нужно принимать одну таблетку один раз в день, да еще и независимо от приема пищи. Но настоящим прорывом в АРВТ станет разработка схем, при которых лекарство достаточно будет принимать всего один или несколько раз в месяц, — пролонгированных схем терапии. Хотя в настоящее время неизвестно, как поведут себя пролонгированные режимы в рутинной практике. Будет ли к ним сохраняться высокая приверженность — как это показывают исследования?
по теме

Общество
Грудное молоко VS смеси при ВИЧ: что говорят эксперты в 2020 году?
Основной недостаток таких таблеток — срок их действия ограничено временем нахождения таблетки в кишечнике и не превышает 12—24 часов. В случае же диареи таблетка может покинуть организм гораздо быстрее, а значит, уменьшится концентрация лекарства в крови, что может быть опасно. Для антиретровирусных препаратов создание таблеток или капсул с замедленным высвобождением лекарственного вещества не очень перспективно — современные схемы уже позволяют принимать терапию один раз в день. То есть удобство применения терапии такие таблетки не повысят.
Если нужно добиться продления эффекта препарата на дни и недели, а лекарство всасываться через кожу упорно не хочет, приходится прибегать к парентеральным пролонгированным формам. Можно зашить под кожу специальную стерильную таблетку, которая будет медленно растворяться и выделять лекарственное вещество: на коже делается небольшой разрез, в него вводят таблетку и зашивают рану.
Помимо таблеток, под кожу можно вводить специальные полимерные импланты, содержащие нужное лекарство. Преимущество имплантов — они могут выделять лекарственное вещество очень долго, до нескольких лет. Чаще всего такие импланты используют для гормональной контрацепции. Так как гормоны действуют в очень маленьких дозах, даже в небольшой по размерам имплант можно сразу поместить запас препарата на несколько лет. Например, противозачаточный препарат Имплантон, который вводится под кожу, продолжает действовать три года. Если действие препарата нужно прекратить — достаточно просто извлечь имплант.
Более простой вариант — ввести в мышцу взвесь маленьких крупинок лекарства в подходящем растворителе. Выглядит это как обычный укол, при этом крупинки лекарства задерживаются в мышце, медленно растворяются и попадают в кровь. Такие способы введения лекарства особенно удобны в случаях, когда пациент может часто пропускать прием препарата, или забывать, принял ли он лекарство. Например, в случае лечения психических заболеваний. Но есть и недостатки: вводить такой препарат должен медицинский работник, а в случае непереносимости или выраженных побочных эффектов лекарство очень трудно быстро удалить из организма.
Что уже доступно на рынке?
Многие фармацевтические компании проводят исследования пролонгированных АРВ-препаратов, но разработка одного такого препарата сама по себе очень большой пользы не принесет — ведь для лечения ВИЧ-инфекции необходимо сочетание нескольких препаратов, то есть нужна комбинированная пролонгированная схема.
Такую схему, разработанную ViiV Healthcare совместно с Janssen, одобрили в марте 2020 года в Канаде — первый пролонгированный комбинированный АРВ-препарат Cabenuva. Схема показала высокую эффективность и безопасность в клинических исследованиях LATTE-2, FLAIR, ATLAS с участием более тысячи пациентов. В состав Cabenuva входят каботегравир и рилпивирин, то есть это двухкомпонентная схема. Препарат вводят один раз в месяц внутримышечно.
Перед началом применения Cabenuva пациент не менее месяца принимает каботегравир в таблетках (называется Vocabria) в комбинации с Эдюрантом — таблетками рилпивирина. Это необходимо, чтобы проверить переносимость такой схемы у конкретного пациента и оценить побочные эффекты. Если схема переносится хорошо, пациенту вводят первую нагрузочную дозу Cabenuva — 3 миллилитра суспензии, содержащей 600 миллиграммов каботегравира, и 3 миллилитра суспензии, содержащей 900 миллиграммов рилпивирина. Суспензии вводятся в разные участки ягодичной мышцы, то есть делают два укола. После этого поддерживающие дозы вводят ежемесячно: 2 мл (400 мг) каботегравира и 2 мл (600 мг) рилпивирина. Если по каким-то причинам введение очередной ежемесячной поддерживающей дозы невозможно, пациент до момента следующей инъекции может принимать пероральную схему (Vocabria + Эдюрант). Пролонгированная форма каботегравира также имеет большие перспективы для использования в качестве доконтактной профилактики ВИЧ-инфекции.
Еще один препарат, который уже применяется в клинической практике, — ибализумаб (Трогарзо) — можно назвать пролонгированным с несколькими оговорками. По химической природе ибализумаб — моноклональное антитело, то есть близок к человеческим иммуноглобулинам. Ибализумаб связывается с некоторыми белками на поверхности вируса и мешает проникновению ВИЧ в клетки. Препарат вводят внутривенно один раз в две недели и часто сочетают с другими АРВ-препаратами. Такая схема — не самый удобный вариант, поэтому сейчас ибализумаб используется только для лечения ВИЧ с множественной лекарственной устойчивостью, когда другие схемы оказываются неэффективными. Поэтому ибализумаб правильнее будет отнести к нишевым препаратам.
К сожалению, на этом и заканчивается не очень длинный перечень пролонгированных АРВ-препаратов, которые уже применяются на практике. Дальше пойдет речь о препаратах, находящихся на разных стадиях исследований.
Что сейчас находится в разработке?
PRO 140
С точки зрения места в клинической практике на ибализумаб похоже еще одно моноклональное антитело, находящееся в стадии клинических исследований, — PRO 140. Этот препарат также можно будет использовать для лечения ВИЧ-инфекции, если у пациента не работают другие схемы. А по механизму действия PRO 140 похож на уже существующий на рынке препарат маравирок (Целзентри). Он связывается с CCR-5 рецепторами на поверхности клеток-мишеней и мешает проникновению вируса в клетку. Строение активного центра молекулы PRO 140 отличается от маравирока, поэтому он активен даже в тех случаях, когда вирус выработал устойчивость к маравироку. Как и маравирок, PRO 140 активен только против CCR-5-тропных подтипов ВИЧ, то есть подойдет не всем пациентам. Препарат вводят внутривенно, один раз в неделю.
Нейтрализующие антитела
На разных стадиях клинических исследований находятся несколько перспективных антител, которые связываются с вирусным белком gp120 и нейтрализуют вирус: VRC01, 3BNC117 и 10-1074. Предполагается, что эти препараты достаточно будет вводить раз в месяц или даже реже и их можно будет применять совместно с другими пролонгированными АРВ-препаратами.
Албувиртид
Аналог уже применяющегося на практике энфувиртида (Фузеон). Этот препарат связывается с вирусным белком gp-41 и мешает проникновению вируса в клетку. Основное отличие в том, что Фузеон вводят подкожно два раза в сутки, что очень неудобно, а албувиртид — только один раз в 2—4 недели. Препарат должен применяться совместно с другими АРВ-лекарствами.
Вирусы могут размножаться только внутри клетки-хозяина, перестраивая ее работу так, что клетка начинает производить новые вирусные частицы. Это серьезно нарушает работу самой клетки и в большинстве случаев ведет к ее гибели. Процесс проникновения и размножения вируса в ней сложный и содержит много стадий, а значит, специальные лекарства могут тормозить его на различных этапах.
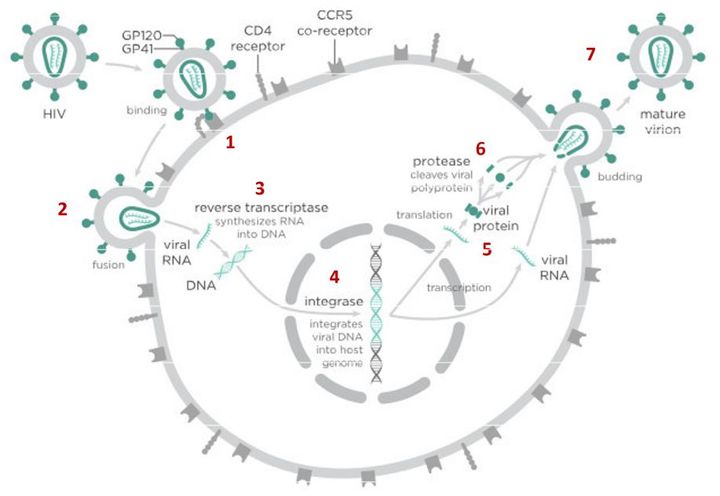
В случае с ВИЧ это выглядит так.
по теме

Лечение
Лучшие научпоп-статьи 2018 года
После того как вирусная частица приклеилась к рецепторам CD4 и CCR5/CXCR4 и закрепилась на поверхности клетки, другой специальный белок вируса gp41 соединяет оболочку вируса с мембраной клетки-мишени и помогает вирусу проникнуть внутрь клетки (цифра 2 на схеме). На этом этапе остановить вирус может другая группа препаратов — ингибиторы слияния, например, энфувиртид. Препарат связывается с вирусным белком gp41 и нарушает его работу.
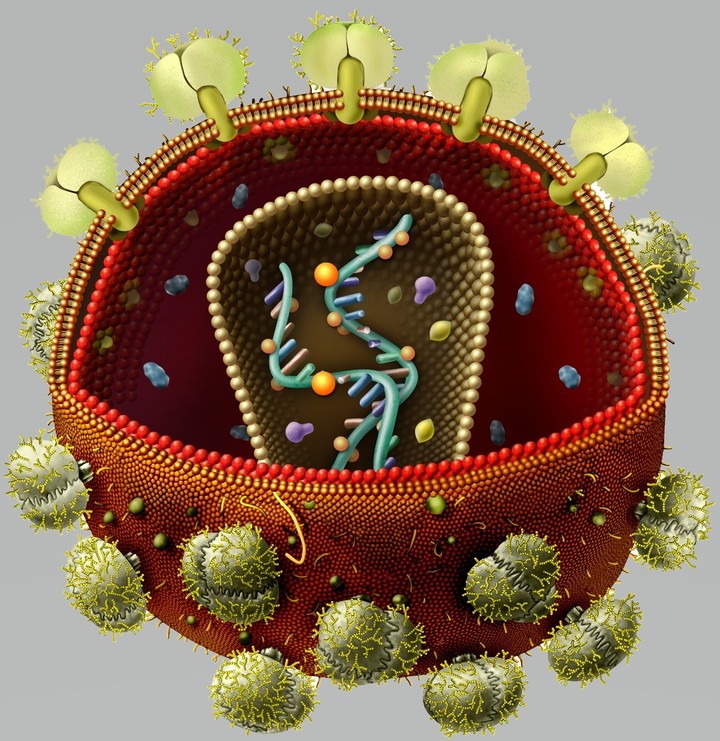
На этом этапе размножение вируса блокирует очень большое количество препаратов из двух классов — нуклеозидные ингибиторы обратной транскриптазы (НИОТ — ламивудин, абакавир, тенофовир) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ — эфавиренз, рилпивирин). Принцип действия у веществ из обеих групп похожий: молекула лекарства связывается с обратной транскриптазой вируса, нарушает ее работу и так блокирует перенос генов вируса из РНК в ДНК. Это не позволяет генам вируса встроиться в ДНК клетки-хозяина и начать производство новых вирусных частиц.
На следующем этапе инфицирования (цифра 4 на схеме) готовая вирусная ДНК проникает в ядро и встраивается в ДНК клетки-хозяина с помощью специального вирусного фермента — интегразы. Работу этого фермента блокируют ингибиторы интегразы, например, долутегравир, не позволяя ДНК вируса встроиться в наши гены.
После того как вирусная ДНК встраивается в ДНК клетки-хозяина, клетка получает неправильную программу и начинает производить вирусные белки и РНК, необходимые для сборки новых частиц вируса (цифра 5 на схеме), используя для этого структуры, которые в норме производят собственные белки клетки. Такая перенастройка производства белка сильно нарушает работу клетки и через некоторое время вызывает ее гибель. Лекарств, которые бы влияли на этот этап размножения вируса, нет, так как здесь вирус использует собственные ферментные системы клетки-хозяина и блокирование их работы какими-то веществами навредит здоровым клеткам.
по теме

Лечение
Ошибка системы. Почему в регионах опять не хватает таблеток от ВИЧ
После синтеза вирусных белков клеткой-хозяином в работу вступает еще один фермент вируса — протеаза (цифра 6 на схеме). Дело в том, что белки ВИЧ синтезируются в виде длинных цепочек белков-предшественников, но они неактивные. Протеаза разрезает эти цепочки на более короткие фрагменты, которые становятся активными белками вируса: из одних собирается вирусная оболочка, другие выполняют функции ферментов (обратная транскриптаза, интеграза, протеаза, о которых мы говорили выше). Класс лекарств, нарушающих работу вирусной протеазы, включает большое количество препаратов от достаточно старого лопинавира до современного дарунавира. Основной недостаток препаратов этого класса — высокая степень перекрестной устойчивости: если вирус приобретает устойчивость к одному препарату, скорее всего, на него не подействует ни один другой препарат из этого класса.
На последнем этапе (цифра 7 на схеме) вирусные частицы собираются из готовых компонентов (синтезированных клеткой вирусных белков и РНК), как конструктор, и покидают клетку-хозяина. Лекарств, которые бы тормозили эти процессы, пока не существует.
ВИЧ имеет высокую склонность к мутациям, что позволяет ему быстро приобретать устойчивость к лекарствам. Мутации изменяют форму молекул ферментов вируса. Если при этом форма изменится существенно, то фермент не сможет нормально работать и такой вирус размножаться перестанет — это вредная для вируса мутация. Однако в некоторых случаях — при полезных мутациях — форма молекулы фермента меняется не сильно, а так, что сам фермент продолжает нормально работать, но молекула лекарства уже не может с ним связаться.
Поэтому для эффективного подавления размножения ВИЧ обычно назначают три разных препарата из разных групп, влияющих на разные ферменты вируса, блокируя его воспроизводство на разных этапах. Исключением является группа ингибиторов обратной транскриптазы (НИОТ и ННИОТ) — эти лекарства связываются с разными участками молекулы вирусного фермента, поэтому могут назначаться вместе, несмотря на то, что относятся к одной группе. В условиях такой терапии вирусу очень трудно выработать устойчивость, потому что одновременно должно произойти несколько полезных мутаций в разных генах вируса, а это бывает крайне редко.
Есть несколько перспективных технологий, например, CRISPR/Cas9, которые могут позволить полностью удалить вирусную ДНК из организма человека, но пока ни одна из них не прошла все необходимые исследования для подтверждения эффективности и безопасности. Исследования продолжаются.

Обзор
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
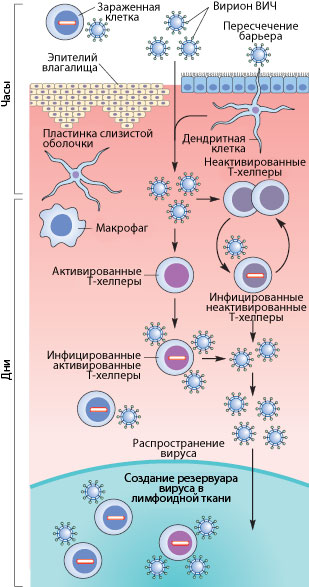
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.




Клиника является первым частным медицинским учреждением России и единственным в Москве и области, успешно прошедшим процедуру сертификации Росздравнадзора (Сертификат №0023/01КБМД от 10.10.2019 г.).
ВИЧ и СПИД – отличия, длительность развития, прогнозы
СПИД – это конечная стадия ВИЧ, которая характеризуется сильно сниженным иммунитетом. Важно не путать два этих понятия. С момента инфицирования ВИЧ болезнь до стадии СПИДа без лечения может развиваться в течение 9-11 лет (в среднем). При постановке диагноза СПИД без лечения продолжительность жизни короткая – в среднем до 19 месяцев.
Если вовремя начать лечение, то на стадии ВИЧ можно прожить очень долгую жизнь – продолжительность жизни таких пациентов благодаря современному лечению составляет 20-50 лет. И хоть при стадии СПИД ситуация гораздо сложнее, но многие пациенты при должном лечении и крепком организме могут прожить более 10 лет.
Очевидно, что прием терапии – важнейший фактор для лечения ВИЧ и полноценной долгой жизни. Более того, именно лечение позволяет значительно снизить вирусную нагрузку и сделать зараженного человека неопасным для партнера, а также членов семьи.
Пути передачи ВИЧ
Основные пути заражения ВИЧ:
- незащищенный секс с зараженным человеком (самый распространенный путь передачи ВИЧ). Заразиться можно как после однократного контакта, так и после нескольких;
- использование иглы для введения наркотиков после зараженного человека. Либо другие варианты ситуаций, при которых происходит контакт крови здорового человека с кровью зараженного;
- передача от матери к плоду во время родов или от матери ребенку во время вскармливания. Важная ремарка: если женщина лечится и находится под контролем врачей, у нее есть все шансы родить здорового малыша;
- переливание инфицированной крови. В современных клиниках и больницах это уже исключено, поскольку все материалы проходят очень серьезную проверку.
Также выделяют так называемые группы риска – это люди, которые больше других подвержены заражению ВИЧ:
- люди, ведущие беспорядочную половую жизнь;
- гомосексуалисты;
- наркоманы, которые колют инъекции;
- люди с партнером, зараженным вирусом.
Такие люди должны постоянно сдавать анализ. В ряде случаев им рекомендованы профилактические препараты (только по рекомендации врача).
Говоря о том, как можно заразиться ВИЧ, следует уточнить, в каких случаях это невозможно:
- во время бытовых контактов;
- при использовании посуды инфицированного;
- при укусе насекомого;
- при поцелуе.
Контакт с ВИЧ-зараженным на бытовом уровне (в семье, на работе, в другом формате общения) абсолютно безопасен и не несет никакой угрозы для окружающих.
Основные стадии заболевания

Стадии ВИЧ делятся на следующие:
- инкубационная. Это стадия, на которой происходит заражение и последующее размножение вируса в крови. Она длится до шести недель, иногда меньше. Даже будучи зараженным, на этом этапе человек не увидит явных признаков, а анализ крови не покажет, что в крови есть антитела;
- первичная. Здесь уже могут появиться первые признаки инфекции. Длится вторая стадия в течение 3 недель – в это время появляются антитела, вирус определяется лабораторно;
- субклиническая. Появляется первый признак болезни – увеличенные лимфоузлы. Ппациент чувствует себя полностью здоровым, на самочувствие не жалуется;
- появление вторичных заболеваний. Иммунитет начинает давать сбои, из-за чего проявляются самые разные болезни: от частых простуд и кандидоза до пневмоний, туберкулеза;
- терминальная. Стадия предполагает истощение (довольно быстрое и прогрессирующее), а также последующую смерть больного.
Стадии не имеют единственно верных временных рамок – они могут отличаться у разных людей. Например, часто ВИЧ-инфицированные годами чувствуют себя хорошо или не обращают внимание на небольшие признаки. Болезнь обнаруживается только на стадии сильного ухудшениям самочувствия или благодаря случайным анализам.
Симптомы ВИЧ
Выяснив, как передается ВИЧ, нужно разобраться с симптомами. Проблема в том, что эти симптомы проявляются на ранней стадии, затем пропадают и долгое время больше не беспокоят человека – буквально годами. А еще они очень похожи на проявления других болезней, что может вводить в заблуждение.
Так, на первом этапе, когда вирус себя проявил, человек может чувствовать:
- боль в горле, повышение температуры;
- болезненность кожи, суставов, костей4
- озноб, лихорадку.
Одновременно с этим увеличиваются шейные лимфоузлы, могут проявиться разные высыпания. Все это часто принимается за признаки ОРВИ или других подобных болезней.
Новые симптомы ВИЧ возвращаются через несколько лет спокойной и здоровой жизни. К ним относятся:
- сильная усталость, быстрая утомляемость;
- увеличение лимфоузлов – не только шейных, а уже нескольких групп;
- снижение веса. Обычно оно выглядит беспричинным, человек не понимает, в чем дело;
- лихорадка, озноб, потливость (преимущественно ночная);
- проблемы с ЖКТ – обычно проявляются жидким стулом без видимых на то причин.
На этом этапе, как правило, и обнаруживается заболевание – потому что пациент обращается к врачу, а специалист назначает дополнительное обследование.
Как диагностируют ВИЧ в Москве
Для диагностики вируса есть два теста: предварительный ИФА и максимально точный иммуноблот. Точность ИФА составляет около 90%. Его рекомендуют проводить через 3-6 месяцев после контакта с вирусом, тогда он дает максимальную точность. Обычный тест ИФА основан на анализе крови, есть также экспресс-тесты, которые помогают получить информацию на основе мочи или слюны. Такие тексты покупают исключительно в аптеке (ни в коем случае не в интернете!), поскольку необходимо использовать официально утвержденные изделия.
Важно: тест не показывает, как передается ВИЧ в конкретной ситуации – то есть определить путь заражения можно только путем анализа собственных действий.
Лечение ВИЧ
Лечение сводится к назначению антиретровирусной терапии. Пациенту составляют схему приема препаратов – и ее нужно соблюдать максимально точно, не отклоняясь от программы. В противном случае вирус может выработать устойчивость к лечению и не поддаваться дальнейшему подавлению.
Показателями качественного лечения являются снижение вирусной нагрузки, а также увеличение в крови клеток CD4+, которое говорит об активности иммунитета.
Лекарства для лечения выдаются в медицинских учреждениях, пациенты ставятся на учет и получают препараты бесплатно, в установленном порядке. Информация о заболевании является конфиденциальной – она не направляется на работу, место учебы или в другие места. Пациент имеет право оставить ее втайне (если это не предусмотрено отдельными рабочими договорами).
При соблюдении правил приема терапии вирус в крови постепенно снижается, со временем пациент становится полностью безопасным для своего полового партнера и не способен никого заразить.
Профилактика ВИЧ-инфекции
Первое и главное правило – регулярно проверяться на ВИЧ даже в том случае, если вы не имели подозрительных контактов. Рекомендуется обследоваться раз в полгода – тем более для этого есть удобные экспресс-тесты.
Внимательно нужно относиться и к выбору партнеров. Не стоит верить на слово человеку, который говорит, что он точно не болеет – лучше попросить результаты исследования и самостоятельно убедиться, что ему можно доверять. Но помните, что в течение полугода даже зараженная кровь может не давать положительных результатов.
Профилактика ВИЧ заключается в следующих моментах:
- защищенный секс с непостоянными половыми партнерами, а также постоянными, если нет уверенности в том, что партнер не болен или хранит верность;
- исключение из жизни наркотиков, беспорядочных половых связей;
- соблюдение общей гигиены. Не стоит делиться бритвой, зубной щеткой, кусачками для ногтей и другими предметами, которые могут контактировать с маленькими ранками.
Главная профилактика заключается в том, чтобы знать об инфекции и всегда помнить об опасности заражения.
Популярные вопросы-ответы про ВИЧ
Как проявляется ВИЧ у мужчин и женщин?
Симптомы ВИЧ у женщин ровно такие же, как и симптомы ВИЧ у мужчин. Проявления могут отличаться только на уровне заболеваний мочеполовой сферы, когда организм уже сильно ослаблен – например, у женщин чаще проявляется молочница. В остальном специфических признаков по полу не наблюдается.
Лечится ли ВИЧ?
Технически можно сказать, что ВИЧ не лечится – пациентам постоянно показана специальная терапия. Но те результаты, которых она позволяет добиться, делают из пациента здорового человека, который может спокойно прожить десятки лет без особых проблем – нужно только постоянно принимать препараты и следить за здоровьем.
ВИЧ давно не является смертельным заболеванием!
ВИЧ – это болезнь наркоманов и людей с беспорядочным образом жизни?
Кто такие ВИЧ-диссиденты?
Это люди, которые вопреки научным данным и здравому смыслу отрицают существование вируса. Они отказываются от лечения, что неминуемо ведет к ранней смерти. Такие люди опасны и тем, что из-за отсутствия лечения распространяют вирус среди своих половых партнеров, не предупреждая их о возможной опасности (поскольку не считают, что она есть).
Успех лечения ВИЧ и долгой жизни заключается в том, чтобы как можно раньше обратиться за помощью и начать терапию. В этом случае человека ждет долгая жизнь без страхов и сложностей.
Читайте также:

