Цирроз печени у вич инфицированных
Обновлено: 19.04.2024
Актуальность. На протяжении последних десятилетий частота встречаемости цирроза печени остается стабильно высокой и составляет 30% от общего числа больных с хроническими диффузными заболеваниями печени, находящихся на лечении в специализированных стационарах. У 50%-85% больных цирроз печени осложняется портальной гипертензией, проявлением которой служит варикозное расширение вен (ВРВ) пищевода и кардиального отдела желудка. Кровотечение из ВРВ возникает у каждого четвертого пациента, достигая 50-70% летальности уже при первом эпизоде.
Цель исследования. Улучшить результаты лечения больных циррозом печени с угрозой развития кровотечения из ВРВ пищевода и кардиального отдела желудка путем внедрения в клиническую практику дифференцированного комплексного подхода к выбору метода хирургического лечения.
Материал и методы исследования. Исследование основано на анализе результатов обследования и лечения 70 пациентов в возрасте от 17 до 68 лет, госпитализированных с диагнозом цирроз печени, осложненный угрозой развития кровотечения из ВРВ пищевода и кардиального отдела желудка. Среди пациентов было 43 женщины и 27 мужчин. Средний возраст больных составил 51 ± 3,4 года. Среди ведущих этиологических факторов цирроза печени были определены вирусные гепатиты В и С и алкогольное поражение печени. В качестве основных критериев угрозы развития кровотечения из варикозных вен пищевода и кардиального отдела желудка рассматривали: размер варикозных вен, их напряжение, истончение стенки, наличие признаков васкулопатии. У большинства пациентов выявлена третья степень ВРВ пищевода и кардиального отдела желудка.
На I этапе при формировании групп больных критериями включения в исследование были:
- наличие цирроза печени;
- наличие у больного угрозы развития кровотечения из ВРВ пищевода и кардиального отдела желудка по данным эзофагогастроскопии;
- согласие пациента на исследование.
Критериями исключения из исследования были:
- печеночная энцефалопатия II-IV стадии;
- гепаторенальный синдром;
- беременность, период лактации.
На II клиническом этапе собрали жалобы, анамнез пациентов, определяли степень тяжести цирроза печени по Child-Pugh, проводили лабораторные и инструментальные методы исследования.
На III этапе в зависимости от вида оперативного вмешательства пациенты были разделены на 4 группы. В первой группе (10 пациентов) наложен портокавальный анастомоз, в частности дистальный спленоренальный анастомоз (ДСРА). Во второй группе (20 пациентов) выполнена операция М. Д. Пациоры или ее сочетание с деваскуляризацией желудка. В третьей группе (20 пациентов) проведено внутрипеченочное портокавальное шунтирование методом туннелирования печени по Ю. М. Ишенину. В четвертой группе (20 пациентов) выполнено эндоскопическое лигирование ВРВ пищевода и кардиального отдела желудка.
Заключительный этап исследования включал: диспансерное наблюдение, статистическую обработку, анализ результатов и формирование выводов.
С целью изучения эффективности включения в состав комплексной консервативной терапии препарата Ремаксол сформирована группа из 40 пациентов.
Дополнительным критерием включения в это исследование было повышение уровня трансаминаз и гамма-ГТП в 1,5 раза и более от нормы.
Дополнительными критериями исключения для этих пациентов из исследования считали: отказ пациента от участия в ходе исследовании; нарушение протокола исследования; нефролитиаз, подагра, гиперурикемия; появление у пациентов аллергических реакций на препарат.
С целью определения критериев отбора больных для оперативного лечения, а также прогнозирования течения послеоперационного периода осуществлен анализ выживаемости пациентов.
Результаты. Достоверно установлено, что общая продолжительность жизни больных в значительной мере определялась функциональным состоянием печени. Максимальные сроки выживаемости пациентов установлены для класса А, минимальные для класса С.
Среди биохимических критериев, определяющих выживаемость пациентов, достоверно определены два критерия - уровень аланинаминотрансферазы и аспартатаминотрансферазы в пределах нормы. Проведен анализ влияния показателей допплерографии на выживаемость пациентов. Установлено, что в I группе пациентов в раннем послеоперационном периоде в 4 случаях выявлены неудовлетворительные результаты в виду развития печеночной энцефалопатии и острой печеночной недостаточности. При этом, уровень исходного объемного кровотока в воротной вене составил 579±23,2 мл/мин. У других 11 пациентов I группы показатель исходного объемного кровотока был на уровне 871± 43,3 мл/мин, при этом осложнений в раннем послеоперационном периоде не было, а в отдаленном периоде были как удовлетворительные, так и неудовлетворительные результаты.
На основании полученных данных составлен алгоритм дифференцированного подхода к выбору метода хирургической профилактики кровотечений, базирующийся на определении степени тяжести цирроза печени, сонографическом исследовании объемного кровотока в воротной вене и показателей цитолиза.
Влияние уровня общего белка, щелочной фосфатазы, гамма-ГТП и креатинина на выживаемость обнаружено не было.
Эндоскопическое лигирование ВРВ пищевода и кардиального отдела желудка является методом выбора для профилактики кровотечений из ВРВ на фоне цирроза печени.
В послеоперационном периоде наименее выраженные симптомы астенического синдрома выявлены у больных IV группы. Это связано с малой травматичностью и хорошей переносимостью пациентами эндоскопического лигирования.
При сравнительном анализе исходных биохимических показателей и показателей в раннем послеоперационном периоде у пациентов I группы выявлено значимое повышение уровня общего билирубина, трансаминаз, щелочной фосфатазы и ГГТП.
Во II группе данная тенденция затронула показатели аспартатаминотрансферазы и щелочной фосфатазы, в III группе - только аспартатаминотрансферазы.
В IV группе достоверных изменений биохимических показателей не было.
На основании данных сонографии в I группе пациентов установлен регресс диаметра воротной вены. Однако объемный кровоток в воротной вене достоверно снизился и лишь в 66% зафиксирован гепатопетальный кровоток.
В III группе достоверного уменьшения диаметра воротной вены не произошло, однако объемный кровоток в воротной вене возрос и у всех пациентов установлен гепатопетальный кровоток. Отдаленный период пациентов III группы в 40% сопровождался сужением внутрипеченочных туннелей, что способствовало расширению диаметра воротной вены вновь и снижению объемного кровотока в ней.
Отдаленный период у пациентов I группы сопровождался исчезновением 3 степени ВРВ пищевода, при этом появились пациенты с 1 степенью ВРВ пищевода или их исчезновением.
Отдаленный период после операции М. Д. Пациоры сопровождался медленным темпом регресса ВРВ пищевода, т.к. в 62% наблюдений обнаружена вновь 3 степень варикоза с признаками угрозы кровотечения.
В дальнейшем было проведено экспериментальное исследование на 10 трупах больных циррозом печени, умерших от кровотечения из варикозных вен пищевода. При этом исследована эффективность дополнения операции М. Д. Пациоры деваскуляризацией желудка с обязательным лигированием левой желудочной вены, левой желудочной артерии, коротких вен желудка, правой и левой желудочно-сальниковых вен. В результате эксперимента по данным хромоангиографии воротной вены ВРВ пищевода были спавшиеся, без признаков красителя, что свидетельствовало об эффективном разобщении портоазигального венозного бассейна.
Отдаленный период пациентов с выполненной операций М. Д. Пациоры в сочетании с деваскуляризацией желудка сопровождался появлением группы пациентов с отсутствием варикозных вен и 1 степенью их расширения.
В III группе в отдаленном периоде преобладали пациенты с 1 степенью ВРВ, при этом обнаружено уменьшение частоты встречаемости 3 степени варикозного расширения вен до 19%.
В отдаленном периоде в IV группе также преобладали пациенты с 1 степенью ВРВП, появилась вновь сформированная группа пациентов с отсутствием варикозных вен и снизилась частота встречаемости 3 степени до 10%.
Рецидив кровотечений из ВРВ пищевода в ранние сроки был выявлен только в III группе.
В отдаленном периоде минимальное количество рецидивов кровотечений из вен пищевода было в IV группе.
В ранние сроки максимальная летальность была в III группе в связи с развитием внутрибрюшного кровотечения и рецидивом кровотечения из варикозных вен пищевода.
В отдаленные сроки летальность во II и IV группах была связана только с прогрессирование печеночно-клеточной недостаточности.
В I группе все летальные исходы были связаны с рецидивами кровотечения из ВРВ пищевода, в III группе один случай связан также с рецидивированием кровотечения, два случая - с прогрессированием печеночно-клеточной недостаточности.
Больные циррозом печени, перенесшие различные виды хирургической профилактики кровотечений из ВРВ пищевода и кардиального отдела желудка, нуждаются в диспансерном наблюдении. Более высокие показатели качества жизни установлены у пациентов после эндоскопического лигирования варикозно расширенных вен пищевода
В первый месяц частота развития кровотечений составила - 11%, через 3 месяца - 33%.
Анализ качества жизни пациентов показал, что в группе пациентов, где диспансерное наблюдение, включающее контроль за течением основного заболевания и его осложнениями, проводилось через 1, 3, 6 и 12 мес. после операции, показатели всех шкал были достоверно выше, чем в группе пациентов с двухкратным в течение первого года диспансерным наблюдением.
В предоперационном периоде во всех группах пациентов выявлены значительно сниженные показатели всех шкал по сравнению с показателями в общей популяцией.
В отдаленном периоде в IV группе пациентов по большинству шкал установлены максимальные значения показателей, что свидетельствует о более высоком качестве жизни. Достоверные отличия выявлены по интегральному показателю физического компонента здоровья.
При сравнительном мониторинге клинической симптоматики пациентов основной группы и группы сравнения, к 8 суткам терапии выявлено значимое снижение частоты распространения астенического и диспепсического синдромов в обеих группах. Однако при межгрупповом сравнении данных более низкая частота распространения этих синдромов обнаружена у пациентов основной группы.
При исследовании когнитивных функций исходный низкий средний балл зафиксирован в обеих группах.
К 8 суткам терапии в основное группе выявлено достоверное повышение уровня среднего балла на 27%, в группе сравнения - на 14%.
При сравнительном анализе динамики биохимических показателей крови установлено снижение уровня трансаминаз и гамма-ГТП в обеих группах, однако более выраженное и значимое снижение уровня данных показателей выявлено в основной группе пациентов.
Выводы
1. Для хирургической профилактики кровотечений из варикозно расширенных вен пищевода при циррозе печени целесообразно применять алгоритм дифференцированного подхода, базирующийся на определении степени тяжести цирроза печени по Child-Pugh, показателей синдрома цитолиза и сонографическом исследовании объемного кровотока в воротной вене.
2. Среди способов хирургической профилактики кровотечений из варикозно расширенных вен пищевода при циррозе печени предпочтительнее выполнение портокавального анастомоза. При наличии противопоказаний к наложению портокавальных анастомозов целесообразно применять операцию М. Д. Пациоры в сочетании с деваскуляризацией желудка или внутрипеченочное портокавальное шунтирование.
3. Эндоскопическое лигирование варикозно расширенных вен пищевода при циррозе печени характеризуются малой травматичностью и низким числом рецидивных кровотечений. Его можно использовать как самостоятельный метод лечения варикозно расширенных вен пищевода и кардиального отдела желудка при декомпенсированном циррозе печени или в качестве подготовительного этапа перед портокавальным анастомозом или внутрипеченочным портокавальным шунтированием.
4. Диспансерное наблюдение за больными циррозом печени, перенесшими различные виды хирургической профилактики кровотечений из варикозно расширенных вен пищевода и кардиального отдела желудка, позволяет контролировать течение основного заболевания и своевременно предпринять мероприятия по профилактике его осложнений.
У 73% больных циррозом печени, осложненным портальной гипертензией, продолжительность жизни после хирургических методов профилактики кровотечений из варикозно расширенных вен пищевода напрямую связана со степенью печеночноклеточной недостаточности.
5. Качество жизни больных циррозом печени после эндоскопических вмешательств, направленных на профилактику кровотечений из варикозно расширенных вен пищевода, по физическому компоненту здоровья достоверно выше, чем у пациентов после портокавальных анастомозов, операции М. Д. Пациоры или ее сочетания с деваскуляризацией желудка, внутрипеченочного портокавального шунтирования.
6. Включение в состав комплексного периоперационного лечения Ремаксола у больных циррозом печени, угрожаемых по кровотечению из варикозно расширенных вен пищевода, способствует более раннему купированию астенического и диспепсического синдромов, улучшению когнитивных функций и биохимических маркеров функционального состояния печени.
Наличие хронического гепатита С (ХГС) и ВИЧ-инфекции одновременно ассоциируется со значительной частотой неблагоприятных исходов вследствие развития цирроза и/или первичного рака печени, а также общностью эпидемиологических, социальных и экономических факторов. При сочетании этих инфекций отмечаются более высокий титр вируса гепатита С, выраженное прогрессирование хронического гепатита и высокий риск цирроза печени. При этом цирроз печени развивается быстрее и в 3 раза чаще у ВИЧ-инфицированных, чем у больных моноинфекцией гепатита С.
Цель исследования: выявить клинические и лабораторные особенности больных ХГС и ВИЧ-инфекцией.
Материал и методы: в исследование включены 173 пациента с ХГС и ВИЧ-инфекцией. Стандартную терапию ХГС (пегилированный интерферон альфа-2а + рибавирин) получали 45 больных, антиретровирусную терапию — 29. Чаще определялся генотип 1 вируса гепатита С (91 пациент, 52,6%). ХГС преобладал у пациентов мужского пола (в группе 1 — 64,3%, в группе 2 — 71,1%) и в наиболее трудоспособном возрасте от 20 до 30 лет (в группе 1 — 68,8%, в группе 2 — 80%).
Результаты исследования: среди больных, поступивших в стационар, 55,5% имели смешанную форму гепатита (ХГС + токсический гепатит) и у 17,2% выявлен цирроз печени. У 22,6% больных противовирусная терапия была отменена вследствие развития побочных реакций или неэффективности. Значительное количество пациентов до поступления в стационар злоупотребляли алкоголем (54,7%), наркотиками (25,8%), имели хронические заболевания: панкреатит, бронхит.
Заключение: среди пациентов с ХГС и ВИЧ-инфекцией, поступающих в стационар, преобладают больные со смешанной формой гепатита (ХГС + токсический гепатит). Большинство больных не получают стандартную противовирусную терапию ХГС вследствие выраженного иммунодефицита, злоупотребления алкоголем, приема психотропных веществ или отказа от лечения.
Ключевые слова: ВИЧ-инфекция, хронический гепатит С, цирроз печени, противовирусная терапия, антиретровирусная терапия, интерферон альфа-2а, рибавирин, генотип, оппортунистические инфекции.
Для цитирования: Сундуков А.В., Мельников Л.В., Евдокимов Е.Ю. Характеристика больных хроническим гепатитом С и ВИЧ-инфекцией. РМЖ. Медицинское обозрение. 2018;2(7(II)):64-67.
A.V. Sundukov 1 , L.V. Melnikov 2 , E.Yu. Evdokimov 3
1 Evdokimov Moscow State University of Medicine and Dentistry
2 Penza State University
3 Central Research Institute of Epidemiology, Moscow
The presence of HIV infection together with chronic hepatitis C (CHC) is associated with a significant incidence of an adverse events due to the development of cirrhosis and/or primary liver cancer, as well as a similarity of epidemiological, social and economic factors. In the case of these infections, there is a higher titer of hepatitis C virus, significant progression of chronic hepatitis and a high risk of the liver cirrhosis. At the same time, liver cirrhosis develops faster and 3 times more often in HIV-infected patients than in patients with hepatitis C monoinfection.
Aim: to identify the clinical and laboratory features of patients with CHC and HIV infection.
Patients and Methods: the study included 173 patients with CHC and HIV infection. 45 patients underwent standard therapy (pegylated interferon alfa-2a + ribavirin) of CHC. Antiretroviral therapy was followed by 29 patients. The 1 genotype of the hepatitis C virus was identified more frequently (91 patients, 52.6%). CHC prevailed in male patients (group 1 — 64.3%, group 2 — 71.1%) at the most working age from 20 to 30 years (group 1 — 68.8%, group 2 — 80%).
Results: among the patients admitted to the hospital, 55.5% had a mixed form of hepatitis (CHC + toxic hepatitis) and 17.2% had cirrhosis of the liver. In 22.6% of patients, antiviral therapy was canceled due to the development of adverse events or non-
response to therapy. A significant number of patients before admission to the hospital abused alcohol (54.7%), drugs (25.8%), had chronic diseases: pancreatitis, bronchitis.
Conclusion: patients with mixed hepatitis (CHC + toxic hepatitis) prevail among patients with CHC and HIV infection admitted to hospital. Most patients do not receive standard antiviral therapy for CHC due to pronounced immunodeficiency, alcohol abuse, psychotropic substances intake, or refusal of treatment.
Key words: HIV infection, chronic hepatitis C, liver cirrhosis, antiviral therapy, antiretroviral therapy, interferon alfa-2a, ribavirin, genotype, opportunistic infections.
For citation: Sundukov A.V., Melnikov L.V., Evdokimov E.Yu. Characteristics of patients with chronic hepatitis C and HIV infection // RMJ. Medical Review. 2018. № 7(II). P. 64–67.
В статье приведены характеристика больных хроническим гепатитом С и ВИЧ-инфекцией с целью определения клинических и лабораторных особенностей больных с данными заболеваниями.
Введение
Актуальность проблемы вируса иммунодефицита человека (ВИЧ) и хронического гепатита С (ХГС) определяется широким распространением этих инфекций, многообразием клинических форм, значительной частотой неблагоприятных исходов вследствие развития цирроза и/или первичного рака печени, а также общностью эпидемиологических, социальных и экономических факторов. Эпидемиологическая ситуация в России по ВИЧ и ХГС остается сложной, и в последнее время отмечается увеличение смешанной инфекции (ВИЧ/ХГС). Из 42 млн ныне живущих ВИЧ-инфицированных людей примерно у 20% (8,4 млн) диагностирован ХГС [1–3]. Как правило, у данной категории пациентов в анамнезе отмечают случаи внутривенного введения наркотиков [4].
В настоящее время более 80% всех случаев ВИЧ-инфекции приходится на потребителей инъекционных наркотиков, и в этой группе маркеры вирусного гепатита С определяются более чем у 90% больных [4–7]. Наличие ХГС и ВИЧ-инфекции одновременно ассоциируется с более высоким титром вируса гепатита С, выраженным прогрессированием хронического гепатита и возрастающим риском цирроза печени. При этом цирроз печени развивается быстрее и в 3 раза чаще у ВИЧ-инфицированных, чем у больных моноинфекцией гепатита С [4, 7, 8].
Цель настоящего исследования: выявить клинические и лабораторные особенности больных ХГС и ВИЧ-инфекцией.
Материал и методы
Работа выполнялась с 2013 по 2017 г. на базе инфекционной клинической больницы (ИКБ) № 2 Москвы и Московского городского центра по борьбе с ВИЧ/СПИД.
Всего под нашим наблюдением находилось 173 пациента с ХГС и ВИЧ-инфекцией. При постановке диагноза использовались эпидемиологические, клинические, биохимические, инструментальные методы исследования. Этиологический диагноз основывался на определении специфических серологических маркеров вирусных гепатитов и результатах молекулярно-биологических исследований с определением генотипа вируса гепатита С в лаборатории ИКБ № 2.
Стадия ВИЧ-инфекции определялась по Российской классификации ВИЧ-инфекции (В.И. Покровский, 2001 г.) [4].
В зависимости от схемы лечения все больные были разделены на 2 группы. Группа 1 включала 128 (74%) больных, которые получали только патогенетическую дезинтоксикационную терапию: раствор 5% глюкозы, солевые растворы, витамины (аскорбиновая кислота, витамины группы В), абсорбенты, гепатопротекторы. Из них 29 (22,6%) человек получали антиретровирусную терапию (АРТ): ламивудин, зидовудин, ставудин, абакавир, эфавиренз и др. Среди не получающих АРТ были пациенты, которым по иммунологическим характеристикам было показано лечение против ВИЧ-инфекции. Однако на фоне злоупотребления алкоголем у этих пациентов отмечалось обострение ХГС, в связи с чем АРТ не назначалась.
Группа 2 состояла из 45 (26%) человек — 32 (71,1%) мужчин и 13 (28,9%) женщин. Они получали стандартную противовирусную терапию (пегилированный интерферон альфа-2а + рибавирин). Пегилированный интерферон альфа-2а назначался в дозе 180 мг 1 р./нед. подкожно, рибавирин — по 800–1200 мг/кг в зависимости от массы тела. Длительность терапии составила 48 нед. Лечение в группе 2 проводилось амбулаторно, назначение АРТ не требовалось.
Статистическую обработку данных проводили с использованием MS Excel 2003 и подсчетом критерия Стьюдента (t).
Результаты исследования
Распределение пациентов в группах в зависимости от генотипа вируса гепатита С представлено на рисунках 1 и 2. Распределение по генотипам ХГС было сопоставимо, при этом генотип 1 встречался наиболее часто: у 67 (52,3%) больных в группе 1 и у 22 (48,9%) — в группе 2. У остальных пациентов в группе 1 генотип 2 встречался у 28 (21,9%) человек, генотип 3 — у 33 (25,8%); в группе 2 — соответственно у 9 и 14 (20,0 и 31,1%).
Большинство больных имели III (бессимптомную) или IVА стадию ВИЧ-инфекции (табл. 1): в группе 1 таких было 95 (74,2%) человек, в группе 2 — 45 (100%). В группе 2 не было больных с поздними стадиями ВИЧ-инфекции, т. к. это является абсолютным противопоказанием для назначения этиотропной терапии ХГС (интерферон + рибавирин).
Смешанную форму гепатита (ХГС + токсический гепатит) диагностировали у 71 (55,5 %) пациента. Хронический гепатит с исходом в цирроз печени отмечался в 22 случаях (17,2 %). Данные представлены на рисунке 3.
Распределение больных в зависимости от пола и возраста представлено в таблице 2.
Чаще ХГС встречался у пациентов мужского пола (в группе 1 — 64,3%, в группе 2 — 71,1%) и в наиболее трудоспособном возрасте от 20 до 30 лет (в группе 1 — 68,8%, в группе 2 — 80%).
Распределение пациентов в зависимости от сопутствующей патологии и оппортунистических инфекций представлено в таблице 3.
Как видно из представленных данных, сопутствующие заболевания встречались в обеих группах, однако, учитывая, что пациенты группы 2 лечились амбулаторно и к врачу обращались в плановом порядке, частота встречаемости сопутствующей патологии у данной группы больных была достоверно ниже. Анализ больных показал, что в группе 1 наиболее часто встречались такие заболевания, как обострение хронического панкреатита (31,3%), обострение хронического бронхита (27,3%), пневмония (19,5%). Выявлена высокая частота наркомании в обеих группах (25,8% и 13,3% соответственно). Часть больных в группе 1 не получала стандартную (этиотропную) терапию ХГС вследствие ряда объективных и субъективных факторов, которые приведены в таблице 4.
Из представленных данных видно, что чаще всего стандартная терапия не назначалась из-за злоупотребления алкоголем и/или приема психоактивных веществ, а также вследствие выраженного иммунодефицита (СД4+ лимфоциты менее 350 клеток). Также большую группу составили пациенты, которым стандартная терапия назначалась, но была отменена в результате развития побочных эффектов (16,4%) и/или неэффективности лечения (6,2%).
В качестве иллюстрации отказа от противовирусной терапии ХГС приводим собственное наблюдение.
Клинический пример
Выводы
Таким образом, в результате анализа клинических и лабораторных данных больных ХГС и ВИЧ-инфекцией можно сделать следующие выводы:
среди пациентов с ХГС и ВИЧ-инфекцией, поступающих в стационар, преобладают больные со смешанной формой гепатита (ХГС + токсический гепатит);
среди токсических причин поражения печени в абсолютном большинстве случаев отмечено злоупотребление алкоголем;
большинство пациентов имеют генотип 1 вируса гепатита С;
основные причины неназначения противовирусной терапии гепатита С: злоупотребление алкоголем, наркомания, низкий иммунный статус и отказ пациента от лечения.
Справка: что такое гепатит С
Вирусные гепатиты — это инфекционные заболевания, поражающие печень. Существуют разные вирусные гепатиты (их обозначают латинскими буквами). Симптомы заболеваний могут быть схожими (а чаще всего их вообще нет), но их возбудители по-разному распространяются и влияют на организм человека. Например, гепатит А — это кратковременная инфекция, а В и С могут протекать десятилетиями, незаметно повреждая печень. С распространением гепатитов А и В успешно борются с помощью прививок, а вот против гепатита С вакцины не существует.
Заражение вирусом гепатита С обычно происходит через контакт с кровью инфицированного человека:
- через шприц у лиц, употребляющих инъекционные наркотики (по статистике это наиболее распространенный способ заражения);
- при незащищенном сексе (риск выше при более травматичных формах, например, анальном сексе);
- через нестерильные медицинские инструменты (например, при экстренных вмешательствах в ограниченных условиях, при стоматологических процедурах и др.);
- через предметы личного пользования (например, бритву);
- при нарушении условий переливания крови (встречается редко, так как компоненты и доноры крови проходят тщательный отбор и обследование);
- от инфицированной матери новорожденному.
Основной способ диагностики гепатита С — анализ крови. Поэтому сложно назвать реальное количество людей, которые являются носителями этого вируса. В 2021 году некоторые эксперты говорили о том, что в России гепатитом С могут быть заражены около 5,7 млн человек.
— Как гепатит С лечили раньше?
— Сначала для терапии использовали рибавирин — неспецифический противовирусный препарат, у которого есть немало побочных эффектов. Потом его стали использовать в комбинации с препаратами интерферона, задача которого — усилить иммунный противовирусный ответ в организме. Но и у интерферона есть побочные явления и нередко — противопоказания к применению. Существуют заболевания, при которых применение интерферона невозможно или дает очень высокие риски осложнений. Зачастую приходилось выбирать, кому из больных проводить терапию по этой схеме, а кому отказывать. Эффективность тоже была заведомо невысокой, можно даже сказать, мы играли в лотерею. Переносимость интерферона, сопутствующие заболевания, риск нежелательных явлений, изменение показателей крови, стадия цирроза печени и в целом состояние печени на момент лечения — от всего этого зависело, можно ли было назначать лечение. Плюс мы выявляли у пациентов определенные генетические показатели, при которых его применение заведомо могло быть малоэффективным.
— Таких пациентов совсем не лечили?
— Гепатопротекторы бесполезны при гепатите?
— Итак, старая схема давала высокие риски, побочные эффекты и низкую эффективность. Что удалось изменить в новых рекомендациях?
— Принципиальный момент, который, наверное, будет самым важным для всех нас — и для пациентов, и для врачей, — возможность назначать терапию на любой стадии хронического гепатита С. Не запущенные стадии, как было раньше, когда у пациента уже возникали фиброз и цирроз печени. Сейчас у нас единственное показание к лечению, как и во всем мире, что мне очень приятно, — это сам факт выявления вируса гепатита С в крови. Поэтому врачам теперь не нужно решать, кому назначать противовирусную терапию, а кому — нет.
— Терапию теперь можно проводить сразу после того, как вирус обнаружили в крови?
— По современным российским рекомендациям это нужно сделать не позднее трех месяцев после обнаружения вируса в крови — возможно начать терапию сразу, иногда понаблюдать 6–12 недель. Это можно делать, потому что в определенных случаях организм побеждает вирус сам. Процент таких больных действительно есть, хотя он намного ниже, например, чем в случаях с гепатитом В (он реже становится хроническим).
— Мы убрали это слово, сейчас такого подхода нет. Конечно, приоритет все равно дается пациентам с циррозом печени или с другими рисками (например, с раком печени и вирусным гепатитом или поражением других органов). Пациенты после после пересадки печени получают лечение незамедлительно, так как инфицирование нового органа наступает неизбежно.
— Схема лечения тоже изменилась?
— Это еще один принципиальный момент, над которым мы целенаправленно работали. Из рекомендаций исчезли препараты интерферона. Это влечет за собой целый ряд позитивных изменений. Как я уже говорил, интерферон многими пациентами переносится тяжело, возникают побочные эффекты, и результаты невысоки, особенно при циррозе печени.
Теперь мы перешли полностью на таблеточные схемы, их эффективность приближается к 100%. Это позволяет бюджетным медицинским учреждениям больше не тратить деньги на закупку интерферона, а закупать только таблеточные формы лекарств и использовать безинтерфероновые высокоэффективные схемы. При этом нужно сказать, что большая часть тех препаратов, которые есть в мире и, в частности, в западных странах, присутствуют и в России.
— Новые схемы лечения эффективнее прежних?
— Они перекрывают все существующие в России типы вирусов гепатита С. Это так называемая пангенотипная схема: когда одна таблетка, одна комбинация препаратов, может вылечить все типы вирусов. К примеру, в России встречаются в основном три типа вируса гепатита С (1а, 1b, 3), и их раньше по разным причинам не всегда удавалось лечить эффективно, особенно на стадии цирроза. Сейчас эта проблема уже не имеет значения. Во всем мире принята следующая концепция упрощенного подхода к лечению: выявляют вирус, но не определяют ни его количество, ни его разновидность, для того чтобы выбрать конкретный препарат. Вместо этого назначают лекарства, которые одинаково эффективны при разных вариантах инфекции.
Для цитирования: Яковлев А.Б. Дерматологические симптомы цирроза печени: значимость междисциплинарной проблемы. РМЖ. 2014;20:1471.
Печень взрослого человека весит около 1,5 кг. Она покрыта тонкой прочной соединительнотканной оболочкой – глиссоновой капсулой [1]. Большая часть печени располагается в правой стороне туловища. Печень проецируется на переднюю брюшную стенку надчревной области. Верхняя граница печени в норме начинается в 10-м межреберье справа по средней подмышечной линии. Отсюда она круто поднимается кверху и медиально. По правой сосковой линии граница печени может достигать в норме 4-го межреберья. Далее граница печени опускается влево, пересекает грудину несколько выше основания мечевидного отростка, верхняя граница печени доходит до середины расстояния между левой грудинной и левой сосковой линией.
Нижняя граница печени также начинается в 10-м межреберье справа, но идет наискосок и медиально, пересекает 9-й и 10-й реберные хрящи справа, идет по области над чревьем наискосок влево и вверх, пересекает реберную дугу на уровне 7-го левого реберного хряща и в 5-м межреберье соединяется с верхней границей [2]. Расположение нижней границы печени – одна из наиболее важных клинических характеристик ее размера. В норме она определяется ниже края реберной дуги справа, выступ должен быть не более чем 2 см.
Печень состоит из 2-х главных долей, правая доля значительно крупнее левой. Нижняя поверхность печени называется висцеральной и соприкасается с некоторыми частями ЖКТ и правой почкой. Верхняя поверхность печени гладкая, непосредственно прилежит к диафрагме. На нижней поверхности печени имеется короткая глубокая поперечная борозда – ворота печени.
Относительная массовая доля печени неодинакова в различные периоды жизни человека: у новорожденного печень занимает большую часть брюшной полости, а масса составляет 1:20 массы тела; у взрослого масса печени – 1:50 массы тела, а ее скелетотопия соответствует описанной выше [2].
Печень состоит из паренхимы, формируемой гепатоцитами, и соединительнотканной стромы. Гепатоциты – функциональные клетки печени, выполняющие не менее 500 различных функций – от накопительных (гликоген) до детоксицирующих (глюкуронид).
Гипертрофические поражения ногтей, их чрезмерное уплотнение (склеронихия), гиппократовы ногти для цирроза печени не характерны.
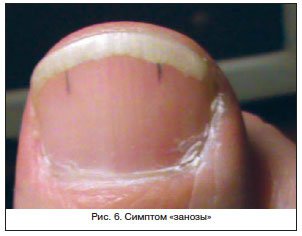
Классическим признаком длительно пьющего человека всегда считалась эритема лица – симптом, описанный во многих художественных произведениях. Между тем сама по себе эритема лица, или розацеа, напрямую не коррелирует с тяжестью поражения печени, а лишь выдает факт злоупотребления алкоголем. Именно под действием алкоголя происходит расширение сосудов лица, которое в дальнейшем становится стойким. Однако считается, что крайняя степень розацеа – ринофима все же определенным образом коррелирует с тяжестью поражения печени и может служить ориентировочным симптомом сформировавшегося цирроза, дающим основание для целенаправленного поиска. Такими ориентировочными симптомами являются многие из описанных кожных изменений. Считается, что ринофима представляет собой завершающую инфильтративно-продуктивную стадию развития розацеа. Процесс может локализоваться в области не только носа (ринофима), но и подбородка (гнатофима), на ушах (отофима), веках (блефарофимоз) [15]. Из 4-х видов ринофимы (гландулярная, фиброзная, фиброангиоматозная, актиническая) для цирроза печени в большей степени характерна форма, связанная с инсоляцией, – актиническая. Но могут наблюдаться все перечисленные формы ринофимы.
Крапивница является неспецифическим синдромом и в целом для цирроза не характерна. Но она может быть одним из признаков активного вирусного гепатита. В далеко зашедших случаях цирротического поражения появление крапивницы обусловлено скорее токсическими влияниями [1, 16].
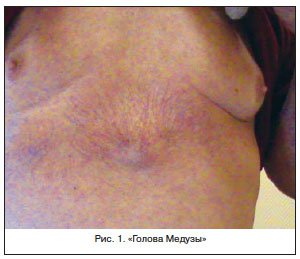
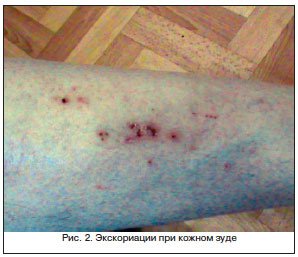
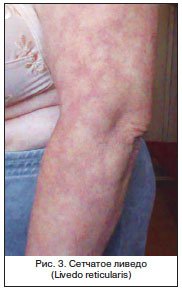
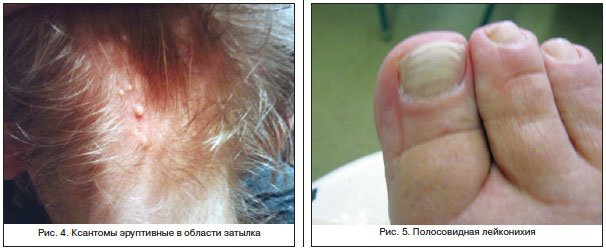
Печень является самым большим внутренним органом. Она расположена справа в верхней части брюшной полости. Несомненно, здоровая печень важна для всех, но особенно для ВИЧ инфицированных. Печень играет важную роль в утилизации лекарственных препаратов, используемых для лечения как ВИЧ-инфекции так и других заболеваний. Вирусы гепатита А, В или С повреждают печень, что может привести к тяжелому заболеванию и одновременно к нарушению функций печени
Главные функции печени
Печень выполняет четыре главные функции:
• Детоксикация: печень очищает кровь путем фильтрации и разрушения токсических веществ
• Секреция: печень продуцирует желчь, которая выделяется в кишечный тракт и участвует в расщеплении жиров
• Запас: печень превращает питательные вещества, полученные с пищей, в энергию, а так же аккумулирует витамины и минеральные вещества
• Синтез: Печень также продуцирует белки и некоторые витамины
Что приводит к повреждению печени
Употребление алкоголя приводит к замещению части печени рубцовой тканью, что приводит к нарушению ее функции.
Кроме алкоголя, все наркотики, также повреждают печень.
Вирусы гепатита вызывают воспалительные изменения в печени и тем самым нарушают ее функцию.
Фиброз и цирроз печени
С целью контроля функции печени инфицированные ВИЧ проходят регулярные тесты. Повышение уровня некоторых печеночных ферментов указывает на повреждение печени и ее функции
Употребление алкоголя, прием наркотических средств а также длительное течение гепатитов В и С- все это приводит к повреждению печеночной ткани и развитию либо фиброза или цирроза.
В случае фиброза участки печени замещаются на плотную рубцовую ткань. Фиброз может регрессировать если причина, приводящая к нему, установлена и своевременно устранена.
При циррозе большая часть печени замещена на рубцовую ткань, что вызывает серьезное нарушение ее функции и приводит к развитию таких симптомов как: желтуха, внутреннее кровотечение и скопление жидкости в брюшной полости. Цирроз чаще всего необратим.
Рак печени
Цирроз, развившийся в результате хронического гепатита В или С, значительно увеличивает риск развития рака печени.
Рак печени – трудно поддающееся лечению заболевание. Хирургическое лечение - трансплантация печени или удаление поврежденной части печени – зачастую является единственными методами лечения рака. Опухоль небольшого размера может быть удалена, хотя риск развития рецидивов опухоли в течении последующих пяти лет очень высок. Химиотерапия, к сожалению, не продлевает сроки выживаемости, хотя может быть использована для облегчения симптомов вызываемых раком.
Вакцинация против гепатита
В настоящее время широко используется профилактическая вакцинация против гепатита А и В. Если у вас нет иммунитета к гепатиту А или В как результат перенесенного в прошлом гепатита, мы советуем вам пройти курс вакцинации.
К сожалению, не всегда удается добиться достаточно высокого уровня иммунитета против гепатита В после первого курса вакцинации среди ВИЧ инфицированных пациентов, особенно с низким уровнем СD4 клеток. Таким пациентам необходимо пройти повторный курс вакцинации.
Завершенный курс вакцинации обеспечивает длительную защиту против гепатита А и В.
В настоящее время вакцины против гепатита С не существует
В настоящее время для лечения гепатита С используются рибавирин и пегилированный интерферон.
Читайте также:

